高中化学人教版(2019)选择性必修三 第三章 第三节 醛 酮 学案(含答案)
文档属性
| 名称 | 高中化学人教版(2019)选择性必修三 第三章 第三节 醛 酮 学案(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-26 00:00:00 | ||
图片预览



文档简介
第三节 醛 酮
[素养发展目标]
1.认识醛、酮的组成和结构特点、性质、转化关系及其在生产生活中的应用。
2.从官能团、化学键的角度分析和推断醛类的化学性质,能通过实验探究乙醛与银氨溶液、新制氢氧化铜的反应,培养科学探究与创新意识的学科核心素养。
3.结合生产、生活实际了解醛、酮对环境和健康可能产生的影响。
知识点一 乙醛
1.醛的结构、组成
2.乙醛的结构
分子式 结构式 结构简式 分子结构模型
C2H4O CH3CHO
3.乙醛的物理性质
乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点20.8 ℃,易挥发,易燃烧,能与水、乙醇等互溶。
4.乙醛的化学性质
(1)加成反应
①催化加氢(还原反应):CH3CHO+H2CH3CH2OH(填化学方程式,下同)。
②与HCN加成:CH3CHO+HCN―→CH3CH(OH)CN。
(2)氧化反应
①银镜反应:CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O。
②与新制Cu(OH)2的反应:CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O。
③催化氧化:2CH3CHO+O22CH3COOH。
④燃烧:2CH3CHO+5O24CO2+4H2O。
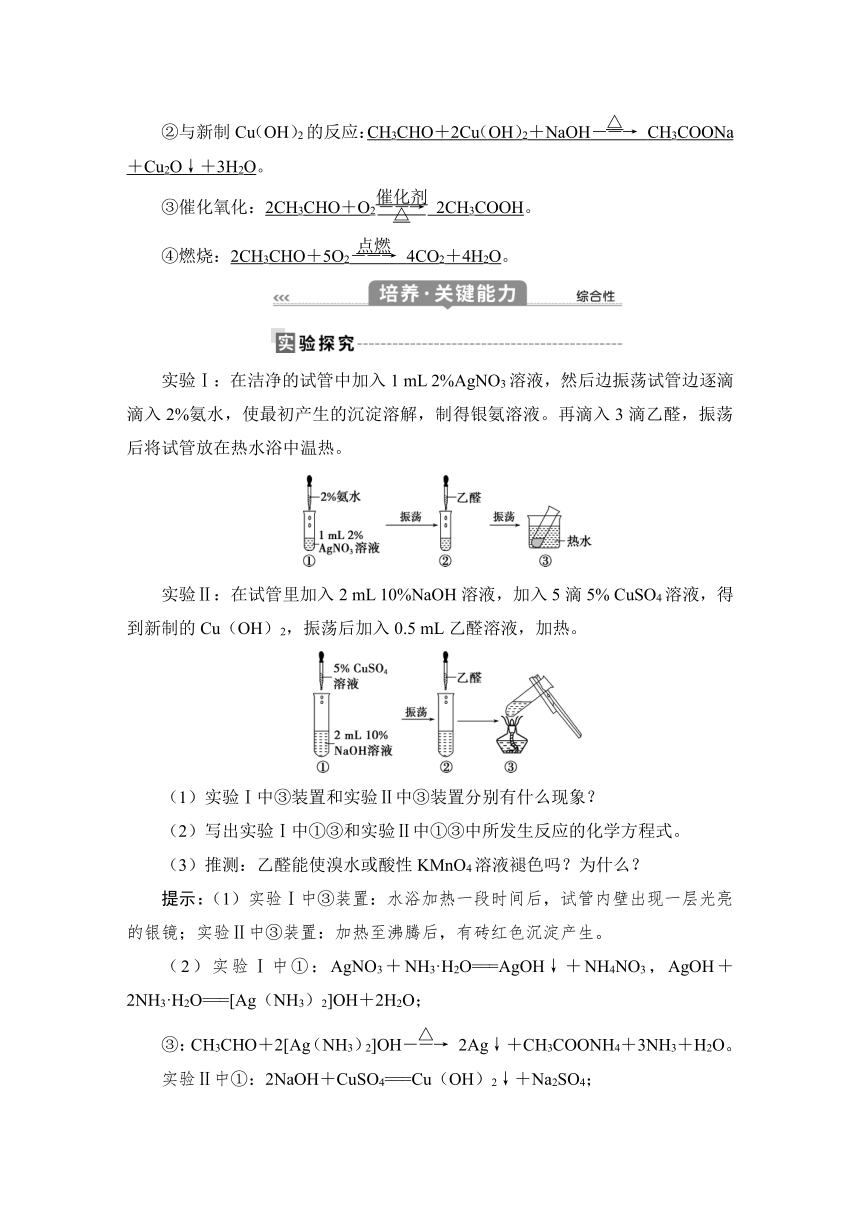
实验Ⅰ:在洁净的试管中加入1 mL 2%AgNO3溶液,然后边振荡试管边逐滴滴入2%氨水,使最初产生的沉淀溶解,制得银氨溶液。再滴入3滴乙醛,振荡后将试管放在热水浴中温热。
实验Ⅱ:在试管里加入2 mL 10%NaOH溶液,加入5滴5% CuSO4溶液,得到新制的Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热。
(1)实验Ⅰ中③装置和实验Ⅱ中③装置分别有什么现象?
(2)写出实验Ⅰ中①③和实验Ⅱ中①③中所发生反应的化学方程式。
(3)推测:乙醛能使溴水或酸性KMnO4溶液褪色吗?为什么?
提示:(1)实验Ⅰ中③装置:水浴加热一段时间后,试管内壁出现一层光亮的银镜;实验Ⅱ中③装置:加热至沸腾后,有砖红色沉淀产生。
(2)实验Ⅰ中①:AgNO3+NH3·H2O===AgOH↓+NH4NO3,AgOH+2NH3·H2O===[Ag(NH3)2]OH+2H2O;
③:CH3CHO+2[Ag(NH3)2]OH2Ag↓+CH3COONH4+3NH3+H2O。
实验Ⅱ中①:2NaOH+CuSO4===Cu(OH)2↓+Na2SO4;
③:CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O。
(3)能。因为醛基有较强的还原性,能被[Ag(NH3)2]OH溶液或新制Cu(OH)2等弱氧化剂氧化。而溴水或酸性KMnO4溶液的氧化能力比[Ag(NH3)2]OH溶液、新制Cu(OH)2强得多,故溴水、酸性KMnO4溶液也能氧化乙醛,自身被还原,从而使溶液褪色。
1.银镜反应实验注意事项
(1)试管要洁净,洗涤试管时一般要先用热的NaOH溶液洗,再用水洗。
(2)银氨溶液必须现用现配,不可久置,否则会生成易爆物质。
(3)配制银氨溶液时,氨水、硝酸银溶液都必须是稀溶液,且是将稀氨水逐滴加入稀硝酸银溶液中(顺序不能颠倒),直到最初产生的沉淀恰好溶解,氨水不能过量,否则也会生成易爆物质。
(4)银镜反应的条件是水浴加热,不能直接加热,加热时不可振荡或摇动试管,以防生成黑色的银,而不能在试管内壁形成光亮的银镜。
(5)实验结束后,试管内壁附着的银镜,可用稀硝酸浸泡,待银溶解后再用自来水、蒸馏水洗涤干净。
2.乙醛与新制Cu(OH)2反应实验注意事项
(1)所用Cu(OH)2悬浊液必须是新制备的。
(2)配制Cu(OH)2悬浊液时,必须保证NaOH溶液过量,即保证所得溶液呈碱性。
(3)用酒精灯直接加热试管至溶液沸腾,才有明显的砖红色沉淀产生。
(4)加热煮沸时间不能过久,否则会导致Cu(OH)2分解成CuO而出现黑色沉淀。
3.醛基的检验
在洁净的试管中加入新制银氨溶液和少量试样后,水浴加热,有银镜生成,或在洁净的试管中加入少量试样和新制的Cu(OH)2,加热煮沸,有砖红色沉淀生成。
1.(2022·北京八中高二阶段练习)下列有机化合物中,属于醛类的是( )
A.(CH3)2CHOH
C.CH3CH2COOH D.HCOOCH3
答案:B
2.下列说法正确的是( )
A.乙醛的分子式为CH3CHO
B.乙醛的结构简式为CH3CHO
C.乙醛是一种有刺激性气味的气体
D.乙醛不溶于有机溶剂,也不溶于水
答案:B
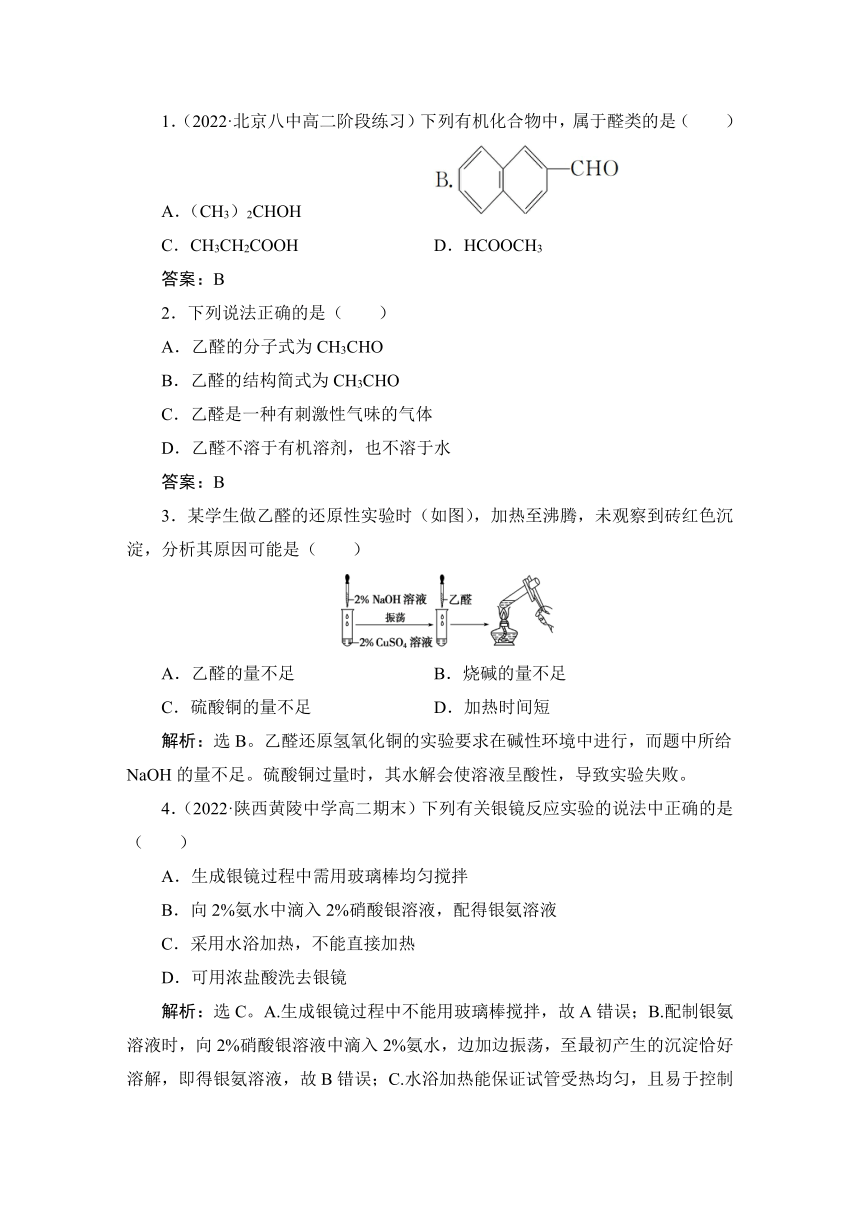
3.某学生做乙醛的还原性实验时(如图),加热至沸腾,未观察到砖红色沉淀,分析其原因可能是( )
A.乙醛的量不足 B.烧碱的量不足
C.硫酸铜的量不足 D.加热时间短
解析:选B。乙醛还原氢氧化铜的实验要求在碱性环境中进行,而题中所给NaOH的量不足。硫酸铜过量时,其水解会使溶液呈酸性,导致实验失败。
4.(2022·陕西黄陵中学高二期末)下列有关银镜反应实验的说法中正确的是( )
A.生成银镜过程中需用玻璃棒均匀搅拌
B.向2%氨水中滴入2%硝酸银溶液,配得银氨溶液
C.采用水浴加热,不能直接加热
D.可用浓盐酸洗去银镜
解析:选C。A.生成银镜过程中不能用玻璃棒搅拌,故A错误;B.配制银氨溶液时,向2%硝酸银溶液中滴入2%氨水,边加边振荡,至最初产生的沉淀恰好溶解,即得银氨溶液,故B错误;C.水浴加热能保证试管受热均匀,且易于控制反应温度,直接加热受热不均匀,不利于银镜的生成,故C正确;D.银和浓盐酸不反应,需要用稀硝酸洗去银镜,故D错误。
知识点二 醛类
1.甲醛与苯甲醛
甲醛(蚁醛) 苯甲醛(苦杏仁油)
结构简式 HCHO
色、味、态 无色、有强烈刺激性气味的气体 无色、有苦杏仁气味的液体
溶解性 易溶于水 微溶于水,能与苯、乙醇等互溶
用途 重要的化工原料,能合成多种有机化合物;其水溶液(又称福尔马林)具有杀菌、防腐性能,可用于消毒和制作生物标本 制造染料、香料及药物的重要原料
2.醛类的化学性质
醛类分子中都含有醛基(—CHO),所以化学性质与乙醛的相似。一般情况下,醛能被还原为醇,被氧化为羧酸,可以发生银镜反应,能与氰化氢加成。
(1)加成反应
R—CHO+H2R—CH2—OH;
R—CHO+HCN―→R—CH(OH)CN。
(2)氧化反应
银镜反应 RCHO+2[Ag(NH3)2]OH2Ag↓+RCOONH4+3NH3+H2O
与新制的Cu(OH)2反应 RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O
催化氧化 2RCHO+O22RCOOH
在中国家庭中肉桂是炖肉、炒菜重要的调味品,在西方人们更是将肉桂打成粉末加入咖啡中调味。由于它是含有特殊芳香气味的植物,肉桂还可以制作比较特殊的香料。科学家已发现,肉桂中的肉桂醛是一种赋予肉桂独特风味的有机化合物,结构简式为
(1)肉桂醛具有醛类物质的通性。请写出其与银氨溶液、新制的Cu(OH)2反应的化学方程式。
(2)1 mol 肉桂醛完全氢化需要氢气的物质的量是多少?
(3)1 mol 肉桂醛充分进行银镜反应生成Ag的物质的量是多少?1 mol 甲醛呢?
提示:(1)
(2)5 mol。
(3)1 mol 肉桂醛充分进行银镜反应生成Ag的物质的量是2 mol,1 mol 甲醛充分进行银镜反应生成Ag的物质的量是4 mol。
1.醛的氧化与还原规律
RCH2OHRCHORCOOH
2.相关定量计算
(1)一元醛发生银镜反应或与新制的Cu(OH)2反应时,定量关系如下:
(2)甲醛发生氧化反应时,可以理解为
所以,甲醛分子中相当于有2个—CHO,与足量的银氨溶液或新制的Cu(OH)2反应时,存在如下定量关系:
1 mol HCHO~4 mol Ag,1 mol HCHO~4 mol Cu(OH)2~2 mol Cu2O。
1.下列关于醛的说法不正确的是( )
A.甲醛是甲基跟醛基相连而构成的醛
B.醛的官能团是—CHO
C.甲醛和丙醛互为同系物
D.饱和一元脂肪醛的通式为CnH2nO(n≥1,n为整数)
解析:选A。A.甲醛的结构简式为HCHO,即甲醛分子中不含烃基,甲醛是氢原子跟醛基相连而构成的醛,故A错误;B.醛的官能团是醛基,即—CHO,故B正确;C.甲醛的结构简式为HCHO,丙醛的结构简式为CH3CH2CHO,甲醛和丙醛结构相似,分子组成相差两个CH2原子团,互为同系物,故C正确;D.饱和一元脂肪醛是指含有一个醛基,烃基中不存在不饱和键的醛,则饱和一元脂肪醛的通式为CnH2nO(n≥1,n为整数),故D正确。
2.某有机化合物的结构简式为CH2===CH—CH2—CHO,下列对其化学性质的判断中错误的是( )
A.能被银氨溶液氧化
B.能使酸性KMnO4溶液褪色
C.1 mol该有机化合物能与2 mol Br2发生加成反应
D.1 mol该有机化合物能与2 mol H2发生加成反应
解析:选C。A.该有机化合物分子中含有醛基,故能被银氨溶液氧化;B.该有机化合物分子中含有碳碳双键和醛基,能使酸性高锰酸钾溶液褪色;C.该有机化合物分子中只有一个碳碳双键,故1 mol该有机化合物只能与1 mol Br2发生加成反应;D.该有机化合物分子中含有醛基和碳碳双键,故1 mol该有机化合物能与2 mol H2发生加成反应。
3.下列各化合物中,能发生酯化、还原、加成、消去四种反应的是( )
A.CH3CH===CHCHO
答案:C
4.丙醛和另一种组成为CnH2nO的物质X的混合物3.2 g,与足量的银氨溶液作用后析出10.8 g银,则混合物中所含X不可能是( )
A.甲基丙醛 B.丙酮()
C.乙醛 D.丁醛
解析:选C。反应中生成银的物质的量是10.8 g÷108 g/mol=0.1 mol,根据方程式RCHO+2[Ag(NH3)2]OHRCOONH4+2Ag↓+3NH3+H2O可知,消耗醛的物质的量是0.05 mol,则混合物的平均相对分子质量是3.2÷0.05=64;丙醛的相对分子质量为58<64,所以另一种是相对分子质量大于64的醛,或是不发生银镜反应的其他物质。A.甲基丙醛的相对分子质量大于64,甲基丙醛可能;B.丙酮不能发生银镜反应,丙酮可能;C.乙醛的相对分子质量小于64,乙醛不可能;D.丁醛的相对分子质量大于64,丁醛可能。
知识点三 酮
1.概念
2.丙酮()——最简单的酮
(1)物理性质
丙酮是无色透明的液体,沸点56.2 ℃,易挥发,能与水、乙醇等互溶。
(2)化学性质
①催化加氢反应:在催化剂存在的条件下,丙酮可以发生催化加氢反应,生成2-丙醇,化学方程式为。
②氧化反应:丙酮能燃烧,被氧气氧化,但不能被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化。
(3)用途
丙酮可用作化学纤维、钢瓶储存乙炔等的溶剂,还用于生产有机玻璃、农药和涂料等。
1.下列有关丙酮的说法正确的是( )
A.是乙醛的同系物
B.可从水中萃取出单质碘
C.与CH3CH2CHO互为同分异构体
D.不易燃烧
解析:选C。A.丙酮与乙醛所含的官能团不同,二者不互为同系物,故A错误;B.丙酮易溶于水,不能从水中萃取出单质碘,故B错误;C.丙酮与CH3CH2CHO的分子式均为C3H6O,但结构不同,二者互为同分异构体,故C正确;D.丙酮能燃烧,故D错误。
2.下列醛、酮的反应属于还原反应的是( )
A.醛的银镜反应
B.醛在空气中久置变质
C.由2-丁酮制备2-丁醇
D.乙醛与新制的氢氧化铜加热有砖红色沉淀产生
解析:选C。A.醛的银镜反应属于醛的氧化反应,A项错误;B.醛在空气中久置变质,属于醛的氧化反应,B项错误;C.由2-丁酮制备2-丁醇,羰基加氢变为羟基,属于酮的还原反应,C项正确;D.乙醛与新制的氢氧化铜加热有砖红色沉淀产生,属于醛的氧化反应,D项错误。
1.(2022·上海奉贤高二阶段练习)下列关于甲醛的描述错误的是( )
A.结构式:
B.电子式:
C.是极性分子
D.球棍模型:
解析:选B。A.甲醛中C、O原子形成双键,C、H原子以单键相连,结构式为,A正确;B.C、O之间形成的是共价双键,且O原子最外层有8个电子,电子式为,B错误;C.根据甲醛的结构式可知其正负电中心不重合,为极性分子,C正确;D.原子半径:C>O>H,结合结构式可知球棍模型为,D正确。
2.(2022·吉林希望高中高二阶段练习)下列说法中,正确的是( )
A.甲醛、乙醛分子中的所有原子都在同一平面上
B.甲醛、乙醛在常温下都是无色有刺激性气味的液体
C.乙醛、丙醛都没有同分异构体
D.醛类既能被氧化为羧酸又能被还原为醇
解析:选D。A.乙醛分子中含有—CH3,所有原子不可能在同一平面上,A不正确;B.甲醛在常温常压下是无色、有刺激性气味的气体,B不正确;C.丙醛与丙酮互为同分异构体,C不正确;D.醛类都含有—CHO,既能被氧化剂(如O2、酸性KMnO4溶液等)氧化为羧酸,又能被还原剂(如H2等)还原为醇,D正确。
3.下列四个反应中,有机化合物发生的反应与其他三个反应类型不同的是( )
A.CH3CHO+H2CH3CH2OH
B.CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O
C.CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O
D.2CH3CHO+O22CH3COOH
解析:选A。A.该反应是乙醛的加成反应,属于还原反应;B.该反应是银镜反应,属于乙醛的氧化反应;C.该反应是乙醛的氧化反应;D.该反应是乙醛的氧化反应。
4.(2022·吉林二中高二阶段练习)只用一种试剂就可鉴别甲酸、乙酸、乙醛、乙醇,这种试剂是( )
A.银氨溶液 B.新制的Cu(OH)2
C.石蕊溶液 D.Na2CO3溶液
解析:选B。A.乙酸与银氨溶液反应没有明显现象,乙醇与银氨溶液不反应,不能鉴别,故A错误。B.甲酸与新制的氢氧化铜反应,变为蓝色溶液,甲酸分子中含有醛基,与新制的氢氧化铜共热会产生砖红色沉淀并有气泡产生;乙酸溶解氢氧化铜,溶液呈蓝色;乙醛具有还原性,与新制的氢氧化铜共热会产生砖红色沉淀;乙醇与新制的氢氧化铜混合后无明显现象;四种溶液现象各不相同,能鉴别,故B正确。C.石蕊溶液为酸碱指示剂,与甲酸和乙酸混合,溶液均呈红色,但无法进一步鉴别,故C错误。D.Na2CO3溶液与乙酸、甲酸反应生成气体,但与乙醛和乙醇不反应,无法全部鉴别,故D错误。
5.柠檬醛是一种具有柠檬香味的有机化合物,广泛存在于香精油中,是食品工业中重要的调味品,且可用于合成维生素A。已知柠檬醛的结构简式如下:
(1)试推测柠檬醛可能发生的反应有_________(填字母)。
①能使溴的四氯化碳溶液褪色
②能与乙醇发生酯化反应
③能发生银镜反应
④能与新制的Cu(OH)2反应
⑤能使酸性KMnO4溶液褪色
A.①③④ B.①②④⑤
C.①③④⑤ D.①②③④⑤
(2)检验柠檬醛分子中含有醛基的方法为
________________________________________________________________
________________________________________________________________,
发生反应的化学方程式为
________________________________________________________________
________________________________________________________________。
(3)检验柠檬醛分子中含有碳碳双键的方法为
________________________________________________________________
________________________________________________________________
________________________________________________________________。
解析:(1)由柠檬醛的结构简式可知其所含官能团为、—CHO。①CC可与Br2发生加成反应,从而使溴的四氯化碳溶液褪色;②分子中无—COOH,不能与C2H5OH发生酯化反应;分子中有—CHO,可以发生③④反应;⑤与—CHO均可以使酸性KMnO4溶液褪色。(2)常利用银镜反应或与新制的Cu(OH)2的反应检验—CHO的存在。(3)当—CHO与同时出现时,应先检验并除去—CHO ,再检验;常用溴的CCl4溶液或酸性KMnO4 溶液来检验的存在。
答案:(1)C
(2)加入银氨溶液后水浴加热,有银镜出现,则含有醛基
+3NH3+H2O(答案合理即可)
(3)在加银氨溶液[或新制的Cu(OH)2]氧化醛基后,调节溶液pH至酸性,再加入溴的四氯化碳溶液(或酸性 KMnO4溶液),若溶液褪色说明含有碳碳双键
[基础检测]
1.下列物质中不属于醛的是( )
A.①③ B.②④
C.②③ D.①④
答案:B
2.不能由醛或酮加氢还原制得的醇是( )
解析:选D。A. 中羟基相连的碳原子上有1个氢原子,说明可以由酮加氢还原制得,A不符合题意;B.CH3CH2CH2OH中与羟基相连的碳原子上有2个氢原子,能够由醛加氢还原制得,B不符合题意;C. 中与羟基相连的碳原子上有2个氢原子,能够由醛加氢还原制得,C不符合题意;D. 中与羟基相连的碳原子上没有氢原子,不能由醛或酮加氢还原制得,D符合题意。
3.将CH3CHO (易溶于水,沸点为20.8 ℃的易挥发性液体)和CH3COOH分离的最佳方法是( )
A.加热蒸馏
B.加入Na2CO3后,通过萃取的方法分离
C.加入烧碱溶液之后蒸出乙醛,再加入硫酸,蒸出乙酸
D.和Na反应后进行分离
解析:选C。A.乙酸易挥发,直接蒸馏得不到纯净物,A不符合题意;B.乙酸与碳酸钠反应后,与乙醛混溶,不能萃取分离,B不符合题意;C.先加入烧碱溶液,乙酸与NaOH反应生成的乙酸钠可增大与乙醛的沸点差异,蒸馏时先蒸出乙醛,再加入H2SO4,使乙酸钠与其反应再生成乙酸,然后蒸出乙酸,C符合题意;D.乙酸与Na反应生成乙酸钠,分离混合物应再使乙酸钠转化为乙酸,D不符合题意。
4.(2022·秦皇岛一中高二开学考试)已知两个醛分子在 NaOH 溶液作用下可以发生如下的加成反应,生成羟基醛:。如果将甲醛、乙醛、丙醛在 NaOH 溶液中发生反应,最多可以形成几种羟基醛( )
A.6 种 B.7 种
C.8 种 D.9 种
解析:选A。根据题干信息可知,甲醛自身不能发生加成反应,乙醛与丙醛在NaOH溶液中可以发生同种醛的加成,产物有2种,即CH3CH(OH)CH2CHO、CH3CH2CH(OH)CH(CH3)CHO,甲醛与乙醛、甲醛与丙醛反应分别生成1种产物,即HOCH2CH2CHO、HOCH2CH(CH3)CHO,乙醛和丙醛反应将得到2种产物,即CH3CH(OH)CH(CH3)CHO、CH3CH2CH(OH)CH2CHO,共6种,故答案为A。
5.(2022·重庆高二阶段练习)乙醛的银镜反应实验步骤如下:
步骤1:向试管中加入1 mL 2% AgNO3溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤3:再向试管中加入1 mL 10%乙醛溶液,振荡,在60~70 ℃水浴中加热,观察到试管内壁形成了光亮银镜。
下列说法不正确的是( )
A.步骤1中观察到的白色沉淀为AgOH
B.步骤2中沉淀溶解是因为生成[Ag(NH3)2]+
C.步骤3中产生银镜说明乙醛被还原
D.试管内壁的银镜可以用稀硝酸洗去
解析:选C。A.氨水少量时,氨水中一水合氨电离出的氢氧根离子和银离子结合成白色的AgOH沉淀,因此步骤1中观察到的白色沉淀为AgOH,A正确;B.AgOH与NH3·H2O反应生成[Ag(NH3)2]OH而溶解,AgOH转变成[Ag(NH3)2]+,B正确;C.[Ag(NH3)2]OH和乙醛发生银镜反应生成Ag,Ag元素化合价降低,被还原,而乙醛发生氧化反应,被氧化,C错误;D.因硝酸具有强氧化性,能溶解Ag,试管内壁的银镜可用稀硝酸洗去, D正确。
6.(2022·蚌埠二中高二期中)某有机化合物的分子式为C5H9BrO,能够与新制的氢氧化铜反应产生砖红色沉淀的同分异构体种数为( )
A.8种 B.9种
C.10种 D.12种
解析:选D。能够与新制的氢氧化铜反应产生砖红色沉淀,说明含有—CHO,该分子的不饱和度为1,共有:(数字表示—CHO位置,后同)、、、,共4+4+3+1=12种,故选D。
7.1,5-戊二醛(简称GA)是一种重要的饱和直链二元醛。2%的GA溶液具有广谱、高效、无刺激、无腐蚀等特点,对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用。下列说法正确的是( )
A.GA的分子式为C5H10O2,符合此分子式的二元醛有2种
B.GA不能在加热条件下和新制氢氧化铜反应
C.GA不能使酸性KMnO4溶液褪色
D.2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用
解析:选D。A.GA的分子式为C5H8O2,戊二醛可以看作是两个醛基取代了丙烷分子中的两个氢原子,且醛基只能在链端,故符合此分子式的二元醛有4种,A项错误;B.GA分子中含有醛基,可以在加热条件下和新制氢氧化铜反应,B项错误;C.GA分子中含有还原性的基团——醛基,可以被酸性KMnO4氧化而使酸性KMnO4溶液褪色,C项错误;D.由题给信息可知,2%的GA溶液对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用,故2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用,D项正确。
8.香料茉莉酮是一种人工合成的有机化合物,其结构简式为,下列关于茉莉酮的说法正确的是( )
A.该有机化合物的分子式是C10H14O
B.1 mol该有机化合物与H2充分反应,消耗4 mol H2
C.该有机化合物属于不饱和酮类物质,能发生银镜反应
D.该有机化合物能发生加成反应,但不能发生氧化反应
解析:选A。A.由茉莉酮的结构简式可知其分子式为C10H14O,故A正确;B.该有机化合物分子中含有一个酮羰基和两个碳碳双键,则1 mol该有机化合物与H2充分反应,消耗3 mol H2,故B错误;C.该有机化合物属于不饱和酮类物质,不含醛基,不能发生银镜反应,故C错误;D.该有机化合物能发生加成反应,也能发生氧化反应,如碳碳双键能被酸性高锰酸钾溶液氧化、点燃时被氧气氧化等,故D错误。
9.已知:R—CH===CH—O—R′(烃基烯基醚)R—CH2CHO+R′OH。烃基烯基醚A的相对分子质量(Mr)为176,分子中碳、氢原子数目比为3∶4。与A相关的反应如下:
请回答下列问题:
(1)A的分子式为_______________。
(2)B的名称是_______________;A的结构简式为_______________。
(3)写出C→D反应的化学方程式:
________________________________________________________________
________________________________________________________________。
(4)写出两种同时符合下列条件的E的同分异构体的结构简式:___________________________、__________________________________。
①属于芳香醛;②苯环上有两种不同环境的氢原子。
解析:由题给信息,结合与A有关的反应过程可知,A反应生成B和E,E为醛,则B应为醇,由B的相对分子质量(Mr=60)可知,B应为CH3CH2CH2OH,B→C发生了催化氧化反应,由醇转化为醛,则C为CH3CH2CHO,C→D发生了银镜反应,则D为CH3CH2COONH4。由题干信息,结合B、E的结构,可计算分析出A的分子式和结构简式。
(1)结合题给信息,A的分子式可写为(C3H4)nO,则据题意有40n+16=176,解得n=4,故A的分子式为C12H16O。
(2)由上述分析可知,B为CH3CH2CH2OH,名称为正丙醇;由B、E及题给信息,结合(1)中A的分子式,逆推可知A的结构简式为
(3)C→D为丙醛与银氨溶液发生银镜反应,反应方程式为CH3CH2CHO+2[Ag(NH3)2]OH CH3CH2COONH4+2Ag↓+3NH3+H2O。
(4)E的同分异构体符合题述条件的有3种:
答案: (1) C12H16O (2) 正丙醇(或1-丙醇)
(3)CH3CH2CHO+2[Ag(NH3)2]OHCH3CH2COONH4+2Ag↓+3NH3+H2O
(4)
(任选两种)
10.以乙烯为原料可进行如下反应生成高分子C:
回答下列问题:
(1)下列对A物质的描述正确的是_______________(填标号)。
A.不能使酸性高锰酸钾溶液褪色
B.能与新制的氢氧化铜发生反应
C.能发生酯化反应
D.一定条件下能与H2发生反应
(2)B物质的含氧官能团名称为_______________;
(3)化合物D的分子式为_______________。
(4)写出第②步反应的化学方程式:
________________________________________________________________
________________________________________________________________;
写出第③步反应的化学方程式:
________________________________________________________________
________________________________________________________________。
解析:由题图可知,H2C===CH2与Cl2发生加成反应,生成1,2-二氯乙烷(),1,2-二氯乙烷水解生成,发生催化氧化生成A(),A与银氨溶液反应后再酸化得到B(),B在NaOH的水溶液中加热发生水解生成,再经过酸化生成,两分子发生酯化反应生成D(),发生聚合反应生成高分子C。
(1)A为。A.A中含有醛基,可使酸性高锰酸钾溶液褪色,A错误;B.A中含有醛基,能与新制的氢氧化铜发生反应,B正确;C.A中没有羟基和羧基,不能发生酯化反应,C错误;D.A中含有醛基,可与H2发生加成反应,D正确。
(2)B为,含氧官能团为羧基。
(3)化合物D为,分子式为C4H4O4。
(4)第②步反应为的催化氧化反应,化学方程式为;第③步反应为与银氨溶液的反应,化学方程式为
答案:(1)BD (2)羧基 (3)C4H4O4
(4)
[素养提升]
11.已知几种醛的名称与分子式如表所示,下列说法错误的是( )
名称 甲醛 乙醛 丙醛 丁醛 乙二醛 丙二醛 丁二醛
分子式 CH2O C2H4O C3H6O C4H8O C2H2O2 C3H4O2 C4H6O2
A.庚醛的分子式为C7H14O
B.乙二醛的结构简式为OHC—CHO
C.丁二醛有二元醛类同分异构体
D.丙醛与丁二醛有可能互为同系物
解析:选D。A.由表中信息可推知庚醛的分子式为C7H14O,故A正确;B.乙二醛分子中含有两个醛基,故B正确;C.2-甲基丙二醛属于二元醛,与丁二醛互为同分异构体,故C正确;D.两种物质中的官能团数目不同,不可能互为同系物,故D错误。
12.环己酮和乙二醇在一定条件下反应可生成环己酮缩乙二醇,其反应过程如图所示。下列说法不正确的是( )
A.生成环己酮缩乙二醇的反应为加成反应
B.相同质量的有机化合物完全燃烧消耗氧气的量:环己酮>环己酮缩乙二醇
C.环己酮的一氯代物有3种(不包含立体异构)
D.环己酮分子中所有碳原子不可能共平面
解析:选A。A.由题图可知,环己酮和乙二醇在一定条件下反应生成环己酮缩乙二醇和水,则该反应不是加成反应,故A错误;B.环己酮的分子式为C6H10O,98 g环己酮完全燃烧消耗氧气的物质的量为8 mol,环己酮缩乙二醇的分子式为C8H14O2,98 g环己酮缩乙二醇完全燃烧消耗氧气的物质的量为×10.5 mol≈7.25 mol<8 mol,故B正确;C.由结构简式可知,环己酮分子中有3种不同化学环境的氢原子,则一氯代物有3种,故C正确;D.环己酮分子中存在多个饱和碳原子,饱和碳原子的空间结构为四面体形,则分子中所有碳原子不可能共平面,故D正确。
13.(2022·德州高二检测)某有机化合物能跟新制的氢氧化铜反应生成砖红色沉淀,该有机化合物的相对分子质量为44。燃烧该有机化合物2.2 g,生成2.24 L(已换算成标准状况下的体积)二氧化碳。下列说法不正确的是( )
A.该有机化合物是乙醛
B.1 mol该有机化合物能够和 1 mol氢气加成
C.燃烧该有机化合物4.4 g,生成1.8 g水
D.0.01 mol该有机化合物与足量银氨溶液充分反应析出2.16 g金属银
解析:选C。由题给信息可知,该有机化合物分子内含醛基。2.2 g(0.05 mol)该有机化合物中n(C)=0.1 mol,所以该有机化合物为乙醛(CH3CHO),A、B正确;燃烧4.4 g乙醛生成0.2 mol水,即3.6 g水,C错误;0.01 mol 乙醛与足量银氨溶液充分反应析出金属银 2.16 g,D正确。
14.探究甲醛与新制Cu(OH)2的反应:①向6 mL 6 mol·L-1 NaOH溶液中滴加8滴2% CuSO4溶液,振荡,加入0.5 mL 15%甲醛溶液,混合均匀,加热,迅速产生红色沉淀,产生无色气体;②反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解;③相同条件下,甲酸钠溶液与新制Cu(OH)2共热,未观察到明显现象。已知:Cu2O-,甲醛是具有强还原性的气体。下列说法正确的是( )
A.红色沉淀的主要成分不是Cu2O,可能是Cu
B.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO
C.从甲醛的结构推测,其氧化产物可能为碳酸(),因此实验中得到的无色气体中大量含有CO2
D.含有—CHO的有机化合物都可以被新制Cu(OH)2氧化
解析:选A。向6 mL 6 mol·L-1NaOH溶液中滴加8滴2% CuSO4溶液,配制成新制的Cu(OH)2,加入0.5 mL 15% 甲醛溶液,混合均匀,加热,甲醛具有强还原性,与新制的Cu(OH)2发生氧化还原反应,迅速产生红色沉淀,产生无色气体。将所得沉淀洗净后加入浓盐酸,不溶解,根据已知信息:Cu2O[CuCl2]-可知,红色沉淀不是Cu2O,可能是Cu,A正确;甲醛是具有挥发性和强还原性的气体,生成的无色气体中混有甲醛气体,可将灼热的CuO还原为铜单质,得到红色固体,所以不能证明气体中含有CO,B错误;配制新制的氢氧化铜时,NaOH是过量的,在碱性溶液中不可能产生二氧化碳,C错误;根据实验操作③,甲酸钠中也含有醛基,与新制的Cu(OH)2反应,未观察到明显现象,说明含有—CHO的甲酸钠没有被新制Cu(OH)2氧化,D错误。
15.已知:
由A合成D的流程如下:
[Mr(D)=130]
请回答下列问题:
(1)饱和一元醇A中氧元素的质量分数约为21.6%,则A的分子式为____________;结构分析显示A分子中只有一个甲基,A的名称为
________________________________________________________________。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为
________________________________________________________________。
(3)C有____________种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂:____________________________________。
(4)第③步的反应类型为____________;D中所含官能团的名称为____________。
解析:饱和一元醇ROH中,×100%=21.6%,解得Mr(R)≈57,则R为C4H9—,由结构分析可知A为CH3CH2CH2CH2OH,名称为正丁醇或1-丁醇。由流程图知B为CH3CH2CH2CHO,由已知信息知C可能为或
,Mr(C)=126。由流程图知Mr(D)=130,则D为
答案:(1)C4H10O 1-丁醇(或正丁醇)
(2)CH3CH2CH2CHO+2Cu(OH)2+NaOH
CH3CH2CH2COONa+Cu2O↓+3H2O
(3)2 银氨溶液、稀盐酸、溴水(答案合理即可)
(4)还原反应(或加成反应) 羟基
[素养发展目标]
1.认识醛、酮的组成和结构特点、性质、转化关系及其在生产生活中的应用。
2.从官能团、化学键的角度分析和推断醛类的化学性质,能通过实验探究乙醛与银氨溶液、新制氢氧化铜的反应,培养科学探究与创新意识的学科核心素养。
3.结合生产、生活实际了解醛、酮对环境和健康可能产生的影响。
知识点一 乙醛
1.醛的结构、组成
2.乙醛的结构
分子式 结构式 结构简式 分子结构模型
C2H4O CH3CHO
3.乙醛的物理性质
乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点20.8 ℃,易挥发,易燃烧,能与水、乙醇等互溶。
4.乙醛的化学性质
(1)加成反应
①催化加氢(还原反应):CH3CHO+H2CH3CH2OH(填化学方程式,下同)。
②与HCN加成:CH3CHO+HCN―→CH3CH(OH)CN。
(2)氧化反应
①银镜反应:CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O。
②与新制Cu(OH)2的反应:CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O。
③催化氧化:2CH3CHO+O22CH3COOH。
④燃烧:2CH3CHO+5O24CO2+4H2O。
实验Ⅰ:在洁净的试管中加入1 mL 2%AgNO3溶液,然后边振荡试管边逐滴滴入2%氨水,使最初产生的沉淀溶解,制得银氨溶液。再滴入3滴乙醛,振荡后将试管放在热水浴中温热。
实验Ⅱ:在试管里加入2 mL 10%NaOH溶液,加入5滴5% CuSO4溶液,得到新制的Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热。
(1)实验Ⅰ中③装置和实验Ⅱ中③装置分别有什么现象?
(2)写出实验Ⅰ中①③和实验Ⅱ中①③中所发生反应的化学方程式。
(3)推测:乙醛能使溴水或酸性KMnO4溶液褪色吗?为什么?
提示:(1)实验Ⅰ中③装置:水浴加热一段时间后,试管内壁出现一层光亮的银镜;实验Ⅱ中③装置:加热至沸腾后,有砖红色沉淀产生。
(2)实验Ⅰ中①:AgNO3+NH3·H2O===AgOH↓+NH4NO3,AgOH+2NH3·H2O===[Ag(NH3)2]OH+2H2O;
③:CH3CHO+2[Ag(NH3)2]OH2Ag↓+CH3COONH4+3NH3+H2O。
实验Ⅱ中①:2NaOH+CuSO4===Cu(OH)2↓+Na2SO4;
③:CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O。
(3)能。因为醛基有较强的还原性,能被[Ag(NH3)2]OH溶液或新制Cu(OH)2等弱氧化剂氧化。而溴水或酸性KMnO4溶液的氧化能力比[Ag(NH3)2]OH溶液、新制Cu(OH)2强得多,故溴水、酸性KMnO4溶液也能氧化乙醛,自身被还原,从而使溶液褪色。
1.银镜反应实验注意事项
(1)试管要洁净,洗涤试管时一般要先用热的NaOH溶液洗,再用水洗。
(2)银氨溶液必须现用现配,不可久置,否则会生成易爆物质。
(3)配制银氨溶液时,氨水、硝酸银溶液都必须是稀溶液,且是将稀氨水逐滴加入稀硝酸银溶液中(顺序不能颠倒),直到最初产生的沉淀恰好溶解,氨水不能过量,否则也会生成易爆物质。
(4)银镜反应的条件是水浴加热,不能直接加热,加热时不可振荡或摇动试管,以防生成黑色的银,而不能在试管内壁形成光亮的银镜。
(5)实验结束后,试管内壁附着的银镜,可用稀硝酸浸泡,待银溶解后再用自来水、蒸馏水洗涤干净。
2.乙醛与新制Cu(OH)2反应实验注意事项
(1)所用Cu(OH)2悬浊液必须是新制备的。
(2)配制Cu(OH)2悬浊液时,必须保证NaOH溶液过量,即保证所得溶液呈碱性。
(3)用酒精灯直接加热试管至溶液沸腾,才有明显的砖红色沉淀产生。
(4)加热煮沸时间不能过久,否则会导致Cu(OH)2分解成CuO而出现黑色沉淀。
3.醛基的检验
在洁净的试管中加入新制银氨溶液和少量试样后,水浴加热,有银镜生成,或在洁净的试管中加入少量试样和新制的Cu(OH)2,加热煮沸,有砖红色沉淀生成。
1.(2022·北京八中高二阶段练习)下列有机化合物中,属于醛类的是( )
A.(CH3)2CHOH
C.CH3CH2COOH D.HCOOCH3
答案:B
2.下列说法正确的是( )
A.乙醛的分子式为CH3CHO
B.乙醛的结构简式为CH3CHO
C.乙醛是一种有刺激性气味的气体
D.乙醛不溶于有机溶剂,也不溶于水
答案:B
3.某学生做乙醛的还原性实验时(如图),加热至沸腾,未观察到砖红色沉淀,分析其原因可能是( )
A.乙醛的量不足 B.烧碱的量不足
C.硫酸铜的量不足 D.加热时间短
解析:选B。乙醛还原氢氧化铜的实验要求在碱性环境中进行,而题中所给NaOH的量不足。硫酸铜过量时,其水解会使溶液呈酸性,导致实验失败。
4.(2022·陕西黄陵中学高二期末)下列有关银镜反应实验的说法中正确的是( )
A.生成银镜过程中需用玻璃棒均匀搅拌
B.向2%氨水中滴入2%硝酸银溶液,配得银氨溶液
C.采用水浴加热,不能直接加热
D.可用浓盐酸洗去银镜
解析:选C。A.生成银镜过程中不能用玻璃棒搅拌,故A错误;B.配制银氨溶液时,向2%硝酸银溶液中滴入2%氨水,边加边振荡,至最初产生的沉淀恰好溶解,即得银氨溶液,故B错误;C.水浴加热能保证试管受热均匀,且易于控制反应温度,直接加热受热不均匀,不利于银镜的生成,故C正确;D.银和浓盐酸不反应,需要用稀硝酸洗去银镜,故D错误。
知识点二 醛类
1.甲醛与苯甲醛
甲醛(蚁醛) 苯甲醛(苦杏仁油)
结构简式 HCHO
色、味、态 无色、有强烈刺激性气味的气体 无色、有苦杏仁气味的液体
溶解性 易溶于水 微溶于水,能与苯、乙醇等互溶
用途 重要的化工原料,能合成多种有机化合物;其水溶液(又称福尔马林)具有杀菌、防腐性能,可用于消毒和制作生物标本 制造染料、香料及药物的重要原料
2.醛类的化学性质
醛类分子中都含有醛基(—CHO),所以化学性质与乙醛的相似。一般情况下,醛能被还原为醇,被氧化为羧酸,可以发生银镜反应,能与氰化氢加成。
(1)加成反应
R—CHO+H2R—CH2—OH;
R—CHO+HCN―→R—CH(OH)CN。
(2)氧化反应
银镜反应 RCHO+2[Ag(NH3)2]OH2Ag↓+RCOONH4+3NH3+H2O
与新制的Cu(OH)2反应 RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O
催化氧化 2RCHO+O22RCOOH
在中国家庭中肉桂是炖肉、炒菜重要的调味品,在西方人们更是将肉桂打成粉末加入咖啡中调味。由于它是含有特殊芳香气味的植物,肉桂还可以制作比较特殊的香料。科学家已发现,肉桂中的肉桂醛是一种赋予肉桂独特风味的有机化合物,结构简式为
(1)肉桂醛具有醛类物质的通性。请写出其与银氨溶液、新制的Cu(OH)2反应的化学方程式。
(2)1 mol 肉桂醛完全氢化需要氢气的物质的量是多少?
(3)1 mol 肉桂醛充分进行银镜反应生成Ag的物质的量是多少?1 mol 甲醛呢?
提示:(1)
(2)5 mol。
(3)1 mol 肉桂醛充分进行银镜反应生成Ag的物质的量是2 mol,1 mol 甲醛充分进行银镜反应生成Ag的物质的量是4 mol。
1.醛的氧化与还原规律
RCH2OHRCHORCOOH
2.相关定量计算
(1)一元醛发生银镜反应或与新制的Cu(OH)2反应时,定量关系如下:
(2)甲醛发生氧化反应时,可以理解为
所以,甲醛分子中相当于有2个—CHO,与足量的银氨溶液或新制的Cu(OH)2反应时,存在如下定量关系:
1 mol HCHO~4 mol Ag,1 mol HCHO~4 mol Cu(OH)2~2 mol Cu2O。
1.下列关于醛的说法不正确的是( )
A.甲醛是甲基跟醛基相连而构成的醛
B.醛的官能团是—CHO
C.甲醛和丙醛互为同系物
D.饱和一元脂肪醛的通式为CnH2nO(n≥1,n为整数)
解析:选A。A.甲醛的结构简式为HCHO,即甲醛分子中不含烃基,甲醛是氢原子跟醛基相连而构成的醛,故A错误;B.醛的官能团是醛基,即—CHO,故B正确;C.甲醛的结构简式为HCHO,丙醛的结构简式为CH3CH2CHO,甲醛和丙醛结构相似,分子组成相差两个CH2原子团,互为同系物,故C正确;D.饱和一元脂肪醛是指含有一个醛基,烃基中不存在不饱和键的醛,则饱和一元脂肪醛的通式为CnH2nO(n≥1,n为整数),故D正确。
2.某有机化合物的结构简式为CH2===CH—CH2—CHO,下列对其化学性质的判断中错误的是( )
A.能被银氨溶液氧化
B.能使酸性KMnO4溶液褪色
C.1 mol该有机化合物能与2 mol Br2发生加成反应
D.1 mol该有机化合物能与2 mol H2发生加成反应
解析:选C。A.该有机化合物分子中含有醛基,故能被银氨溶液氧化;B.该有机化合物分子中含有碳碳双键和醛基,能使酸性高锰酸钾溶液褪色;C.该有机化合物分子中只有一个碳碳双键,故1 mol该有机化合物只能与1 mol Br2发生加成反应;D.该有机化合物分子中含有醛基和碳碳双键,故1 mol该有机化合物能与2 mol H2发生加成反应。
3.下列各化合物中,能发生酯化、还原、加成、消去四种反应的是( )
A.CH3CH===CHCHO
答案:C
4.丙醛和另一种组成为CnH2nO的物质X的混合物3.2 g,与足量的银氨溶液作用后析出10.8 g银,则混合物中所含X不可能是( )
A.甲基丙醛 B.丙酮()
C.乙醛 D.丁醛
解析:选C。反应中生成银的物质的量是10.8 g÷108 g/mol=0.1 mol,根据方程式RCHO+2[Ag(NH3)2]OHRCOONH4+2Ag↓+3NH3+H2O可知,消耗醛的物质的量是0.05 mol,则混合物的平均相对分子质量是3.2÷0.05=64;丙醛的相对分子质量为58<64,所以另一种是相对分子质量大于64的醛,或是不发生银镜反应的其他物质。A.甲基丙醛的相对分子质量大于64,甲基丙醛可能;B.丙酮不能发生银镜反应,丙酮可能;C.乙醛的相对分子质量小于64,乙醛不可能;D.丁醛的相对分子质量大于64,丁醛可能。
知识点三 酮
1.概念
2.丙酮()——最简单的酮
(1)物理性质
丙酮是无色透明的液体,沸点56.2 ℃,易挥发,能与水、乙醇等互溶。
(2)化学性质
①催化加氢反应:在催化剂存在的条件下,丙酮可以发生催化加氢反应,生成2-丙醇,化学方程式为。
②氧化反应:丙酮能燃烧,被氧气氧化,但不能被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化。
(3)用途
丙酮可用作化学纤维、钢瓶储存乙炔等的溶剂,还用于生产有机玻璃、农药和涂料等。
1.下列有关丙酮的说法正确的是( )
A.是乙醛的同系物
B.可从水中萃取出单质碘
C.与CH3CH2CHO互为同分异构体
D.不易燃烧
解析:选C。A.丙酮与乙醛所含的官能团不同,二者不互为同系物,故A错误;B.丙酮易溶于水,不能从水中萃取出单质碘,故B错误;C.丙酮与CH3CH2CHO的分子式均为C3H6O,但结构不同,二者互为同分异构体,故C正确;D.丙酮能燃烧,故D错误。
2.下列醛、酮的反应属于还原反应的是( )
A.醛的银镜反应
B.醛在空气中久置变质
C.由2-丁酮制备2-丁醇
D.乙醛与新制的氢氧化铜加热有砖红色沉淀产生
解析:选C。A.醛的银镜反应属于醛的氧化反应,A项错误;B.醛在空气中久置变质,属于醛的氧化反应,B项错误;C.由2-丁酮制备2-丁醇,羰基加氢变为羟基,属于酮的还原反应,C项正确;D.乙醛与新制的氢氧化铜加热有砖红色沉淀产生,属于醛的氧化反应,D项错误。
1.(2022·上海奉贤高二阶段练习)下列关于甲醛的描述错误的是( )
A.结构式:
B.电子式:
C.是极性分子
D.球棍模型:
解析:选B。A.甲醛中C、O原子形成双键,C、H原子以单键相连,结构式为,A正确;B.C、O之间形成的是共价双键,且O原子最外层有8个电子,电子式为,B错误;C.根据甲醛的结构式可知其正负电中心不重合,为极性分子,C正确;D.原子半径:C>O>H,结合结构式可知球棍模型为,D正确。
2.(2022·吉林希望高中高二阶段练习)下列说法中,正确的是( )
A.甲醛、乙醛分子中的所有原子都在同一平面上
B.甲醛、乙醛在常温下都是无色有刺激性气味的液体
C.乙醛、丙醛都没有同分异构体
D.醛类既能被氧化为羧酸又能被还原为醇
解析:选D。A.乙醛分子中含有—CH3,所有原子不可能在同一平面上,A不正确;B.甲醛在常温常压下是无色、有刺激性气味的气体,B不正确;C.丙醛与丙酮互为同分异构体,C不正确;D.醛类都含有—CHO,既能被氧化剂(如O2、酸性KMnO4溶液等)氧化为羧酸,又能被还原剂(如H2等)还原为醇,D正确。
3.下列四个反应中,有机化合物发生的反应与其他三个反应类型不同的是( )
A.CH3CHO+H2CH3CH2OH
B.CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O
C.CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O
D.2CH3CHO+O22CH3COOH
解析:选A。A.该反应是乙醛的加成反应,属于还原反应;B.该反应是银镜反应,属于乙醛的氧化反应;C.该反应是乙醛的氧化反应;D.该反应是乙醛的氧化反应。
4.(2022·吉林二中高二阶段练习)只用一种试剂就可鉴别甲酸、乙酸、乙醛、乙醇,这种试剂是( )
A.银氨溶液 B.新制的Cu(OH)2
C.石蕊溶液 D.Na2CO3溶液
解析:选B。A.乙酸与银氨溶液反应没有明显现象,乙醇与银氨溶液不反应,不能鉴别,故A错误。B.甲酸与新制的氢氧化铜反应,变为蓝色溶液,甲酸分子中含有醛基,与新制的氢氧化铜共热会产生砖红色沉淀并有气泡产生;乙酸溶解氢氧化铜,溶液呈蓝色;乙醛具有还原性,与新制的氢氧化铜共热会产生砖红色沉淀;乙醇与新制的氢氧化铜混合后无明显现象;四种溶液现象各不相同,能鉴别,故B正确。C.石蕊溶液为酸碱指示剂,与甲酸和乙酸混合,溶液均呈红色,但无法进一步鉴别,故C错误。D.Na2CO3溶液与乙酸、甲酸反应生成气体,但与乙醛和乙醇不反应,无法全部鉴别,故D错误。
5.柠檬醛是一种具有柠檬香味的有机化合物,广泛存在于香精油中,是食品工业中重要的调味品,且可用于合成维生素A。已知柠檬醛的结构简式如下:
(1)试推测柠檬醛可能发生的反应有_________(填字母)。
①能使溴的四氯化碳溶液褪色
②能与乙醇发生酯化反应
③能发生银镜反应
④能与新制的Cu(OH)2反应
⑤能使酸性KMnO4溶液褪色
A.①③④ B.①②④⑤
C.①③④⑤ D.①②③④⑤
(2)检验柠檬醛分子中含有醛基的方法为
________________________________________________________________
________________________________________________________________,
发生反应的化学方程式为
________________________________________________________________
________________________________________________________________。
(3)检验柠檬醛分子中含有碳碳双键的方法为
________________________________________________________________
________________________________________________________________
________________________________________________________________。
解析:(1)由柠檬醛的结构简式可知其所含官能团为、—CHO。①CC可与Br2发生加成反应,从而使溴的四氯化碳溶液褪色;②分子中无—COOH,不能与C2H5OH发生酯化反应;分子中有—CHO,可以发生③④反应;⑤与—CHO均可以使酸性KMnO4溶液褪色。(2)常利用银镜反应或与新制的Cu(OH)2的反应检验—CHO的存在。(3)当—CHO与同时出现时,应先检验并除去—CHO ,再检验;常用溴的CCl4溶液或酸性KMnO4 溶液来检验的存在。
答案:(1)C
(2)加入银氨溶液后水浴加热,有银镜出现,则含有醛基
+3NH3+H2O(答案合理即可)
(3)在加银氨溶液[或新制的Cu(OH)2]氧化醛基后,调节溶液pH至酸性,再加入溴的四氯化碳溶液(或酸性 KMnO4溶液),若溶液褪色说明含有碳碳双键
[基础检测]
1.下列物质中不属于醛的是( )
A.①③ B.②④
C.②③ D.①④
答案:B
2.不能由醛或酮加氢还原制得的醇是( )
解析:选D。A. 中羟基相连的碳原子上有1个氢原子,说明可以由酮加氢还原制得,A不符合题意;B.CH3CH2CH2OH中与羟基相连的碳原子上有2个氢原子,能够由醛加氢还原制得,B不符合题意;C. 中与羟基相连的碳原子上有2个氢原子,能够由醛加氢还原制得,C不符合题意;D. 中与羟基相连的碳原子上没有氢原子,不能由醛或酮加氢还原制得,D符合题意。
3.将CH3CHO (易溶于水,沸点为20.8 ℃的易挥发性液体)和CH3COOH分离的最佳方法是( )
A.加热蒸馏
B.加入Na2CO3后,通过萃取的方法分离
C.加入烧碱溶液之后蒸出乙醛,再加入硫酸,蒸出乙酸
D.和Na反应后进行分离
解析:选C。A.乙酸易挥发,直接蒸馏得不到纯净物,A不符合题意;B.乙酸与碳酸钠反应后,与乙醛混溶,不能萃取分离,B不符合题意;C.先加入烧碱溶液,乙酸与NaOH反应生成的乙酸钠可增大与乙醛的沸点差异,蒸馏时先蒸出乙醛,再加入H2SO4,使乙酸钠与其反应再生成乙酸,然后蒸出乙酸,C符合题意;D.乙酸与Na反应生成乙酸钠,分离混合物应再使乙酸钠转化为乙酸,D不符合题意。
4.(2022·秦皇岛一中高二开学考试)已知两个醛分子在 NaOH 溶液作用下可以发生如下的加成反应,生成羟基醛:。如果将甲醛、乙醛、丙醛在 NaOH 溶液中发生反应,最多可以形成几种羟基醛( )
A.6 种 B.7 种
C.8 种 D.9 种
解析:选A。根据题干信息可知,甲醛自身不能发生加成反应,乙醛与丙醛在NaOH溶液中可以发生同种醛的加成,产物有2种,即CH3CH(OH)CH2CHO、CH3CH2CH(OH)CH(CH3)CHO,甲醛与乙醛、甲醛与丙醛反应分别生成1种产物,即HOCH2CH2CHO、HOCH2CH(CH3)CHO,乙醛和丙醛反应将得到2种产物,即CH3CH(OH)CH(CH3)CHO、CH3CH2CH(OH)CH2CHO,共6种,故答案为A。
5.(2022·重庆高二阶段练习)乙醛的银镜反应实验步骤如下:
步骤1:向试管中加入1 mL 2% AgNO3溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤3:再向试管中加入1 mL 10%乙醛溶液,振荡,在60~70 ℃水浴中加热,观察到试管内壁形成了光亮银镜。
下列说法不正确的是( )
A.步骤1中观察到的白色沉淀为AgOH
B.步骤2中沉淀溶解是因为生成[Ag(NH3)2]+
C.步骤3中产生银镜说明乙醛被还原
D.试管内壁的银镜可以用稀硝酸洗去
解析:选C。A.氨水少量时,氨水中一水合氨电离出的氢氧根离子和银离子结合成白色的AgOH沉淀,因此步骤1中观察到的白色沉淀为AgOH,A正确;B.AgOH与NH3·H2O反应生成[Ag(NH3)2]OH而溶解,AgOH转变成[Ag(NH3)2]+,B正确;C.[Ag(NH3)2]OH和乙醛发生银镜反应生成Ag,Ag元素化合价降低,被还原,而乙醛发生氧化反应,被氧化,C错误;D.因硝酸具有强氧化性,能溶解Ag,试管内壁的银镜可用稀硝酸洗去, D正确。
6.(2022·蚌埠二中高二期中)某有机化合物的分子式为C5H9BrO,能够与新制的氢氧化铜反应产生砖红色沉淀的同分异构体种数为( )
A.8种 B.9种
C.10种 D.12种
解析:选D。能够与新制的氢氧化铜反应产生砖红色沉淀,说明含有—CHO,该分子的不饱和度为1,共有:(数字表示—CHO位置,后同)、、、,共4+4+3+1=12种,故选D。
7.1,5-戊二醛(简称GA)是一种重要的饱和直链二元醛。2%的GA溶液具有广谱、高效、无刺激、无腐蚀等特点,对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用。下列说法正确的是( )
A.GA的分子式为C5H10O2,符合此分子式的二元醛有2种
B.GA不能在加热条件下和新制氢氧化铜反应
C.GA不能使酸性KMnO4溶液褪色
D.2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用
解析:选D。A.GA的分子式为C5H8O2,戊二醛可以看作是两个醛基取代了丙烷分子中的两个氢原子,且醛基只能在链端,故符合此分子式的二元醛有4种,A项错误;B.GA分子中含有醛基,可以在加热条件下和新制氢氧化铜反应,B项错误;C.GA分子中含有还原性的基团——醛基,可以被酸性KMnO4氧化而使酸性KMnO4溶液褪色,C项错误;D.由题给信息可知,2%的GA溶液对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用,故2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用,D项正确。
8.香料茉莉酮是一种人工合成的有机化合物,其结构简式为,下列关于茉莉酮的说法正确的是( )
A.该有机化合物的分子式是C10H14O
B.1 mol该有机化合物与H2充分反应,消耗4 mol H2
C.该有机化合物属于不饱和酮类物质,能发生银镜反应
D.该有机化合物能发生加成反应,但不能发生氧化反应
解析:选A。A.由茉莉酮的结构简式可知其分子式为C10H14O,故A正确;B.该有机化合物分子中含有一个酮羰基和两个碳碳双键,则1 mol该有机化合物与H2充分反应,消耗3 mol H2,故B错误;C.该有机化合物属于不饱和酮类物质,不含醛基,不能发生银镜反应,故C错误;D.该有机化合物能发生加成反应,也能发生氧化反应,如碳碳双键能被酸性高锰酸钾溶液氧化、点燃时被氧气氧化等,故D错误。
9.已知:R—CH===CH—O—R′(烃基烯基醚)R—CH2CHO+R′OH。烃基烯基醚A的相对分子质量(Mr)为176,分子中碳、氢原子数目比为3∶4。与A相关的反应如下:
请回答下列问题:
(1)A的分子式为_______________。
(2)B的名称是_______________;A的结构简式为_______________。
(3)写出C→D反应的化学方程式:
________________________________________________________________
________________________________________________________________。
(4)写出两种同时符合下列条件的E的同分异构体的结构简式:___________________________、__________________________________。
①属于芳香醛;②苯环上有两种不同环境的氢原子。
解析:由题给信息,结合与A有关的反应过程可知,A反应生成B和E,E为醛,则B应为醇,由B的相对分子质量(Mr=60)可知,B应为CH3CH2CH2OH,B→C发生了催化氧化反应,由醇转化为醛,则C为CH3CH2CHO,C→D发生了银镜反应,则D为CH3CH2COONH4。由题干信息,结合B、E的结构,可计算分析出A的分子式和结构简式。
(1)结合题给信息,A的分子式可写为(C3H4)nO,则据题意有40n+16=176,解得n=4,故A的分子式为C12H16O。
(2)由上述分析可知,B为CH3CH2CH2OH,名称为正丙醇;由B、E及题给信息,结合(1)中A的分子式,逆推可知A的结构简式为
(3)C→D为丙醛与银氨溶液发生银镜反应,反应方程式为CH3CH2CHO+2[Ag(NH3)2]OH CH3CH2COONH4+2Ag↓+3NH3+H2O。
(4)E的同分异构体符合题述条件的有3种:
答案: (1) C12H16O (2) 正丙醇(或1-丙醇)
(3)CH3CH2CHO+2[Ag(NH3)2]OHCH3CH2COONH4+2Ag↓+3NH3+H2O
(4)
(任选两种)
10.以乙烯为原料可进行如下反应生成高分子C:
回答下列问题:
(1)下列对A物质的描述正确的是_______________(填标号)。
A.不能使酸性高锰酸钾溶液褪色
B.能与新制的氢氧化铜发生反应
C.能发生酯化反应
D.一定条件下能与H2发生反应
(2)B物质的含氧官能团名称为_______________;
(3)化合物D的分子式为_______________。
(4)写出第②步反应的化学方程式:
________________________________________________________________
________________________________________________________________;
写出第③步反应的化学方程式:
________________________________________________________________
________________________________________________________________。
解析:由题图可知,H2C===CH2与Cl2发生加成反应,生成1,2-二氯乙烷(),1,2-二氯乙烷水解生成,发生催化氧化生成A(),A与银氨溶液反应后再酸化得到B(),B在NaOH的水溶液中加热发生水解生成,再经过酸化生成,两分子发生酯化反应生成D(),发生聚合反应生成高分子C。
(1)A为。A.A中含有醛基,可使酸性高锰酸钾溶液褪色,A错误;B.A中含有醛基,能与新制的氢氧化铜发生反应,B正确;C.A中没有羟基和羧基,不能发生酯化反应,C错误;D.A中含有醛基,可与H2发生加成反应,D正确。
(2)B为,含氧官能团为羧基。
(3)化合物D为,分子式为C4H4O4。
(4)第②步反应为的催化氧化反应,化学方程式为;第③步反应为与银氨溶液的反应,化学方程式为
答案:(1)BD (2)羧基 (3)C4H4O4
(4)
[素养提升]
11.已知几种醛的名称与分子式如表所示,下列说法错误的是( )
名称 甲醛 乙醛 丙醛 丁醛 乙二醛 丙二醛 丁二醛
分子式 CH2O C2H4O C3H6O C4H8O C2H2O2 C3H4O2 C4H6O2
A.庚醛的分子式为C7H14O
B.乙二醛的结构简式为OHC—CHO
C.丁二醛有二元醛类同分异构体
D.丙醛与丁二醛有可能互为同系物
解析:选D。A.由表中信息可推知庚醛的分子式为C7H14O,故A正确;B.乙二醛分子中含有两个醛基,故B正确;C.2-甲基丙二醛属于二元醛,与丁二醛互为同分异构体,故C正确;D.两种物质中的官能团数目不同,不可能互为同系物,故D错误。
12.环己酮和乙二醇在一定条件下反应可生成环己酮缩乙二醇,其反应过程如图所示。下列说法不正确的是( )
A.生成环己酮缩乙二醇的反应为加成反应
B.相同质量的有机化合物完全燃烧消耗氧气的量:环己酮>环己酮缩乙二醇
C.环己酮的一氯代物有3种(不包含立体异构)
D.环己酮分子中所有碳原子不可能共平面
解析:选A。A.由题图可知,环己酮和乙二醇在一定条件下反应生成环己酮缩乙二醇和水,则该反应不是加成反应,故A错误;B.环己酮的分子式为C6H10O,98 g环己酮完全燃烧消耗氧气的物质的量为8 mol,环己酮缩乙二醇的分子式为C8H14O2,98 g环己酮缩乙二醇完全燃烧消耗氧气的物质的量为×10.5 mol≈7.25 mol<8 mol,故B正确;C.由结构简式可知,环己酮分子中有3种不同化学环境的氢原子,则一氯代物有3种,故C正确;D.环己酮分子中存在多个饱和碳原子,饱和碳原子的空间结构为四面体形,则分子中所有碳原子不可能共平面,故D正确。
13.(2022·德州高二检测)某有机化合物能跟新制的氢氧化铜反应生成砖红色沉淀,该有机化合物的相对分子质量为44。燃烧该有机化合物2.2 g,生成2.24 L(已换算成标准状况下的体积)二氧化碳。下列说法不正确的是( )
A.该有机化合物是乙醛
B.1 mol该有机化合物能够和 1 mol氢气加成
C.燃烧该有机化合物4.4 g,生成1.8 g水
D.0.01 mol该有机化合物与足量银氨溶液充分反应析出2.16 g金属银
解析:选C。由题给信息可知,该有机化合物分子内含醛基。2.2 g(0.05 mol)该有机化合物中n(C)=0.1 mol,所以该有机化合物为乙醛(CH3CHO),A、B正确;燃烧4.4 g乙醛生成0.2 mol水,即3.6 g水,C错误;0.01 mol 乙醛与足量银氨溶液充分反应析出金属银 2.16 g,D正确。
14.探究甲醛与新制Cu(OH)2的反应:①向6 mL 6 mol·L-1 NaOH溶液中滴加8滴2% CuSO4溶液,振荡,加入0.5 mL 15%甲醛溶液,混合均匀,加热,迅速产生红色沉淀,产生无色气体;②反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解;③相同条件下,甲酸钠溶液与新制Cu(OH)2共热,未观察到明显现象。已知:Cu2O-,甲醛是具有强还原性的气体。下列说法正确的是( )
A.红色沉淀的主要成分不是Cu2O,可能是Cu
B.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO
C.从甲醛的结构推测,其氧化产物可能为碳酸(),因此实验中得到的无色气体中大量含有CO2
D.含有—CHO的有机化合物都可以被新制Cu(OH)2氧化
解析:选A。向6 mL 6 mol·L-1NaOH溶液中滴加8滴2% CuSO4溶液,配制成新制的Cu(OH)2,加入0.5 mL 15% 甲醛溶液,混合均匀,加热,甲醛具有强还原性,与新制的Cu(OH)2发生氧化还原反应,迅速产生红色沉淀,产生无色气体。将所得沉淀洗净后加入浓盐酸,不溶解,根据已知信息:Cu2O[CuCl2]-可知,红色沉淀不是Cu2O,可能是Cu,A正确;甲醛是具有挥发性和强还原性的气体,生成的无色气体中混有甲醛气体,可将灼热的CuO还原为铜单质,得到红色固体,所以不能证明气体中含有CO,B错误;配制新制的氢氧化铜时,NaOH是过量的,在碱性溶液中不可能产生二氧化碳,C错误;根据实验操作③,甲酸钠中也含有醛基,与新制的Cu(OH)2反应,未观察到明显现象,说明含有—CHO的甲酸钠没有被新制Cu(OH)2氧化,D错误。
15.已知:
由A合成D的流程如下:
[Mr(D)=130]
请回答下列问题:
(1)饱和一元醇A中氧元素的质量分数约为21.6%,则A的分子式为____________;结构分析显示A分子中只有一个甲基,A的名称为
________________________________________________________________。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为
________________________________________________________________。
(3)C有____________种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂:____________________________________。
(4)第③步的反应类型为____________;D中所含官能团的名称为____________。
解析:饱和一元醇ROH中,×100%=21.6%,解得Mr(R)≈57,则R为C4H9—,由结构分析可知A为CH3CH2CH2CH2OH,名称为正丁醇或1-丁醇。由流程图知B为CH3CH2CH2CHO,由已知信息知C可能为或
,Mr(C)=126。由流程图知Mr(D)=130,则D为
答案:(1)C4H10O 1-丁醇(或正丁醇)
(2)CH3CH2CH2CHO+2Cu(OH)2+NaOH
CH3CH2CH2COONa+Cu2O↓+3H2O
(3)2 银氨溶液、稀盐酸、溴水(答案合理即可)
(4)还原反应(或加成反应) 羟基
