3.1.1认识有机化合物的一般性质(教学课件)(共24张PPT)——2022-2023学年高一化学鲁科版(2019)必修第二册
文档属性
| 名称 | 3.1.1认识有机化合物的一般性质(教学课件)(共24张PPT)——2022-2023学年高一化学鲁科版(2019)必修第二册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-27 00:00:00 | ||
图片预览






文档简介
(共24张PPT)
第3章 简单的有机化合物
第1节 认识有机化合物
第1课时 认识有机化合物的一般性质
碳原子的成键特点
【核心素养目标】
1. 能从元素组成、结构、性质等角度概括有机化合物的共同点,知道有机化合物分子是有空间结构的,知道有机化合物与无机物的差异。
2. 以烷烃为例发现有机化合物中同系物的存在,能够对简单的有机化合物进行分类。
3. 以甲烷、乙烯、乙炔、苯为例认识碳原子的成键特点,能概括常见有机化合物中碳原子的成键类型。能描述甲烷、乙烯、乙炔的分子结构特征并能搭建甲烷和乙烷的立体模型。
【重难点】
碳原子成键特点
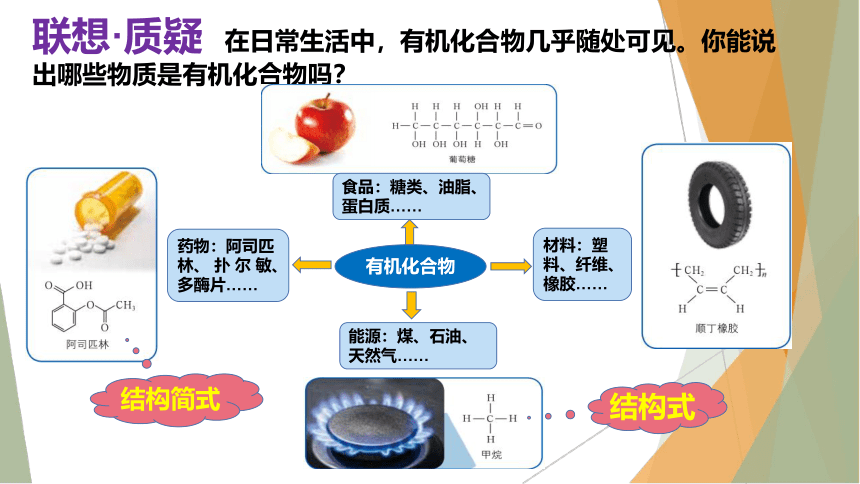
联想·质疑 在日常生活中,有机化合物几乎随处可见。你能说出哪些物质是有机化合物吗?
有机化合物
食品:糖类、油脂、
蛋白质……
能源:煤、石油、
天然气……
药物:阿司匹林、 扑 尔 敏、
多酶片……
材料:塑料、纤维、橡胶……
结构式
结构简式
一、认识有机化合物的一般性质
1.概念
有机化合物是指大多数含有 元素的化合物
碳
思考:含碳元素的化合物一定是有机化合物吗?
不一定,少数含碳化合物如:CO、CO2、H2CO3、碳酸盐、
碳酸氢盐等,由于它们的组成与性质更接近于无机物,
因此仍把它们归为无机物
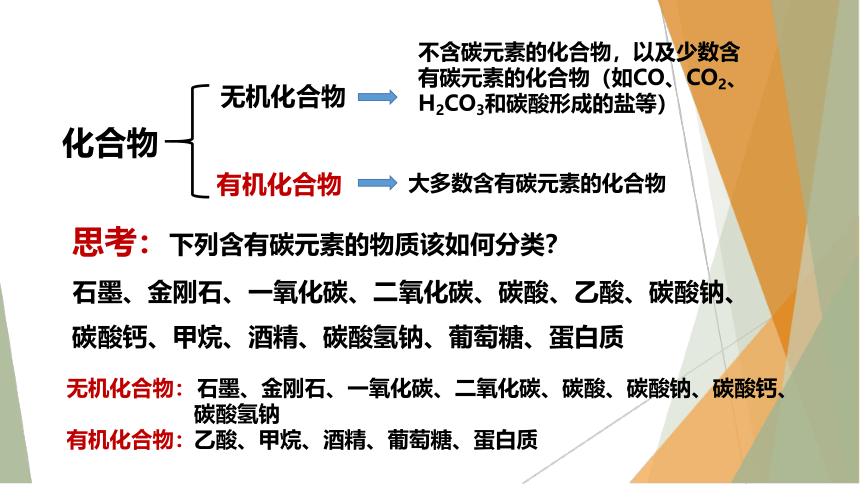
化合物
大多数含有碳元素的化合物
无机化合物
有机化合物
不含碳元素的化合物,以及少数含有碳元素的化合物(如CO、CO2、H2CO3和碳酸形成的盐等)
思考:下列含有碳元素的物质该如何分类?
石墨、金刚石、一氧化碳、二氧化碳、碳酸、乙酸、碳酸钠、碳酸钙、甲烷、酒精、碳酸氢钠、葡萄糖、蛋白质
石墨、金刚石、一氧化碳、二氧化碳、碳酸、碳酸钠、碳酸钙、
碳酸氢钠
乙酸、甲烷、酒精、葡萄糖、蛋白质
无机化合物:
有机化合物:
观察·思考(课本P77页)
生活中的许多物质都是有机化合物或由有机化合物组成的混合物,如酒精、汽油、植物油、聚乙烯塑料等。有机化合物通常会有哪些性质?请通过观察下列实验的现象,了解有机化合物的性质。
【实验 1】用棉签蘸取酒精,涂抹在手上,观察现象并感受能量变化。
【实验 2】向两支试管中加入适量水,然后分别加入体积相近的汽油和酒精,振荡试管,观察现象。
【实验 3】用坩埚钳夹取一片聚乙烯塑料,置于酒精灯火焰上加热至燃烧,观察现象。
【实验 4】向试管中加入适量碘水,再滴入适量植物油,振荡后静置,观察现象。
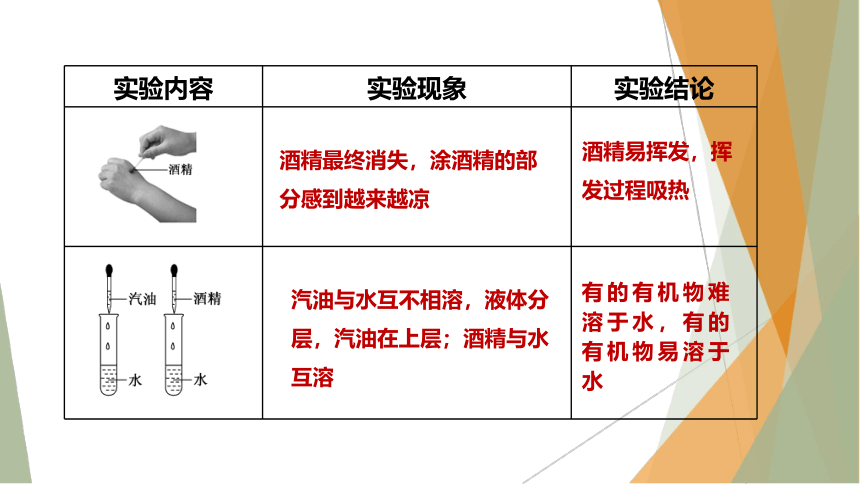
实验内容 实验现象 实验结论
酒精最终消失,涂酒精的部分感到越来越凉
酒精易挥发,挥发过程吸热
汽油与水互不相溶,液体分层,汽油在上层;酒精与水互溶
有的有机物难溶于水,有的有机物易溶于水
实验内容 实验现象 实验结论
火焰明亮,冒黑烟
液体分层,水层变为无色,植物油层在上层,为紫红色
碘更易溶于植物油(有机溶剂)
聚乙烯塑料易燃烧
思考:根据以上实验你能得出哪些结论?这些实验对你认识有机化合物的性质有何启示?
2.有机化合物一般性质(课本P77页)
共性:熔点较低,常温下多为固态或液态
一般难溶于水,易溶于有机溶剂
绝大多数受热易分解,容易燃烧
差异性:
挥发性:乙醇、苯易挥发,甘油难挥发
溶解性:大多数难溶于水,有的易溶于水如酒精、乙酸
热稳定性:大多受热易分解,如聚乙烯
有的具有较强热稳定性 ,如酚醛树脂
特性:乙醇可以被高锰酸钾氧化而使紫色酸性 KMnO4 溶液褪色
阻燃保温材料
建筑工地有时会使用大量的聚苯板(主要成分为聚苯乙烯)等保温材料。这些材料存在火灾隐患,而选用阻燃材料是解决这一问题的重要途径。酚醛树脂泡沫素有“保温材料之王”的美誉,它由热固性酚醛树脂发泡而成,在火中不燃烧、不熔化,是国际上公认的建筑行业中最有发展前途的一种新型阻燃保温材料。
身 边 的 化 学
问题:有机化合物的用途是由它们的性质决定的,有机化合物的性质又由它们的结构决定,那么,有机化合物的结构又有什么特点呢?有机物种类繁多的原因是什么?
结构
性质
用途
决定
决定
二、认识有机化合物的结构特点
1.有机化合物组成元素
从组成上看,有机化合物均含有 元素,大多数有机化合物含有 、 元素,有些有机化合物还含有 、 、 、 卤素等元素
碳
氢
氧
氮
硫
磷
2.烃
仅由 和 两种元素组成的有机化合物称为烃,也叫作 。 是组成最简单的烃
碳
氢
碳氢化合物
CH4
观察·思考(课本P78页)
球棍模型能够表示分子的空间结构和分子内原子之间的成键类型。球棍模型中,“球”表示原子,“棍”表示共价键。
空间填充模型可以表示分子的空间结构。
思考: 1. 甲烷分子中,碳原子与氢原子是怎样形成化学键的?甲烷分子是平面的还是立体的?
2. 请尝试从碳原子的结构特点解释碳、氢原子形成化学键的原因。
109°28′
3.甲烷的组成与结构
分子式:CH4
电子式:
结构式:
正四面体结构
结论:碳原子最外层的 4 个电子分别与 4 个氢原子的核外电子形成 4 对共用电子,5 个原子不在同一平面内,而是形成了一个正四面体形的结构:
碳原子位于正四面体的中心,4个氢原子分别位于正四面体的4个顶点,任意两个碳氢键之间的夹角均为109°28′
碳原子的最外层有 4 个电子,它不易失去或得到电子形成离子,通常通过共价键与其他原子结合
活动·探究(课本P79页)
实验目的
通过搭建有机化合物分子的球棍模型,认识有机化合物的结构特点。
实验步骤
试用不同颜色的小球分别代表碳原子、氢原子、氧原子和氯原子等,按下列要求动手搭建有机化合物分子的球棍模型,并写出相应有机化合物分子的结构式或结构简式。
1. 搭建甲烷分子的球棍模型。
2. 尽可能多地搭建含两个或三个碳原子的烃分子的球棍模型。
3. 在甲烷分子球棍模型的基础上搭建下列有机化合物分子的球棍模型:一氯甲烷(CH 3 Cl)、乙醇(CH 3 CH 2 OH)和乙酸(CH 3 COOH)。
思考:
在有机化合物分子中,碳原子可能以哪些成键方式满足“碳四价”原则?
单键
双键
三键
链状
环状
4.碳原子的成键特点
(1)碳原子的最外层有 4 个电子,它不易失去或得到电子形成离子,通常通过共价键与其他原子结合
(2)碳原子之间可以通过单键结合,也可以通过双键和三键结合
(3)分子中有 3 个或 3 个以上碳原子时,碳原子之间既可以形成链状还可以形成碳环
组成有机化合物的元素种类很少,但有机化合物的种类却多达上亿种。碳原子的成键特点是有机化合物种类繁多的根本原因
方法导引(教材P80页)
有机化合物的结构式书写及命名方法
结构式:
结构简式:
用元素符号和短线“—”表示分子中原子的排列顺序和成键方式的式子。
甲烷的结构式
乙烷的结构式
甲烷的结构简式
乙烷的结构简式
将结构式中表示单键的短线“—”省略后的式子称为结构简式。
烷烃
碳原子数为 1 ~ 10:
甲、乙、丙、丁、戊、己、庚、辛、壬、癸
碳原子数在 10 以上:
用中文数字命名
CH 4 甲烷 CH 3 CH 3 乙烷
CH 3 (CH 2 ) 9 CH 3 十一烷
方法导引(教材P80页)
有机化合物的结构式书写及命名方法
简单的有机化合物(分子不含支链)通常按分子含有的碳原子数来命名
5.烃的分类
烃
链烃
环烃
烷烃
(饱和链烃)
不饱和链烃
烃分子中,碳原子之间都以单键结合成碳链,碳原子的剩余价键均与氢原子结的烃。
分子中有碳环的烃
碳原子还有能与氢原子结合的价键,碳原子的最外层电子没有被充分利用,即没有达到“饱和”状态的烃。
6.几种常见烃的空间构型
直线形分子
平面形分子
立体形分子
180°
约120°
约109°28′
观察甲烷、乙烷、丙烷、丁烷、戊烷的元素组成和分子结构特点。思考烷烃分子在组成上有何规律?
观察·思考
相邻烷烃分子在组成上均相差一个 CH 2 原子团
烷烃的分子式可以用通式C n H 2n+ 2 表示
7.同系物
结构相似、分子组成相差一个或若干个 CH 2 原子团的有机化合物互称为同系物
同系物一定是同一类物质
分子式只相差CH2
思考:乙烯和环丙烷相差一个CH2原子团,二者互为同系物吗
乙烯和环丙烷是不同类别的物质,二者不是同系物
第3章 简单的有机化合物
第1节 认识有机化合物
第1课时 认识有机化合物的一般性质
碳原子的成键特点
【核心素养目标】
1. 能从元素组成、结构、性质等角度概括有机化合物的共同点,知道有机化合物分子是有空间结构的,知道有机化合物与无机物的差异。
2. 以烷烃为例发现有机化合物中同系物的存在,能够对简单的有机化合物进行分类。
3. 以甲烷、乙烯、乙炔、苯为例认识碳原子的成键特点,能概括常见有机化合物中碳原子的成键类型。能描述甲烷、乙烯、乙炔的分子结构特征并能搭建甲烷和乙烷的立体模型。
【重难点】
碳原子成键特点
联想·质疑 在日常生活中,有机化合物几乎随处可见。你能说出哪些物质是有机化合物吗?
有机化合物
食品:糖类、油脂、
蛋白质……
能源:煤、石油、
天然气……
药物:阿司匹林、 扑 尔 敏、
多酶片……
材料:塑料、纤维、橡胶……
结构式
结构简式
一、认识有机化合物的一般性质
1.概念
有机化合物是指大多数含有 元素的化合物
碳
思考:含碳元素的化合物一定是有机化合物吗?
不一定,少数含碳化合物如:CO、CO2、H2CO3、碳酸盐、
碳酸氢盐等,由于它们的组成与性质更接近于无机物,
因此仍把它们归为无机物
化合物
大多数含有碳元素的化合物
无机化合物
有机化合物
不含碳元素的化合物,以及少数含有碳元素的化合物(如CO、CO2、H2CO3和碳酸形成的盐等)
思考:下列含有碳元素的物质该如何分类?
石墨、金刚石、一氧化碳、二氧化碳、碳酸、乙酸、碳酸钠、碳酸钙、甲烷、酒精、碳酸氢钠、葡萄糖、蛋白质
石墨、金刚石、一氧化碳、二氧化碳、碳酸、碳酸钠、碳酸钙、
碳酸氢钠
乙酸、甲烷、酒精、葡萄糖、蛋白质
无机化合物:
有机化合物:
观察·思考(课本P77页)
生活中的许多物质都是有机化合物或由有机化合物组成的混合物,如酒精、汽油、植物油、聚乙烯塑料等。有机化合物通常会有哪些性质?请通过观察下列实验的现象,了解有机化合物的性质。
【实验 1】用棉签蘸取酒精,涂抹在手上,观察现象并感受能量变化。
【实验 2】向两支试管中加入适量水,然后分别加入体积相近的汽油和酒精,振荡试管,观察现象。
【实验 3】用坩埚钳夹取一片聚乙烯塑料,置于酒精灯火焰上加热至燃烧,观察现象。
【实验 4】向试管中加入适量碘水,再滴入适量植物油,振荡后静置,观察现象。
实验内容 实验现象 实验结论
酒精最终消失,涂酒精的部分感到越来越凉
酒精易挥发,挥发过程吸热
汽油与水互不相溶,液体分层,汽油在上层;酒精与水互溶
有的有机物难溶于水,有的有机物易溶于水
实验内容 实验现象 实验结论
火焰明亮,冒黑烟
液体分层,水层变为无色,植物油层在上层,为紫红色
碘更易溶于植物油(有机溶剂)
聚乙烯塑料易燃烧
思考:根据以上实验你能得出哪些结论?这些实验对你认识有机化合物的性质有何启示?
2.有机化合物一般性质(课本P77页)
共性:熔点较低,常温下多为固态或液态
一般难溶于水,易溶于有机溶剂
绝大多数受热易分解,容易燃烧
差异性:
挥发性:乙醇、苯易挥发,甘油难挥发
溶解性:大多数难溶于水,有的易溶于水如酒精、乙酸
热稳定性:大多受热易分解,如聚乙烯
有的具有较强热稳定性 ,如酚醛树脂
特性:乙醇可以被高锰酸钾氧化而使紫色酸性 KMnO4 溶液褪色
阻燃保温材料
建筑工地有时会使用大量的聚苯板(主要成分为聚苯乙烯)等保温材料。这些材料存在火灾隐患,而选用阻燃材料是解决这一问题的重要途径。酚醛树脂泡沫素有“保温材料之王”的美誉,它由热固性酚醛树脂发泡而成,在火中不燃烧、不熔化,是国际上公认的建筑行业中最有发展前途的一种新型阻燃保温材料。
身 边 的 化 学
问题:有机化合物的用途是由它们的性质决定的,有机化合物的性质又由它们的结构决定,那么,有机化合物的结构又有什么特点呢?有机物种类繁多的原因是什么?
结构
性质
用途
决定
决定
二、认识有机化合物的结构特点
1.有机化合物组成元素
从组成上看,有机化合物均含有 元素,大多数有机化合物含有 、 元素,有些有机化合物还含有 、 、 、 卤素等元素
碳
氢
氧
氮
硫
磷
2.烃
仅由 和 两种元素组成的有机化合物称为烃,也叫作 。 是组成最简单的烃
碳
氢
碳氢化合物
CH4
观察·思考(课本P78页)
球棍模型能够表示分子的空间结构和分子内原子之间的成键类型。球棍模型中,“球”表示原子,“棍”表示共价键。
空间填充模型可以表示分子的空间结构。
思考: 1. 甲烷分子中,碳原子与氢原子是怎样形成化学键的?甲烷分子是平面的还是立体的?
2. 请尝试从碳原子的结构特点解释碳、氢原子形成化学键的原因。
109°28′
3.甲烷的组成与结构
分子式:CH4
电子式:
结构式:
正四面体结构
结论:碳原子最外层的 4 个电子分别与 4 个氢原子的核外电子形成 4 对共用电子,5 个原子不在同一平面内,而是形成了一个正四面体形的结构:
碳原子位于正四面体的中心,4个氢原子分别位于正四面体的4个顶点,任意两个碳氢键之间的夹角均为109°28′
碳原子的最外层有 4 个电子,它不易失去或得到电子形成离子,通常通过共价键与其他原子结合
活动·探究(课本P79页)
实验目的
通过搭建有机化合物分子的球棍模型,认识有机化合物的结构特点。
实验步骤
试用不同颜色的小球分别代表碳原子、氢原子、氧原子和氯原子等,按下列要求动手搭建有机化合物分子的球棍模型,并写出相应有机化合物分子的结构式或结构简式。
1. 搭建甲烷分子的球棍模型。
2. 尽可能多地搭建含两个或三个碳原子的烃分子的球棍模型。
3. 在甲烷分子球棍模型的基础上搭建下列有机化合物分子的球棍模型:一氯甲烷(CH 3 Cl)、乙醇(CH 3 CH 2 OH)和乙酸(CH 3 COOH)。
思考:
在有机化合物分子中,碳原子可能以哪些成键方式满足“碳四价”原则?
单键
双键
三键
链状
环状
4.碳原子的成键特点
(1)碳原子的最外层有 4 个电子,它不易失去或得到电子形成离子,通常通过共价键与其他原子结合
(2)碳原子之间可以通过单键结合,也可以通过双键和三键结合
(3)分子中有 3 个或 3 个以上碳原子时,碳原子之间既可以形成链状还可以形成碳环
组成有机化合物的元素种类很少,但有机化合物的种类却多达上亿种。碳原子的成键特点是有机化合物种类繁多的根本原因
方法导引(教材P80页)
有机化合物的结构式书写及命名方法
结构式:
结构简式:
用元素符号和短线“—”表示分子中原子的排列顺序和成键方式的式子。
甲烷的结构式
乙烷的结构式
甲烷的结构简式
乙烷的结构简式
将结构式中表示单键的短线“—”省略后的式子称为结构简式。
烷烃
碳原子数为 1 ~ 10:
甲、乙、丙、丁、戊、己、庚、辛、壬、癸
碳原子数在 10 以上:
用中文数字命名
CH 4 甲烷 CH 3 CH 3 乙烷
CH 3 (CH 2 ) 9 CH 3 十一烷
方法导引(教材P80页)
有机化合物的结构式书写及命名方法
简单的有机化合物(分子不含支链)通常按分子含有的碳原子数来命名
5.烃的分类
烃
链烃
环烃
烷烃
(饱和链烃)
不饱和链烃
烃分子中,碳原子之间都以单键结合成碳链,碳原子的剩余价键均与氢原子结的烃。
分子中有碳环的烃
碳原子还有能与氢原子结合的价键,碳原子的最外层电子没有被充分利用,即没有达到“饱和”状态的烃。
6.几种常见烃的空间构型
直线形分子
平面形分子
立体形分子
180°
约120°
约109°28′
观察甲烷、乙烷、丙烷、丁烷、戊烷的元素组成和分子结构特点。思考烷烃分子在组成上有何规律?
观察·思考
相邻烷烃分子在组成上均相差一个 CH 2 原子团
烷烃的分子式可以用通式C n H 2n+ 2 表示
7.同系物
结构相似、分子组成相差一个或若干个 CH 2 原子团的有机化合物互称为同系物
同系物一定是同一类物质
分子式只相差CH2
思考:乙烯和环丙烷相差一个CH2原子团,二者互为同系物吗
乙烯和环丙烷是不同类别的物质,二者不是同系物
