7.3.1乙醇与乙酸(1)【教学课件】(共33张PPT)-【优课堂】2022-2023学年高一化学同步备课系列(人教版2019必修第二册)
文档属性
| 名称 | 7.3.1乙醇与乙酸(1)【教学课件】(共33张PPT)-【优课堂】2022-2023学年高一化学同步备课系列(人教版2019必修第二册) |  | |
| 格式 | zip | ||
| 文件大小 | 57.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-27 11:14:31 | ||
图片预览







文档简介
(共33张PPT)
第三节 乙醇与乙酸
第1课时
第七章 有机化合物
2
1
本节重点
本节难点
乙醇的分子结构和化学性质
烃的衍生物,官能团的概念
Spirytus Rektyfikowany是一款原产于波兰的伏特加,被西方人称为“生命之水”。
生命之水
经过了反复70回以上的蒸馏,达到96%的酒精度数,是世界上纯度最高的烈酒。
白酒中酒精,化学上,我们称之为乙醇。
那么,乙醇有哪些性质呢?
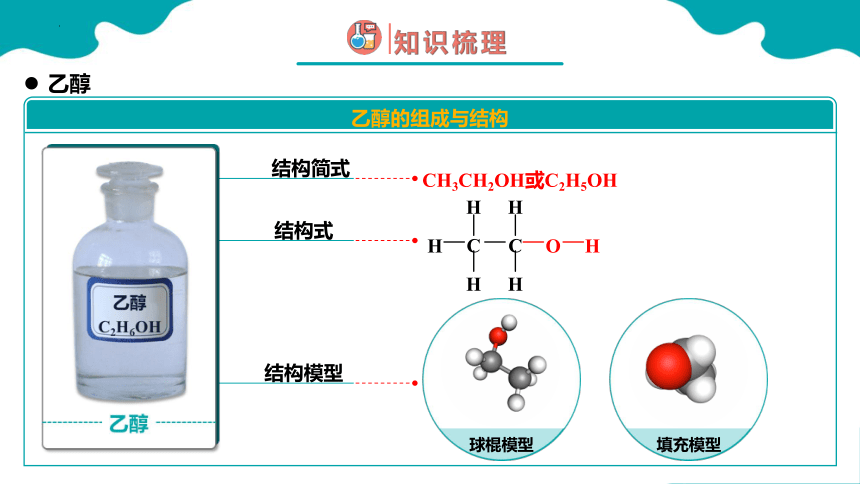
结构简式
乙醇
乙醇的组成与结构
CH3CH2OH或C2H5OH
H
H
O
H
C
H
H
C
H
球棍模型
填充模型
结构式
结构模型
乙醇
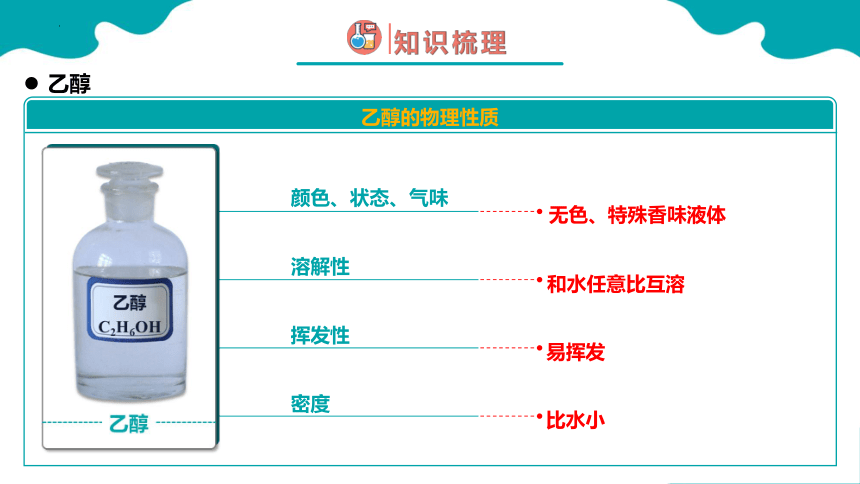
无色、特殊香味液体
和水任意比互溶
易挥发
比水小
乙醇的物理性质
颜色、状态、气味
溶解性
密度
挥发性
H
H
H
C
H
H
C
H
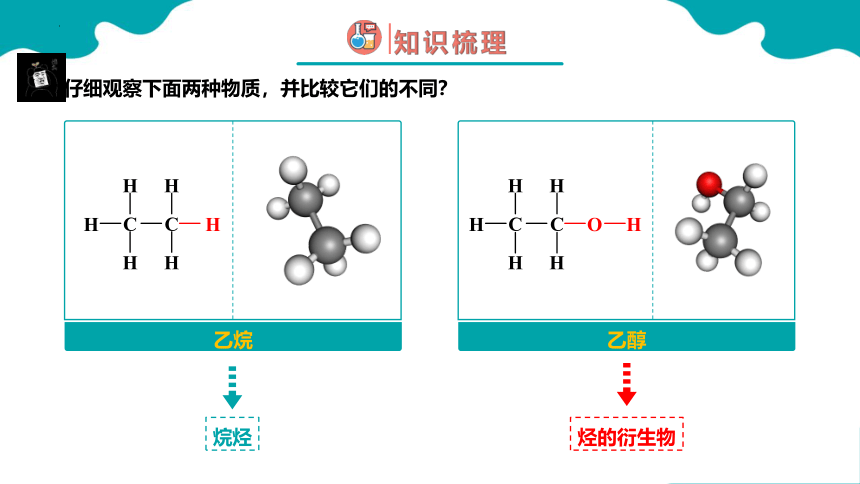
乙烷
乙醇
H
H
O
H
C
H
H
C
H
仔细观察下面两种物质,并比较它们的不同?
烷烃
烃的衍生物
烃分子中的 被 所取代而生成的一系列化合物。
概念
氢原子
其他原子或原子团
烃的衍生物
示例
CH3I
CH2BrCH2Br
CH3CH2Cl
烃的衍生物是指烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物,其他原子或原子团不能是烃结构中的原子或原子团。
判断正误:乙烷(CH3CH3)可以看成CH4分子中的一个H原子被甲基(—CH3)所取代而生成的产物,故乙烷为烃的衍生物。
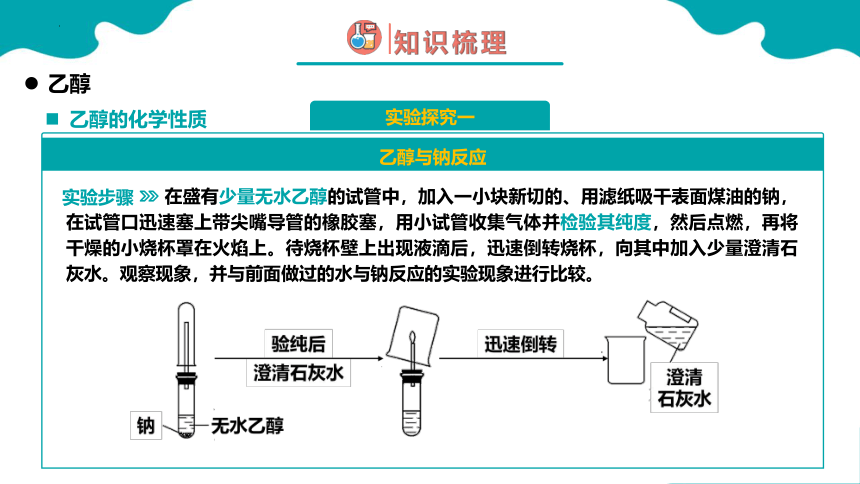
实验探究一
乙醇与钠反应
乙醇
乙醇的化学性质
实验步骤
在盛有少量无水乙醇的试管中,加入一小块新切的、用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞,用小试管收集气体并检验其纯度,然后点燃,再将干燥的小烧杯罩在火焰上。待烧杯壁上出现液滴后,迅速倒转烧杯,向其中加入少量澄清石灰水。观察现象,并与前面做过的水与钠反应的实验现象进行比较。
化学方程式
实验探究一
乙醇与钠反应
乙醇
乙醇的化学性质
2Na+2CH3CH2OH―→ 2CH3CH2ONa+H2↑
乙醇钠
例如:—CH3叫甲基, —CH2CH3叫乙基
烃分子失去1个氢原子后所剩余的部分叫做烃基,可以用 —R来表示
烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的
例如:乙醇分子可以看成是由乙基和羟基组成的CH3CH2—OH
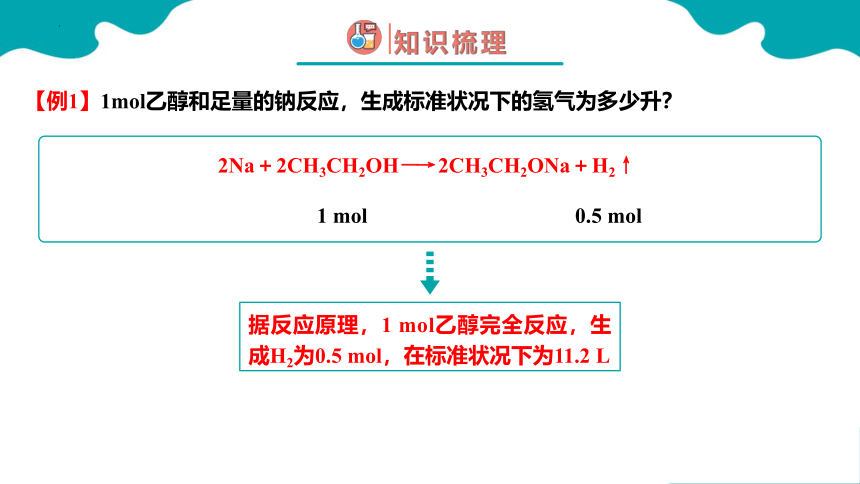
【例1】1mol乙醇和足量的钠反应,生成标准状况下的氢气为多少升?
1 mol
0.5 mol
2Na+2CH3CH2OH―→ 2CH3CH2ONa+H2↑
据反应原理,1 mol乙醇完全反应,生成H2为0.5 mol,在标准状况下为11.2 L
化学方程式
实验探究一
乙醇与钠反应
乙醇
乙醇的化学性质
2Na+2CH3CH2OH―→ 2CH3CH2ONa+H2↑
实验分析
乙醇由于分子中羟基的存在,可以与钠发生反应。在该反应中,钠置换了羟基中的氢,生成了氢气和乙醇钠
乙醇钠
H
H
O
H
C
H
H
C
H
观察:钠与水和乙醇的反应,你能得出什么结论?
钠和水的反应
钠和乙醇的反应
实验结论:
乙醇羟基中的氢原子不如水分子中的氢原子活泼
实验现象:
乙醇与钠的反应比相同条件下水与钠的反应缓和得多
H
H
H
C
H
H
C
H
乙烷
乙醇
H
H
O
H
C
H
H
C
H
像这种决定有机化合物特性的原子或原子团叫做官能团
乙醇具有与乙烷不同的性质,从分子结构角度分析,是因为取代氢原子的羟基对乙醇的性质产生了影响
几种常见物质的官能团
物质 CH2==CH2 CH≡CH CH3CH2OH CH3CHO CH3COOH
官能团 结构简式 —C≡C— —Br —OH —CHO —COOH
官能团 名称 碳碳双键 碳碳三键 溴原子 羟基 醛基 羧基
官能团
实验探究二
乙醇的燃烧
乙醇
乙醇的化学性质
点燃装满乙醇蒸汽的水桶
CH3CH2OH+3O2 2CO2+3H2O
点燃
化学方程式
实验现象
化学方程式
乙醇在空气中燃烧时生成二氧化碳和水
燃烧时发出淡蓝色的火焰,同时放出大量的热
实验探究三
乙醇的催化氧化
乙醇
乙醇的化学性质
实验步骤
向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇,反复几次。注意观察反应现象,小心地闻试管中液体产生的气味
变黑
变红
刺激性气味
铜丝灼烧时 ,插入乙醇后 ,反复几次可闻到___________
实验现象
实验探究三
乙醇的催化氧化
乙醇
乙醇的化学性质
反应原理
乙醇
乙醇的化学性质
实验探究三
乙醇的催化氧化
H
H
O
H
C
H
H
C
H
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
2Cu +O2
2CuO
CuO
+
H
O
H
C
H
H
C
Cu
+
H2O
+
化学方程式
醛基
(-CHO)
Cu或Ag在该反应中作催化剂,反应前后质量不变
乙醇
乙醇的化学性质
实验分析
实验探究三
乙醇的催化氧化
乙醇催化氧化反应的实质是脱去与羟基相连的碳原子上的氢原子和羟基上的氢原子,这两个氢原子与氧原子结合形成H2O,若醇分子中与羟基相连的碳原子上无氢原子,则不能被催化氧化。
H
H
O
H
C
H
H
C
H
α
β
CH3
H
O
C
CH3
CH3
H
C
H
α
β
乙醇
乙醇的化学性质
乙醇还可以与酸性高锰酸钾溶液(KMnO4)或酸性重铬酸钾(K2Cr2O7)溶液反应,被氧化成乙酸
酸性高锰酸钾溶液(KMnO4)
酸性重铬酸钾溶液(K2Cr2O7)
乙醇
乙醇的化学性质
归纳总结:乙醇的氧化反应
乙酸(CH3COOH)
燃烧
催化氧化
酸性高锰酸钾溶液(KMnO4)
酸性重铬酸钾溶液(K2Cr2O7)
CH3CH2OH+3O2 2CO2+3H2O
点燃
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
CH3CH2OH
乙醇
乙醇
乙醇的用途
世界上最原始酒的起源
古猿以采集野果为生,他们把当天吃不完的野果藏在树洞、石洼中,以便饥饿时取用。
因为某种原因,果实放的时间久了,便渐渐腐烂。野果本身就含有一定的糖分,经过附着在果皮上的菌类自然发酵,就成了含有低量酒精的液体,这就是猿猴藏酒(猴儿酒)。
1.下列物质不属于烃的衍生物的是( )
A.
B.CH3CH2OH
C.
D.CH2=CH2
D
2.下列物质不含有官能团的是( )
A.CH2==CH2 B.CH3CH2OH C.CH3CHO D.CH3CH3
D
3.向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述中正确的是( )
A.钠块沉在乙醇液面之下
B.钠块熔化成小球
C.钠块在乙醇的液面上游动
D.向烧杯中滴入几滴酚酞溶液变红色
A
4.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说明不正确的是( )
A.和金属钠反应时①键断裂
B.在铜催化共热下与O2反应时断裂①键和③键
C.在铜催化共热下与O2反应时断裂①键和⑤键
D.在空气中完全燃烧时断裂①②③④⑤键
C
5.下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子不同的是( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以和水任意比互溶
C.1 mol乙醇跟足量的Na作用得0.5 mol H2
D.乙醇可被酸性KMnO4氧化为乙酸(CH3COOH)
C
第三节
乙醇与乙酸
第1课时
乙醇
烃的衍生物
组成与结构
化学性质
概念
示例
物理性质
用途
官能团
概念
常见物质的官能团
THANKS
谢谢聆听
第三节 乙醇与乙酸
第1课时
第七章 有机化合物
2
1
本节重点
本节难点
乙醇的分子结构和化学性质
烃的衍生物,官能团的概念
Spirytus Rektyfikowany是一款原产于波兰的伏特加,被西方人称为“生命之水”。
生命之水
经过了反复70回以上的蒸馏,达到96%的酒精度数,是世界上纯度最高的烈酒。
白酒中酒精,化学上,我们称之为乙醇。
那么,乙醇有哪些性质呢?
结构简式
乙醇
乙醇的组成与结构
CH3CH2OH或C2H5OH
H
H
O
H
C
H
H
C
H
球棍模型
填充模型
结构式
结构模型
乙醇
无色、特殊香味液体
和水任意比互溶
易挥发
比水小
乙醇的物理性质
颜色、状态、气味
溶解性
密度
挥发性
H
H
H
C
H
H
C
H
乙烷
乙醇
H
H
O
H
C
H
H
C
H
仔细观察下面两种物质,并比较它们的不同?
烷烃
烃的衍生物
烃分子中的 被 所取代而生成的一系列化合物。
概念
氢原子
其他原子或原子团
烃的衍生物
示例
CH3I
CH2BrCH2Br
CH3CH2Cl
烃的衍生物是指烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物,其他原子或原子团不能是烃结构中的原子或原子团。
判断正误:乙烷(CH3CH3)可以看成CH4分子中的一个H原子被甲基(—CH3)所取代而生成的产物,故乙烷为烃的衍生物。
实验探究一
乙醇与钠反应
乙醇
乙醇的化学性质
实验步骤
在盛有少量无水乙醇的试管中,加入一小块新切的、用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞,用小试管收集气体并检验其纯度,然后点燃,再将干燥的小烧杯罩在火焰上。待烧杯壁上出现液滴后,迅速倒转烧杯,向其中加入少量澄清石灰水。观察现象,并与前面做过的水与钠反应的实验现象进行比较。
化学方程式
实验探究一
乙醇与钠反应
乙醇
乙醇的化学性质
2Na+2CH3CH2OH―→ 2CH3CH2ONa+H2↑
乙醇钠
例如:—CH3叫甲基, —CH2CH3叫乙基
烃分子失去1个氢原子后所剩余的部分叫做烃基,可以用 —R来表示
烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的
例如:乙醇分子可以看成是由乙基和羟基组成的CH3CH2—OH
【例1】1mol乙醇和足量的钠反应,生成标准状况下的氢气为多少升?
1 mol
0.5 mol
2Na+2CH3CH2OH―→ 2CH3CH2ONa+H2↑
据反应原理,1 mol乙醇完全反应,生成H2为0.5 mol,在标准状况下为11.2 L
化学方程式
实验探究一
乙醇与钠反应
乙醇
乙醇的化学性质
2Na+2CH3CH2OH―→ 2CH3CH2ONa+H2↑
实验分析
乙醇由于分子中羟基的存在,可以与钠发生反应。在该反应中,钠置换了羟基中的氢,生成了氢气和乙醇钠
乙醇钠
H
H
O
H
C
H
H
C
H
观察:钠与水和乙醇的反应,你能得出什么结论?
钠和水的反应
钠和乙醇的反应
实验结论:
乙醇羟基中的氢原子不如水分子中的氢原子活泼
实验现象:
乙醇与钠的反应比相同条件下水与钠的反应缓和得多
H
H
H
C
H
H
C
H
乙烷
乙醇
H
H
O
H
C
H
H
C
H
像这种决定有机化合物特性的原子或原子团叫做官能团
乙醇具有与乙烷不同的性质,从分子结构角度分析,是因为取代氢原子的羟基对乙醇的性质产生了影响
几种常见物质的官能团
物质 CH2==CH2 CH≡CH CH3CH2OH CH3CHO CH3COOH
官能团 结构简式 —C≡C— —Br —OH —CHO —COOH
官能团 名称 碳碳双键 碳碳三键 溴原子 羟基 醛基 羧基
官能团
实验探究二
乙醇的燃烧
乙醇
乙醇的化学性质
点燃装满乙醇蒸汽的水桶
CH3CH2OH+3O2 2CO2+3H2O
点燃
化学方程式
实验现象
化学方程式
乙醇在空气中燃烧时生成二氧化碳和水
燃烧时发出淡蓝色的火焰,同时放出大量的热
实验探究三
乙醇的催化氧化
乙醇
乙醇的化学性质
实验步骤
向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇,反复几次。注意观察反应现象,小心地闻试管中液体产生的气味
变黑
变红
刺激性气味
铜丝灼烧时 ,插入乙醇后 ,反复几次可闻到___________
实验现象
实验探究三
乙醇的催化氧化
乙醇
乙醇的化学性质
反应原理
乙醇
乙醇的化学性质
实验探究三
乙醇的催化氧化
H
H
O
H
C
H
H
C
H
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
2Cu +O2
2CuO
CuO
+
H
O
H
C
H
H
C
Cu
+
H2O
+
化学方程式
醛基
(-CHO)
Cu或Ag在该反应中作催化剂,反应前后质量不变
乙醇
乙醇的化学性质
实验分析
实验探究三
乙醇的催化氧化
乙醇催化氧化反应的实质是脱去与羟基相连的碳原子上的氢原子和羟基上的氢原子,这两个氢原子与氧原子结合形成H2O,若醇分子中与羟基相连的碳原子上无氢原子,则不能被催化氧化。
H
H
O
H
C
H
H
C
H
α
β
CH3
H
O
C
CH3
CH3
H
C
H
α
β
乙醇
乙醇的化学性质
乙醇还可以与酸性高锰酸钾溶液(KMnO4)或酸性重铬酸钾(K2Cr2O7)溶液反应,被氧化成乙酸
酸性高锰酸钾溶液(KMnO4)
酸性重铬酸钾溶液(K2Cr2O7)
乙醇
乙醇的化学性质
归纳总结:乙醇的氧化反应
乙酸(CH3COOH)
燃烧
催化氧化
酸性高锰酸钾溶液(KMnO4)
酸性重铬酸钾溶液(K2Cr2O7)
CH3CH2OH+3O2 2CO2+3H2O
点燃
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
CH3CH2OH
乙醇
乙醇
乙醇的用途
世界上最原始酒的起源
古猿以采集野果为生,他们把当天吃不完的野果藏在树洞、石洼中,以便饥饿时取用。
因为某种原因,果实放的时间久了,便渐渐腐烂。野果本身就含有一定的糖分,经过附着在果皮上的菌类自然发酵,就成了含有低量酒精的液体,这就是猿猴藏酒(猴儿酒)。
1.下列物质不属于烃的衍生物的是( )
A.
B.CH3CH2OH
C.
D.CH2=CH2
D
2.下列物质不含有官能团的是( )
A.CH2==CH2 B.CH3CH2OH C.CH3CHO D.CH3CH3
D
3.向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述中正确的是( )
A.钠块沉在乙醇液面之下
B.钠块熔化成小球
C.钠块在乙醇的液面上游动
D.向烧杯中滴入几滴酚酞溶液变红色
A
4.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说明不正确的是( )
A.和金属钠反应时①键断裂
B.在铜催化共热下与O2反应时断裂①键和③键
C.在铜催化共热下与O2反应时断裂①键和⑤键
D.在空气中完全燃烧时断裂①②③④⑤键
C
5.下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子不同的是( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以和水任意比互溶
C.1 mol乙醇跟足量的Na作用得0.5 mol H2
D.乙醇可被酸性KMnO4氧化为乙酸(CH3COOH)
C
第三节
乙醇与乙酸
第1课时
乙醇
烃的衍生物
组成与结构
化学性质
概念
示例
物理性质
用途
官能团
概念
常见物质的官能团
THANKS
谢谢聆听
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
