第八单元金属和金属材料检测题(含答案)-2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 第八单元金属和金属材料检测题(含答案)-2022-2023学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 95.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-26 00:00:00 | ||
图片预览

文档简介
第八单元《金属和金属材料》检测题
一、单选题
1.在FeSO4和CuSO4的混合溶液中加入一定量锌粉,充分反应后得到一定量固体。过滤后向固体中加入少量稀硫酸,有气泡产生。对固体成分的说法正确的是
①一定含有Zn ②一定含有Fe ③一定含有Cu ④可能含有Zn ⑤可能含有Fe
A.①②③ B.②③④ C.③④⑤ D.①②④
2.推理是化学学习中常用的思维方法。下列推理正确的是
A.点燃可燃性气体前要验纯,所以点燃H2前一定要验纯
B.离子是带电的粒子,所以带电的粒子一定是离子
C.H2O和H2O2的元素组成相同,所以它们的化学性质相同
D.置换反应有单质生成,所以有单质生成的反应一定是置换反应
3.在铁路线上,把两根铁轨接到一起时,工程技术人员常用如下反应来焊接钢轨间的缝隙:2Al+Fe2O3Al2O3+2Fe.有关此反应的下列说法中正确的是
A.该反应属于化合反应 B.该反应属于分解反应
C.该反应属于置换反应 D.该反应中铁元素化合价升高
4.下列图像分别与选项的操作相对应,其中合理的是
A.向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉
B.向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液
C.温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
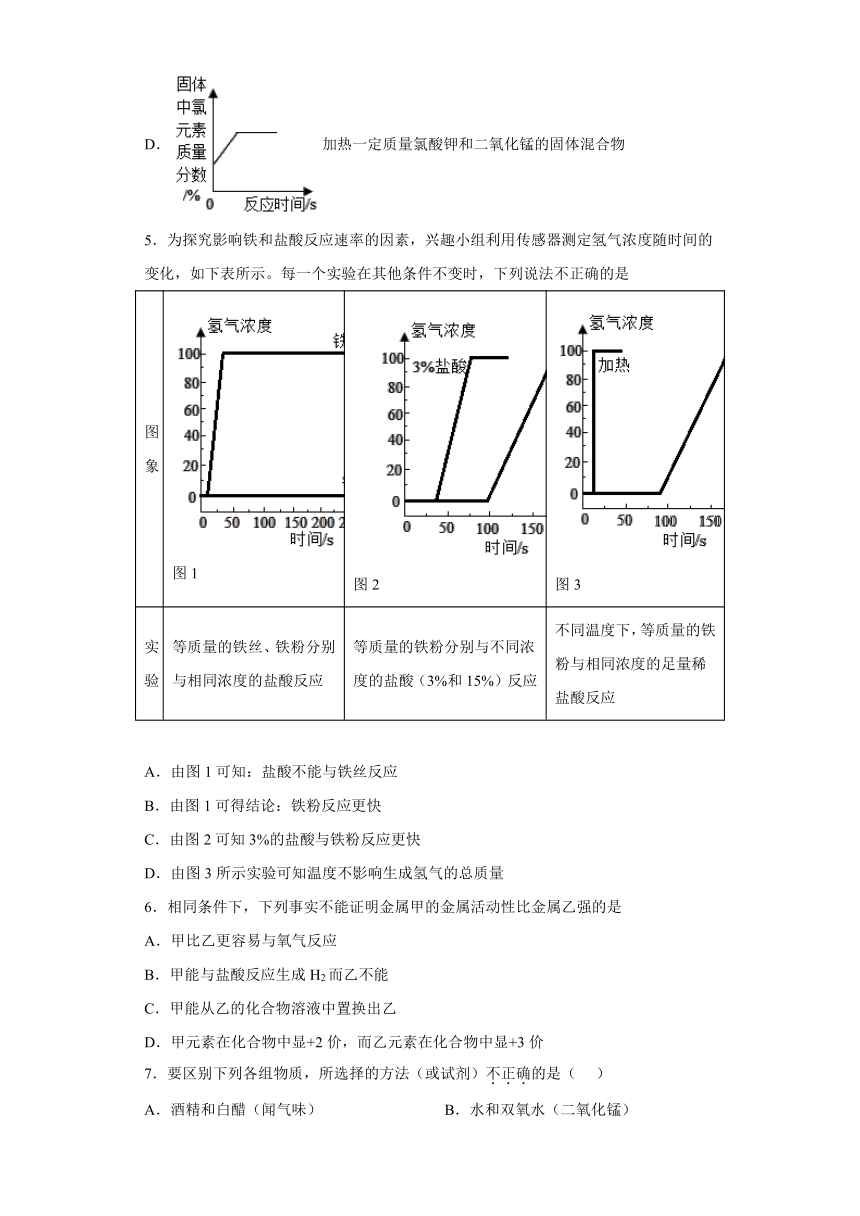
D.加热一定质量氯酸钾和二氧化锰的固体混合物
5.为探究影响铁和盐酸反应速率的因素,兴趣小组利用传感器测定氢气浓度随时间的变化,如下表所示。每一个实验在其他条件不变时,下列说法不正确的是
图象 图1 图2 图3
实验 等质量的铁丝、铁粉分别与相同浓度的盐酸反应 等质量的铁粉分别与不同浓度的盐酸(3%和15%)反应 不同温度下,等质量的铁粉与相同浓度的足量稀盐酸反应
A.由图1可知:盐酸不能与铁丝反应
B.由图1可得结论:铁粉反应更快
C.由图2可知3%的盐酸与铁粉反应更快
D.由图3所示实验可知温度不影响生成氢气的总质量
6.相同条件下,下列事实不能证明金属甲的金属活动性比金属乙强的是
A.甲比乙更容易与氧气反应
B.甲能与盐酸反应生成H2而乙不能
C.甲能从乙的化合物溶液中置换出乙
D.甲元素在化合物中显+2价,而乙元素在化合物中显+3价
7.要区别下列各组物质,所选择的方法(或试剂)不正确的是( )
A.酒精和白醋(闻气味) B.水和双氧水(二氧化锰)
C.氧化铜和二氧化锰 (观察颜色) D.铁丝和铜丝 (观察颜色)
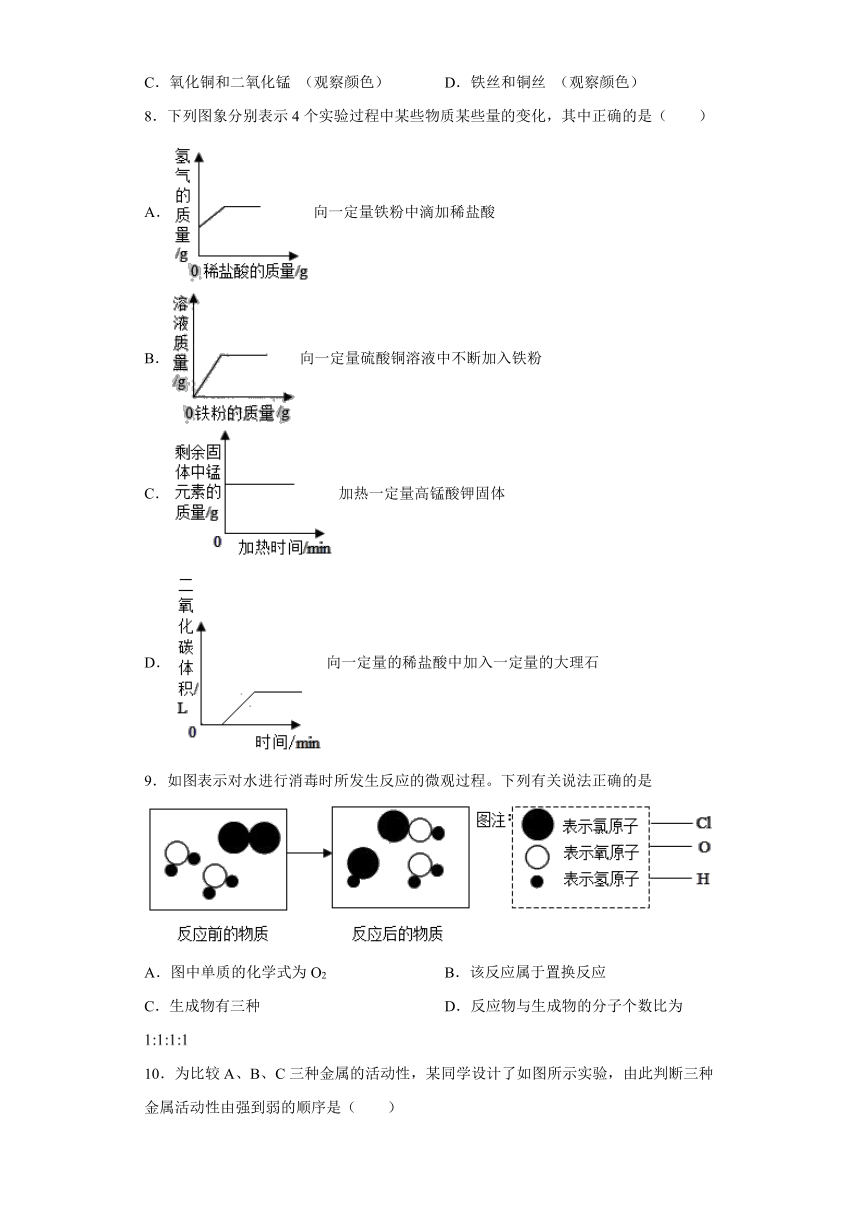
8.下列图象分别表示4个实验过程中某些物质某些量的变化,其中正确的是( )
A.向一定量铁粉中滴加稀盐酸
B.向一定量硫酸铜溶液中不断加入铁粉
C.加热一定量高锰酸钾固体
D.向一定量的稀盐酸中加入一定量的大理石
9.如图表示对水进行消毒时所发生反应的微观过程。下列有关说法正确的是
A.图中单质的化学式为O2 B.该反应属于置换反应
C.生成物有三种 D.反应物与生成物的分子个数比为
10.为比较A、B、C三种金属的活动性,某同学设计了如图所示实验,由此判断三种金属活动性由强到弱的顺序是( )
A.A>C>B B.A>B>C C.C>A>B D.B>C>A
11.下列属于金属材料的是( )
A.玻璃 B.钢铁 C.木材 D.氧化铁
12.除去一氧化碳中混有的少量水蒸气、氧气、二氧化碳气体,混合气体应依次通过
A.干燥剂、灼热铜网、足量石灰水 B.灼热的铜网、足量石灰水、干燥剂
C.干燥剂、足量石灰水、灼热的铜网 D.灼热的铜网、干燥剂、足量石灰水
二、填空题
13.利用生铁制造铸铁锅,是因为铁有良好的的___性,但极易生锈,使用后应如何保养___。
14.回答与金属有关的问题。
(1)在Zn、Ag、Fe三种金属中,通常不能与稀盐酸发生置换反应的是____;
(2)在铁制品表面涂油漆能防止铁制品生锈,原因是____;
(3)向含有Cu(NO3)2和AgNO3溶液烧杯中加入一定量的Mg粉,充分反应后过滤,得到滤液和滤渣,向滤液中滴加稀盐酸产生白色沉淀,则滤渣的成分是____。
15.人类的生产生活都离不开金属,请回答下列问题:
(1)生活中常用铜做导线,主要是利用了铜的_____;
(2)铁锅生锈的原因是_____;
(3)使用完铁锅后,防止生锈的办法是_____;
(4)废弃铁锅回收利用的意义是_____。
三、实验题
16.化学小组同学用如图所示装置模拟工业炼铁,请回答下列问题:
(1)写出如图装置中玻璃管A内发生反应的现象_______,化学方程式______。
(2)从环保角度考虑,对以上装置的改进措施是______。
(3)实验加热前先通一氧化碳的目的_______。
四、计算题
17.黄铜是铜和锌的合金(Cu﹣Zn),它可用来制造电器零件及日用品,为了测定某黄铜样品中锌的质量分数(不考虑黄铜中的其他杂质),现将15mL稀硫酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见表,试回答下列问题:
第一次 第二次 第三次
加入稀硫酸的体积(mL) 5 5 5
生成氢气的质量(g) 0.04 m 0.02
(1)写出反应的化学方程式______.
(2)m=______.
(3)列出第一次反应中参加反应的锌的质量(x)的比例式是______.
(4)此黄铜样品中锌的质量分数是______.
(5)若工业上用含Cu2S80%的辉铜矿135t(炼制过程中辉铜矿的损失率为20%),能炼出上述黄铜的质量为______.
18.向 133.4 克稀盐酸中加入锌粉(杂质不溶于水也不溶于酸),所加锌粉的质量与产生气体的 质量的关系如下图所示。求:
(1)该反应中化合价改变的元素是______(填名称)。
(2)原稀盐酸中溶质的质量分数为多少?(结果精确到 0.1%)
参考答案:
1.B
2.A
3.C
4.D
5.A
6.D
7.C
8.C
9.D
10.B
11.B
12.B
13. 导热 保持表面干燥
14. Ag 能隔绝铁与氧气、水的接触 银
15. 导电性 铁与水和氧气充分接触生成氧化铁 洗净擦干 既节约金属资源,又可以防止造成环境的污染
16.(1) 红色粉末变成黑色
(2)增加尾气处理装置(答案合理即可)
(3)排出装置中的空气,防止一氧化碳和空气混合,发生爆炸
17.(1)(2)0.04(3)(4)32.5%(5)102.4t
18.(1)锌元素与氢元素
(2)解:设稀盐酸中溶质的质量分数为x
答:稀盐酸中溶质的质量分数为10.9%。
一、单选题
1.在FeSO4和CuSO4的混合溶液中加入一定量锌粉,充分反应后得到一定量固体。过滤后向固体中加入少量稀硫酸,有气泡产生。对固体成分的说法正确的是
①一定含有Zn ②一定含有Fe ③一定含有Cu ④可能含有Zn ⑤可能含有Fe
A.①②③ B.②③④ C.③④⑤ D.①②④
2.推理是化学学习中常用的思维方法。下列推理正确的是
A.点燃可燃性气体前要验纯,所以点燃H2前一定要验纯
B.离子是带电的粒子,所以带电的粒子一定是离子
C.H2O和H2O2的元素组成相同,所以它们的化学性质相同
D.置换反应有单质生成,所以有单质生成的反应一定是置换反应
3.在铁路线上,把两根铁轨接到一起时,工程技术人员常用如下反应来焊接钢轨间的缝隙:2Al+Fe2O3Al2O3+2Fe.有关此反应的下列说法中正确的是
A.该反应属于化合反应 B.该反应属于分解反应
C.该反应属于置换反应 D.该反应中铁元素化合价升高
4.下列图像分别与选项的操作相对应,其中合理的是
A.向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉
B.向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液
C.温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
D.加热一定质量氯酸钾和二氧化锰的固体混合物
5.为探究影响铁和盐酸反应速率的因素,兴趣小组利用传感器测定氢气浓度随时间的变化,如下表所示。每一个实验在其他条件不变时,下列说法不正确的是
图象 图1 图2 图3
实验 等质量的铁丝、铁粉分别与相同浓度的盐酸反应 等质量的铁粉分别与不同浓度的盐酸(3%和15%)反应 不同温度下,等质量的铁粉与相同浓度的足量稀盐酸反应
A.由图1可知:盐酸不能与铁丝反应
B.由图1可得结论:铁粉反应更快
C.由图2可知3%的盐酸与铁粉反应更快
D.由图3所示实验可知温度不影响生成氢气的总质量
6.相同条件下,下列事实不能证明金属甲的金属活动性比金属乙强的是
A.甲比乙更容易与氧气反应
B.甲能与盐酸反应生成H2而乙不能
C.甲能从乙的化合物溶液中置换出乙
D.甲元素在化合物中显+2价,而乙元素在化合物中显+3价
7.要区别下列各组物质,所选择的方法(或试剂)不正确的是( )
A.酒精和白醋(闻气味) B.水和双氧水(二氧化锰)
C.氧化铜和二氧化锰 (观察颜色) D.铁丝和铜丝 (观察颜色)
8.下列图象分别表示4个实验过程中某些物质某些量的变化,其中正确的是( )
A.向一定量铁粉中滴加稀盐酸
B.向一定量硫酸铜溶液中不断加入铁粉
C.加热一定量高锰酸钾固体
D.向一定量的稀盐酸中加入一定量的大理石
9.如图表示对水进行消毒时所发生反应的微观过程。下列有关说法正确的是
A.图中单质的化学式为O2 B.该反应属于置换反应
C.生成物有三种 D.反应物与生成物的分子个数比为
10.为比较A、B、C三种金属的活动性,某同学设计了如图所示实验,由此判断三种金属活动性由强到弱的顺序是( )
A.A>C>B B.A>B>C C.C>A>B D.B>C>A
11.下列属于金属材料的是( )
A.玻璃 B.钢铁 C.木材 D.氧化铁
12.除去一氧化碳中混有的少量水蒸气、氧气、二氧化碳气体,混合气体应依次通过
A.干燥剂、灼热铜网、足量石灰水 B.灼热的铜网、足量石灰水、干燥剂
C.干燥剂、足量石灰水、灼热的铜网 D.灼热的铜网、干燥剂、足量石灰水
二、填空题
13.利用生铁制造铸铁锅,是因为铁有良好的的___性,但极易生锈,使用后应如何保养___。
14.回答与金属有关的问题。
(1)在Zn、Ag、Fe三种金属中,通常不能与稀盐酸发生置换反应的是____;
(2)在铁制品表面涂油漆能防止铁制品生锈,原因是____;
(3)向含有Cu(NO3)2和AgNO3溶液烧杯中加入一定量的Mg粉,充分反应后过滤,得到滤液和滤渣,向滤液中滴加稀盐酸产生白色沉淀,则滤渣的成分是____。
15.人类的生产生活都离不开金属,请回答下列问题:
(1)生活中常用铜做导线,主要是利用了铜的_____;
(2)铁锅生锈的原因是_____;
(3)使用完铁锅后,防止生锈的办法是_____;
(4)废弃铁锅回收利用的意义是_____。
三、实验题
16.化学小组同学用如图所示装置模拟工业炼铁,请回答下列问题:
(1)写出如图装置中玻璃管A内发生反应的现象_______,化学方程式______。
(2)从环保角度考虑,对以上装置的改进措施是______。
(3)实验加热前先通一氧化碳的目的_______。
四、计算题
17.黄铜是铜和锌的合金(Cu﹣Zn),它可用来制造电器零件及日用品,为了测定某黄铜样品中锌的质量分数(不考虑黄铜中的其他杂质),现将15mL稀硫酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见表,试回答下列问题:
第一次 第二次 第三次
加入稀硫酸的体积(mL) 5 5 5
生成氢气的质量(g) 0.04 m 0.02
(1)写出反应的化学方程式______.
(2)m=______.
(3)列出第一次反应中参加反应的锌的质量(x)的比例式是______.
(4)此黄铜样品中锌的质量分数是______.
(5)若工业上用含Cu2S80%的辉铜矿135t(炼制过程中辉铜矿的损失率为20%),能炼出上述黄铜的质量为______.
18.向 133.4 克稀盐酸中加入锌粉(杂质不溶于水也不溶于酸),所加锌粉的质量与产生气体的 质量的关系如下图所示。求:
(1)该反应中化合价改变的元素是______(填名称)。
(2)原稀盐酸中溶质的质量分数为多少?(结果精确到 0.1%)
参考答案:
1.B
2.A
3.C
4.D
5.A
6.D
7.C
8.C
9.D
10.B
11.B
12.B
13. 导热 保持表面干燥
14. Ag 能隔绝铁与氧气、水的接触 银
15. 导电性 铁与水和氧气充分接触生成氧化铁 洗净擦干 既节约金属资源,又可以防止造成环境的污染
16.(1) 红色粉末变成黑色
(2)增加尾气处理装置(答案合理即可)
(3)排出装置中的空气,防止一氧化碳和空气混合,发生爆炸
17.(1)(2)0.04(3)(4)32.5%(5)102.4t
18.(1)锌元素与氢元素
(2)解:设稀盐酸中溶质的质量分数为x
答:稀盐酸中溶质的质量分数为10.9%。
同课章节目录
