2022-2023学年鲁科版高中化学必修一 1.3.3物质的量浓度 课件(共18张PPT)
文档属性
| 名称 | 2022-2023学年鲁科版高中化学必修一 1.3.3物质的量浓度 课件(共18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 47.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-28 00:00:00 | ||
图片预览




文档简介
(共18张PPT)
第3课时 物质的量浓度
鲁科版必修一 第一章第三节化学中常用的物理量——物质的量
牛奶
1.会设计实验方案并配制一定物质的量浓度的溶液
加强科学探究意识
规范操作严谨求实
2.会用物质的量浓度表示溶液的组成并指导生产生活
学会分析推理
建立模型认知
3.能从物质的量的角度认识化学反应
素养
素养
知识
知识
知识
学习目标
核心素养
素养
会结合微观与宏观两个视角分析问题
如何配制100g质量分数为5%的NaCl溶液?
需要用到哪些实验用品?
知识回顾
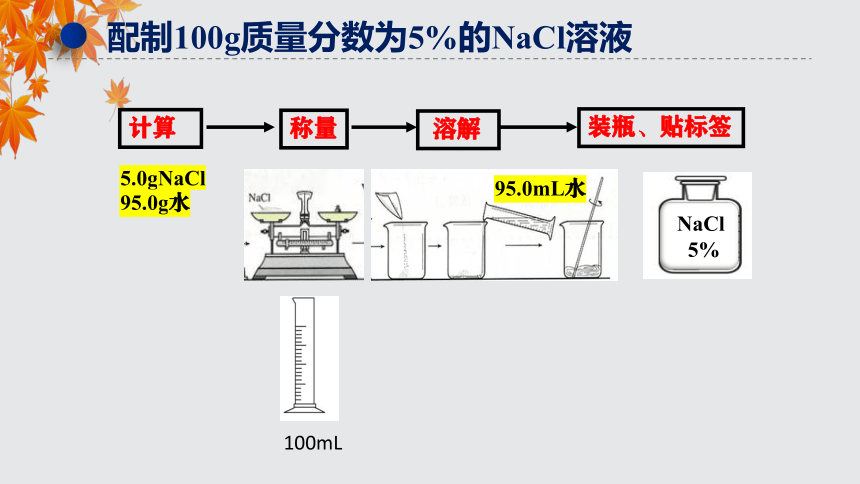
计算
装瓶、贴标签
NaCl
5%
5.0gNaCl
95.0g水
溶解
95.0mL水
配制100g质量分数为5%的NaCl溶液
称量
100mL
【任务一】 配制一定物质的量浓度的溶液
如何配制溶质的物质的量为0.04mol
体积为0.1L的NaCl溶液
思考
m=nM
=0.04mol×58.5g·mol-1
观察
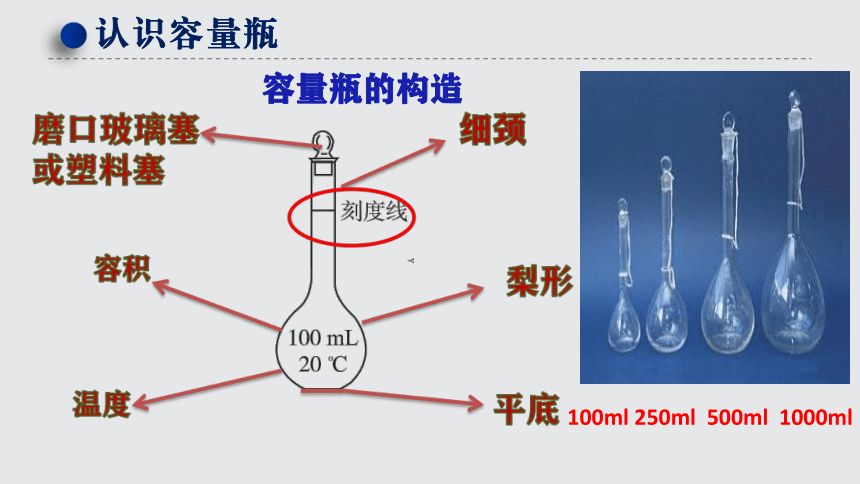
细颈
梨形
平底
磨口玻璃塞
或塑料塞
容积
温度
容量瓶的构造
认识容量瓶
100ml 250ml 500ml 1000ml
为了保证配制溶液浓度的精确度,操作时注意哪些问题?
【任务一】 配制一定物质的量浓度的溶液
问题探究
尽可能将溶质全
部转移到容量瓶
氯化钠0.04mol
向容量瓶中加水时溶液凹液面不超过刻度线
溶液体积为0.1L
延时符
01
02
03
04
实验步骤
具体操作
实验仪器
分组实验
【任务一】 配制一定物质的量浓度的溶液
小组讨论
配制一定物质的量浓度溶液步骤
溶解
(室温)
洗涤
转移
转移
摇匀
装瓶、贴标签
注意烧杯尖嘴位置和玻璃棒位置
容量瓶漏 液行吗?
定容
计算
2.34g
称量
电子天平
可称2.34g
2.3g
小组汇报
分组实验
【任务一】 配制一定物质的量浓度的溶液
分工合作 规范操作
1.将配好的氯化钠溶液转移到试剂瓶中
标签纸应该如何填写?
问题探究
2.如何定义物质的量浓度?
【任务二】 用物质的量浓度表示溶液的组成
物质的
量浓度
含义
单位体积溶液所含溶质B的
物质的量
表达式
单位
mol·L-1或mol·m-3或 mmol·L-1
解读血液报告单
迁移应用
【概念辨析】 用物质的量浓度表示溶液的组成
①将 58.5gNaCl 溶于1L水中则c(NaCl)= 1 mol·L-1
② 从 1L 1 mol·L-1 的 NaOH 溶液中取出 20mL则c(NaCl)= 1 mol·L-1
判断下列说法是否正确?
√
×
污水处理取样测定
迁移应用
【任务三】 实验误差分析
操作 mB V cB
1.未洗涤烧杯和玻璃棒
2.定容时俯视刻度
3.摇匀后液面下降,补充水
4.超过刻度线,吸出一部分水
偏小
无影响
偏小
无影响
偏小
偏大
偏小
无影响
偏小
无影响
偏大
偏小
偏大
偏小
重新配制
N
n
m
÷NA
×M
×NA
÷M
V(气体)
×Vm
÷Vm
(标准状况 22.4L·mol-1)
V(溶液)
÷CB
×CB
【概括整合】构建n和m、N、CB、 V 网络关系
微观
宏观
第3课时 物质的量浓度
鲁科版必修一 第一章第三节化学中常用的物理量——物质的量
牛奶
1.会设计实验方案并配制一定物质的量浓度的溶液
加强科学探究意识
规范操作严谨求实
2.会用物质的量浓度表示溶液的组成并指导生产生活
学会分析推理
建立模型认知
3.能从物质的量的角度认识化学反应
素养
素养
知识
知识
知识
学习目标
核心素养
素养
会结合微观与宏观两个视角分析问题
如何配制100g质量分数为5%的NaCl溶液?
需要用到哪些实验用品?
知识回顾
计算
装瓶、贴标签
NaCl
5%
5.0gNaCl
95.0g水
溶解
95.0mL水
配制100g质量分数为5%的NaCl溶液
称量
100mL
【任务一】 配制一定物质的量浓度的溶液
如何配制溶质的物质的量为0.04mol
体积为0.1L的NaCl溶液
思考
m=nM
=0.04mol×58.5g·mol-1
观察
细颈
梨形
平底
磨口玻璃塞
或塑料塞
容积
温度
容量瓶的构造
认识容量瓶
100ml 250ml 500ml 1000ml
为了保证配制溶液浓度的精确度,操作时注意哪些问题?
【任务一】 配制一定物质的量浓度的溶液
问题探究
尽可能将溶质全
部转移到容量瓶
氯化钠0.04mol
向容量瓶中加水时溶液凹液面不超过刻度线
溶液体积为0.1L
延时符
01
02
03
04
实验步骤
具体操作
实验仪器
分组实验
【任务一】 配制一定物质的量浓度的溶液
小组讨论
配制一定物质的量浓度溶液步骤
溶解
(室温)
洗涤
转移
转移
摇匀
装瓶、贴标签
注意烧杯尖嘴位置和玻璃棒位置
容量瓶漏 液行吗?
定容
计算
2.34g
称量
电子天平
可称2.34g
2.3g
小组汇报
分组实验
【任务一】 配制一定物质的量浓度的溶液
分工合作 规范操作
1.将配好的氯化钠溶液转移到试剂瓶中
标签纸应该如何填写?
问题探究
2.如何定义物质的量浓度?
【任务二】 用物质的量浓度表示溶液的组成
物质的
量浓度
含义
单位体积溶液所含溶质B的
物质的量
表达式
单位
mol·L-1或mol·m-3或 mmol·L-1
解读血液报告单
迁移应用
【概念辨析】 用物质的量浓度表示溶液的组成
①将 58.5gNaCl 溶于1L水中则c(NaCl)= 1 mol·L-1
② 从 1L 1 mol·L-1 的 NaOH 溶液中取出 20mL则c(NaCl)= 1 mol·L-1
判断下列说法是否正确?
√
×
污水处理取样测定
迁移应用
【任务三】 实验误差分析
操作 mB V cB
1.未洗涤烧杯和玻璃棒
2.定容时俯视刻度
3.摇匀后液面下降,补充水
4.超过刻度线,吸出一部分水
偏小
无影响
偏小
无影响
偏小
偏大
偏小
无影响
偏小
无影响
偏大
偏小
偏大
偏小
重新配制
N
n
m
÷NA
×M
×NA
÷M
V(气体)
×Vm
÷Vm
(标准状况 22.4L·mol-1)
V(溶液)
÷CB
×CB
【概括整合】构建n和m、N、CB、 V 网络关系
微观
宏观
