专题3 微粒间作用力与物质性质 单元检测题 (含答案) 2022-2023学年高二化学苏教版(2019)选择性必修2
文档属性
| 名称 | 专题3 微粒间作用力与物质性质 单元检测题 (含答案) 2022-2023学年高二化学苏教版(2019)选择性必修2 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-02 00:00:00 | ||
图片预览


文档简介
专题3《微粒间作用力与物质性质》单元检测题
一、单选题(共13题)
1.已知晶体属立方晶系,晶胞边长a。将掺杂到该晶胞中,可得到一种高性能的p型太阳能电池材料,其结构单元如图所示。
假定掺杂后的晶胞参数不发生变化,下列说法正确的是
A.该结构单元中O原子数为3 B.Ni和Mg间的最短距离是
C.Ni的配位数为4 D.该物质的化学式为
2.下列有关晶体的说法中一定正确的是( )
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤分子晶体的堆积均为分子密堆积
⑥离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
⑦金属晶体和离子晶体都能导电
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
A.①③⑦ B.只有⑥ C.②④⑤⑦ D.⑤⑥⑧
3.下列化合物中,不可能含有离子键的是
A.酸 B.碱 C.盐 D.氧化物
4.有5种元素X、Y、Z、Q、T。X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的核外电子总数等于Q原子的最外层电子数;Q原子的L电子层的p能级上只有一对成对电子;T原子有1个3p空轨道。下列叙述错误的是
A.元素Y和Q可形成化合物Y2Q3
B.气态氢化物的稳定性:Q>T>Z
C.X和Q结合生成的化合物晶体类型为分子晶体
D.T和Z的最高价氧化物均为酸性氧化物
5.在新型催化剂作用下,氧化可获得,反应为 。下列说法正确的是
A.该反应中反应物键能总和大于生成物键能总和
B.反应中和的总能量大于的总能量
C.上述反应过程中有极性键和非极性键的断裂和形成
D.的使用能降低该反应的焓变
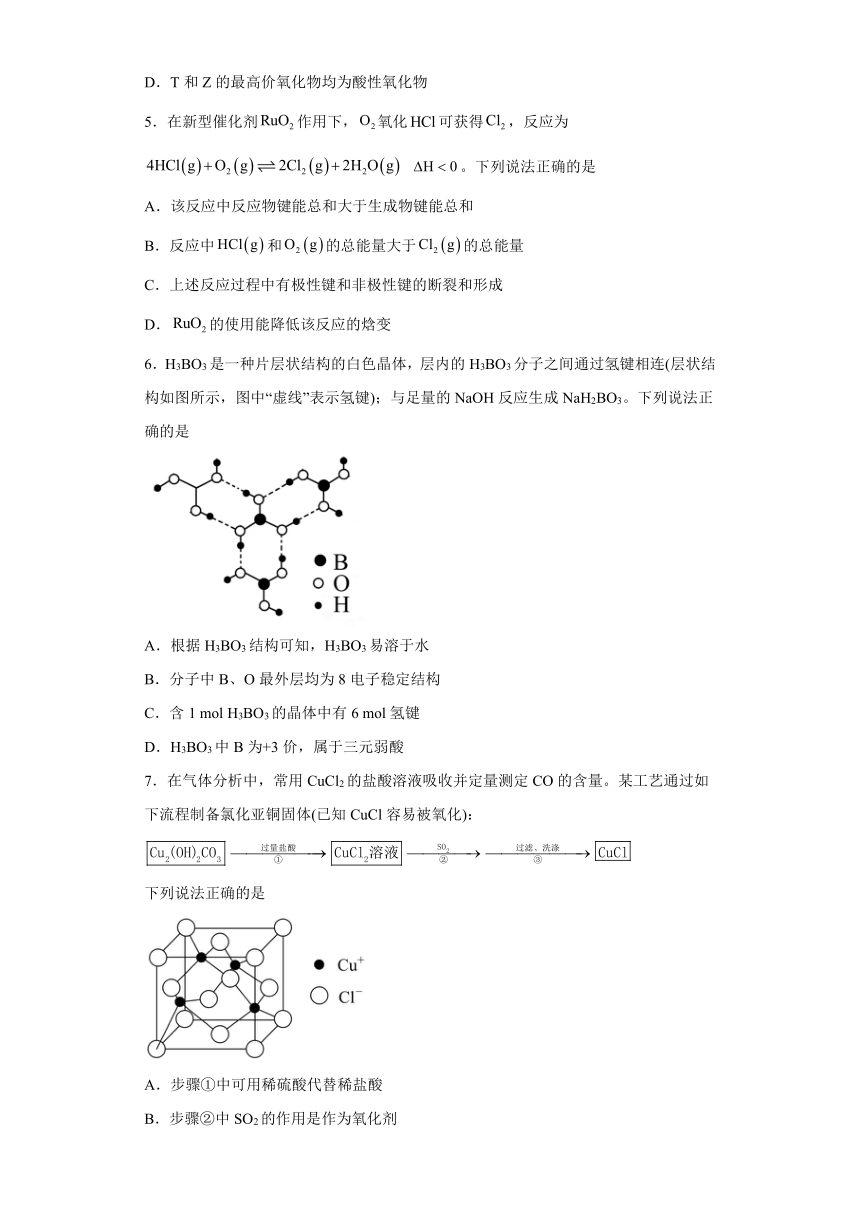
6.H3BO3是一种片层状结构的白色晶体,层内的H3BO3分子之间通过氢键相连(层状结构如图所示,图中“虚线”表示氢键);与足量的NaOH反应生成NaH2BO3。下列说法正确的是
A.根据H3BO3结构可知,H3BO3易溶于水
B.分子中B、O最外层均为8电子稳定结构
C.含1 mol H3BO3的晶体中有6 mol氢键
D.H3BO3中B为+3价,属于三元弱酸
7.在气体分析中,常用CuCl2的盐酸溶液吸收并定量测定CO的含量。某工艺通过如下流程制备氯化亚铜固体(已知CuCl容易被氧化):
下列说法正确的是
A.步骤①中可用稀硫酸代替稀盐酸
B.步骤②中SO2的作用是作为氧化剂
C.步骤③中用SO2水溶液洗涤比较有效
D.CuCl晶胞结构如图所示,每个氯离子周围与之距离最近的氯离子数目为4
8.下列说法正确的是
A.含有金属元素的化合物一定是离子化合物
B.完全由非金属元素组成的化合物可能是离子化合物
C.IA族和VIIA族元素原子间只能形成离子键
D.金属键只存在于金属单质中
9.砷化镓是一种重要的半导体材料,熔点1238。它在600以下,能在空气中稳定存在,并且不被非氧化性的酸侵蚀。砷化镓晶胞结构如图。下列说法正确的是
A.砷化镓是一种分子晶体
B.砷化镓中不存在配位键
C.晶胞中Ga原子与As原子的数量比为4:1
D.晶胞中Ga与周围等距且最近的As形成的空间构型为正四面体
10.下列物质中有氧离子存在的是
A.CaO B.H2O C.KClO3 D.KOH
11.反应Cl2+2NaOH = NaClO+NaCl+H2O,可用于制备含氯消毒剂,下列说法正确的是
A.Cl2中共价键类型为极性共价键 B.NaOH的电子式:
C.中子数为18的Cl原子:Cl D.基态Na原子的外围电子排布式为3s1
12.下列说法不正确的是
A.NaCl和晶体所含化学键的类型相同
B.和是同素异形体
C.干冰、二氧化硅均属于原子晶体
D.合成纤维是一类高分子化合物
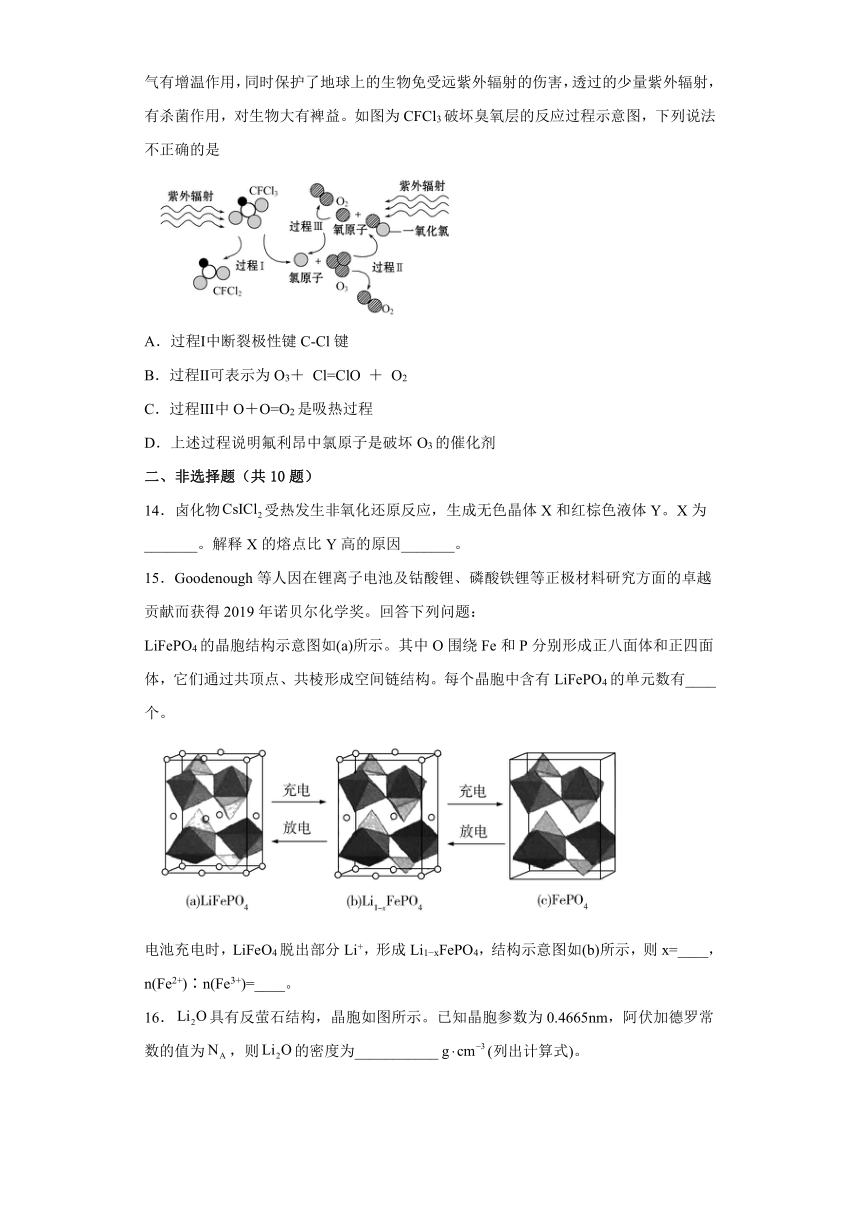
13.臭氧层是大气层的平流层中臭氧浓度高的层次。紫外辐射在高空被臭氧吸收,对大气有增温作用,同时保护了地球上的生物免受远紫外辐射的伤害,透过的少量紫外辐射,有杀菌作用,对生物大有裨益。如图为CFCl3破坏臭氧层的反应过程示意图,下列说法不正确的是
A.过程Ⅰ中断裂极性键C-Cl键
B.过程Ⅱ可表示为O3+ Cl=ClO + O2
C.过程Ⅲ中O+O=O2是吸热过程
D.上述过程说明氟利昂中氯原子是破坏O3的催化剂
二、非选择题(共10题)
14.卤化物受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。解释X的熔点比Y高的原因_______。
15.Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有____个。
电池充电时,LiFeO4脱出部分Li+,形成Li1 xFePO4,结构示意图如(b)所示,则x=____,n(Fe2+)∶n(Fe3+)=____。
16.具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为,则的密度为___________(列出计算式)。
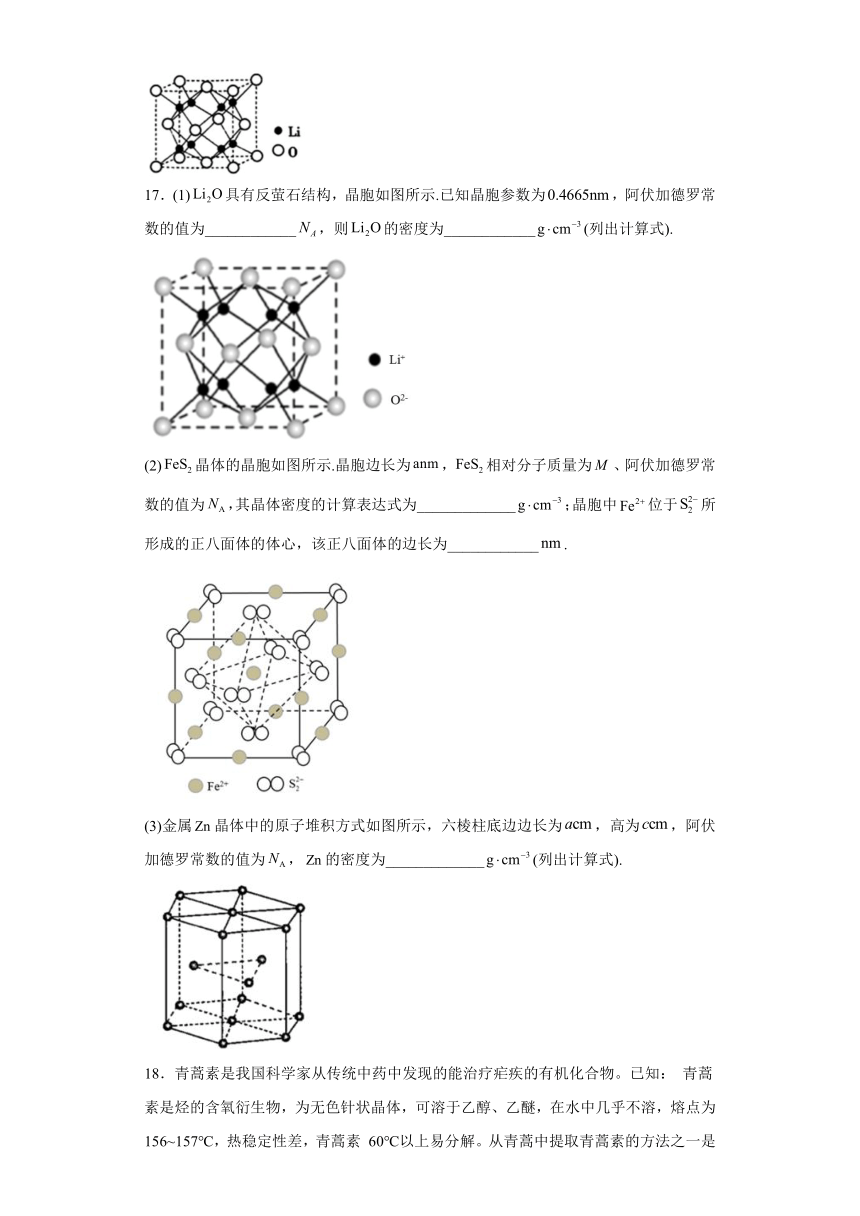
17.(1)具有反萤石结构,晶胞如图所示.已知晶胞参数为,阿伏加德罗常数的值为____________,则的密度为____________(列出计算式).
(2)晶体的晶胞如图所示.晶胞边长为,相对分子质量为、阿伏加德罗常数的值为,其晶体密度的计算表达式为_____________;晶胞中位于所形成的正八面体的体心,该正八面体的边长为____________.
(3)金属晶体中的原子堆积方式如图所示,六棱柱底边边长为,高为,阿伏加德罗常数的值为,的密度为_____________(列出计算式).
18.青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物。已知: 青蒿素是烃的含氧衍生物,为无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素 60℃以上易分解。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的。
(1)从青蒿中提取青蒿素的流程如下:研究团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
溶剂 水 乙醇 乙醚
沸点/℃ 100 78 34.5
提取效率 几乎为 0 35% 95%
①分离残渣与提取液的实验操作是___________;操作Ⅱ的名称是___________。
②提取青蒿素使用的溶剂最好选择___________。
③研究发现,青蒿素分子中的某个基团受热不稳定,据此分析用乙醇作溶剂,提取效率偏低,不能达到理想效果的原因是___________。
④操作Ⅲ的主要过程可能是___________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶 B.加 95%的乙醇,浓缩、结晶、过滤 C.加入乙醚进行萃取分液
(2)某学生对青蒿素的性质进行探究。将青蒿素加入含有 NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与______ (填字母)具有相似的性质。A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(3)青蒿素的质谱数据中有一个峰值与另一种抗疟药鹰爪素相同,而鹰爪素的该质谱峰对应过氧基团,于是推测青蒿素中也含有过氧基团,请写出过氧基的电子式:___________。青蒿素所属晶体类型为___________晶体。
(4)研究还发现,将青蒿素通过下面反应转化为双氢青蒿素,治疗疟疾的效果更好。
该反应的反应类型是___________反应。
(5)科学家对 H2O2分子结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:甲:、乙: H—O—O—H,甲式中 O→O 表示配位键,在化学反应中 O→O 键遇到还原剂时易断裂。化学家 Baeyer 和 Villiyer 为研究 H2O2的分子结构,设计并完成了下列实验:
a.将 C2H5OH 与浓 H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与 H2O2反应,只生成 A 和 H2SO4;
c.将生成的 A 与 H2反应(已知该反应中 H2作还原剂)。
①如果 H2O2的结构如甲所示,实验 c 中化学反应方程式为(A 写结构简式)___________。
②为了进一步确定 H2O2的结构,还需要在实验 c 后添加一步实验 d,请设计 d 的实验方案:___________。
19.某同学设计了如图所示的装置,可比较HNO3、H2CO3、H2SiO3的酸性强弱,进而比较氮、碳、硅元素非金属性强弱。供选择的试剂:稀硝酸、稀硫酸、碳酸钙固体、碳酸钠固体、硅酸钠溶液、澄清石灰水、饱和碳酸氢钠溶液
(1)仪器a的名称:___________。
(2)锥形瓶中装有某可溶性正盐,a中所盛试剂为___________。
(3)装置B所盛试剂是___________,其作用是___________。
(4)装置C所盛试剂是___________,C中反应的离子方程式是___________。
(5)通过实验证明碳、氮、硅的非金属性由强到弱的顺序是___________。
(6)写出碳、氮、硅三元素的简单气态氢化物的稳定性由强到弱的顺序是(写化学式)___________。
(7)写出碳、氮、硅三元素的简单气态氢化物的沸点由高到低的顺序是(写化学式)___________。
20.为探究某物质X(仅含两种元素)的组成和性质,设计并完成如下实验。(气体体积已转化为标况体积)
请回答下列问题:
(1)X的化学式为___________。
(2)A的结构式为________,E属于_______化合物(填离子或共价)。
21.硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。某些硅酸盐具有筛选分子的功能,一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期。两元素原子的质子数之和为24。
(1)该硅酸盐中同周期元素原子半径由大到小的顺序为_______;写出M原子核外能量最高的电子的电子排布式为_______;
(2)常温下,不能与R单质发生反应的是_______(选填序号);
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.Na2CO3溶液
(3)写出M、R两种元素的最高价氧化物对应的水化物反应的离子方程式_______。
(4) 氮化硅(Si3N4)陶瓷材料硬度大、熔点高。Si3N4晶体中只有极性共价键,则氮原子的化合价为_______。
(5)C3N4的结构与Si3N4相似。请比较二者熔点高低并说明理由:_______。
(6)可由下列反应制得Si3N4,配平该反应并标出电子转移的数目和方向:_______。
_______SiO2+_______C+_______N2_______Si3N4+_______CO
(7)如果上述反应在10L的密闭容器中进行,一段时间后测得气体密度增加了2.8g/L,则制得的Si3N4质量为_______。
22.下表是元素周期表的一部分,请据表标注的元素回答(用化学符号作答):
族 周期 I A IIA IIIA IVA VA VIA VIIA 0
1 a f
2 b d e
3 g h k m n
(1)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为___________(用物质化学式表示);
(2)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有___________;
(3)写出由元素a、e、g组成的化合物的电子式:___________;
(4)写出由元素b、e组成的化合物be2的结构式:___________;
23.已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号主族元素,A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子外围电子排布式:____。写出F的离子电子排布式:______。
(2)试解释工业冶炼D的单质不以DE3为原料而是以D2A3为原料的原因:_______。
(3)CE、FA的晶格能分别为,试分析导致两者晶格能差异的主要原因是_______。
(4)F与B可形成离子化合物,其晶胞结构如图所示。F与B形成的离子化合物的化学式为_______;该离子化合物晶体的密度为,则晶胞的体积是_______(只要求列出计算式)。
参考答案:
1.B 2.B 3.A 4.B 5.C 6.A 7.C 8.B 9.D 10.A 11.D 12.C
13.C
14. 为离子晶体,为分子晶体
15. 4 或0.1875 13:3
16.
17.
18.(1) 过滤 蒸馏 乙醚 乙醇沸点相对乙醚来说较高,分离时易造成青蒿素受热被破坏,导致其提取效率偏低 B
(2)C
(3) 分子晶体
(4)还原反应
(5) +H2→C2H5OC2H5+H2O 用无水硫酸铜检验c的反应产物中有没有水(或其他合理答案)
19.(1)分液漏斗
(2)稀硝酸
(3) 饱和碳酸氢钠溶液 吸收气体中硝酸
(4) 硅酸钠溶液 SiO+CO2+H2O=H2SiO3↓+CO
(5)N>C>Si
(6)NH3>CH4>SiH4
(7)NH3>SiH4>CH4
20. Fe3C O=C=O 离子
21.(1) r(Na)>r(Al)>r(Si) 3s1
(2)bd
(3)OH-+Al(OH)3=+2H2O
(4) 3
(5)C3N4熔点比Si3N4熔点高,原因为两者都是原子晶体,碳原子半径比硅原子半径小,键长短,键能大,因此C3N4熔点比Si3N4熔点高
(6)
(7)35g
22.(1)HClO4>H2SO4>H2SiO3
(2)离子键和共价键
(3)
(4)O=C=O
23.(1)
(2)为离子晶体(或者离子化合物),而为分子晶体(或者共价化合物)
(3)晶体中带的电荷数大于晶体中的电荷数
(4)
一、单选题(共13题)
1.已知晶体属立方晶系,晶胞边长a。将掺杂到该晶胞中,可得到一种高性能的p型太阳能电池材料,其结构单元如图所示。
假定掺杂后的晶胞参数不发生变化,下列说法正确的是
A.该结构单元中O原子数为3 B.Ni和Mg间的最短距离是
C.Ni的配位数为4 D.该物质的化学式为
2.下列有关晶体的说法中一定正确的是( )
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤分子晶体的堆积均为分子密堆积
⑥离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
⑦金属晶体和离子晶体都能导电
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
A.①③⑦ B.只有⑥ C.②④⑤⑦ D.⑤⑥⑧
3.下列化合物中,不可能含有离子键的是
A.酸 B.碱 C.盐 D.氧化物
4.有5种元素X、Y、Z、Q、T。X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的核外电子总数等于Q原子的最外层电子数;Q原子的L电子层的p能级上只有一对成对电子;T原子有1个3p空轨道。下列叙述错误的是
A.元素Y和Q可形成化合物Y2Q3
B.气态氢化物的稳定性:Q>T>Z
C.X和Q结合生成的化合物晶体类型为分子晶体
D.T和Z的最高价氧化物均为酸性氧化物
5.在新型催化剂作用下,氧化可获得,反应为 。下列说法正确的是
A.该反应中反应物键能总和大于生成物键能总和
B.反应中和的总能量大于的总能量
C.上述反应过程中有极性键和非极性键的断裂和形成
D.的使用能降低该反应的焓变
6.H3BO3是一种片层状结构的白色晶体,层内的H3BO3分子之间通过氢键相连(层状结构如图所示,图中“虚线”表示氢键);与足量的NaOH反应生成NaH2BO3。下列说法正确的是
A.根据H3BO3结构可知,H3BO3易溶于水
B.分子中B、O最外层均为8电子稳定结构
C.含1 mol H3BO3的晶体中有6 mol氢键
D.H3BO3中B为+3价,属于三元弱酸
7.在气体分析中,常用CuCl2的盐酸溶液吸收并定量测定CO的含量。某工艺通过如下流程制备氯化亚铜固体(已知CuCl容易被氧化):
下列说法正确的是
A.步骤①中可用稀硫酸代替稀盐酸
B.步骤②中SO2的作用是作为氧化剂
C.步骤③中用SO2水溶液洗涤比较有效
D.CuCl晶胞结构如图所示,每个氯离子周围与之距离最近的氯离子数目为4
8.下列说法正确的是
A.含有金属元素的化合物一定是离子化合物
B.完全由非金属元素组成的化合物可能是离子化合物
C.IA族和VIIA族元素原子间只能形成离子键
D.金属键只存在于金属单质中
9.砷化镓是一种重要的半导体材料,熔点1238。它在600以下,能在空气中稳定存在,并且不被非氧化性的酸侵蚀。砷化镓晶胞结构如图。下列说法正确的是
A.砷化镓是一种分子晶体
B.砷化镓中不存在配位键
C.晶胞中Ga原子与As原子的数量比为4:1
D.晶胞中Ga与周围等距且最近的As形成的空间构型为正四面体
10.下列物质中有氧离子存在的是
A.CaO B.H2O C.KClO3 D.KOH
11.反应Cl2+2NaOH = NaClO+NaCl+H2O,可用于制备含氯消毒剂,下列说法正确的是
A.Cl2中共价键类型为极性共价键 B.NaOH的电子式:
C.中子数为18的Cl原子:Cl D.基态Na原子的外围电子排布式为3s1
12.下列说法不正确的是
A.NaCl和晶体所含化学键的类型相同
B.和是同素异形体
C.干冰、二氧化硅均属于原子晶体
D.合成纤维是一类高分子化合物
13.臭氧层是大气层的平流层中臭氧浓度高的层次。紫外辐射在高空被臭氧吸收,对大气有增温作用,同时保护了地球上的生物免受远紫外辐射的伤害,透过的少量紫外辐射,有杀菌作用,对生物大有裨益。如图为CFCl3破坏臭氧层的反应过程示意图,下列说法不正确的是
A.过程Ⅰ中断裂极性键C-Cl键
B.过程Ⅱ可表示为O3+ Cl=ClO + O2
C.过程Ⅲ中O+O=O2是吸热过程
D.上述过程说明氟利昂中氯原子是破坏O3的催化剂
二、非选择题(共10题)
14.卤化物受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。解释X的熔点比Y高的原因_______。
15.Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有____个。
电池充电时,LiFeO4脱出部分Li+,形成Li1 xFePO4,结构示意图如(b)所示,则x=____,n(Fe2+)∶n(Fe3+)=____。
16.具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为,则的密度为___________(列出计算式)。
17.(1)具有反萤石结构,晶胞如图所示.已知晶胞参数为,阿伏加德罗常数的值为____________,则的密度为____________(列出计算式).
(2)晶体的晶胞如图所示.晶胞边长为,相对分子质量为、阿伏加德罗常数的值为,其晶体密度的计算表达式为_____________;晶胞中位于所形成的正八面体的体心,该正八面体的边长为____________.
(3)金属晶体中的原子堆积方式如图所示,六棱柱底边边长为,高为,阿伏加德罗常数的值为,的密度为_____________(列出计算式).
18.青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物。已知: 青蒿素是烃的含氧衍生物,为无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素 60℃以上易分解。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的。
(1)从青蒿中提取青蒿素的流程如下:研究团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
溶剂 水 乙醇 乙醚
沸点/℃ 100 78 34.5
提取效率 几乎为 0 35% 95%
①分离残渣与提取液的实验操作是___________;操作Ⅱ的名称是___________。
②提取青蒿素使用的溶剂最好选择___________。
③研究发现,青蒿素分子中的某个基团受热不稳定,据此分析用乙醇作溶剂,提取效率偏低,不能达到理想效果的原因是___________。
④操作Ⅲ的主要过程可能是___________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶 B.加 95%的乙醇,浓缩、结晶、过滤 C.加入乙醚进行萃取分液
(2)某学生对青蒿素的性质进行探究。将青蒿素加入含有 NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与______ (填字母)具有相似的性质。A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(3)青蒿素的质谱数据中有一个峰值与另一种抗疟药鹰爪素相同,而鹰爪素的该质谱峰对应过氧基团,于是推测青蒿素中也含有过氧基团,请写出过氧基的电子式:___________。青蒿素所属晶体类型为___________晶体。
(4)研究还发现,将青蒿素通过下面反应转化为双氢青蒿素,治疗疟疾的效果更好。
该反应的反应类型是___________反应。
(5)科学家对 H2O2分子结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:甲:、乙: H—O—O—H,甲式中 O→O 表示配位键,在化学反应中 O→O 键遇到还原剂时易断裂。化学家 Baeyer 和 Villiyer 为研究 H2O2的分子结构,设计并完成了下列实验:
a.将 C2H5OH 与浓 H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与 H2O2反应,只生成 A 和 H2SO4;
c.将生成的 A 与 H2反应(已知该反应中 H2作还原剂)。
①如果 H2O2的结构如甲所示,实验 c 中化学反应方程式为(A 写结构简式)___________。
②为了进一步确定 H2O2的结构,还需要在实验 c 后添加一步实验 d,请设计 d 的实验方案:___________。
19.某同学设计了如图所示的装置,可比较HNO3、H2CO3、H2SiO3的酸性强弱,进而比较氮、碳、硅元素非金属性强弱。供选择的试剂:稀硝酸、稀硫酸、碳酸钙固体、碳酸钠固体、硅酸钠溶液、澄清石灰水、饱和碳酸氢钠溶液
(1)仪器a的名称:___________。
(2)锥形瓶中装有某可溶性正盐,a中所盛试剂为___________。
(3)装置B所盛试剂是___________,其作用是___________。
(4)装置C所盛试剂是___________,C中反应的离子方程式是___________。
(5)通过实验证明碳、氮、硅的非金属性由强到弱的顺序是___________。
(6)写出碳、氮、硅三元素的简单气态氢化物的稳定性由强到弱的顺序是(写化学式)___________。
(7)写出碳、氮、硅三元素的简单气态氢化物的沸点由高到低的顺序是(写化学式)___________。
20.为探究某物质X(仅含两种元素)的组成和性质,设计并完成如下实验。(气体体积已转化为标况体积)
请回答下列问题:
(1)X的化学式为___________。
(2)A的结构式为________,E属于_______化合物(填离子或共价)。
21.硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。某些硅酸盐具有筛选分子的功能,一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期。两元素原子的质子数之和为24。
(1)该硅酸盐中同周期元素原子半径由大到小的顺序为_______;写出M原子核外能量最高的电子的电子排布式为_______;
(2)常温下,不能与R单质发生反应的是_______(选填序号);
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.Na2CO3溶液
(3)写出M、R两种元素的最高价氧化物对应的水化物反应的离子方程式_______。
(4) 氮化硅(Si3N4)陶瓷材料硬度大、熔点高。Si3N4晶体中只有极性共价键,则氮原子的化合价为_______。
(5)C3N4的结构与Si3N4相似。请比较二者熔点高低并说明理由:_______。
(6)可由下列反应制得Si3N4,配平该反应并标出电子转移的数目和方向:_______。
_______SiO2+_______C+_______N2_______Si3N4+_______CO
(7)如果上述反应在10L的密闭容器中进行,一段时间后测得气体密度增加了2.8g/L,则制得的Si3N4质量为_______。
22.下表是元素周期表的一部分,请据表标注的元素回答(用化学符号作答):
族 周期 I A IIA IIIA IVA VA VIA VIIA 0
1 a f
2 b d e
3 g h k m n
(1)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为___________(用物质化学式表示);
(2)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有___________;
(3)写出由元素a、e、g组成的化合物的电子式:___________;
(4)写出由元素b、e组成的化合物be2的结构式:___________;
23.已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号主族元素,A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子外围电子排布式:____。写出F的离子电子排布式:______。
(2)试解释工业冶炼D的单质不以DE3为原料而是以D2A3为原料的原因:_______。
(3)CE、FA的晶格能分别为,试分析导致两者晶格能差异的主要原因是_______。
(4)F与B可形成离子化合物,其晶胞结构如图所示。F与B形成的离子化合物的化学式为_______;该离子化合物晶体的密度为,则晶胞的体积是_______(只要求列出计算式)。
参考答案:
1.B 2.B 3.A 4.B 5.C 6.A 7.C 8.B 9.D 10.A 11.D 12.C
13.C
14. 为离子晶体,为分子晶体
15. 4 或0.1875 13:3
16.
17.
18.(1) 过滤 蒸馏 乙醚 乙醇沸点相对乙醚来说较高,分离时易造成青蒿素受热被破坏,导致其提取效率偏低 B
(2)C
(3) 分子晶体
(4)还原反应
(5) +H2→C2H5OC2H5+H2O 用无水硫酸铜检验c的反应产物中有没有水(或其他合理答案)
19.(1)分液漏斗
(2)稀硝酸
(3) 饱和碳酸氢钠溶液 吸收气体中硝酸
(4) 硅酸钠溶液 SiO+CO2+H2O=H2SiO3↓+CO
(5)N>C>Si
(6)NH3>CH4>SiH4
(7)NH3>SiH4>CH4
20. Fe3C O=C=O 离子
21.(1) r(Na)>r(Al)>r(Si) 3s1
(2)bd
(3)OH-+Al(OH)3=+2H2O
(4) 3
(5)C3N4熔点比Si3N4熔点高,原因为两者都是原子晶体,碳原子半径比硅原子半径小,键长短,键能大,因此C3N4熔点比Si3N4熔点高
(6)
(7)35g
22.(1)HClO4>H2SO4>H2SiO3
(2)离子键和共价键
(3)
(4)O=C=O
23.(1)
(2)为离子晶体(或者离子化合物),而为分子晶体(或者共价化合物)
(3)晶体中带的电荷数大于晶体中的电荷数
(4)
