山东省济南市钢城区2022-2023学年八年级下学期4月期中化学试题(无答案)
文档属性
| 名称 | 山东省济南市钢城区2022-2023学年八年级下学期4月期中化学试题(无答案) |  | |
| 格式 | docx | ||
| 文件大小 | 261.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-28 18:52:05 | ||
图片预览


文档简介
2022-2023学年度下学期期中考试
初三化学试题
分值:100分 时间:60分钟
可能用到的相对原子质量: H-1 C-12 O-16 Ca-40
一、单项选择题(每题2分,共20分,每题只有一个符合题意的选项)
1.用灯帽熄灭酒精灯,该灭火方法的主要原理是( )
A.清除可燃物
B.降低可燃物着火点
C.隔绝空气
D.使可燃物的温度降到着火点以下
2. 炼焦和石油分馏是开发利用化石燃料的两项重要化工工艺,其解释正确的是( )
A.两者都属于物理变化
B.两者都属于化学变化
C.前者属于物理变化,后者属于化学变化
D.前者属于化学变化,后者属于物理变化
3.森林着火时,救火员开辟防火隔离带的目的是( )
A.隔绝空气
B.开辟道路以利于运水灭火
C.隔离可燃物
D.使可燃物温度降低到着火点以下
4.发现火险或遭遇火灾时,做法错误的是( )
A.拨打119火警电话
B.室内电器着火,未切断电源时,用水灭火
C.不能逃生时,应沉着应对,等待救援
D.逃生时用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域
5. 实验室制取二氧化碳有以下几个步骤:①按要求装好仪器 ②向漏斗中加入盐酸 ③向反应器中放入块状石灰石 ④检验装置气密性 ⑤收集生成气体。以上操作正确的排列顺序是( )
A.①③②④⑤ B.②①④③⑤ C.①④③②⑤ D.①②④③⑤
6. 燃着的火柴梗竖直向上,火柴梗不易继续燃烧,其原因是( )
A. 火柴梗的温度达不到着火点
B. 火柴梗的着火点高
C. 火柴梗的着火点低
D. 火柴梗接触的氧气少
7. 常用燃烧法测定有机物的组成。现取3 .2 g某有机物在足量的氧气中充分燃烧,生成 了4. 4 g C02和3.6 g H20,则该有机物中 ( )
A.一定含有C、H、O三种元素
B.只含有C、H两种元素,不含O元素
C.一定含有C、H两种元素,可能含O元素
D.一定含有C、0两种元素,可能含H元素
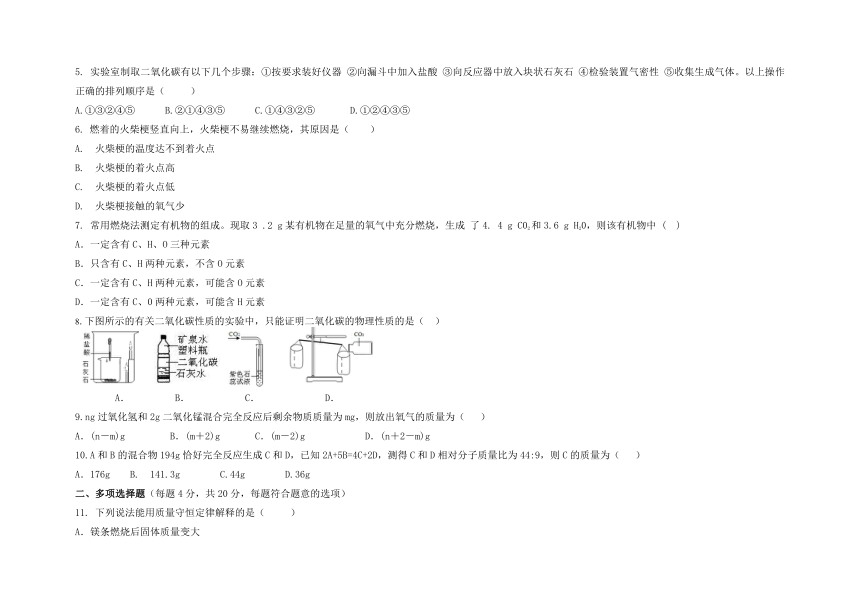
8.下图所示的有关二氧化碳性质的实验中,只能证明二氧化碳的物理性质的是( )
A. B. C. D.
9.ng过氧化氢和2g二氧化锰混合完全反应后剩余物质质量为mg,则放出氧气的质量为( )
A.(n-m)g B.(m+2)g C.(m-2)g D.(n+2-m)g
10.A和B的混合物194g恰好完全反应生成C和D,已知2A+5B=4C+2D,测得C和D相对分子质量比为44:9,则C的质量为( )
A.176g B. 141.3g C.44g D.36g
二、多项选择题(每题4分,共20分,每题符合题意的选项)
11. 下列说法能用质量守恒定律解释的是( )
镁条燃烧后固体质量变大
62g磷和80g的氧反应生成142g五氧化二磷
C.20g食盐溶于80g水得到100g的食盐
D.拧开盛酒精的瓶盖一段时间后质量变小
12.常温常压下在实验室收集NH3(气体),与选择收集方法有关的信息是( )
A.NH3的密度
B.NH3在水中的溶解性
C.空气的密度
D.NH3的质量
13.在一个密闭的容器中放入A、B、C、D四种物质,在一定的条件下发生化学反应,一段时间后,测得有关数据如下:
A B C D
反应前质量(g) 9 2 22 1
反应后质量(g) x 2 6 21
下列说法正确的是( )
A.反应的反应物是AB;生成物是CD
B.表中x=5g
C.由表中数据分析可知,B可能催化剂
D.这一反应类型是化合反应。
14.下列二氧化碳的用途中,正确的是( )
A.供给呼吸 B.用作气体肥料 C.用于灭火 D.生产碳酸饮料
15. 为防止灾后疫情出现,防疫人员用过氧乙酸( C2H4O3 )、次氯酸钠(NaClO)进行消毒。下列说法正确的是( )
A.次氯酸钠中氯元素的化合价为—1
B.次氯酸钠是氧化物
C.过氧乙酸的相对分子质量为76
D.过氧乙酸由碳元素、氢元素和氧元素组成
三、理解与应用
16.在氢气、氧气、一氧化碳、二氧化碳等四种气体中选择适当的物质(用化学式表示)填空:
最清洁的燃料__________;有毒的气体__________;
能灭火的气体__________;能支持燃烧的气体__________。
17.(1)天然气的主要成分是 (填化学式);煤矿的矿井里有时会逸出该气体,若达到一定浓度,遇到明火就会发生爆炸,这就是人们常说的瓦斯爆炸.试写出瓦斯爆炸的化学方程式 .
(2)以纳米级的某种氧化物作催化剂,可使汽车尾气中有毒的一氧化碳和一氧化氮发生反应,生成两种气体,一种是光合作用的原料,另一种是空气中最多的气体.这两种气体是 和 .试写出该反应的化学方程式 。
(3)摩托罗拉公司研发了一种由甲醇为原料的新型手机电池,其容量为锂电池的10倍,可连续使用一个月才充一次电,其电池反应原理为: 2CH3OH + 3X + 4NaOH == 2Na2CO3 + 6H2O其中X的化学式为
(4)写出下列叙述涉及的化学方程式
①氢能源以热值高、零污染、制氢原料丰富而而成为未来最理想的燃料:
②镁燃烧时产生耀眼的白光,军事上可以以制作照明弹:_
③石灰浆粉刷墙壁,室内放炭火盆,墙壁“流汗”
18.白磷、红磷都是可燃物,都可以在一定条件下燃烧。以下是利用它们的可燃性进行的三个实验,请分别回答问题。
实验1 实验2 实验3
通过实验1可以探究燃烧的条件。烧杯中放有热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧。
a与c对比;明燃烧需要的条件是 ,a与b对比,说明燃烧需要的条件是 ,白磷燃烧的化学方程式为 。
(2)通过实验2可以测定 。待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到 的现象时,可达到该实验目的。用铜粉也可以完成这个实验,反应化学方程式为
(3)通过实验3可以验证质量守恒定律。实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡。整个实验过程中气球会出现的现象是 。
综合分析上述三个实验,以下说法正确的是 。(填①~⑥序号)
①实验1中的热水只起隔绝空气的作用
②实验2中红磷可以换成木炭
③实验2若未达到实验目的,可能是由于装置气密性不好
④实验3中的气球起到了平衡瓶内外气体压强的作用
⑤实验3中的气球作用是收集产生的气体
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂
19.请根据下列实验装置图回答有关问题:
(1)请写出图中仪器的名称:①___________,② ___________。
(2)实验室里常用大理石和稀盐酸反应制取二氧化碳,化学方程式是____________,可选用的发生装置和收集装置是_________(选填字母),检验该发生装置气密性的方法是___________。
(3)若用B 作为氧气的发生装置,化学方程式是___________________。
20.下图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的的实验装置
图,试根据题目要求回答下列问题:
(1)装置B的作用是_________,装置C中观察到的现象是______________________,化学方程式__________________ 。
(2)装置D中观察到 ,说明二氧化碳的性质是 ,由此可知,二氧化碳在生活中可用于 。
(3)实验室用装置E来收集二氧化碳时,二氧化碳应从 (填“c端”或“d端”)通入。
四、 计算题
21. 将10g大理石(主要成分是碳酸钙)投入到50g稀盐酸中完全反应,反应后剩余质量57.8g,
求:(1) 生成CO2的质量;
(2) 大理石中碳酸钙的质量分数。
初三化学试题
分值:100分 时间:60分钟
可能用到的相对原子质量: H-1 C-12 O-16 Ca-40
一、单项选择题(每题2分,共20分,每题只有一个符合题意的选项)
1.用灯帽熄灭酒精灯,该灭火方法的主要原理是( )
A.清除可燃物
B.降低可燃物着火点
C.隔绝空气
D.使可燃物的温度降到着火点以下
2. 炼焦和石油分馏是开发利用化石燃料的两项重要化工工艺,其解释正确的是( )
A.两者都属于物理变化
B.两者都属于化学变化
C.前者属于物理变化,后者属于化学变化
D.前者属于化学变化,后者属于物理变化
3.森林着火时,救火员开辟防火隔离带的目的是( )
A.隔绝空气
B.开辟道路以利于运水灭火
C.隔离可燃物
D.使可燃物温度降低到着火点以下
4.发现火险或遭遇火灾时,做法错误的是( )
A.拨打119火警电话
B.室内电器着火,未切断电源时,用水灭火
C.不能逃生时,应沉着应对,等待救援
D.逃生时用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域
5. 实验室制取二氧化碳有以下几个步骤:①按要求装好仪器 ②向漏斗中加入盐酸 ③向反应器中放入块状石灰石 ④检验装置气密性 ⑤收集生成气体。以上操作正确的排列顺序是( )
A.①③②④⑤ B.②①④③⑤ C.①④③②⑤ D.①②④③⑤
6. 燃着的火柴梗竖直向上,火柴梗不易继续燃烧,其原因是( )
A. 火柴梗的温度达不到着火点
B. 火柴梗的着火点高
C. 火柴梗的着火点低
D. 火柴梗接触的氧气少
7. 常用燃烧法测定有机物的组成。现取3 .2 g某有机物在足量的氧气中充分燃烧,生成 了4. 4 g C02和3.6 g H20,则该有机物中 ( )
A.一定含有C、H、O三种元素
B.只含有C、H两种元素,不含O元素
C.一定含有C、H两种元素,可能含O元素
D.一定含有C、0两种元素,可能含H元素
8.下图所示的有关二氧化碳性质的实验中,只能证明二氧化碳的物理性质的是( )
A. B. C. D.
9.ng过氧化氢和2g二氧化锰混合完全反应后剩余物质质量为mg,则放出氧气的质量为( )
A.(n-m)g B.(m+2)g C.(m-2)g D.(n+2-m)g
10.A和B的混合物194g恰好完全反应生成C和D,已知2A+5B=4C+2D,测得C和D相对分子质量比为44:9,则C的质量为( )
A.176g B. 141.3g C.44g D.36g
二、多项选择题(每题4分,共20分,每题符合题意的选项)
11. 下列说法能用质量守恒定律解释的是( )
镁条燃烧后固体质量变大
62g磷和80g的氧反应生成142g五氧化二磷
C.20g食盐溶于80g水得到100g的食盐
D.拧开盛酒精的瓶盖一段时间后质量变小
12.常温常压下在实验室收集NH3(气体),与选择收集方法有关的信息是( )
A.NH3的密度
B.NH3在水中的溶解性
C.空气的密度
D.NH3的质量
13.在一个密闭的容器中放入A、B、C、D四种物质,在一定的条件下发生化学反应,一段时间后,测得有关数据如下:
A B C D
反应前质量(g) 9 2 22 1
反应后质量(g) x 2 6 21
下列说法正确的是( )
A.反应的反应物是AB;生成物是CD
B.表中x=5g
C.由表中数据分析可知,B可能催化剂
D.这一反应类型是化合反应。
14.下列二氧化碳的用途中,正确的是( )
A.供给呼吸 B.用作气体肥料 C.用于灭火 D.生产碳酸饮料
15. 为防止灾后疫情出现,防疫人员用过氧乙酸( C2H4O3 )、次氯酸钠(NaClO)进行消毒。下列说法正确的是( )
A.次氯酸钠中氯元素的化合价为—1
B.次氯酸钠是氧化物
C.过氧乙酸的相对分子质量为76
D.过氧乙酸由碳元素、氢元素和氧元素组成
三、理解与应用
16.在氢气、氧气、一氧化碳、二氧化碳等四种气体中选择适当的物质(用化学式表示)填空:
最清洁的燃料__________;有毒的气体__________;
能灭火的气体__________;能支持燃烧的气体__________。
17.(1)天然气的主要成分是 (填化学式);煤矿的矿井里有时会逸出该气体,若达到一定浓度,遇到明火就会发生爆炸,这就是人们常说的瓦斯爆炸.试写出瓦斯爆炸的化学方程式 .
(2)以纳米级的某种氧化物作催化剂,可使汽车尾气中有毒的一氧化碳和一氧化氮发生反应,生成两种气体,一种是光合作用的原料,另一种是空气中最多的气体.这两种气体是 和 .试写出该反应的化学方程式 。
(3)摩托罗拉公司研发了一种由甲醇为原料的新型手机电池,其容量为锂电池的10倍,可连续使用一个月才充一次电,其电池反应原理为: 2CH3OH + 3X + 4NaOH == 2Na2CO3 + 6H2O其中X的化学式为
(4)写出下列叙述涉及的化学方程式
①氢能源以热值高、零污染、制氢原料丰富而而成为未来最理想的燃料:
②镁燃烧时产生耀眼的白光,军事上可以以制作照明弹:_
③石灰浆粉刷墙壁,室内放炭火盆,墙壁“流汗”
18.白磷、红磷都是可燃物,都可以在一定条件下燃烧。以下是利用它们的可燃性进行的三个实验,请分别回答问题。
实验1 实验2 实验3
通过实验1可以探究燃烧的条件。烧杯中放有热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧。
a与c对比;明燃烧需要的条件是 ,a与b对比,说明燃烧需要的条件是 ,白磷燃烧的化学方程式为 。
(2)通过实验2可以测定 。待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到 的现象时,可达到该实验目的。用铜粉也可以完成这个实验,反应化学方程式为
(3)通过实验3可以验证质量守恒定律。实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡。整个实验过程中气球会出现的现象是 。
综合分析上述三个实验,以下说法正确的是 。(填①~⑥序号)
①实验1中的热水只起隔绝空气的作用
②实验2中红磷可以换成木炭
③实验2若未达到实验目的,可能是由于装置气密性不好
④实验3中的气球起到了平衡瓶内外气体压强的作用
⑤实验3中的气球作用是收集产生的气体
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂
19.请根据下列实验装置图回答有关问题:
(1)请写出图中仪器的名称:①___________,② ___________。
(2)实验室里常用大理石和稀盐酸反应制取二氧化碳,化学方程式是____________,可选用的发生装置和收集装置是_________(选填字母),检验该发生装置气密性的方法是___________。
(3)若用B 作为氧气的发生装置,化学方程式是___________________。
20.下图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的的实验装置
图,试根据题目要求回答下列问题:
(1)装置B的作用是_________,装置C中观察到的现象是______________________,化学方程式__________________ 。
(2)装置D中观察到 ,说明二氧化碳的性质是 ,由此可知,二氧化碳在生活中可用于 。
(3)实验室用装置E来收集二氧化碳时,二氧化碳应从 (填“c端”或“d端”)通入。
四、 计算题
21. 将10g大理石(主要成分是碳酸钙)投入到50g稀盐酸中完全反应,反应后剩余质量57.8g,
求:(1) 生成CO2的质量;
(2) 大理石中碳酸钙的质量分数。
同课章节目录
