第3章 有机合成及其应用 合成高分子化合物 检测题 2022-2023学年高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第3章 有机合成及其应用 合成高分子化合物 检测题 2022-2023学年高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 607.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-03 00:00:00 | ||
图片预览




文档简介
第三章《有机合成及其应用 合成高分子化合物》检测题
一、单选题(共13题)
1.葡酚酮是由葡萄籽提取的一种花青素类衍生物(结构简式如图),具有良好的抗氧化活性。下列关于葡酚酮叙述错误的是
A.可形成分子内氢键 B.有4种含氧官能团
C.可使酸性高锰酸钾溶液褪色 D.不与Na2CO3水溶液发生反应
2.下列说法中正确的是
A.糖类、油脂、蛋白质都属于天然高分子化合物
B.涤纶、锦纶、蚕丝都属于合成纤维
C.聚乙烯、聚氯乙烯都不能使溴水褪色
D.麦芽糖和蔗糖互为同分异构体,水解的产物均为葡萄糖
3.下列实验能获得成功的是
A.用水鉴别乙醇、苯、四氯化碳
B.向卤代烃的水解产物中加硝酸银溶液,检验卤代烃中含有的卤族元素种类
C.光照条件下,用氯气和甲烷发生取代反应制取纯净的一氯甲烷
D.通入酸性KMnO4溶液除甲烷中的乙烯
4.下列说法中错误的是
A.红外光谱仪、核磁共振仪都可用于有机物的结构分析
B.中含有的4种官能团
C.1mol最多能和4molH2发生加成反应
D.2,5—二甲基己烷的核磁共振氢谱中出现了三个峰
5.下列叙述正确的是
A.标准状况下,11.2L二氯甲烷所含的分子数为0.5NA
B.用酸性高锰酸钾溶液、浓溴水鉴别己烯、苯、甲苯、苯酚溶液
C.除去苯中少量的苯酚:加足量浓溴水,过滤
D.相同物质的量的乙烯、乙醇、乙酸乙酯完全燃烧时消耗的氧气的物质的量相同
6.可用于鉴别以下两种化合物的一组试剂是
A.苯 B.溴的四氯化碳溶液 C.氯化铁溶液 D.氢氧化钠溶液
7.当两种有机物总质量一定时,以任意比例混合后,充分燃烧,所得的CO2和H2O的物质的量总是相等的是
A.乙醇、乙醚 B.乙烯、丁烯 C.苯、苯酚 D.甲烷、甲醇
8.某有机物A的结构简式如图,关于它的性质描述正确的是
①能发生加成反应②能溶解于NaOH溶液中,且1molA最多能消耗3molNaOH③能水解生成两种酸④不能使溴水褪色⑤能发生酯化反应⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
9.莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是
A.两种酸都能与溴水反应
B.两种酸遇三氯化铁溶液都显色
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量金属钠反应产生氢气的量不同
10.化合物M(结构式如图)是结构的重要组成部分,其中元素Y、Z、W在同一周期,X与其他元素不在同一周期,且原子半径最小。W的一种核素常用于测定文物年代。下列说法正确的是
A.原子半径:
B.最高价氧化物对应水化物的酸性:
C.M是共价化合物,分子中每个原子都满足8电子稳定结构
D.X与Y形成的化合物的沸点一定高于X与W形成的化合物的沸点
11.下列根据实验操作和现象所得出的结论正确的是
选项 操作 现象 结论
A 取涂改液与KOH溶液混合加热充分反应,取上层清液,加入稀硝酸酸化,加入硝酸银溶液 出现白色沉淀 说明涂改液中存在含氯有机化合物
B 将乙醇与浓混合加热,将产生的气体通入酸性溶液中 溶液紫红色褪去 产生的气体中一定含有乙烯
C 向3mL苯酚溶液中滴加2滴浓溴水,振荡 无白色沉淀 苯酚与溴水尚未发生反应
D 向油脂皂化反应后的溶液中滴入酚酞 溶液变红 油脂已经完全皂化
A.A B.B C.C D.D
12.透骨草又名药曲草,蝇毒草等。其中一种抗氧化性活性成分结构如图。下列说法正确的是
A.在一定条件下能发生氧化反应、取代反应、加成反应和消去反应
B.苯环上的一溴代物共5种
C.1mol该化合物最多与4molNaOH反应
D.该分子中最多有7个碳原子共面
13.下列说法不正确的是
A.乙酸与葡萄糖最简式相同,等物质的量的二者燃烧时耗氧量相同
B.的系统命名为2,3,6-三甲基庚烷
C.CH3CH=CHCl存在顺反异构
D.李比希法与质谱法结合可确定有机物的分子式
二、非选择题(共10题)
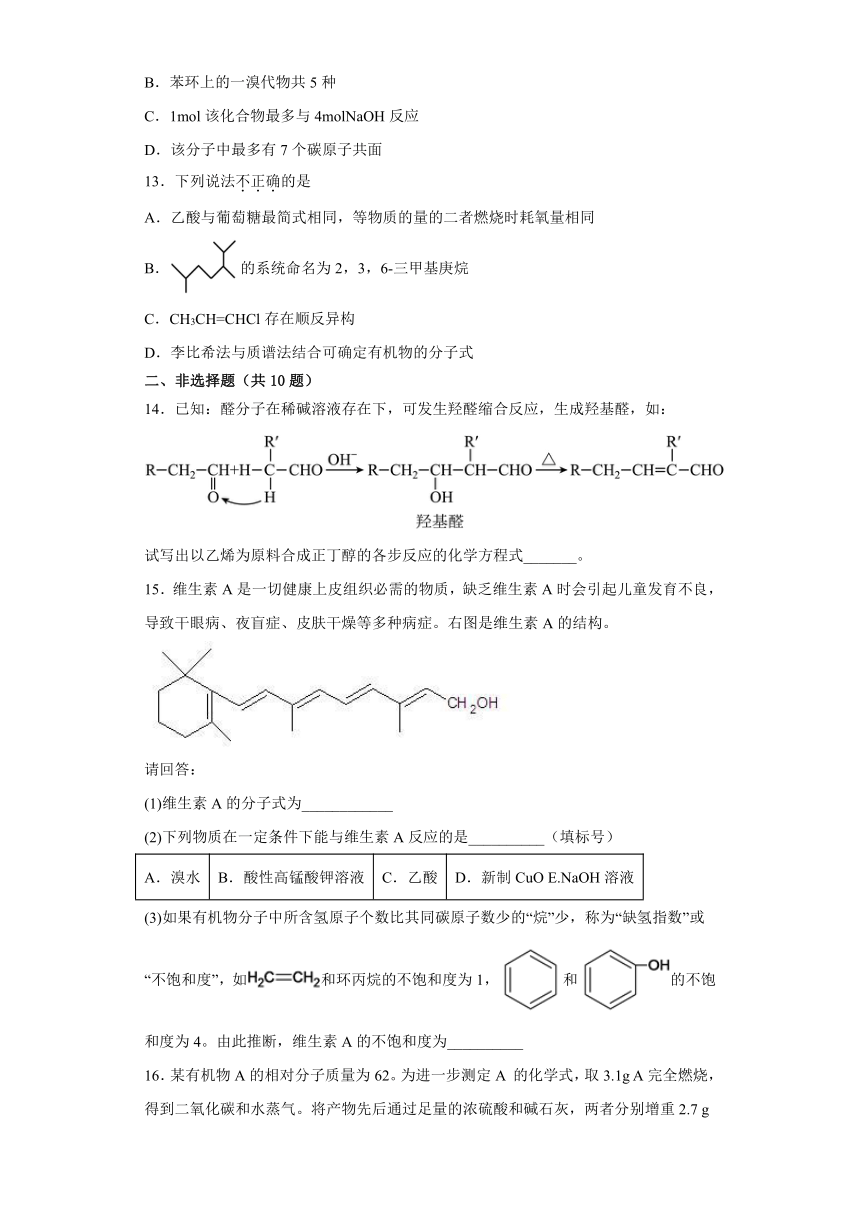
14.已知:醛分子在稀碱溶液存在下,可发生羟醛缩合反应,生成羟基醛,如:
试写出以乙烯为原料合成正丁醇的各步反应的化学方程式_______。
15.维生素A是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致干眼病、夜盲症、皮肤干燥等多种病症。右图是维生素A的结构。
请回答:
(1)维生素A的分子式为____________
(2)下列物质在一定条件下能与维生素A反应的是__________(填标号)
A.溴水 B.酸性高锰酸钾溶液 C.乙酸 D.新制CuO E.NaOH溶液
(3)如果有机物分子中所含氢原子个数比其同碳原子数少的“烷”少,称为“缺氢指数”或“不饱和度”,如和环丙烷的不饱和度为1,和的不饱和度为4。由此推断,维生素A的不饱和度为__________
16.某有机物A的相对分子质量为62。为进一步测定A 的化学式,取3.1g A完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重2.7 g和4.4 g(假设每步反应完全)。
(1)该有机物的实验式是__________________;分子式是________________。
(2)红外光谱显示有“C—C”键和“O—H”键的振动吸收,若核磁共振氢谱只有2个吸收峰且峰面积之比为1∶2,推断该有机物的结构简式是__________________。
(3)该有机物与金属钠反应的化学方程式是____________________。
17.标准状况下1.12L的烃A,完全燃烧后,若将产物通入足量的澄清石灰水中,可得到白色沉淀20.0g;若用足量的五氧化二磷吸收,增重3.6g。
(1)烃A的分子式为_______。
(2)A的同分异构体(不含空间异构)有______种,若A的核磁共振氢谱有两个吸收峰且峰面积之比为2∶6,则A的结构简式为______。
(3)0.1molA与一定量的氧气完全反应,将反应后的气体通入足量的碱石灰中,气体体积减少一半,剩余气体通入炽热的氧化铜后可以被100mL 3mol/LNaOH溶液全部吸收,则该溶液的溶质为_______(填化学式)。
18.已知下列三个反应的热化学反应方程式:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+58 kJ/mol;②2CH3OH(g)+O2(g)=2CO2(g)+4H2(g) △H2;③2H2O(g)=2H2(g)+O2(g) △H3=+483.6kJ/mol
(1)反应②的△H2=__________kJ/mol。
(2)已知反应① 中的相关的化学键键能数据如下表所示:
化学键 C-H C-O H-O C=O H-H
键能(kJ/mol) 413 343 465 X 436
表中X=__________。
(3)CH3OH(g)、H2O(g)、O2(g)的混合气在绝热条件下经①②恰好完全反应,体系温度反应前后不发生变化,将生成的气体通过足量Na2O2 固体,过氧化钠增重56g,则原混合气体中CH3OH(g) 、H2O(g)、O2(g)对应的物质的量为__________、__________、__________。
19.通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图所示的是用燃烧法确定有机物分子式的常用装置。
现准确称取样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重,B管增重。请回答:
(1)根据气流方向将装置进行连接,其接口连接顺序为:___________(每套装置最多只能用一次)。
(2)B管的作用是___________。
(3)E中应盛装的试剂是___________。
(4)该有机物的最简式为___________。
(5)如果把网去掉,A管增重将___________(填“增大”“减小”或“不变”)。
(6)要确定该有机物的分子式,还必须知道的数据是___________(填序号)。
A.消耗液体E的质量 B.样品的摩尔质量 C.固体减小的质量
D.C装置增加的质量 E.燃烧消耗的物质的量
(7)在整个实验开始之前,需先让D装置产生的气体通过整套装置一段时间,其目的是___________。
(8)有人认为该装置还有缺陷,请补充完整___________。
20.化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。
回答下列问题:
(1)A装置中分液漏斗盛放的物质是___________,写出有关反应的化学方程式___________。
(2)C装置(燃烧管)中CuO的作用是___________。
(3)写出E装置中所盛放试剂的名称___________,它的作用是___________。
(4)若准确称取2.40g样品(只含C、H、O三种元素中的两种或三种)。经充分燃烧后,E管质量增加3.52g,D管质量增加1.44g,则该有机物的最简式为___________。
(5)要确定该有机物的化学式,还需要测定___________。
21.I、 X、Y、Z三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物。已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多1个电子层。试回答:
(1)X在周期表中的位置___________,Z2Y2的电子式_________,含有的化学键____________。
(2)Z2Y2溶在水中的反应方程式为__________________________。
(3)用电子式表示Z2X的形成过程_________________________。
II、以乙烯为原料可以合成很多的化工产品,已知有机物D是一种有水果香味的油状液体。试根据下图回答有关问题:
(4)反应①②的反应类型分别是__________、__________。
(5)决定有机物A、C的化学特性的原子团的名称分别是_____________。
(6)写出图示反应②、③的化学方程式:
②_________________________________________;
③__________________________________________。
22.化合物F是一种重要的有机合成中间体,它的合成路线如图:
(1)化合物F中含氧官能团的名称是______和______,由A生成B的化学反应类型是______;
(2)写出化合物B的结构简式:______;
(3)写出化合物C与乙酸反应生成酯的化学方程式:______;
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:______(任写一种);
23.从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;B是一种比水轻的油状液态烃,0.1mol该烃在足量的氧气中完全燃烧,生成0.6molCO2和0.3mol水。回答下列问题:
(1)A 的电子式为_____,B 的结构简式为______。
(2)与A 相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:____,反应类型:____。
(3)在碘水中加入B物质,充分振荡、静置后的现象:_________。
(4)B与浓硫酸和浓硝酸在55~60℃条件下反应的化学方程式:_______,反应类型:______。
(5)等质量的A、B完全燃烧时消耗O2的物质的量:_______(填“A>B”“A参考答案:
1.D 2.C 3.A 4.B 5.B 6.C 7.B 8.D 9.A 10.B 11.A 12.B 13.A
14.(1)
(2)
(3)
(4)
(5)
15.(1)
(2)ABCD
(3)6
16. CH3O C2H6O2 CH2OHCH2OH CH2OHCH2OH+2NaCH2ONaCH2ONa+H2
17. C4H8 5 CH2=C(CH3)2 、CH3CH=CHCH3 Na2CO3、NaHCO3
18. -367.6 805.5 2mol 1.52mol 0.24mol
19.(1)g接f,e接h,i接c或(d),d或(c)接a或(b)
(2)吸收生成的水蒸气
(3)H2O2
(4)CHO2
(5)减小
(6)B
(7)赶出装置内空气,减小实验误差
(8)在A后再连接1个A装置
20.(1) H2O2(或H2O) 2H2O22H2O+O2↑(或2Na2O2+2H2O=4NaOH+O2↑)
(2)使有机物充分氧化生成CO2和H2O
(3) 碱石灰或氢氧化钠 吸收CO2
(4)CH2O
(5)有机物的相对分子质量
21. 第三周期第VIA族 离子键和非极性共价键 2Na2O2+2H2O=4NaOH+O2↑ 加成反应 酯化反应 羟基、 羧基 n CH2=CH2
22. 醛基 羰基 取代反应 CH3COOH+ + H2O
23. CH2=CHCH3+Br2→CH2BrCHBrCH3 加成反应 溶液分层,下层无色,上层呈紫红色 +HO-NO2(浓)+H2O 取代反应 A>B
一、单选题(共13题)
1.葡酚酮是由葡萄籽提取的一种花青素类衍生物(结构简式如图),具有良好的抗氧化活性。下列关于葡酚酮叙述错误的是
A.可形成分子内氢键 B.有4种含氧官能团
C.可使酸性高锰酸钾溶液褪色 D.不与Na2CO3水溶液发生反应
2.下列说法中正确的是
A.糖类、油脂、蛋白质都属于天然高分子化合物
B.涤纶、锦纶、蚕丝都属于合成纤维
C.聚乙烯、聚氯乙烯都不能使溴水褪色
D.麦芽糖和蔗糖互为同分异构体,水解的产物均为葡萄糖
3.下列实验能获得成功的是
A.用水鉴别乙醇、苯、四氯化碳
B.向卤代烃的水解产物中加硝酸银溶液,检验卤代烃中含有的卤族元素种类
C.光照条件下,用氯气和甲烷发生取代反应制取纯净的一氯甲烷
D.通入酸性KMnO4溶液除甲烷中的乙烯
4.下列说法中错误的是
A.红外光谱仪、核磁共振仪都可用于有机物的结构分析
B.中含有的4种官能团
C.1mol最多能和4molH2发生加成反应
D.2,5—二甲基己烷的核磁共振氢谱中出现了三个峰
5.下列叙述正确的是
A.标准状况下,11.2L二氯甲烷所含的分子数为0.5NA
B.用酸性高锰酸钾溶液、浓溴水鉴别己烯、苯、甲苯、苯酚溶液
C.除去苯中少量的苯酚:加足量浓溴水,过滤
D.相同物质的量的乙烯、乙醇、乙酸乙酯完全燃烧时消耗的氧气的物质的量相同
6.可用于鉴别以下两种化合物的一组试剂是
A.苯 B.溴的四氯化碳溶液 C.氯化铁溶液 D.氢氧化钠溶液
7.当两种有机物总质量一定时,以任意比例混合后,充分燃烧,所得的CO2和H2O的物质的量总是相等的是
A.乙醇、乙醚 B.乙烯、丁烯 C.苯、苯酚 D.甲烷、甲醇
8.某有机物A的结构简式如图,关于它的性质描述正确的是
①能发生加成反应②能溶解于NaOH溶液中,且1molA最多能消耗3molNaOH③能水解生成两种酸④不能使溴水褪色⑤能发生酯化反应⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
9.莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是
A.两种酸都能与溴水反应
B.两种酸遇三氯化铁溶液都显色
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量金属钠反应产生氢气的量不同
10.化合物M(结构式如图)是结构的重要组成部分,其中元素Y、Z、W在同一周期,X与其他元素不在同一周期,且原子半径最小。W的一种核素常用于测定文物年代。下列说法正确的是
A.原子半径:
B.最高价氧化物对应水化物的酸性:
C.M是共价化合物,分子中每个原子都满足8电子稳定结构
D.X与Y形成的化合物的沸点一定高于X与W形成的化合物的沸点
11.下列根据实验操作和现象所得出的结论正确的是
选项 操作 现象 结论
A 取涂改液与KOH溶液混合加热充分反应,取上层清液,加入稀硝酸酸化,加入硝酸银溶液 出现白色沉淀 说明涂改液中存在含氯有机化合物
B 将乙醇与浓混合加热,将产生的气体通入酸性溶液中 溶液紫红色褪去 产生的气体中一定含有乙烯
C 向3mL苯酚溶液中滴加2滴浓溴水,振荡 无白色沉淀 苯酚与溴水尚未发生反应
D 向油脂皂化反应后的溶液中滴入酚酞 溶液变红 油脂已经完全皂化
A.A B.B C.C D.D
12.透骨草又名药曲草,蝇毒草等。其中一种抗氧化性活性成分结构如图。下列说法正确的是
A.在一定条件下能发生氧化反应、取代反应、加成反应和消去反应
B.苯环上的一溴代物共5种
C.1mol该化合物最多与4molNaOH反应
D.该分子中最多有7个碳原子共面
13.下列说法不正确的是
A.乙酸与葡萄糖最简式相同,等物质的量的二者燃烧时耗氧量相同
B.的系统命名为2,3,6-三甲基庚烷
C.CH3CH=CHCl存在顺反异构
D.李比希法与质谱法结合可确定有机物的分子式
二、非选择题(共10题)
14.已知:醛分子在稀碱溶液存在下,可发生羟醛缩合反应,生成羟基醛,如:
试写出以乙烯为原料合成正丁醇的各步反应的化学方程式_______。
15.维生素A是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致干眼病、夜盲症、皮肤干燥等多种病症。右图是维生素A的结构。
请回答:
(1)维生素A的分子式为____________
(2)下列物质在一定条件下能与维生素A反应的是__________(填标号)
A.溴水 B.酸性高锰酸钾溶液 C.乙酸 D.新制CuO E.NaOH溶液
(3)如果有机物分子中所含氢原子个数比其同碳原子数少的“烷”少,称为“缺氢指数”或“不饱和度”,如和环丙烷的不饱和度为1,和的不饱和度为4。由此推断,维生素A的不饱和度为__________
16.某有机物A的相对分子质量为62。为进一步测定A 的化学式,取3.1g A完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重2.7 g和4.4 g(假设每步反应完全)。
(1)该有机物的实验式是__________________;分子式是________________。
(2)红外光谱显示有“C—C”键和“O—H”键的振动吸收,若核磁共振氢谱只有2个吸收峰且峰面积之比为1∶2,推断该有机物的结构简式是__________________。
(3)该有机物与金属钠反应的化学方程式是____________________。
17.标准状况下1.12L的烃A,完全燃烧后,若将产物通入足量的澄清石灰水中,可得到白色沉淀20.0g;若用足量的五氧化二磷吸收,增重3.6g。
(1)烃A的分子式为_______。
(2)A的同分异构体(不含空间异构)有______种,若A的核磁共振氢谱有两个吸收峰且峰面积之比为2∶6,则A的结构简式为______。
(3)0.1molA与一定量的氧气完全反应,将反应后的气体通入足量的碱石灰中,气体体积减少一半,剩余气体通入炽热的氧化铜后可以被100mL 3mol/LNaOH溶液全部吸收,则该溶液的溶质为_______(填化学式)。
18.已知下列三个反应的热化学反应方程式:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+58 kJ/mol;②2CH3OH(g)+O2(g)=2CO2(g)+4H2(g) △H2;③2H2O(g)=2H2(g)+O2(g) △H3=+483.6kJ/mol
(1)反应②的△H2=__________kJ/mol。
(2)已知反应① 中的相关的化学键键能数据如下表所示:
化学键 C-H C-O H-O C=O H-H
键能(kJ/mol) 413 343 465 X 436
表中X=__________。
(3)CH3OH(g)、H2O(g)、O2(g)的混合气在绝热条件下经①②恰好完全反应,体系温度反应前后不发生变化,将生成的气体通过足量Na2O2 固体,过氧化钠增重56g,则原混合气体中CH3OH(g) 、H2O(g)、O2(g)对应的物质的量为__________、__________、__________。
19.通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图所示的是用燃烧法确定有机物分子式的常用装置。
现准确称取样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重,B管增重。请回答:
(1)根据气流方向将装置进行连接,其接口连接顺序为:___________(每套装置最多只能用一次)。
(2)B管的作用是___________。
(3)E中应盛装的试剂是___________。
(4)该有机物的最简式为___________。
(5)如果把网去掉,A管增重将___________(填“增大”“减小”或“不变”)。
(6)要确定该有机物的分子式,还必须知道的数据是___________(填序号)。
A.消耗液体E的质量 B.样品的摩尔质量 C.固体减小的质量
D.C装置增加的质量 E.燃烧消耗的物质的量
(7)在整个实验开始之前,需先让D装置产生的气体通过整套装置一段时间,其目的是___________。
(8)有人认为该装置还有缺陷,请补充完整___________。
20.化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。
回答下列问题:
(1)A装置中分液漏斗盛放的物质是___________,写出有关反应的化学方程式___________。
(2)C装置(燃烧管)中CuO的作用是___________。
(3)写出E装置中所盛放试剂的名称___________,它的作用是___________。
(4)若准确称取2.40g样品(只含C、H、O三种元素中的两种或三种)。经充分燃烧后,E管质量增加3.52g,D管质量增加1.44g,则该有机物的最简式为___________。
(5)要确定该有机物的化学式,还需要测定___________。
21.I、 X、Y、Z三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物。已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多1个电子层。试回答:
(1)X在周期表中的位置___________,Z2Y2的电子式_________,含有的化学键____________。
(2)Z2Y2溶在水中的反应方程式为__________________________。
(3)用电子式表示Z2X的形成过程_________________________。
II、以乙烯为原料可以合成很多的化工产品,已知有机物D是一种有水果香味的油状液体。试根据下图回答有关问题:
(4)反应①②的反应类型分别是__________、__________。
(5)决定有机物A、C的化学特性的原子团的名称分别是_____________。
(6)写出图示反应②、③的化学方程式:
②_________________________________________;
③__________________________________________。
22.化合物F是一种重要的有机合成中间体,它的合成路线如图:
(1)化合物F中含氧官能团的名称是______和______,由A生成B的化学反应类型是______;
(2)写出化合物B的结构简式:______;
(3)写出化合物C与乙酸反应生成酯的化学方程式:______;
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:______(任写一种);
23.从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;B是一种比水轻的油状液态烃,0.1mol该烃在足量的氧气中完全燃烧,生成0.6molCO2和0.3mol水。回答下列问题:
(1)A 的电子式为_____,B 的结构简式为______。
(2)与A 相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:____,反应类型:____。
(3)在碘水中加入B物质,充分振荡、静置后的现象:_________。
(4)B与浓硫酸和浓硝酸在55~60℃条件下反应的化学方程式:_______,反应类型:______。
(5)等质量的A、B完全燃烧时消耗O2的物质的量:_______(填“A>B”“A
1.D 2.C 3.A 4.B 5.B 6.C 7.B 8.D 9.A 10.B 11.A 12.B 13.A
14.(1)
(2)
(3)
(4)
(5)
15.(1)
(2)ABCD
(3)6
16. CH3O C2H6O2 CH2OHCH2OH CH2OHCH2OH+2NaCH2ONaCH2ONa+H2
17. C4H8 5 CH2=C(CH3)2 、CH3CH=CHCH3 Na2CO3、NaHCO3
18. -367.6 805.5 2mol 1.52mol 0.24mol
19.(1)g接f,e接h,i接c或(d),d或(c)接a或(b)
(2)吸收生成的水蒸气
(3)H2O2
(4)CHO2
(5)减小
(6)B
(7)赶出装置内空气,减小实验误差
(8)在A后再连接1个A装置
20.(1) H2O2(或H2O) 2H2O22H2O+O2↑(或2Na2O2+2H2O=4NaOH+O2↑)
(2)使有机物充分氧化生成CO2和H2O
(3) 碱石灰或氢氧化钠 吸收CO2
(4)CH2O
(5)有机物的相对分子质量
21. 第三周期第VIA族 离子键和非极性共价键 2Na2O2+2H2O=4NaOH+O2↑ 加成反应 酯化反应 羟基、 羧基 n CH2=CH2
22. 醛基 羰基 取代反应 CH3COOH+ + H2O
23. CH2=CHCH3+Br2→CH2BrCHBrCH3 加成反应 溶液分层,下层无色,上层呈紫红色 +HO-NO2(浓)+H2O 取代反应 A>B
