2.1.3 脂肪烃综合含解析
文档属性
| 名称 | 2.1.3 脂肪烃综合含解析 |
|
|
| 格式 | docx | ||
| 文件大小 | 732.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-03 00:00:00 | ||
图片预览


文档简介
第 4 讲 脂肪烃综合
模块 1 乙炔的制备及性质实验
一、乙炔的实验室制取
1 实验原理:
CaC 2 +2H 2 O → C 2 H 2 ↑ +Ca(OH) 2
2 实验药品: 电石 (主要成分为 CaC 2 )、饱和氯化钠溶液。
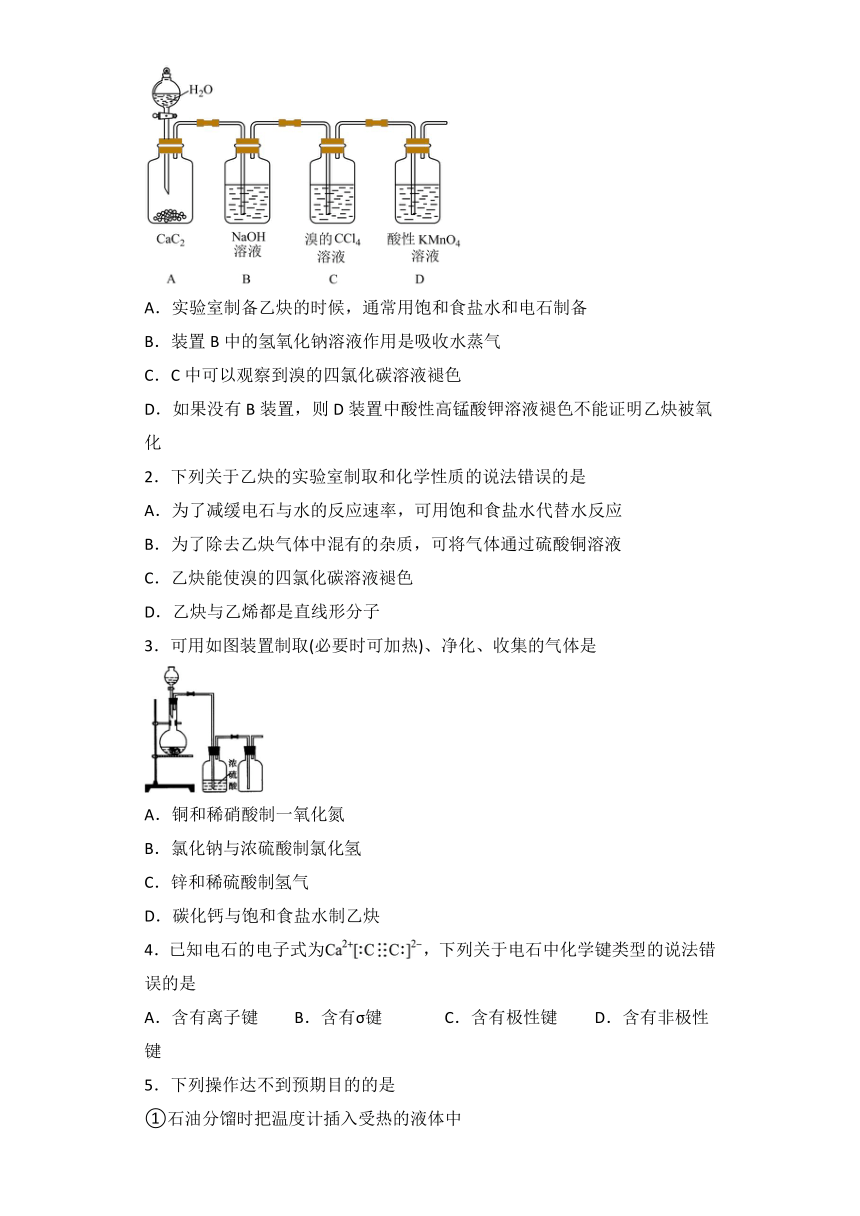
3 实验装置
通过实验可以得到平稳的乙炔气流,观察到硫酸铜溶液中有黑色沉淀产生,同时红棕色溴水褪色。
小结
(1) 实验中用饱和的食盐水代替水—减缓乙炔气流速度,降低反应速率;
(2) 在实验装置中要使用分液漏斗—控制流量,减缓反应速率;
(3) 制取出的乙炔有刺激性气味—产生 H 2 S,PH 3 等杂质气体,用CuSO 4 溶液除去。
知识精炼
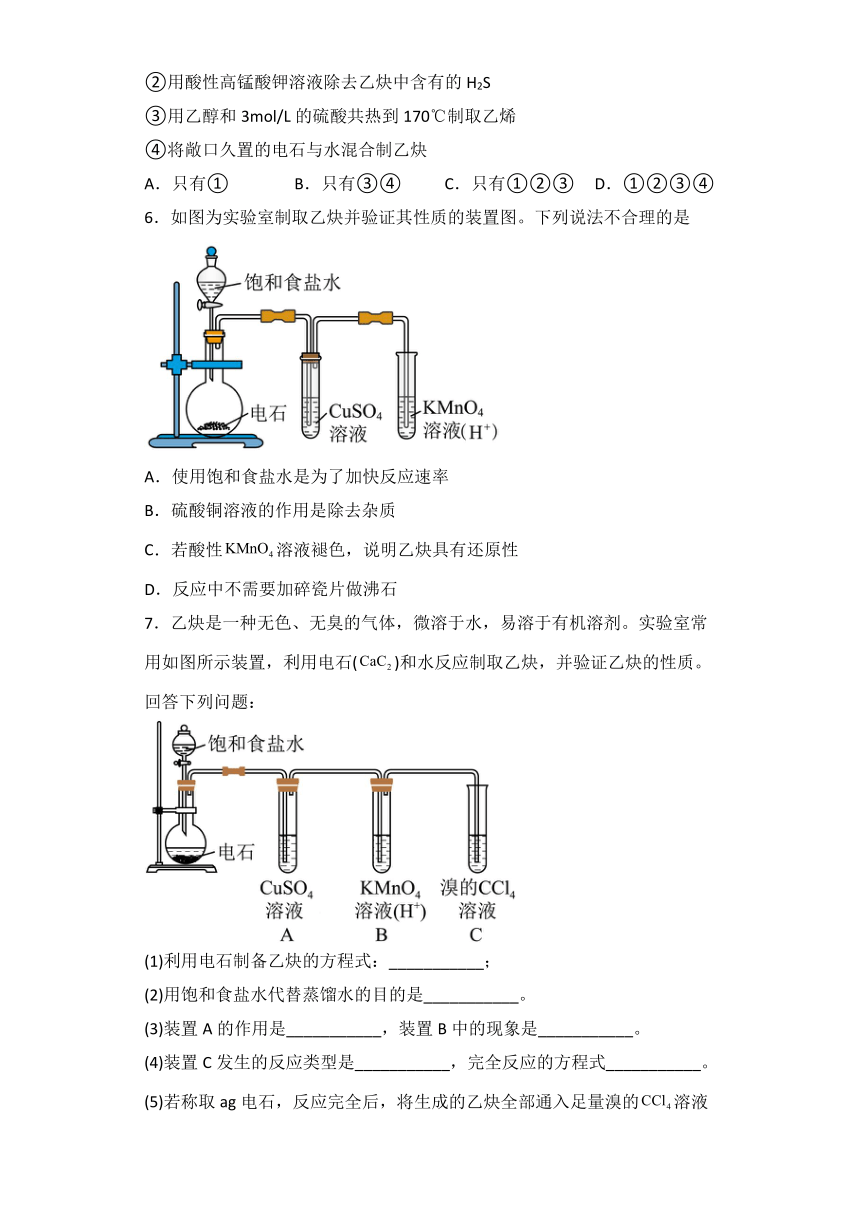
1.实验室用如图所示装置制备乙炔,并验证乙炔的某些化学性质,下列说法不正确的是
A.实验室制备乙炔的时候,通常用饱和食盐水和电石制备
B.装置B中的氢氧化钠溶液作用是吸收水蒸气
C.C中可以观察到溴的四氯化碳溶液褪色
D.如果没有B装置,则D装置中酸性高锰酸钾溶液褪色不能证明乙炔被氧化
2.下列关于乙炔的实验室制取和化学性质的说法错误的是
A.为了减缓电石与水的反应速率,可用饱和食盐水代替水反应
B.为了除去乙炔气体中混有的杂质,可将气体通过硫酸铜溶液
C.乙炔能使溴的四氯化碳溶液褪色
D.乙炔与乙烯都是直线形分子
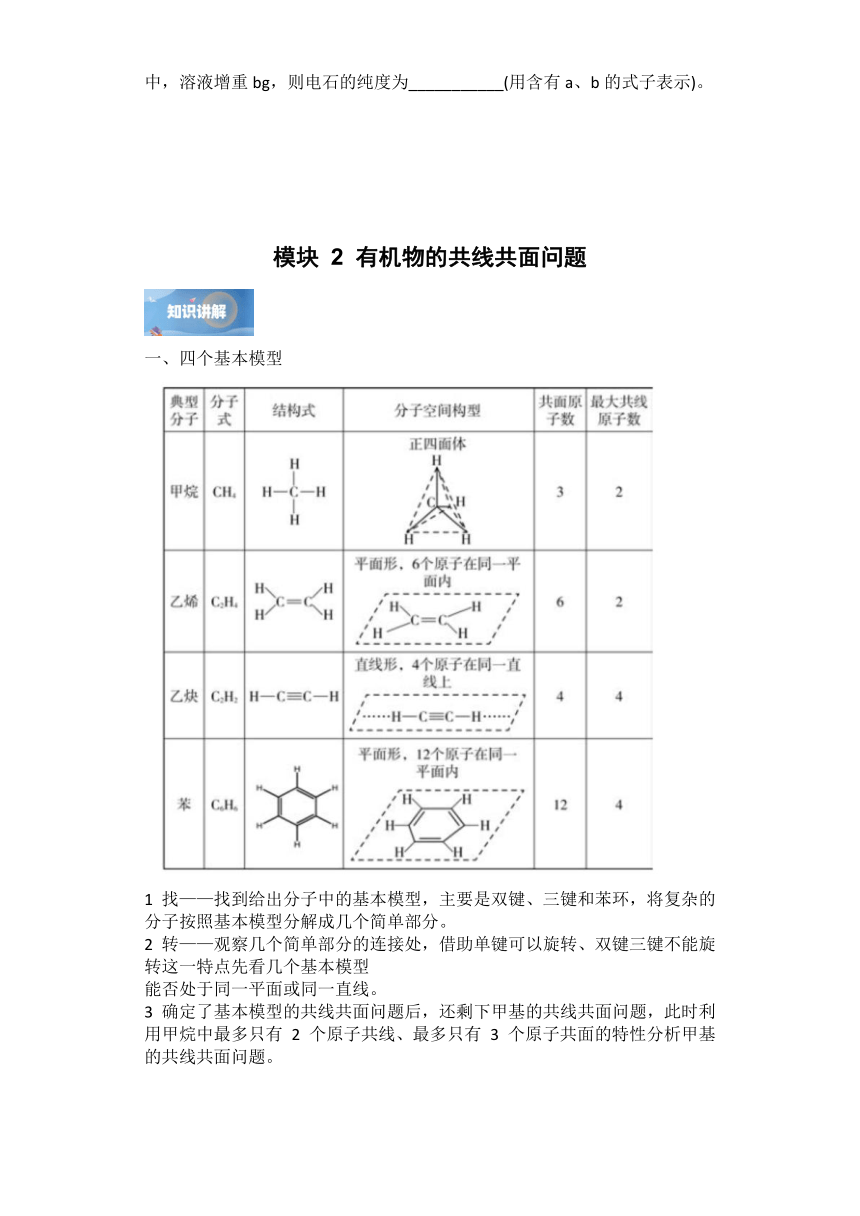
3.可用如图装置制取(必要时可加热)、净化、收集的气体是
A.铜和稀硝酸制一氧化氮
B.氯化钠与浓硫酸制氯化氢
C.锌和稀硫酸制氢气
D.碳化钙与饱和食盐水制乙炔
4.已知电石的电子式为,下列关于电石中化学键类型的说法错误的是
A.含有离子键 B.含有σ键 C.含有极性键 D.含有非极性键
5.下列操作达不到预期目的的是
①石油分馏时把温度计插入受热的液体中
②用酸性高锰酸钾溶液除去乙炔中含有的H2S
③用乙醇和3mol/L的硫酸共热到170℃制取乙烯
④将敞口久置的电石与水混合制乙炔
A.只有① B.只有③④ C.只有①②③ D.①②③④
6.如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是
A.使用饱和食盐水是为了加快反应速率
B.硫酸铜溶液的作用是除去杂质
C.若酸性溶液褪色,说明乙炔具有还原性
D.反应中不需要加碎瓷片做沸石
7.乙炔是一种无色、无臭的气体,微溶于水,易溶于有机溶剂。实验室常用如图所示装置,利用电石()和水反应制取乙炔,并验证乙炔的性质。回答下列问题:
(1)利用电石制备乙炔的方程式:___________;
(2)用饱和食盐水代替蒸馏水的目的是___________。
(3)装置A的作用是___________,装置B中的现象是___________。
(4)装置C发生的反应类型是___________,完全反应的方程式___________。
(5)若称取ag电石,反应完全后,将生成的乙炔全部通入足量溴的溶液中,溶液增重bg,则电石的纯度为___________(用含有a、b的式子表示)。
模块 2 有机物的共线共面问题
四个基本模型
1 找——找到给出分子中的基本模型,主要是双键、三键和苯环,将复杂的分子按照基本模型分解成几个简单部分。
2 转——观察几个简单部分的连接处,借助单键可以旋转、双键三键不能旋转这一特点先看几个基本模型
能否处于同一平面或同一直线。
3 确定了基本模型的共线共面问题后,还剩下甲基的共线共面问题,此时利用甲烷中最多只有 2 个原子共线、最多只有 3 个原子共面的特性分析甲基的共线共面问题。
知识精炼
8.酚酞是中学化学中常用的酸碱指示剂,其结构如下。
回答下列问题:
(1)酚酞的分子式为____。
(2)1个酚酞分子中含有____个饱和碳原子和____个不饱和碳原子。
(3)酚酞分子中的双键有____种,它(们)是______。
(4)酚酞分子中的极性键有________(写2种即可)。
(5)酚酞分子中,所有的原子可能都在同一平面上吗 ____(填“可能”或“不可能”)。
(6) 1mol酚酞分子最多可以和____mol金属钠反应。
9.已知为平面结构,则W(HOOC-CH=CH-CH=CH-COOH)分子中最多有________个原子在同一平面内。
10.某有机化合物的结构简式如下,分析其结构并回答下列问题。
(1)写出其分子式:________。
(2)分子中含有___个不饱和碳原子,分子中有___种双键。
(3)分子中的极性键有___________。
(4)分子中的饱和碳原子有______个;一定与苯环处于同一平面的碳原子(包括苯环上的碳原子)有_______个。
(5)分子中C—C=O的键角约为___,C≡C-H的键角为___。
11.I.按要求完成下列问题:
(1)甲基的电子式__________;
(2) 含有的官能团的名称为__________;
II.某有机物的结构简式为 ,据此填写下列的空。
(1)该物质苯环上一氯代物有__________种;
(2)lmol该物质和溴水混合,消耗Br2的物质的量为__________mol;
(3)lmol该物质和H2加成需H2__________mol。
III.与一定量的Br2发生加成反应,生成的产物可能是__________。
A.
B.
C.
D.
12.请说明下列有机化合物中的所有碳原子是否能处于同一平面上。
(1) _______
(2) _______
(3) _______
(4) _______
13.有机物 分子中最多有___________个碳原子在同一平面内,最多有___________个原子在同一条直线上,与苯环共面的碳原子至少有___________个。
14.烃的分类和结构
(1)烷烃:分子中,碳原子之间都以_______结合成碳链,碳原子的剩余价键均与_______结合的烃。
烷烃分子中每个碳原子的最外层电子都被充分利用,达到“饱和”状态,因此这样的烃也叫作_______。
(2)不饱和链烃:碳原子还有_______的价键,每个碳原子的最外层电子没有被充分利用,即没有达到“饱和”状态的烃。
(3)环烃:分子中有_______的烃。
(4)常见烃的空间结构:乙烷分子中,同一个碳原子上的碳碳单键和三个碳氢键中,任意两个键之间的夹角都近似于_______分子中碳氢键的键角,所有原子_______同一平面上;乙烯分子是_______形分子,同一个碳原子上的碳碳双键和两个碳氢键中,任意两个键之间的夹角都约为_______;乙炔分子是_______形分子,碳碳三键和碳氢键之间的夹角为_______。
15.如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
a. b. c. d. e. f.
(1)写出有机物a的系统命名法的名称___________
(2)有机物a有一种同分异构体,试写出其结构简式___________
(3)上述有机物中与c互为同分异构体的是___________(填代号,下同)
(4)上述有机物中不能与溴反应并使其褪色的有___________
(5)abcd四种物质中,4个碳原子一定处于同一平面的有___________
(6)c通入酸性KMnO4溶液中,溶液褪色是发生___________反应,e通入溴的CCl4溶液中,溶液褪色发生___________反应。
试卷第1页,共3页
参考答案:
1.B
【分析】A中生成乙炔,通过氢氧化钠溶液除去氯化氢等气体,通过溴的四氯化碳溶液、酸性高锰酸钾溶液检验乙炔的性质;
【详解】A.实验室制备乙炔的时候,通常用饱和食盐水和电石制备,使用分液漏斗控制饱和食盐水的加入使得两者反应生成乙炔,A正确;
B.装置B作用是除去氯化氢、磷化氢等气体,需要使用硫酸铜溶液,B不正确;
C.乙炔能和溴发生加成反应,C中可以观察到溴的四氯化碳溶液褪色,C正确;
D.硫化氢气体也能使酸性高锰酸钾溶液褪色,故如果没有B装置,则D装置中酸性高锰酸钾溶液褪色不能证明乙炔被氧化,D正确;
故选B。
2.D
【详解】A.制取乙炔时常用饱和食盐水代替水反应,是为了减缓反应速率,故A正确;
B.乙炔中的硫化氢可以和硫酸铜溶液生成硫化铜沉淀,可用硫酸铜溶液除去乙炔气体中混有的杂质,故B正确;
C.乙炔中含有不饱和键,能使溴的四氯化碳溶液褪色;故C正确;
D.乙烯是平面分子,故D错误;
故答案选D。
3.B
【分析】从题给的装置看所得气体应具备下列特点:①可用浓H2SO4干燥(即不与浓H2SO4反应),②能用排空气法收集且密度比空气大(从收集装置进气管看);
【详解】A.NO易被氧化,不能利用排空气法收集,选项A不选;
B.氯化钠与浓硫酸共热反应生成氯化氢,可利用浓硫酸干燥,然后用向上排空气法收集,选项B选;
C.生成氢气的密度比空气密度小,应选向下排空气法收集,选项C不选;
D.生成乙炔的密度比空气密度小,应选向下排空气法收集,选项D不选;
答案选B。
4.C
【详解】由电子式可知,碳化钙为离子化合物,化合物中含有离子键、非极性共价三键,碳碳三键中含有1个σ键和2个π键,不含有极性键,故选C。
5.D
【详解】①石油分馏时把温度计测量馏分温度,所以温度计水银球位于蒸馏烧瓶支管口处,故错误;
②酸性高锰酸钾溶液和乙炔、H2S都发生氧化还原反应,所以不能用酸性高锰酸钾溶液除去乙炔中的硫化氢,可以用碱溶液除去硫化氢,故错误;
③应该用乙醇和浓硫酸共热到170℃制取乙烯,故错误;
④将敞口久置的电石与蒸馏水混合制乙炔时,因为敞口所以不能收集到乙炔,故错误;
故选D。
6.A
【详解】A.用饱和食盐水代替水是为了减小化学反应速率,A错误;
B.溶液的作用是除去等杂质,B正确;
C.酸性溶液褪色体现了乙炔具有还原性,C正确;
D.电石作为固体,能达到防暴沸的效果,反应中不需要加碎瓷片做沸石,D正确。
故答案选A。
7.(1)
(2)减小反应速率,使产生的乙炔气流平稳
(3) 除去乙炔中的气体 溶液的紫色褪去
(4) 加成反应
(5)
【分析】电石和水制取乙炔,由于电石中会混有硫、磷等杂质,所以生成的乙炔中会混有硫化氢、磷化氢等化合物,导致生成的乙炔有特殊难闻的臭味,硫酸铜溶液可以除去硫化氢和磷化氢。乙炔可以使酸性高锰酸钾溶液褪色,也可以和溴发生加成反应。
【详解】(1)电石(碳化钙CaC2)与水制取乙炔的化学方程式为:CaC2+2H2O→Ca(OH)2+HC≡CH↑。
(2)电石和水反应非常剧烈,可以用饱和食盐水代替蒸馏水减慢反应速率。
(3)硫酸铜和H2S可以发生复分解反应从而除去H2S:H2S+CuSO4=CuS↓+H2SO4,除去乙炔中的气体;乙炔能把酸性高锰酸钾溶液还原成Mn2+,所以高锰酸钾溶液的紫色会褪去。
(4)装置C乙炔和溴的四氯化碳溶液发生加成反应,化学方程式为。
(5)乙炔全部通入足量溴的CCl4溶液中,乙炔和溴发生加成反应,溶液增重的b g即为生成的乙炔的质量,所以乙炔的物质的量为mol,根据反应方程式CaC2+2H2O→Ca(OH)2+HC≡CH↑,乙炔和碳化钙的物质的量相等,所以碳化钙的质量为×64g,则CaC2的纯度为。
8. C20H14O4 1 19 1 C=O 碳氢键、碳氧键和氢氧键(任写两种) 不可能 2
【详解】(1)根据酚酞的结构式,得知酚酞的分子式为C20H14O4;
(2)根据碳原子的结构特点,与4个原子形成共价键的碳原子称为饱和碳原子,其他的碳原子称为不饱和碳原子,所以此分子中含有1个饱和碳原子,19个不饱和碳原子;
(3)此分子中只有碳氧双键1种双键,苯环中的碳碳双键是一种介于碳碳单键和碳碳双键之间的特殊的共价键,不是碳碳双键;
(4)不同原子间形成的共价键为极性键,此分子中有碳氢键、碳氧键和氢氧键三种极性键;
(5)与三个苯环相连的碳原子形成4个碳碳单键,为四面体构型,则所有的原子不可能都在同一个平面上;
(6)金属钠与羟基发生反应,与酯基不发生反应,故1mol酚酞分子最多可以和2mol金属钠反应。
9.16
【详解】由题中信息可知与直接相连的原子在同一平面上,又知与直接相连的原子在同一平面上,而且碳碳单键可以旋转,因此W分子中所有原子有可能都处在同一平面上,即最多有16个原子在同一平面内。
10. C16H16O5 12 2 H—C、H—O、O—C、C=O 4 10 120° 180°
【详解】(1)分析该有机物的结构简式,可知其分子式为C16H16O5,故答案为C16H16O5。
(2)苯环上的6个碳原子,碳碳双键上的2个碳原子,碳碳三键上的2个碳原子,酯基中的1个碳原子以及羧基中的1个碳原子,均为不饱和碳原子,共12个。该分子中有C=C、C=O两种双键,故答案为12,2。
(3)分子中的极性键有H—C、H—O、O—C、C=O,故答案为H—C、H—O、O—C、C=O。
(4)1个—CH3、2个―CH2―和1个中的碳原子为饱和碳原子,共4个;结合乙炔的直线形结构和苯的平面结构可知该有机物中一定与苯环处于同一平面的碳原子(包括苯环上的碳原子)有10个;故答案为4;10。
(5)分子中C—C=O的键角约为120°,C≡C-H的键角为180°,故答案为120°,180°。
11. 碳碳三键、溴原子 4 2 5 B
【详解】I、(1)甲基是由甲烷分子去掉一个氢原子形成的,且呈电中性,电子式为;
(2) 含有的官能团名称是碳碳三键、溴原子。苯基不属于官能团。
II、(1) 该分子苯环没有对称因素,苯环上的4个氢原子属于4种不同的等效氢原子,所以该物质苯环上的一氯代物有4种;
(2) 分子中的2个碳碳双键可与溴水加成,所以1mol该物质消耗Br2的物质的量为2mol;
(3) 结构中苯基、碳碳三键、碳碳双键都可与H2加成,所以1mol该有机物加成需要5molH2;
III、该二烯烃属于共轭二烯,与Br2加成时有1,2-加成、1,4-加成和全加成等三种情况,加成产物有以下几种:CH2BrCHBrCH=CHCH3、CH2=CHCHBrCHBrCH3、CH2BrCH=CHCHBrCH3、CH2BrCHBrCHBrCHBrCH3,答案选B。
【点睛】分析有机物分子里的官能团时,注意烷基、苯基不是官能团;分析多烯烃的加成反应时,要注意共轭二烯烃结构的特殊性所决定的性质的特殊性。
12. 不能 不能 能 不能
【分析】在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断。
【详解】(1)由于甲烷是正四面体结构,2号碳为四面体结构,1,2,3号碳原子构成一个平面,和4号碳原子不在同一平面内,故答案为:不能;
(2)甲烷是正四面体结构,左边的四个碳原子不在同一平面内,故答案为:不能;
(3)乙烯为平面结构,CH2═CH-CH═CH2中所有碳原子都处在同一平面上,故答案为:能;
(4)甲烷是正四面体结构,(CH3)3C-C≡C-CH=CHCH3CH2左边起第二个碳原子连接四个碳原子,不在同一平面内,故答案为:不能;
13. 11 6 9
【详解】以碳碳双键为中心,根据乙烯、苯、乙炔、甲烷的结构,可以画出如图所示结构。由于碳碳单键可以绕轴自由旋转,炔直线一定在苯平面内,苯平面和烯平面可能共面,也可能不共面。因而该有机物分子中的所有碳原子可能共面,最多有个碳原子共面,至少有个碳原子在苯平面内。由于苯分子、乙烯分子的键角均为,炔直线与所在苯环正六边形对角线上的碳原子共线,因而最多有5个碳原子和炔基上的1个氢原子共线,即。 ,故答案为:11;6;9。
14.(1) 单键 氢原子 饱和烃
(2)双键和三键
(3)碳环
(4) 甲烷 不在 平面 120° 直线 180°
【解析】略
15. 2-甲基丙烷 CH3CH2CH2CH3 bf af bc 氧化 加成
【详解】(1)有机物a分子中C原子之间都以单键结合形成链状,该物质属于烷烃,其分子中最长碳链上含有3个C原子,在中间C原子上有一个甲基,则该物质的系统命名法的名称为2-甲基丙烷;
(2)有机物a分子式是C4H10,该物质有一种同分异构体,其结构简式为CH3CH2CH2CH3;
(3)物质c是2-丁烯,分子式是C4H8,在上述有机物中与c互为同分异构体的是2-甲基丙烯和环丁烷,故合理选项是bf;
(4)含有碳碳双键或碳碳三键的物质能够与溴发生加成反应而使溴水褪色,在上述有机物中b中的2-甲基丙烯、c中的2-丁烯、d中的1,3-丁二烯、e中的1-丁炔都含有不饱和键,它们都能够使溴水褪色,而a中的2-甲基丙烷和f中的环丁烷由于分子中C原子之间都以单键结合,因此不能与溴发生反应并使其褪色,故合理选项有af;
(5)a.甲烷是正四面体结构,2-甲基丙烷可看作是甲烷分子中3个H原子被3个甲基取代产生的物质,因此4个C原子不在同一平面上,a不符合题意;
b.乙烯是平面分子,分子中的2个C原子和4个H原子在同一平面上。b可看作是乙烯分子中一个C原子上的2个H原子被2个甲基C原子取代,则四个C原子在同一平面上,b符合题意;
c.2-丁烯可看作是乙烯分子中2个不同C原子上的2个H原子被2个甲基取代产生的物质,因此分子中的四个C原子在同一平面上,c符合题意;
d.1,3-丁二烯分子中含有2个乙烯平面结构,两个平面共直线,可能在同一平面上,也可能不在同一平面上,d不符合题意;
故合理选项是bc;
(6)c是2-丁烯,分子中含有不饱和的碳碳双键,可以被酸性KMnO4溶液氧化而使溶液褪色,因此褪色原因是由于发生氧化反应;
e是1-丁炔,分子中含有不饱和的碳碳三键,将其通入溴的CCl4溶液中,由于发生加成反应而使溶液褪色,故溶液褪色原因是由于发生加成反应。
模块 1 乙炔的制备及性质实验
一、乙炔的实验室制取
1 实验原理:
CaC 2 +2H 2 O → C 2 H 2 ↑ +Ca(OH) 2
2 实验药品: 电石 (主要成分为 CaC 2 )、饱和氯化钠溶液。
3 实验装置
通过实验可以得到平稳的乙炔气流,观察到硫酸铜溶液中有黑色沉淀产生,同时红棕色溴水褪色。
小结
(1) 实验中用饱和的食盐水代替水—减缓乙炔气流速度,降低反应速率;
(2) 在实验装置中要使用分液漏斗—控制流量,减缓反应速率;
(3) 制取出的乙炔有刺激性气味—产生 H 2 S,PH 3 等杂质气体,用CuSO 4 溶液除去。
知识精炼
1.实验室用如图所示装置制备乙炔,并验证乙炔的某些化学性质,下列说法不正确的是
A.实验室制备乙炔的时候,通常用饱和食盐水和电石制备
B.装置B中的氢氧化钠溶液作用是吸收水蒸气
C.C中可以观察到溴的四氯化碳溶液褪色
D.如果没有B装置,则D装置中酸性高锰酸钾溶液褪色不能证明乙炔被氧化
2.下列关于乙炔的实验室制取和化学性质的说法错误的是
A.为了减缓电石与水的反应速率,可用饱和食盐水代替水反应
B.为了除去乙炔气体中混有的杂质,可将气体通过硫酸铜溶液
C.乙炔能使溴的四氯化碳溶液褪色
D.乙炔与乙烯都是直线形分子
3.可用如图装置制取(必要时可加热)、净化、收集的气体是
A.铜和稀硝酸制一氧化氮
B.氯化钠与浓硫酸制氯化氢
C.锌和稀硫酸制氢气
D.碳化钙与饱和食盐水制乙炔
4.已知电石的电子式为,下列关于电石中化学键类型的说法错误的是
A.含有离子键 B.含有σ键 C.含有极性键 D.含有非极性键
5.下列操作达不到预期目的的是
①石油分馏时把温度计插入受热的液体中
②用酸性高锰酸钾溶液除去乙炔中含有的H2S
③用乙醇和3mol/L的硫酸共热到170℃制取乙烯
④将敞口久置的电石与水混合制乙炔
A.只有① B.只有③④ C.只有①②③ D.①②③④
6.如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是
A.使用饱和食盐水是为了加快反应速率
B.硫酸铜溶液的作用是除去杂质
C.若酸性溶液褪色,说明乙炔具有还原性
D.反应中不需要加碎瓷片做沸石
7.乙炔是一种无色、无臭的气体,微溶于水,易溶于有机溶剂。实验室常用如图所示装置,利用电石()和水反应制取乙炔,并验证乙炔的性质。回答下列问题:
(1)利用电石制备乙炔的方程式:___________;
(2)用饱和食盐水代替蒸馏水的目的是___________。
(3)装置A的作用是___________,装置B中的现象是___________。
(4)装置C发生的反应类型是___________,完全反应的方程式___________。
(5)若称取ag电石,反应完全后,将生成的乙炔全部通入足量溴的溶液中,溶液增重bg,则电石的纯度为___________(用含有a、b的式子表示)。
模块 2 有机物的共线共面问题
四个基本模型
1 找——找到给出分子中的基本模型,主要是双键、三键和苯环,将复杂的分子按照基本模型分解成几个简单部分。
2 转——观察几个简单部分的连接处,借助单键可以旋转、双键三键不能旋转这一特点先看几个基本模型
能否处于同一平面或同一直线。
3 确定了基本模型的共线共面问题后,还剩下甲基的共线共面问题,此时利用甲烷中最多只有 2 个原子共线、最多只有 3 个原子共面的特性分析甲基的共线共面问题。
知识精炼
8.酚酞是中学化学中常用的酸碱指示剂,其结构如下。
回答下列问题:
(1)酚酞的分子式为____。
(2)1个酚酞分子中含有____个饱和碳原子和____个不饱和碳原子。
(3)酚酞分子中的双键有____种,它(们)是______。
(4)酚酞分子中的极性键有________(写2种即可)。
(5)酚酞分子中,所有的原子可能都在同一平面上吗 ____(填“可能”或“不可能”)。
(6) 1mol酚酞分子最多可以和____mol金属钠反应。
9.已知为平面结构,则W(HOOC-CH=CH-CH=CH-COOH)分子中最多有________个原子在同一平面内。
10.某有机化合物的结构简式如下,分析其结构并回答下列问题。
(1)写出其分子式:________。
(2)分子中含有___个不饱和碳原子,分子中有___种双键。
(3)分子中的极性键有___________。
(4)分子中的饱和碳原子有______个;一定与苯环处于同一平面的碳原子(包括苯环上的碳原子)有_______个。
(5)分子中C—C=O的键角约为___,C≡C-H的键角为___。
11.I.按要求完成下列问题:
(1)甲基的电子式__________;
(2) 含有的官能团的名称为__________;
II.某有机物的结构简式为 ,据此填写下列的空。
(1)该物质苯环上一氯代物有__________种;
(2)lmol该物质和溴水混合,消耗Br2的物质的量为__________mol;
(3)lmol该物质和H2加成需H2__________mol。
III.与一定量的Br2发生加成反应,生成的产物可能是__________。
A.
B.
C.
D.
12.请说明下列有机化合物中的所有碳原子是否能处于同一平面上。
(1) _______
(2) _______
(3) _______
(4) _______
13.有机物 分子中最多有___________个碳原子在同一平面内,最多有___________个原子在同一条直线上,与苯环共面的碳原子至少有___________个。
14.烃的分类和结构
(1)烷烃:分子中,碳原子之间都以_______结合成碳链,碳原子的剩余价键均与_______结合的烃。
烷烃分子中每个碳原子的最外层电子都被充分利用,达到“饱和”状态,因此这样的烃也叫作_______。
(2)不饱和链烃:碳原子还有_______的价键,每个碳原子的最外层电子没有被充分利用,即没有达到“饱和”状态的烃。
(3)环烃:分子中有_______的烃。
(4)常见烃的空间结构:乙烷分子中,同一个碳原子上的碳碳单键和三个碳氢键中,任意两个键之间的夹角都近似于_______分子中碳氢键的键角,所有原子_______同一平面上;乙烯分子是_______形分子,同一个碳原子上的碳碳双键和两个碳氢键中,任意两个键之间的夹角都约为_______;乙炔分子是_______形分子,碳碳三键和碳氢键之间的夹角为_______。
15.如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
a. b. c. d. e. f.
(1)写出有机物a的系统命名法的名称___________
(2)有机物a有一种同分异构体,试写出其结构简式___________
(3)上述有机物中与c互为同分异构体的是___________(填代号,下同)
(4)上述有机物中不能与溴反应并使其褪色的有___________
(5)abcd四种物质中,4个碳原子一定处于同一平面的有___________
(6)c通入酸性KMnO4溶液中,溶液褪色是发生___________反应,e通入溴的CCl4溶液中,溶液褪色发生___________反应。
试卷第1页,共3页
参考答案:
1.B
【分析】A中生成乙炔,通过氢氧化钠溶液除去氯化氢等气体,通过溴的四氯化碳溶液、酸性高锰酸钾溶液检验乙炔的性质;
【详解】A.实验室制备乙炔的时候,通常用饱和食盐水和电石制备,使用分液漏斗控制饱和食盐水的加入使得两者反应生成乙炔,A正确;
B.装置B作用是除去氯化氢、磷化氢等气体,需要使用硫酸铜溶液,B不正确;
C.乙炔能和溴发生加成反应,C中可以观察到溴的四氯化碳溶液褪色,C正确;
D.硫化氢气体也能使酸性高锰酸钾溶液褪色,故如果没有B装置,则D装置中酸性高锰酸钾溶液褪色不能证明乙炔被氧化,D正确;
故选B。
2.D
【详解】A.制取乙炔时常用饱和食盐水代替水反应,是为了减缓反应速率,故A正确;
B.乙炔中的硫化氢可以和硫酸铜溶液生成硫化铜沉淀,可用硫酸铜溶液除去乙炔气体中混有的杂质,故B正确;
C.乙炔中含有不饱和键,能使溴的四氯化碳溶液褪色;故C正确;
D.乙烯是平面分子,故D错误;
故答案选D。
3.B
【分析】从题给的装置看所得气体应具备下列特点:①可用浓H2SO4干燥(即不与浓H2SO4反应),②能用排空气法收集且密度比空气大(从收集装置进气管看);
【详解】A.NO易被氧化,不能利用排空气法收集,选项A不选;
B.氯化钠与浓硫酸共热反应生成氯化氢,可利用浓硫酸干燥,然后用向上排空气法收集,选项B选;
C.生成氢气的密度比空气密度小,应选向下排空气法收集,选项C不选;
D.生成乙炔的密度比空气密度小,应选向下排空气法收集,选项D不选;
答案选B。
4.C
【详解】由电子式可知,碳化钙为离子化合物,化合物中含有离子键、非极性共价三键,碳碳三键中含有1个σ键和2个π键,不含有极性键,故选C。
5.D
【详解】①石油分馏时把温度计测量馏分温度,所以温度计水银球位于蒸馏烧瓶支管口处,故错误;
②酸性高锰酸钾溶液和乙炔、H2S都发生氧化还原反应,所以不能用酸性高锰酸钾溶液除去乙炔中的硫化氢,可以用碱溶液除去硫化氢,故错误;
③应该用乙醇和浓硫酸共热到170℃制取乙烯,故错误;
④将敞口久置的电石与蒸馏水混合制乙炔时,因为敞口所以不能收集到乙炔,故错误;
故选D。
6.A
【详解】A.用饱和食盐水代替水是为了减小化学反应速率,A错误;
B.溶液的作用是除去等杂质,B正确;
C.酸性溶液褪色体现了乙炔具有还原性,C正确;
D.电石作为固体,能达到防暴沸的效果,反应中不需要加碎瓷片做沸石,D正确。
故答案选A。
7.(1)
(2)减小反应速率,使产生的乙炔气流平稳
(3) 除去乙炔中的气体 溶液的紫色褪去
(4) 加成反应
(5)
【分析】电石和水制取乙炔,由于电石中会混有硫、磷等杂质,所以生成的乙炔中会混有硫化氢、磷化氢等化合物,导致生成的乙炔有特殊难闻的臭味,硫酸铜溶液可以除去硫化氢和磷化氢。乙炔可以使酸性高锰酸钾溶液褪色,也可以和溴发生加成反应。
【详解】(1)电石(碳化钙CaC2)与水制取乙炔的化学方程式为:CaC2+2H2O→Ca(OH)2+HC≡CH↑。
(2)电石和水反应非常剧烈,可以用饱和食盐水代替蒸馏水减慢反应速率。
(3)硫酸铜和H2S可以发生复分解反应从而除去H2S:H2S+CuSO4=CuS↓+H2SO4,除去乙炔中的气体;乙炔能把酸性高锰酸钾溶液还原成Mn2+,所以高锰酸钾溶液的紫色会褪去。
(4)装置C乙炔和溴的四氯化碳溶液发生加成反应,化学方程式为。
(5)乙炔全部通入足量溴的CCl4溶液中,乙炔和溴发生加成反应,溶液增重的b g即为生成的乙炔的质量,所以乙炔的物质的量为mol,根据反应方程式CaC2+2H2O→Ca(OH)2+HC≡CH↑,乙炔和碳化钙的物质的量相等,所以碳化钙的质量为×64g,则CaC2的纯度为。
8. C20H14O4 1 19 1 C=O 碳氢键、碳氧键和氢氧键(任写两种) 不可能 2
【详解】(1)根据酚酞的结构式,得知酚酞的分子式为C20H14O4;
(2)根据碳原子的结构特点,与4个原子形成共价键的碳原子称为饱和碳原子,其他的碳原子称为不饱和碳原子,所以此分子中含有1个饱和碳原子,19个不饱和碳原子;
(3)此分子中只有碳氧双键1种双键,苯环中的碳碳双键是一种介于碳碳单键和碳碳双键之间的特殊的共价键,不是碳碳双键;
(4)不同原子间形成的共价键为极性键,此分子中有碳氢键、碳氧键和氢氧键三种极性键;
(5)与三个苯环相连的碳原子形成4个碳碳单键,为四面体构型,则所有的原子不可能都在同一个平面上;
(6)金属钠与羟基发生反应,与酯基不发生反应,故1mol酚酞分子最多可以和2mol金属钠反应。
9.16
【详解】由题中信息可知与直接相连的原子在同一平面上,又知与直接相连的原子在同一平面上,而且碳碳单键可以旋转,因此W分子中所有原子有可能都处在同一平面上,即最多有16个原子在同一平面内。
10. C16H16O5 12 2 H—C、H—O、O—C、C=O 4 10 120° 180°
【详解】(1)分析该有机物的结构简式,可知其分子式为C16H16O5,故答案为C16H16O5。
(2)苯环上的6个碳原子,碳碳双键上的2个碳原子,碳碳三键上的2个碳原子,酯基中的1个碳原子以及羧基中的1个碳原子,均为不饱和碳原子,共12个。该分子中有C=C、C=O两种双键,故答案为12,2。
(3)分子中的极性键有H—C、H—O、O—C、C=O,故答案为H—C、H—O、O—C、C=O。
(4)1个—CH3、2个―CH2―和1个中的碳原子为饱和碳原子,共4个;结合乙炔的直线形结构和苯的平面结构可知该有机物中一定与苯环处于同一平面的碳原子(包括苯环上的碳原子)有10个;故答案为4;10。
(5)分子中C—C=O的键角约为120°,C≡C-H的键角为180°,故答案为120°,180°。
11. 碳碳三键、溴原子 4 2 5 B
【详解】I、(1)甲基是由甲烷分子去掉一个氢原子形成的,且呈电中性,电子式为;
(2) 含有的官能团名称是碳碳三键、溴原子。苯基不属于官能团。
II、(1) 该分子苯环没有对称因素,苯环上的4个氢原子属于4种不同的等效氢原子,所以该物质苯环上的一氯代物有4种;
(2) 分子中的2个碳碳双键可与溴水加成,所以1mol该物质消耗Br2的物质的量为2mol;
(3) 结构中苯基、碳碳三键、碳碳双键都可与H2加成,所以1mol该有机物加成需要5molH2;
III、该二烯烃属于共轭二烯,与Br2加成时有1,2-加成、1,4-加成和全加成等三种情况,加成产物有以下几种:CH2BrCHBrCH=CHCH3、CH2=CHCHBrCHBrCH3、CH2BrCH=CHCHBrCH3、CH2BrCHBrCHBrCHBrCH3,答案选B。
【点睛】分析有机物分子里的官能团时,注意烷基、苯基不是官能团;分析多烯烃的加成反应时,要注意共轭二烯烃结构的特殊性所决定的性质的特殊性。
12. 不能 不能 能 不能
【分析】在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断。
【详解】(1)由于甲烷是正四面体结构,2号碳为四面体结构,1,2,3号碳原子构成一个平面,和4号碳原子不在同一平面内,故答案为:不能;
(2)甲烷是正四面体结构,左边的四个碳原子不在同一平面内,故答案为:不能;
(3)乙烯为平面结构,CH2═CH-CH═CH2中所有碳原子都处在同一平面上,故答案为:能;
(4)甲烷是正四面体结构,(CH3)3C-C≡C-CH=CHCH3CH2左边起第二个碳原子连接四个碳原子,不在同一平面内,故答案为:不能;
13. 11 6 9
【详解】以碳碳双键为中心,根据乙烯、苯、乙炔、甲烷的结构,可以画出如图所示结构。由于碳碳单键可以绕轴自由旋转,炔直线一定在苯平面内,苯平面和烯平面可能共面,也可能不共面。因而该有机物分子中的所有碳原子可能共面,最多有个碳原子共面,至少有个碳原子在苯平面内。由于苯分子、乙烯分子的键角均为,炔直线与所在苯环正六边形对角线上的碳原子共线,因而最多有5个碳原子和炔基上的1个氢原子共线,即。 ,故答案为:11;6;9。
14.(1) 单键 氢原子 饱和烃
(2)双键和三键
(3)碳环
(4) 甲烷 不在 平面 120° 直线 180°
【解析】略
15. 2-甲基丙烷 CH3CH2CH2CH3 bf af bc 氧化 加成
【详解】(1)有机物a分子中C原子之间都以单键结合形成链状,该物质属于烷烃,其分子中最长碳链上含有3个C原子,在中间C原子上有一个甲基,则该物质的系统命名法的名称为2-甲基丙烷;
(2)有机物a分子式是C4H10,该物质有一种同分异构体,其结构简式为CH3CH2CH2CH3;
(3)物质c是2-丁烯,分子式是C4H8,在上述有机物中与c互为同分异构体的是2-甲基丙烯和环丁烷,故合理选项是bf;
(4)含有碳碳双键或碳碳三键的物质能够与溴发生加成反应而使溴水褪色,在上述有机物中b中的2-甲基丙烯、c中的2-丁烯、d中的1,3-丁二烯、e中的1-丁炔都含有不饱和键,它们都能够使溴水褪色,而a中的2-甲基丙烷和f中的环丁烷由于分子中C原子之间都以单键结合,因此不能与溴发生反应并使其褪色,故合理选项有af;
(5)a.甲烷是正四面体结构,2-甲基丙烷可看作是甲烷分子中3个H原子被3个甲基取代产生的物质,因此4个C原子不在同一平面上,a不符合题意;
b.乙烯是平面分子,分子中的2个C原子和4个H原子在同一平面上。b可看作是乙烯分子中一个C原子上的2个H原子被2个甲基C原子取代,则四个C原子在同一平面上,b符合题意;
c.2-丁烯可看作是乙烯分子中2个不同C原子上的2个H原子被2个甲基取代产生的物质,因此分子中的四个C原子在同一平面上,c符合题意;
d.1,3-丁二烯分子中含有2个乙烯平面结构,两个平面共直线,可能在同一平面上,也可能不在同一平面上,d不符合题意;
故合理选项是bc;
(6)c是2-丁烯,分子中含有不饱和的碳碳双键,可以被酸性KMnO4溶液氧化而使溶液褪色,因此褪色原因是由于发生氧化反应;
e是1-丁炔,分子中含有不饱和的碳碳三键,将其通入溴的CCl4溶液中,由于发生加成反应而使溶液褪色,故溶液褪色原因是由于发生加成反应。
