3.3.2 甲醛 学案(含解析) 高中化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.3.2 甲醛 学案(含解析) 高中化学人教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-03 00:00:00 | ||
图片预览




文档简介
第 8 讲 醛和酮
模块 1 甲醛
1.理解甲醛的结构与性质。
2.记忆掌握甲醛的化学方程式。
一、甲醛概述
甲醛又叫蚁醛,分子式为 CH 2 O,结构式为,甲醛分子中所有原子在同一平面内。
甲醛是重要的有机合成原料,常用于制造酚醛树脂、脲醛树脂、涤纶和染料等,但同时也是室内的重要污染源。35% 40% 的甲醛水溶液叫做福尔马林,具有很好的杀菌、防腐功能,可用作农药、消毒剂和防腐剂。
知识精炼
1.化学与生活紧密相关,下列有关说法不正确的是
A.TNT是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等
B.乙二醇可用于生产汽车防冻剂
C.福尔马林具有杀菌、防腐性能,可用于制作生物标本
D.医用酒精是指体积分数为95%的乙醇溶液,常用作消毒剂
2.福尔马林的主要成分是
A.乙醇 B.甲醛 C.乙醛 D.乙酸
3.下列说法中正确的是
A.福尔马林是的甲醛水溶液,可用于浸制生物标本
B.乙醛能发生银镜反应,表明了醛具有氧化性
C.凡能起银镜反应的物质一定是醛
D.在加热和有催化剂的条件下,醇都能被空气中的O2所氧化,生成对应的醛
4.化学与生活紧密相关,下列有关说法不正确的是
A.TNT是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等
B.医用酒精是指体积分数为95%的乙醇溶液,常用作消毒剂
C.福尔马林具有杀菌、防腐性能,可用于制作生物标本
D.乙二醇可用于生产汽车防冻剂
5.在医学、日常生活中常见的溶液:①福尔马林②医用消毒酒精③生理盐水④食醋,这些溶液中的溶质质量分数由大到小顺序为
A.①②③④ B.①②④③ C.③②④① D.②①④③
6.下列表示正确的是
A.或比例模型 B.乙烯的球棍模型
C.2 甲基戊烷的键线式 D.甲醛的电子式
7.下列各物质中,最简式相同,但既不是同系物,又不是同分异构体的是
A.乙醇和乙醚 B.乙烯和丙烯
C.乙烷和苯 D.甲醛和乙酸
8.下列化学用语使用不正确的是
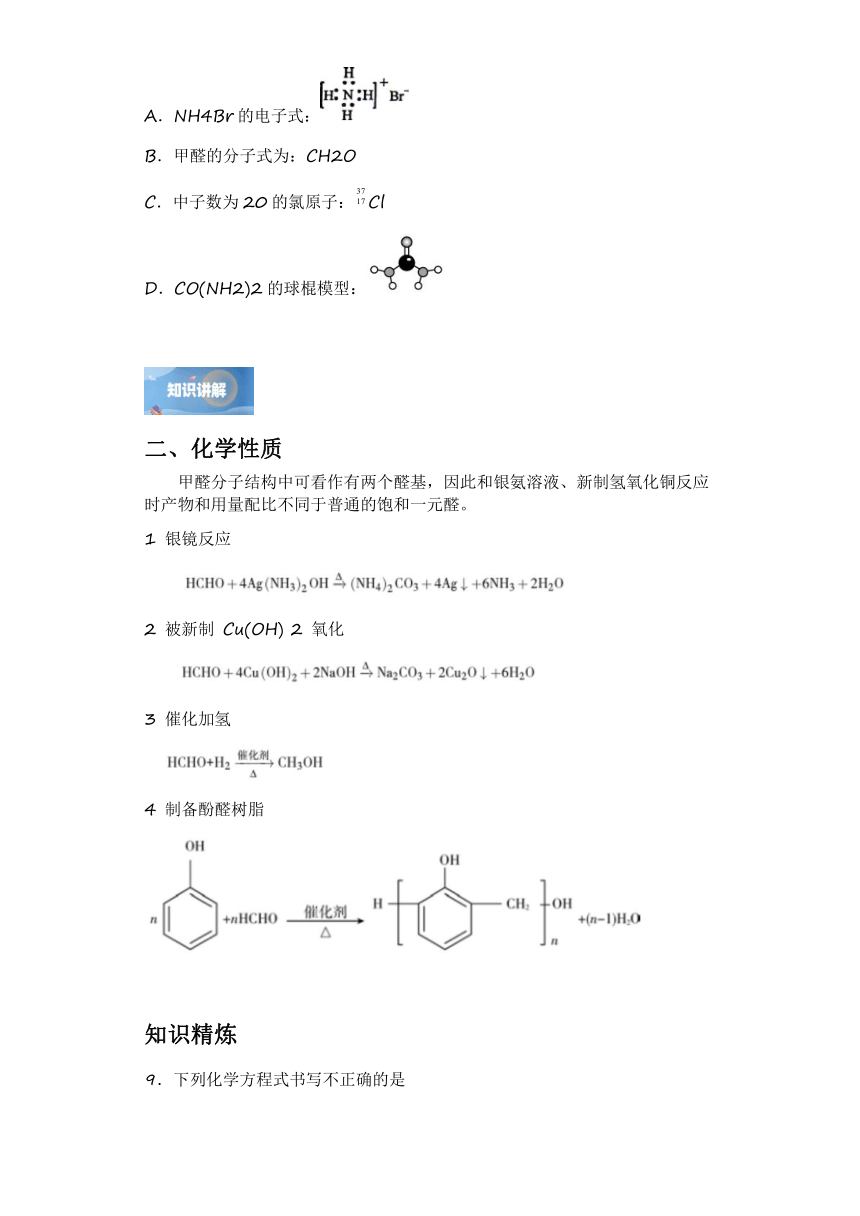
A.NH4Br的电子式:
B.甲醛的分子式为:CH2O
C.中子数为20的氯原子:Cl
D.CO(NH2)2的球棍模型:
二、化学性质
甲醛分子结构中可看作有两个醛基,因此和银氨溶液、新制氢氧化铜反应时产物和用量配比不同于普通的饱和一元醛。
1 银镜反应
2 被新制 Cu(OH) 2 氧化
3 催化加氢
4 制备酚醛树脂
知识精炼
9.下列化学方程式书写不正确的是
A.乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:
B.溴乙烷与NaOH的乙醇溶液共热:
C.向苯酚钠溶液中通入:+CO2+H2O+NaHCO3
D.甲醛溶液中加入足量的银氨溶液并加热:
10.一首脍炙人口的民歌《茉莉花》唱得沁人心脾。茉莉醛具有浓郁的茉莉花香,其结构简式如图所示。下列关于茉莉醛的叙述中,正确的是
A.茉莉醛与苯甲醛互为同系物
B.在加热和催化剂作用下加氢,每摩尔茉莉醛最多能消耗
C.一定条件下,茉莉醛能发生氧化、还原、酯化等反应
D.从理论上说,202g茉莉醛能从足量银氨溶液中还原出216g银
11.甲烷经过一系列反应后能够合成,合成路线如图所示。下列说法错误的是
A.步骤2的反应类型为取代反应
B.可用红外光谱鉴别甲醇和甲醛
C.0.1mol HCHO与足量银氨溶液反应最多生成21.6gAg
D.步骤3的反应条件和所需试剂为加热、铜
12.酚醛树脂具有绝缘、阻燃等性能,由苯酚和甲醛合成酚醛树脂的反应如下:
下列说法正确的是
A.化学方程式中水的化学计量数是
B.常温下比更难溶于水
C.1molHCHO与银氨溶液反应最多可以生成2molAg
D.的单体是和HCHO
13.下列对应的反应方程式正确的是
A.实验室制备乙烯:
B.苯的磺化反应: +HO-SO3H+H2O
C.乙酸乙酯的制备:
D.甲醛溶液中加入足量的银氨溶液并加热:
14.下列文字表述与反应方程式对应且正确的是
A.氯乙酸乙酯在足量溶液中加热:
B.向甲酸中加入过量新制悬浊液:
C.向苯酚钠溶液中通入少量:
D.苯与溴水的混合物中加入:
15.研究甲醛与新制Cu(OH)2反应的固体产物(固体A),实验如图。
已知:Cu2O、CuO均能溶于浓氨水,分别产生。
下列说法不正确的是
A.甲醛与新制Cu(OH)2反应时,甲醛被氧化
B.②→④无色溶液变蓝,说明固体A中存在Cu2O
C.根据以上实验现象,推测固体A中含有Cu2O、Cu
D.将试管①替换为,放置一段时间后发现溶液变蓝,也能确认固体A的成分
16.除去下列物质中所含少量杂质(括号内为杂质),所选试剂和方法均正确的是
A.乙烯(H2S):将混合气体通入酸性高锰酸钾溶液,洗气
B.甲酸(甲醛):新制Cu(OH)2悬浊液,过滤
C.乙醇(水):加足量生石灰,蒸馏
D.乙酸乙酯(乙酸):氢氧化钠溶液,分液
17.有机化合物与人类的生活密切相关,以下叙述中,正确的是
①乙醇和乙酸都是常用调味品的主要成分
②米酒变酸的过程涉及了氧化反应
③福尔马林溶液可以用来保存标本,是35~40%的甲醇水溶液
④酒越陈越香是因为发生了酯化反应
A.①②④ B.②③ C.①②③ D.①③④
18.化学与生活关系密切,有关物质用途说法错误的是
A.明矾可用于水的消毒、杀菌 B.甲醛溶液可以用于浸泡生物标本
C.醋可用于除去热水瓶胆中的水垢 D.硫酸钡医疗上可用作“钡餐”
19.有机化合物在生活中无处不在,下列说法不正确的是
A.福尔马林是甲醛的水溶液,具有杀菌防腐能力,也可用于保鲜鱼、肉等食品
B.食品包装材料聚乙烯由乙烯发生加聚反应而制得
C.苯酚有毒但可以制成药皂,具有杀菌消毒的功效
D.甘油加水可做护肤剂
20.“关爱生命,拥抱健康”是人类永恒的主题,下列说法科学的是
A.福尔马林虽有防腐作用,但不能用于浸泡食材
B.铁强化酱油因添加了铁单质可预防贫血病
C.纤维素不能被人体消化,因此对人体健康无益
D.医用酒精用于防疫消毒,其中乙醇的质量分数为75%
21.三分子甲醛在一定条件下反应可生成三聚甲醛(),三聚甲醛可用作合成工程塑料等,还是日用化妆品冷烫精及脱毛剂的主要原料。下列有关三聚甲醛的说法中正确的是
A.三聚甲醛属于高分子化合物
B.三聚甲醛与甘油互为同分异构体
C.依三聚甲醛的结构可推测三聚乙醛的结构为
D.1 mol的三聚甲醛燃烧时生成CO2和H2O的物质的量相等
22(多选).我国科学家成功利用人工合淀粉,使淀粉生产方式从农业种植转为工业制造成为可能,其原理如下所示。下列说法错误的是
A.反应①的化学方程式为
B.30g的b物质与足量银氨溶液反应可生成216gAg
C.等质量的b与c物质完全燃烧,消耗氧气的量相同
D.淀粉属于多糖,分子式为,是纯净物
23.1molHCHO与足量银氨溶液在水浴加热条件下充分反应,最多生成2molAg____
24.甲醛与新制氢氧化铜反应的产物随反应条件改变而有所不同。实验室对该反应在一定条件下所得产物成分进行探究,具体过程如下。
取一定量的溶液、溶液和甲醛于锥形瓬中,控制温度为40~50℃回流,收集到大量气体,并有红色沉淀生成。
(1)①“控制温度为40~50℃”的常用加热方法是___________。
②气体能燃烧且完全燃烧产物不会使澄清石床水变浑浊,说明该气体是___________。
(2)在探究甲醛的氧化产物时,发现未生成。为了进一步确定甲醛是否被氧化为,进行如图实验(夹持装置和加热装置已省略,甲酸与浓硫酸反应能生成,而可将银氨溶液还原成银单质)。
①仪器a的名称是___________。
②b中,溶液的作用是___________。
③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为___________。
(3)已知:(无色),遇空气容易被氧化成(蓝色);验证红色沉淀中含,进行如下实验步骤和现象记录:取样品,___________,说明红色固体中含。
(4)若最终测得红色沉淀为和少量的,且的物质的量和气体X的相等,则该条件下甲醛与新制氢氧化铜、氢氧化钠溶液反应生成和气体X的化学方程式___________。
25.在人口居住密度较大的城区和建筑群中,室内空气的污染有时会比室外更严重。目前已发现的室内空气污染物达300多种。
(1)室内装修材料及家具挥发出来的_______是室内空气的主要污染物,该气体_______(填“易”或“难”)溶于水,常温下有强烈的刺激性气味,当温度超过20℃时,挥发速度加快,根据该气体的这些性质,判断下列做法错误的是_______。
A.入住前房间内保持一定温度并通风
B.装修尽可能选择在温度较高的季节
C. 请环境监测部门检测室内甲醛含量低于国家标准后入住
D.紧闭门窗一段时间后入住
(2)在入住装修过的新房之前在房间内,放置适量的吊兰、芦荟等植物有利于净化空气,但晚上在密闭的居室内放置大型绿色植物,可能影响人体健康。主要原因是其_______。
26.天然气化工是重要的支柱产业之一,以天然气为原料经下列反应路线可得工程塑料PBT。
(1)B分子结构中只有一种氢、一种氧、一种碳,则B的结构简式是_______;B的同分异构体中与葡萄糖具有类似结构的是________(写结构简式)。
(2)F的结构简式是_________;PBT属于_______类有机高分子化合物.
(3)由A、D生成E的反应方程式为_______,其反应类型为_________。
(4)E的同分异构体G不能发生银镜反应,能使溴水褪色,能水解且产物的碳原子数不等,则G在NaOH溶液中发生水解反应的化学方程式是___________。
试卷第1页,共3页
参考答案:
1.D
【详解】A.TNT是2,4,6-三硝基甲苯,是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等,A项正确;
B.乙二醇熔点低,可用于生产汽车防冻剂,B项正确;
C.福尔马林是甲醛水溶液,具有杀菌、防腐性能,可用于制作生物标本,C项正确;
D.医用酒精是指体积分数为75%的乙醇溶液,常用作消毒剂,D项错误;
故答案选D。
2.B
【详解】A.乙醇俗名酒精,故A不符合题意;
B.甲醛的水溶液交福尔马林,故B符合题意;
C.乙醛化学式为CH3CHO,故C不符合题意;
D.乙酸俗名醋酸,故D不符合题意。
综上所述,答案为B。
3.A
【详解】A.福尔马林是的甲醛水溶液,福尔马林能使蛋白质变性,因此可用于浸制生物标本,故A正确;
B.乙醛能发生银镜反应,银化合价降低,乙醛化合价升高,表明乙醛具有还原性,故B错误;
C.凡能起银镜反应的物质一定含有醛基,但不一定是醛,比如甲酸也能发生银镜反应,故C错误;
D.在加热和有催化剂的条件下, CH2OH被催化氧化变为醛,被催化氧化变为酮,不会被催化氧化,故D错误。
综上所述,答案为A。
4.B
【详解】A.2,4,6 三硝基甲苯俗名TNT,是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等,故A正确;
B.医用酒精是指体积分数为75%的乙醇溶液,能使蛋白质变性,具有消毒杀菌作用,故B错误;
C.福尔马林是甲醛水溶液,能使蛋白质变性,具有杀菌、防腐性能,可用于制作生物标本,故C正确;
D.乙二醇(HOCH2CH2OH)熔点低,常用于生产汽车防冻剂,故D正确。
综上所述,答案为B。
5.D
【详解】福尔马林是溶质质量分数为35~40%的甲醛水溶液,医用消毒酒精是体积分数为75%的乙醇水溶液,生理盐水是溶质质量分数为0.9%的氯化钠溶液,食醋是质量分数为5~8%的醋酸溶液,则溶质质量分数由大到小顺序为②①④③,故选D。
6.B
【详解】A.氢原子半径比碳原子半径小,氯原子半径比碳原子半径大,因此该比例模型只能是的比例模型,不是的比例模型,故A错误;
B.乙烯含有碳碳双键,该球棍模型是乙烯的球棍模型,故B正确;
C.2 甲基戊烷的键线式 ,故C错误;
D.甲醛中氧还有孤对电子,其电子式 ,故D错误。
综上所述,答案为B。
7.D
【详解】A.乙醇的分子式为C2H6O、乙醚的分子式为C4H10O,两者的最简式不相同,故A不符合题意;
B.乙烯的分子式为C2H4、丙烯的分子式为C3H6,两者的最简式都为CH2,但两者都为烯烃,互为同系物,故B不符合题意;
C.乙烷的分子式C2H6、苯的分子式为C6H6,两者的最简式不相同,故C不符合题意;
D.甲醛的分子式为CH2O、乙酸的分子式为C2H4O2,两者的最简式都为CH2O,两者既不是同系物,又不是同分异构体,故D符合题意;
故选D。
8.A
【详解】A.NH4Br的电子式:,故A错误;
B.甲醛由一个氢原子连接醛基而成,其分子式为:CH2O,故B正确;
C.中子数为20的氯原子:Cl,故C正确;
D.CO(NH2)2由羰基连接两个氨基组成,其球棍模型:,故D正确;
故选:A;
9.D
【详解】A.乙醛与碱性氢氧化铜悬浊液混合后加热被氧化成乙酸钠,氢氧化铜被还原成氧化亚铜和水,故A正确;
B.溴乙烷属于卤代烃,与NaOH的乙醇溶液共热,发生消去反应,生成乙烯,故B正确;
C.由于碳酸的酸性强于苯酚,苯酚的酸性强于碳酸氢根离子,则向苯酚钠溶液中通入,生成的是苯酚和碳酸氢钠,故C正确;
D.甲醛溶液中加入足量的银氨溶液并加热,甲醛被氧化生成碳酸铵,其反应的化学方程式为
,故D错误;
答案D。
10.D
【详解】A.苯甲醛中不含碳碳双键,茉莉醛中含有碳碳双键,所以苯甲醛和茉莉醛的结构不同,不属于同系物,故A错误;
B.在一定条件下,能和氢气发生加成反应的有苯环、碳碳双键、醛基,1mol该物质含有1mol苯环、1mol碳碳双键、1mol醛基,所以1mol茉莉醛最多能与5mol氢气加成,故B错误;
C.含-CHO,能发生氧化、还原反应,但不能发生酯化反应,故C错误;
D.含1个-CHO,茉莉醛的相对分子质量为202,202g茉莉醛的物质的量为1mol,可从足量银氨溶液中还原出2mol银,质量为216g,故D正确;
故选:D。
11.C
【详解】A.步骤2的反应为一氯甲烷在氢氧化钠溶液中发生取代反应生成甲醇,故A正确;
B.甲醇的官能团羟基、甲醛的官能团为醛基,两者的官能团不同,红外光谱的谱图不同,所以可以用红外光谱鉴别,故B正确;
C.甲醛与足量银氨溶液共热反应到方程式为HCHO+4Ag(NH3)2OH(NH4)2CO3+4Ag↓+6NH3+2H2O,则0.1mol甲醛与足量银氨溶液反应最多生成银的质量为0.1mol×4×108g/mol=43.2g,故C错误;
D.步骤3的反应为在铜做催化剂的条件下,甲醇与氧气共热发生催化氧化反应生成甲醛,反应条件和所需试剂为加热、铜,故D正确;
故选C。
12.D
【分析】苯酚与甲醛缩聚形成酚醛树脂时,苯环上酚羟基邻位或对位的氢被活化,与醛基碳氧双键中的氧结合生成水,甲醛的亚甲基则与苯环相连生成聚合物,在酸性条件下苯酚与甲醛缩聚形成链状高分子聚合物;在碱性条件下苯酚与甲醛缩聚形成具有立体空间结构的网状高分子聚合物。
【详解】A.从化学方程式可以看出,水的化学计量数是,A项错误;
B.1个中含有2个亲水基团,而1个中只含有1个亲水基团,前者比后者易溶于水,B项错误;
C.1mol HCHO中相当于含有2mol醛基,故与银氨溶液反应最多可以生成4molAg,C项错误;
D.的单体是苯酚和甲醛,D项正确;
故选D。
【点睛】含有基团的高聚物是HCHO和苯酚发生缩聚反应生成的产物。
13.B
【详解】A. 实验室中用乙醇在浓硫酸催化和维持条件下制得乙烯,140℃时生成乙醚,故A错误;
B. 苯环上的H被磺酸基取代的反应称为磺化反应,苯的磺化反应:+HO-SO3H+H2O,故B正确;
C. 羧酸与醇发生酯化反应的机理为“酸去羟基醇去氢”则正确的方程式为,故C错误;
D. 甲醛溶液中加入足量的银氨溶液并加热,反应的离子方程式为:,故D错误;
故选B。
14.B
【详解】A.氯乙酸乙酯在足量溶液中加热发生氯代烃的水解反应和酯的水解反应,故为,故A错误;
B.向甲酸中加入过量新制Cu(OH)2悬浊液发生氧化反应生成HOOCOOH即碳酸,碳酸与NaOH溶液反应生成碳酸钠,反应方程式为,故B正确;
C.苯酚的酸性比碳酸弱,向苯酚钠溶液中通入少量CO2生成苯酚和碳酸氢钠,反应方程式为,故C错误;
D.苯和液溴发生取代反应,苯和溴水不反应,故D错误;
故选B。
15.D
【详解】A.甲醛与新制Cu(OH)2反应时,反应生成Cu2O,铜元素化合价降低,则Cu(OH)2被还原,甲醛被氧化,故A正确;
B.由已知Cu(NH3)(无色),Cu(NH3)(蓝色),且Cu2O能溶于浓氨水,则②→④无色溶液变蓝,说明固体A中存在Cu2O,故B正确;
C.Cu2O、CuO均能溶于浓氨水,故固体A经浓氨水浸泡后得到的红色固体应为Cu,结合B项可知固体A中含有Cu2O、Cu,故C正确;
D.将试管①替换为,没有密封,空气中的氧气可能'参与反应,则放置一段时间后发现溶液变蓝,不能确认固体A的成分,故D错误;
故选D。
16.C
【详解】A.乙烯与杂质H2S都能够被酸性高锰酸钾溶液氧化,因此不能通过洗气除去杂质H2S,A错误;
B.甲酸能够与新制Cu(OH)2悬浊液发生中和反应而溶解;而甲醛能够溶于水,因此不能通过加入新制Cu(OH)2悬浊液,然后过滤除杂,B错误;
C.水与生石灰发生反应产生Ca(OH)2,Ca(OH)2熔沸点高,而乙醇沸点低,然后通过蒸馏分离得到乙醇,C正确;
D.乙酸乙酯和杂质乙酸都能够与NaOH发生反应,因此不能用加入氢氧化钠溶液,然后通过分液方法除杂,D错误;
故合理选项是C。
17.A
【详解】①在家庭厨房中,常使用料酒和食醋,它们的主要成分分别是乙醇和乙酸;
②米酒变酸的过程中,发生乙醇的催化氧化过程,涉及了氧化反应;
③福尔马林是35~40%的甲醛水溶液,能使蛋白质变性,可用来保存标本;
④酒越陈越香是因为有少量乙醇被氧化为乙酸,乙醇与乙酸发生了酯化反应,生成的酯具有香味;
综合以上分析,①②④正确,故选A。
18.A
【详解】A.明矾在水中形成胶体,能吸附水中的悬浮物质,不能用于水的消毒杀菌,A错误;
B.甲醛能使蛋白质变性,35%-40%甲醛水溶液俗称福尔马林,具有防腐杀菌性能,可用来浸制生物标本,B正确;
C.醋酸的酸性大于碳酸,可用于除去热水瓶胆中的水垢(主要成分为CaCO3),C正确;
D.硫酸钡不溶于水,与盐酸也不反应,所以在医疗上可用作钡餐为胃病病人透视,D正确;
故选A。
19.A
【详解】A.甲醛有毒,不能用于浸泡食物,故A错误;
B.聚乙烯可用于制作食品包装袋,在一定条件下可通过乙烯的加聚反应生成聚乙烯,故B正确;
C.苯酚有毒,低浓度的苯酚制成的药皂,可以起到杀菌消毒的作用,故C正确;
D.甘油易溶于水,甘油可以起到护肤的作用,故D正确;
故选A。
20.A
【详解】A.福尔马林虽有防腐作用,福尔马林有毒,因此不能用于浸泡食材,故A符合题意;
B.铁强化酱油因添加了亚铁离子不是铁单质,故B不符合题意;
C.纤维素不能被人体消化,因此对人体健康起肠胃蠕动的作用,故C不符合题意;
D.医用酒精用于防疫消毒,其中乙醇的体积分数为75%,不是质量分数,故D不符合题意。
综上所述,答案为A。
21.C
【详解】A.高分子化合物相对分子质量在10000以上,该分子相对分子质量较小,所以不属于高分子化合物,故A错误;
B.分子式相同结构不同的有机物互为同分异构体,丙三醇分子式为C3H8O3,三聚甲醛分子式为C3H6O3,所以不是同分异构体,故B错误;
C.三分子甲醛在一定条件下反应可生成三聚甲醛,该反应符合加成反应特点,则三分子乙醛在一定条件下反应可生成三聚乙醛,三聚乙醛的结构应该为,故C正确;
D.三聚甲醛的分子式为C3H6O3,根据原子守恒知,如果完全燃烧生成二氧化碳和水的物质的量相等,如果生成CO,则生成的二氧化碳和水的物质的量不等,故D错误;
故选C。
【点睛】本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系、物质结构特点及基本概念是解本题关键。本题的易错选项是D,易忽略不完全燃烧而导致错误。
22.BD
【详解】A.根据图中信息得到反应①的化学方程式为, A正确;
B.根据关系式HCHO~4Ag,30g的b物质(物质的量为1mol)与足量银氨溶液反应可生成4molAg即432gAg,故B错误;
C.b(HCHO)与c(HOCH2COCH2OH)通式相同,因此等质量的b(HCHO)与c(HOCH2COCH2OH)物质完全燃烧,消耗氧气的量相同,故C正确;
D.淀粉属于多糖,分子式为,是混合物,故D错误。
综上所述,答案为BD。
23.错误
【详解】1molHCHO与足量银氨溶液在水浴加热条件下充分反应,最多生成4molAg,错误;
24.(1) 水浴加热 H2
(2) 分液漏斗 除去CO中混有的HCOOH蒸气 2∶1
(3)方案一:溶于氨水,向所得溶液中通入空气(或通入氧气或在空气中放置一段时间),观察溶液变蓝色;方案二:将样品溶于硫酸,观察到溶液呈蓝色
(4)2HCHO+Cu(OH)2 +2NaOHCu+2HCOONa+2H2O+H2↑
【详解】(1)①控制温度在40~50℃,低于水的沸点,所以可以采用水浴加热。②气体X能燃烧且完全燃烧后产物不会使澄清石灰水变浑浊,根据原子守恒可知该气体应为H2。答案:水浴加热;H2;
(2)浓硫酸与反应液反应,若甲醛被氧化为HCOONa,则浓硫酸会与其反应生成CO,由于甲酸具有挥发性且能与银氨溶液反应,应先将其除去,再通入银氨溶液,银氨溶液中出现黑色沉淀,说明有CO生成,进而说明甲醛被氧化为HCOONa,气球可以收集尾气。①仪器a为分液漏斗。②甲酸具有挥发性,且含有结构,能和银氨溶液反应,所以需要用NaOH溶液除去CO中混有的HCOOH蒸气。③银氨溶液中出现黑色沉淀,说明CO将银氨溶液还原为银单质,氧化剂为[Ag(NH3)]+,还原剂为CO,根据得失电子守恒,可知氧化剂与还原剂的物质的量之比为2∶1。
答案:分液漏斗;除去CO中混有的HCOOH蒸气;2∶1;
(3)红色沉淀可能为Cu或CuO或二者都有,因为Cu不溶于氨水或硫酸,若红色固体中含有Cu2O,则固体溶于氨水得无色溶液,在空气中放置一段时间后, 遇空气容易被氧化成(蓝色),溶液变蓝色,或将Cu2O溶于硫酸,Cu2O发生歧化反应,得到CuSO4蓝色溶液和单质Cu,答案:方案一:溶于氨水,向所得溶液中通入空气(或通入氧气或在空气中放置一段时间),观察溶液变蓝色;方案二:将样品溶于硫酸,观察到溶液呈蓝色;
(4)根据上述分析可知,甲醛与新制的Cu(OH)反应生成的气体为H2,甲醛与新制氢氧化铜、氢氧化钠溶液反应生成等物质的量的和H2,根据得失电子守恒和原子守恒可写出该反应的化学方程式:2HCHO+Cu(OH)2+2NaOHCu+2HCOONa+2H2O+H2↑。
25.(1) 甲醛 易 D
(2)大型绿色植物晚上通过呼吸作用会消耗大量氧气
【解析】(1)
内装修材料及家具挥发出来的甲醛是室内空气的主要污染物,该气体易溶于水,常温下有强烈的刺激性气味。装修尽可能选择在温度较高的季节,入住前房间内保持一定温度并通风并请环境监测部门检测室内甲醛含量低于国家标准后入住,不能紧闭门窗一段时间后入住。
(2)
大型绿色植物晚上通过呼吸作用会消耗大量氧气,晚上在密闭的居室内放置大型绿色植物会影响健康。
26. HO—CH2—CH2—CH2—CH2—OH 酯 HC≡CH+2HCHOHOCH2C≡CCH2OH 加成反应 CH2=CH—COOCH3+NaOH→CH2=CH—COONa+CH3OH
【分析】甲醇在Cu作催化剂、加热条件被氧气氧化生成甲醛(HCHO),则A为HCHO,结合A、B的分子式可知,B为3分子甲醛形成,B分子结构为六元环状化合物,B分子结构中只有一种氢、一种氧、一种碳,应是3分子甲醛之间的加成反应生成B,则B为;由E→F的转化及F分子式可知,E中含有4个C原子,由HCHO+D→E,再根据已知反应信息可知,该反应为2分子甲醛与乙炔发生加成反应,D为HC≡CH,E为HOCH2-C≡C-CH2OH,E与氢气发生加成反应生成F,F与二元羧酸通过酯化反应形成高聚物PBT,据此分析解答。
【详解】(1)甲醇氧化生成甲醛(HCHO),结合A、B的分子式可知,B为3分子甲醛形成,B分子结构为六元环状化合物,B分子结构中只有一种氢、一种氧、一种碳,应是3分子甲醛之间的加成反应生成B,则B的结构简式为:;B的同分异构体与葡萄糖结构类似,该异构体中含有1个-CHO,2个羟基-OH,为链状结构,该同分异构体的结构简式为,故答案为;;
(2)由E→F的转化及F分子式可知,E中含有4个C原子,由HCHO+D→E,再根据已知反应信息可知,该反应为2分子甲醛与乙炔发生加成反应,D为HC≡CH,E为HOCH2-C≡C-CH2OH,E与氢气发生加成反应生成F,故F结构简式为HO-CH2-CH2-CH2-CH2-OH,F与二元羧酸通过酯化反应形成高聚物PBT,PBT属于酯类,故答案为HO-CH2-CH2-CH2-CH2-OH;酯;
(3)由(2)中分析可知,该反应为该反应为2分子甲醛与乙炔发生加成反应生成HOCH2-C≡C-CH2OH,由A、D生成E的反应方程式为:HC≡CH+2HCHO HOCH2C≡CCH2OH,故答案为HC≡CH+2HCHO HOCH2C≡CCH2OH;加成反应;
(4)HOCH2-C≡C-CH2OH的同分异构体G不能发生银镜反应,分子中不含醛基-CHO或-OOCH,能使溴水褪色,含有不饱和键,能水解且产物的碳原子数不等,含有酯基,故含有1个C=C双键、1个酯基,且形成该酯的羧酸含有3个碳原子,醇为甲醇,故G的结构简式为:CH2=CH-COOCH3,CH2=CH-COOCH3在氢氧化钠溶液中发生水解方程式为:
CH2=CH-COOCH3+NaOH→CH2=CH-COONa+CH3OH,故答案为CH2=CH-COOCH3+NaOH→CH2=CH-COONa+CH3OH。
模块 1 甲醛
1.理解甲醛的结构与性质。
2.记忆掌握甲醛的化学方程式。
一、甲醛概述
甲醛又叫蚁醛,分子式为 CH 2 O,结构式为,甲醛分子中所有原子在同一平面内。
甲醛是重要的有机合成原料,常用于制造酚醛树脂、脲醛树脂、涤纶和染料等,但同时也是室内的重要污染源。35% 40% 的甲醛水溶液叫做福尔马林,具有很好的杀菌、防腐功能,可用作农药、消毒剂和防腐剂。
知识精炼
1.化学与生活紧密相关,下列有关说法不正确的是
A.TNT是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等
B.乙二醇可用于生产汽车防冻剂
C.福尔马林具有杀菌、防腐性能,可用于制作生物标本
D.医用酒精是指体积分数为95%的乙醇溶液,常用作消毒剂
2.福尔马林的主要成分是
A.乙醇 B.甲醛 C.乙醛 D.乙酸
3.下列说法中正确的是
A.福尔马林是的甲醛水溶液,可用于浸制生物标本
B.乙醛能发生银镜反应,表明了醛具有氧化性
C.凡能起银镜反应的物质一定是醛
D.在加热和有催化剂的条件下,醇都能被空气中的O2所氧化,生成对应的醛
4.化学与生活紧密相关,下列有关说法不正确的是
A.TNT是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等
B.医用酒精是指体积分数为95%的乙醇溶液,常用作消毒剂
C.福尔马林具有杀菌、防腐性能,可用于制作生物标本
D.乙二醇可用于生产汽车防冻剂
5.在医学、日常生活中常见的溶液:①福尔马林②医用消毒酒精③生理盐水④食醋,这些溶液中的溶质质量分数由大到小顺序为
A.①②③④ B.①②④③ C.③②④① D.②①④③
6.下列表示正确的是
A.或比例模型 B.乙烯的球棍模型
C.2 甲基戊烷的键线式 D.甲醛的电子式
7.下列各物质中,最简式相同,但既不是同系物,又不是同分异构体的是
A.乙醇和乙醚 B.乙烯和丙烯
C.乙烷和苯 D.甲醛和乙酸
8.下列化学用语使用不正确的是
A.NH4Br的电子式:
B.甲醛的分子式为:CH2O
C.中子数为20的氯原子:Cl
D.CO(NH2)2的球棍模型:
二、化学性质
甲醛分子结构中可看作有两个醛基,因此和银氨溶液、新制氢氧化铜反应时产物和用量配比不同于普通的饱和一元醛。
1 银镜反应
2 被新制 Cu(OH) 2 氧化
3 催化加氢
4 制备酚醛树脂
知识精炼
9.下列化学方程式书写不正确的是
A.乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:
B.溴乙烷与NaOH的乙醇溶液共热:
C.向苯酚钠溶液中通入:+CO2+H2O+NaHCO3
D.甲醛溶液中加入足量的银氨溶液并加热:
10.一首脍炙人口的民歌《茉莉花》唱得沁人心脾。茉莉醛具有浓郁的茉莉花香,其结构简式如图所示。下列关于茉莉醛的叙述中,正确的是
A.茉莉醛与苯甲醛互为同系物
B.在加热和催化剂作用下加氢,每摩尔茉莉醛最多能消耗
C.一定条件下,茉莉醛能发生氧化、还原、酯化等反应
D.从理论上说,202g茉莉醛能从足量银氨溶液中还原出216g银
11.甲烷经过一系列反应后能够合成,合成路线如图所示。下列说法错误的是
A.步骤2的反应类型为取代反应
B.可用红外光谱鉴别甲醇和甲醛
C.0.1mol HCHO与足量银氨溶液反应最多生成21.6gAg
D.步骤3的反应条件和所需试剂为加热、铜
12.酚醛树脂具有绝缘、阻燃等性能,由苯酚和甲醛合成酚醛树脂的反应如下:
下列说法正确的是
A.化学方程式中水的化学计量数是
B.常温下比更难溶于水
C.1molHCHO与银氨溶液反应最多可以生成2molAg
D.的单体是和HCHO
13.下列对应的反应方程式正确的是
A.实验室制备乙烯:
B.苯的磺化反应: +HO-SO3H+H2O
C.乙酸乙酯的制备:
D.甲醛溶液中加入足量的银氨溶液并加热:
14.下列文字表述与反应方程式对应且正确的是
A.氯乙酸乙酯在足量溶液中加热:
B.向甲酸中加入过量新制悬浊液:
C.向苯酚钠溶液中通入少量:
D.苯与溴水的混合物中加入:
15.研究甲醛与新制Cu(OH)2反应的固体产物(固体A),实验如图。
已知:Cu2O、CuO均能溶于浓氨水,分别产生。
下列说法不正确的是
A.甲醛与新制Cu(OH)2反应时,甲醛被氧化
B.②→④无色溶液变蓝,说明固体A中存在Cu2O
C.根据以上实验现象,推测固体A中含有Cu2O、Cu
D.将试管①替换为,放置一段时间后发现溶液变蓝,也能确认固体A的成分
16.除去下列物质中所含少量杂质(括号内为杂质),所选试剂和方法均正确的是
A.乙烯(H2S):将混合气体通入酸性高锰酸钾溶液,洗气
B.甲酸(甲醛):新制Cu(OH)2悬浊液,过滤
C.乙醇(水):加足量生石灰,蒸馏
D.乙酸乙酯(乙酸):氢氧化钠溶液,分液
17.有机化合物与人类的生活密切相关,以下叙述中,正确的是
①乙醇和乙酸都是常用调味品的主要成分
②米酒变酸的过程涉及了氧化反应
③福尔马林溶液可以用来保存标本,是35~40%的甲醇水溶液
④酒越陈越香是因为发生了酯化反应
A.①②④ B.②③ C.①②③ D.①③④
18.化学与生活关系密切,有关物质用途说法错误的是
A.明矾可用于水的消毒、杀菌 B.甲醛溶液可以用于浸泡生物标本
C.醋可用于除去热水瓶胆中的水垢 D.硫酸钡医疗上可用作“钡餐”
19.有机化合物在生活中无处不在,下列说法不正确的是
A.福尔马林是甲醛的水溶液,具有杀菌防腐能力,也可用于保鲜鱼、肉等食品
B.食品包装材料聚乙烯由乙烯发生加聚反应而制得
C.苯酚有毒但可以制成药皂,具有杀菌消毒的功效
D.甘油加水可做护肤剂
20.“关爱生命,拥抱健康”是人类永恒的主题,下列说法科学的是
A.福尔马林虽有防腐作用,但不能用于浸泡食材
B.铁强化酱油因添加了铁单质可预防贫血病
C.纤维素不能被人体消化,因此对人体健康无益
D.医用酒精用于防疫消毒,其中乙醇的质量分数为75%
21.三分子甲醛在一定条件下反应可生成三聚甲醛(),三聚甲醛可用作合成工程塑料等,还是日用化妆品冷烫精及脱毛剂的主要原料。下列有关三聚甲醛的说法中正确的是
A.三聚甲醛属于高分子化合物
B.三聚甲醛与甘油互为同分异构体
C.依三聚甲醛的结构可推测三聚乙醛的结构为
D.1 mol的三聚甲醛燃烧时生成CO2和H2O的物质的量相等
22(多选).我国科学家成功利用人工合淀粉,使淀粉生产方式从农业种植转为工业制造成为可能,其原理如下所示。下列说法错误的是
A.反应①的化学方程式为
B.30g的b物质与足量银氨溶液反应可生成216gAg
C.等质量的b与c物质完全燃烧,消耗氧气的量相同
D.淀粉属于多糖,分子式为,是纯净物
23.1molHCHO与足量银氨溶液在水浴加热条件下充分反应,最多生成2molAg____
24.甲醛与新制氢氧化铜反应的产物随反应条件改变而有所不同。实验室对该反应在一定条件下所得产物成分进行探究,具体过程如下。
取一定量的溶液、溶液和甲醛于锥形瓬中,控制温度为40~50℃回流,收集到大量气体,并有红色沉淀生成。
(1)①“控制温度为40~50℃”的常用加热方法是___________。
②气体能燃烧且完全燃烧产物不会使澄清石床水变浑浊,说明该气体是___________。
(2)在探究甲醛的氧化产物时,发现未生成。为了进一步确定甲醛是否被氧化为,进行如图实验(夹持装置和加热装置已省略,甲酸与浓硫酸反应能生成,而可将银氨溶液还原成银单质)。
①仪器a的名称是___________。
②b中,溶液的作用是___________。
③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为___________。
(3)已知:(无色),遇空气容易被氧化成(蓝色);验证红色沉淀中含,进行如下实验步骤和现象记录:取样品,___________,说明红色固体中含。
(4)若最终测得红色沉淀为和少量的,且的物质的量和气体X的相等,则该条件下甲醛与新制氢氧化铜、氢氧化钠溶液反应生成和气体X的化学方程式___________。
25.在人口居住密度较大的城区和建筑群中,室内空气的污染有时会比室外更严重。目前已发现的室内空气污染物达300多种。
(1)室内装修材料及家具挥发出来的_______是室内空气的主要污染物,该气体_______(填“易”或“难”)溶于水,常温下有强烈的刺激性气味,当温度超过20℃时,挥发速度加快,根据该气体的这些性质,判断下列做法错误的是_______。
A.入住前房间内保持一定温度并通风
B.装修尽可能选择在温度较高的季节
C. 请环境监测部门检测室内甲醛含量低于国家标准后入住
D.紧闭门窗一段时间后入住
(2)在入住装修过的新房之前在房间内,放置适量的吊兰、芦荟等植物有利于净化空气,但晚上在密闭的居室内放置大型绿色植物,可能影响人体健康。主要原因是其_______。
26.天然气化工是重要的支柱产业之一,以天然气为原料经下列反应路线可得工程塑料PBT。
(1)B分子结构中只有一种氢、一种氧、一种碳,则B的结构简式是_______;B的同分异构体中与葡萄糖具有类似结构的是________(写结构简式)。
(2)F的结构简式是_________;PBT属于_______类有机高分子化合物.
(3)由A、D生成E的反应方程式为_______,其反应类型为_________。
(4)E的同分异构体G不能发生银镜反应,能使溴水褪色,能水解且产物的碳原子数不等,则G在NaOH溶液中发生水解反应的化学方程式是___________。
试卷第1页,共3页
参考答案:
1.D
【详解】A.TNT是2,4,6-三硝基甲苯,是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等,A项正确;
B.乙二醇熔点低,可用于生产汽车防冻剂,B项正确;
C.福尔马林是甲醛水溶液,具有杀菌、防腐性能,可用于制作生物标本,C项正确;
D.医用酒精是指体积分数为75%的乙醇溶液,常用作消毒剂,D项错误;
故答案选D。
2.B
【详解】A.乙醇俗名酒精,故A不符合题意;
B.甲醛的水溶液交福尔马林,故B符合题意;
C.乙醛化学式为CH3CHO,故C不符合题意;
D.乙酸俗名醋酸,故D不符合题意。
综上所述,答案为B。
3.A
【详解】A.福尔马林是的甲醛水溶液,福尔马林能使蛋白质变性,因此可用于浸制生物标本,故A正确;
B.乙醛能发生银镜反应,银化合价降低,乙醛化合价升高,表明乙醛具有还原性,故B错误;
C.凡能起银镜反应的物质一定含有醛基,但不一定是醛,比如甲酸也能发生银镜反应,故C错误;
D.在加热和有催化剂的条件下, CH2OH被催化氧化变为醛,被催化氧化变为酮,不会被催化氧化,故D错误。
综上所述,答案为A。
4.B
【详解】A.2,4,6 三硝基甲苯俗名TNT,是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等,故A正确;
B.医用酒精是指体积分数为75%的乙醇溶液,能使蛋白质变性,具有消毒杀菌作用,故B错误;
C.福尔马林是甲醛水溶液,能使蛋白质变性,具有杀菌、防腐性能,可用于制作生物标本,故C正确;
D.乙二醇(HOCH2CH2OH)熔点低,常用于生产汽车防冻剂,故D正确。
综上所述,答案为B。
5.D
【详解】福尔马林是溶质质量分数为35~40%的甲醛水溶液,医用消毒酒精是体积分数为75%的乙醇水溶液,生理盐水是溶质质量分数为0.9%的氯化钠溶液,食醋是质量分数为5~8%的醋酸溶液,则溶质质量分数由大到小顺序为②①④③,故选D。
6.B
【详解】A.氢原子半径比碳原子半径小,氯原子半径比碳原子半径大,因此该比例模型只能是的比例模型,不是的比例模型,故A错误;
B.乙烯含有碳碳双键,该球棍模型是乙烯的球棍模型,故B正确;
C.2 甲基戊烷的键线式 ,故C错误;
D.甲醛中氧还有孤对电子,其电子式 ,故D错误。
综上所述,答案为B。
7.D
【详解】A.乙醇的分子式为C2H6O、乙醚的分子式为C4H10O,两者的最简式不相同,故A不符合题意;
B.乙烯的分子式为C2H4、丙烯的分子式为C3H6,两者的最简式都为CH2,但两者都为烯烃,互为同系物,故B不符合题意;
C.乙烷的分子式C2H6、苯的分子式为C6H6,两者的最简式不相同,故C不符合题意;
D.甲醛的分子式为CH2O、乙酸的分子式为C2H4O2,两者的最简式都为CH2O,两者既不是同系物,又不是同分异构体,故D符合题意;
故选D。
8.A
【详解】A.NH4Br的电子式:,故A错误;
B.甲醛由一个氢原子连接醛基而成,其分子式为:CH2O,故B正确;
C.中子数为20的氯原子:Cl,故C正确;
D.CO(NH2)2由羰基连接两个氨基组成,其球棍模型:,故D正确;
故选:A;
9.D
【详解】A.乙醛与碱性氢氧化铜悬浊液混合后加热被氧化成乙酸钠,氢氧化铜被还原成氧化亚铜和水,故A正确;
B.溴乙烷属于卤代烃,与NaOH的乙醇溶液共热,发生消去反应,生成乙烯,故B正确;
C.由于碳酸的酸性强于苯酚,苯酚的酸性强于碳酸氢根离子,则向苯酚钠溶液中通入,生成的是苯酚和碳酸氢钠,故C正确;
D.甲醛溶液中加入足量的银氨溶液并加热,甲醛被氧化生成碳酸铵,其反应的化学方程式为
,故D错误;
答案D。
10.D
【详解】A.苯甲醛中不含碳碳双键,茉莉醛中含有碳碳双键,所以苯甲醛和茉莉醛的结构不同,不属于同系物,故A错误;
B.在一定条件下,能和氢气发生加成反应的有苯环、碳碳双键、醛基,1mol该物质含有1mol苯环、1mol碳碳双键、1mol醛基,所以1mol茉莉醛最多能与5mol氢气加成,故B错误;
C.含-CHO,能发生氧化、还原反应,但不能发生酯化反应,故C错误;
D.含1个-CHO,茉莉醛的相对分子质量为202,202g茉莉醛的物质的量为1mol,可从足量银氨溶液中还原出2mol银,质量为216g,故D正确;
故选:D。
11.C
【详解】A.步骤2的反应为一氯甲烷在氢氧化钠溶液中发生取代反应生成甲醇,故A正确;
B.甲醇的官能团羟基、甲醛的官能团为醛基,两者的官能团不同,红外光谱的谱图不同,所以可以用红外光谱鉴别,故B正确;
C.甲醛与足量银氨溶液共热反应到方程式为HCHO+4Ag(NH3)2OH(NH4)2CO3+4Ag↓+6NH3+2H2O,则0.1mol甲醛与足量银氨溶液反应最多生成银的质量为0.1mol×4×108g/mol=43.2g,故C错误;
D.步骤3的反应为在铜做催化剂的条件下,甲醇与氧气共热发生催化氧化反应生成甲醛,反应条件和所需试剂为加热、铜,故D正确;
故选C。
12.D
【分析】苯酚与甲醛缩聚形成酚醛树脂时,苯环上酚羟基邻位或对位的氢被活化,与醛基碳氧双键中的氧结合生成水,甲醛的亚甲基则与苯环相连生成聚合物,在酸性条件下苯酚与甲醛缩聚形成链状高分子聚合物;在碱性条件下苯酚与甲醛缩聚形成具有立体空间结构的网状高分子聚合物。
【详解】A.从化学方程式可以看出,水的化学计量数是,A项错误;
B.1个中含有2个亲水基团,而1个中只含有1个亲水基团,前者比后者易溶于水,B项错误;
C.1mol HCHO中相当于含有2mol醛基,故与银氨溶液反应最多可以生成4molAg,C项错误;
D.的单体是苯酚和甲醛,D项正确;
故选D。
【点睛】含有基团的高聚物是HCHO和苯酚发生缩聚反应生成的产物。
13.B
【详解】A. 实验室中用乙醇在浓硫酸催化和维持条件下制得乙烯,140℃时生成乙醚,故A错误;
B. 苯环上的H被磺酸基取代的反应称为磺化反应,苯的磺化反应:+HO-SO3H+H2O,故B正确;
C. 羧酸与醇发生酯化反应的机理为“酸去羟基醇去氢”则正确的方程式为,故C错误;
D. 甲醛溶液中加入足量的银氨溶液并加热,反应的离子方程式为:,故D错误;
故选B。
14.B
【详解】A.氯乙酸乙酯在足量溶液中加热发生氯代烃的水解反应和酯的水解反应,故为,故A错误;
B.向甲酸中加入过量新制Cu(OH)2悬浊液发生氧化反应生成HOOCOOH即碳酸,碳酸与NaOH溶液反应生成碳酸钠,反应方程式为,故B正确;
C.苯酚的酸性比碳酸弱,向苯酚钠溶液中通入少量CO2生成苯酚和碳酸氢钠,反应方程式为,故C错误;
D.苯和液溴发生取代反应,苯和溴水不反应,故D错误;
故选B。
15.D
【详解】A.甲醛与新制Cu(OH)2反应时,反应生成Cu2O,铜元素化合价降低,则Cu(OH)2被还原,甲醛被氧化,故A正确;
B.由已知Cu(NH3)(无色),Cu(NH3)(蓝色),且Cu2O能溶于浓氨水,则②→④无色溶液变蓝,说明固体A中存在Cu2O,故B正确;
C.Cu2O、CuO均能溶于浓氨水,故固体A经浓氨水浸泡后得到的红色固体应为Cu,结合B项可知固体A中含有Cu2O、Cu,故C正确;
D.将试管①替换为,没有密封,空气中的氧气可能'参与反应,则放置一段时间后发现溶液变蓝,不能确认固体A的成分,故D错误;
故选D。
16.C
【详解】A.乙烯与杂质H2S都能够被酸性高锰酸钾溶液氧化,因此不能通过洗气除去杂质H2S,A错误;
B.甲酸能够与新制Cu(OH)2悬浊液发生中和反应而溶解;而甲醛能够溶于水,因此不能通过加入新制Cu(OH)2悬浊液,然后过滤除杂,B错误;
C.水与生石灰发生反应产生Ca(OH)2,Ca(OH)2熔沸点高,而乙醇沸点低,然后通过蒸馏分离得到乙醇,C正确;
D.乙酸乙酯和杂质乙酸都能够与NaOH发生反应,因此不能用加入氢氧化钠溶液,然后通过分液方法除杂,D错误;
故合理选项是C。
17.A
【详解】①在家庭厨房中,常使用料酒和食醋,它们的主要成分分别是乙醇和乙酸;
②米酒变酸的过程中,发生乙醇的催化氧化过程,涉及了氧化反应;
③福尔马林是35~40%的甲醛水溶液,能使蛋白质变性,可用来保存标本;
④酒越陈越香是因为有少量乙醇被氧化为乙酸,乙醇与乙酸发生了酯化反应,生成的酯具有香味;
综合以上分析,①②④正确,故选A。
18.A
【详解】A.明矾在水中形成胶体,能吸附水中的悬浮物质,不能用于水的消毒杀菌,A错误;
B.甲醛能使蛋白质变性,35%-40%甲醛水溶液俗称福尔马林,具有防腐杀菌性能,可用来浸制生物标本,B正确;
C.醋酸的酸性大于碳酸,可用于除去热水瓶胆中的水垢(主要成分为CaCO3),C正确;
D.硫酸钡不溶于水,与盐酸也不反应,所以在医疗上可用作钡餐为胃病病人透视,D正确;
故选A。
19.A
【详解】A.甲醛有毒,不能用于浸泡食物,故A错误;
B.聚乙烯可用于制作食品包装袋,在一定条件下可通过乙烯的加聚反应生成聚乙烯,故B正确;
C.苯酚有毒,低浓度的苯酚制成的药皂,可以起到杀菌消毒的作用,故C正确;
D.甘油易溶于水,甘油可以起到护肤的作用,故D正确;
故选A。
20.A
【详解】A.福尔马林虽有防腐作用,福尔马林有毒,因此不能用于浸泡食材,故A符合题意;
B.铁强化酱油因添加了亚铁离子不是铁单质,故B不符合题意;
C.纤维素不能被人体消化,因此对人体健康起肠胃蠕动的作用,故C不符合题意;
D.医用酒精用于防疫消毒,其中乙醇的体积分数为75%,不是质量分数,故D不符合题意。
综上所述,答案为A。
21.C
【详解】A.高分子化合物相对分子质量在10000以上,该分子相对分子质量较小,所以不属于高分子化合物,故A错误;
B.分子式相同结构不同的有机物互为同分异构体,丙三醇分子式为C3H8O3,三聚甲醛分子式为C3H6O3,所以不是同分异构体,故B错误;
C.三分子甲醛在一定条件下反应可生成三聚甲醛,该反应符合加成反应特点,则三分子乙醛在一定条件下反应可生成三聚乙醛,三聚乙醛的结构应该为,故C正确;
D.三聚甲醛的分子式为C3H6O3,根据原子守恒知,如果完全燃烧生成二氧化碳和水的物质的量相等,如果生成CO,则生成的二氧化碳和水的物质的量不等,故D错误;
故选C。
【点睛】本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系、物质结构特点及基本概念是解本题关键。本题的易错选项是D,易忽略不完全燃烧而导致错误。
22.BD
【详解】A.根据图中信息得到反应①的化学方程式为, A正确;
B.根据关系式HCHO~4Ag,30g的b物质(物质的量为1mol)与足量银氨溶液反应可生成4molAg即432gAg,故B错误;
C.b(HCHO)与c(HOCH2COCH2OH)通式相同,因此等质量的b(HCHO)与c(HOCH2COCH2OH)物质完全燃烧,消耗氧气的量相同,故C正确;
D.淀粉属于多糖,分子式为,是混合物,故D错误。
综上所述,答案为BD。
23.错误
【详解】1molHCHO与足量银氨溶液在水浴加热条件下充分反应,最多生成4molAg,错误;
24.(1) 水浴加热 H2
(2) 分液漏斗 除去CO中混有的HCOOH蒸气 2∶1
(3)方案一:溶于氨水,向所得溶液中通入空气(或通入氧气或在空气中放置一段时间),观察溶液变蓝色;方案二:将样品溶于硫酸,观察到溶液呈蓝色
(4)2HCHO+Cu(OH)2 +2NaOHCu+2HCOONa+2H2O+H2↑
【详解】(1)①控制温度在40~50℃,低于水的沸点,所以可以采用水浴加热。②气体X能燃烧且完全燃烧后产物不会使澄清石灰水变浑浊,根据原子守恒可知该气体应为H2。答案:水浴加热;H2;
(2)浓硫酸与反应液反应,若甲醛被氧化为HCOONa,则浓硫酸会与其反应生成CO,由于甲酸具有挥发性且能与银氨溶液反应,应先将其除去,再通入银氨溶液,银氨溶液中出现黑色沉淀,说明有CO生成,进而说明甲醛被氧化为HCOONa,气球可以收集尾气。①仪器a为分液漏斗。②甲酸具有挥发性,且含有结构,能和银氨溶液反应,所以需要用NaOH溶液除去CO中混有的HCOOH蒸气。③银氨溶液中出现黑色沉淀,说明CO将银氨溶液还原为银单质,氧化剂为[Ag(NH3)]+,还原剂为CO,根据得失电子守恒,可知氧化剂与还原剂的物质的量之比为2∶1。
答案:分液漏斗;除去CO中混有的HCOOH蒸气;2∶1;
(3)红色沉淀可能为Cu或CuO或二者都有,因为Cu不溶于氨水或硫酸,若红色固体中含有Cu2O,则固体溶于氨水得无色溶液,在空气中放置一段时间后, 遇空气容易被氧化成(蓝色),溶液变蓝色,或将Cu2O溶于硫酸,Cu2O发生歧化反应,得到CuSO4蓝色溶液和单质Cu,答案:方案一:溶于氨水,向所得溶液中通入空气(或通入氧气或在空气中放置一段时间),观察溶液变蓝色;方案二:将样品溶于硫酸,观察到溶液呈蓝色;
(4)根据上述分析可知,甲醛与新制的Cu(OH)反应生成的气体为H2,甲醛与新制氢氧化铜、氢氧化钠溶液反应生成等物质的量的和H2,根据得失电子守恒和原子守恒可写出该反应的化学方程式:2HCHO+Cu(OH)2+2NaOHCu+2HCOONa+2H2O+H2↑。
25.(1) 甲醛 易 D
(2)大型绿色植物晚上通过呼吸作用会消耗大量氧气
【解析】(1)
内装修材料及家具挥发出来的甲醛是室内空气的主要污染物,该气体易溶于水,常温下有强烈的刺激性气味。装修尽可能选择在温度较高的季节,入住前房间内保持一定温度并通风并请环境监测部门检测室内甲醛含量低于国家标准后入住,不能紧闭门窗一段时间后入住。
(2)
大型绿色植物晚上通过呼吸作用会消耗大量氧气,晚上在密闭的居室内放置大型绿色植物会影响健康。
26. HO—CH2—CH2—CH2—CH2—OH 酯 HC≡CH+2HCHOHOCH2C≡CCH2OH 加成反应 CH2=CH—COOCH3+NaOH→CH2=CH—COONa+CH3OH
【分析】甲醇在Cu作催化剂、加热条件被氧气氧化生成甲醛(HCHO),则A为HCHO,结合A、B的分子式可知,B为3分子甲醛形成,B分子结构为六元环状化合物,B分子结构中只有一种氢、一种氧、一种碳,应是3分子甲醛之间的加成反应生成B,则B为;由E→F的转化及F分子式可知,E中含有4个C原子,由HCHO+D→E,再根据已知反应信息可知,该反应为2分子甲醛与乙炔发生加成反应,D为HC≡CH,E为HOCH2-C≡C-CH2OH,E与氢气发生加成反应生成F,F与二元羧酸通过酯化反应形成高聚物PBT,据此分析解答。
【详解】(1)甲醇氧化生成甲醛(HCHO),结合A、B的分子式可知,B为3分子甲醛形成,B分子结构为六元环状化合物,B分子结构中只有一种氢、一种氧、一种碳,应是3分子甲醛之间的加成反应生成B,则B的结构简式为:;B的同分异构体与葡萄糖结构类似,该异构体中含有1个-CHO,2个羟基-OH,为链状结构,该同分异构体的结构简式为,故答案为;;
(2)由E→F的转化及F分子式可知,E中含有4个C原子,由HCHO+D→E,再根据已知反应信息可知,该反应为2分子甲醛与乙炔发生加成反应,D为HC≡CH,E为HOCH2-C≡C-CH2OH,E与氢气发生加成反应生成F,故F结构简式为HO-CH2-CH2-CH2-CH2-OH,F与二元羧酸通过酯化反应形成高聚物PBT,PBT属于酯类,故答案为HO-CH2-CH2-CH2-CH2-OH;酯;
(3)由(2)中分析可知,该反应为该反应为2分子甲醛与乙炔发生加成反应生成HOCH2-C≡C-CH2OH,由A、D生成E的反应方程式为:HC≡CH+2HCHO HOCH2C≡CCH2OH,故答案为HC≡CH+2HCHO HOCH2C≡CCH2OH;加成反应;
(4)HOCH2-C≡C-CH2OH的同分异构体G不能发生银镜反应,分子中不含醛基-CHO或-OOCH,能使溴水褪色,含有不饱和键,能水解且产物的碳原子数不等,含有酯基,故含有1个C=C双键、1个酯基,且形成该酯的羧酸含有3个碳原子,醇为甲醇,故G的结构简式为:CH2=CH-COOCH3,CH2=CH-COOCH3在氢氧化钠溶液中发生水解方程式为:
CH2=CH-COOCH3+NaOH→CH2=CH-COONa+CH3OH,故答案为CH2=CH-COOCH3+NaOH→CH2=CH-COONa+CH3OH。
