3.1.3铁盐和亚铁盐 学案(含解析)
文档属性
| 名称 | 3.1.3铁盐和亚铁盐 学案(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 642.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-04 00:00:00 | ||
图片预览




文档简介
3.1.3铁盐和亚铁盐
1. 掌握铁离子和亚铁离子的相关性质。
2. 掌握铁离子和亚铁离子的鉴别。
我们已经知道了铁离子 (Fe3+) 在溶液中呈黄色,亚铁离子 (Fe2+) 在溶液中呈浅绿色。除此之外它们还具有哪些性质呢?
一、铁离子 (Fe3+) 的氧化性
Fe3+ 处于较高价态,有较强的氧化性,可以与一些金属以及一些还原性的离子发生反应。
1.与金属反应
Fe 与 FeCl3 的反应:2FeCl3+Fe=3FeCl2,离子方程式为:
2Fe3+ +Fe = 3Fe2+。
Cu 与 FeCl3 的反应:2FeCl3+Cu=2FeCl2+CuCl2,离子方程式为:
2Fe3+ +Cu = 2Fe2+ +Cu2+。
2.与还原性离子的反应
除了以上反应之外,Fe3+ 还可以氧化 I-、SO32- 等,Fe3+ 均被还原为 Fe2+。
2Fe3++2I-=2Fe2++I2
2Fe3++SO32- +H2O=2Fe2++SO42- +2H+
二、亚铁离子 (Fe2+) 的还原性
Fe2+ 处于较低价态,在反应中常体现出强还原性,很容易被氧化剂 (如 Cl2、O2、KMnO4 等) 氧化,如氯化亚铁溶液中通入氯气:
2FeCl2+Cl2=2FeCl3
题型演练
1.(2021·高一课时练习)已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是
A.3Cl2+6FeI2=2FeCl3+4FeI3
B.Cl2+FeI2=FeCl2+I2
C.Co2O3+6HCl(浓)=2CoCl2+Cl2↑+3H2O
D.2Fe3++2I-=2Fe2++I2
2.(2021·高一课时练习)下列说法中,不正确的是( )
A.FeCl3溶液和FeCl2溶液都是黄色的
B.Fe(OH)2是白色的,Fe(OH)3是红褐色的
C.FeO、 Fe2O3都能与盐酸反应
D.FeCl3溶液、FeCl2溶液都能与NaOH溶液反应
3.(2022秋·高一课时练习)向盛有2mLFeCl3溶液的试管中加入少量铁粉,进行如下实验。下列分析正确的是
A.只加入KSCN溶液可检验试管1中是否含有Fe2+
B.试管2中无现象,则表明试管1中溶液不含Fe3+
C.试管3中的离子反应为:Fe2++Cl2=Fe3++2Cl-
D.试管3中必定有红色沉淀生成
4.(2022·高一课时练习)欲证明某溶液中不含而含有,下列实验操作顺序正确的是
①加入足量新制氯水②加入足量溶液③加入少量溶液
A.①③ B.③② C.③① D.①②③
5.(2021·高一课时练习)为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现象、实验结论及离子方程式均正确的是
选项 实验操作 实验现象 实验结论 离子方程式
A 向溶液中加入片 浅绿色溶液变为无色,溶液中有黑色固体生成 具有还原性
B 向溶液中滴加新制氯水 浅绿色溶液变为棕黄色 具有还原性
C 向溶液中加入铁粉 棕黄色溶液变为浅绿色 具有还原性
D 向溶液中加入铜粉 蓝色溶液变为棕黄色 具有氧化性
A.A B.B C.C D.D
6.(2021·高一课时练习)下列关于铁及其化合物的说法错误的是
A.若FeCl2溶液中混有FeCl3可通过滴加氯水除去
B.可用KSCN溶液检验FeCl2溶液是否变质
C.实验室保存FeCl2溶液时常加入铁粉
D.向FeCl2溶液中加入NaOH溶液,最终可观察到红褐色沉淀
7.(2021·高一课时练习)下列关于Fe3+的叙述中,错误的是
A.Fe3+不可能大量存在于碱性溶液中
B.Fe3+水溶液中加入氢氧化钠溶液产生红褐色沉淀
C.Fe3+具有氧化性,能与金属锌、铁、铜等反应
D.Fe3+溶液中滴入含硫氰化钾的溶液,有红色沉淀产生
8.(2022·高一课时练习)为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其中结论正确的是
A.若滴加KSCN溶液,溶液变红,说明铁粉变质
B.若滴加KSCN溶液,溶液未变红,说明铁粉未变质
C.若依次滴加氯水,KSCN溶液,溶液变红,说明铁粉全部变质
D.若滴加KSCN溶液,溶液未变红;再滴加氯水,溶液变红,说明铁粉全部变质
9.(2022秋·高一课时练习)以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是
A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素
B.人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血
C.过滤步骤说明硫酸亚铁晶体难溶于水
D.实验过程不直接蒸发结晶的原因是防止FeSO4水解生成Fe(OH)2
10.(2022秋·高一课时练习)能验证某溶液中含有,不含的实验事实是
A.向溶液中滴加溶液,溶液变红
B.向溶液中滴加溶液,无明显变化;再滴加几滴氯水,溶液变红
C.向溶液中依次滴加氯水、溶液,溶液变红
D.向溶液中滴加少量溶液,产生红褐色沉淀
三、铁离子与亚铁离子的鉴别方法
题型演练
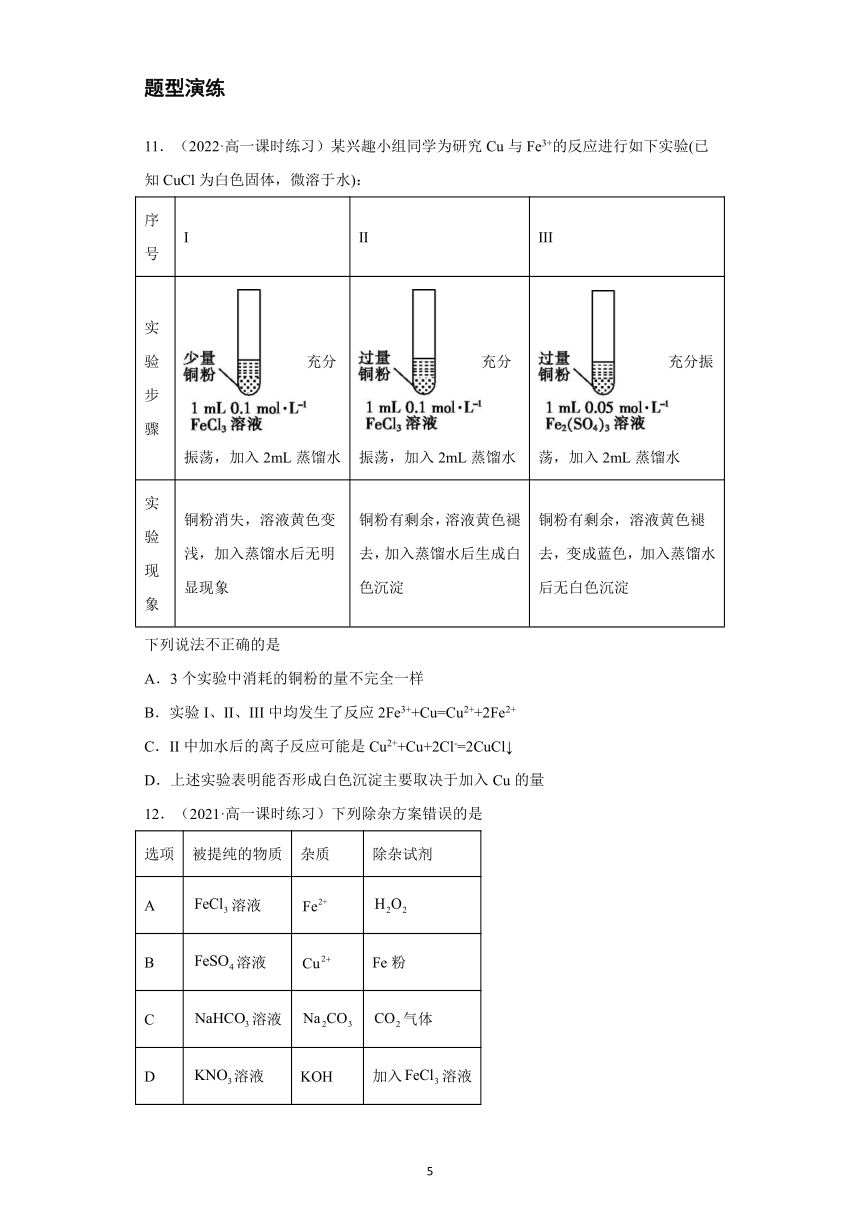
11.(2022·高一课时练习)某兴趣小组同学为研究Cu与Fe3+的反应进行如下实验(已知CuCl为白色固体,微溶于水):
序号 I II III
实验步骤 充分振荡,加入2mL蒸馏水 充分振荡,加入2mL蒸馏水 充分振荡,加入2mL蒸馏水
实验现象 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀
下列说法不正确的是
A.3个实验中消耗的铜粉的量不完全一样
B.实验I、II、III中均发生了反应2Fe3++Cu=Cu2++2Fe2+
C.II中加水后的离子反应可能是Cu2++Cu+2Cl-=2CuCl↓
D.上述实验表明能否形成白色沉淀主要取决于加入Cu的量
12.(2021·高一课时练习)下列除杂方案错误的是
选项 被提纯的物质 杂质 除杂试剂
A 溶液
B 溶液 Fe粉
C 溶液 气体
D 溶液 KOH 加入溶液
A.A B.B C.C D.D
13.(2022·高一课时练习)下列除杂的操作不正确的是
A.溶液中混有少量:加入足量镁充分反应后过滤
B.溶液中混有少量:加入过量铁粉充分反应后过滤
C.溶液中混有少量:加入NaOH溶液充分反应后过滤
D.溶液中混有少量:加入过量铁粉充分反应后过滤
14.(2022·高一课时练习)下列有关铁及其化合物的说法正确的是
A.铁与水蒸气在高温下的反应产物为Fe2O3和H2
B.向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
C.配制FeSO4溶液时,可在溶液中加入少量铁粉
D.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入Cu粉,然后过滤
15.(2021·高一课时练习)按如图所示的方法进行实验,下列有关说法错误的是
A.①中反应的离子方程式为
B.②中加入溶液后溶液不变红
C.③中加入新制氯水后溶液变红
D.氧化性:
16.(2022·高一课时练习)电子工业常用FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某研究小组同学为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,设计了如图流程:
请回答:
(1)FeCl3溶液与铜箔反应,生成FeCl2和CuCl2,反应的离子方程式是___________,若反应过程中有2mol电子发生转移,会有___________g铜溶解。
(2)①~③所涉及的实验操作方法中,属于过滤的是___________(填序号)。①中发生反应的离子方程式是___________。
(3)气体C的化学式是___________,检验FeCl3溶液中金属阳离子的操作和现象是___________。
(4)①中反应消耗铁粉11.2g,废液中Fe3+的物质的量浓度是___________。
试卷第1页,共3页
参考答案:
1.A
【分析】根据氧化还原反应中,氧化性:氧化剂>氧化产物,以此对下列方程式进行判断。
【详解】A.由于I-的还原性强于Fe2+,所以Cl2应先氧化I-,而不应先氧化Fe2+,A错误;
B.Cl2氧化性强于I2,反应方程式正确,B正确;
C.氧化性Co2O3>Cl2,反应方程式正确,C正确;
D.氧化性Fe3+>I2,反应方程式正确,D正确;
故答案选A。
2.A
【详解】A.FeCl3溶液是黄色的,FeCl2溶液是浅绿色的,A项错误;
B.Fe(OH)2是白色的,Fe(OH)3是红褐色的,B项正确;
C.FeO、 Fe2O3都是金属氧化物,金属氧化物一般都能与盐酸反应,C项正确;
D.FeCl3溶液、FeCl2溶液与NaOH溶液反应分别生成氢氧化铁沉淀和氢氧化亚铁沉淀,故FeCl3溶液、FeCl2溶液都能与NaOH溶液反应,D项正确;
答案选A。
3.B
【详解】A.加入KSCN溶液可检验Fe3+,故A错误;
B.加入KSCN溶液可检验Fe3+,试管2中无现象,则表明试管1中溶液不含Fe3+,故B正确;
C.试管3中的离子反应为:2Fe2++Cl2=2Fe3++2Cl-,故C错误;
D.试管3中加入氯水将Fe2+氧化为Fe3+,试管2中上层清液含KSCN溶液,与Fe3+结合生成血红色配合物,不是沉淀,故D错误;
故选:B。
4.C
【详解】先加入溶液,溶液不变红,证明原溶液中不含,再加入足量新制氯水,溶液变红,证明原溶液中含有,故选:C。
5.B
【详解】A.锌具有还原性,氯化亚铁溶液中价的铁具有氧化性,能氧化锌,A错误;
B.氯化亚铁溶液为浅绿色,向氯化亚铁溶液中滴加新制氯水,价的铁被氯水氧化,生成价的铁,溶液由浅绿色变为棕黄色,离子方程式正确,B正确;
C.向溶液中加入铁粉,发生反应生成氯化亚铁,棕黄色溶液变为浅绿色,离子方程式为,C错误;
D.反应前氯化铁溶液为棕黄色,具有氧化性,与铜发生反应生成氯化亚铁和氯化铜,氯化亚铁溶液为浅绿色,氯化铜溶液为蓝绿色,离子方程式为,D错误;
故答案为:B。
6.A
【详解】A.氯气与氯化铁不反应,但是氯气能够氧化亚铁离子生成铁离子,所以应该用铁粉除去氯化亚铁中的铁离子,故A错误;
B.KSCN溶液与铁离子反应生成硫氰化铁而呈现血红色,亚铁离子与硫氰化钾溶液不反应,所以可用KSCN溶液检验FeCl2溶液是否变质,故B正确;
C.亚铁离子不稳定,易被氧化生成铁离子,铁能够还原铁离子为亚铁离子;所以实验室为防止氯化亚铁被氧化,在保存FeCl2溶液时常加入铁粉,故C正确;
D.氢氧化亚铁能够被空气氧化生成红褐色氢氧化铁,所以向FeCl2溶液中加入NaOH溶液,先生成白色沉淀,立即转化为灰绿色,最终转化为红褐色沉淀,所以最终可观察到红褐色沉淀,故D正确;
故选A。
7.D
【详解】A.Fe3+能与碱反应生成氢氧化铁红褐色沉淀,在碱性溶液中不可能存在,故A正确;
B.Fe3+能与碱反应生成氢氧化铁红褐色沉淀,Fe3+水溶液中加入氢氧化钠溶液产生红褐色沉淀,故B正确;
C.Fe3+具有氧化性,能与金属锌、铁、铜等还原剂反应,生成Fe或Fe2+,故C正确;
D.Fe3+溶液中加入含硫氰化钾的溶液,其溶液变为血红色,无红色沉淀生成,故D错误;
故答案为D。
8.A
【详解】A.滴加KSCN溶液,溶液变红,说明溶液中含有Fe3+,故还原铁粉即Fe变质,故A选项正确;
B.滴加KSCN溶液,溶液未变红,说明溶液中不含Fe3+,但溶液中可能含Fe2+,不能说明铁粉未变质,故B选项错误;
C.滴加氯水时可能把溶液中存在的Fe2+氧化成了Fe3+,再滴加硫氰化钾溶液,溶液变红,则不能说明铁粉全部变质,故C选项错误;
D.若先滴加KSCN溶液,溶液未变红,说明溶液中不含Fe3+,再滴加氯水,溶液变红说明溶液中存在Fe2+,被氯水氧化成了Fe3+,但不能说明铁粉全部变质,故D选项错误。
故选A选项。
9.B
【分析】废铁屑用稀硫酸酸浸后得到FeSO4溶液,FeSO4溶液经结晶、过滤得到硫酸亚铁晶体。
【详解】A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明酸浸后的溶液中不存在Fe3+,但不能说明废铁屑中不含+3价铁元素,因为废铁屑中若含+3价铁元素,在酸浸时会被Fe还原成Fe2+,A项错误;
B.人体血红素是亚铁离子配合物,硫酸亚铁可提供亚铁离子,从而可用于治疗缺铁性贫血,B项正确;
C.硫酸亚铁晶体溶于水,题给实验过程中是经结晶析出晶体后过滤的,C项错误;
D.实验过程不直接蒸发结晶的原因是:防止硫酸亚铁被氧化、防止硫酸亚铁晶体失去结晶水,D项错误;
答案选B。
10.B
【详解】A.向溶液中滴加溶液,溶液变红,说明含,故不选A;
B.向溶液中滴加溶液,无明显变化,说明不含;再滴加几滴氯水,溶液变红,说明被氯气氧化为,故选B;
C.氯水能把氧化为,向溶液中依次滴加氯水,溶液,溶液变红,说明溶液中含有或,故不选C;
D.和OH-反应生成红褐色氢氧化铁沉淀,向溶液中滴加少量溶液,产生红褐色沉淀,证明含有,故不选D;
选B。
11.D
【详解】A.实验Ⅱ中Cu部分转化为Cu(I)消耗的铜粉多于其它两个实验,选项A正确;
B.实验Ⅰ、Ⅱ、Ⅲ中溶液黄色均褪去,推测都发生了反应2Fe3++Cu=Cu2++2Fe2+,选项B正确;
C.Ⅱ中加水后生成白色沉淀,根据元素种类推测应为CuCl,可能的离子反应Cu2++Cu+2Cl-=2CuCl↓,选项C正确;
D.实验Ⅱ、Ⅲ均加入过量的铜,后者未产生白色沉淀,表明能否形成白色沉淀由Cu的量和Cl-的浓度共同决定,选项D不正确。
答案选D。
12.D
【详解】A.Fe2+具有还原性,加入H2O2,可以将Fe2+氧化为Fe3+,而且H2O2的还原产物为水,不会引入新杂质,故A正确;
B.铁的还原性大于铜,混合液中加入足量的铁粉,反应生成铜和硫酸亚铁,过滤后得到铜和铁粉的混合物,滤液为纯净的硫酸亚铁溶液,故B正确;
C.碳酸钠溶液与足量的二氧化碳反应生成碳酸氢钠,能够除去杂质且不引入新杂质,故C正确;
D.除去KNO3溶液中的KOH,加入FeCl3溶液,虽然能生成Fe(OH)3沉淀,但引入了新杂质Cl-,故D错误;
故选D。
13.C
【详解】A.镁与FeCl3反应生成FeCl2,过量镁可与氯化亚铁发生置换反应置换出Fe,可除去杂质,所以A选项是正确的;
B.铁与FeCl3反应生成FeCl2,可除去杂质,所以B选项是正确的;
C.加入NaOH溶液,Cu2+、Fe3+均转化成氢氧化物沉淀,不符合除杂要求,故C错误;
D.铁与反应生成FeCl2,可除去杂质,所以D选项是正确的。
故答案选C。
14.C
【详解】A.铁与水蒸气在高温下的反应产物为Fe3O4和H2,故A错误;
B.FeCl3溶液中滴加过量氨水生成Fe(OH)3沉淀,所以不能用饱和FeCl3溶液与过量氨水制取Fe(OH)3胶体,故B错误;
C.配制硫酸亚铁溶液时,为防止产生Fe3+,可在溶液中加入少量铁粉,为了抑制亚铁离子被氧化而变质,故C正确;
D.Fe与氯化铁反应生成氯化亚铁,则加铁粉、过滤除去FeCl2溶液中的FeCl3杂质,故D错误。
故选C。
15.AD
【详解】A.①中反应的离子方程式为,故A错误;
B.①中为过量铁粉与反应,则②中无,故加入溶液后,溶液不变红,故B正确;
C.②中含有和,③中滴加新制氯水后,则被氧化为,溶液变红,故C正确;
D.同一个氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,则由③可知氧化性:,由①可知氧化性,故D错误;
故答案为AD。
16.(1) 2Fe3++Cu=2Fe2++Cu2+ 64
(2) ①② 2Fe3++Fe=3Fe2+、Cu2++Fe=Cu+Fe2+
(3) Cl2 取少量溶液于试管中,滴加几滴KSCN溶液,若出现红色,证明有Fe3+
(4)0.4mol/L
【分析】Cu和FeCl3发生反应Cu+2FeCl3=2FeCl2+2CuCl2,所以废液中含有Cu2+、Fe2+,可能含有Fe3+,向废液中加入过量Fe粉,发生反应2Fe3++Fe=3Fe2+、Cu2++Fe=Fe2++Cu,然后过滤,固体A中含有Fe、Cu,溶液A中含有FeCl2,向固体A中加入过量稀盐酸,发生反应Fe+2HCl=FeCl2+H2↑,然后过滤,得到的6.4g固体B是Cu,溶液B中含有HCl、FeCl2,将滤液②⑤混合,然后通入Cl2,发生反应2FeCl2+Cl2=2FeCl3,所以得到氯化铁溶液,以此解题。
(1)
FeCl3溶液与铜箔反应,生成FeCl2和CuCl2,反应的离子方程式:2Fe3++Cu═2Fe2++Cu2+,该反应中电子转移2mol,反应铜1mol,质量为64g;
(2)
过滤后得到滤液和固体,由流程图可知,①~③所涉及的实验操作方法中,属于过滤的是①②;①中加入铁粉和废液中的三价铁离子和铜离子反应生成二价铁,发生反应的离子方程式是2Fe3++Fe=3Fe2+、Cu2++Fe=Cu+Fe2+;
(3)
由分析可知气体C为氯气,氯气的化学式是:Cl2;三价铁遇到硫氰化钾显红色,故检验FeCl3溶液中金属阳离子的操作和现象是:取少量溶液于试管中,滴加几滴KSCN溶液,若出现红色,证明有Fe3+;
(4)
①中反应消耗铁粉11.2g,物质的量==0.2mol,2Fe3++Fe=3Fe2+、Cu2++Fe=Cu+Fe2+,其中铜离子物质的量==0.1mol,消耗铁0.1mol,则和铁离子反应的铁0.1mol,消耗铁离子物质的量0.2mol,废液中Fe3+的物质的量浓度==0.4mol/L。
1. 掌握铁离子和亚铁离子的相关性质。
2. 掌握铁离子和亚铁离子的鉴别。
我们已经知道了铁离子 (Fe3+) 在溶液中呈黄色,亚铁离子 (Fe2+) 在溶液中呈浅绿色。除此之外它们还具有哪些性质呢?
一、铁离子 (Fe3+) 的氧化性
Fe3+ 处于较高价态,有较强的氧化性,可以与一些金属以及一些还原性的离子发生反应。
1.与金属反应
Fe 与 FeCl3 的反应:2FeCl3+Fe=3FeCl2,离子方程式为:
2Fe3+ +Fe = 3Fe2+。
Cu 与 FeCl3 的反应:2FeCl3+Cu=2FeCl2+CuCl2,离子方程式为:
2Fe3+ +Cu = 2Fe2+ +Cu2+。
2.与还原性离子的反应
除了以上反应之外,Fe3+ 还可以氧化 I-、SO32- 等,Fe3+ 均被还原为 Fe2+。
2Fe3++2I-=2Fe2++I2
2Fe3++SO32- +H2O=2Fe2++SO42- +2H+
二、亚铁离子 (Fe2+) 的还原性
Fe2+ 处于较低价态,在反应中常体现出强还原性,很容易被氧化剂 (如 Cl2、O2、KMnO4 等) 氧化,如氯化亚铁溶液中通入氯气:
2FeCl2+Cl2=2FeCl3
题型演练
1.(2021·高一课时练习)已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是
A.3Cl2+6FeI2=2FeCl3+4FeI3
B.Cl2+FeI2=FeCl2+I2
C.Co2O3+6HCl(浓)=2CoCl2+Cl2↑+3H2O
D.2Fe3++2I-=2Fe2++I2
2.(2021·高一课时练习)下列说法中,不正确的是( )
A.FeCl3溶液和FeCl2溶液都是黄色的
B.Fe(OH)2是白色的,Fe(OH)3是红褐色的
C.FeO、 Fe2O3都能与盐酸反应
D.FeCl3溶液、FeCl2溶液都能与NaOH溶液反应
3.(2022秋·高一课时练习)向盛有2mLFeCl3溶液的试管中加入少量铁粉,进行如下实验。下列分析正确的是
A.只加入KSCN溶液可检验试管1中是否含有Fe2+
B.试管2中无现象,则表明试管1中溶液不含Fe3+
C.试管3中的离子反应为:Fe2++Cl2=Fe3++2Cl-
D.试管3中必定有红色沉淀生成
4.(2022·高一课时练习)欲证明某溶液中不含而含有,下列实验操作顺序正确的是
①加入足量新制氯水②加入足量溶液③加入少量溶液
A.①③ B.③② C.③① D.①②③
5.(2021·高一课时练习)为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现象、实验结论及离子方程式均正确的是
选项 实验操作 实验现象 实验结论 离子方程式
A 向溶液中加入片 浅绿色溶液变为无色,溶液中有黑色固体生成 具有还原性
B 向溶液中滴加新制氯水 浅绿色溶液变为棕黄色 具有还原性
C 向溶液中加入铁粉 棕黄色溶液变为浅绿色 具有还原性
D 向溶液中加入铜粉 蓝色溶液变为棕黄色 具有氧化性
A.A B.B C.C D.D
6.(2021·高一课时练习)下列关于铁及其化合物的说法错误的是
A.若FeCl2溶液中混有FeCl3可通过滴加氯水除去
B.可用KSCN溶液检验FeCl2溶液是否变质
C.实验室保存FeCl2溶液时常加入铁粉
D.向FeCl2溶液中加入NaOH溶液,最终可观察到红褐色沉淀
7.(2021·高一课时练习)下列关于Fe3+的叙述中,错误的是
A.Fe3+不可能大量存在于碱性溶液中
B.Fe3+水溶液中加入氢氧化钠溶液产生红褐色沉淀
C.Fe3+具有氧化性,能与金属锌、铁、铜等反应
D.Fe3+溶液中滴入含硫氰化钾的溶液,有红色沉淀产生
8.(2022·高一课时练习)为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其中结论正确的是
A.若滴加KSCN溶液,溶液变红,说明铁粉变质
B.若滴加KSCN溶液,溶液未变红,说明铁粉未变质
C.若依次滴加氯水,KSCN溶液,溶液变红,说明铁粉全部变质
D.若滴加KSCN溶液,溶液未变红;再滴加氯水,溶液变红,说明铁粉全部变质
9.(2022秋·高一课时练习)以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是
A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素
B.人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血
C.过滤步骤说明硫酸亚铁晶体难溶于水
D.实验过程不直接蒸发结晶的原因是防止FeSO4水解生成Fe(OH)2
10.(2022秋·高一课时练习)能验证某溶液中含有,不含的实验事实是
A.向溶液中滴加溶液,溶液变红
B.向溶液中滴加溶液,无明显变化;再滴加几滴氯水,溶液变红
C.向溶液中依次滴加氯水、溶液,溶液变红
D.向溶液中滴加少量溶液,产生红褐色沉淀
三、铁离子与亚铁离子的鉴别方法
题型演练
11.(2022·高一课时练习)某兴趣小组同学为研究Cu与Fe3+的反应进行如下实验(已知CuCl为白色固体,微溶于水):
序号 I II III
实验步骤 充分振荡,加入2mL蒸馏水 充分振荡,加入2mL蒸馏水 充分振荡,加入2mL蒸馏水
实验现象 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀
下列说法不正确的是
A.3个实验中消耗的铜粉的量不完全一样
B.实验I、II、III中均发生了反应2Fe3++Cu=Cu2++2Fe2+
C.II中加水后的离子反应可能是Cu2++Cu+2Cl-=2CuCl↓
D.上述实验表明能否形成白色沉淀主要取决于加入Cu的量
12.(2021·高一课时练习)下列除杂方案错误的是
选项 被提纯的物质 杂质 除杂试剂
A 溶液
B 溶液 Fe粉
C 溶液 气体
D 溶液 KOH 加入溶液
A.A B.B C.C D.D
13.(2022·高一课时练习)下列除杂的操作不正确的是
A.溶液中混有少量:加入足量镁充分反应后过滤
B.溶液中混有少量:加入过量铁粉充分反应后过滤
C.溶液中混有少量:加入NaOH溶液充分反应后过滤
D.溶液中混有少量:加入过量铁粉充分反应后过滤
14.(2022·高一课时练习)下列有关铁及其化合物的说法正确的是
A.铁与水蒸气在高温下的反应产物为Fe2O3和H2
B.向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
C.配制FeSO4溶液时,可在溶液中加入少量铁粉
D.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入Cu粉,然后过滤
15.(2021·高一课时练习)按如图所示的方法进行实验,下列有关说法错误的是
A.①中反应的离子方程式为
B.②中加入溶液后溶液不变红
C.③中加入新制氯水后溶液变红
D.氧化性:
16.(2022·高一课时练习)电子工业常用FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某研究小组同学为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,设计了如图流程:
请回答:
(1)FeCl3溶液与铜箔反应,生成FeCl2和CuCl2,反应的离子方程式是___________,若反应过程中有2mol电子发生转移,会有___________g铜溶解。
(2)①~③所涉及的实验操作方法中,属于过滤的是___________(填序号)。①中发生反应的离子方程式是___________。
(3)气体C的化学式是___________,检验FeCl3溶液中金属阳离子的操作和现象是___________。
(4)①中反应消耗铁粉11.2g,废液中Fe3+的物质的量浓度是___________。
试卷第1页,共3页
参考答案:
1.A
【分析】根据氧化还原反应中,氧化性:氧化剂>氧化产物,以此对下列方程式进行判断。
【详解】A.由于I-的还原性强于Fe2+,所以Cl2应先氧化I-,而不应先氧化Fe2+,A错误;
B.Cl2氧化性强于I2,反应方程式正确,B正确;
C.氧化性Co2O3>Cl2,反应方程式正确,C正确;
D.氧化性Fe3+>I2,反应方程式正确,D正确;
故答案选A。
2.A
【详解】A.FeCl3溶液是黄色的,FeCl2溶液是浅绿色的,A项错误;
B.Fe(OH)2是白色的,Fe(OH)3是红褐色的,B项正确;
C.FeO、 Fe2O3都是金属氧化物,金属氧化物一般都能与盐酸反应,C项正确;
D.FeCl3溶液、FeCl2溶液与NaOH溶液反应分别生成氢氧化铁沉淀和氢氧化亚铁沉淀,故FeCl3溶液、FeCl2溶液都能与NaOH溶液反应,D项正确;
答案选A。
3.B
【详解】A.加入KSCN溶液可检验Fe3+,故A错误;
B.加入KSCN溶液可检验Fe3+,试管2中无现象,则表明试管1中溶液不含Fe3+,故B正确;
C.试管3中的离子反应为:2Fe2++Cl2=2Fe3++2Cl-,故C错误;
D.试管3中加入氯水将Fe2+氧化为Fe3+,试管2中上层清液含KSCN溶液,与Fe3+结合生成血红色配合物,不是沉淀,故D错误;
故选:B。
4.C
【详解】先加入溶液,溶液不变红,证明原溶液中不含,再加入足量新制氯水,溶液变红,证明原溶液中含有,故选:C。
5.B
【详解】A.锌具有还原性,氯化亚铁溶液中价的铁具有氧化性,能氧化锌,A错误;
B.氯化亚铁溶液为浅绿色,向氯化亚铁溶液中滴加新制氯水,价的铁被氯水氧化,生成价的铁,溶液由浅绿色变为棕黄色,离子方程式正确,B正确;
C.向溶液中加入铁粉,发生反应生成氯化亚铁,棕黄色溶液变为浅绿色,离子方程式为,C错误;
D.反应前氯化铁溶液为棕黄色,具有氧化性,与铜发生反应生成氯化亚铁和氯化铜,氯化亚铁溶液为浅绿色,氯化铜溶液为蓝绿色,离子方程式为,D错误;
故答案为:B。
6.A
【详解】A.氯气与氯化铁不反应,但是氯气能够氧化亚铁离子生成铁离子,所以应该用铁粉除去氯化亚铁中的铁离子,故A错误;
B.KSCN溶液与铁离子反应生成硫氰化铁而呈现血红色,亚铁离子与硫氰化钾溶液不反应,所以可用KSCN溶液检验FeCl2溶液是否变质,故B正确;
C.亚铁离子不稳定,易被氧化生成铁离子,铁能够还原铁离子为亚铁离子;所以实验室为防止氯化亚铁被氧化,在保存FeCl2溶液时常加入铁粉,故C正确;
D.氢氧化亚铁能够被空气氧化生成红褐色氢氧化铁,所以向FeCl2溶液中加入NaOH溶液,先生成白色沉淀,立即转化为灰绿色,最终转化为红褐色沉淀,所以最终可观察到红褐色沉淀,故D正确;
故选A。
7.D
【详解】A.Fe3+能与碱反应生成氢氧化铁红褐色沉淀,在碱性溶液中不可能存在,故A正确;
B.Fe3+能与碱反应生成氢氧化铁红褐色沉淀,Fe3+水溶液中加入氢氧化钠溶液产生红褐色沉淀,故B正确;
C.Fe3+具有氧化性,能与金属锌、铁、铜等还原剂反应,生成Fe或Fe2+,故C正确;
D.Fe3+溶液中加入含硫氰化钾的溶液,其溶液变为血红色,无红色沉淀生成,故D错误;
故答案为D。
8.A
【详解】A.滴加KSCN溶液,溶液变红,说明溶液中含有Fe3+,故还原铁粉即Fe变质,故A选项正确;
B.滴加KSCN溶液,溶液未变红,说明溶液中不含Fe3+,但溶液中可能含Fe2+,不能说明铁粉未变质,故B选项错误;
C.滴加氯水时可能把溶液中存在的Fe2+氧化成了Fe3+,再滴加硫氰化钾溶液,溶液变红,则不能说明铁粉全部变质,故C选项错误;
D.若先滴加KSCN溶液,溶液未变红,说明溶液中不含Fe3+,再滴加氯水,溶液变红说明溶液中存在Fe2+,被氯水氧化成了Fe3+,但不能说明铁粉全部变质,故D选项错误。
故选A选项。
9.B
【分析】废铁屑用稀硫酸酸浸后得到FeSO4溶液,FeSO4溶液经结晶、过滤得到硫酸亚铁晶体。
【详解】A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明酸浸后的溶液中不存在Fe3+,但不能说明废铁屑中不含+3价铁元素,因为废铁屑中若含+3价铁元素,在酸浸时会被Fe还原成Fe2+,A项错误;
B.人体血红素是亚铁离子配合物,硫酸亚铁可提供亚铁离子,从而可用于治疗缺铁性贫血,B项正确;
C.硫酸亚铁晶体溶于水,题给实验过程中是经结晶析出晶体后过滤的,C项错误;
D.实验过程不直接蒸发结晶的原因是:防止硫酸亚铁被氧化、防止硫酸亚铁晶体失去结晶水,D项错误;
答案选B。
10.B
【详解】A.向溶液中滴加溶液,溶液变红,说明含,故不选A;
B.向溶液中滴加溶液,无明显变化,说明不含;再滴加几滴氯水,溶液变红,说明被氯气氧化为,故选B;
C.氯水能把氧化为,向溶液中依次滴加氯水,溶液,溶液变红,说明溶液中含有或,故不选C;
D.和OH-反应生成红褐色氢氧化铁沉淀,向溶液中滴加少量溶液,产生红褐色沉淀,证明含有,故不选D;
选B。
11.D
【详解】A.实验Ⅱ中Cu部分转化为Cu(I)消耗的铜粉多于其它两个实验,选项A正确;
B.实验Ⅰ、Ⅱ、Ⅲ中溶液黄色均褪去,推测都发生了反应2Fe3++Cu=Cu2++2Fe2+,选项B正确;
C.Ⅱ中加水后生成白色沉淀,根据元素种类推测应为CuCl,可能的离子反应Cu2++Cu+2Cl-=2CuCl↓,选项C正确;
D.实验Ⅱ、Ⅲ均加入过量的铜,后者未产生白色沉淀,表明能否形成白色沉淀由Cu的量和Cl-的浓度共同决定,选项D不正确。
答案选D。
12.D
【详解】A.Fe2+具有还原性,加入H2O2,可以将Fe2+氧化为Fe3+,而且H2O2的还原产物为水,不会引入新杂质,故A正确;
B.铁的还原性大于铜,混合液中加入足量的铁粉,反应生成铜和硫酸亚铁,过滤后得到铜和铁粉的混合物,滤液为纯净的硫酸亚铁溶液,故B正确;
C.碳酸钠溶液与足量的二氧化碳反应生成碳酸氢钠,能够除去杂质且不引入新杂质,故C正确;
D.除去KNO3溶液中的KOH,加入FeCl3溶液,虽然能生成Fe(OH)3沉淀,但引入了新杂质Cl-,故D错误;
故选D。
13.C
【详解】A.镁与FeCl3反应生成FeCl2,过量镁可与氯化亚铁发生置换反应置换出Fe,可除去杂质,所以A选项是正确的;
B.铁与FeCl3反应生成FeCl2,可除去杂质,所以B选项是正确的;
C.加入NaOH溶液,Cu2+、Fe3+均转化成氢氧化物沉淀,不符合除杂要求,故C错误;
D.铁与反应生成FeCl2,可除去杂质,所以D选项是正确的。
故答案选C。
14.C
【详解】A.铁与水蒸气在高温下的反应产物为Fe3O4和H2,故A错误;
B.FeCl3溶液中滴加过量氨水生成Fe(OH)3沉淀,所以不能用饱和FeCl3溶液与过量氨水制取Fe(OH)3胶体,故B错误;
C.配制硫酸亚铁溶液时,为防止产生Fe3+,可在溶液中加入少量铁粉,为了抑制亚铁离子被氧化而变质,故C正确;
D.Fe与氯化铁反应生成氯化亚铁,则加铁粉、过滤除去FeCl2溶液中的FeCl3杂质,故D错误。
故选C。
15.AD
【详解】A.①中反应的离子方程式为,故A错误;
B.①中为过量铁粉与反应,则②中无,故加入溶液后,溶液不变红,故B正确;
C.②中含有和,③中滴加新制氯水后,则被氧化为,溶液变红,故C正确;
D.同一个氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,则由③可知氧化性:,由①可知氧化性,故D错误;
故答案为AD。
16.(1) 2Fe3++Cu=2Fe2++Cu2+ 64
(2) ①② 2Fe3++Fe=3Fe2+、Cu2++Fe=Cu+Fe2+
(3) Cl2 取少量溶液于试管中,滴加几滴KSCN溶液,若出现红色,证明有Fe3+
(4)0.4mol/L
【分析】Cu和FeCl3发生反应Cu+2FeCl3=2FeCl2+2CuCl2,所以废液中含有Cu2+、Fe2+,可能含有Fe3+,向废液中加入过量Fe粉,发生反应2Fe3++Fe=3Fe2+、Cu2++Fe=Fe2++Cu,然后过滤,固体A中含有Fe、Cu,溶液A中含有FeCl2,向固体A中加入过量稀盐酸,发生反应Fe+2HCl=FeCl2+H2↑,然后过滤,得到的6.4g固体B是Cu,溶液B中含有HCl、FeCl2,将滤液②⑤混合,然后通入Cl2,发生反应2FeCl2+Cl2=2FeCl3,所以得到氯化铁溶液,以此解题。
(1)
FeCl3溶液与铜箔反应,生成FeCl2和CuCl2,反应的离子方程式:2Fe3++Cu═2Fe2++Cu2+,该反应中电子转移2mol,反应铜1mol,质量为64g;
(2)
过滤后得到滤液和固体,由流程图可知,①~③所涉及的实验操作方法中,属于过滤的是①②;①中加入铁粉和废液中的三价铁离子和铜离子反应生成二价铁,发生反应的离子方程式是2Fe3++Fe=3Fe2+、Cu2++Fe=Cu+Fe2+;
(3)
由分析可知气体C为氯气,氯气的化学式是:Cl2;三价铁遇到硫氰化钾显红色,故检验FeCl3溶液中金属阳离子的操作和现象是:取少量溶液于试管中,滴加几滴KSCN溶液,若出现红色,证明有Fe3+;
(4)
①中反应消耗铁粉11.2g,物质的量==0.2mol,2Fe3++Fe=3Fe2+、Cu2++Fe=Cu+Fe2+,其中铜离子物质的量==0.1mol,消耗铁0.1mol,则和铁离子反应的铁0.1mol,消耗铁离子物质的量0.2mol,废液中Fe3+的物质的量浓度==0.4mol/L。
