3-1-3铁及其化合物之间的转化关系课件(共24张PPT)2022-2023学年高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 3-1-3铁及其化合物之间的转化关系课件(共24张PPT)2022-2023学年高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 704.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-03 00:00:00 | ||
图片预览






文档简介
(共24张PPT)
Fe
Fe3+
Fe2+
(Cl2、Br2、
稀HNO3)
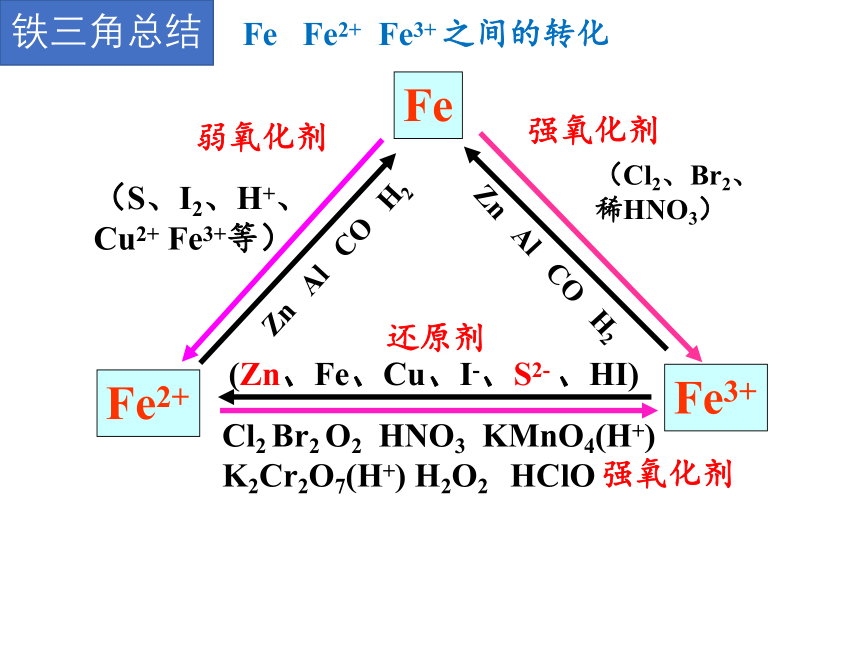
强氧化剂
弱氧化剂
(S、I2、H+、
Cu2+ Fe3+等)
(Zn、Fe、Cu、I-、S2- 、HI)
铁三角总结
Fe Fe2+ Fe3+ 之间的转化
强氧化剂
Cl2 Br2 O2 HNO3 KMnO4(H+) K2Cr2O7(H+) H2O2 HClO
Zn Al CO H2
Zn Al CO H2
还原剂
Fe2+ Fe3+
氧化剂:O2、H2O2、 HNO3等
2Fe2+ + H2O2 + 2H+ =2Fe3+ + 2H2O
4Fe2+ + O2 + 4H+ =4Fe3+ + 2H2O
3Fe2++ 4H++NO3-=3Fe3++ NO↑+2H2O
Fe3+ Fe2+
还原剂 Al Zn Fe Cu I- S2- H2S等
2Fe3++Zn (少) =2Fe2++Zn2+
2Fe3++3Zn (过) =2Fe + 3Zn2+
Fe3+ Fe2+
2Fe3+ + S2- (少) = S↓ + 2Fe2+
2Fe3+ + 3S2- (过) = S↓ + 2FeS↓
还原剂 Al Zn Fe Cu I- HI S2- H2S SO32-
2Fe3+ + H2S (少) = S↓ + 2Fe2+ + 2H+
2Fe3+ + H2S (过) = S↓ + 2Fe2+ + 2H+
FeS是黑色块状固体,常温下难溶于水,易溶于酸生成
能溶于水的H2S气体。
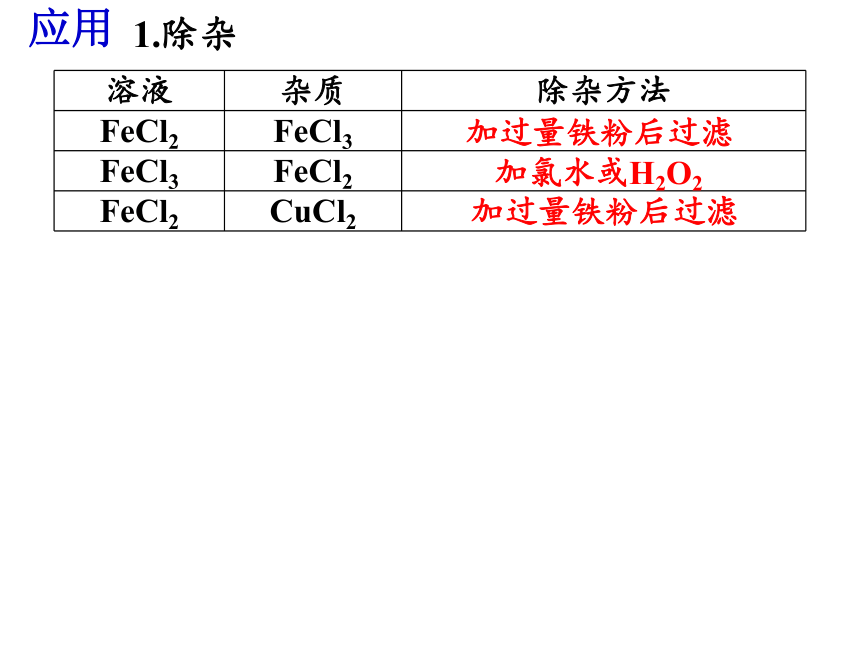
溶液 杂质 除杂方法
FeCl2 FeCl3
FeCl3 FeCl2
FeCl2 CuCl2
1.除杂
应用
加过量铁粉后过滤
加氯水或H2O2
加过量铁粉后过滤
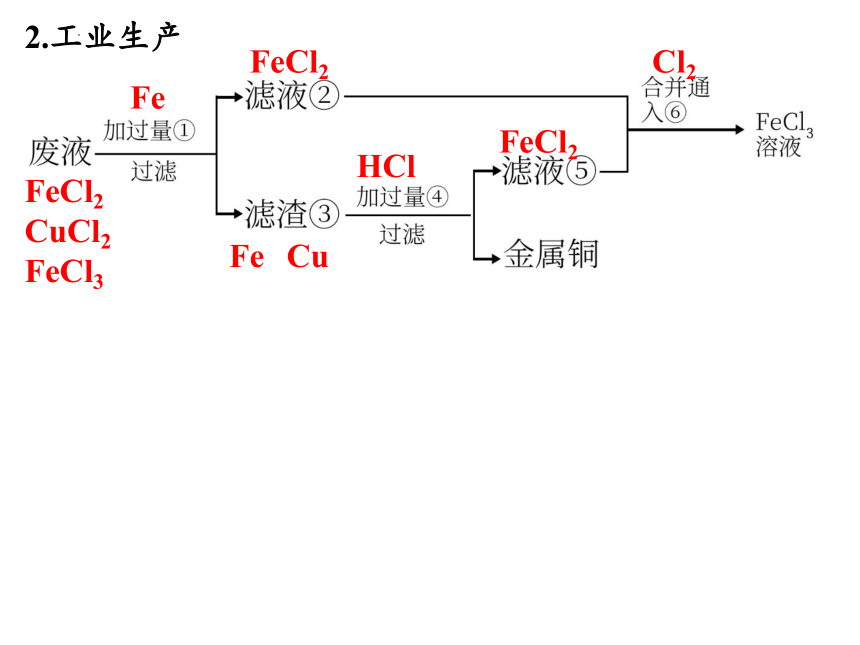
2.工业生产
FeCl2
CuCl2
FeCl3
Fe Cu
Fe
FeCl2
HCl
FeCl2
Cl2
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤。
(1)若滤渣既无Fe又无Cu,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是_______________________________
有可能
Fe2+ 、Cu2+或Fe2+、Cu2+ 、 Fe2+
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤。
(2)若滤渣只有Cu,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是___________________(若无可能,不需作答);
有可能
Fe2+或Fe2+、Cu2+
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤,
(3)若滤渣既有Fe又有Cu,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是___________________(若无可能,不需作答);
有可能
Fe2+
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤,
(4)若滤渣只有Fe,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是___________________(若无可能,不需作答);
不可能
例、把等物质的量的Cu、Fe粉投入一定量的FeCl3溶液
中充分反应,然后取出部分溶液。
(1)若滴加一滴KSCN溶液,溶液显红色,则溶液中
存在的离子有________________。
(2)若滴加一滴KSCN溶液,溶液不显红色,则溶液
中一定存在的离子有________________,可能存在
的金属粉末有________。
(3)若加入的金属全部溶解,则溶液中
n(Cu2+)∶n(Fe2+)=________。
(4)若(3)反应后的溶液中有三种金属离子,欲从中回
收Cu和FeCl3,需要用到的试剂有(按反应顺序填写)
__________________________________。
Cu2+、Fe2+、Fe3+、Cl-
Fe、Cu混合物或只有Cu
Fe2+、Cl-
1∶5
Fe、稀盐酸、新制氯水
练习: (1)少量Cl2通入FeI2(aq)
过量Cl2通入FeI2 (aq)
2I-+ Cl2 (少)= 2Cl- + I2
2Fe2++4I-+3Cl2(过)=2Fe3++2I2+6Cl-
(2) 少量Cl2通入FeBr2 (aq)
过量Cl2通入FeBr2 (aq)
2Fe2+ + Cl2(少) == 2Fe3+ + 2Cl-
2Fe2+ + 4Br- + 3Cl2 (过)== 2Fe3+ + 2Br2 + 6Cl-
(3)含有a mol FeI2的溶液中,通入x mol Cl2。下列各项为通入Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
A.x≤a,2I +Cl2=I2+2Cl
B.x=1.2a,10Fe2++14I +12Cl2=10Fe3++7I2+24Cl
C.x=1.4a,4Fe2++10I +7Cl2=4Fe3++5I2+14Cl
D.x≥1.5a,2Fe2++4I +3Cl2=2Fe3++2I2+6Cl
B
(4)已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-
的溶液中通入适量氯气,溶液中各种离子的物质的量变化
如下图所示。有关说法不正确的是
A.线段BC代表Fe3+ 物质的量
的变化情况
B.原混合溶液中c(FeBr2)=
6 mol/L
C.当通入Cl2 2mol时,溶液中
已发生的反应可表示为:
2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中n (Fe2+): n (I-): n(Br-)
=2:1:3
B
1、铁元素的常见化合价有+2价和+3价.据研究,铁在浓硝酸中发生钝化时,可以生成一种化学式为Fe8O11的化合物,它可以看作是由FeO和Fe2O3组成的复杂氧化物。该化合物可以表示为( )
A. FeO·3Fe2O3
B. 2FeO·3Fe2O3
C. FeO·2Fe2O3
D. 2FeO·Fe2O3
B
2、准确称取某铁的氧化物2.88g,用定量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4g,则这种氧化物为( )
A. Fe3O4 B. Fe2O3 C. FeO D. 以上均不是
C
3、有一铁的氧化物样品,用5 mol·L-1的盐酸140 mL
恰好完全溶解,所得溶液与通入的0.025molCl2反应,
使Fe2+全部转化为Fe3+,则此氧化物为( )
A.Fe2O3 B.Fe3O4 C.Fe4O5 D.Fe5O7
D
4、已知:氯气可以把Fe2+氧化为Fe3+,某铁的氧化物
(FexO)1.52g 溶于足量盐酸中,向所得溶液中通入标准状况下112mlCl2,恰好将Fe2+完全氧化。x值为( )
A.0.80 B.0.85 C.0.90 D.0.93
A
5、向一定量的FeO、Fe、Fe2O3、Fe3O4的混合物中加入
100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出
标准状况下的气体224 mL,加入KSCN溶液后,无颜色
变化。若用足量的CO在高温下还原相同量的此混合物,
能得到铁的质量为( )
2.8 g
6、15 g铁粉和氧化铁的混合物,放入150 mL稀H2SO4中,发现固体完全溶解,并放出1.68 L H2(标准状况),加入KSCN溶液后,无颜色变化。为了使Fe2+完全转化为Fe(OH)2沉淀,共耗用200 mL 3 mol/L NaOH溶液,则原硫酸溶液的物质的量浓度为( )
2 mol/L
Fe
Fe3+
Fe2+
(Cl2、Br2、
稀HNO3)
强氧化剂
弱氧化剂
(S、I2、H+、
Cu2+ Fe3+等)
(Zn、Fe、Cu、I-、S2- 、HI)
铁三角总结
Fe Fe2+ Fe3+ 之间的转化
强氧化剂
Cl2 Br2 O2 HNO3 KMnO4(H+) K2Cr2O7(H+) H2O2 HClO
Zn Al CO H2
Zn Al CO H2
还原剂
Fe2+ Fe3+
氧化剂:O2、H2O2、 HNO3等
2Fe2+ + H2O2 + 2H+ =2Fe3+ + 2H2O
4Fe2+ + O2 + 4H+ =4Fe3+ + 2H2O
3Fe2++ 4H++NO3-=3Fe3++ NO↑+2H2O
Fe3+ Fe2+
还原剂 Al Zn Fe Cu I- S2- H2S等
2Fe3++Zn (少) =2Fe2++Zn2+
2Fe3++3Zn (过) =2Fe + 3Zn2+
Fe3+ Fe2+
2Fe3+ + S2- (少) = S↓ + 2Fe2+
2Fe3+ + 3S2- (过) = S↓ + 2FeS↓
还原剂 Al Zn Fe Cu I- HI S2- H2S SO32-
2Fe3+ + H2S (少) = S↓ + 2Fe2+ + 2H+
2Fe3+ + H2S (过) = S↓ + 2Fe2+ + 2H+
FeS是黑色块状固体,常温下难溶于水,易溶于酸生成
能溶于水的H2S气体。
溶液 杂质 除杂方法
FeCl2 FeCl3
FeCl3 FeCl2
FeCl2 CuCl2
1.除杂
应用
加过量铁粉后过滤
加氯水或H2O2
加过量铁粉后过滤
2.工业生产
FeCl2
CuCl2
FeCl3
Fe Cu
Fe
FeCl2
HCl
FeCl2
Cl2
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤。
(1)若滤渣既无Fe又无Cu,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是_______________________________
有可能
Fe2+ 、Cu2+或Fe2+、Cu2+ 、 Fe2+
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤。
(2)若滤渣只有Cu,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是___________________(若无可能,不需作答);
有可能
Fe2+或Fe2+、Cu2+
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤,
(3)若滤渣既有Fe又有Cu,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是___________________(若无可能,不需作答);
有可能
Fe2+
例、在含有Cu2+、Fe3+、Cl-的溶液中,加入一定量的铁粉,充分反应后,过滤,
(4)若滤渣只有Fe,这种情况有可能吗?________。若有可能则溶液中的金属阳离子是___________________(若无可能,不需作答);
不可能
例、把等物质的量的Cu、Fe粉投入一定量的FeCl3溶液
中充分反应,然后取出部分溶液。
(1)若滴加一滴KSCN溶液,溶液显红色,则溶液中
存在的离子有________________。
(2)若滴加一滴KSCN溶液,溶液不显红色,则溶液
中一定存在的离子有________________,可能存在
的金属粉末有________。
(3)若加入的金属全部溶解,则溶液中
n(Cu2+)∶n(Fe2+)=________。
(4)若(3)反应后的溶液中有三种金属离子,欲从中回
收Cu和FeCl3,需要用到的试剂有(按反应顺序填写)
__________________________________。
Cu2+、Fe2+、Fe3+、Cl-
Fe、Cu混合物或只有Cu
Fe2+、Cl-
1∶5
Fe、稀盐酸、新制氯水
练习: (1)少量Cl2通入FeI2(aq)
过量Cl2通入FeI2 (aq)
2I-+ Cl2 (少)= 2Cl- + I2
2Fe2++4I-+3Cl2(过)=2Fe3++2I2+6Cl-
(2) 少量Cl2通入FeBr2 (aq)
过量Cl2通入FeBr2 (aq)
2Fe2+ + Cl2(少) == 2Fe3+ + 2Cl-
2Fe2+ + 4Br- + 3Cl2 (过)== 2Fe3+ + 2Br2 + 6Cl-
(3)含有a mol FeI2的溶液中,通入x mol Cl2。下列各项为通入Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
A.x≤a,2I +Cl2=I2+2Cl
B.x=1.2a,10Fe2++14I +12Cl2=10Fe3++7I2+24Cl
C.x=1.4a,4Fe2++10I +7Cl2=4Fe3++5I2+14Cl
D.x≥1.5a,2Fe2++4I +3Cl2=2Fe3++2I2+6Cl
B
(4)已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-
的溶液中通入适量氯气,溶液中各种离子的物质的量变化
如下图所示。有关说法不正确的是
A.线段BC代表Fe3+ 物质的量
的变化情况
B.原混合溶液中c(FeBr2)=
6 mol/L
C.当通入Cl2 2mol时,溶液中
已发生的反应可表示为:
2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中n (Fe2+): n (I-): n(Br-)
=2:1:3
B
1、铁元素的常见化合价有+2价和+3价.据研究,铁在浓硝酸中发生钝化时,可以生成一种化学式为Fe8O11的化合物,它可以看作是由FeO和Fe2O3组成的复杂氧化物。该化合物可以表示为( )
A. FeO·3Fe2O3
B. 2FeO·3Fe2O3
C. FeO·2Fe2O3
D. 2FeO·Fe2O3
B
2、准确称取某铁的氧化物2.88g,用定量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4g,则这种氧化物为( )
A. Fe3O4 B. Fe2O3 C. FeO D. 以上均不是
C
3、有一铁的氧化物样品,用5 mol·L-1的盐酸140 mL
恰好完全溶解,所得溶液与通入的0.025molCl2反应,
使Fe2+全部转化为Fe3+,则此氧化物为( )
A.Fe2O3 B.Fe3O4 C.Fe4O5 D.Fe5O7
D
4、已知:氯气可以把Fe2+氧化为Fe3+,某铁的氧化物
(FexO)1.52g 溶于足量盐酸中,向所得溶液中通入标准状况下112mlCl2,恰好将Fe2+完全氧化。x值为( )
A.0.80 B.0.85 C.0.90 D.0.93
A
5、向一定量的FeO、Fe、Fe2O3、Fe3O4的混合物中加入
100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出
标准状况下的气体224 mL,加入KSCN溶液后,无颜色
变化。若用足量的CO在高温下还原相同量的此混合物,
能得到铁的质量为( )
2.8 g
6、15 g铁粉和氧化铁的混合物,放入150 mL稀H2SO4中,发现固体完全溶解,并放出1.68 L H2(标准状况),加入KSCN溶液后,无颜色变化。为了使Fe2+完全转化为Fe(OH)2沉淀,共耗用200 mL 3 mol/L NaOH溶液,则原硫酸溶液的物质的量浓度为( )
2 mol/L
