第二章 烃 第三节 芳香烃第1课时 苯课件(共21张PPT)2022-2023学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第二章 烃 第三节 芳香烃第1课时 苯课件(共21张PPT)2022-2023学年下学期高二化学人教版(2019)选择性必修3 |  | |
| 格式 | pptx | ||
| 文件大小 | 18.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-03 09:06:38 | ||
图片预览



文档简介
(共21张PPT)
第 二 章 烃
第 三 节 芳 香 烃
第 1 课 时 苯
选择性必修三
化学家预言第一次世界大战
1912-1913年,德国在国际市场上大量收购石油。由于有利可图,许多国家的石油商都不惜压低价格争着与德国人做生意,但令人不可理解的是,德国人只要婆罗洲的石油,其他的一概不要,并急急忙忙地把收购到婆罗洲的石油运到德国本土去。在石油商人感到百思不得其解时,一位化学家提醒世人说:“德国人在准备发动战争了!”果然不出化学家所料,德国于1914年发动了第一次世界大战。
这一奇怪现象引起了一位化学家的注意他经过化验,发现婆罗洲的石油成分与其他地区的不同,它含有很少的直链烃,它含有大量的苯和甲苯等芳香烃。
一、苯的发现
1825年,
[英]法拉第从煤焦油中分离出“苯”,略带香味,常温为液态,确定结构式为CH
18世纪中期,
[法]热拉尔等测得苯相对分子质量为78,确定分子式为C6H6,
奥地利化学家洛施密特提出苯具有环状结构。
不饱和程度很大
凯库勒在1866年提出三点假设:
(1) 苯的六个碳原子形成闭合环状,即平面六边形
(2) 每个碳原子均连接一个氢原子
(3) 各碳原子间存在着单、双键交替形式
说明苯分子具有不同于烯烃和炔烃的特殊结构
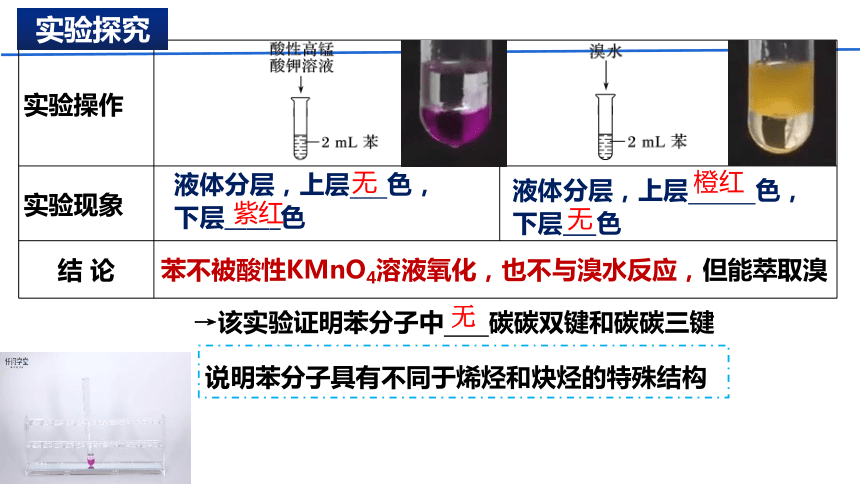
实验操作
实验现象
结 论
液体分层,上层 色,
下层_____色
液体分层,上层 色,
下层___色
无
紫红
橙红
无
→该实验证明苯分子中 碳碳双键和碳碳三键
无
实验探究
苯不被酸性KMnO4溶液氧化,也不与溴水反应,但能萃取溴
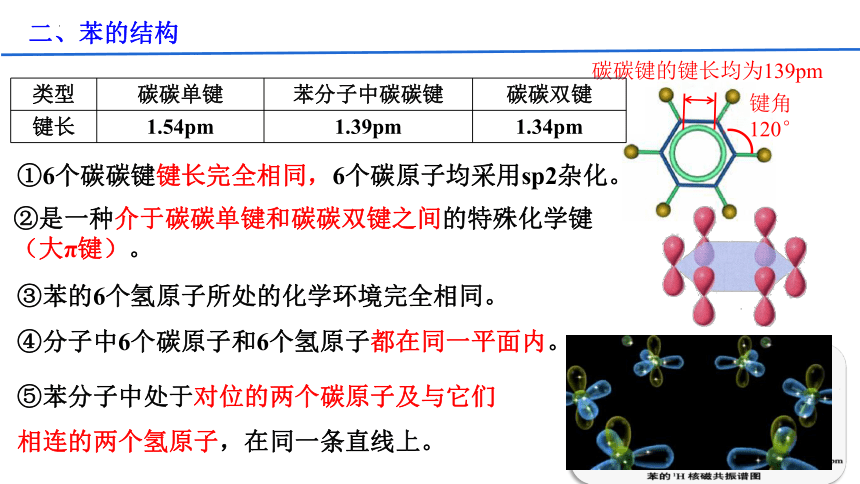
④分子中6个碳原子和6个氢原子都在同一平面内。
①6个碳碳键键长完全相同,6个碳原子均采用sp2杂化。
②是一种介于碳碳单键和碳碳双键之间的特殊化学键(大π键)。
⑤苯分子中处于对位的两个碳原子及与它们相连的两个氢原子,在同一条直线上。
③苯的6个氢原子所处的化学环境完全相同。
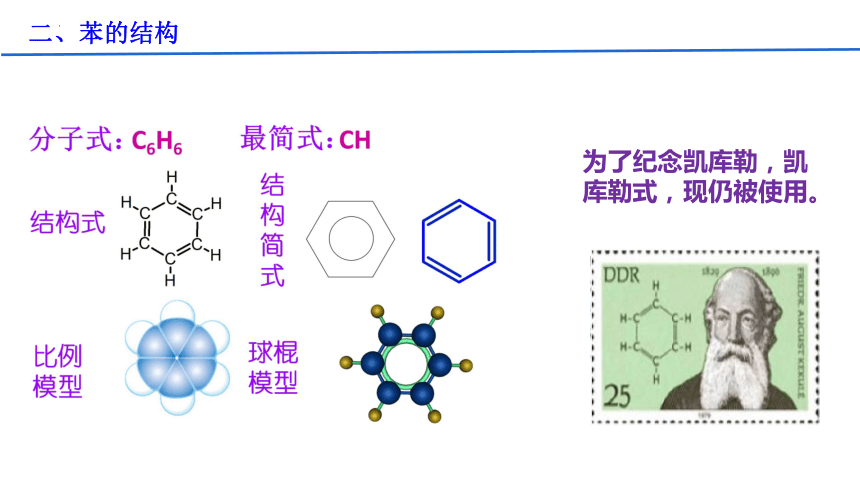
二、苯的结构
键角120°
碳碳键的键长均为139pm
类型 碳碳单键 苯分子中碳碳键 碳碳双键
键长 1.54pm 1.39pm 1.34pm
【例1】下列化学事实能说明苯分子结构中不存在碳碳单键和碳碳双键交替的是( )
①苯的间位二元取代物只有一种
②苯的邻位二元取代物只有一种
③苯不能使酸性KMnO4溶液褪色
④苯能在一定条下与氢气反应生成环己烷
⑤苯不因化学反应使溴水褪色.
A.①③④ B.③④⑤ C.②③⑤ D.①③⑤
C
【归纳总结】哪些事实可证明苯分子中不存在单双键交替的结构
1.苯的邻位二元取代物只有一种 2.苯不能使溴水褪色
3.苯不能使酸性高锰酸钾溶液褪色 4.经测定,苯环中碳碳键的键能均相等 5.经测定,苯环上碳碳键的键长相等,都是1.39×10-10m
为了纪念凯库勒,凯库勒式,现仍被使用。
二、苯的结构
现象:
火焰明亮,伴有浓重的黑烟 (与乙炔相同)
方程式:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
①苯不能使酸性高锰酸钾溶液褪色。
②可燃性:
三、苯的化学性质—— 氧化反应
大π键使苯环结构稳定,不易断裂
FeBr3作催化剂,苯环上氢原子被溴原子所取代
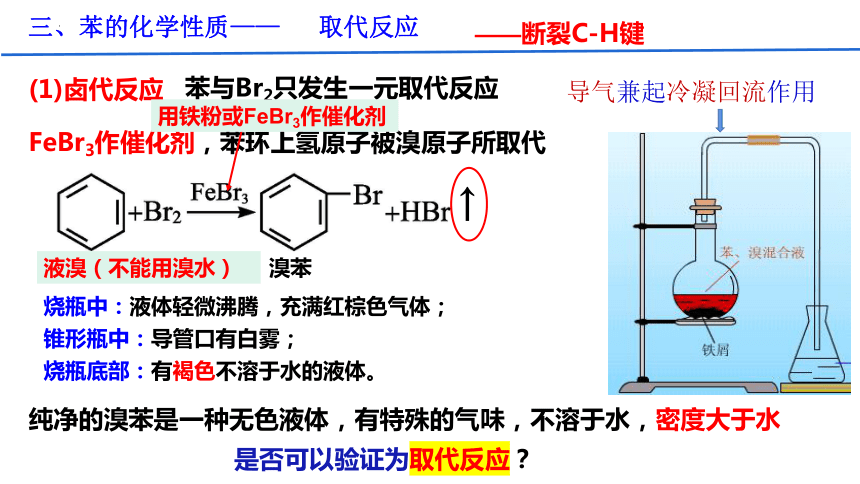
(1)卤代反应
溴苯
纯净的溴苯是一种无色液体,有特殊的气味,不溶于水,密度大于水
液溴(不能用溴水)
↑
——断裂C-H键
苯与Br2只发生一元取代反应
烧瓶中:液体轻微沸腾,充满红棕色气体;
锥形瓶中:导管口有白雾;
烧瓶底部:有褐色不溶于水的液体。
三、苯的化学性质—— 取代反应
用铁粉或FeBr3作催化剂
是否可以验证为取代反应?
导气兼起冷凝回流作用
注意:1.必须为液溴;催化剂也可用Fe粉;
2.反应强烈放热,无需加热。
3..反应制得产品因含溴呈红褐色,必须用稀NaOH溶液除去Br2
4.向锥形瓶中的蒸馏水加入AgNO3产生淡黄色沉淀, 说明有HBr生成,该反应为取代反应。
②苯与浓硝酸(硝化反应)
——断裂C-H键
在浓硫酸的作用下,苯在50~60℃时与浓硝酸
发生硝化反应,生成硝基苯。
纯净的硝基苯是一种无色液体,有苦
杏仁气味,不溶于水,密度大于水
+ HNO3(浓)
NO2
+ H2O
浓H2SO4
HO-NO2
硝基苯
催化剂和吸水剂
水浴加热
混酸与苯
三、苯的化学性质—— 取代反应
1.试剂的加入顺序:
先加浓硝酸,再加浓硫酸,等混合液冷却到50-60℃后,再加苯
3.用水浴加热,控制温度在50-60℃,温度计放在水浴中。温度过高,苯挥发,硝酸分解。 水浴加热的优点:容易控制温度,受热均匀
2.浓硫酸的作用:催化剂、吸水剂
5.试管上方的长导管的作用是导气、冷凝回流,减少反应物的挥发。
6.产物:纯净的硝基苯是无色、有苦杏仁味的油状液体,密度比水大,有毒,难溶于水;但实验室制得的硝基苯呈淡黄色,原因:硝酸部分分解产生的NO2气体溶于硝基苯
4.为什么硝化反应控制在50--60℃?温度计的作用及其水银球的位置?
温度低于50℃,不易反应;温度过高,苯易挥发,且硝酸也会分解,同时苯和浓硫酸反应生成苯磺酸等副反应;温度计的水银球位于水浴中,控制水浴温度,温度计的水银球插入水浴中测量温度,水银球不能触及烧杯底部及烧杯壁。
知识链接
70~80℃
磺酸基:-SO3H
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作是硫酸分子里的一个羟基被苯环取代的产物。磺化反应可用于制备合成洗涤剂。
三、苯的化学性质—— 取代反应
②苯与浓硫酸(磺化反应)
+ H2
催化剂(Ni)
△
环己烷
3
①苯与H2加成:
②苯与Cl2在紫外线作用下加成
六氯环己烷
或
(农药六六六)
苯的大π键比较稳定,通常状态下不易发生加成反应
(Pt或Ni作为催化剂并且加热)
+ 3Cl2
紫外线
三、苯的化学性质—— 加成反应
注意:反应条件不同,反应原理相差很大。
+ Cl2
Cl
+ HCl
FeCl3
取代反应
加成反应
对比反应
不同点
三、苯的化学性质对比
2.易取代:
3.难加成:
磺化反应
与氢气、氯气加成
卤代反应
硝化反应
+ HO-NO2
浓H2SO4
500C—600C
NO2
+ H2O
+HO-SO3H
70℃~80℃
-SO3H
+ H2O
+ Br2
FeBr3
Br
+ HBr
总体来说,苯的化学性质是“易取代,能加成,难氧化”
1.氧化反应:可燃性(注:不能使酸性高锰酸钾溶液褪色)
(注:不能和溴水发生加成反应)
↑
归纳小结
大π键使苯环结构稳定,不易断裂
苯
物理性质
颜色
气味
毒性
水溶性
挥发性
熔点
沸点
密度
无色
有特殊气味
有毒
不溶于水
易挥发
80.1℃
5.5℃
0.88g/cm3
苯是一种重要的化工原料和有机溶剂
有毒:对人的神经系统、造血系统有伤害,
可导致白血病。
环保油漆采用无苯溶剂
四、苯的物理性质
下列关于苯的叙述正确的是( )
A.反应①为取代反应,有机产物的密度比水小
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,有机产物是一种烃
D.反应④中1 mol苯最多与3 mol H2发生加成反应,因为苯分子中含有三个碳碳双键
B
【练习】
除去溴苯
中的溴
除去溴蒸汽,
净化HBr气体
检验HBr酸性
检验HBr
除去HBr尾气
防倒吸
①有分液漏斗,控制液溴的量。
②加装一个用苯(CCl4)除溴蒸气的装置。
③倒扣的漏斗可以防倒吸,还有利于尾气吸收
生成的HBr中常混有溴蒸气,此时用AgNO3溶液对HBr的检验结果是否可靠?
为什么?如何除去混在HBr中的溴蒸气?
不可靠,因为溴易挥发。
溴蒸气溶于水,
也能生成HBr
与AgNO3溶液
反应生成淡黄色沉淀。
将产生的气体
①通过苯(CCl4)洗气
(除去其中的溴)
②再通入AgNO3溶液中
AgNO3 +HBr = AgBr↓ +HNO3
HBr
【课后提升】苯的溴代反应装置改进
思考:如何获得纯净的溴苯?
产物中可能含有溴苯、苯、
HBr和Br2
试剂:
操作:
目的:
水
分液
除HBr
HBr水溶液
溴苯
苯、溴
试剂:
操作:
目的:
NaOH
分液
除Br2
NaBr溶液
NaBrO溶液
溴苯
苯
溴苯
苯
蒸馏
除苯
操作:
目的:
【课后提升】
思考:如何获得纯净的硝基苯?
产物中可能含有硝基苯、苯、硫酸、硝酸、NO2
试剂:
操作:
目的:
水
分液
除酸
酸液
硝基苯
苯
残余酸
试剂:
操作:
目的:
NaOH
分液
除酸
盐溶液
硝基苯
苯
硝基苯
苯
蒸馏
除苯
操作:
目的:
第 二 章 烃
第 三 节 芳 香 烃
第 1 课 时 苯
选择性必修三
化学家预言第一次世界大战
1912-1913年,德国在国际市场上大量收购石油。由于有利可图,许多国家的石油商都不惜压低价格争着与德国人做生意,但令人不可理解的是,德国人只要婆罗洲的石油,其他的一概不要,并急急忙忙地把收购到婆罗洲的石油运到德国本土去。在石油商人感到百思不得其解时,一位化学家提醒世人说:“德国人在准备发动战争了!”果然不出化学家所料,德国于1914年发动了第一次世界大战。
这一奇怪现象引起了一位化学家的注意他经过化验,发现婆罗洲的石油成分与其他地区的不同,它含有很少的直链烃,它含有大量的苯和甲苯等芳香烃。
一、苯的发现
1825年,
[英]法拉第从煤焦油中分离出“苯”,略带香味,常温为液态,确定结构式为CH
18世纪中期,
[法]热拉尔等测得苯相对分子质量为78,确定分子式为C6H6,
奥地利化学家洛施密特提出苯具有环状结构。
不饱和程度很大
凯库勒在1866年提出三点假设:
(1) 苯的六个碳原子形成闭合环状,即平面六边形
(2) 每个碳原子均连接一个氢原子
(3) 各碳原子间存在着单、双键交替形式
说明苯分子具有不同于烯烃和炔烃的特殊结构
实验操作
实验现象
结 论
液体分层,上层 色,
下层_____色
液体分层,上层 色,
下层___色
无
紫红
橙红
无
→该实验证明苯分子中 碳碳双键和碳碳三键
无
实验探究
苯不被酸性KMnO4溶液氧化,也不与溴水反应,但能萃取溴
④分子中6个碳原子和6个氢原子都在同一平面内。
①6个碳碳键键长完全相同,6个碳原子均采用sp2杂化。
②是一种介于碳碳单键和碳碳双键之间的特殊化学键(大π键)。
⑤苯分子中处于对位的两个碳原子及与它们相连的两个氢原子,在同一条直线上。
③苯的6个氢原子所处的化学环境完全相同。
二、苯的结构
键角120°
碳碳键的键长均为139pm
类型 碳碳单键 苯分子中碳碳键 碳碳双键
键长 1.54pm 1.39pm 1.34pm
【例1】下列化学事实能说明苯分子结构中不存在碳碳单键和碳碳双键交替的是( )
①苯的间位二元取代物只有一种
②苯的邻位二元取代物只有一种
③苯不能使酸性KMnO4溶液褪色
④苯能在一定条下与氢气反应生成环己烷
⑤苯不因化学反应使溴水褪色.
A.①③④ B.③④⑤ C.②③⑤ D.①③⑤
C
【归纳总结】哪些事实可证明苯分子中不存在单双键交替的结构
1.苯的邻位二元取代物只有一种 2.苯不能使溴水褪色
3.苯不能使酸性高锰酸钾溶液褪色 4.经测定,苯环中碳碳键的键能均相等 5.经测定,苯环上碳碳键的键长相等,都是1.39×10-10m
为了纪念凯库勒,凯库勒式,现仍被使用。
二、苯的结构
现象:
火焰明亮,伴有浓重的黑烟 (与乙炔相同)
方程式:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
①苯不能使酸性高锰酸钾溶液褪色。
②可燃性:
三、苯的化学性质—— 氧化反应
大π键使苯环结构稳定,不易断裂
FeBr3作催化剂,苯环上氢原子被溴原子所取代
(1)卤代反应
溴苯
纯净的溴苯是一种无色液体,有特殊的气味,不溶于水,密度大于水
液溴(不能用溴水)
↑
——断裂C-H键
苯与Br2只发生一元取代反应
烧瓶中:液体轻微沸腾,充满红棕色气体;
锥形瓶中:导管口有白雾;
烧瓶底部:有褐色不溶于水的液体。
三、苯的化学性质—— 取代反应
用铁粉或FeBr3作催化剂
是否可以验证为取代反应?
导气兼起冷凝回流作用
注意:1.必须为液溴;催化剂也可用Fe粉;
2.反应强烈放热,无需加热。
3..反应制得产品因含溴呈红褐色,必须用稀NaOH溶液除去Br2
4.向锥形瓶中的蒸馏水加入AgNO3产生淡黄色沉淀, 说明有HBr生成,该反应为取代反应。
②苯与浓硝酸(硝化反应)
——断裂C-H键
在浓硫酸的作用下,苯在50~60℃时与浓硝酸
发生硝化反应,生成硝基苯。
纯净的硝基苯是一种无色液体,有苦
杏仁气味,不溶于水,密度大于水
+ HNO3(浓)
NO2
+ H2O
浓H2SO4
HO-NO2
硝基苯
催化剂和吸水剂
水浴加热
混酸与苯
三、苯的化学性质—— 取代反应
1.试剂的加入顺序:
先加浓硝酸,再加浓硫酸,等混合液冷却到50-60℃后,再加苯
3.用水浴加热,控制温度在50-60℃,温度计放在水浴中。温度过高,苯挥发,硝酸分解。 水浴加热的优点:容易控制温度,受热均匀
2.浓硫酸的作用:催化剂、吸水剂
5.试管上方的长导管的作用是导气、冷凝回流,减少反应物的挥发。
6.产物:纯净的硝基苯是无色、有苦杏仁味的油状液体,密度比水大,有毒,难溶于水;但实验室制得的硝基苯呈淡黄色,原因:硝酸部分分解产生的NO2气体溶于硝基苯
4.为什么硝化反应控制在50--60℃?温度计的作用及其水银球的位置?
温度低于50℃,不易反应;温度过高,苯易挥发,且硝酸也会分解,同时苯和浓硫酸反应生成苯磺酸等副反应;温度计的水银球位于水浴中,控制水浴温度,温度计的水银球插入水浴中测量温度,水银球不能触及烧杯底部及烧杯壁。
知识链接
70~80℃
磺酸基:-SO3H
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作是硫酸分子里的一个羟基被苯环取代的产物。磺化反应可用于制备合成洗涤剂。
三、苯的化学性质—— 取代反应
②苯与浓硫酸(磺化反应)
+ H2
催化剂(Ni)
△
环己烷
3
①苯与H2加成:
②苯与Cl2在紫外线作用下加成
六氯环己烷
或
(农药六六六)
苯的大π键比较稳定,通常状态下不易发生加成反应
(Pt或Ni作为催化剂并且加热)
+ 3Cl2
紫外线
三、苯的化学性质—— 加成反应
注意:反应条件不同,反应原理相差很大。
+ Cl2
Cl
+ HCl
FeCl3
取代反应
加成反应
对比反应
不同点
三、苯的化学性质对比
2.易取代:
3.难加成:
磺化反应
与氢气、氯气加成
卤代反应
硝化反应
+ HO-NO2
浓H2SO4
500C—600C
NO2
+ H2O
+HO-SO3H
70℃~80℃
-SO3H
+ H2O
+ Br2
FeBr3
Br
+ HBr
总体来说,苯的化学性质是“易取代,能加成,难氧化”
1.氧化反应:可燃性(注:不能使酸性高锰酸钾溶液褪色)
(注:不能和溴水发生加成反应)
↑
归纳小结
大π键使苯环结构稳定,不易断裂
苯
物理性质
颜色
气味
毒性
水溶性
挥发性
熔点
沸点
密度
无色
有特殊气味
有毒
不溶于水
易挥发
80.1℃
5.5℃
0.88g/cm3
苯是一种重要的化工原料和有机溶剂
有毒:对人的神经系统、造血系统有伤害,
可导致白血病。
环保油漆采用无苯溶剂
四、苯的物理性质
下列关于苯的叙述正确的是( )
A.反应①为取代反应,有机产物的密度比水小
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,有机产物是一种烃
D.反应④中1 mol苯最多与3 mol H2发生加成反应,因为苯分子中含有三个碳碳双键
B
【练习】
除去溴苯
中的溴
除去溴蒸汽,
净化HBr气体
检验HBr酸性
检验HBr
除去HBr尾气
防倒吸
①有分液漏斗,控制液溴的量。
②加装一个用苯(CCl4)除溴蒸气的装置。
③倒扣的漏斗可以防倒吸,还有利于尾气吸收
生成的HBr中常混有溴蒸气,此时用AgNO3溶液对HBr的检验结果是否可靠?
为什么?如何除去混在HBr中的溴蒸气?
不可靠,因为溴易挥发。
溴蒸气溶于水,
也能生成HBr
与AgNO3溶液
反应生成淡黄色沉淀。
将产生的气体
①通过苯(CCl4)洗气
(除去其中的溴)
②再通入AgNO3溶液中
AgNO3 +HBr = AgBr↓ +HNO3
HBr
【课后提升】苯的溴代反应装置改进
思考:如何获得纯净的溴苯?
产物中可能含有溴苯、苯、
HBr和Br2
试剂:
操作:
目的:
水
分液
除HBr
HBr水溶液
溴苯
苯、溴
试剂:
操作:
目的:
NaOH
分液
除Br2
NaBr溶液
NaBrO溶液
溴苯
苯
溴苯
苯
蒸馏
除苯
操作:
目的:
【课后提升】
思考:如何获得纯净的硝基苯?
产物中可能含有硝基苯、苯、硫酸、硝酸、NO2
试剂:
操作:
目的:
水
分液
除酸
酸液
硝基苯
苯
残余酸
试剂:
操作:
目的:
NaOH
分液
除酸
盐溶液
硝基苯
苯
硝基苯
苯
蒸馏
除苯
操作:
目的:
