化学人教版(2019)必修第二册7.2.1乙烯(共38张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.2.1乙烯(共38张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 9.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-04 00:00:00 | ||
图片预览









文档简介
(共38张PPT)
第七章 有机化合物
第2节 乙烯与有机高分子材料
第1课时 乙烯
情景导入
教学目标
预习检查
问题导学
随堂巩固
思维导图
学习目标
1、会写乙烯的分子式、结构式、结构简式、电子式。
2.知道乙烯能够发生氧化反应、加成反应、聚合反应。
3、理解加成反应的概念。
教学目标
教学重点和难点
1、重点:从宏观和微观两个方面研究乙烯的结构如何决定其性质。
2、难点:乙烯加成反应和加聚反应的基本规律。
教学目标
为了促进香蕉成熟,
可在密封袋子中放一些成熟的苹果
情景导入
乙烯是石油化学工业重要的基本原料,通过一系列化学反应,可以从乙烯得到有机高分子材料、药物等成千上万种有用的物质。
乙烯的用途广泛,其产量可以用来衡量一个国家石油化学工业的发展水平。
情景导入
知识点一 乙烯的组成、结构与物理性质
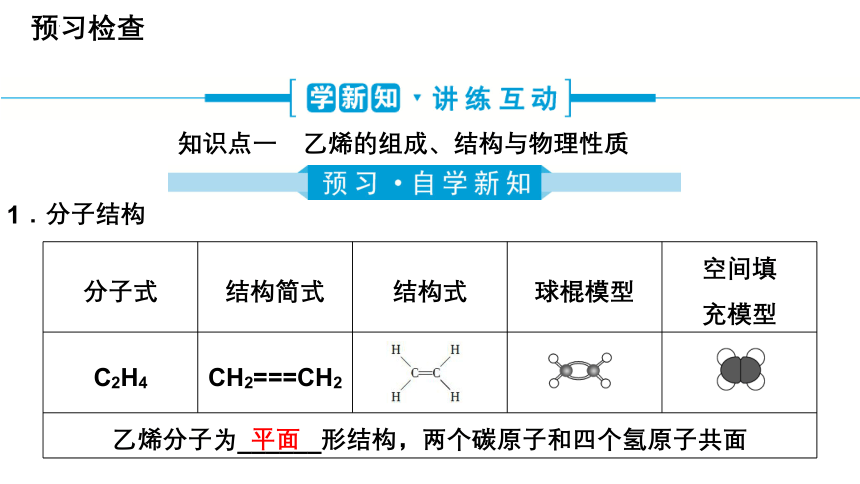
1.分子结构
分子式 结构简式 结构式 球棍模型 空间填
充模型
C2H4 CH2===CH2
乙烯分子为______形结构,两个碳原子和四个氢原子共面
平面
预习检查
2.物理性质:乙烯是一种无色、稍有气味的气体,密度比空气的略小,____溶于水。
难
预习检查
知识点二 乙烯的化学性质与用途
1.化学性质
2.氧化反应
预习检查
溶液紫红色褪去
预习检查
预习检查
乙烯用途
Q1:乙烯的结构式什么样的?
6个原子共平面,键角120°,平面型分子,分子中有碳碳双键,碳原子的价键没有全部被氢原子“饱和”。
分子式 电子式
结构式 结构简式
C2H4
CH2 = CH2
H : C :: C : H
.. .
H H
CH2 CH2
一、乙烯的结构
乙烯是一种无色,稍有气味的气体,密度比空气略小,难溶于水。
新课讲授
随堂巩固
Q2:乙烯的物理性质有哪些?
二、乙烯的物理性质
颜色 气味 状态 密度 溶解性
无色 稍有气味 气体 比空气____ ____溶于水
小
难
新课讲授
Q3:乙烯的化学性质有哪些?
(1)、氧化反应
CH2=CH2
+
3O2
点燃
2CO2 + 2H2O
① 燃烧
现象:火焰明亮并伴有黑烟
三、乙烯的化学性质
现象:溶液的紫色褪去
应用:鉴别乙烯(与烷烃比)
② 被(酸性KMnO4溶液)氧化
新课讲授
三、乙烯的化学性质
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
乙烯使溴的四氯化碳褪色
新课讲授
我是
溴分子
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
(2)、加成反应
三、乙烯的化学性质
H — C=C — H+Br—Br H — C — C — H
H
H
Br
Br
H
H
碳碳双键中有一个键易断
有机物分子中的不饱和键(双键 或 三键)两端的碳原子与其他原子或原子团直接结合成新化合物的反应叫加成反应。
1,2-二溴乙烷
新课讲授
(2)、加成反应
三、乙烯的化学性质
乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应,你能尝试写一下吗?
CH2=CH2 + H—H
催化剂
△
CH2=CH2 + H—OH
催化剂
△,P
CH3—CH3 (乙烷)
CH3CH2—OH(乙醇)
工业上乙烯水化法制酒精的原理
新课讲授
烯烃加成反应的特点
加成反应是有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应,
其特点是:“断一加二,都进来”,
“断一”是指双键中的一个不稳定键断裂;
“加二”是指加两个其他原子或原子团,每一个不饱和碳原子上各加上一个。
新课讲授
练习
丙烯与乙烯互为同系物,由乙烯的结构和性质推测丙烯(CH2=CH—CH3)与HCl在一定条件下能加成的产物有几种 写出结构简式。
乙烯分子内碳碳双键的键能(615KJ/mol)小于碳碳单键键能(348KJ/mol)的二倍,说明其中有一条碳碳键键能小,容易断裂。
乙烯分子的碳碳双键中的一个键容易断裂。
所以,乙烯的化学性质比较活泼。
乙烯的结构特点
乙烯模型
思考讨论
(1) 比较CH4、CH2=CH2 的化学性质
物质 甲烷 乙烯
与Br2 反应 试剂类型 ________ ______________
反应条件 _____ 无
反应类型 _____ _____
氧化 反应 燃烧 火焰呈 色 火焰____________
酸性KMnO4溶液 ____________ _______________
Br2蒸气
溴水或溴的 CCl4 溶液
光照
取代
加成
淡蓝
明亮、伴有黑烟
稳定,不反应
酸性 KMnO4 溶液褪色
纯净
(2)鉴别乙烯和甲烷有哪些方法?
(提示:鉴别乙烯和甲烷的方法)
新课讲授
乙烯的性质
稍有气味水难溶,
高锰酸钾溴反应。
现象相同理不同,
前因氧化后加成。
加氧燃烧黑烟冒。
【归纳总结】
新课讲授
1.下列关于乙烯结构与性质的叙述中,错误的是( )
A.乙烯分子中6个原子在同一平面内
B.乙烯能与酸性KMnO4溶液发生加成反应而使其褪色
C.乙烯能与溴的四氯化碳溶液发生加成反应
D.乙烯能与水发生加成反应生成乙醇
解析:B项发生的是氧化反应而不是加成反应。
√
课后巩固评价
√
随堂巩固
3.(2020·福州高一检测)下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,回答下列问题。
课后巩固评价
(1)C装置中反应的化学方程式为__________________。
(2)B装置中可观察到的现象是____________。
(3)查阅资料,乙烯与酸性高锰酸钾溶液反应产生二氧化碳,反应类型为______。
(4)下列物质中,可以通过乙烯的加成反应得到的是________(填字母)。
A.CH3CH3
B.CH3CHCl2 C.CH3CH2OH
答案
(1)CH2===CH2+Br2―→BrCH2—CH2Br
(2)溶液紫(或紫红)色褪去
(3)氧化反应
(4)AC
课后巩固评价
第七章 有机化合物
第2节 乙烯与有机高分子材料
第1课时 乙烯
情景导入
教学目标
预习检查
问题导学
随堂巩固
思维导图
学习目标
1、会写乙烯的分子式、结构式、结构简式、电子式。
2.知道乙烯能够发生氧化反应、加成反应、聚合反应。
3、理解加成反应的概念。
教学目标
教学重点和难点
1、重点:从宏观和微观两个方面研究乙烯的结构如何决定其性质。
2、难点:乙烯加成反应和加聚反应的基本规律。
教学目标
为了促进香蕉成熟,
可在密封袋子中放一些成熟的苹果
情景导入
乙烯是石油化学工业重要的基本原料,通过一系列化学反应,可以从乙烯得到有机高分子材料、药物等成千上万种有用的物质。
乙烯的用途广泛,其产量可以用来衡量一个国家石油化学工业的发展水平。
情景导入
知识点一 乙烯的组成、结构与物理性质
1.分子结构
分子式 结构简式 结构式 球棍模型 空间填
充模型
C2H4 CH2===CH2
乙烯分子为______形结构,两个碳原子和四个氢原子共面
平面
预习检查
2.物理性质:乙烯是一种无色、稍有气味的气体,密度比空气的略小,____溶于水。
难
预习检查
知识点二 乙烯的化学性质与用途
1.化学性质
2.氧化反应
预习检查
溶液紫红色褪去
预习检查
预习检查
乙烯用途
Q1:乙烯的结构式什么样的?
6个原子共平面,键角120°,平面型分子,分子中有碳碳双键,碳原子的价键没有全部被氢原子“饱和”。
分子式 电子式
结构式 结构简式
C2H4
CH2 = CH2
H : C :: C : H
.. .
H H
CH2 CH2
一、乙烯的结构
乙烯是一种无色,稍有气味的气体,密度比空气略小,难溶于水。
新课讲授
随堂巩固
Q2:乙烯的物理性质有哪些?
二、乙烯的物理性质
颜色 气味 状态 密度 溶解性
无色 稍有气味 气体 比空气____ ____溶于水
小
难
新课讲授
Q3:乙烯的化学性质有哪些?
(1)、氧化反应
CH2=CH2
+
3O2
点燃
2CO2 + 2H2O
① 燃烧
现象:火焰明亮并伴有黑烟
三、乙烯的化学性质
现象:溶液的紫色褪去
应用:鉴别乙烯(与烷烃比)
② 被(酸性KMnO4溶液)氧化
新课讲授
三、乙烯的化学性质
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
乙烯使溴的四氯化碳褪色
新课讲授
我是
溴分子
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
加成反应机理
三、乙烯的化学性质
新课讲授
(2)、加成反应
三、乙烯的化学性质
H — C=C — H+Br—Br H — C — C — H
H
H
Br
Br
H
H
碳碳双键中有一个键易断
有机物分子中的不饱和键(双键 或 三键)两端的碳原子与其他原子或原子团直接结合成新化合物的反应叫加成反应。
1,2-二溴乙烷
新课讲授
(2)、加成反应
三、乙烯的化学性质
乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应,你能尝试写一下吗?
CH2=CH2 + H—H
催化剂
△
CH2=CH2 + H—OH
催化剂
△,P
CH3—CH3 (乙烷)
CH3CH2—OH(乙醇)
工业上乙烯水化法制酒精的原理
新课讲授
烯烃加成反应的特点
加成反应是有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应,
其特点是:“断一加二,都进来”,
“断一”是指双键中的一个不稳定键断裂;
“加二”是指加两个其他原子或原子团,每一个不饱和碳原子上各加上一个。
新课讲授
练习
丙烯与乙烯互为同系物,由乙烯的结构和性质推测丙烯(CH2=CH—CH3)与HCl在一定条件下能加成的产物有几种 写出结构简式。
乙烯分子内碳碳双键的键能(615KJ/mol)小于碳碳单键键能(348KJ/mol)的二倍,说明其中有一条碳碳键键能小,容易断裂。
乙烯分子的碳碳双键中的一个键容易断裂。
所以,乙烯的化学性质比较活泼。
乙烯的结构特点
乙烯模型
思考讨论
(1) 比较CH4、CH2=CH2 的化学性质
物质 甲烷 乙烯
与Br2 反应 试剂类型 ________ ______________
反应条件 _____ 无
反应类型 _____ _____
氧化 反应 燃烧 火焰呈 色 火焰____________
酸性KMnO4溶液 ____________ _______________
Br2蒸气
溴水或溴的 CCl4 溶液
光照
取代
加成
淡蓝
明亮、伴有黑烟
稳定,不反应
酸性 KMnO4 溶液褪色
纯净
(2)鉴别乙烯和甲烷有哪些方法?
(提示:鉴别乙烯和甲烷的方法)
新课讲授
乙烯的性质
稍有气味水难溶,
高锰酸钾溴反应。
现象相同理不同,
前因氧化后加成。
加氧燃烧黑烟冒。
【归纳总结】
新课讲授
1.下列关于乙烯结构与性质的叙述中,错误的是( )
A.乙烯分子中6个原子在同一平面内
B.乙烯能与酸性KMnO4溶液发生加成反应而使其褪色
C.乙烯能与溴的四氯化碳溶液发生加成反应
D.乙烯能与水发生加成反应生成乙醇
解析:B项发生的是氧化反应而不是加成反应。
√
课后巩固评价
√
随堂巩固
3.(2020·福州高一检测)下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,回答下列问题。
课后巩固评价
(1)C装置中反应的化学方程式为__________________。
(2)B装置中可观察到的现象是____________。
(3)查阅资料,乙烯与酸性高锰酸钾溶液反应产生二氧化碳,反应类型为______。
(4)下列物质中,可以通过乙烯的加成反应得到的是________(填字母)。
A.CH3CH3
B.CH3CHCl2 C.CH3CH2OH
答案
(1)CH2===CH2+Br2―→BrCH2—CH2Br
(2)溶液紫(或紫红)色褪去
(3)氧化反应
(4)AC
课后巩固评价
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
