解答题3——2023年浙江省中考科学特训练习(含解析)
文档属性
| 名称 | 解答题3——2023年浙江省中考科学特训练习(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-05-04 00:00:00 | ||
图片预览



文档简介
解答题3——2023年浙江省中考科学特训练习
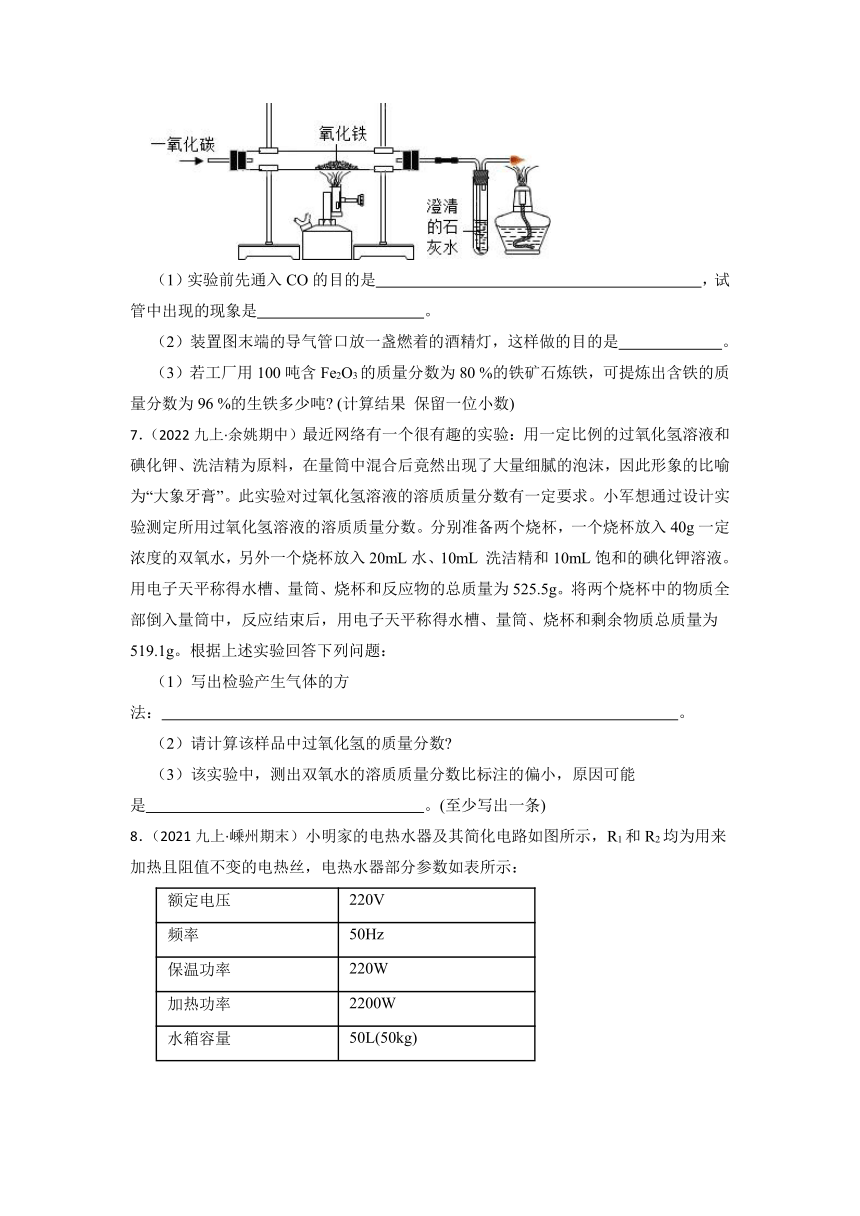
1.(2021九上·舟山期末)人体血液循环系统由心脏、血管和血液组成,图甲表示心脏局部结构与主动脉弹性作用示意图,图乙表示各类血管结构示意图。请据图回答下列问题:
(1)心脏为血液循环提供动力。心脏有四个腔,除图甲中所示的两个腔外,还包括
(2)由图甲可知,左心室收缩时,① (填结构名称)关闭,②动脉瓣打开,血液的流动途径是左心室→ →各级动脉→毛细血管,与组织细胞进行物质交换。
(3)由图甲可知,左心室舒张时,②动脉瓣关闭,但血液还在连续流动,是因为血管A中暂时储存着部分血液,此时血管A弹性回缩,使暂存的血液继续流向组织细胞。由血管A的功能可推断它的结构,图乙中表示血管A的是 (选填序号)。
(4)图甲和图乙表明,生物的结构与功能相适应。请你说出与人体小肠消化功能相适应的结构特点 。(写出两种即可)
2.(2022·滨江模拟)国之重器一新光华号半潜船,为10万吨级半潜船,是国内最大、全球第二大半潜船。该轮船总长255米,宽68米,下潜吃水深度30.5米,空载时的质量为51500吨,载重量为98000吨。全船有118个压载水舱,每一个压载水舱都有一个阀门。装载前半潜船空载漂浮于海面,装载时需向船体水舱注水,船体重力增加,巨大的甲板下沉至海面以下,拖船将漂浮的货物拖至半潜船的甲板上方并固定好,半潜船排出水舱中的水,甲板上浮刚好至海面,半潜船就可以驮着货物离开,如图所示。
(1)半潜船是靠改变什么来实现上浮和下沉的?
(2)求半潜船空载时浸入海水的体积。(海水密度为1.03×103千克/米3)
(3)半潜船在如图所示空载、下沉、载货的三种状态下所受的浮力分别为F1、F2、F3,分析比较它们的大小关系。
3.(2022九上·舟山期中)含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,据图回答:(结果保留0.1%)
(1)写出PM段所观察到现象 。
(2)P点时溶液中的溶质是 。
(3)求M点溶液中溶质的质量。
(4)求出m1的值
4.(2022九上·杭州期中)某同学称取13.3g的NaOH样品(杂质为Na2CO3),加水配成溶液100g,然后向溶液中逐滴加入稀盘酸,根据生成CO2的质量测定Na2CO3的质量。实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示。
(1)据图可知完全反应后生成的二氧化碳质量为 克。
(2)求样品中Na2CO3的质量分数。
(3)求反应结束后所得溶液的溶质质量为 克。
5.(2022·温州模拟)研究性小组开展了《温室效应研究》的课题。温室效应是由大气中的大量二氧化碳、氟氯烃、甲烷和水蒸气等温室气体引起,其中主要是二氧化碳,像玻璃罩一样紧紧地照在我们的上空,如图甲所示,太阳照射在地球上的热量无法逸散,从而出现地球增温的现象。
物质 大气中的含量(体积百分比) 温窒效应指数
H2O 1 0.1
CO2 0.03 1
CH4 2×10-4 30
(1)在图乙实验中,控制温度计初温相同,得到 现象,说明甲烷也是产生温室效应的气体。
(2)小海同学用鸡蛋壳制取二氧化碳如图丙所示,他取6g鸡蛋壳(鸡蛋壳中的其他成分不与盐酸反应)于烧杯中,将100g稀盐酸平均四次分别加入烧杯中,测得部分实验数据如下。求稀盐酸的质量分数(写出计算过程,结果保留至0.1%)
实验次数 第一次 第二次 第三次 第四次
加入稀盐酸的质量 25 25 25 25
产生气体的总质量 m 2 n 2.2
(3)表中的“温室效应指数”指以二氧化碳为相对标准,测量一定大气压下每单位体积的气体所吸收的热量,表中展示了部分气体的数据,据此可得出,大气中水蒸汽和甲烷哪种气体对全球温室效应的影响更大,说明理由: 。
6.(2022九上·苍南期中)实验室可用如图装置模拟工业炼铁。
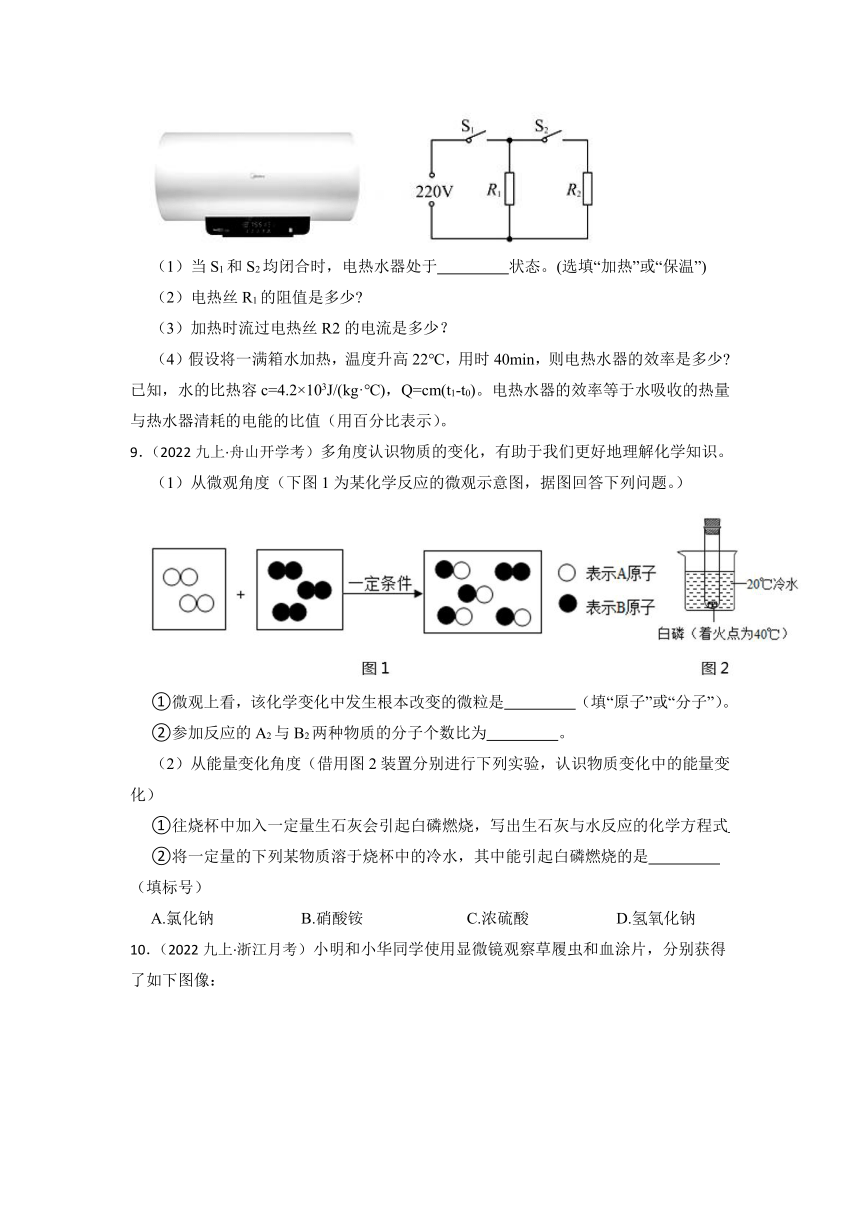
(1)实验前先通入CO的目的是 ,试管中出现的现象是 。
(2)装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是 。
(3)若工厂用100吨含Fe2O3的质量分数为80 %的铁矿石炼铁,可提炼出含铁的质量分数为96 %的生铁多少吨 (计算结果 保留一位小数)
7.(2022九上·余姚期中)最近网络有一个很有趣的实验:用一定比例的过氧化氢溶液和碘化钾、洗洁精为原料,在量筒中混合后竟然出现了大量细腻的泡沫,因此形象的比喻为“大象牙膏”。此实验对过氧化氢溶液的溶质质量分数有一定要求。小军想通过设计实验测定所用过氧化氢溶液的溶质质量分数。分别准备两个烧杯,一个烧杯放入40g一定浓度的双氧水,另外一个烧杯放入20mL水、10mL 洗洁精和10mL饱和的碘化钾溶液。用电子天平称得水槽、量筒、烧杯和反应物的总质量为525.5g。将两个烧杯中的物质全部倒入量筒中,反应结束后,用电子天平称得水槽、量筒、烧杯和剩余物质总质量为519.1g。根据上述实验回答下列问题:
(1)写出检验产生气体的方法: 。
(2)请计算该样品中过氧化氢的质量分数
(3)该实验中,测出双氧水的溶质质量分数比标注的偏小,原因可能是 。(至少写出一条)
8.(2021九上·嵊州期末)小明家的电热水器及其简化电路如图所示,R1和R2均为用来加热且阻值不变的电热丝,电热水器部分参数如表所示:
额定电压 220V
频率 50Hz
保温功率 220W
加热功率 2200W
水箱容量 50L(50kg)
(1)当S1和S2均闭合时,电热水器处于 状态。(选填“加热”或“保温”)
(2)电热丝R1的阻值是多少
(3)加热时流过电热丝R2的电流是多少?
(4)假设将一满箱水加热,温度升高22℃,用时40min,则电热水器的效率是多少 已知,水的比热容c=4.2×103J/(kg·℃),Q=cm(t1-t0)。电热水器的效率等于水吸收的热量与热水器清耗的电能的比值(用百分比表示)。
9.(2022九上·舟山开学考)多角度认识物质的变化,有助于我们更好地理解化学知识。
(1)从微观角度(下图1为某化学反应的微观示意图,据图回答下列问题。)
①微观上看,该化学变化中发生根本改变的微粒是 (填“原子”或“分子”)。
②参加反应的A2与B2两种物质的分子个数比为 。
(2)从能量变化角度(借用图2装置分别进行下列实验,认识物质变化中的能量变化)
①往烧杯中加入一定量生石灰会引起白磷燃烧,写出生石灰与水反应的化学方程式
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是 (填标号)
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
10.(2022九上·浙江月考)小明和小华同学使用显微镜观察草履虫和血涂片,分别获得了如下图像:
(1)小明想将视野中如图甲所示的像转化成如图乙所示的像,则应将载玻片 ( )
A.顺时针转动 90° B.逆时针转动 90°
C.向左上角移动 D.向右下角移动
(2)小华图中的①、②、③是视野中观察到的三种血细胞。其中能保护身体,抵抗细菌等侵袭,参与非特异性免疫的是 (填图中的序号) 。
(3)人的ABO血型由红细胞上凝集原的种类决定。已知甲、乙、丙、丁四人的ABO血型各不相同,丙、丁的红细胞能与B型血的血清发生凝集反应,又知丁的血清能与乙的红细胞发生凝集反应。则甲的血型是 。
11.(2022·萧山期中)如图甲所示,柱形容器内装有深度大于10cm的某种液体,物体C是一个体积为1000cm3的均匀正方体,质量为480g。在液体中静止时,有2/5的体积露出液面。则:
(1)图甲中物体C静止时所受的浮力为多少?
(2)液体的密度为多少?
(3)若在C上表面放置一个物体A,使C恰好完全浸没于液体中,则物体A的质量应为多少?
12.(2022九下·义乌开学考)电梯的简化模型如图甲所示,考虑安全、舒适、省时等因素,电梯速度要经过增大、不变和 减小的过程。这一过程是通过改变拉力大小来实现的。某次上升过程中电梯所受拉力 F 随上升高 度 h 变化的图象如图乙所示。这个过程用时 1 分钟,求这个过程中:
(1)电梯上升的平均速度;
(2)拉力做的功;
(3)拉力做功的功率。
13.(2022九上·宁波月考)高氯酸是已知酸中酸性最强的酸,化学式:HClO4。
(1)高氯酸由 种元素组成。
(2)高氯酸中氢、氯两种元素的质量比为 。
(3)若在高氯酸的无色溶液中滴入紫色石蕊试液,观察到溶液呈 色。
14.(2022·宁波模拟)如图所示为某研究性学习小组参观某农场时绘出的模式图。
(1)请写出图中的一条食物链: 。
(2)将蘑菇房与蔬菜大棚相通,可提高蔬菜产量,其原因是 。
(3)大棚蔬菜种植过程中发现:如果在大棚内长期使用某种农药,害虫对这种农药的抗药性会越来越强。下列关于害虫抗药性的说法正确的 (填字母).
A.害虫抗药性的增强是农药对害虫不断选择的结果
B.对害虫来说抗药性变异是有利变异
C.害虫能够将抗药性变异遗传给下一代
D.害虫的抗药性是在农药的作用下产生的
15.(2022·温州模拟)自然界中生物的能量都直接或间接来自太阳能,绿色植物通过光合作用,将太阳能转化为化学能储存,其他生物通过一定方式,直接或间接从植物中获取能量。
请回答以下问题:
(1)如图是生物生命活动的能量流动的示意图,图中各成分还不能构成一个生态系统,从生态系统的组成成分分析,还缺乏 .
(2)图中共有四种生物,鹰、鼬、鼠、小麦,请写出一条食物链: 。
(3)能量在沿食物链流动的过程中,会不断减少,试分析原因: 。
16.(2023·宁波模拟)如图所示是我国具有完全自主知识产权的大型喷气式民用飞机C919从上海飞抵海口开展验证飞行。在海口美兰机场接受“过水门”仪式。若C919匀速巡航432 km,用时40分钟,共消耗航空燃油3t,飞机发动机的功率为3.6×103W。求: (航空燃油的热值为5×107J/kg)
(1)C919在匀速巡航中的速度。
(2)C919在匀速巡航中所受的阻力。
(3)C919在匀速巡航中发动机的工作效率。
17.(2021九上·新昌期末)向一定量的氢氧化钡溶液中先滴加硫酸铜溶液,反应生成沉淀的质量如图所示。向反应后的溶液中再滴加足量的稀硫酸,请分析沉淀质量随加入稀硫酸的变化关系,并将变化关系画在图上。(提示:当同时存在可溶性碱与难溶性碱时,酸先与可溶性碱反应)
18.(2022·嵊州模拟)现有一份水垢样品,其成分为氢氧化镁和碳酸钙。已知:氢氧化镁受热易分解,反应的化学方程式为:Mg(OH)2=加热=MgO+H2O;碳酸钙高温下才分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如图所示。
(1)水垢样品受热分解生成的水的质量为 。
(2)水垢样品中Mg(OH)2的质量分数为多少 (精确到0.1%)
(3) x的值为多少 (要写出计算过程)
(4)当剩余固体中钙元素的质量分数为36.0%时,剩余固体的成分是 .
19.(2022·温州)小设计了如图甲所示的多功能电饭煲模拟电路,能实现“煮饭时保持高温快煮,快煮后自动保温”。
〖电路简介〗
工作电路:S1为电源开关;S2为定时器开关,其闭合后自动开始计时,计时结束后自动断开,不再闭合;R1为可调电阻;R2为电饭堡内的电热丝。
控制电路:电磁继电器A和B完全相同,Ra和Rb是分别安装在电饭堡内的热敏电阻,它们的阻值随温度的变化如图乙所示,当温度达到120℃时,La就吸引弹性衔铁使Sa断开,当温度降到110℃时,La释放弹性衔铁使Sa闭合。
〖快煮模式〗闭合开关S、S1、S2,电饭煲进入快煮模式直至定时开关S2自动断开。在快煮过程中温度将维持在110℃~120℃,工作电路的电热丝在高功率和低功率之间切换,其功率随时间变化如图丙所示。
〖保温模式〗开关S2断开后,电饭煲进入保温模式,最后温度维持在60℃~80℃。
(1)由图丙可知,电饭煲在24分钟快煮过程中,电热丝高功率加热的时间为 分钟。
(2)若R1接入电路的阻值为840欧,R2阻值为40欧,工作电路电源电压为220伏,则电饭煲完成一次快煮,电热R2消耗的电能为多少焦?
(3)请结合图甲、乙说明开关S2断开后,电饭煲实现自动保温的工作原理。
20.(2022九上·余姚期末)如图甲为陶瓷电煎药查,其简化的工作电路如图乙所示,电源电压为220V,S1为单刀双掷开关,R1和R2均为电加热丝。电煎药壶刚开始工作时先武火档快速加热,当药液的温度达到98℃时自动跳到文火档慢熬,药液熬制一段时间后自动跳到保温档防止药液烧干。已知电煎药壶在220V电压下正常工作时,武火快速加热功率为500w,文火慢熬功率为100W,某次救药时药液的温度与电煎药壶工作时间的关系图像如图丙所示。
(1)根据题意可知,当单刀双掷开关S1拨到“2"位置,同时开关S2 (填 “闭合"或“断开”)时,电煎药壶处于文火档。
(2)电加热丝R2的阻值是 欧。
(3)求电煎药壶处于保温档时的功率。
(4)分析图像可知,电放药壶武火加热前半段时间对药液的加热效率 。(填 “大于”“小于”或“等于”)后半段时间的加热效率。
答案解析部分
1.(1)右心房、左心房
(2)房室辫;主动脉
(3)③
(4)小肠很长,小肠内表面有许多皱襞,皱襞上有许多小肠毛绒、小肠内有多种消化液
【解析】1.心脏主要由心肌构成。它有4个空腔,按照位置关系,这4个腔分别叫作左心房、左心室、右心房、右心室。
2.体循环的路线为:左心室→主动脉→全身各级动脉→全身各处毛细血管→全身各级静脉→上、下腔静脉→右心房。
3.血液的变化:血液流经身体各部分组织细胞周围的毛细血管时,把氧气输送给细胞,把细胞产生的二氧化碳等废物带走,血液由动脉血变成静脉血。
(1)心脏为血液循环提供动力。心脏有四个腔,除图甲中所示的两个腔外,还包括右心房、左心房。
(2)由图甲可知,左心室收缩时,①房室辫关闭,②动脉瓣打开,血液的流动途径是左心室→主动脉→各级动脉→毛细血管,与组织细胞进行物质交换。
(3)动脉是由心室发出的血管,在行程中断分支,形成大、中、小动脉。动脉由于承受较大的压力,管壁较厚,管腔断面呈圆形。
静脉是引导血液回心的血管,小静脉起于毛细血管网,行程中逐渐汇成中静脉、大静脉,最后开口于心房。静脉因所承受压力小,故管壁薄、平滑肌和弹力纤维均较少,弹性和收缩性均较弱,管腔在断面上呈扁椭圆形。故图乙中③表示的是动脉。图甲中血管A表示主动脉。图乙中表示血管A的是③。
(4)人体小肠消化功能相适应的结构特点:小肠很长,小肠内表面有许多皱襞,皱襞上有许多小肠毛绒、小肠内有多种消化液。
2.(1)根据“装载时需向船体水舱注水,船体重力增加,巨大的甲板下沉至海面以下”可知,半潜船是靠改变水舱里面水的多少,也就是改变自身重力实现下沉和上浮的。
(2)半潜船空载时的质量为51500吨,
则它受到的浮力F浮=G;
ρ液gV排=mg;
ρ液V排=m;
即:。
(3)根据图片可知,半潜船排开水的体积:V空载【解析】(1)根据题目的描述分析半潜船浮沉的原理;
(2)根据浮沉条件和阿基米德原理计算出空载时排开海水的体积;
(3)根据图片比较半潜船排开海水的体积,然后根据阿基米德原理F浮=ρ液gV排比较所受到浮力的大小。
3.(1)产生蓝色絮状沉淀
(2)CuCl2和NaCl
(3)解:由图像可知,氢氧化钠与氯化铜反应生成氢氧化铜质量为9.8g,设此时生成氯化钠质量为x
CuCl2 +2NaOH=Cu(OH)2 +2NaCl
98 117
9.8g x
98:117=9.8g:x
x=11.7g
与盐酸反应的氢氧化钠质量为40g×10%=4g,依据钠元素质量守恒可知,此时生成氯化钠质量为,则 M点溶液中溶质的质量 5.85g+11.7g=17.55g ;
(4)解:设与氯化铜反应消耗氢氧化钠溶液质量为y
CuCl2 +2NaOH=Cu(OH)2 +2NaCl
80 98
10%y 9.8g
80:98=10%y:9.8g
y=80g
则 m1 =40g+80g=120g.
【解析】(1)根据向氯化铜和盐酸的混合溶液中加入氢氧化钠,氢氧化钠先与盐酸反应,然后再与氯化铜反应,氯化铜与氢氧化钠的反应生成氢氧化铜沉淀分析;
(2)根据p点盐酸恰好完全反应分析;
(3)根据生成氢氧化铜沉淀质量及方程式中物质间质量关系计算生成氯化钠质量,由与盐酸反应的氢氧化钠质量计算生成氯化钠质量,M点对应溶质为两份氯化钠之和分析;
(4)根据氢氧化铜质量计算出与氯化铜反应的氢氧化钠溶液质量,再由图像确定与盐酸反应的氢氧化钠溶液质量,从而计算m1数值分析。
(1)向氯化铜和盐酸的混合溶液中加入氢氧化钠,氢氧化钠先与盐酸反应,然后再与氯化铜反应,PM段为氯化铜与氢氧化钠的反应,现象是产生蓝色沉淀;
(2)P点为盐酸恰好与氢氧化钠反应的点,溶液中溶质为氯化钠和氯化铜;
4.(1)2.2
(2)解:设样品中碳酸钠的质量为x。碳酸钠与盐酸反应产生的氯化钠质量为y,氢氧化钠与盐酸反应产生的氯化钠质量为z。
Na2CO3+2HCl= 2NaCl+H2O+ CO2↑
106 117 44
x y 2.2g
得x=5.3g;y=5.85g
NaOH+HCl= NaCl+H2O
40 58.5
13.3g-x z
13.3g-5.3g =8g
(3)17.55
【解析】由图示确定出生成二氧化碳质量,再由二氧化碳质量及方程式中物质间质量关系计算出固体碳酸钠质量和碳酸钠生成的氯化钠质量,再由总固体质量计算出氢氧化钠质量,再计算出氢氧化钠反应生成的氯化钠质量,从而计算碳酸钠质量分数及反应后溶液中溶质质量。
(1)由图示可知,最终反应完全后产生二氧化碳质量为2.2克;
(3)反应结束后所得溶液的溶质为氯化钠,设氢氧化钠反应生成氯化钠质量为z
NaOH+HCl= NaCl+H2O
40
8g 58.5
z
40:58.5=8g:z
z=11.7g
则总的氯化钠质量为5.85g+11.7g=17.55g。
故答案为:(1)2.2;(2)39.8%;(3)17.55.
5.(1)盛有甲烷气体的锥形瓶温度高
(2)根据表格分析,第二次盐酸反应完,产生二氧化碳气体的质量为2.克。
设稀盐酸的质量为X。
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
X 2g
x=3.32g
稀盐酸的质量分数:
(3)甲烷温室效应指数是水蒸气的300倍
【解析】研究产生温室效应的气体:二氧化碳、甲烷、二氧化氮等气体;所以实验中要测温度,证明CO2是产生温室效应的气体,要与空气作对比,比较谁的温度变化较大,根据二氧化碳的来源来分析采取的防止“温室效应”的措施。
再根据实验的注意事项分析。
(1)图乙装置研究产生温室效应的气体为甲烷,它与空气形成对比;在图乙实验中,控制温度计初温相同,得到盛有甲烷气体的锥形瓶温度高现象,说明甲烷也是产生温室效应的气体。
(2)根据表格分析,第二次盐酸反应完,产生二氧化碳气体的质量为2.克。
设稀盐酸的质量为X。
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
X 2g
x=3.32g
稀盐酸的质量分数:
(3)根据表格数据分析,甲烷温室效应指数比二氧化碳高很多,故甲烷对全球温室效应的影响更大,因为其温室效应指数是水蒸气的300倍。
6.(1)排尽装置内原有的空气,避免发生爆炸。;澄清石灰水变浑浊
(2)除去尾气
(3)设可提炼出含铁的质量分数为96 %的生铁质量为x
3CO+Fe2O32Fe+3CO2
160 112
100t×80% 96%x
160:112=(100t×80%):96%x
x=58.3t
【解析】(1)根据CO与空气混合加热易发生爆炸分析;
(2)根据尾气中CO污染空气分析;
(3)根据铁矿石中氧化铁的纯度先计算氧化铁的质量,再利用方程式中物质间质量关系计算铁的质量分析。
(1)CO与空气混合加热易发生爆炸,实验前先通入CO的目的是排尽装置内原有的空气,避免发生爆炸,一氧化碳与氧化铁反应会产生二氧化碳,二氧化碳会使澄清石灰水变浑浊;
(2)尾气中含有CO,排放到空气中会污染空气, 装置图末端的导气管口放一盏燃着的酒精灯,是会了除去尾气;
(3)设可提炼出含铁的质量分数为96 %的生铁质量为x
3CO+Fe2O32Fe+3CO2
160 112
100t×80% 96%x
160:112=(100t×80%):96%x
x=58.3t
故答案为:(1)排尽装置内原有的空气,避免发生爆炸;澄清石灰水变浑浊;(2)除去尾气;(3)58.3t。
7.(1)用带火星木条靠近量筒口处的泡沫附近,若木条复燃,则证明是氧气
(2)由实验可知,反应后产生氧气质量为525.5g-519.1g=6.4g
设过氧化氢溶液质量分数为x
2H2O2=2H2O+O2↑
68 32
40gx 6.4g
68:32=40gx:6.4g
x=34%
(3)部分氧气还残留在量筒内的泡沫中
【解析】(1)根据氧气的验证方法分析;
(2)根据反应后减少质量为生成氧气质量,利用方程式中物质间质量关系计算过氧化氢溶液的浓度分析;
(3)根据反应后氧气可能会残留在量筒内分析。
(1)过氧化氢分解会产生氧气,用用带火星木条靠近量筒口处的泡沫附近,若木条复燃,则证明是氧气;
(2)由实验可知,反应后产生氧气质量为525.5g-519.1g=6.4g
设过氧化氢溶液质量分数为x
2H2O2=2H2O+O2↑
68 32
40gx 6.4g
68:32=40gx:6.4g
x=34%
(3)反应后装置内可能有氧气残留,若部分氧气还残留在量筒内的泡沫中,会使得结果偏小。
故答案为:(1)用带火星木条靠近量筒口处的泡沫附近,若木条复燃,则证明是氧气;(3) 部分氧气还残留在量筒内的泡沫中。
8.(1)加热
(2)解:R1= =220欧
(3)解:P2=2200瓦-200瓦=1980瓦
I2= =9安
(4)解:Q=Cm(t1-t0)=4200 J/(Kg·℃) ×50Kg×22℃=4.62×106焦
W=Pt=2200瓦×40×60秒=5.28×106焦
η= =87.5%
【解析】(1)根据功率公式比较两种状态下总功率的大小,从而确定对应的状态。
(2)根据公式 计算出R1的电阻;
(3)首先根据P2=P热-P保计算出R2的电功率,再根据 计算出通过它的电流。
(4)根据公式Q=cm(t1-t0)计算出水吸收的热量,再根据W=Pt计算出消耗的电能,最后根据 计算出电热水器的效率。
(1)当开关S1闭合时,只有R1工作,此时的总电阻为R1;
当开关S1和S2闭合时,R1与R2并联,此时的总电阻为R并;
则R1>R并;
根据公式可知,当电压相同时,功率与电阻成反比;
则功率P1那么前者为保温状态,后者为加热状态。
9.(1)分子;1:1
(2);CD
【解析】(1)①根据图1确定分子和原子是否发生改变;
②将图1中反应前后都存在的分子去掉,然后确定参加反应的物质的分子数之比。
(2)①确定反应物、反应条件和生成物,据此写出反应的化学方程式。
②根据物质溶于水时吸热还是放热解答。
(1)①根据图1可知,反应前后原子的种类没有改变,而分子的种类发生改变;
②根据图1可知,反应前后共同存在一个,将其去掉后如下图所示:
则参加反应的A2与B2两种物质的分子个数比为:2:2=1:1。
(2)①生石灰与水反应,生成氢氧化钙,反应的方程式为: 。
②白磷燃烧需要将温度升高到着火点,因此放入冷水中的物质溶解时应该向外放热。
氯化钠溶于水时水温几乎不变,故A不合题意;
硝酸铵溶于水时吸热,温度降低,故B不合题意;
浓硫酸溶于水时放热,温度升高,故C符合题意;
氢氧化钠溶于水时放热,温度升高,故D符合题意。
故选CD。
10.(1)B
(2)③
(3)O 型
【解析】血清中的凝集素能与红细胞外面的凝集原发生凝集反应,B血型中有抗A凝集素,他能和A型或AB型血发生凝集反应;A凝集原遇到抗A凝集素会发生凝集反应;红细胞,内含血红蛋白,帮助氧气的运输,血小板,有加快凝血的作用,白细胞, 能保护身体,抵抗细菌等侵袭;
(1)显微镜成倒立的像,物像的移动方向和玻片中的移动方向相反,但是旋转方向不受影响,因此图甲逆时针旋转90°后得到物像是图乙;
(2)①是红细胞,内含血红蛋白,帮助氧气的运输;②是血小板,有加快凝血的作用;③是白细胞, 能保护身体,抵抗细菌等侵袭 ,参与非特异性免疫;
(3)血清中的凝集素能与红细胞外面的凝集原发生凝集反应; 丙、丁的红细胞能与B型血的血清发生凝集反应, B型血中由抗A凝集素,所以丙和丁,有一个为A型,一个为AB型;又已知丁的血清能与乙的红细胞发生凝集反应。说明丁是A型血,丙是AB型血,乙是B型血,那么甲是O型血;
故答案为:(1)B(2)③(3) O 型
11.(1)解:F浮=mg=0.48kg×10N/kg=4.8N
(2)解:ρ液= =800kg/m3
(3)解:G总=F浮=ρ液gV排=800kg/m3×10N/kg×1×10-3m3=8N
m总= =0.8kg
mA=0.8kg-0.48kg=0.32kg
【解析】(1)当物体漂浮在液面上时,它受到的重力与浮力为一对平衡力,即F浮=G=mg;
(2)根据阿基米德原理的变形式 计算出液体的密度;
(3)当物体A全部浸没时,它受到向上的浮力,向下的重力与压力,而压力等于A的重力。根据二力平衡的条件得到:F浮=G+GA。首先根据阿基米德原理 F浮=ρ液gV排 计算出此时的浮力,再根据前面的关系计算出A的重力,最后计算A的质量即可。
12.(1)解:电梯上升的高度h=48m,用时间t﹦60s,
电梯上升的平均速度:v= =0.8m/s
答:电梯上升的平均速度为0.8m/s
(2)解:拉力在0﹣4m做的功:W1=F1h1=2.5×104N×4m=1.0×105J,
拉力在4﹣44m做的功:W2=F2h2=2.0×104N×40m=8.0×105J,
拉力在44﹣48m做的功:W3=F3h3=1.5×104N×4m=0.6×105J,
所以,上升过程拉力做的功:W=W1+W2+W3=1.0×105J+8.0×105J+0.6×105J=9.6×105J
答:拉力做的功是9.6×105J
(3)解:拉力做功的功率:P= =1.6×104W
答:拉力做功的功率是1.6×104W
【解析】(1)已知高度和时间,根据公式计算电梯上升的速度;
(2)根据图乙,分别确定每段距离对应的拉力,然后根据W=Fs分别计算出所做的功,最后将它们相加即可。
(3)根据公式 计算拉力做功的功率。
13.(1)三或3
(2)2:71
(3)红
【解析】(1)根据化学式确定物质元素组成分析;(2)根据元素质量比为相对原子质量×原子个数之比分析;(3)根据酸性溶液能使石蕊变红分析。
(1)高氯酸由氢、氯、氧三种元素组成;
(2) 高氯酸中氢、氯两种元素的质量比为 1:35.5=2:71;
(3) 高氯酸呈酸性,若在高氯酸的无色溶液中滴入紫色石蕊试液,观察到溶液呈红色。
故答案为:(1)三;(2)2:71;(3)红。
14.(1)大豆、玉米→鸡→人
(2)蘑菇细胞呼吸放出二氧化碳,为蔬菜的光合作用提供原料
(3)A;B
【解析】1.生态工程是指人类利用生态学和系统学等学科的基本原理和方法,通过系统设计、调控和技术组装,对已经破坏的生态系统进行修复重建,对造成环境污染和破坏的传统生产方式进行改善,并提高生态系统的生产力,从而促进人类社会与自然环境的和谐发展;生态工程的特点是:少消耗,多效益,可持续;生态系统的基本原理包括,物质循环再生原理,物种多样性原理,整体性原理,协调与平衡原理,系统学和工程学原理。
2.食物链是生态系统中生物之间由食物关系而形成的一种链状结构.每条食物链的起点都是生产者(绿色植物),箭头指向初级消费者(植食性动物)箭头指向次级消费者(食肉动物),到最高营养级结束。
(1)图中的一条食物链: 大豆、玉米→鸡→人 。
(2)将蘑菇房与蔬菜大棚相通,可提高蔬菜产量,其原因是蘑菇细胞呼吸放出二氧化碳,为蔬菜的光合作用提供原料。
(3)大棚蔬菜种植过程中发现:如果在大棚内长期使用某种农药,害虫对这种农药的抗药性会越来越强。关于害虫抗药性的说法正确的A:害虫抗药性的增强是农药对害虫不断选择的结果;B:对害虫来说抗药性变异是有利变异。
故选AB。
15.(1)分解者
(2)小麦→鼠→鹰( 小麦→鼠→鼬)
(3)①本身生命活动消耗能量;②生物遗体、遗物内含能量。(合理即可)
【解析】(1)生态系统包括生物成分和非生物成分,生物成分包括生产者、分解者和消费者;非生物成分包括阳光、空气、水分等因素。
(2)食物链是生产者和消费者之间由于食物关系而构成链条.它表示的是生产者和消费者之间的关系。其写法是:起点是生产者,依次是初级消费者、次级消费者、三级消费者...一直到最高消费者,中间用箭头连接,箭头总是指向捕食者。
(1)如图是生物生命活动的能量流动的示意图,图中各成分还不能构成一个生态系统,从生态系统的组成成分分析,还缺乏分解者。
(2)图中共有四种生物,鹰、鼬、鼠、小麦,一条食物链:小麦→鼠→鹰( 小麦→鼠→鼬)。
(3)能量在沿食物链流动的过程中,会不断减少,试分析原因:①本身生命活动消耗能量;②生物遗体、遗物内含能量。
16.(1)v= = 180 m/s
答:C919在匀速巡航中的速度为180 m/s
(2)f=F率= =2×105N
答:C919在匀速巡航中所受的阻力为2×105N
(3)Q放= mq=3×103kg×5×107J/kg=1.5×1011J
η= = 57.6%
答:C919在匀速巡航中发动机的工作效率为57.6%
【解析】(1)根据公式计算飞机的巡航速度。
(2)首先根据功率的计算式计算出飞机发动机产生的牵引力,再根据二力平衡的知识计算飞机受到的阻力,即f=F。
(3)根据Q放=qm计算出燃油完全燃烧放出的热量,再根据W=Pt计算飞机发动机做的机械功,最后根据公式 计算发动机的工作效率。
17.加入的硫酸铜与氢氧化钡发生反应, ;
当氢氧化钡完全反应,加入的稀硫酸与生成的沉淀 反应, ,导致沉淀质量减少,但因为还有沉淀 ,所以沉淀质量不会等于0;当氢氧化钡未完全反应,加入的稀硫酸先与氢氧化钡反应, ,沉淀质量先增加,再与沉淀 反应,导致沉淀质量减少,反应完全后沉淀质量最后保持不变。
【解析】根据氢氧化钡溶液中先滴加硫酸铜溶液,硫酸铜与氢氧化钡反应生成氢氧化铜和硫酸钡两种沉淀,氢氧化钡可能恰好完全反应,也可能有剩余,再加入稀硫酸时,若氢氧化钡有剩余,则沉淀会继续增加,至氢氧化钡完全反应,然后硫酸再与氢氧化铜反应,沉淀再减少,至氢氧化铜完全反应后保持不变,若氢氧化钡完全反应,则加入硫酸后,氢氧化铜与硫酸反应,沉淀减少,至氢氧化铜完全反应后保持不变分析。
18.(1)0.9
(2)解:Mg(OH)2 的质量为2.9克,Mg(OH)2%=22.5%
(3)解:生成CaO的质量为5.6克,MgO的质量为2克,x=5.6+2=7.6克
另法:生成CO2的质量为4.4克,x=12-4.4=7.6 克
(4)MgO CaO CaCO3
【解析】根据图片可知,从a~b,固体的质量不断减小,应该为氢氧化镁分解,生成氧化镁和水。从b~c,固体质量不变,此时氢氧化镁完全反应,而温度尚未达到碳酸钙的分解温度。从c~d时,固体质量不断减小,即碳酸钙分解生成氧化钙和二氧化碳。从d~e,固体的质量保持不变,即整个分解反应结束,据此分析解答。
(1)水垢样品中分解生成水的质量为:12.9g-12g=0.9g;
(2)设氢氧化镁的质量为x,生成氧化镁的质量为y;
;
58 40 18
xg y 0.9g
;
解得:x=2.9g,y=2g;
水垢样品中氢氧化镁的质量分数:;
(3)碳酸钙的质量为:12.9g-2.9g=10g;
设反应生成氧化钙的质量为z,
;
100 56
10g z
;
解得:z=5.6g;
那么最终剩余固体的质量为:x=2g+5.6g=7.6g。
(4)根据上面的计算可知,如果剩余固体为氧化镁和氧化钙,
那么其中钙元素的质量分数为:;
而实际钙元素的质量分数为36%<53%,
那么碳酸钙应该没有完全分解;
即剩余固体的成分是MgO、CaO和CaCO3。
19.(1)12
(2)解:R总=R1+R2=840欧+40欧=880欧
I= = = 0.25安
由W=UIt得:
W1=I2R2t1=(0.25安)2×40欧×720秒=1800焦
W1= = =8.712×105焦
W总=W1+W2=8.712×105焦+1800焦=8.73×105焦
答:电饭煲完成一次快煮,电热丝R2消耗的电能为8.73×105焦。
(3)当S2断开后,R2低功率工作,降温至110℃及以下,Sa始终闭合。继续降温至60℃时,Sb闭合,R1被短路,R2高功率工作,升温至80℃时,Sb断开,R1与R2串联,R2低功率工作,开始降温,如此往复,实现自动保温。
【解析】(1)根据图丙找到电热丝高功率工作的时间段,然后将它们相加即可。
(2)当低功率工作时,两个电阻串联,根据 R总=R1+R2 计算出此时的总电阻,再根据 计算出此时的总电流,接下来根据 W1=I2R2t1 计算出R2消耗的电能。高功率工作时,只有R2自己工作,根据公式 计算出它消耗的电能,最后将两个电能相加即可。
(3)注意分析温度变化时,两个热敏电阻对电路状态的影响,结合电功率的变化分析自动保温原理。
(1)根据图丙可知,快煮24分钟内电热丝高功率加热的时间:t=6min+(11-9)min+(16-14)min+(21-19)min=12min。
20.(1)断开
(2)484
(3)解:当开关S1接2、S2闭合时,R1与R2并联,电煎药壶处于武火挡,
因并联电路中各支路独立工作、互不影响,且电路的总功率等于各用电器功率之和,所以,电加热丝R1的电功率: P1=P武火-P文火= 500W- 100W= 400W,
因并联电路中各支路两端的电压相等,
所以,电加热丝R1的阻值: R1= =121Ω,
当开关S1接1、S2断开时,R1与R2串联,电煎药壶处于保温挡,
电煎药壶处于保温挡时的功率: P保温= =80W
答:电煎药壶处于保温挡时的功率80W
(4)小于
【解析】(1)根据公式比较开关在不同组合时的总功率大小,从而确定所处的状态;
(2)当开关S1接“2”,S2断开时,只有R2自己工作,此时为文火,根据公式计算出R2的阻值;
(3)对电路图进行分析可知,文火功率与武火功率的差就是电阻R1单独工作时的电功率,可根据计算R1的电阻。当开关S1接1、S2断开时,R1与R2串联,电煎药壶处于保温档,可根据 公式计算出此时的功率。
(4)根据加热效率分析解答。
(1)根据图片可知,当开关S1接“2”,S2闭合时,两个电阻并联,此时的总电阻为R并;
当开关S1接“2”,S2断开时,只有R2自己工作,此时电阻为R2;
当开关S1接“1”,S2断开时,两个电阻串联,此时电阻为R串;
则总电阻R并根据公式可知,总功率P并>P2>P串;
则三者对应的状态分别为:武火档、文火档和保温档。
(2)当开关S1接“2”,S2断开时,只有R2自己工作,此时为文火档,
R2的阻值;
(4)根据丙图可知,在武火档加热时,从0~7min时,药液温度上升:48℃-18℃=30℃;从7~14min时,药液温度升高:98℃-48℃=50℃。
根据公式可知,电热药壶武火加热前半段时间对药液的加热效率小于后半段时间的加热效率。
1.(2021九上·舟山期末)人体血液循环系统由心脏、血管和血液组成,图甲表示心脏局部结构与主动脉弹性作用示意图,图乙表示各类血管结构示意图。请据图回答下列问题:
(1)心脏为血液循环提供动力。心脏有四个腔,除图甲中所示的两个腔外,还包括
(2)由图甲可知,左心室收缩时,① (填结构名称)关闭,②动脉瓣打开,血液的流动途径是左心室→ →各级动脉→毛细血管,与组织细胞进行物质交换。
(3)由图甲可知,左心室舒张时,②动脉瓣关闭,但血液还在连续流动,是因为血管A中暂时储存着部分血液,此时血管A弹性回缩,使暂存的血液继续流向组织细胞。由血管A的功能可推断它的结构,图乙中表示血管A的是 (选填序号)。
(4)图甲和图乙表明,生物的结构与功能相适应。请你说出与人体小肠消化功能相适应的结构特点 。(写出两种即可)
2.(2022·滨江模拟)国之重器一新光华号半潜船,为10万吨级半潜船,是国内最大、全球第二大半潜船。该轮船总长255米,宽68米,下潜吃水深度30.5米,空载时的质量为51500吨,载重量为98000吨。全船有118个压载水舱,每一个压载水舱都有一个阀门。装载前半潜船空载漂浮于海面,装载时需向船体水舱注水,船体重力增加,巨大的甲板下沉至海面以下,拖船将漂浮的货物拖至半潜船的甲板上方并固定好,半潜船排出水舱中的水,甲板上浮刚好至海面,半潜船就可以驮着货物离开,如图所示。
(1)半潜船是靠改变什么来实现上浮和下沉的?
(2)求半潜船空载时浸入海水的体积。(海水密度为1.03×103千克/米3)
(3)半潜船在如图所示空载、下沉、载货的三种状态下所受的浮力分别为F1、F2、F3,分析比较它们的大小关系。
3.(2022九上·舟山期中)含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,据图回答:(结果保留0.1%)
(1)写出PM段所观察到现象 。
(2)P点时溶液中的溶质是 。
(3)求M点溶液中溶质的质量。
(4)求出m1的值
4.(2022九上·杭州期中)某同学称取13.3g的NaOH样品(杂质为Na2CO3),加水配成溶液100g,然后向溶液中逐滴加入稀盘酸,根据生成CO2的质量测定Na2CO3的质量。实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示。
(1)据图可知完全反应后生成的二氧化碳质量为 克。
(2)求样品中Na2CO3的质量分数。
(3)求反应结束后所得溶液的溶质质量为 克。
5.(2022·温州模拟)研究性小组开展了《温室效应研究》的课题。温室效应是由大气中的大量二氧化碳、氟氯烃、甲烷和水蒸气等温室气体引起,其中主要是二氧化碳,像玻璃罩一样紧紧地照在我们的上空,如图甲所示,太阳照射在地球上的热量无法逸散,从而出现地球增温的现象。
物质 大气中的含量(体积百分比) 温窒效应指数
H2O 1 0.1
CO2 0.03 1
CH4 2×10-4 30
(1)在图乙实验中,控制温度计初温相同,得到 现象,说明甲烷也是产生温室效应的气体。
(2)小海同学用鸡蛋壳制取二氧化碳如图丙所示,他取6g鸡蛋壳(鸡蛋壳中的其他成分不与盐酸反应)于烧杯中,将100g稀盐酸平均四次分别加入烧杯中,测得部分实验数据如下。求稀盐酸的质量分数(写出计算过程,结果保留至0.1%)
实验次数 第一次 第二次 第三次 第四次
加入稀盐酸的质量 25 25 25 25
产生气体的总质量 m 2 n 2.2
(3)表中的“温室效应指数”指以二氧化碳为相对标准,测量一定大气压下每单位体积的气体所吸收的热量,表中展示了部分气体的数据,据此可得出,大气中水蒸汽和甲烷哪种气体对全球温室效应的影响更大,说明理由: 。
6.(2022九上·苍南期中)实验室可用如图装置模拟工业炼铁。
(1)实验前先通入CO的目的是 ,试管中出现的现象是 。
(2)装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是 。
(3)若工厂用100吨含Fe2O3的质量分数为80 %的铁矿石炼铁,可提炼出含铁的质量分数为96 %的生铁多少吨 (计算结果 保留一位小数)
7.(2022九上·余姚期中)最近网络有一个很有趣的实验:用一定比例的过氧化氢溶液和碘化钾、洗洁精为原料,在量筒中混合后竟然出现了大量细腻的泡沫,因此形象的比喻为“大象牙膏”。此实验对过氧化氢溶液的溶质质量分数有一定要求。小军想通过设计实验测定所用过氧化氢溶液的溶质质量分数。分别准备两个烧杯,一个烧杯放入40g一定浓度的双氧水,另外一个烧杯放入20mL水、10mL 洗洁精和10mL饱和的碘化钾溶液。用电子天平称得水槽、量筒、烧杯和反应物的总质量为525.5g。将两个烧杯中的物质全部倒入量筒中,反应结束后,用电子天平称得水槽、量筒、烧杯和剩余物质总质量为519.1g。根据上述实验回答下列问题:
(1)写出检验产生气体的方法: 。
(2)请计算该样品中过氧化氢的质量分数
(3)该实验中,测出双氧水的溶质质量分数比标注的偏小,原因可能是 。(至少写出一条)
8.(2021九上·嵊州期末)小明家的电热水器及其简化电路如图所示,R1和R2均为用来加热且阻值不变的电热丝,电热水器部分参数如表所示:
额定电压 220V
频率 50Hz
保温功率 220W
加热功率 2200W
水箱容量 50L(50kg)
(1)当S1和S2均闭合时,电热水器处于 状态。(选填“加热”或“保温”)
(2)电热丝R1的阻值是多少
(3)加热时流过电热丝R2的电流是多少?
(4)假设将一满箱水加热,温度升高22℃,用时40min,则电热水器的效率是多少 已知,水的比热容c=4.2×103J/(kg·℃),Q=cm(t1-t0)。电热水器的效率等于水吸收的热量与热水器清耗的电能的比值(用百分比表示)。
9.(2022九上·舟山开学考)多角度认识物质的变化,有助于我们更好地理解化学知识。
(1)从微观角度(下图1为某化学反应的微观示意图,据图回答下列问题。)
①微观上看,该化学变化中发生根本改变的微粒是 (填“原子”或“分子”)。
②参加反应的A2与B2两种物质的分子个数比为 。
(2)从能量变化角度(借用图2装置分别进行下列实验,认识物质变化中的能量变化)
①往烧杯中加入一定量生石灰会引起白磷燃烧,写出生石灰与水反应的化学方程式
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是 (填标号)
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
10.(2022九上·浙江月考)小明和小华同学使用显微镜观察草履虫和血涂片,分别获得了如下图像:
(1)小明想将视野中如图甲所示的像转化成如图乙所示的像,则应将载玻片 ( )
A.顺时针转动 90° B.逆时针转动 90°
C.向左上角移动 D.向右下角移动
(2)小华图中的①、②、③是视野中观察到的三种血细胞。其中能保护身体,抵抗细菌等侵袭,参与非特异性免疫的是 (填图中的序号) 。
(3)人的ABO血型由红细胞上凝集原的种类决定。已知甲、乙、丙、丁四人的ABO血型各不相同,丙、丁的红细胞能与B型血的血清发生凝集反应,又知丁的血清能与乙的红细胞发生凝集反应。则甲的血型是 。
11.(2022·萧山期中)如图甲所示,柱形容器内装有深度大于10cm的某种液体,物体C是一个体积为1000cm3的均匀正方体,质量为480g。在液体中静止时,有2/5的体积露出液面。则:
(1)图甲中物体C静止时所受的浮力为多少?
(2)液体的密度为多少?
(3)若在C上表面放置一个物体A,使C恰好完全浸没于液体中,则物体A的质量应为多少?
12.(2022九下·义乌开学考)电梯的简化模型如图甲所示,考虑安全、舒适、省时等因素,电梯速度要经过增大、不变和 减小的过程。这一过程是通过改变拉力大小来实现的。某次上升过程中电梯所受拉力 F 随上升高 度 h 变化的图象如图乙所示。这个过程用时 1 分钟,求这个过程中:
(1)电梯上升的平均速度;
(2)拉力做的功;
(3)拉力做功的功率。
13.(2022九上·宁波月考)高氯酸是已知酸中酸性最强的酸,化学式:HClO4。
(1)高氯酸由 种元素组成。
(2)高氯酸中氢、氯两种元素的质量比为 。
(3)若在高氯酸的无色溶液中滴入紫色石蕊试液,观察到溶液呈 色。
14.(2022·宁波模拟)如图所示为某研究性学习小组参观某农场时绘出的模式图。
(1)请写出图中的一条食物链: 。
(2)将蘑菇房与蔬菜大棚相通,可提高蔬菜产量,其原因是 。
(3)大棚蔬菜种植过程中发现:如果在大棚内长期使用某种农药,害虫对这种农药的抗药性会越来越强。下列关于害虫抗药性的说法正确的 (填字母).
A.害虫抗药性的增强是农药对害虫不断选择的结果
B.对害虫来说抗药性变异是有利变异
C.害虫能够将抗药性变异遗传给下一代
D.害虫的抗药性是在农药的作用下产生的
15.(2022·温州模拟)自然界中生物的能量都直接或间接来自太阳能,绿色植物通过光合作用,将太阳能转化为化学能储存,其他生物通过一定方式,直接或间接从植物中获取能量。
请回答以下问题:
(1)如图是生物生命活动的能量流动的示意图,图中各成分还不能构成一个生态系统,从生态系统的组成成分分析,还缺乏 .
(2)图中共有四种生物,鹰、鼬、鼠、小麦,请写出一条食物链: 。
(3)能量在沿食物链流动的过程中,会不断减少,试分析原因: 。
16.(2023·宁波模拟)如图所示是我国具有完全自主知识产权的大型喷气式民用飞机C919从上海飞抵海口开展验证飞行。在海口美兰机场接受“过水门”仪式。若C919匀速巡航432 km,用时40分钟,共消耗航空燃油3t,飞机发动机的功率为3.6×103W。求: (航空燃油的热值为5×107J/kg)
(1)C919在匀速巡航中的速度。
(2)C919在匀速巡航中所受的阻力。
(3)C919在匀速巡航中发动机的工作效率。
17.(2021九上·新昌期末)向一定量的氢氧化钡溶液中先滴加硫酸铜溶液,反应生成沉淀的质量如图所示。向反应后的溶液中再滴加足量的稀硫酸,请分析沉淀质量随加入稀硫酸的变化关系,并将变化关系画在图上。(提示:当同时存在可溶性碱与难溶性碱时,酸先与可溶性碱反应)
18.(2022·嵊州模拟)现有一份水垢样品,其成分为氢氧化镁和碳酸钙。已知:氢氧化镁受热易分解,反应的化学方程式为:Mg(OH)2=加热=MgO+H2O;碳酸钙高温下才分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如图所示。
(1)水垢样品受热分解生成的水的质量为 。
(2)水垢样品中Mg(OH)2的质量分数为多少 (精确到0.1%)
(3) x的值为多少 (要写出计算过程)
(4)当剩余固体中钙元素的质量分数为36.0%时,剩余固体的成分是 .
19.(2022·温州)小设计了如图甲所示的多功能电饭煲模拟电路,能实现“煮饭时保持高温快煮,快煮后自动保温”。
〖电路简介〗
工作电路:S1为电源开关;S2为定时器开关,其闭合后自动开始计时,计时结束后自动断开,不再闭合;R1为可调电阻;R2为电饭堡内的电热丝。
控制电路:电磁继电器A和B完全相同,Ra和Rb是分别安装在电饭堡内的热敏电阻,它们的阻值随温度的变化如图乙所示,当温度达到120℃时,La就吸引弹性衔铁使Sa断开,当温度降到110℃时,La释放弹性衔铁使Sa闭合。
〖快煮模式〗闭合开关S、S1、S2,电饭煲进入快煮模式直至定时开关S2自动断开。在快煮过程中温度将维持在110℃~120℃,工作电路的电热丝在高功率和低功率之间切换,其功率随时间变化如图丙所示。
〖保温模式〗开关S2断开后,电饭煲进入保温模式,最后温度维持在60℃~80℃。
(1)由图丙可知,电饭煲在24分钟快煮过程中,电热丝高功率加热的时间为 分钟。
(2)若R1接入电路的阻值为840欧,R2阻值为40欧,工作电路电源电压为220伏,则电饭煲完成一次快煮,电热R2消耗的电能为多少焦?
(3)请结合图甲、乙说明开关S2断开后,电饭煲实现自动保温的工作原理。
20.(2022九上·余姚期末)如图甲为陶瓷电煎药查,其简化的工作电路如图乙所示,电源电压为220V,S1为单刀双掷开关,R1和R2均为电加热丝。电煎药壶刚开始工作时先武火档快速加热,当药液的温度达到98℃时自动跳到文火档慢熬,药液熬制一段时间后自动跳到保温档防止药液烧干。已知电煎药壶在220V电压下正常工作时,武火快速加热功率为500w,文火慢熬功率为100W,某次救药时药液的温度与电煎药壶工作时间的关系图像如图丙所示。
(1)根据题意可知,当单刀双掷开关S1拨到“2"位置,同时开关S2 (填 “闭合"或“断开”)时,电煎药壶处于文火档。
(2)电加热丝R2的阻值是 欧。
(3)求电煎药壶处于保温档时的功率。
(4)分析图像可知,电放药壶武火加热前半段时间对药液的加热效率 。(填 “大于”“小于”或“等于”)后半段时间的加热效率。
答案解析部分
1.(1)右心房、左心房
(2)房室辫;主动脉
(3)③
(4)小肠很长,小肠内表面有许多皱襞,皱襞上有许多小肠毛绒、小肠内有多种消化液
【解析】1.心脏主要由心肌构成。它有4个空腔,按照位置关系,这4个腔分别叫作左心房、左心室、右心房、右心室。
2.体循环的路线为:左心室→主动脉→全身各级动脉→全身各处毛细血管→全身各级静脉→上、下腔静脉→右心房。
3.血液的变化:血液流经身体各部分组织细胞周围的毛细血管时,把氧气输送给细胞,把细胞产生的二氧化碳等废物带走,血液由动脉血变成静脉血。
(1)心脏为血液循环提供动力。心脏有四个腔,除图甲中所示的两个腔外,还包括右心房、左心房。
(2)由图甲可知,左心室收缩时,①房室辫关闭,②动脉瓣打开,血液的流动途径是左心室→主动脉→各级动脉→毛细血管,与组织细胞进行物质交换。
(3)动脉是由心室发出的血管,在行程中断分支,形成大、中、小动脉。动脉由于承受较大的压力,管壁较厚,管腔断面呈圆形。
静脉是引导血液回心的血管,小静脉起于毛细血管网,行程中逐渐汇成中静脉、大静脉,最后开口于心房。静脉因所承受压力小,故管壁薄、平滑肌和弹力纤维均较少,弹性和收缩性均较弱,管腔在断面上呈扁椭圆形。故图乙中③表示的是动脉。图甲中血管A表示主动脉。图乙中表示血管A的是③。
(4)人体小肠消化功能相适应的结构特点:小肠很长,小肠内表面有许多皱襞,皱襞上有许多小肠毛绒、小肠内有多种消化液。
2.(1)根据“装载时需向船体水舱注水,船体重力增加,巨大的甲板下沉至海面以下”可知,半潜船是靠改变水舱里面水的多少,也就是改变自身重力实现下沉和上浮的。
(2)半潜船空载时的质量为51500吨,
则它受到的浮力F浮=G;
ρ液gV排=mg;
ρ液V排=m;
即:。
(3)根据图片可知,半潜船排开水的体积:V空载
(2)根据浮沉条件和阿基米德原理计算出空载时排开海水的体积;
(3)根据图片比较半潜船排开海水的体积,然后根据阿基米德原理F浮=ρ液gV排比较所受到浮力的大小。
3.(1)产生蓝色絮状沉淀
(2)CuCl2和NaCl
(3)解:由图像可知,氢氧化钠与氯化铜反应生成氢氧化铜质量为9.8g,设此时生成氯化钠质量为x
CuCl2 +2NaOH=Cu(OH)2 +2NaCl
98 117
9.8g x
98:117=9.8g:x
x=11.7g
与盐酸反应的氢氧化钠质量为40g×10%=4g,依据钠元素质量守恒可知,此时生成氯化钠质量为,则 M点溶液中溶质的质量 5.85g+11.7g=17.55g ;
(4)解:设与氯化铜反应消耗氢氧化钠溶液质量为y
CuCl2 +2NaOH=Cu(OH)2 +2NaCl
80 98
10%y 9.8g
80:98=10%y:9.8g
y=80g
则 m1 =40g+80g=120g.
【解析】(1)根据向氯化铜和盐酸的混合溶液中加入氢氧化钠,氢氧化钠先与盐酸反应,然后再与氯化铜反应,氯化铜与氢氧化钠的反应生成氢氧化铜沉淀分析;
(2)根据p点盐酸恰好完全反应分析;
(3)根据生成氢氧化铜沉淀质量及方程式中物质间质量关系计算生成氯化钠质量,由与盐酸反应的氢氧化钠质量计算生成氯化钠质量,M点对应溶质为两份氯化钠之和分析;
(4)根据氢氧化铜质量计算出与氯化铜反应的氢氧化钠溶液质量,再由图像确定与盐酸反应的氢氧化钠溶液质量,从而计算m1数值分析。
(1)向氯化铜和盐酸的混合溶液中加入氢氧化钠,氢氧化钠先与盐酸反应,然后再与氯化铜反应,PM段为氯化铜与氢氧化钠的反应,现象是产生蓝色沉淀;
(2)P点为盐酸恰好与氢氧化钠反应的点,溶液中溶质为氯化钠和氯化铜;
4.(1)2.2
(2)解:设样品中碳酸钠的质量为x。碳酸钠与盐酸反应产生的氯化钠质量为y,氢氧化钠与盐酸反应产生的氯化钠质量为z。
Na2CO3+2HCl= 2NaCl+H2O+ CO2↑
106 117 44
x y 2.2g
得x=5.3g;y=5.85g
NaOH+HCl= NaCl+H2O
40 58.5
13.3g-x z
13.3g-5.3g =8g
(3)17.55
【解析】由图示确定出生成二氧化碳质量,再由二氧化碳质量及方程式中物质间质量关系计算出固体碳酸钠质量和碳酸钠生成的氯化钠质量,再由总固体质量计算出氢氧化钠质量,再计算出氢氧化钠反应生成的氯化钠质量,从而计算碳酸钠质量分数及反应后溶液中溶质质量。
(1)由图示可知,最终反应完全后产生二氧化碳质量为2.2克;
(3)反应结束后所得溶液的溶质为氯化钠,设氢氧化钠反应生成氯化钠质量为z
NaOH+HCl= NaCl+H2O
40
8g 58.5
z
40:58.5=8g:z
z=11.7g
则总的氯化钠质量为5.85g+11.7g=17.55g。
故答案为:(1)2.2;(2)39.8%;(3)17.55.
5.(1)盛有甲烷气体的锥形瓶温度高
(2)根据表格分析,第二次盐酸反应完,产生二氧化碳气体的质量为2.克。
设稀盐酸的质量为X。
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
X 2g
x=3.32g
稀盐酸的质量分数:
(3)甲烷温室效应指数是水蒸气的300倍
【解析】研究产生温室效应的气体:二氧化碳、甲烷、二氧化氮等气体;所以实验中要测温度,证明CO2是产生温室效应的气体,要与空气作对比,比较谁的温度变化较大,根据二氧化碳的来源来分析采取的防止“温室效应”的措施。
再根据实验的注意事项分析。
(1)图乙装置研究产生温室效应的气体为甲烷,它与空气形成对比;在图乙实验中,控制温度计初温相同,得到盛有甲烷气体的锥形瓶温度高现象,说明甲烷也是产生温室效应的气体。
(2)根据表格分析,第二次盐酸反应完,产生二氧化碳气体的质量为2.克。
设稀盐酸的质量为X。
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
X 2g
x=3.32g
稀盐酸的质量分数:
(3)根据表格数据分析,甲烷温室效应指数比二氧化碳高很多,故甲烷对全球温室效应的影响更大,因为其温室效应指数是水蒸气的300倍。
6.(1)排尽装置内原有的空气,避免发生爆炸。;澄清石灰水变浑浊
(2)除去尾气
(3)设可提炼出含铁的质量分数为96 %的生铁质量为x
3CO+Fe2O32Fe+3CO2
160 112
100t×80% 96%x
160:112=(100t×80%):96%x
x=58.3t
【解析】(1)根据CO与空气混合加热易发生爆炸分析;
(2)根据尾气中CO污染空气分析;
(3)根据铁矿石中氧化铁的纯度先计算氧化铁的质量,再利用方程式中物质间质量关系计算铁的质量分析。
(1)CO与空气混合加热易发生爆炸,实验前先通入CO的目的是排尽装置内原有的空气,避免发生爆炸,一氧化碳与氧化铁反应会产生二氧化碳,二氧化碳会使澄清石灰水变浑浊;
(2)尾气中含有CO,排放到空气中会污染空气, 装置图末端的导气管口放一盏燃着的酒精灯,是会了除去尾气;
(3)设可提炼出含铁的质量分数为96 %的生铁质量为x
3CO+Fe2O32Fe+3CO2
160 112
100t×80% 96%x
160:112=(100t×80%):96%x
x=58.3t
故答案为:(1)排尽装置内原有的空气,避免发生爆炸;澄清石灰水变浑浊;(2)除去尾气;(3)58.3t。
7.(1)用带火星木条靠近量筒口处的泡沫附近,若木条复燃,则证明是氧气
(2)由实验可知,反应后产生氧气质量为525.5g-519.1g=6.4g
设过氧化氢溶液质量分数为x
2H2O2=2H2O+O2↑
68 32
40gx 6.4g
68:32=40gx:6.4g
x=34%
(3)部分氧气还残留在量筒内的泡沫中
【解析】(1)根据氧气的验证方法分析;
(2)根据反应后减少质量为生成氧气质量,利用方程式中物质间质量关系计算过氧化氢溶液的浓度分析;
(3)根据反应后氧气可能会残留在量筒内分析。
(1)过氧化氢分解会产生氧气,用用带火星木条靠近量筒口处的泡沫附近,若木条复燃,则证明是氧气;
(2)由实验可知,反应后产生氧气质量为525.5g-519.1g=6.4g
设过氧化氢溶液质量分数为x
2H2O2=2H2O+O2↑
68 32
40gx 6.4g
68:32=40gx:6.4g
x=34%
(3)反应后装置内可能有氧气残留,若部分氧气还残留在量筒内的泡沫中,会使得结果偏小。
故答案为:(1)用带火星木条靠近量筒口处的泡沫附近,若木条复燃,则证明是氧气;(3) 部分氧气还残留在量筒内的泡沫中。
8.(1)加热
(2)解:R1= =220欧
(3)解:P2=2200瓦-200瓦=1980瓦
I2= =9安
(4)解:Q=Cm(t1-t0)=4200 J/(Kg·℃) ×50Kg×22℃=4.62×106焦
W=Pt=2200瓦×40×60秒=5.28×106焦
η= =87.5%
【解析】(1)根据功率公式比较两种状态下总功率的大小,从而确定对应的状态。
(2)根据公式 计算出R1的电阻;
(3)首先根据P2=P热-P保计算出R2的电功率,再根据 计算出通过它的电流。
(4)根据公式Q=cm(t1-t0)计算出水吸收的热量,再根据W=Pt计算出消耗的电能,最后根据 计算出电热水器的效率。
(1)当开关S1闭合时,只有R1工作,此时的总电阻为R1;
当开关S1和S2闭合时,R1与R2并联,此时的总电阻为R并;
则R1>R并;
根据公式可知,当电压相同时,功率与电阻成反比;
则功率P1
9.(1)分子;1:1
(2);CD
【解析】(1)①根据图1确定分子和原子是否发生改变;
②将图1中反应前后都存在的分子去掉,然后确定参加反应的物质的分子数之比。
(2)①确定反应物、反应条件和生成物,据此写出反应的化学方程式。
②根据物质溶于水时吸热还是放热解答。
(1)①根据图1可知,反应前后原子的种类没有改变,而分子的种类发生改变;
②根据图1可知,反应前后共同存在一个,将其去掉后如下图所示:
则参加反应的A2与B2两种物质的分子个数比为:2:2=1:1。
(2)①生石灰与水反应,生成氢氧化钙,反应的方程式为: 。
②白磷燃烧需要将温度升高到着火点,因此放入冷水中的物质溶解时应该向外放热。
氯化钠溶于水时水温几乎不变,故A不合题意;
硝酸铵溶于水时吸热,温度降低,故B不合题意;
浓硫酸溶于水时放热,温度升高,故C符合题意;
氢氧化钠溶于水时放热,温度升高,故D符合题意。
故选CD。
10.(1)B
(2)③
(3)O 型
【解析】血清中的凝集素能与红细胞外面的凝集原发生凝集反应,B血型中有抗A凝集素,他能和A型或AB型血发生凝集反应;A凝集原遇到抗A凝集素会发生凝集反应;红细胞,内含血红蛋白,帮助氧气的运输,血小板,有加快凝血的作用,白细胞, 能保护身体,抵抗细菌等侵袭;
(1)显微镜成倒立的像,物像的移动方向和玻片中的移动方向相反,但是旋转方向不受影响,因此图甲逆时针旋转90°后得到物像是图乙;
(2)①是红细胞,内含血红蛋白,帮助氧气的运输;②是血小板,有加快凝血的作用;③是白细胞, 能保护身体,抵抗细菌等侵袭 ,参与非特异性免疫;
(3)血清中的凝集素能与红细胞外面的凝集原发生凝集反应; 丙、丁的红细胞能与B型血的血清发生凝集反应, B型血中由抗A凝集素,所以丙和丁,有一个为A型,一个为AB型;又已知丁的血清能与乙的红细胞发生凝集反应。说明丁是A型血,丙是AB型血,乙是B型血,那么甲是O型血;
故答案为:(1)B(2)③(3) O 型
11.(1)解:F浮=mg=0.48kg×10N/kg=4.8N
(2)解:ρ液= =800kg/m3
(3)解:G总=F浮=ρ液gV排=800kg/m3×10N/kg×1×10-3m3=8N
m总= =0.8kg
mA=0.8kg-0.48kg=0.32kg
【解析】(1)当物体漂浮在液面上时,它受到的重力与浮力为一对平衡力,即F浮=G=mg;
(2)根据阿基米德原理的变形式 计算出液体的密度;
(3)当物体A全部浸没时,它受到向上的浮力,向下的重力与压力,而压力等于A的重力。根据二力平衡的条件得到:F浮=G+GA。首先根据阿基米德原理 F浮=ρ液gV排 计算出此时的浮力,再根据前面的关系计算出A的重力,最后计算A的质量即可。
12.(1)解:电梯上升的高度h=48m,用时间t﹦60s,
电梯上升的平均速度:v= =0.8m/s
答:电梯上升的平均速度为0.8m/s
(2)解:拉力在0﹣4m做的功:W1=F1h1=2.5×104N×4m=1.0×105J,
拉力在4﹣44m做的功:W2=F2h2=2.0×104N×40m=8.0×105J,
拉力在44﹣48m做的功:W3=F3h3=1.5×104N×4m=0.6×105J,
所以,上升过程拉力做的功:W=W1+W2+W3=1.0×105J+8.0×105J+0.6×105J=9.6×105J
答:拉力做的功是9.6×105J
(3)解:拉力做功的功率:P= =1.6×104W
答:拉力做功的功率是1.6×104W
【解析】(1)已知高度和时间,根据公式计算电梯上升的速度;
(2)根据图乙,分别确定每段距离对应的拉力,然后根据W=Fs分别计算出所做的功,最后将它们相加即可。
(3)根据公式 计算拉力做功的功率。
13.(1)三或3
(2)2:71
(3)红
【解析】(1)根据化学式确定物质元素组成分析;(2)根据元素质量比为相对原子质量×原子个数之比分析;(3)根据酸性溶液能使石蕊变红分析。
(1)高氯酸由氢、氯、氧三种元素组成;
(2) 高氯酸中氢、氯两种元素的质量比为 1:35.5=2:71;
(3) 高氯酸呈酸性,若在高氯酸的无色溶液中滴入紫色石蕊试液,观察到溶液呈红色。
故答案为:(1)三;(2)2:71;(3)红。
14.(1)大豆、玉米→鸡→人
(2)蘑菇细胞呼吸放出二氧化碳,为蔬菜的光合作用提供原料
(3)A;B
【解析】1.生态工程是指人类利用生态学和系统学等学科的基本原理和方法,通过系统设计、调控和技术组装,对已经破坏的生态系统进行修复重建,对造成环境污染和破坏的传统生产方式进行改善,并提高生态系统的生产力,从而促进人类社会与自然环境的和谐发展;生态工程的特点是:少消耗,多效益,可持续;生态系统的基本原理包括,物质循环再生原理,物种多样性原理,整体性原理,协调与平衡原理,系统学和工程学原理。
2.食物链是生态系统中生物之间由食物关系而形成的一种链状结构.每条食物链的起点都是生产者(绿色植物),箭头指向初级消费者(植食性动物)箭头指向次级消费者(食肉动物),到最高营养级结束。
(1)图中的一条食物链: 大豆、玉米→鸡→人 。
(2)将蘑菇房与蔬菜大棚相通,可提高蔬菜产量,其原因是蘑菇细胞呼吸放出二氧化碳,为蔬菜的光合作用提供原料。
(3)大棚蔬菜种植过程中发现:如果在大棚内长期使用某种农药,害虫对这种农药的抗药性会越来越强。关于害虫抗药性的说法正确的A:害虫抗药性的增强是农药对害虫不断选择的结果;B:对害虫来说抗药性变异是有利变异。
故选AB。
15.(1)分解者
(2)小麦→鼠→鹰( 小麦→鼠→鼬)
(3)①本身生命活动消耗能量;②生物遗体、遗物内含能量。(合理即可)
【解析】(1)生态系统包括生物成分和非生物成分,生物成分包括生产者、分解者和消费者;非生物成分包括阳光、空气、水分等因素。
(2)食物链是生产者和消费者之间由于食物关系而构成链条.它表示的是生产者和消费者之间的关系。其写法是:起点是生产者,依次是初级消费者、次级消费者、三级消费者...一直到最高消费者,中间用箭头连接,箭头总是指向捕食者。
(1)如图是生物生命活动的能量流动的示意图,图中各成分还不能构成一个生态系统,从生态系统的组成成分分析,还缺乏分解者。
(2)图中共有四种生物,鹰、鼬、鼠、小麦,一条食物链:小麦→鼠→鹰( 小麦→鼠→鼬)。
(3)能量在沿食物链流动的过程中,会不断减少,试分析原因:①本身生命活动消耗能量;②生物遗体、遗物内含能量。
16.(1)v= = 180 m/s
答:C919在匀速巡航中的速度为180 m/s
(2)f=F率= =2×105N
答:C919在匀速巡航中所受的阻力为2×105N
(3)Q放= mq=3×103kg×5×107J/kg=1.5×1011J
η= = 57.6%
答:C919在匀速巡航中发动机的工作效率为57.6%
【解析】(1)根据公式计算飞机的巡航速度。
(2)首先根据功率的计算式计算出飞机发动机产生的牵引力,再根据二力平衡的知识计算飞机受到的阻力,即f=F。
(3)根据Q放=qm计算出燃油完全燃烧放出的热量,再根据W=Pt计算飞机发动机做的机械功,最后根据公式 计算发动机的工作效率。
17.加入的硫酸铜与氢氧化钡发生反应, ;
当氢氧化钡完全反应,加入的稀硫酸与生成的沉淀 反应, ,导致沉淀质量减少,但因为还有沉淀 ,所以沉淀质量不会等于0;当氢氧化钡未完全反应,加入的稀硫酸先与氢氧化钡反应, ,沉淀质量先增加,再与沉淀 反应,导致沉淀质量减少,反应完全后沉淀质量最后保持不变。
【解析】根据氢氧化钡溶液中先滴加硫酸铜溶液,硫酸铜与氢氧化钡反应生成氢氧化铜和硫酸钡两种沉淀,氢氧化钡可能恰好完全反应,也可能有剩余,再加入稀硫酸时,若氢氧化钡有剩余,则沉淀会继续增加,至氢氧化钡完全反应,然后硫酸再与氢氧化铜反应,沉淀再减少,至氢氧化铜完全反应后保持不变,若氢氧化钡完全反应,则加入硫酸后,氢氧化铜与硫酸反应,沉淀减少,至氢氧化铜完全反应后保持不变分析。
18.(1)0.9
(2)解:Mg(OH)2 的质量为2.9克,Mg(OH)2%=22.5%
(3)解:生成CaO的质量为5.6克,MgO的质量为2克,x=5.6+2=7.6克
另法:生成CO2的质量为4.4克,x=12-4.4=7.6 克
(4)MgO CaO CaCO3
【解析】根据图片可知,从a~b,固体的质量不断减小,应该为氢氧化镁分解,生成氧化镁和水。从b~c,固体质量不变,此时氢氧化镁完全反应,而温度尚未达到碳酸钙的分解温度。从c~d时,固体质量不断减小,即碳酸钙分解生成氧化钙和二氧化碳。从d~e,固体的质量保持不变,即整个分解反应结束,据此分析解答。
(1)水垢样品中分解生成水的质量为:12.9g-12g=0.9g;
(2)设氢氧化镁的质量为x,生成氧化镁的质量为y;
;
58 40 18
xg y 0.9g
;
解得:x=2.9g,y=2g;
水垢样品中氢氧化镁的质量分数:;
(3)碳酸钙的质量为:12.9g-2.9g=10g;
设反应生成氧化钙的质量为z,
;
100 56
10g z
;
解得:z=5.6g;
那么最终剩余固体的质量为:x=2g+5.6g=7.6g。
(4)根据上面的计算可知,如果剩余固体为氧化镁和氧化钙,
那么其中钙元素的质量分数为:;
而实际钙元素的质量分数为36%<53%,
那么碳酸钙应该没有完全分解;
即剩余固体的成分是MgO、CaO和CaCO3。
19.(1)12
(2)解:R总=R1+R2=840欧+40欧=880欧
I= = = 0.25安
由W=UIt得:
W1=I2R2t1=(0.25安)2×40欧×720秒=1800焦
W1= = =8.712×105焦
W总=W1+W2=8.712×105焦+1800焦=8.73×105焦
答:电饭煲完成一次快煮,电热丝R2消耗的电能为8.73×105焦。
(3)当S2断开后,R2低功率工作,降温至110℃及以下,Sa始终闭合。继续降温至60℃时,Sb闭合,R1被短路,R2高功率工作,升温至80℃时,Sb断开,R1与R2串联,R2低功率工作,开始降温,如此往复,实现自动保温。
【解析】(1)根据图丙找到电热丝高功率工作的时间段,然后将它们相加即可。
(2)当低功率工作时,两个电阻串联,根据 R总=R1+R2 计算出此时的总电阻,再根据 计算出此时的总电流,接下来根据 W1=I2R2t1 计算出R2消耗的电能。高功率工作时,只有R2自己工作,根据公式 计算出它消耗的电能,最后将两个电能相加即可。
(3)注意分析温度变化时,两个热敏电阻对电路状态的影响,结合电功率的变化分析自动保温原理。
(1)根据图丙可知,快煮24分钟内电热丝高功率加热的时间:t=6min+(11-9)min+(16-14)min+(21-19)min=12min。
20.(1)断开
(2)484
(3)解:当开关S1接2、S2闭合时,R1与R2并联,电煎药壶处于武火挡,
因并联电路中各支路独立工作、互不影响,且电路的总功率等于各用电器功率之和,所以,电加热丝R1的电功率: P1=P武火-P文火= 500W- 100W= 400W,
因并联电路中各支路两端的电压相等,
所以,电加热丝R1的阻值: R1= =121Ω,
当开关S1接1、S2断开时,R1与R2串联,电煎药壶处于保温挡,
电煎药壶处于保温挡时的功率: P保温= =80W
答:电煎药壶处于保温挡时的功率80W
(4)小于
【解析】(1)根据公式比较开关在不同组合时的总功率大小,从而确定所处的状态;
(2)当开关S1接“2”,S2断开时,只有R2自己工作,此时为文火,根据公式计算出R2的阻值;
(3)对电路图进行分析可知,文火功率与武火功率的差就是电阻R1单独工作时的电功率,可根据计算R1的电阻。当开关S1接1、S2断开时,R1与R2串联,电煎药壶处于保温档,可根据 公式计算出此时的功率。
(4)根据加热效率分析解答。
(1)根据图片可知,当开关S1接“2”,S2闭合时,两个电阻并联,此时的总电阻为R并;
当开关S1接“2”,S2断开时,只有R2自己工作,此时电阻为R2;
当开关S1接“1”,S2断开时,两个电阻串联,此时电阻为R串;
则总电阻R并
则三者对应的状态分别为:武火档、文火档和保温档。
(2)当开关S1接“2”,S2断开时,只有R2自己工作,此时为文火档,
R2的阻值;
(4)根据丙图可知,在武火档加热时,从0~7min时,药液温度上升:48℃-18℃=30℃;从7~14min时,药液温度升高:98℃-48℃=50℃。
根据公式可知,电热药壶武火加热前半段时间对药液的加热效率小于后半段时间的加热效率。
