黑龙江省齐齐哈尔市2022-2023学年高一下学期4月期中考试化学试题(含答案)
文档属性
| 名称 | 黑龙江省齐齐哈尔市2022-2023学年高一下学期4月期中考试化学试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 647.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-05 00:00:00 | ||
图片预览

文档简介
齐齐哈尔市2022-2023学年高一下学期4月期中考试
化学
考生注意:
1.本试卷满分100分,考试时间90分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:必修第二册第五章、第六章。
5.可能用到的相对原子质量: 1 12 14 16 28 32 56 64
一、选择题(本题共18小题,每小题3分,共54分。在每小题给出的四个选项中只有一项是符合题目要求的)
1.化学与生活密切相关。下列说法正确的是( )
A.具有抗氧化的作用,是一种重要的食品添加剂
B.豆科植物的根瘤菌可以将转化成,从而实现自然固氮
C.常温下可用铝制容器盛装浓硝酸,因为浓硝酸不与铝反应
D.难溶于水且不容易被X射线透过,可用作“钡餐”
2.下列变化过程能实现化学能转化为电能的是( )
A.水力发电 B.水果电池 C.燃气燃烧 D.电动车充电
3.下列生活中常见的措施,其目的主要是减慢化学反应速率的是( )
A.糕点包装袋内放置除氧剂
B.将煤块粉碎后燃烧
C.用洗衣粉洗衣服时,用温水浸泡
D.制作面食时,需要加入酵母
4.下列物品使用了硅酸盐材料的是( )
A.陶瓷餐具 B.光导纤维 C.水晶镜片 D.硅太阳能电池
5.下列生活中发生的反应属于吸热反应的是( )
A.食物的腐败 B.铁和稀盐酸反应
C.蒸馒头时小苏打受热分解 D.生石灰制熟石灰
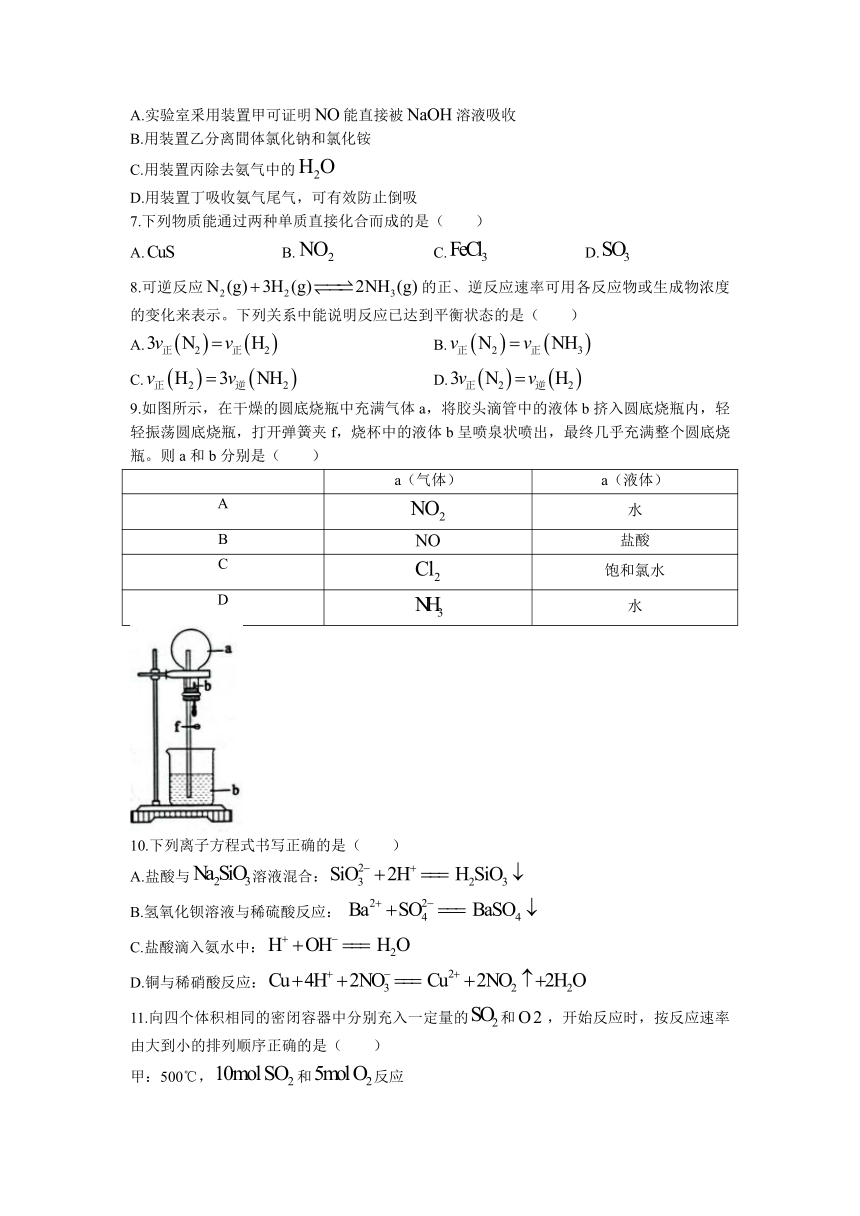
6.下列有关含氮化合物的实验装置和原理能达到相应实验目的的是( )
A.实验室釆用装置甲可证明能直接被溶液吸收
B.用装置乙分离間体氯化钠和氯化铵
C.用装置丙除去氨气中的
D.用装置丁吸收氨气尾气,可有效防止倒吸
7.下列物质能通过两种单质直接化合而成的是( )
A. B. C. D.
8.可逆反应的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是( )
A. B.
C. D.
9.如图所示,在干燥的圆底烧瓶中充满气体a,将胶头滴管中的液体b挤入圆底烧瓶内,轻轻振荡圆底烧瓶,打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个圆底烧瓶。则a和b分别是( )
a(气体) a(液体)
A 水
B 盐酸
C 饱和氯水
D 水
10.下列离子方程式书写正确的是( )
A.盐酸与溶液混合:
B.氢氧化钡溶液与稀硫酸反应:
C.盐酸滴入氨水中:
D.铜与稀硝酸反应:
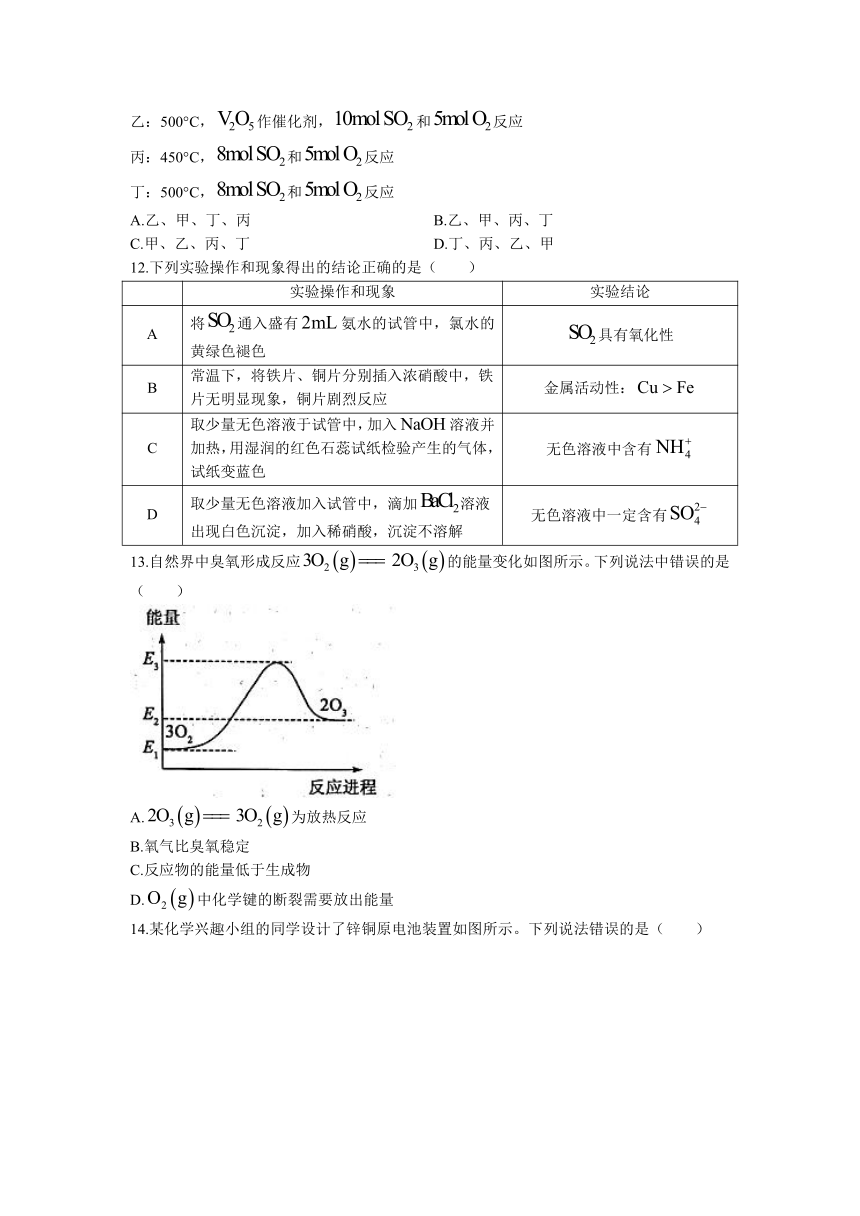
11.向四个体积相同的密闭容器中分别充入一定量的和,开始反应时,按反应速率由大到小的排列顺序正确的是( )
甲:500℃,和反应
乙:500°C,作催化剂,和反应
丙:450°C,和反应
丁:500°C,和反应
A.乙、甲、丁、丙 B.乙、甲、丙、丁
C.甲、乙、丙、丁 D.丁、丙、乙、甲
12.下列实验操作和现象得出的结论正确的是( )
实验操作和现象 实验结论
A 将通入盛有氨水的试管中,氯水的黄绿色褪色 具有氧化性
B 常温下,将铁片、铜片分别插入浓硝酸中,铁片无明显现象,铜片剧烈反应 金属活动性:
C 取少量无色溶液于试管中,加入溶液并加热,用湿润的红色石蕊试纸检验产生的气体,试纸变蓝色 无色溶液中含有
D 取少量无色溶液加入试管中,滴加溶液出现白色沉淀,加入稀硝酸,沉淀不溶解 无色溶液中一定含有
13.自然界中臭氧形成反应的能量变化如图所示。下列说法中错误的是( )
A.为放热反应
B.氧气比臭氧稳定
C.反应物的能量低于生成物
D.中化学键的断裂需要放出能量
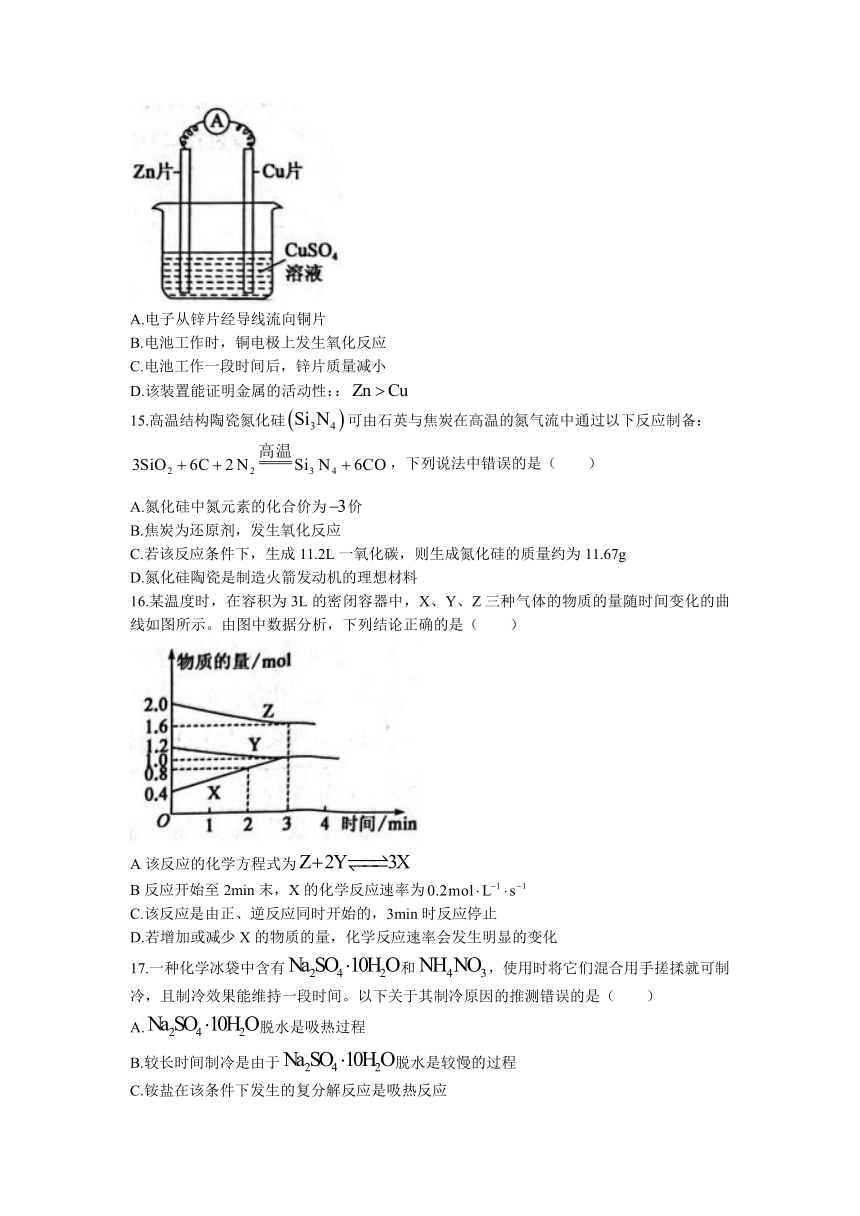
14.某化学兴趣小组的同学设计了锌铜原电池装置如图所示。下列说法错误的是( )
A.电子从锌片经导线流向铜片
B.电池工作时,铜电极上发生氧化反应
C.电池工作一段时间后,锌片质量减小
D.该装置能证明金属的活动性::
15.高温结构陶瓷氮化硅可由石英与焦炭在高温的氮气流中通过以下反应制备:
,下列说法中错误的是( )
A.氮化硅中氮元素的化合价为价
B.焦炭为还原剂,发生氧化反应
C.若该反应条件下,生成11.2L一氧化碳,则生成氮化硅的质量约为11.67g
D.氮化硅陶瓷是制造火箭发动机的理想材料
16.某温度时,在容积为3L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。由图中数据分析,下列结论正确的是( )
A该反应的化学方程式为
B反应开始至2min末,X的化学反应速率为
C.该反应是由正、逆反应同时开始的,3min时反应停止
D.若增加或减少X的物质的量,化学反应速率会发生明显的变化
17.一种化学冰袋中含有和,使用时将它们混合用手搓揉就可制冷,且制冷效果能维持一段时间。以下关于其制冷原因的推测错误的是( )
A.脱水是吸热过程
B.较长时间制冷是由于脱水是较慢的过程
C.铵盐在该条件下发生的复分解反应是吸热反应
D.溶于水会吸收热量
18.足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和、的混合气体2.24L(标准状况),这些气体与一定体积(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入溶液至恰好完全沉淀,则消耗溶液的体积是50mL,下列说法正确的是( )
A.参加反应的硝酸是0.2mol
B.消耗氧气的体积为1.68L(标准状况)
C.此反应过程中转移的电子为0.3mol
D.混合气体中含(标准状况)
二、非选择题(本题包括4小题,共46分)
19.(10分)为检验浓硫酸与木炭在加热条件下反应产生的和气体,设计了如图所示实验装置,D中放有用和淀粉的蓝色溶液浸湿的脱脂棉。
回答下列问题:
(1)装置A中发生反应的化学方程式为______,该反应体现了浓硫酸的______。
(2)实验时,装置B的作用是______。
(3)装置D中发生反应的离子方程式为______;当D中产生______现象时,可以说明使E中澄清石灰水变浑浊的是,而不是。
(4)若不设置装置C,判断该装置是否也能证明浓硫酸与木炭在加热条件下能产生并说明理由:______。
20.(12分)人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,回答下列问题:
(1)某小组在实验室模拟以为原料,制备少最硝态氮肥,转化途径如下(转化所需试剂及条件已略去):
①写岀实验室用和消石灰共热制备気气的化学反应方程式:__________________。
②写出发生催化氧化反应生成的化学方程式:__________________。
③将转化为,列举两种不同类别的化合物M:__________________(写化学式)。
(2)是一种铵态氮肥,需阴凉处保存,原因是__________________(用化学方程式表示)。
(3)过渡施用氮肥将导致大气中含量增高,加剧雾鐘的形成。,是雾霾的成分之一,其形成过程如图所示(转化所需试剂及条件已略去):
①X可能是或__________________。
②尿素是一种常用有机氮肥,缓慢与发生非氧化还原反应释放出和另外一种气体,该反应的化学方程式为_________________。
21.(12分)能源与人类的生存和发展息息相关,化学反应在人类利用能源的历史过程中充当重要的角色。回答下列问题:
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是_________________(填“离子键”或“共价键”)。
(2)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。若断开1mol氢气中的化学键消耗的能虽为,断开1mol氧气中的化学键消耗的能量为,形成1mol水中的化学键释放的能量为,则下列关系正确的是______(填字母)。
A. B.
C. D.
(3)下列化学反应在理论上可以设计成原电池的是______(填字母)。
A. B.
C. D.
(4)如图为某燃料电池的结构示意图,电解质溶液为溶液,电极材料为疏松多孔的石墨棒。冋答下列问题:
xxx
若该燃料电池为氢氧燃料电池。
①a极通入的物质为______(壊物质名称),电解质溶液中的移向______(“负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:____________。
22.(12分)300°C时,向2L的恒容密闭容器中,充入和使之发生反应,测得各物质的物质的最浓度变化如图所示:
(1)由图可知,的浓度随时间的变化为曲线______(填“a”“b”或“c”);0~2min内的平均反应速率为______。
(2)已知:反应至2min时(未达到平衡),改变了某一反应条件。由图可知,0~2min内的生成速率______(填“a大于”“小于”或“等于”)2~4min内的生成速率。据图判断,2min时改变的反应条件可能是______(填字母)。
A.加入催化剂 B.升高温度 C.降低温度 D.增加的物质的量
(3)5min时,的转化率(反应时消耗的物质的量占起始投入的物质的量的百分比)为______,此时容器内气体总压强与反应前容器内气体总压强之比为______。
齐齐哈尔市2022-2023学年高一下学期4月期中考试
化学
参考答案、提示及评分细则
1.A 具有抗氧化的作用,适量可以杀菌,是一种重要的食品添加剂,A正确;豆科植物的根瘤菌可以将转化成氨,从而实现自然固氮,B错误:常温下可用铝制容器盛装浓硝酸或浓硫酸,是因为浓硝酸或 浓硫酸能使铝的表面形成一层致密的氧化膜,C错误:可用作“钡餐”,的是,D错误。
2.B 水力发电是水的重力势能转化为电能,A不符合题意;水果电池是将化学能转化为电能,B符合题意;燃 气燃烧是将化学能变为热能,C不符合题意;电动车充电是将电能变为化学能,D不符合题意。
3.A
4.A 陶瓷餐具使用了硅酸盐材料,A正确;光导纤维的主要成分是二氧化硅,B错误;水晶镜片的主要成分是 二氧化硅,C错误;硅太阳能电池的主要成分是硅,D错误。
5.C 食物的腐败,发生氧化反应,属于放热反应,A不符合题意;铁和稀盐酸反应,铁发生氧化反应,属于放热反应,B不符合题意;蒸馒头时小苏打受热分解属于吸热反应,C符合题意;生石灰制熟石灰是化合反应,属 于放热反应,D不符合题意。
6.B 7.C
8.D 反应达到平衡状态时,正反应速率与逆反应速率相等,D中,D正确。 9.D
10.A 盐酸与硅酸钠反应生成硅酸沉淀和氯化钠,反应的离子方程式为,A正确:氢氧化钡溶液与稀硫酸反应生成硫酸钡沉淀和水,反应的离子方程式为,B错误;一水合氨为弱碱,书写离子方程式时不能拆,盐酸滴人氨水中反应的离子方程式为,C错误;铜与稀硝酸反应生成硝酸铜、一氧化氮、水,反应的离子方程式为,D错误。
11.A 反应温度、反应物浓度相同的条件下,有催化剂的反应速率更快,所以有乙>甲,无催化剂且温度相同的条件下,反应物浓度越高,反应速率越快,所以有甲>丁,无催化剂且反应物浓度相同的条件下,温度越高,反应速率越快,所以有丁>丙,综上可知,A正确。
12.C
13.D 根据图示,生成物总能量大于反应物总能量,为吸热反应,为放热 反应,A正确;氧气的能量比臭氧低,所以氧气比臭氧稳定,B正确;根据图示,反应物的能量低于生成物,C 正确;化学键断裂需要吸收能量,D错误。
14.B
15.C 氮的非金属性强于硅,由化合价代数和为0得:中硅显价,氮元素的化合价为价,A正确:C由0价升高为价,焦炭为还原剂,发生氧化反应,B正确:题中未标明是标准状况,无法计算的物质的量,C错误;氮化硅陶瓷是耐热材料,是制造火箭发动机的理想材料,D正确。
16.D 由图象可以看出,反应中Z、Y的物质的量减少,应为反物。X的物质的量增多,应为生成物,当反应尖锐。,,则 ::,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:,A错误:反应开始至2min末,,容器体积为3L,所X的化学反应速率为,B错误;X、Y、Z起始量不为0,该反应是由正、逆反应同时开始的,3min时反应达到平衡,反应并未停止,C错误;若增加或减少X的物质的量,生成物的浓度发生变化,逆反应速率会发生改变,
②
17.C 脱水是吸热过程,A正确;因为+水硫酸钠脱水较慢,因此制冷效果可以维持较长时间,B正确;和不能发生复分解反应,C错误;硝酸铵夺取硫酸钠结晶水,是一个吸热反应,同时溶解吸热,D正确。
18. D
19.(1)(2分) 氧化(1分)
(2)作安全瓶,防止倒吸(合理即可,1分)
(3)(2分) 蓝色溶液不再变浅(2分)
(4)能证明。因为装置D中物质可以与反应且能观察到现象(合理即可,2分)
20. (每空2分)
(1)① ②
③、(合理即可)
(2)
(3)① ②
21.(每空2分)
(1)共价键
(2)B
(3)A
(4)①氢气负 ②
22.(每空 2分)
(1)a (不带单位扣1分)
(2)小于 AB
(3)30%
化学
考生注意:
1.本试卷满分100分,考试时间90分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:必修第二册第五章、第六章。
5.可能用到的相对原子质量: 1 12 14 16 28 32 56 64
一、选择题(本题共18小题,每小题3分,共54分。在每小题给出的四个选项中只有一项是符合题目要求的)
1.化学与生活密切相关。下列说法正确的是( )
A.具有抗氧化的作用,是一种重要的食品添加剂
B.豆科植物的根瘤菌可以将转化成,从而实现自然固氮
C.常温下可用铝制容器盛装浓硝酸,因为浓硝酸不与铝反应
D.难溶于水且不容易被X射线透过,可用作“钡餐”
2.下列变化过程能实现化学能转化为电能的是( )
A.水力发电 B.水果电池 C.燃气燃烧 D.电动车充电
3.下列生活中常见的措施,其目的主要是减慢化学反应速率的是( )
A.糕点包装袋内放置除氧剂
B.将煤块粉碎后燃烧
C.用洗衣粉洗衣服时,用温水浸泡
D.制作面食时,需要加入酵母
4.下列物品使用了硅酸盐材料的是( )
A.陶瓷餐具 B.光导纤维 C.水晶镜片 D.硅太阳能电池
5.下列生活中发生的反应属于吸热反应的是( )
A.食物的腐败 B.铁和稀盐酸反应
C.蒸馒头时小苏打受热分解 D.生石灰制熟石灰
6.下列有关含氮化合物的实验装置和原理能达到相应实验目的的是( )
A.实验室釆用装置甲可证明能直接被溶液吸收
B.用装置乙分离間体氯化钠和氯化铵
C.用装置丙除去氨气中的
D.用装置丁吸收氨气尾气,可有效防止倒吸
7.下列物质能通过两种单质直接化合而成的是( )
A. B. C. D.
8.可逆反应的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是( )
A. B.
C. D.
9.如图所示,在干燥的圆底烧瓶中充满气体a,将胶头滴管中的液体b挤入圆底烧瓶内,轻轻振荡圆底烧瓶,打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个圆底烧瓶。则a和b分别是( )
a(气体) a(液体)
A 水
B 盐酸
C 饱和氯水
D 水
10.下列离子方程式书写正确的是( )
A.盐酸与溶液混合:
B.氢氧化钡溶液与稀硫酸反应:
C.盐酸滴入氨水中:
D.铜与稀硝酸反应:
11.向四个体积相同的密闭容器中分别充入一定量的和,开始反应时,按反应速率由大到小的排列顺序正确的是( )
甲:500℃,和反应
乙:500°C,作催化剂,和反应
丙:450°C,和反应
丁:500°C,和反应
A.乙、甲、丁、丙 B.乙、甲、丙、丁
C.甲、乙、丙、丁 D.丁、丙、乙、甲
12.下列实验操作和现象得出的结论正确的是( )
实验操作和现象 实验结论
A 将通入盛有氨水的试管中,氯水的黄绿色褪色 具有氧化性
B 常温下,将铁片、铜片分别插入浓硝酸中,铁片无明显现象,铜片剧烈反应 金属活动性:
C 取少量无色溶液于试管中,加入溶液并加热,用湿润的红色石蕊试纸检验产生的气体,试纸变蓝色 无色溶液中含有
D 取少量无色溶液加入试管中,滴加溶液出现白色沉淀,加入稀硝酸,沉淀不溶解 无色溶液中一定含有
13.自然界中臭氧形成反应的能量变化如图所示。下列说法中错误的是( )
A.为放热反应
B.氧气比臭氧稳定
C.反应物的能量低于生成物
D.中化学键的断裂需要放出能量
14.某化学兴趣小组的同学设计了锌铜原电池装置如图所示。下列说法错误的是( )
A.电子从锌片经导线流向铜片
B.电池工作时,铜电极上发生氧化反应
C.电池工作一段时间后,锌片质量减小
D.该装置能证明金属的活动性::
15.高温结构陶瓷氮化硅可由石英与焦炭在高温的氮气流中通过以下反应制备:
,下列说法中错误的是( )
A.氮化硅中氮元素的化合价为价
B.焦炭为还原剂,发生氧化反应
C.若该反应条件下,生成11.2L一氧化碳,则生成氮化硅的质量约为11.67g
D.氮化硅陶瓷是制造火箭发动机的理想材料
16.某温度时,在容积为3L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。由图中数据分析,下列结论正确的是( )
A该反应的化学方程式为
B反应开始至2min末,X的化学反应速率为
C.该反应是由正、逆反应同时开始的,3min时反应停止
D.若增加或减少X的物质的量,化学反应速率会发生明显的变化
17.一种化学冰袋中含有和,使用时将它们混合用手搓揉就可制冷,且制冷效果能维持一段时间。以下关于其制冷原因的推测错误的是( )
A.脱水是吸热过程
B.较长时间制冷是由于脱水是较慢的过程
C.铵盐在该条件下发生的复分解反应是吸热反应
D.溶于水会吸收热量
18.足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和、的混合气体2.24L(标准状况),这些气体与一定体积(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入溶液至恰好完全沉淀,则消耗溶液的体积是50mL,下列说法正确的是( )
A.参加反应的硝酸是0.2mol
B.消耗氧气的体积为1.68L(标准状况)
C.此反应过程中转移的电子为0.3mol
D.混合气体中含(标准状况)
二、非选择题(本题包括4小题,共46分)
19.(10分)为检验浓硫酸与木炭在加热条件下反应产生的和气体,设计了如图所示实验装置,D中放有用和淀粉的蓝色溶液浸湿的脱脂棉。
回答下列问题:
(1)装置A中发生反应的化学方程式为______,该反应体现了浓硫酸的______。
(2)实验时,装置B的作用是______。
(3)装置D中发生反应的离子方程式为______;当D中产生______现象时,可以说明使E中澄清石灰水变浑浊的是,而不是。
(4)若不设置装置C,判断该装置是否也能证明浓硫酸与木炭在加热条件下能产生并说明理由:______。
20.(12分)人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,回答下列问题:
(1)某小组在实验室模拟以为原料,制备少最硝态氮肥,转化途径如下(转化所需试剂及条件已略去):
①写岀实验室用和消石灰共热制备気气的化学反应方程式:__________________。
②写出发生催化氧化反应生成的化学方程式:__________________。
③将转化为,列举两种不同类别的化合物M:__________________(写化学式)。
(2)是一种铵态氮肥,需阴凉处保存,原因是__________________(用化学方程式表示)。
(3)过渡施用氮肥将导致大气中含量增高,加剧雾鐘的形成。,是雾霾的成分之一,其形成过程如图所示(转化所需试剂及条件已略去):
①X可能是或__________________。
②尿素是一种常用有机氮肥,缓慢与发生非氧化还原反应释放出和另外一种气体,该反应的化学方程式为_________________。
21.(12分)能源与人类的生存和发展息息相关,化学反应在人类利用能源的历史过程中充当重要的角色。回答下列问题:
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,水分解断裂的化学键是_________________(填“离子键”或“共价键”)。
(2)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。若断开1mol氢气中的化学键消耗的能虽为,断开1mol氧气中的化学键消耗的能量为,形成1mol水中的化学键释放的能量为,则下列关系正确的是______(填字母)。
A. B.
C. D.
(3)下列化学反应在理论上可以设计成原电池的是______(填字母)。
A. B.
C. D.
(4)如图为某燃料电池的结构示意图,电解质溶液为溶液,电极材料为疏松多孔的石墨棒。冋答下列问题:
xxx
若该燃料电池为氢氧燃料电池。
①a极通入的物质为______(壊物质名称),电解质溶液中的移向______(“负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:____________。
22.(12分)300°C时,向2L的恒容密闭容器中,充入和使之发生反应,测得各物质的物质的最浓度变化如图所示:
(1)由图可知,的浓度随时间的变化为曲线______(填“a”“b”或“c”);0~2min内的平均反应速率为______。
(2)已知:反应至2min时(未达到平衡),改变了某一反应条件。由图可知,0~2min内的生成速率______(填“a大于”“小于”或“等于”)2~4min内的生成速率。据图判断,2min时改变的反应条件可能是______(填字母)。
A.加入催化剂 B.升高温度 C.降低温度 D.增加的物质的量
(3)5min时,的转化率(反应时消耗的物质的量占起始投入的物质的量的百分比)为______,此时容器内气体总压强与反应前容器内气体总压强之比为______。
齐齐哈尔市2022-2023学年高一下学期4月期中考试
化学
参考答案、提示及评分细则
1.A 具有抗氧化的作用,适量可以杀菌,是一种重要的食品添加剂,A正确;豆科植物的根瘤菌可以将转化成氨,从而实现自然固氮,B错误:常温下可用铝制容器盛装浓硝酸或浓硫酸,是因为浓硝酸或 浓硫酸能使铝的表面形成一层致密的氧化膜,C错误:可用作“钡餐”,的是,D错误。
2.B 水力发电是水的重力势能转化为电能,A不符合题意;水果电池是将化学能转化为电能,B符合题意;燃 气燃烧是将化学能变为热能,C不符合题意;电动车充电是将电能变为化学能,D不符合题意。
3.A
4.A 陶瓷餐具使用了硅酸盐材料,A正确;光导纤维的主要成分是二氧化硅,B错误;水晶镜片的主要成分是 二氧化硅,C错误;硅太阳能电池的主要成分是硅,D错误。
5.C 食物的腐败,发生氧化反应,属于放热反应,A不符合题意;铁和稀盐酸反应,铁发生氧化反应,属于放热反应,B不符合题意;蒸馒头时小苏打受热分解属于吸热反应,C符合题意;生石灰制熟石灰是化合反应,属 于放热反应,D不符合题意。
6.B 7.C
8.D 反应达到平衡状态时,正反应速率与逆反应速率相等,D中,D正确。 9.D
10.A 盐酸与硅酸钠反应生成硅酸沉淀和氯化钠,反应的离子方程式为,A正确:氢氧化钡溶液与稀硫酸反应生成硫酸钡沉淀和水,反应的离子方程式为,B错误;一水合氨为弱碱,书写离子方程式时不能拆,盐酸滴人氨水中反应的离子方程式为,C错误;铜与稀硝酸反应生成硝酸铜、一氧化氮、水,反应的离子方程式为,D错误。
11.A 反应温度、反应物浓度相同的条件下,有催化剂的反应速率更快,所以有乙>甲,无催化剂且温度相同的条件下,反应物浓度越高,反应速率越快,所以有甲>丁,无催化剂且反应物浓度相同的条件下,温度越高,反应速率越快,所以有丁>丙,综上可知,A正确。
12.C
13.D 根据图示,生成物总能量大于反应物总能量,为吸热反应,为放热 反应,A正确;氧气的能量比臭氧低,所以氧气比臭氧稳定,B正确;根据图示,反应物的能量低于生成物,C 正确;化学键断裂需要吸收能量,D错误。
14.B
15.C 氮的非金属性强于硅,由化合价代数和为0得:中硅显价,氮元素的化合价为价,A正确:C由0价升高为价,焦炭为还原剂,发生氧化反应,B正确:题中未标明是标准状况,无法计算的物质的量,C错误;氮化硅陶瓷是耐热材料,是制造火箭发动机的理想材料,D正确。
16.D 由图象可以看出,反应中Z、Y的物质的量减少,应为反物。X的物质的量增多,应为生成物,当反应尖锐。,,则 ::,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:,A错误:反应开始至2min末,,容器体积为3L,所X的化学反应速率为,B错误;X、Y、Z起始量不为0,该反应是由正、逆反应同时开始的,3min时反应达到平衡,反应并未停止,C错误;若增加或减少X的物质的量,生成物的浓度发生变化,逆反应速率会发生改变,
②
17.C 脱水是吸热过程,A正确;因为+水硫酸钠脱水较慢,因此制冷效果可以维持较长时间,B正确;和不能发生复分解反应,C错误;硝酸铵夺取硫酸钠结晶水,是一个吸热反应,同时溶解吸热,D正确。
18. D
19.(1)(2分) 氧化(1分)
(2)作安全瓶,防止倒吸(合理即可,1分)
(3)(2分) 蓝色溶液不再变浅(2分)
(4)能证明。因为装置D中物质可以与反应且能观察到现象(合理即可,2分)
20. (每空2分)
(1)① ②
③、(合理即可)
(2)
(3)① ②
21.(每空2分)
(1)共价键
(2)B
(3)A
(4)①氢气负 ②
22.(每空 2分)
(1)a (不带单位扣1分)
(2)小于 AB
(3)30%
同课章节目录
