第二章《烃》测试题(含答案)2022-2023学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第二章《烃》测试题(含答案)2022-2023学年下学期高二化学人教版(2019)选择性必修3 |  | |
| 格式 | docx | ||
| 文件大小 | 660.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-06 09:27:48 | ||
图片预览



文档简介
第二章《烃》测试题
一、单选题(共13题)
1.某烃1mol跟2mol氯化氢发生加成反应,其产物又可被10mol氯气完全取代,该烃可能是
A.1,3—丁二烯 B.1—戊炔 C.丙炔 D.丁炔
2.已知:,如果要合成,所用的原始原料可以是
A.2—甲基—1,3—丁二烯和2—丁炔 B.1,3—戊二烯和2—丁炔
C.2,3—二甲基—1,3—戊二烯和乙炔 D.1,3—丁二烯和丙炔
3.下列有关物质的比较错误的是
A.常压下的沸点:正戊烷>异戊烷>新戊烷>正丁烷>异丁烷
B.不考虑立体异构,同分异构体种数:戊烷>戊烯>丁烷
C.点燃时火焰明亮程度:乙炔>乙烯>甲烷
D.常温下的密度:己烷<水<溴乙烷
4.有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚乙烯;⑧环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是
A.①②③⑤ B.①④⑥⑦ C.④⑥⑦⑧ D.②③⑧
5.阿魏酸是阿魏、当归、酸枣仁等中药材的有效成分之一,具有抗辐射、抗氧化、抗病毒等功效,其结构如图所示。关于该有机物的说法中不正确的是
A.该有机物的分子式为C10H10O4
B.该有机物苯环上具有相同取代基的同分异构体共6种
C.1mol该分子最多与4molH2发生加成反应
D.阿魏酸分子中所有的碳原子可能共平面
6.下列化学用语正确的是
A.氨基的电子式: B.乙烯的实验式:
C.的结构示意图: D.的比例模型:
7.下列说法正确的是
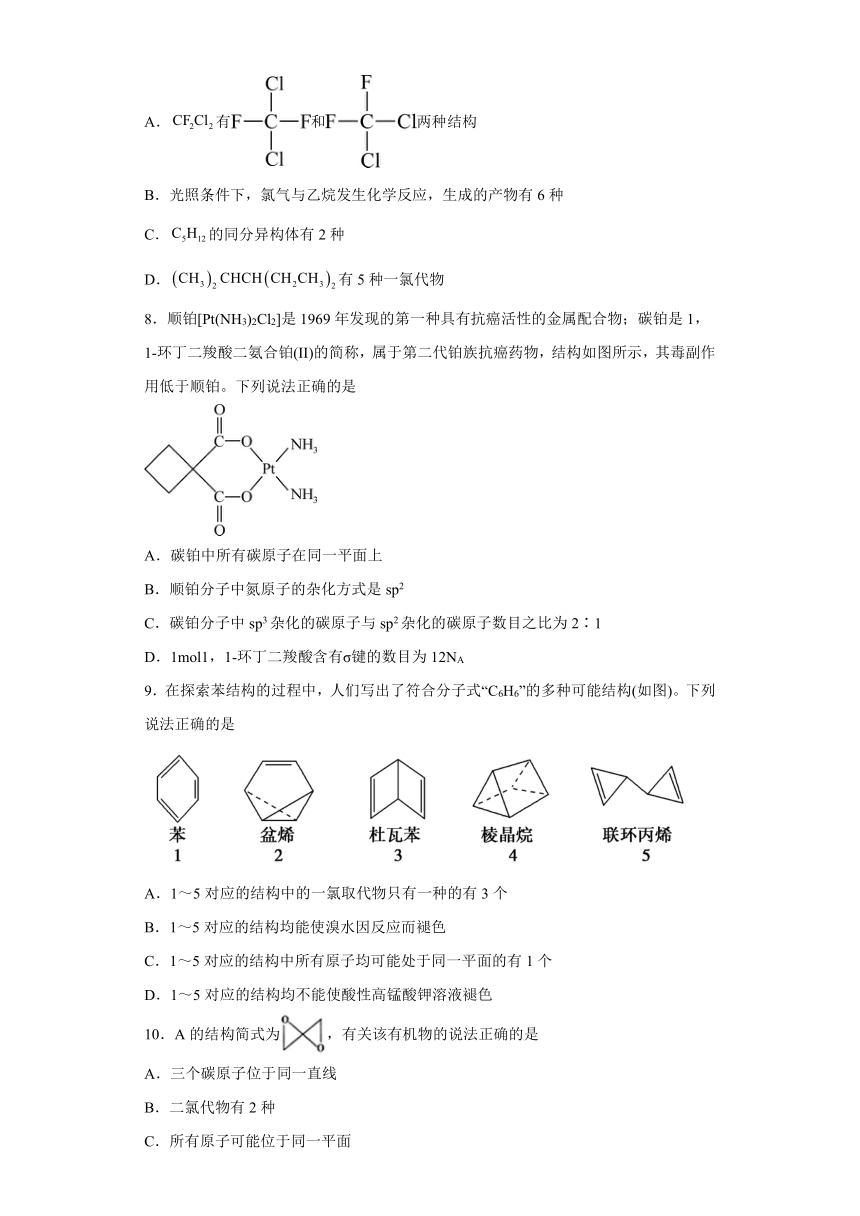
A.有和两种结构
B.光照条件下,氯气与乙烷发生化学反应,生成的产物有6种
C.的同分异构体有2种
D.有5种一氯代物
8.顺铂[Pt(NH3)2Cl2]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是1,1-环丁二羧酸二氨合铂(II)的简称,属于第二代铂族抗癌药物,结构如图所示,其毒副作用低于顺铂。下列说法正确的是
A.碳铂中所有碳原子在同一平面上
B.顺铂分子中氮原子的杂化方式是sp2
C.碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子数目之比为2∶1
D.1mol1,1-环丁二羧酸含有σ键的数目为12NA
9.在探索苯结构的过程中,人们写出了符合分子式“C6H6”的多种可能结构(如图)。下列说法正确的是
A.1~5对应的结构中的一氯取代物只有一种的有3个
B.1~5对应的结构均能使溴水因反应而褪色
C.1~5对应的结构中所有原子均可能处于同一平面的有1个
D.1~5对应的结构均不能使酸性高锰酸钾溶液褪色
10.A的结构简式为,有关该有机物的说法正确的是
A.三个碳原子位于同一直线
B.二氯代物有2种
C.所有原子可能位于同一平面
D.与其互为同分异构体的化合物有3种
11.下列说法正确的是
A.苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴
B.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
C.用新制Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖
D.分子 所有碳原子一定不能共平面
12.下列有机物的系统命名中正确的是
A.3-甲基-4-乙基戊烷 B.2,3-二甲基戊烷
C.3,4,4-三甲基己烷 D.3,5-二甲基己烷
13.如图是正丁烷的球棍模型,有关该结构说法正确的是
A.正丁烷的分子式为 B.分子中共含有12个共价键
C.与甲烷互为同系物 D.存有多种(2种以上)同分异构体
二、非选择题(共10题)
14.请按要求回答下列问题。
Ⅰ.请写出下列物质所含官能团的名称:
(1);___________
Ⅱ.请写出下列物质所含官能团的结构简式:
(2);___________
(3);___________
Ⅲ.请按照系统命名法为下列物质命名:
(4);___________
Ⅳ.按照要求写出键线式
(5)请写出2-丁烯的键线式:___________
Ⅴ.请按照要求画出相应的同分异构体:
(6)分子式为的醛共有___________种;在这些醛中,醛A的核磁共振氢谱中的信号数量最少(即峰数最少),A的结构简式是___________。
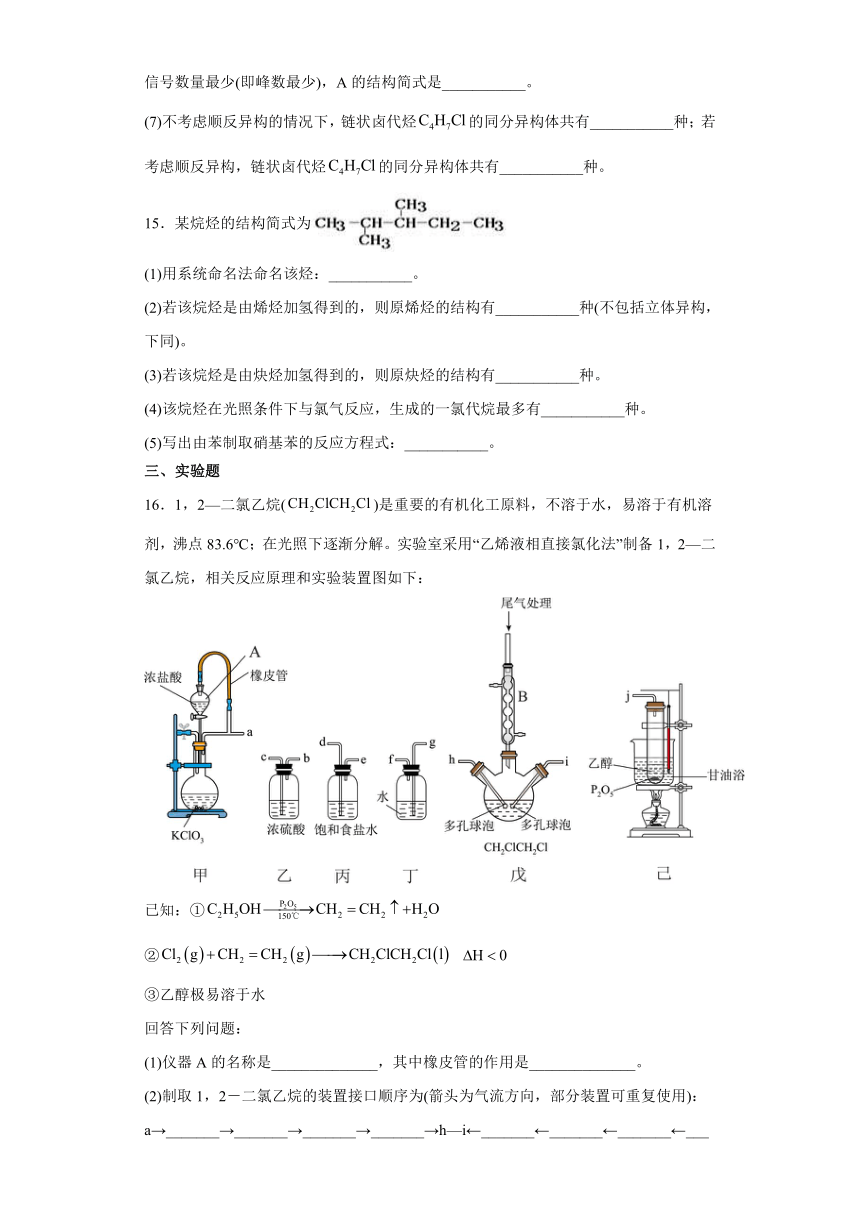
(7)不考虑顺反异构的情况下,链状卤代烃的同分异构体共有___________种;若考虑顺反异构,链状卤代烃的同分异构体共有___________种。
15.某烷烃的结构简式为
(1)用系统命名法命名该烃:___________。
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构有___________种(不包括立体异构,下同)。
(3)若该烷烃是由炔烃加氢得到的,则原炔烃的结构有___________种。
(4)该烷烃在光照条件下与氯气反应,生成的一氯代烷最多有___________种。
(5)写出由苯制取硝基苯的反应方程式:___________。
三、实验题
16.1,2—二氯乙烷()是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2—二氯乙烷,相关反应原理和实验装置图如下:
已知:①
②
③乙醇极易溶于水
回答下列问题:
(1)仪器A的名称是______________,其中橡皮管的作用是______________。
(2)制取1,2-二氯乙烷的装置接口顺序为(箭头为气流方向,部分装置可重复使用):a→_______→_______→_______→_______→h—i←_______←_______←_______←_______←j ________。
(3)丁装置的作用是____________。
(4)戊装置中B仪器的作用是_____。反应开始前先向戊中装入1,2-二氯乙烷液体,其作用是_____(填序号)。
a.溶解和乙烯 b.作催化剂 c.促进气体反应物间的接触
(5)戊装置排出尾气可以通过盛有____、NaOH溶液的洗气瓶进行吸收。
(6)产品纯度的测定:量取5.0 mL逐出和乙烯后的产品,产品密度为,加足量稀NaOH溶液,加热充分反应:
所得溶液先用稀硝酸中和至酸性,然后加入的标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35 g白色固体,则产品中1,2—二氯乙烷的纯度为__________%。
17.—硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯)
实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸);
②在三颈烧瓶里装15 mL甲苯(密度为0.866 g·cm-3);
③装好其他药品,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,大约反应10分钟至三颈烧瓶底有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯共15 g.
根据上述实验,回答下列问题:
(1)本实验的关键是控制温度在30℃左右,如果温度过高,则会产生__________等副产品(填物质名称)
(2)简述配制混酸的方法:____________________.
(3)A仪器名称是__________,进水口是__________ (填"a"或"b").
(4)写出甲苯与混酸反应生成对硝基甲苯的化学方程式:___________________________.
(5)分离产品方案如下:
操作2的名称是___________.经测定,产品2的核磁共振氢谱中有5个峰,它的名称为___________.
(6)本实验中一硝基甲苯的产率为___________ (结果保留三位有效数字)
18.利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
完成下列填空:
(1)A中反应的离子方程式是___________;有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法___________(填“正确”或“不正确”),理由是___________。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③___________。
(3)设=x,若想理论上获得最多的氯化氢,则x≥___________。
(4)一段时间后发现D中的石棉由白色变为蓝色,则棉花上可能预先滴有___________溶液。
(5)E中除盐酸外,还可能含有机物,从E中分离出盐酸的最佳方法为___________(选填编号)。
a.水洗分液法b.蒸馏法c.萃取分液法d.结晶法
(6)该装置的缺陷是,有些尾气没能处理掉,该尾气的主要成分为___________(选填编号)。
a.CH4b.CH3Clc.CH2Cl2d.CHCl3
四、计算题
19.(1)有两种气态烃组成的混和气体,对氢气的相对密度为13,取此混和气体4.48L(标准状况下)通入足量溴水中,溴水增重2.8g,则此混和气体的组成是______
A.CH4与C3H6 B.C2H4与C3H6 C.C2H4与CH4 D.CH4与C4H8
(2)0.2mol某烃A在氧气中充分燃烧后,生成物B、C 各1.2 mol。
① 烃A的分子式为_______
② 若烃A能使溴水褪色,在催化剂的作用下可与氢气加成,其产物分子中含有4个甲基,则所有符合条件的烃A的结构简式为___________
20.按要求填空:
(1)用系统命法命名
①_______。
② (CH3)2C=C(CH3)2_______。
(2)顺-2-丁烯的结构简式为:_______。
(3)3-甲基-1-丁烯的结构简式为:_______。
(4)燃烧3克某有机物生成0.1mol CO2和1.8克H2O,该有机物的蒸气对H2的相对密度为30,则该有机物的化学式为:_______。
21.现有CH4、C2H4、C2H6三种有机化合物:
(1)等质量的以上三种物质完全燃烧时消耗O2的量最多的是_______________。
(2)常温常压下,同体积的以上三种物质完全燃烧时消耗O2的量最多的是__________________。
(3)等质量的以上三种物质燃烧时,生成二氧化碳的量最多的是_____________,生成水的量最多的是_______________。
(4)在120℃、1.01×105Pa下,以上三种物质中的两种和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是_________________。
22.元素W、X、Y、Z的原子序数依次增加。p、q、r是由这些元素组成的二元化合物,m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体。
请回答下列问题:
(1)X 元素的最高价氧化物对应的水化物的阴离子构型为________________。
(2)n在水中溶解度_________(填“大于”或“小于”)n在p中溶解度,理由是:______________。
(3)n 与p 反应的化学方程式为:______________。
(4)分子式为X4W8的有机物有______________种同分异构体(考虑顺反异构)。
(5)下列化合物中属于p的同系物的是______________。
A. B. C. D.
23.下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
请按要求填空:
(1)I的电子式是___________;
(2)反应⑥的化学方程式是__________,反应③在工业上的一个重要用途是___________;
(3)反应④的化学方程式是_____________________;
(4)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是___________。
参考答案:
1.B 2.A 3.B 4.B 5.B 6.B 7.D 8.C 9.C 10.B 11.C 12.B 13.C
14.(1)碳碳双键
(2)-COOH
(3)C-Br
(4)2,4-二甲基己烷
(5)
(6) 4
(7) 8 11
15. 2,3 二甲基戊烷 5 1 6 +HO NO2+H2O
16.(1) 分液漏斗 平衡气压,使浓盐酸能顺利流下
(2)a→d→e→c→b→h—i←b←c←f←g←j
(3)除去乙烯中混有的乙醇
(4) 冷凝回流 ac
(5)溴水或酸性高锰酸钾溶液
(6)82.5%
17. 二硝基甲苯、三硝基甲苯 取一定量浓硝酸于烧杯中,向烧杯里缓缓注入浓硫酸,并用玻璃棒不断搅拌 (球形)冷凝管 a +HO-NO2+H2O 蒸馏 邻硝基甲苯 77.5%
18. 正确 若氯气与甲烷发生置换反应,也有氯化氢生成 干燥氯气和氯化氢 4 淀粉-KI a ab
19. D C6H12 (CH3)2C=C(CH3)2、CH2=C(CH3)C(CH3)2、CH2=CHC(CH3)3
20. 3,3,6-三甲基辛烷 2,3-二甲基2-丁烯 C2H4O2
21. CH4 C2H6 C2H4 CH4 CH4和C2H4
22.(1)平面三角形
(2) 小于 H2O是极性分子,苯和Br2是非极性分子,相似相溶
(3)+Br2+HBr
(4)6
(5)A
23. Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO 制漂白粉或漂白精 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O CaO2
一、单选题(共13题)
1.某烃1mol跟2mol氯化氢发生加成反应,其产物又可被10mol氯气完全取代,该烃可能是
A.1,3—丁二烯 B.1—戊炔 C.丙炔 D.丁炔
2.已知:,如果要合成,所用的原始原料可以是
A.2—甲基—1,3—丁二烯和2—丁炔 B.1,3—戊二烯和2—丁炔
C.2,3—二甲基—1,3—戊二烯和乙炔 D.1,3—丁二烯和丙炔
3.下列有关物质的比较错误的是
A.常压下的沸点:正戊烷>异戊烷>新戊烷>正丁烷>异丁烷
B.不考虑立体异构,同分异构体种数:戊烷>戊烯>丁烷
C.点燃时火焰明亮程度:乙炔>乙烯>甲烷
D.常温下的密度:己烷<水<溴乙烷
4.有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚乙烯;⑧环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是
A.①②③⑤ B.①④⑥⑦ C.④⑥⑦⑧ D.②③⑧
5.阿魏酸是阿魏、当归、酸枣仁等中药材的有效成分之一,具有抗辐射、抗氧化、抗病毒等功效,其结构如图所示。关于该有机物的说法中不正确的是
A.该有机物的分子式为C10H10O4
B.该有机物苯环上具有相同取代基的同分异构体共6种
C.1mol该分子最多与4molH2发生加成反应
D.阿魏酸分子中所有的碳原子可能共平面
6.下列化学用语正确的是
A.氨基的电子式: B.乙烯的实验式:
C.的结构示意图: D.的比例模型:
7.下列说法正确的是
A.有和两种结构
B.光照条件下,氯气与乙烷发生化学反应,生成的产物有6种
C.的同分异构体有2种
D.有5种一氯代物
8.顺铂[Pt(NH3)2Cl2]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是1,1-环丁二羧酸二氨合铂(II)的简称,属于第二代铂族抗癌药物,结构如图所示,其毒副作用低于顺铂。下列说法正确的是
A.碳铂中所有碳原子在同一平面上
B.顺铂分子中氮原子的杂化方式是sp2
C.碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子数目之比为2∶1
D.1mol1,1-环丁二羧酸含有σ键的数目为12NA
9.在探索苯结构的过程中,人们写出了符合分子式“C6H6”的多种可能结构(如图)。下列说法正确的是
A.1~5对应的结构中的一氯取代物只有一种的有3个
B.1~5对应的结构均能使溴水因反应而褪色
C.1~5对应的结构中所有原子均可能处于同一平面的有1个
D.1~5对应的结构均不能使酸性高锰酸钾溶液褪色
10.A的结构简式为,有关该有机物的说法正确的是
A.三个碳原子位于同一直线
B.二氯代物有2种
C.所有原子可能位于同一平面
D.与其互为同分异构体的化合物有3种
11.下列说法正确的是
A.苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴
B.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
C.用新制Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖
D.分子 所有碳原子一定不能共平面
12.下列有机物的系统命名中正确的是
A.3-甲基-4-乙基戊烷 B.2,3-二甲基戊烷
C.3,4,4-三甲基己烷 D.3,5-二甲基己烷
13.如图是正丁烷的球棍模型,有关该结构说法正确的是
A.正丁烷的分子式为 B.分子中共含有12个共价键
C.与甲烷互为同系物 D.存有多种(2种以上)同分异构体
二、非选择题(共10题)
14.请按要求回答下列问题。
Ⅰ.请写出下列物质所含官能团的名称:
(1);___________
Ⅱ.请写出下列物质所含官能团的结构简式:
(2);___________
(3);___________
Ⅲ.请按照系统命名法为下列物质命名:
(4);___________
Ⅳ.按照要求写出键线式
(5)请写出2-丁烯的键线式:___________
Ⅴ.请按照要求画出相应的同分异构体:
(6)分子式为的醛共有___________种;在这些醛中,醛A的核磁共振氢谱中的信号数量最少(即峰数最少),A的结构简式是___________。
(7)不考虑顺反异构的情况下,链状卤代烃的同分异构体共有___________种;若考虑顺反异构,链状卤代烃的同分异构体共有___________种。
15.某烷烃的结构简式为
(1)用系统命名法命名该烃:___________。
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构有___________种(不包括立体异构,下同)。
(3)若该烷烃是由炔烃加氢得到的,则原炔烃的结构有___________种。
(4)该烷烃在光照条件下与氯气反应,生成的一氯代烷最多有___________种。
(5)写出由苯制取硝基苯的反应方程式:___________。
三、实验题
16.1,2—二氯乙烷()是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2—二氯乙烷,相关反应原理和实验装置图如下:
已知:①
②
③乙醇极易溶于水
回答下列问题:
(1)仪器A的名称是______________,其中橡皮管的作用是______________。
(2)制取1,2-二氯乙烷的装置接口顺序为(箭头为气流方向,部分装置可重复使用):a→_______→_______→_______→_______→h—i←_______←_______←_______←_______←j ________。
(3)丁装置的作用是____________。
(4)戊装置中B仪器的作用是_____。反应开始前先向戊中装入1,2-二氯乙烷液体,其作用是_____(填序号)。
a.溶解和乙烯 b.作催化剂 c.促进气体反应物间的接触
(5)戊装置排出尾气可以通过盛有____、NaOH溶液的洗气瓶进行吸收。
(6)产品纯度的测定:量取5.0 mL逐出和乙烯后的产品,产品密度为,加足量稀NaOH溶液,加热充分反应:
所得溶液先用稀硝酸中和至酸性,然后加入的标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35 g白色固体,则产品中1,2—二氯乙烷的纯度为__________%。
17.—硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯)
实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸);
②在三颈烧瓶里装15 mL甲苯(密度为0.866 g·cm-3);
③装好其他药品,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,大约反应10分钟至三颈烧瓶底有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯共15 g.
根据上述实验,回答下列问题:
(1)本实验的关键是控制温度在30℃左右,如果温度过高,则会产生__________等副产品(填物质名称)
(2)简述配制混酸的方法:____________________.
(3)A仪器名称是__________,进水口是__________ (填"a"或"b").
(4)写出甲苯与混酸反应生成对硝基甲苯的化学方程式:___________________________.
(5)分离产品方案如下:
操作2的名称是___________.经测定,产品2的核磁共振氢谱中有5个峰,它的名称为___________.
(6)本实验中一硝基甲苯的产率为___________ (结果保留三位有效数字)
18.利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
完成下列填空:
(1)A中反应的离子方程式是___________;有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法___________(填“正确”或“不正确”),理由是___________。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③___________。
(3)设=x,若想理论上获得最多的氯化氢,则x≥___________。
(4)一段时间后发现D中的石棉由白色变为蓝色,则棉花上可能预先滴有___________溶液。
(5)E中除盐酸外,还可能含有机物,从E中分离出盐酸的最佳方法为___________(选填编号)。
a.水洗分液法b.蒸馏法c.萃取分液法d.结晶法
(6)该装置的缺陷是,有些尾气没能处理掉,该尾气的主要成分为___________(选填编号)。
a.CH4b.CH3Clc.CH2Cl2d.CHCl3
四、计算题
19.(1)有两种气态烃组成的混和气体,对氢气的相对密度为13,取此混和气体4.48L(标准状况下)通入足量溴水中,溴水增重2.8g,则此混和气体的组成是______
A.CH4与C3H6 B.C2H4与C3H6 C.C2H4与CH4 D.CH4与C4H8
(2)0.2mol某烃A在氧气中充分燃烧后,生成物B、C 各1.2 mol。
① 烃A的分子式为_______
② 若烃A能使溴水褪色,在催化剂的作用下可与氢气加成,其产物分子中含有4个甲基,则所有符合条件的烃A的结构简式为___________
20.按要求填空:
(1)用系统命法命名
①_______。
② (CH3)2C=C(CH3)2_______。
(2)顺-2-丁烯的结构简式为:_______。
(3)3-甲基-1-丁烯的结构简式为:_______。
(4)燃烧3克某有机物生成0.1mol CO2和1.8克H2O,该有机物的蒸气对H2的相对密度为30,则该有机物的化学式为:_______。
21.现有CH4、C2H4、C2H6三种有机化合物:
(1)等质量的以上三种物质完全燃烧时消耗O2的量最多的是_______________。
(2)常温常压下,同体积的以上三种物质完全燃烧时消耗O2的量最多的是__________________。
(3)等质量的以上三种物质燃烧时,生成二氧化碳的量最多的是_____________,生成水的量最多的是_______________。
(4)在120℃、1.01×105Pa下,以上三种物质中的两种和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是_________________。
22.元素W、X、Y、Z的原子序数依次增加。p、q、r是由这些元素组成的二元化合物,m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体。
请回答下列问题:
(1)X 元素的最高价氧化物对应的水化物的阴离子构型为________________。
(2)n在水中溶解度_________(填“大于”或“小于”)n在p中溶解度,理由是:______________。
(3)n 与p 反应的化学方程式为:______________。
(4)分子式为X4W8的有机物有______________种同分异构体(考虑顺反异构)。
(5)下列化合物中属于p的同系物的是______________。
A. B. C. D.
23.下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
请按要求填空:
(1)I的电子式是___________;
(2)反应⑥的化学方程式是__________,反应③在工业上的一个重要用途是___________;
(3)反应④的化学方程式是_____________________;
(4)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是___________。
参考答案:
1.B 2.A 3.B 4.B 5.B 6.B 7.D 8.C 9.C 10.B 11.C 12.B 13.C
14.(1)碳碳双键
(2)-COOH
(3)C-Br
(4)2,4-二甲基己烷
(5)
(6) 4
(7) 8 11
15. 2,3 二甲基戊烷 5 1 6 +HO NO2+H2O
16.(1) 分液漏斗 平衡气压,使浓盐酸能顺利流下
(2)a→d→e→c→b→h—i←b←c←f←g←j
(3)除去乙烯中混有的乙醇
(4) 冷凝回流 ac
(5)溴水或酸性高锰酸钾溶液
(6)82.5%
17. 二硝基甲苯、三硝基甲苯 取一定量浓硝酸于烧杯中,向烧杯里缓缓注入浓硫酸,并用玻璃棒不断搅拌 (球形)冷凝管 a +HO-NO2+H2O 蒸馏 邻硝基甲苯 77.5%
18. 正确 若氯气与甲烷发生置换反应,也有氯化氢生成 干燥氯气和氯化氢 4 淀粉-KI a ab
19. D C6H12 (CH3)2C=C(CH3)2、CH2=C(CH3)C(CH3)2、CH2=CHC(CH3)3
20. 3,3,6-三甲基辛烷 2,3-二甲基2-丁烯 C2H4O2
21. CH4 C2H6 C2H4 CH4 CH4和C2H4
22.(1)平面三角形
(2) 小于 H2O是极性分子,苯和Br2是非极性分子,相似相溶
(3)+Br2+HBr
(4)6
(5)A
23. Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO 制漂白粉或漂白精 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O CaO2
