3.1《认识晶体》第1课时 选择性必修2 鲁科版(2019)
文档属性
| 名称 | 3.1《认识晶体》第1课时 选择性必修2 鲁科版(2019) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-08 00:00:00 | ||
图片预览










文档简介
(共32张PPT)
第1课时 晶体的特性和晶体结构的堆积模型
第3章 第1节 认识晶体
【学习目标】
1.了解晶体的概念、重要特征和简单分类。
2.通过等径圆球与非等径圆球的堆积模型认识晶体中微粒排列的周期性规律。
观察图片,这些固体在外形上有什么区别?
金刚石
Cu晶体结构示意图
构成晶体与非晶体的微粒在空间的排列有何不同
NaCl晶体结构示意图
1.晶体与非晶体
(1)晶体:内部微粒(原子、离子或分子)在空间按一定规律做周期性重复排列构成的固体物质。如食盐、冰、金属、宝石、水晶、大部分矿石等。
(2)非晶体:内部微粒的排列呈现杂乱无章的分布状态。如玻璃、橡胶、石蜡、松香 等。
一、认识晶体
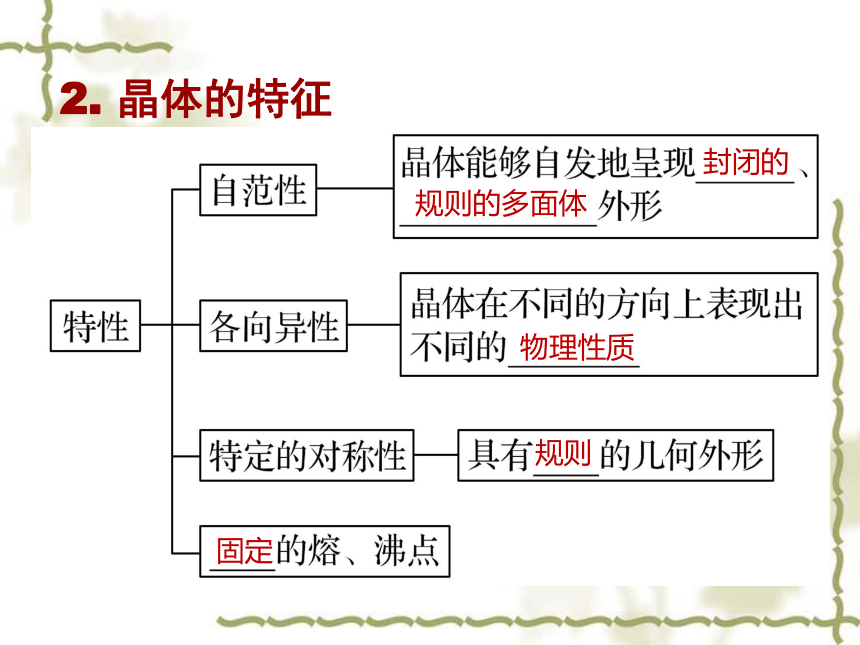
2. 晶体的特征
封闭的
规则的多面体
物理性质
规则
固定
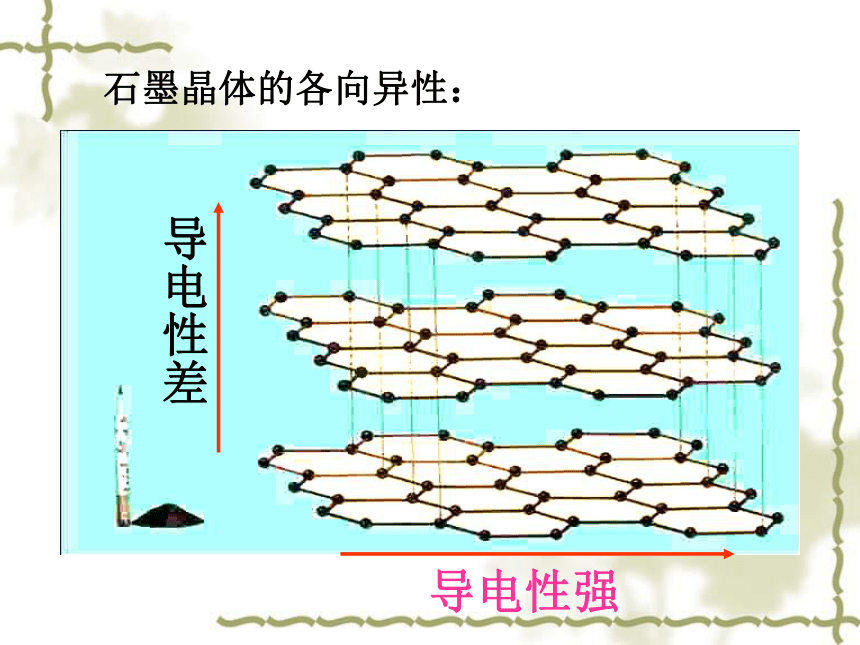
导电性差
导电性强
石墨晶体的各向异性:
涂有石蜡的水晶片
热的铁针
涂有石蜡的玻璃片
热的铁针
石蜡融化的对比性实验:
晶体有各向异性;非晶体有各向同性。
3.常见的四种晶体类型
晶体类型 构成微粒种类 微粒间的相互作用
实例
离子晶体
NaCl
金属晶体
Cu
原子晶体
金刚石
分子晶体
干冰
阴、阳离子
离子键
金属阳离子、自由电子
金属键
原子
共价键
分子
分子间作用力
1、判断题:
(1)有规则几何外形或美观、对称外形的固体,一定是晶体。
(2)具有固定组成的物质也不一定是晶体。
(3)晶体一定都有规则的几何外形。
答案:
(1)错。如玻璃制品既可以塑造出规则的几何外形,也可以具有美观、对称的外形。
(2)对。如某些无定形体也有固定的组成。
(3)错。如玛瑙。
【知识点睛】晶体与非晶体的区别:
1、要区分一种固体是晶体还是非晶体,你有哪些方法?
2、决定晶体与非晶体性质不同的本质原因是什么?
3、确定固体是晶体的最科学的方法是什么?
答:外观、自范性、各向异性、熔沸点等方法进行综合区分。
答:物质内部微粒是否有规则的排列。
答:X射线衍射实验。
二、晶体结构的堆积模型
【问题导学】
1、各类晶体的构成微粒为什么尽可能采取密堆积的形式形成晶体?
2、如何通过建立模型认知紧密堆积模型?
3、各类晶体内部微粒的堆积原理有何异同?
思考感悟
1、为什么在金属晶体、离子晶体、分子晶体中各微粒尽量采取紧密堆积的排列方式?
【提示】 由于在金属晶体、离子晶体和分子晶体的结构中,金属键、离子键和分子间作用力均无方向性,因此都趋向于使原子、离子或分子吸引尽可能多的其他原子、离子或分子分布于其周围,并以密堆积的方式降低体系的能量,使晶体变得比较稳定。
2、构建等径圆球的密堆积模型
由于金属键没有方向性,每个金属原子中的电子分布基本是球对称的,所以可以把金属晶体看成是由直径相等的圆球的三维空间堆积而成的。
等径圆球密堆积模型的构建要通过对微粒排成列、面、多层等多种堆积方式进行逐一探究,请同学们通过实验进行探究建模过程。
——金属晶体的密堆积结构
1. 等径圆球在同一平面上有几种最紧密排列型式?
2. 同一密置层内每个球可以紧密接触的球有几个?
【构建等径圆球的密堆积模型】
4. 在密置双层上再加一密置层,有几种最密堆积方式?
5. A3型最密堆积的周期性如何体现?
A1型最密堆积的周期性如何体现?
3. 等径圆球的密置双层有几种型式?
【列】在一列上的密堆积排列:
所有的圆球都在一条直线上排列
【一层】在一个平面上的密堆积排列:
在一个层中,最紧密的堆积方式是:一个球与周围6个球相切,在中心的周围形成6个凹位,将其算为第一层 ————————————————密置层
一种常见的非密置层
密置层
1
2
3
4
5
6
【 第二层】对第二层来讲最紧密的堆积方式是将球对准1,3,5 位或对准 2,4,6 位,其情形是一样的 ----密置双层
1
2
3
4
5
6
在密置双层的基础上再加【第三层】的方式:
第三层球与第一层球重叠(即A3型密堆积)
第三层球的位置不同于第一、二层球的位置(即A 1型密堆积)
下图是A3型最密堆积的前视图
A
B
A
B
A
第一种是排列方式:将球对准第一层的球。
1
2
3
4
5
6
于是每两层形成一个周期,即 AB AB 堆积方式,形成 A3型最密堆积
关键是第三层,对第一、二层来说,第三层可以有两种最紧密的堆积方式。
第二种排列方式: 是将球对准第一层的 2,4,6 位,不同于 AB 两层的位置,这是 C 层。
1
2
3
4
5
6
1
2
3
4
5
6
1
2
3
4
5
6
1
2
3
4
5
6
A1型最密堆积的前视图
A
B
C
A
A
B
C
第四层再排 A,于是形成 ABC ABC 三层一个周期。 得到A1型最密堆积
配位数:在密堆积中,一个原子或离子周围所邻接的原子或离子数目。
A3型最密堆积
A1型最密堆积
配位数 12
( 同层 6,上下层各3 )
配位数 12
( 同层 6,上下层各3 )
3、构建非等径圆球的密堆积模型
——离子晶体的密堆积模型
大球先按一定的方式做等径圆球密堆积
小球再填充到大球所形成的空隙中
NaCl: 离子先以A1型紧密堆积, 离子再填充到空隙中。
ZnS: 离子先以A1型紧密堆积, 离子再填充到空隙中。
Cl-
Na+
S2-
Zn2+
由于范德华力没有方向性和饱和性,因此分子间尽可能采取紧密排列方式,但分子的排列方式与分子的形状有关。如:CO2作为直线型分子的二氧化碳在空间是以A1型密堆积方式形成晶体的。
4、分子晶体的堆积方式(紧密堆积方式)
5、原子晶体堆积方式
—— 不服从紧密堆积方式
原因:共价键具有饱和性和方向性,因此就决定了一个原子周围的其他原子的数目不仅是有限的,而且堆积方向是一定的,所以不是密堆积。
第1课时 晶体的特性和晶体结构的堆积模型
第3章 第1节 认识晶体
【学习目标】
1.了解晶体的概念、重要特征和简单分类。
2.通过等径圆球与非等径圆球的堆积模型认识晶体中微粒排列的周期性规律。
观察图片,这些固体在外形上有什么区别?
金刚石
Cu晶体结构示意图
构成晶体与非晶体的微粒在空间的排列有何不同
NaCl晶体结构示意图
1.晶体与非晶体
(1)晶体:内部微粒(原子、离子或分子)在空间按一定规律做周期性重复排列构成的固体物质。如食盐、冰、金属、宝石、水晶、大部分矿石等。
(2)非晶体:内部微粒的排列呈现杂乱无章的分布状态。如玻璃、橡胶、石蜡、松香 等。
一、认识晶体
2. 晶体的特征
封闭的
规则的多面体
物理性质
规则
固定
导电性差
导电性强
石墨晶体的各向异性:
涂有石蜡的水晶片
热的铁针
涂有石蜡的玻璃片
热的铁针
石蜡融化的对比性实验:
晶体有各向异性;非晶体有各向同性。
3.常见的四种晶体类型
晶体类型 构成微粒种类 微粒间的相互作用
实例
离子晶体
NaCl
金属晶体
Cu
原子晶体
金刚石
分子晶体
干冰
阴、阳离子
离子键
金属阳离子、自由电子
金属键
原子
共价键
分子
分子间作用力
1、判断题:
(1)有规则几何外形或美观、对称外形的固体,一定是晶体。
(2)具有固定组成的物质也不一定是晶体。
(3)晶体一定都有规则的几何外形。
答案:
(1)错。如玻璃制品既可以塑造出规则的几何外形,也可以具有美观、对称的外形。
(2)对。如某些无定形体也有固定的组成。
(3)错。如玛瑙。
【知识点睛】晶体与非晶体的区别:
1、要区分一种固体是晶体还是非晶体,你有哪些方法?
2、决定晶体与非晶体性质不同的本质原因是什么?
3、确定固体是晶体的最科学的方法是什么?
答:外观、自范性、各向异性、熔沸点等方法进行综合区分。
答:物质内部微粒是否有规则的排列。
答:X射线衍射实验。
二、晶体结构的堆积模型
【问题导学】
1、各类晶体的构成微粒为什么尽可能采取密堆积的形式形成晶体?
2、如何通过建立模型认知紧密堆积模型?
3、各类晶体内部微粒的堆积原理有何异同?
思考感悟
1、为什么在金属晶体、离子晶体、分子晶体中各微粒尽量采取紧密堆积的排列方式?
【提示】 由于在金属晶体、离子晶体和分子晶体的结构中,金属键、离子键和分子间作用力均无方向性,因此都趋向于使原子、离子或分子吸引尽可能多的其他原子、离子或分子分布于其周围,并以密堆积的方式降低体系的能量,使晶体变得比较稳定。
2、构建等径圆球的密堆积模型
由于金属键没有方向性,每个金属原子中的电子分布基本是球对称的,所以可以把金属晶体看成是由直径相等的圆球的三维空间堆积而成的。
等径圆球密堆积模型的构建要通过对微粒排成列、面、多层等多种堆积方式进行逐一探究,请同学们通过实验进行探究建模过程。
——金属晶体的密堆积结构
1. 等径圆球在同一平面上有几种最紧密排列型式?
2. 同一密置层内每个球可以紧密接触的球有几个?
【构建等径圆球的密堆积模型】
4. 在密置双层上再加一密置层,有几种最密堆积方式?
5. A3型最密堆积的周期性如何体现?
A1型最密堆积的周期性如何体现?
3. 等径圆球的密置双层有几种型式?
【列】在一列上的密堆积排列:
所有的圆球都在一条直线上排列
【一层】在一个平面上的密堆积排列:
在一个层中,最紧密的堆积方式是:一个球与周围6个球相切,在中心的周围形成6个凹位,将其算为第一层 ————————————————密置层
一种常见的非密置层
密置层
1
2
3
4
5
6
【 第二层】对第二层来讲最紧密的堆积方式是将球对准1,3,5 位或对准 2,4,6 位,其情形是一样的 ----密置双层
1
2
3
4
5
6
在密置双层的基础上再加【第三层】的方式:
第三层球与第一层球重叠(即A3型密堆积)
第三层球的位置不同于第一、二层球的位置(即A 1型密堆积)
下图是A3型最密堆积的前视图
A
B
A
B
A
第一种是排列方式:将球对准第一层的球。
1
2
3
4
5
6
于是每两层形成一个周期,即 AB AB 堆积方式,形成 A3型最密堆积
关键是第三层,对第一、二层来说,第三层可以有两种最紧密的堆积方式。
第二种排列方式: 是将球对准第一层的 2,4,6 位,不同于 AB 两层的位置,这是 C 层。
1
2
3
4
5
6
1
2
3
4
5
6
1
2
3
4
5
6
1
2
3
4
5
6
A1型最密堆积的前视图
A
B
C
A
A
B
C
第四层再排 A,于是形成 ABC ABC 三层一个周期。 得到A1型最密堆积
配位数:在密堆积中,一个原子或离子周围所邻接的原子或离子数目。
A3型最密堆积
A1型最密堆积
配位数 12
( 同层 6,上下层各3 )
配位数 12
( 同层 6,上下层各3 )
3、构建非等径圆球的密堆积模型
——离子晶体的密堆积模型
大球先按一定的方式做等径圆球密堆积
小球再填充到大球所形成的空隙中
NaCl: 离子先以A1型紧密堆积, 离子再填充到空隙中。
ZnS: 离子先以A1型紧密堆积, 离子再填充到空隙中。
Cl-
Na+
S2-
Zn2+
由于范德华力没有方向性和饱和性,因此分子间尽可能采取紧密排列方式,但分子的排列方式与分子的形状有关。如:CO2作为直线型分子的二氧化碳在空间是以A1型密堆积方式形成晶体的。
4、分子晶体的堆积方式(紧密堆积方式)
5、原子晶体堆积方式
—— 不服从紧密堆积方式
原因:共价键具有饱和性和方向性,因此就决定了一个原子周围的其他原子的数目不仅是有限的,而且堆积方向是一定的,所以不是密堆积。
