江西省2022-2023学年高二下学期5月联合调研考试化学试题(含答案)
文档属性
| 名称 | 江西省2022-2023学年高二下学期5月联合调研考试化学试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 515.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-08 00:00:00 | ||
图片预览




文档简介
机密★启用前
江西省2022-2023学年高二下学期5月联合调研考试
化学试卷
本试卷共8页,19题.全卷满分100分.考试时间75分钟.
★祝考试顺利★
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置.
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑.写在试卷、草稿纸和答题卡上的非答题区域均无效.
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内.写在试卷、草稿纸和答题卡的非答题区域均无效.
4.考试结束后,请将本试卷和答题卡一并上交.
可能用到的相对原子质量:H 1 Li 7 C 12 O 16 S 32 Cl 35.5 Ag 108
一、选择题:本题共15小题,每小题3分,共45分.在每小题列出的四个选项中,只有一项是符合题目要求的.
1.化学创造美好生活.下列叙述中没有涉及化学变化的是( )
A.过氧乙酸用于公共场所的消毒
B.以丙酸为原料生产退烧药布洛芬
C.北京冬奥会场馆用跨临界直冷制冰
D.科学家成功将转化为淀粉促进“碳中和”
2.是新一代超高压绝缘介质材料.其制备原理为:.下列说法错误的是( )
A.中心原子价层电子对数为6 B.电负性:
C.半径: D.为直线形分子
3.是阿伏加德罗常数的值.下列说法正确的是( )
A.中配位键数目为
B.的溶液中含氢原子数为
C.标准状况下,中杂化的原子数目为
D.乙烯和丙烯的混合物中含C原子数为
4.能正确表示下列反应的化学方程式是( )
A.苯与溴水、Fe粉混合:
B.溴乙烷与的醇溶液共热:
C.向苯酚钠溶液中通入足量:
D.乙酸与乙醇反应制取乙酸乙酯:
5.Calanolide A用于治疗HIV-1感染.其结构简式如右图所示.下列关于Calanolide A的说法错误的是( )
A.属于芳香族化合物 B.含3个手性C原子
C.遇溶液显紫色 D.可发生加成、氧化和水解反应
6.2022年,中科院以富勒烯为原料合成了典型半导体——单层聚合.富勒烯和单层聚合结构如图所示,下列说法错误的是( )
A.富勒烯和单层聚合均为分子晶体 B.熔、沸点:单层聚合富勒烯
C.富勒烯中的碳原子采取杂化 D.富勒烯和单层聚合互为同素异形体
7.短周期元素X、Y、Z、M、N、W原子序数依次递增,六种元素形成的一种化合物结构如图所示,元素Z的s能级电子数与p能级电子数相等.下列说法错误的是( )
A.最高价氧化物对应水化物的酸性:
B.X与M可形成离子化合物
C.Z的氢化物沸点不一定高于Y的氢化物沸点
D.N与W形成的化合物中各原子均满足稳定结构
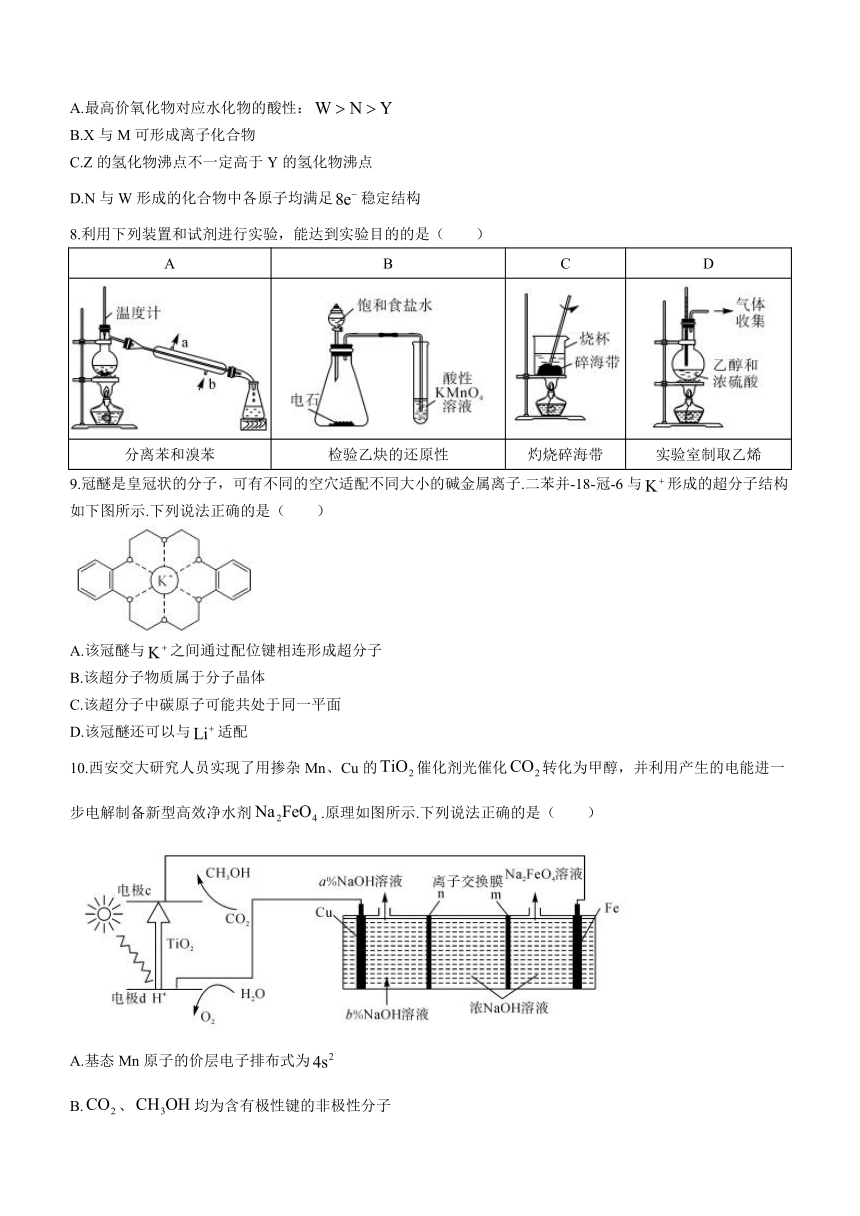
8.利用下列装置和试剂进行实验,能达到实验目的的是( )
A B C D
分离苯和溴苯 检验乙炔的还原性 灼烧碎海带 实验室制取乙烯
9.冠醚是皇冠状的分子,可有不同的空穴适配不同大小的碱金属离子.二苯并-18-冠-6与形成的超分子结构如下图所示.下列说法正确的是( )
A.该冠醚与之间通过配位键相连形成超分子
B.该超分子物质属于分子晶体
C.该超分子中碳原子可能共处于同一平面
D.该冠醚还可以与适配
10.西安交大研究人员实现了用掺杂Mn、Cu的催化剂光催化转化为甲醇,并利用产生的电能进一步电解制备新型高效净水剂.原理如图所示.下列说法正确的是( )
A.基态Mn原子的价层电子排布式为
B.、均为含有极性键的非极性分子
C.的VSEPR模型为三角锥形
D.该装置实现了光能→电能→化学能的转化
11.酮基布洛芬片是用于治疗各种关节肿痛、牙痛等的非处方药.可由物质A经一系列反应制得,下列说法错误的是( )
A.物质A与苯甲酸互为同系物
B.1 mol酮基布洛芬最多可与发生加成反应
C.物质A中所有碳原子一定共平面
D.可用酸性高锰酸钾溶液来鉴别物质A和酮基布洛芬
12.下列说法错误的是( )
A.键能:,因此比稳定
B.沸点:,因为分子间范德华力更强
C.键角:,因为的成键电子对间的排斥力更大
D.极性:,因此酸性
13.1,3-丁二烯与溴单质按物质的量1:1发生加成反应时,会生成两种物质M和N(不考虑立体异构),其反应机理如图甲所示,下列说法错误的是( )
A.N存在顺反两种异构体
B.M、N互为同分异构体
C.该过程涉及非极性键的断裂和形成
D.根据以上反应机理,一定条件下,将1,3-丁二烯和水蒸汽等物质的量混合,有3种物质生成
14.确定有机化合物组成和结构的方法很多,下列说法错误的是( )
A.质谱仪可用于有机物相对分子质量的测定
B.异丁烷的核磁共振氢谱中有2组峰
C.红外光谱可检测未知物中是否含单键、双键、氢键等化学键
D.X-射线衍射法鉴别某是否属于晶体
15.苯甲酸是常用的食品添加剂,实验室用以下方法可获得纯净的苯甲酸.下列说法正确的是( )
已知:苯甲酸100℃以上易升华,微溶于冷水,易溶于热水、乙醇等.
A.若要得到纯度更高的苯甲酸,应采用多次萃取的方法
B.步骤③涉及的操作为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C.洗涤晶体时应选择乙醇
D.干燥晶体时,温度不宜过高,主要是防止苯甲酸晶体升华造成产品产率降低
二、非选择题:本题共4小题,共55分.
16.(12分)我国在新型锂离子电池电极材料研究方面取得重大突破:膨胀石墨(EG)纳米复合材料、PET复合Cu箔、黑磷-石墨复合材料的使用极大提高了电池的能量和安全性.回答下列问题:
(1)Ni元素在周期表中的位置是__________,与Ni同周期元素中,基态原子的未成对电子数与Ni相同的有___________种.
(2)第二电离能:Fe__________Cu(选填“>”或“<”),原因是__________________.
(3)白磷、红磷、黑磷是P元素形成的三种常见单质.黑磷结构与石墨类似,也具有层状结构(如图1),黑磷-石墨复合材料单层结构俯视图如图2.
下列说法正确的是___________(填字母).
A.黑磷中P-P键键能完全相同
B.P的三种常见单质中,黑磷的熔沸点最高
C.黑磷中存在大键,易导电
D.在结合区,P原子与C原子之间的作用力属范德华力
(4)是目前正在开发的电池正极活性物质,其晶胞结构如图3.
①图3中的配位数为______________;
②已知A的坐标为,B的坐标为__________;
③设阿伏加德罗常数的值为,则晶体的密度为___________(用含,的代数式表示).
17.(14分)氯化苄常用于染料、药物的合成.实验室用甲苯和干燥为原料在光照和加热时合成并提纯氯化苄装置图(加持装置略去)如下:
各物质熔沸点如下表:
物质 甲苯 氯化苄 二氯化苄 三氯化苄
熔点(℃) -95 -39 -16 -7
沸点(℃) 110 179 205 220
回答下列问题:
(1)a的名称是_________,相比于分液漏斗,a的优点_______________.
(2)D中加热前需要加几粒沸石,目的是_____________,装置E的作用是_________________.
(3)A中的离子反应方程式为_______________________________.
(4)实验结束后,为得到纯净的氯化苄,应关闭__________,打开(填,,),加热三颈烧瓶,蒸馏.收集氯化苄时温度计的读数范围是____________.
(5)检测氯化苄样品的纯度:
①称取13.00g样品于烧杯中,加入溶液,水浴加热,冷却后加入足量溶液,充分振荡加水配成100mL溶液.取20.00mL溶液于试管中,加入足量的溶液,充分振荡,过滤、洗涤、干燥,称量固体质量为2.87g,则该样品的纯度为____________%(结果保留小数点后1位).
②实际测量结果往往会偏高,原因是_______________________________.
(6)指出该装置中可能存在的缺点___________________________.
18.(13分)某化学小组为探究和新制反应的产物,进行如下实验:向试管中依次加入溶液、溶液,的甲醛溶液,65℃水浴加热,反应结束后试管中有红色固体生成,量筒中收集到无色气体.回答下列问题:
(1)NaOH溶液过量的目的是__________;使用水浴加热的目的是_____________.
(2)小组同学对实验中红色固体产物的组成作出猜想:
猜想一:只有;
猜想二:只有Cu;
猜想三:_________________.
为了验证固体产物,设计如下实验方案并进行实验(以下每步均充分反应):
已知:i.
ii.
①中,中心离子的配位数为__________,配体的空间构型为_______________;
②将容量瓶ii中的溶解稀释50倍后,溶液的颜色与容量瓶i相近,则猜想________(填“一”“二”或“三”)正确.
(3)小组同学猜测收集的气体可能是、中的一种或两种,将收集的气体利用如图所示的装置进行实验(部分夹持仪器略去).
①依次连接的合理顺序为:(量筒中气体)→B→_______→_______→_______→_______→G.
②最终确认气体产物中含CO而不含,依据是_________________________.
(4)在该小组同学的实验条件下,HCHO与新制反应的方程式为_______________.
19.(16分)氟他胺(G)是可用于治疗肿瘤.实验室由芳香烃A制备G的合成路线如下图:
已知:①;
②吡啶是一种有机碱.
(1)A的一氯取代物有_________种;G中含有的官能团名称为________________.
(2)该合成路线中属于取代反应的有_______________(填序号).
(3)⑤的化学方程式为__________________,吡啶的作用是____________________.
(4)C经反应可得H,有多种同分异构体,写出满足下列条件的同分异体__________.
①属于芳香族化合物;
②能发生银镜反应;
③核磁共振氢谱有4组峰,且峰面积比为1:2:2:1.
(5)由苯甲醚()为原料可制取4-甲氧基乙酰苯胺().请结合上述流程信息,将合成路线补充完整.
江西省2022-2023学年高二下学期5月联合调研考试
化学
参考答案、提示及评分细则
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C D A C C A D A A D D B C C D
16.【参考答案及评分细则】
(1)第四周期第Ⅷ族(1分.周期或族答错均不得分);3(2分)
(2)(1分);、的价电子排布式分别为、,的轨道全充满较稳定,难再失去一个电子,所以第二电离能(2分)
(3)BC(2分.对一个得1分,全对2分,有其他错误选项得0分)
(4)8(1分);(1分);(2分)
17.【参考答案及评分细则】
(1)恒压滴液漏斗(1分.有错别字得0分);平衡漏斗与烧瓶内压强,使浓盐酸顺利滴下(1分)
(2)防暴沸(1分);冷凝回流(1分.或回答“使有机物冷凝回流,提高反应物转化率和生成物产率”得1分)
(3)(2分.未打“”得1分,有其他错误得0分)
(4)、(1分.全对得1分);(1分);(1分)
(5)97.3(2分);样品中混有二氯化苄等杂质(1分)
(6)应在氢氧化钠溶液与E之间加一干燥装置,防止水蒸气进入装置D(2分)
18.【参考答案及评分细则】
(1)提供碱性环境(1分);受热均匀,温度易控制(2分)
(2)和的混合物(1分);4(1分);三角锥形(1分);三(1分)
(3)EFDC(2分.全对2分,有错误不得分);F中黑色固体变红色(或C中的澄清石灰水变浑浊),D中固体不变蓝色(2分.只写一个现象不得分)
(4)(2分.条件末写,“”未打总共扣1分)
19.【参考答案及评分细则】
(1)4(1分);硝基、碳氟键、酰胺基(3分.1个1分,全对得3分)
(2)①②③⑤⑥(2分.全对2分,只对1个不得分,对2~4个得1分,见错无分)
(3)(2分.条件未写得1分);
吸收反应生成的,提高反应转化率(2分)
(4)(或)(2分)
(5)
(全对4分.浓,浓,Δ写对得1分;,写对得1分;写对得1分;写对得1分)
江西省2022-2023学年高二下学期5月联合调研考试
化学试卷
本试卷共8页,19题.全卷满分100分.考试时间75分钟.
★祝考试顺利★
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置.
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑.写在试卷、草稿纸和答题卡上的非答题区域均无效.
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内.写在试卷、草稿纸和答题卡的非答题区域均无效.
4.考试结束后,请将本试卷和答题卡一并上交.
可能用到的相对原子质量:H 1 Li 7 C 12 O 16 S 32 Cl 35.5 Ag 108
一、选择题:本题共15小题,每小题3分,共45分.在每小题列出的四个选项中,只有一项是符合题目要求的.
1.化学创造美好生活.下列叙述中没有涉及化学变化的是( )
A.过氧乙酸用于公共场所的消毒
B.以丙酸为原料生产退烧药布洛芬
C.北京冬奥会场馆用跨临界直冷制冰
D.科学家成功将转化为淀粉促进“碳中和”
2.是新一代超高压绝缘介质材料.其制备原理为:.下列说法错误的是( )
A.中心原子价层电子对数为6 B.电负性:
C.半径: D.为直线形分子
3.是阿伏加德罗常数的值.下列说法正确的是( )
A.中配位键数目为
B.的溶液中含氢原子数为
C.标准状况下,中杂化的原子数目为
D.乙烯和丙烯的混合物中含C原子数为
4.能正确表示下列反应的化学方程式是( )
A.苯与溴水、Fe粉混合:
B.溴乙烷与的醇溶液共热:
C.向苯酚钠溶液中通入足量:
D.乙酸与乙醇反应制取乙酸乙酯:
5.Calanolide A用于治疗HIV-1感染.其结构简式如右图所示.下列关于Calanolide A的说法错误的是( )
A.属于芳香族化合物 B.含3个手性C原子
C.遇溶液显紫色 D.可发生加成、氧化和水解反应
6.2022年,中科院以富勒烯为原料合成了典型半导体——单层聚合.富勒烯和单层聚合结构如图所示,下列说法错误的是( )
A.富勒烯和单层聚合均为分子晶体 B.熔、沸点:单层聚合富勒烯
C.富勒烯中的碳原子采取杂化 D.富勒烯和单层聚合互为同素异形体
7.短周期元素X、Y、Z、M、N、W原子序数依次递增,六种元素形成的一种化合物结构如图所示,元素Z的s能级电子数与p能级电子数相等.下列说法错误的是( )
A.最高价氧化物对应水化物的酸性:
B.X与M可形成离子化合物
C.Z的氢化物沸点不一定高于Y的氢化物沸点
D.N与W形成的化合物中各原子均满足稳定结构
8.利用下列装置和试剂进行实验,能达到实验目的的是( )
A B C D
分离苯和溴苯 检验乙炔的还原性 灼烧碎海带 实验室制取乙烯
9.冠醚是皇冠状的分子,可有不同的空穴适配不同大小的碱金属离子.二苯并-18-冠-6与形成的超分子结构如下图所示.下列说法正确的是( )
A.该冠醚与之间通过配位键相连形成超分子
B.该超分子物质属于分子晶体
C.该超分子中碳原子可能共处于同一平面
D.该冠醚还可以与适配
10.西安交大研究人员实现了用掺杂Mn、Cu的催化剂光催化转化为甲醇,并利用产生的电能进一步电解制备新型高效净水剂.原理如图所示.下列说法正确的是( )
A.基态Mn原子的价层电子排布式为
B.、均为含有极性键的非极性分子
C.的VSEPR模型为三角锥形
D.该装置实现了光能→电能→化学能的转化
11.酮基布洛芬片是用于治疗各种关节肿痛、牙痛等的非处方药.可由物质A经一系列反应制得,下列说法错误的是( )
A.物质A与苯甲酸互为同系物
B.1 mol酮基布洛芬最多可与发生加成反应
C.物质A中所有碳原子一定共平面
D.可用酸性高锰酸钾溶液来鉴别物质A和酮基布洛芬
12.下列说法错误的是( )
A.键能:,因此比稳定
B.沸点:,因为分子间范德华力更强
C.键角:,因为的成键电子对间的排斥力更大
D.极性:,因此酸性
13.1,3-丁二烯与溴单质按物质的量1:1发生加成反应时,会生成两种物质M和N(不考虑立体异构),其反应机理如图甲所示,下列说法错误的是( )
A.N存在顺反两种异构体
B.M、N互为同分异构体
C.该过程涉及非极性键的断裂和形成
D.根据以上反应机理,一定条件下,将1,3-丁二烯和水蒸汽等物质的量混合,有3种物质生成
14.确定有机化合物组成和结构的方法很多,下列说法错误的是( )
A.质谱仪可用于有机物相对分子质量的测定
B.异丁烷的核磁共振氢谱中有2组峰
C.红外光谱可检测未知物中是否含单键、双键、氢键等化学键
D.X-射线衍射法鉴别某是否属于晶体
15.苯甲酸是常用的食品添加剂,实验室用以下方法可获得纯净的苯甲酸.下列说法正确的是( )
已知:苯甲酸100℃以上易升华,微溶于冷水,易溶于热水、乙醇等.
A.若要得到纯度更高的苯甲酸,应采用多次萃取的方法
B.步骤③涉及的操作为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C.洗涤晶体时应选择乙醇
D.干燥晶体时,温度不宜过高,主要是防止苯甲酸晶体升华造成产品产率降低
二、非选择题:本题共4小题,共55分.
16.(12分)我国在新型锂离子电池电极材料研究方面取得重大突破:膨胀石墨(EG)纳米复合材料、PET复合Cu箔、黑磷-石墨复合材料的使用极大提高了电池的能量和安全性.回答下列问题:
(1)Ni元素在周期表中的位置是__________,与Ni同周期元素中,基态原子的未成对电子数与Ni相同的有___________种.
(2)第二电离能:Fe__________Cu(选填“>”或“<”),原因是__________________.
(3)白磷、红磷、黑磷是P元素形成的三种常见单质.黑磷结构与石墨类似,也具有层状结构(如图1),黑磷-石墨复合材料单层结构俯视图如图2.
下列说法正确的是___________(填字母).
A.黑磷中P-P键键能完全相同
B.P的三种常见单质中,黑磷的熔沸点最高
C.黑磷中存在大键,易导电
D.在结合区,P原子与C原子之间的作用力属范德华力
(4)是目前正在开发的电池正极活性物质,其晶胞结构如图3.
①图3中的配位数为______________;
②已知A的坐标为,B的坐标为__________;
③设阿伏加德罗常数的值为,则晶体的密度为___________(用含,的代数式表示).
17.(14分)氯化苄常用于染料、药物的合成.实验室用甲苯和干燥为原料在光照和加热时合成并提纯氯化苄装置图(加持装置略去)如下:
各物质熔沸点如下表:
物质 甲苯 氯化苄 二氯化苄 三氯化苄
熔点(℃) -95 -39 -16 -7
沸点(℃) 110 179 205 220
回答下列问题:
(1)a的名称是_________,相比于分液漏斗,a的优点_______________.
(2)D中加热前需要加几粒沸石,目的是_____________,装置E的作用是_________________.
(3)A中的离子反应方程式为_______________________________.
(4)实验结束后,为得到纯净的氯化苄,应关闭__________,打开(填,,),加热三颈烧瓶,蒸馏.收集氯化苄时温度计的读数范围是____________.
(5)检测氯化苄样品的纯度:
①称取13.00g样品于烧杯中,加入溶液,水浴加热,冷却后加入足量溶液,充分振荡加水配成100mL溶液.取20.00mL溶液于试管中,加入足量的溶液,充分振荡,过滤、洗涤、干燥,称量固体质量为2.87g,则该样品的纯度为____________%(结果保留小数点后1位).
②实际测量结果往往会偏高,原因是_______________________________.
(6)指出该装置中可能存在的缺点___________________________.
18.(13分)某化学小组为探究和新制反应的产物,进行如下实验:向试管中依次加入溶液、溶液,的甲醛溶液,65℃水浴加热,反应结束后试管中有红色固体生成,量筒中收集到无色气体.回答下列问题:
(1)NaOH溶液过量的目的是__________;使用水浴加热的目的是_____________.
(2)小组同学对实验中红色固体产物的组成作出猜想:
猜想一:只有;
猜想二:只有Cu;
猜想三:_________________.
为了验证固体产物,设计如下实验方案并进行实验(以下每步均充分反应):
已知:i.
ii.
①中,中心离子的配位数为__________,配体的空间构型为_______________;
②将容量瓶ii中的溶解稀释50倍后,溶液的颜色与容量瓶i相近,则猜想________(填“一”“二”或“三”)正确.
(3)小组同学猜测收集的气体可能是、中的一种或两种,将收集的气体利用如图所示的装置进行实验(部分夹持仪器略去).
①依次连接的合理顺序为:(量筒中气体)→B→_______→_______→_______→_______→G.
②最终确认气体产物中含CO而不含,依据是_________________________.
(4)在该小组同学的实验条件下,HCHO与新制反应的方程式为_______________.
19.(16分)氟他胺(G)是可用于治疗肿瘤.实验室由芳香烃A制备G的合成路线如下图:
已知:①;
②吡啶是一种有机碱.
(1)A的一氯取代物有_________种;G中含有的官能团名称为________________.
(2)该合成路线中属于取代反应的有_______________(填序号).
(3)⑤的化学方程式为__________________,吡啶的作用是____________________.
(4)C经反应可得H,有多种同分异构体,写出满足下列条件的同分异体__________.
①属于芳香族化合物;
②能发生银镜反应;
③核磁共振氢谱有4组峰,且峰面积比为1:2:2:1.
(5)由苯甲醚()为原料可制取4-甲氧基乙酰苯胺().请结合上述流程信息,将合成路线补充完整.
江西省2022-2023学年高二下学期5月联合调研考试
化学
参考答案、提示及评分细则
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C D A C C A D A A D D B C C D
16.【参考答案及评分细则】
(1)第四周期第Ⅷ族(1分.周期或族答错均不得分);3(2分)
(2)(1分);、的价电子排布式分别为、,的轨道全充满较稳定,难再失去一个电子,所以第二电离能(2分)
(3)BC(2分.对一个得1分,全对2分,有其他错误选项得0分)
(4)8(1分);(1分);(2分)
17.【参考答案及评分细则】
(1)恒压滴液漏斗(1分.有错别字得0分);平衡漏斗与烧瓶内压强,使浓盐酸顺利滴下(1分)
(2)防暴沸(1分);冷凝回流(1分.或回答“使有机物冷凝回流,提高反应物转化率和生成物产率”得1分)
(3)(2分.未打“”得1分,有其他错误得0分)
(4)、(1分.全对得1分);(1分);(1分)
(5)97.3(2分);样品中混有二氯化苄等杂质(1分)
(6)应在氢氧化钠溶液与E之间加一干燥装置,防止水蒸气进入装置D(2分)
18.【参考答案及评分细则】
(1)提供碱性环境(1分);受热均匀,温度易控制(2分)
(2)和的混合物(1分);4(1分);三角锥形(1分);三(1分)
(3)EFDC(2分.全对2分,有错误不得分);F中黑色固体变红色(或C中的澄清石灰水变浑浊),D中固体不变蓝色(2分.只写一个现象不得分)
(4)(2分.条件末写,“”未打总共扣1分)
19.【参考答案及评分细则】
(1)4(1分);硝基、碳氟键、酰胺基(3分.1个1分,全对得3分)
(2)①②③⑤⑥(2分.全对2分,只对1个不得分,对2~4个得1分,见错无分)
(3)(2分.条件未写得1分);
吸收反应生成的,提高反应转化率(2分)
(4)(或)(2分)
(5)
(全对4分.浓,浓,Δ写对得1分;,写对得1分;写对得1分;写对得1分)
同课章节目录
