第八章常见的酸、碱、盐测试题(含答案) ---2022-2023学年九年级化学科粤版(2012)下册
文档属性
| 名称 | 第八章常见的酸、碱、盐测试题(含答案) ---2022-2023学年九年级化学科粤版(2012)下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 196.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-10 00:00:00 | ||
图片预览



文档简介
第八章《常见的酸、碱、盐》测试题
一、单选题
1.下列化肥中属于复合肥的是( )
A.KCl B.NH4H2PO4
C.CO(NH2)2 D.Ca3(PO4)2
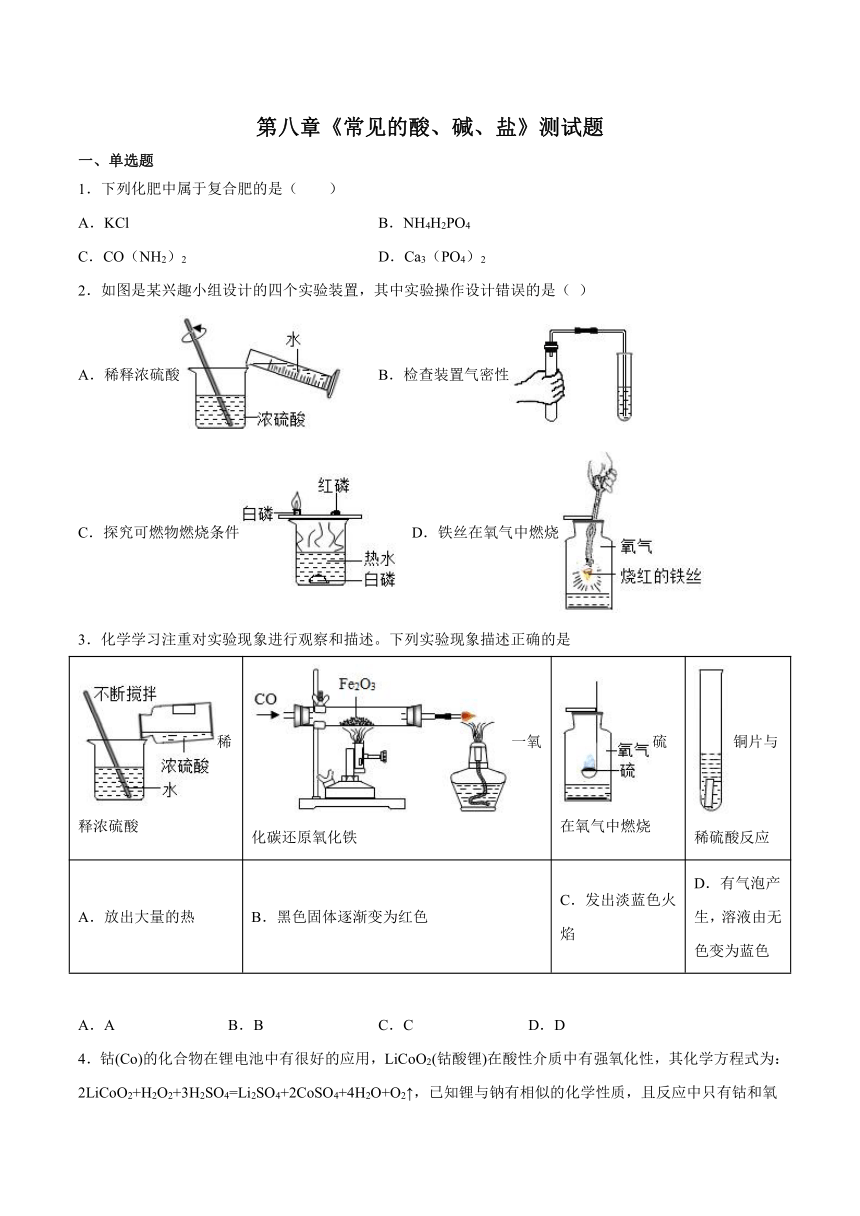
2.如图是某兴趣小组设计的四个实验装置,其中实验操作设计错误的是( )
A.稀释浓硫酸 B.检查装置气密性
C.探究可燃物燃烧条件 D.铁丝在氧气中燃烧
3.化学学习注重对实验现象进行观察和描述。下列实验现象描述正确的是
稀释浓硫酸 一氧化碳还原氧化铁 硫在氧气中燃烧 铜片与稀硫酸反应
A.放出大量的热 B.黑色固体逐渐变为红色 C.发出淡蓝色火焰 D.有气泡产生,溶液由无色变为蓝色
A.A B.B C.C D.D
4.钴(Co)的化合物在锂电池中有很好的应用,LiCoO2(钴酸锂)在酸性介质中有强氧化性,其化学方程式为:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+4H2O+O2↑,已知锂与钠有相似的化学性质,且反应中只有钴和氧元素的化合价发生了改变,则下列说法正确的是( )
A.该反应是复分解反应
B.该反应中钴的化合价由+3价变为+2价
C.该反应中氧的化合价降低
D.钴酸根离子式
5.下列物质长期暴露在空气中溶液质量减少且溶质质量分数也减少的是
①浓盐酸 ②浓硫酸 ③烧碱溶液 ④饱和石灰水
A.①②③ B.②④ C.③④ D.①④
6.下列各组物质在水溶液中能够共存,而且加入酚酞显红色的是( )
A.NaOH 、CuSO4 、H2SO4 B.NaCl、Na2SO4、NaHSO4
C.NaCl、Ba(NO3)2、HCl D.KNO3、NaOH、Na2SO4
7.近年来有人提出了利用处理后的海水(主要成份是氯化钠溶液)吸收含二氧化硫的废气,该方法的流程如下图所示。下列说法正确的是
A.反应中硫元素的化合价发生变化
B.图中反应① 属于分解反应
C.反应③中,反应前后分子数目没有变化
D.反应④中的反应物是两种酸
8.人体内的一些液体的正常pH范围如下表,其中酸性最强的是
液体 胃液 胆汁 胰液 血浆
pH 0.9~1.5 7.1~7.3 7.5~8.0 7.3~7.4
A.胃液 B.胆汁 C.胰液 D.血浆
9.2018年5月,某杂志介绍了我国的项研究成果:在一种新催化剂作用下可实现二氧化碳高效转化为甲醇,相关反应如图所示,关于甲乙反应的有关说法正确的是( )
A.该反应是置换反应
B.该反应甲乙反应物的分子个数比为3:2
C.该反应的化学反应方程式为 CO2+3H2CH3OH+H2O
D.该反应是复分解反应
10.根据下图所示物质的pH,判断下列说法正确的是( )
A.胃酸过多的人可以多喝橘子汁
B.将酚酞溶液滴入牛奶中,溶液变红色
C.蚊虫叮咬后可以涂抹肥皂水止痒
D.厨房清洁剂与厕所清洁剂可混合使用
11.下列实例不属于中和反应的是( )
A.用熟石灰改良酸性土壤 B.用氢氧化铝治疗胃酸过多
C.被蚊中叮咬后涂抹肥皂水减轻痛痒 D.用稀盐酸清除金属表面的铁锈
二、填空题
12.氧化物、酸、碱、盐等化合物在化学实验和工农业生产中起着非常重要的作用。
(1)生活中的食醋中含有的酸,“联合制碱法”制得的碱,化学式分别是___________(填字母)。
a.HCl、NaOH b.CH3COOH、Na2CO3 c.C2H5OH、Na2CO3 d.CH3COOH、NaOH
(2)在农业上常用来改良酸性土壤的物质是___________(用化学式表示)。
(3)甲、乙两种固体物质的溶解度曲线如图所示。
①a1°C时,甲、乙两种物质的溶解度___________ (选填“相等”或“不相等”)。
②要使接近饱和的甲溶液变成饱和溶液,可采用的方法有___________(写一种即可)。
③a2°C时,将65g甲的饱和溶液稀释为10%,需加水___________g。
(4)某同学利用数字化实验设备,测定稀盐酸与氢氧化钠溶液反应时pH变化实验结果如图所示。
①根据图示判断,该实验是将___________(选填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
②当滴入溶液的体积为V2时,所得溶液中溶质的化学式为___________。
13.我们的生活离不开化学。现有①氯化钠、②碳酸氢钠、③碳酸钙、④生石灰、⑤氢氧化钠、⑥硝酸钾等六种物质,选择适当的物质进行填空(填序号)。
(1)可用作补钙剂的是_____;
(2)属于复合肥科的是_____;
(3)可用于食品干燥剂的是_____;
(4)可用于配制生理盐水的是_____;
(5)焙制糕点所用的发酵粉的主要成分之一是_____;
(6)广泛应用于制造肥皂、石油、造纸等工业的是_____。
三、实验题
14.固体样品 M 可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。某同学为探究其成分做了以下实验如图一:(硝酸钠和硝酸钡溶液均呈中性)。
①操作的名称 _____ 。
②取固体 A 于试管中加足量稀硝酸,固体质量随加入稀硝酸质量的变化如图二根据上述实验分析,固体样品 M 中一定有 _____ 。
③为进一步探究该固体样品M成分,进行如下实验:
Ⅰ. 甲同学取少量溶液 B 于试管中,滴加酚酞试液,溶液呈红色,证明固体 M 中 _____ (选填“一定”或“可能”)有氢氧化钠。
Ⅱ. 乙同学取少量溶液 B 于试管中, _____ ,产生白色沉淀,证明固体 M 中有氯化钠。
四、简答题
15.(1)“84消毒液”是现在家庭中常用的消毒剂和漂白剂(能使酸碱指示剂等有机色素褪色的物质),它的有效成分是。“84消毒液”呈碱性,向稀释过的“84消毒液”中滴加无色酚酞,会出现的现象是 ______ 。
(2)“84消毒液”的制取原理为Cl2+2NaOH=NaClO+NaCl+H2O,次氯酸钠中氯元素的化合价为 ______ 。
(3)若配制“84消毒液”需要质量分数为的溶液,实验室配制该 溶液,需要用到图中的玻璃仪器为 ______ (填字母编号)。在配制过程中,若烧杯内壁附着水珠,会导致所配溶液溶质质量分数 ______ (填“偏大”“偏小”或“不变”)。
16.请根据图示回答相关问题。
(1)写出有标号仪器的名称:a_______;b__________。
(2)上述四个实验中,操作正确的是_________。
(3)选择上图错误操作中的一个,写出可能导致的后果____,其正确操作是_____。
五、计算题
17.某纯碱样品中含有少量氯化钠杂质,一同学想知道该样品中纯碱的质量分数,先后进行了四次实验,实验数据如下表:
第一次 第二次 第三次 第四次
所取纯碱样品/g 12 12 12 12
所加盐酸的质量/g 30 60 90 120
生成气体的质量/g 2 4 4.4 m
请回答问题:
(1)上表中m的值是 g
(2)该纯碱样品中碳酸钠的质量分数是多少
(3)第四次反应得到的混合物中钠元素的质量是 g
18.Na2SO4 常用于配制印染织物的促染剂,其溶质的质量分数一般在 3%-5%范围。
(1)Na2SO4 中硫、氧元素的质量比为 ______ 。
(2)某工厂需用 1000Kg 上述有效促染剂,则需要 Na2SO4 的质量至少为多少Kg。
(3)现欲测定某长期放置的促染剂中 Na2SO4 的质量分数,取 100g 促染剂滴入足量的氯化钡溶液 100g,恰好完全反应后过滤、洗涤、干燥得滤渣质量为 6.99g。
①求该促染剂中 Na2SO4 的质量分数。
②若滤渣没有洗涤、干燥,则测定的 Na2SO4 的质量分数会______填“偏大”、“偏小”或“无影响”)
参考答案:
1.B 2.A 3.A 4.B 5.D 6.D 7.C 8.A 9.C 10.C 11.D
12.(1)b
(2)Ca(OH)2
(3) 相等 增加甲物质(或蒸发水或降低温度) 85g
(4) 稀盐酸 NaCl、HCl
13. ③ ⑥ ④ ① ② ⑤
14. 过滤 Na2CO3 可能 滴加AgNO3溶液
15. 溶液先变红,后褪色 BDF 偏小
16. 胶头滴管(或滴管) 酒精灯 C 引发火灾,(或沾污滴管。或酸液飞溅。) 用灯帽盖灭(或滴管竖直在试管口上方。或把浓硫酸沿器壁慢慢倒入水中)
17.(1)4.4
(2)设碳酸钠的质量为x
x=10.6g
所以,样品中碳酸钠的质量分数为×100%=88%
答:样品中碳酸钠的质量分数为88%。
(3)5.15
18.(1) 1:2;(2)30;(3)4.26% ;偏大
一、单选题
1.下列化肥中属于复合肥的是( )
A.KCl B.NH4H2PO4
C.CO(NH2)2 D.Ca3(PO4)2
2.如图是某兴趣小组设计的四个实验装置,其中实验操作设计错误的是( )
A.稀释浓硫酸 B.检查装置气密性
C.探究可燃物燃烧条件 D.铁丝在氧气中燃烧
3.化学学习注重对实验现象进行观察和描述。下列实验现象描述正确的是
稀释浓硫酸 一氧化碳还原氧化铁 硫在氧气中燃烧 铜片与稀硫酸反应
A.放出大量的热 B.黑色固体逐渐变为红色 C.发出淡蓝色火焰 D.有气泡产生,溶液由无色变为蓝色
A.A B.B C.C D.D
4.钴(Co)的化合物在锂电池中有很好的应用,LiCoO2(钴酸锂)在酸性介质中有强氧化性,其化学方程式为:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+4H2O+O2↑,已知锂与钠有相似的化学性质,且反应中只有钴和氧元素的化合价发生了改变,则下列说法正确的是( )
A.该反应是复分解反应
B.该反应中钴的化合价由+3价变为+2价
C.该反应中氧的化合价降低
D.钴酸根离子式
5.下列物质长期暴露在空气中溶液质量减少且溶质质量分数也减少的是
①浓盐酸 ②浓硫酸 ③烧碱溶液 ④饱和石灰水
A.①②③ B.②④ C.③④ D.①④
6.下列各组物质在水溶液中能够共存,而且加入酚酞显红色的是( )
A.NaOH 、CuSO4 、H2SO4 B.NaCl、Na2SO4、NaHSO4
C.NaCl、Ba(NO3)2、HCl D.KNO3、NaOH、Na2SO4
7.近年来有人提出了利用处理后的海水(主要成份是氯化钠溶液)吸收含二氧化硫的废气,该方法的流程如下图所示。下列说法正确的是
A.反应中硫元素的化合价发生变化
B.图中反应① 属于分解反应
C.反应③中,反应前后分子数目没有变化
D.反应④中的反应物是两种酸
8.人体内的一些液体的正常pH范围如下表,其中酸性最强的是
液体 胃液 胆汁 胰液 血浆
pH 0.9~1.5 7.1~7.3 7.5~8.0 7.3~7.4
A.胃液 B.胆汁 C.胰液 D.血浆
9.2018年5月,某杂志介绍了我国的项研究成果:在一种新催化剂作用下可实现二氧化碳高效转化为甲醇,相关反应如图所示,关于甲乙反应的有关说法正确的是( )
A.该反应是置换反应
B.该反应甲乙反应物的分子个数比为3:2
C.该反应的化学反应方程式为 CO2+3H2CH3OH+H2O
D.该反应是复分解反应
10.根据下图所示物质的pH,判断下列说法正确的是( )
A.胃酸过多的人可以多喝橘子汁
B.将酚酞溶液滴入牛奶中,溶液变红色
C.蚊虫叮咬后可以涂抹肥皂水止痒
D.厨房清洁剂与厕所清洁剂可混合使用
11.下列实例不属于中和反应的是( )
A.用熟石灰改良酸性土壤 B.用氢氧化铝治疗胃酸过多
C.被蚊中叮咬后涂抹肥皂水减轻痛痒 D.用稀盐酸清除金属表面的铁锈
二、填空题
12.氧化物、酸、碱、盐等化合物在化学实验和工农业生产中起着非常重要的作用。
(1)生活中的食醋中含有的酸,“联合制碱法”制得的碱,化学式分别是___________(填字母)。
a.HCl、NaOH b.CH3COOH、Na2CO3 c.C2H5OH、Na2CO3 d.CH3COOH、NaOH
(2)在农业上常用来改良酸性土壤的物质是___________(用化学式表示)。
(3)甲、乙两种固体物质的溶解度曲线如图所示。
①a1°C时,甲、乙两种物质的溶解度___________ (选填“相等”或“不相等”)。
②要使接近饱和的甲溶液变成饱和溶液,可采用的方法有___________(写一种即可)。
③a2°C时,将65g甲的饱和溶液稀释为10%,需加水___________g。
(4)某同学利用数字化实验设备,测定稀盐酸与氢氧化钠溶液反应时pH变化实验结果如图所示。
①根据图示判断,该实验是将___________(选填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
②当滴入溶液的体积为V2时,所得溶液中溶质的化学式为___________。
13.我们的生活离不开化学。现有①氯化钠、②碳酸氢钠、③碳酸钙、④生石灰、⑤氢氧化钠、⑥硝酸钾等六种物质,选择适当的物质进行填空(填序号)。
(1)可用作补钙剂的是_____;
(2)属于复合肥科的是_____;
(3)可用于食品干燥剂的是_____;
(4)可用于配制生理盐水的是_____;
(5)焙制糕点所用的发酵粉的主要成分之一是_____;
(6)广泛应用于制造肥皂、石油、造纸等工业的是_____。
三、实验题
14.固体样品 M 可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。某同学为探究其成分做了以下实验如图一:(硝酸钠和硝酸钡溶液均呈中性)。
①操作的名称 _____ 。
②取固体 A 于试管中加足量稀硝酸,固体质量随加入稀硝酸质量的变化如图二根据上述实验分析,固体样品 M 中一定有 _____ 。
③为进一步探究该固体样品M成分,进行如下实验:
Ⅰ. 甲同学取少量溶液 B 于试管中,滴加酚酞试液,溶液呈红色,证明固体 M 中 _____ (选填“一定”或“可能”)有氢氧化钠。
Ⅱ. 乙同学取少量溶液 B 于试管中, _____ ,产生白色沉淀,证明固体 M 中有氯化钠。
四、简答题
15.(1)“84消毒液”是现在家庭中常用的消毒剂和漂白剂(能使酸碱指示剂等有机色素褪色的物质),它的有效成分是。“84消毒液”呈碱性,向稀释过的“84消毒液”中滴加无色酚酞,会出现的现象是 ______ 。
(2)“84消毒液”的制取原理为Cl2+2NaOH=NaClO+NaCl+H2O,次氯酸钠中氯元素的化合价为 ______ 。
(3)若配制“84消毒液”需要质量分数为的溶液,实验室配制该 溶液,需要用到图中的玻璃仪器为 ______ (填字母编号)。在配制过程中,若烧杯内壁附着水珠,会导致所配溶液溶质质量分数 ______ (填“偏大”“偏小”或“不变”)。
16.请根据图示回答相关问题。
(1)写出有标号仪器的名称:a_______;b__________。
(2)上述四个实验中,操作正确的是_________。
(3)选择上图错误操作中的一个,写出可能导致的后果____,其正确操作是_____。
五、计算题
17.某纯碱样品中含有少量氯化钠杂质,一同学想知道该样品中纯碱的质量分数,先后进行了四次实验,实验数据如下表:
第一次 第二次 第三次 第四次
所取纯碱样品/g 12 12 12 12
所加盐酸的质量/g 30 60 90 120
生成气体的质量/g 2 4 4.4 m
请回答问题:
(1)上表中m的值是 g
(2)该纯碱样品中碳酸钠的质量分数是多少
(3)第四次反应得到的混合物中钠元素的质量是 g
18.Na2SO4 常用于配制印染织物的促染剂,其溶质的质量分数一般在 3%-5%范围。
(1)Na2SO4 中硫、氧元素的质量比为 ______ 。
(2)某工厂需用 1000Kg 上述有效促染剂,则需要 Na2SO4 的质量至少为多少Kg。
(3)现欲测定某长期放置的促染剂中 Na2SO4 的质量分数,取 100g 促染剂滴入足量的氯化钡溶液 100g,恰好完全反应后过滤、洗涤、干燥得滤渣质量为 6.99g。
①求该促染剂中 Na2SO4 的质量分数。
②若滤渣没有洗涤、干燥,则测定的 Na2SO4 的质量分数会______填“偏大”、“偏小”或“无影响”)
参考答案:
1.B 2.A 3.A 4.B 5.D 6.D 7.C 8.A 9.C 10.C 11.D
12.(1)b
(2)Ca(OH)2
(3) 相等 增加甲物质(或蒸发水或降低温度) 85g
(4) 稀盐酸 NaCl、HCl
13. ③ ⑥ ④ ① ② ⑤
14. 过滤 Na2CO3 可能 滴加AgNO3溶液
15. 溶液先变红,后褪色 BDF 偏小
16. 胶头滴管(或滴管) 酒精灯 C 引发火灾,(或沾污滴管。或酸液飞溅。) 用灯帽盖灭(或滴管竖直在试管口上方。或把浓硫酸沿器壁慢慢倒入水中)
17.(1)4.4
(2)设碳酸钠的质量为x
x=10.6g
所以,样品中碳酸钠的质量分数为×100%=88%
答:样品中碳酸钠的质量分数为88%。
(3)5.15
18.(1) 1:2;(2)30;(3)4.26% ;偏大
同课章节目录
