山东省济南市莱芜区陈毅中学片区联盟2022-2023学年八年级下学期期中考试化学试题(含答案)
文档属性
| 名称 | 山东省济南市莱芜区陈毅中学片区联盟2022-2023学年八年级下学期期中考试化学试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 221.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-12 00:00:00 | ||
图片预览


文档简介
济南市莱芜区陈毅中学片区联盟2022-2023学年度第下学期期中考试
八年级化学试题
相对原子质量:H:1 C:12 O:16 Mg:24
选择题(本题共包括10个小题,每小题3分,共30分)
1.下列事实能用质量守恒定律解释的是( )
A.10mL酒精与10mL水混合,溶液体积小于20mL
B.10g蔗糖溶解在90g水中,形成100g蔗糖溶液
C.镁条在空气中燃烧后,固体质量变大
D.酒精灯长时间不盖灯帽后,酒精的量变少
2.火箭燃料用偏二甲肼(C2H8N2)与四氧化二氮(N2O4)作常规推进剂,两者发生反应的化学方程式为C2H8N2+2N2O43N2↑+2X↑+4H2O,则X的化学式为( )
A.O2 B.CO C.CO2 D.H2
3.下列化学方程式书写正确的是( )
A.Cu+HSO4═CuSO4+H2↑ B.4Fe+3O22Fe2O3
C.S+O2SO2 D.2Al+O2═2AlO
4.下列采取的安全措施不正确的是( )
A.室内起火,迅速打开所有门窗通风
B.电器着火,迅速切断电源
C.遇水易发生爆炸的物质,不能露天存放
D.酒精灯不慎打翻起火,用湿抹布盖灭
5.下列实验(天平未画出)能够直接用于验证质量守恒定律的是( )
A. B.
C. D.
6.铜制品长期暴露在空气中表面生成铜锈[主要成分Cu2(OH)2CO3]。下列物质与铜制品生锈无关的是( )
A.O2 B.N2 C.H2O D.CO2
7.在3A+B=2C+D的反应中,已知30克A和10克B恰好完全反应,生成5克D,且已知C的相对分子质量为70,则D的相对分子质量是( )
A.20 B.30 C.40 D.55
8.在工业上,通过增大氧气的浓度或增大可燃物与氧气的接触面积都能提高燃料利用率,下列提高燃料利用率的方法中,与其他方法原理不同的是( )
A.工厂炼钢时常充入氧气
B.给锅炉鼓风,增加空气供给量
C.把柴油喷成雾状进行燃烧
D.铁丝在空气中不能燃烧,而在纯氧气中剧烈燃烧
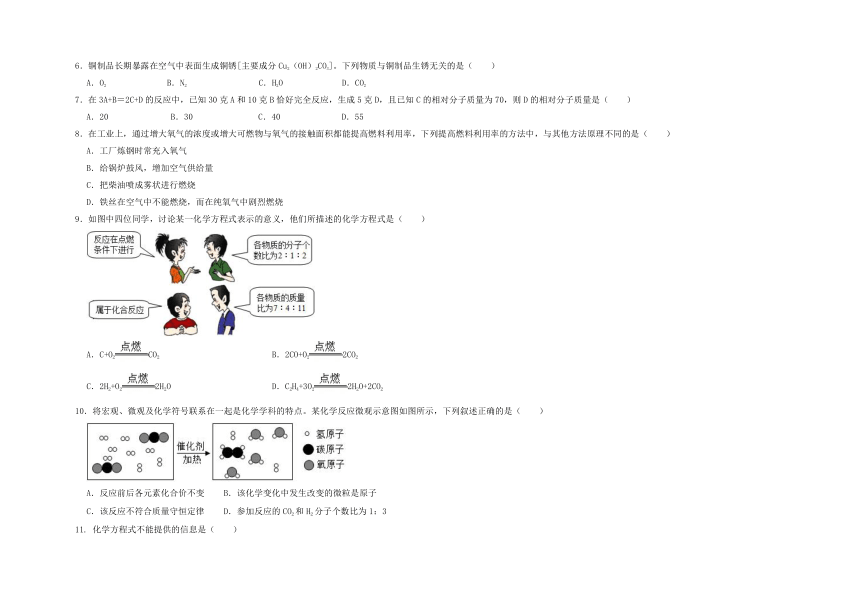
9.如图中四位同学,讨论某一化学方程式表示的意义,他们所描述的化学方程式是( )
A.C+O2CO2 B.2CO+O22CO2
C.2H2+O22H2O D.C2H4+3O22H2O+2CO2
10.将宏观、微观及化学符号联系在一起是化学学科的特点。某化学反应微观示意图如图所示,下列叙述正确的是( )
A.反应前后各元素化合价不变 B.该化学变化中发生改变的微粒是原子
C.该反应不符合质量守恒定律 D.参加反应的CO2和H2分子个数比为1:3
11. 化学方程式不能提供的信息是( )
A.通过什么条件反应 B.哪些物质参加反应
C.化学反应速率的快慢 D.各粒子的相对数量
12.构建化学基本观念是学好化学的基础,下列认识错误的是( )
A.微粒观:保持氧气化学性质的最小微粒是氧分子
B.守恒观:12g镁和12g氧气反应,生成24g氧化镁
C.变化观:酒精在充足的氧气中燃烧生成水和二氧化碳
D.元素观:二氧化碳和一氧化碳的组成元素相同
多选题(本题包括5个小题,每小题4分,共20分,错选不得分,少选得3分)
13.在化学反应前后,一定发生改变的是( )
A.物质种类 B.元素种类 C.分子种类 D.原子种类
14.在化学方程式aC2H6+bO2═m CO2+nH2O中,各化学式系数之间的关系正确的是( )
A.2m=a B.3a=n C.3m=2n D.2b=2m+n
15.根据化学方程式4NH3+5O26H2O+4NO获得的相关信息正确的是( )
A.氨气和氧气在高温条件和催化剂的作用下,反应生成水和一氧化氮
B.每4份质量的氨气和5份质量的氧气完全反应生成6份质量的水和4份质量的一氧化氮
C.每4个氨分子与5个氧分子完全反应成生6个水分子和4个一氧化氮分子
D.氨气与氧气的质量比等于水和一氧化氮的质量比
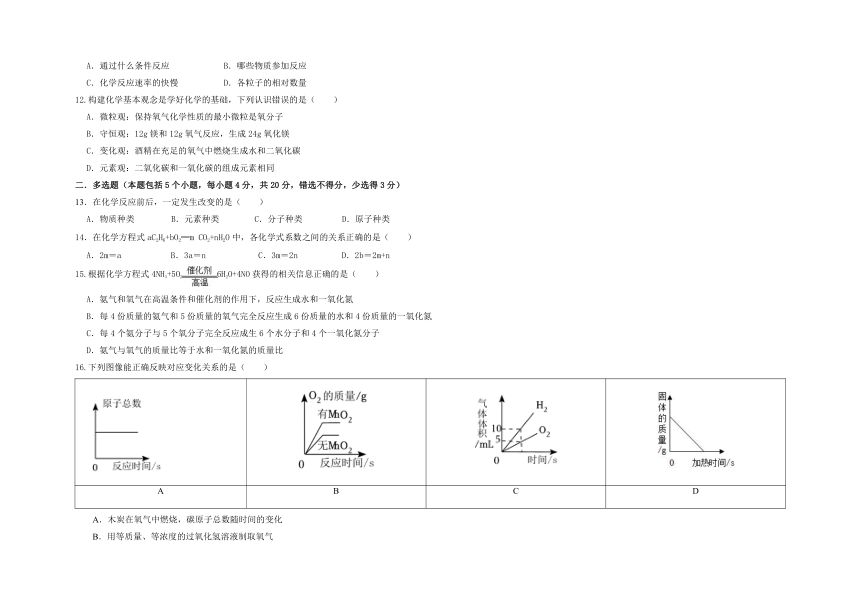
16.下列图像能正确反映对应变化关系的是( )
A B C D
A.木炭在氧气中燃烧,碳原子总数随时间的变化
B.用等质量、等浓度的过氧化氢溶液制取氧气
C.水通电电解一段时间生成气体体积变化
D.加热密闭装置中一定质量的铜粉
17.一定条件下,在一密闭的容器中发生某反应,测得反应过程中各物质的质量如下表所示,下列判断正确的是( )
物质 X Y Z Q
第一次测得的质量(克) 32 51 待测 6
第一次测得的质量(克) 60 17 11 12
A.该反应中X和Q的质量变化比为5:1
B.该反应的化学表达式可表示为Y→X+Z+Q
C.Z可能是该反应的催化剂
D.该反应是分解反应
18.已知3.2g化合物M与氧气恰好完全反应,生成4.4g二氧化碳和3.6g水。下列判断正确的是( )
A.化合物M中只含碳、氢元素 B.化合物M中碳元素质量分数为37.5%
C.参加反应的氧气质量为6.4g D.M分子中碳原子与氢原子个数比为1:4
三.填空题(30分)
19.随着对“火”的认识和使用。人类能够更好地改造自然,改善生活,火让人类从蛮荒走向文明。
(1)人类目前使用的化石燃料有煤、 和天然气,它们都属于 (选填“可再生”或“不可再生”)能源。其中,天然气(主要成分为CH4)是一种很重要化石燃料。天然气燃烧反应的微观示意图如图。
写出该反应的化学方程式
(2)磷在氧气中燃烧的化学方程式是:2Mg+O22MgO
这个式子不仅表明了反应物、生成物、反应条件,还表示了参加反应的各物质之间的质量关系,即在点燃的条件下,每 份质量镁的与 份质量的氧气恰好完全反应生成 份质量的氧化镁.
(3)冬天取暖大量使用含硫煤,排放的 (填化学式)气体,会形成酸雨,其中硫元素的化合价为 。使用低硫煤可以避免酸雨,但无法避免过多二氧化碳造成的 (环境污染)
20.按要求写出下列反应的化学方程式。
(1)铁丝在氧气中燃烧: 。
(2) 实验室常温下制取氧气的原理: 。
(3)镁是一种很活泼的金属,点燃后它能在二氧化碳气体中燃烧,生成碳和一种金属氧化物,则反应的化学方程式为 。
21.用“”和“”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,请回答下列问题:
(1)参加反应的“”和“”分子的个数比是
(2)如果“〇”表示氢原子、“●”表示氮原子,请写出生成物的化学式
(3)根据上述示意图可知,该反应属于 反应.
(4)从微观角度分析,化学反应前后各物质的质量总和相等的原因是 。
四.实验题(10分)
22.小明和同学分别设计了两组实验验证质量守恒定律和可燃物燃烧的条件,请你根据实验内容,完成下列题目。
(1)A实验中,白磷燃烧的化学方程式为 。
(2)实验结束后,天平保持平衡的是 (填A或B)实验,另一个实验中天平不平衡的原因是 。
(3)要用B装置继续探究质量守恒定律,若药品不变,改变装置的方法 。
若装置不变,可以改变药品为 (任举一例即可)。
(4)某同学为探究可燃物燃烧的条件,按图A、图B所示装置进行对比实验:
资料:白磷的着火点为40℃,红磷的着火点为240℃。
①用图A所示装置进行实验,观察到的现象如下:
铜片上的白磷燃烧,而铜片上的红磷不燃烧,说明可燃物燃烧需要的条件是 。
而铜片上的白磷燃烧,水中的白磷不燃烧,说明可燃物燃烧需要的条件是 。
②再用图B所示装置进行实验,通氧气时,热水中的白磷 。
③图A中热水的作用是 。
五.计算题(10分)
23.实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的 和 都没有发生变化;
(2)反应生成氧气的质量为 g;
(3)参加反应的H2O2的质量是多少?
八年级化学答案
一、选择题(单选题每小题3分,多选题每小题4分,共60分)
1 2 3 4 5 6 7 8 9 10
C C C A C B A C B D
11 12 13 14 15 16 17 18
C B AC BCD AC AC CD BD
二、填空题(共20分)
19、(1)石油,不可再生,CH4+2O2CO2+2H2O
(2)48,32,80
(3)SO2,+4,温室效应
评分标准:每空1分,化学方程式2分
20、(1)3Fe+2O2Fe3O4
(2)2H2O22H2O+O2↑
(3)2Mg+CO22MgO+C
(1)3:1 (2)NH3 (3)化合(4)略)
实验题(共10分)
(1)4P+5O22P2O5
A,反应生成的CO2逸出
改成密闭容器,NaOH,CuSO4(符合题意即可)
①温度达到可燃物着火点,与充足空气(氧气接触)
②燃烧 ③隔绝氧气,提供热量
四、计算题(共10分)
解:(1)质量,化学性质
(2)根据质量守恒定律可得,生成的氧气的质量为70g﹣68.4g=1.6g
(3)设参加反应过氧化氢的质量为x。
2H2O22H2O+O2↑
68 32
x 1.6g
x=3.4g
答:反应消耗的过氧化氢的质量是3.4g。
八年级化学试题
相对原子质量:H:1 C:12 O:16 Mg:24
选择题(本题共包括10个小题,每小题3分,共30分)
1.下列事实能用质量守恒定律解释的是( )
A.10mL酒精与10mL水混合,溶液体积小于20mL
B.10g蔗糖溶解在90g水中,形成100g蔗糖溶液
C.镁条在空气中燃烧后,固体质量变大
D.酒精灯长时间不盖灯帽后,酒精的量变少
2.火箭燃料用偏二甲肼(C2H8N2)与四氧化二氮(N2O4)作常规推进剂,两者发生反应的化学方程式为C2H8N2+2N2O43N2↑+2X↑+4H2O,则X的化学式为( )
A.O2 B.CO C.CO2 D.H2
3.下列化学方程式书写正确的是( )
A.Cu+HSO4═CuSO4+H2↑ B.4Fe+3O22Fe2O3
C.S+O2SO2 D.2Al+O2═2AlO
4.下列采取的安全措施不正确的是( )
A.室内起火,迅速打开所有门窗通风
B.电器着火,迅速切断电源
C.遇水易发生爆炸的物质,不能露天存放
D.酒精灯不慎打翻起火,用湿抹布盖灭
5.下列实验(天平未画出)能够直接用于验证质量守恒定律的是( )
A. B.
C. D.
6.铜制品长期暴露在空气中表面生成铜锈[主要成分Cu2(OH)2CO3]。下列物质与铜制品生锈无关的是( )
A.O2 B.N2 C.H2O D.CO2
7.在3A+B=2C+D的反应中,已知30克A和10克B恰好完全反应,生成5克D,且已知C的相对分子质量为70,则D的相对分子质量是( )
A.20 B.30 C.40 D.55
8.在工业上,通过增大氧气的浓度或增大可燃物与氧气的接触面积都能提高燃料利用率,下列提高燃料利用率的方法中,与其他方法原理不同的是( )
A.工厂炼钢时常充入氧气
B.给锅炉鼓风,增加空气供给量
C.把柴油喷成雾状进行燃烧
D.铁丝在空气中不能燃烧,而在纯氧气中剧烈燃烧
9.如图中四位同学,讨论某一化学方程式表示的意义,他们所描述的化学方程式是( )
A.C+O2CO2 B.2CO+O22CO2
C.2H2+O22H2O D.C2H4+3O22H2O+2CO2
10.将宏观、微观及化学符号联系在一起是化学学科的特点。某化学反应微观示意图如图所示,下列叙述正确的是( )
A.反应前后各元素化合价不变 B.该化学变化中发生改变的微粒是原子
C.该反应不符合质量守恒定律 D.参加反应的CO2和H2分子个数比为1:3
11. 化学方程式不能提供的信息是( )
A.通过什么条件反应 B.哪些物质参加反应
C.化学反应速率的快慢 D.各粒子的相对数量
12.构建化学基本观念是学好化学的基础,下列认识错误的是( )
A.微粒观:保持氧气化学性质的最小微粒是氧分子
B.守恒观:12g镁和12g氧气反应,生成24g氧化镁
C.变化观:酒精在充足的氧气中燃烧生成水和二氧化碳
D.元素观:二氧化碳和一氧化碳的组成元素相同
多选题(本题包括5个小题,每小题4分,共20分,错选不得分,少选得3分)
13.在化学反应前后,一定发生改变的是( )
A.物质种类 B.元素种类 C.分子种类 D.原子种类
14.在化学方程式aC2H6+bO2═m CO2+nH2O中,各化学式系数之间的关系正确的是( )
A.2m=a B.3a=n C.3m=2n D.2b=2m+n
15.根据化学方程式4NH3+5O26H2O+4NO获得的相关信息正确的是( )
A.氨气和氧气在高温条件和催化剂的作用下,反应生成水和一氧化氮
B.每4份质量的氨气和5份质量的氧气完全反应生成6份质量的水和4份质量的一氧化氮
C.每4个氨分子与5个氧分子完全反应成生6个水分子和4个一氧化氮分子
D.氨气与氧气的质量比等于水和一氧化氮的质量比
16.下列图像能正确反映对应变化关系的是( )
A B C D
A.木炭在氧气中燃烧,碳原子总数随时间的变化
B.用等质量、等浓度的过氧化氢溶液制取氧气
C.水通电电解一段时间生成气体体积变化
D.加热密闭装置中一定质量的铜粉
17.一定条件下,在一密闭的容器中发生某反应,测得反应过程中各物质的质量如下表所示,下列判断正确的是( )
物质 X Y Z Q
第一次测得的质量(克) 32 51 待测 6
第一次测得的质量(克) 60 17 11 12
A.该反应中X和Q的质量变化比为5:1
B.该反应的化学表达式可表示为Y→X+Z+Q
C.Z可能是该反应的催化剂
D.该反应是分解反应
18.已知3.2g化合物M与氧气恰好完全反应,生成4.4g二氧化碳和3.6g水。下列判断正确的是( )
A.化合物M中只含碳、氢元素 B.化合物M中碳元素质量分数为37.5%
C.参加反应的氧气质量为6.4g D.M分子中碳原子与氢原子个数比为1:4
三.填空题(30分)
19.随着对“火”的认识和使用。人类能够更好地改造自然,改善生活,火让人类从蛮荒走向文明。
(1)人类目前使用的化石燃料有煤、 和天然气,它们都属于 (选填“可再生”或“不可再生”)能源。其中,天然气(主要成分为CH4)是一种很重要化石燃料。天然气燃烧反应的微观示意图如图。
写出该反应的化学方程式
(2)磷在氧气中燃烧的化学方程式是:2Mg+O22MgO
这个式子不仅表明了反应物、生成物、反应条件,还表示了参加反应的各物质之间的质量关系,即在点燃的条件下,每 份质量镁的与 份质量的氧气恰好完全反应生成 份质量的氧化镁.
(3)冬天取暖大量使用含硫煤,排放的 (填化学式)气体,会形成酸雨,其中硫元素的化合价为 。使用低硫煤可以避免酸雨,但无法避免过多二氧化碳造成的 (环境污染)
20.按要求写出下列反应的化学方程式。
(1)铁丝在氧气中燃烧: 。
(2) 实验室常温下制取氧气的原理: 。
(3)镁是一种很活泼的金属,点燃后它能在二氧化碳气体中燃烧,生成碳和一种金属氧化物,则反应的化学方程式为 。
21.用“”和“”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,请回答下列问题:
(1)参加反应的“”和“”分子的个数比是
(2)如果“〇”表示氢原子、“●”表示氮原子,请写出生成物的化学式
(3)根据上述示意图可知,该反应属于 反应.
(4)从微观角度分析,化学反应前后各物质的质量总和相等的原因是 。
四.实验题(10分)
22.小明和同学分别设计了两组实验验证质量守恒定律和可燃物燃烧的条件,请你根据实验内容,完成下列题目。
(1)A实验中,白磷燃烧的化学方程式为 。
(2)实验结束后,天平保持平衡的是 (填A或B)实验,另一个实验中天平不平衡的原因是 。
(3)要用B装置继续探究质量守恒定律,若药品不变,改变装置的方法 。
若装置不变,可以改变药品为 (任举一例即可)。
(4)某同学为探究可燃物燃烧的条件,按图A、图B所示装置进行对比实验:
资料:白磷的着火点为40℃,红磷的着火点为240℃。
①用图A所示装置进行实验,观察到的现象如下:
铜片上的白磷燃烧,而铜片上的红磷不燃烧,说明可燃物燃烧需要的条件是 。
而铜片上的白磷燃烧,水中的白磷不燃烧,说明可燃物燃烧需要的条件是 。
②再用图B所示装置进行实验,通氧气时,热水中的白磷 。
③图A中热水的作用是 。
五.计算题(10分)
23.实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的 和 都没有发生变化;
(2)反应生成氧气的质量为 g;
(3)参加反应的H2O2的质量是多少?
八年级化学答案
一、选择题(单选题每小题3分,多选题每小题4分,共60分)
1 2 3 4 5 6 7 8 9 10
C C C A C B A C B D
11 12 13 14 15 16 17 18
C B AC BCD AC AC CD BD
二、填空题(共20分)
19、(1)石油,不可再生,CH4+2O2CO2+2H2O
(2)48,32,80
(3)SO2,+4,温室效应
评分标准:每空1分,化学方程式2分
20、(1)3Fe+2O2Fe3O4
(2)2H2O22H2O+O2↑
(3)2Mg+CO22MgO+C
(1)3:1 (2)NH3 (3)化合(4)略)
实验题(共10分)
(1)4P+5O22P2O5
A,反应生成的CO2逸出
改成密闭容器,NaOH,CuSO4(符合题意即可)
①温度达到可燃物着火点,与充足空气(氧气接触)
②燃烧 ③隔绝氧气,提供热量
四、计算题(共10分)
解:(1)质量,化学性质
(2)根据质量守恒定律可得,生成的氧气的质量为70g﹣68.4g=1.6g
(3)设参加反应过氧化氢的质量为x。
2H2O22H2O+O2↑
68 32
x 1.6g
x=3.4g
答:反应消耗的过氧化氢的质量是3.4g。
同课章节目录
