黑龙江省绥化市绥棱县克音河学校(五四学制)2022-2023学年八年级下学期期中化学试题(含答案)
文档属性
| 名称 | 黑龙江省绥化市绥棱县克音河学校(五四学制)2022-2023学年八年级下学期期中化学试题(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 384.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-12 00:00:00 | ||
图片预览


文档简介
绥棱县克音河乡学校初三化学期中检测试题
可能用到的相对原子质量:O-16 C-12 H-1 K-39 Mn-55 Cl-35.5 N-14 Mg-24
一、选择题(1-12题每题一个选项符合题意,13-15 每题1-2个选项符合题意,每小题2分,共30分)
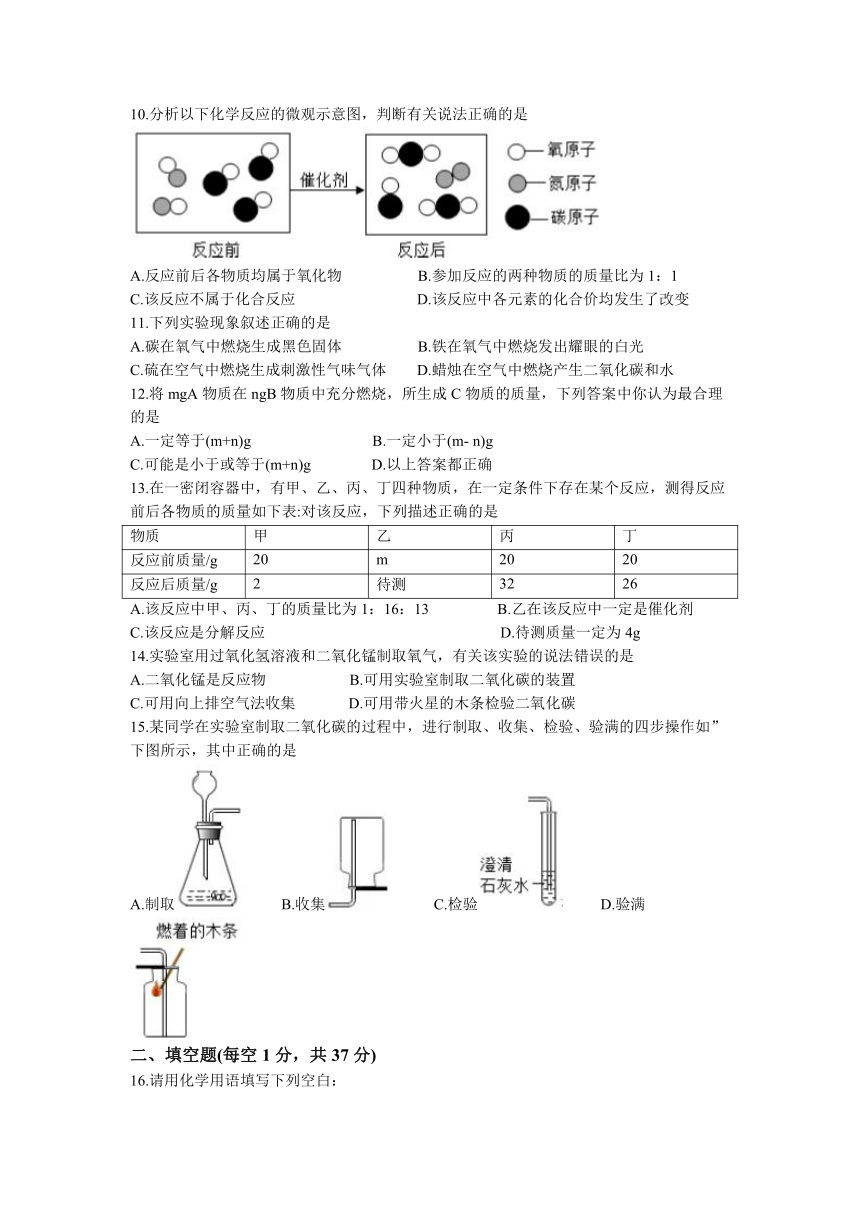
1.下列成语主要涉及化学变化的是
A.刻舟求剑 B.星火燎原 C.滴水成冰 D. 沙里淘金
2.高铁是“中国制造"- -张耀眼的名片,它带领中国走向世界。高铁列车与电路连接的石墨电刷没有用到石墨性质的是
A.稳定性 B.还原性 C.滑腻感 D.导电性
3.下列物质中,前者属于混合物,后者属于纯净物的是
A.五氧化二磷 汞 B.水 空气 C.硫 二氧化碳 D.糖水 氮气
4.我国古代某些字画用墨(用炭黑等制成)绘制或书写而成,能够保存至今而不变色的原因是
A.碳在常温下化学性质不活泼 B.炭黑具有很强的吸附能力
C.碳具有还原性 D.碳单质不溶于水
5.性质决定用途。下列碳单质的性质与其用途不相符的是
A.石墨导电性好——用于制铅笔芯
B. C60分子很稳定,有超导性——广泛用于超导领域
C.活性炭吸附性强——用作冰箱除味剂
D.炭黑在常温下化学性质不活泼——用于制墨汁
6.下图所示的实验操作正确的是
A.加热液体 B.倾倒药品
C.称量药品 D.检验氧气收集满
7.金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用X表示):12HF+3Na2CO3+ 2Al(OH)3=2X+ 3CO2+9H2O,则X的化学式为
A. AlF3 B. NaF C. NaAlF4 D. Na3AlF6
8.小华对妈妈说:“你说菠菜中富含铁,为什么我用磁铁无法把菠菜吸起来呢 ”小华认为的“铁”是指
A.金属铁 B.铁分子 C.铁元素 D.铁原子
9.“酒香不怕巷子深”,从分子的角度解释原因是
A.分子体积小 B.分子质量小 C.分子之间有间隔 D.分子在不断地运动
10.分析以下化学反应的微观示意图,判断有关说法正确的是
A.反应前后各物质均属于氧化物 B.参加反应的两种物质的质量比为1:1
C.该反应不属于化合反应 D.该反应中各元素的化合价均发生了改变
11.下列实验现象叙述正确的是
A.碳在氧气中燃烧生成黑色固体 B.铁在氧气中燃烧发出耀眼的白光
C.硫在空气中燃烧生成刺激性气味气体 D.蜡烛在空气中燃烧产生二氧化碳和水
12.将mgA物质在ngB物质中充分燃烧,所生成C物质的质量,下列答案中你认为最合理的是
A.一定等于(m+n)g B.一定小于(m- n)g
C.可能是小于或等于(m+n)g D.以上答案都正确
13.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:对该反应,下列描述正确的是
物质 甲 乙 丙 丁
反应前质量/g 20 m 20 20
反应后质量/g 2 待测 32 26
A.该反应中甲、丙、丁的质量比为1:16:13 B.乙在该反应中一定是催化剂
C.该反应是分解反应 D.待测质量一定为4g
14.实验室用过氧化氢溶液和二氧化锰制取氧气,有关该实验的说法错误的是
A.二氧化锰是反应物 B.可用实验室制取二氧化碳的装置
C.可用向上排空气法收集 D.可用带火星的木条检验二氧化碳
15.某同学在实验室制取二氧化碳的过程中,进行制取、收集、检验、验满的四步操作如”下图所示,其中正确的是
A.制取 B.收集 C.检验 D.验满
二、填空题(每空1分,共37分)
16.请用化学用语填写下列空白:
(1)+5价的磷元素__________________。
(2)2个氢氧根离子____________。
(3)氯化钾_______________。
(4)3个五氧化二磷分子________________。
17.下列物质中属于混合物的是______________,属于纯净物的是________________(均填序号)。
①海水 ②铜 ③食盐水 ④洁净的空气 ⑤液氧 ⑥二氧化碳 ⑦冰水混合物
18.现有:①氧气 ②石墨 ③一氧化碳 ④二氧化碳,请根据题意回答问题__________(填序号)。
(1)能供给呼吸的是:___________________。
(3)能使燃着的木条熄灭的是:___________________。
(4)能使氧化铜变成铜的氧化物是:___________________。
19.在2Mg+O22MgO中镁、氧气和氧化镁的质量比为________________。
20.在A+B=C+D的反应中,如果生成物C和D的质量比为3:5,参加反应的A和B的质量总和为160g,则生成D的质量为_______________。
21.下图是用来表示某物质发生化学变化的微观示意图。图中●和分别表示两种元素的原子,仔细观察图,回答下列问题:
(1)C物质属于______ ( 填“混合物”、“单质"或“化合物”)。
(2)该反应的基本反应类型为____________。
(3)若A、B、C为初中化学中的常见物质,写出符合该反应的化学方程式______________。
(4)根据上述示意图,你能得到哪些化学变化的信息 ___________(请写一条)
22.碳及其化合物的综合利用是世界关注的热点。
(一)认识“碳”
(1)石墨与金刚石互称为同素异形体,从微观角度看两者物理性质差异的主要原因是_____________;CO2与CO的化学性质不同,是因为________________。
(2)金刚石用于裁玻璃是因为金刚石__________, 石墨用来作电极体现石墨有良好的_______性。
(3)制糖工业中利用活性炭脱色制白糖,体现活性炭的______性。
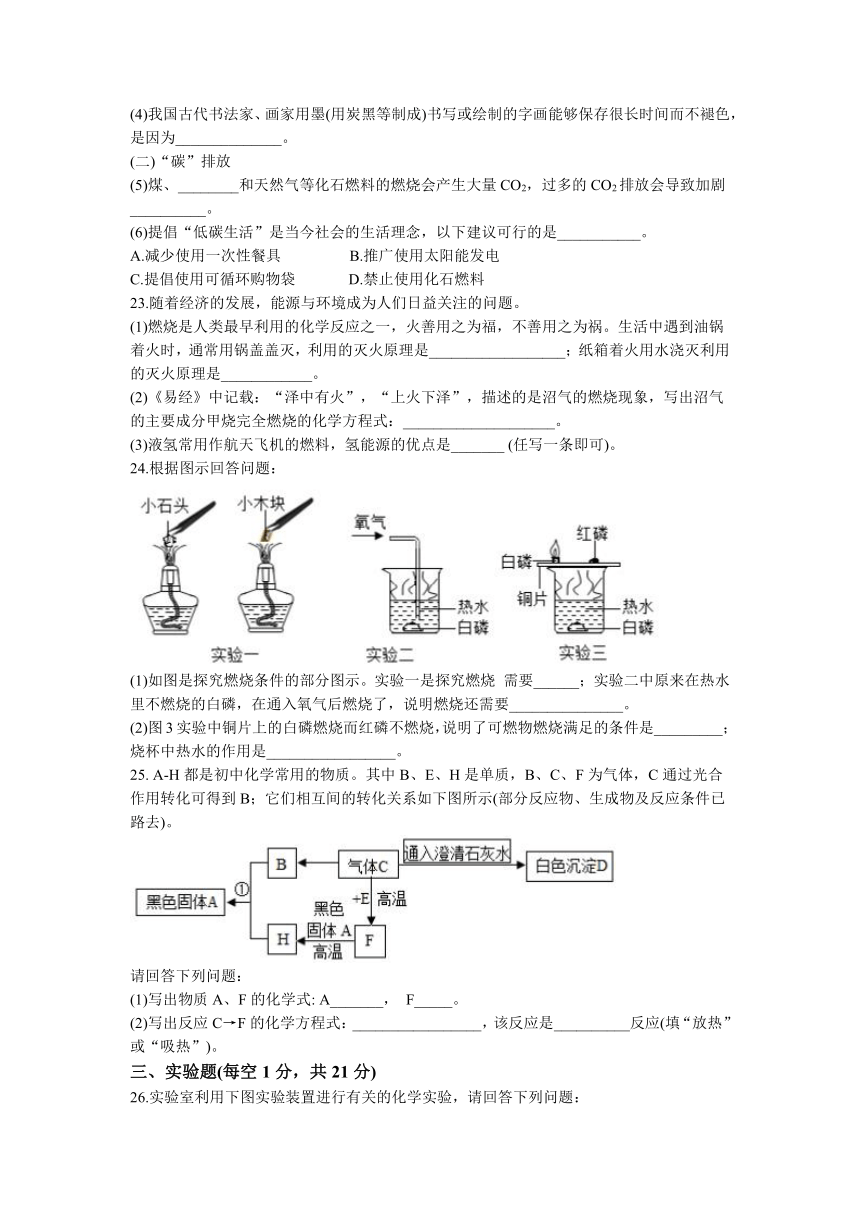
(4)我国古代书法家、画家用墨(用炭黑等制成)书写或绘制的字画能够保存很长时间而不褪色,是因为______________。
(二)“碳”排放
(5)煤、________和天然气等化石燃料的燃烧会产生大量CO2,过多的CO2排放会导致加剧__________。
(6)提倡“低碳生活”是当今社会的生活理念,以下建议可行的是___________。
A.减少使用一次性餐具 B.推广使用太阳能发电
C.提倡使用可循环购物袋 D.禁止使用化石燃料
23.随着经济的发展,能源与环境成为人们日益关注的问题。
(1)燃烧是人类最早利用的化学反应之一,火善用之为福,不善用之为祸。生活中遇到油锅着火时,通常用锅盖盖灭,利用的灭火原理是__________________;纸箱着火用水浇灭利用的灭火原理是____________。
(2)《易经》中记载:“泽中有火”,“上火下泽”,描述的是沼气的燃烧现象,写出沼气的主要成分甲烧完全燃烧的化学方程式:____________________。
(3)液氢常用作航天飞机的燃料,氢能源的优点是_______ (任写一条即可)。
24.根据图示回答问题:
(1)如图是探究燃烧条件的部分图示。实验一是探究燃烧 需要______;实验二中原来在热水里不燃烧的白磷,在通入氧气后燃烧了,说明燃烧还需要_______________。
(2)图3实验中铜片上的白磷燃烧而红磷不燃烧,说明了可燃物燃烧满足的条件是_________;烧杯中热水的作用是_________________。
25. A-H都是初中化学常用的物质。其中B、E、H是单质,B、C、F为气体,C通过光合作用转化可得到B;它们相互间的转化关系如下图所示(部分反应物、生成物及反应条件已路去)。
请回答下列问题:
(1)写出物质A、F的化学式: A_______, F_____。
(2)写出反应C→F的化学方程式:_________________,该反应是__________反应(填“放热”或“吸热”)。
三、实验题(每空1分,共21分)
26.实验室利用下图实验装置进行有关的化学实验,请回答下列问题:
(1)请你写出仪器乙的名称:__________________。
(2)实验室制取二氧化碳,发生装置可选择图中的_________(填序号), 写出该反应的化学反应方程式______________。
(3)实验室制取二氧化碳选用装置C作为发生装置,优点是__________;利用向上排空气法用装置E收集二氧化碳,验满时燃着的木条应放在________(填“a”或“b”)端。
27.把刚烘干的木炭粉末和氧化铜粉末混合均匀,小心地铺放进试管,并把试管固定在铁架台上,试管口装有通入澄清石灰水的导管(如图)。用酒精灯给混合物加热,使其充分反应。
(1)图中酒精灯火焰上方加了一个金属网罩,这样做的好处是____________。
(2)被加热的试管中发生的化学反应方程式为_____________, 可观察到的现象为________________。
(3)刚开始加热时试管中有气泡冒出,澄清石灰水不变浑浊的原因是___________________。
(4)实验结束时,应先________(填“熄灭酒精灯”或“撤走导管”)。
(5)实验结束后,待试管冷却后再把试管里的粉末倒在纸上,原因是_________________。
28.为了探究二氧化碳能与水发生反应生成具有酸性的物质,A、B两同学分别设计了探究实验方案。A同学的方案是将二氧化碳通入紫色石蕊试剂中(紫色石蕊试剂遇酸变红色),观察溶液的颜色变化,如图甲所示,B同学的实验方案是取四朵用石蕊试液染成紫色的干燥小花,按图乙中的步骤Ⅰ~ Ⅳ依次进行实验,观察小花颜色变化。
请对A、B两同学的实验探究方案进行评价后回答下列问题:
(1)哪个同学的方案合理_____________,理由是_________________。
(2) B同学的方案中观察到纸花的颜色变化是:
Ⅰ.纸花变红 Ⅱ. 纸花不变红 Ⅲ.纸花不变色 Ⅳ.______________。
(3)B同学进行的Ⅰ、Ⅱ两项实验,说明了什么__________________。
(4)写出B同学方案中实验IV中发生反应的化学方程式______________。
29.为探究燃烧的条件,某同学进行如图所示的实验:
(1)实验Ⅰ能验证可燃物燃烧需要氧气的现象是_______________,化学方程式是______________。
(2)设计实验Ⅱ的目的是_______________。
(3)铜片上的红磷没有燃烧的原因是______________。
(4)实验中水的作用是_______________。
四、计算题(共12分)
30.最近,科学家研究确认,一些油炸食品含有致癌物质丙烯酰胺(C3H5ON)。回答并计算(不要求写计算过程):
(1)丙烯酰胺由_____________种元素组成,1个丙烯酰胺分子由____个原子构成;
(2)丙烯酰胺的相对分子质量为______________;
(3)丙烯酰胺中碳、氢、氧、氮四种元索的质量比为_____________;
(4)丙烯酰胺中氮元素的质量分数为______________。
31.实验室加热氯酸钾与二氧化锰的混合物制取氧气,加热28g此混合物至不再产生气体为止,冷却后测得剩余固体质量为18.4g。试计算:
(1)生成的氧气的质量____________。
(2)原混合物中二氧化锰的质量____________。.
参考答案:
1.B 2.B 3.D 4.A 5.A 6.A 7.D 8.A 9.D 10.C 11.C 12.C 13.C 14.AD 15.C
16.(1);(2)2OH-;(3)KCl;(4)3P2O5
17.①③④;②⑤⑥⑦
18.(1)①;(2)②;(3)④;(4)③
19.3:2:5
20.100g
21.(1)化合物;(2)化合反应(3);(4)在化学反应前后元素的种类不变
22.(1)碳原子的排列方式不同 ;分子构成不同;(2)硬度大;导电;(3)吸附;(4)常温下碳的化学性质稳定;(5)石油 ;温室效应;(6)ABC
23.(1)隔绝氧气/空气;降低温度到可燃物着火点以下
(2)CH4+2O2CO2+2H2O
(3)无污染、热值高等
24.(1)可燃物;氧气;O2
(2)温度达到着火点;提供热量、隔绝氧气
25.(1)CuO;CO;(2) ;吸热
26.(1)锥形瓶
(2)B;C;D;
(3)随时控制反应的发生与停止;b
27. (1)集中火焰,提高温度;(2);黑色粉末变为红色;(3)刚开始加热时逸出的气体是空气;(4)撤走导管;(5)防止热的铜与空气中的氧气反应重新生成氧化铜
28. B;无法证明是二氧化碳使石蕊试液变红,还是二氧化碳和水反应生成的碳酸使石蕊试液变红;湿润的纸花变红;酸能使石蕊变红,而水不能使石蕊变红;H2O+CO2=H2CO3
29.(1)①铜片上的白磷燃烧,热水中的白磷不燃烧; ②;(2)探究燃烧需要氧气;(3)温度没有达到红磷的着火点;(4)提供热量、隔绝氧气
30. (1) 4;10;(2)71;(3)36︰5︰16︰14;(4)19.7 %
31. (1)9.6g;根据质量守恒定律,反应生成氧气的质量为28g-18.4g=9.6g;
(2)3.5g
解:设原混合物中氯酸钾的质量为x,
故混合物中二氧化锰质量为28g-24.5g=3.5g;
答:生成的氧气的质量为9.6g;原混合物中二氧化锰的质量为3.5g。
可能用到的相对原子质量:O-16 C-12 H-1 K-39 Mn-55 Cl-35.5 N-14 Mg-24
一、选择题(1-12题每题一个选项符合题意,13-15 每题1-2个选项符合题意,每小题2分,共30分)
1.下列成语主要涉及化学变化的是
A.刻舟求剑 B.星火燎原 C.滴水成冰 D. 沙里淘金
2.高铁是“中国制造"- -张耀眼的名片,它带领中国走向世界。高铁列车与电路连接的石墨电刷没有用到石墨性质的是
A.稳定性 B.还原性 C.滑腻感 D.导电性
3.下列物质中,前者属于混合物,后者属于纯净物的是
A.五氧化二磷 汞 B.水 空气 C.硫 二氧化碳 D.糖水 氮气
4.我国古代某些字画用墨(用炭黑等制成)绘制或书写而成,能够保存至今而不变色的原因是
A.碳在常温下化学性质不活泼 B.炭黑具有很强的吸附能力
C.碳具有还原性 D.碳单质不溶于水
5.性质决定用途。下列碳单质的性质与其用途不相符的是
A.石墨导电性好——用于制铅笔芯
B. C60分子很稳定,有超导性——广泛用于超导领域
C.活性炭吸附性强——用作冰箱除味剂
D.炭黑在常温下化学性质不活泼——用于制墨汁
6.下图所示的实验操作正确的是
A.加热液体 B.倾倒药品
C.称量药品 D.检验氧气收集满
7.金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用X表示):12HF+3Na2CO3+ 2Al(OH)3=2X+ 3CO2+9H2O,则X的化学式为
A. AlF3 B. NaF C. NaAlF4 D. Na3AlF6
8.小华对妈妈说:“你说菠菜中富含铁,为什么我用磁铁无法把菠菜吸起来呢 ”小华认为的“铁”是指
A.金属铁 B.铁分子 C.铁元素 D.铁原子
9.“酒香不怕巷子深”,从分子的角度解释原因是
A.分子体积小 B.分子质量小 C.分子之间有间隔 D.分子在不断地运动
10.分析以下化学反应的微观示意图,判断有关说法正确的是
A.反应前后各物质均属于氧化物 B.参加反应的两种物质的质量比为1:1
C.该反应不属于化合反应 D.该反应中各元素的化合价均发生了改变
11.下列实验现象叙述正确的是
A.碳在氧气中燃烧生成黑色固体 B.铁在氧气中燃烧发出耀眼的白光
C.硫在空气中燃烧生成刺激性气味气体 D.蜡烛在空气中燃烧产生二氧化碳和水
12.将mgA物质在ngB物质中充分燃烧,所生成C物质的质量,下列答案中你认为最合理的是
A.一定等于(m+n)g B.一定小于(m- n)g
C.可能是小于或等于(m+n)g D.以上答案都正确
13.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:对该反应,下列描述正确的是
物质 甲 乙 丙 丁
反应前质量/g 20 m 20 20
反应后质量/g 2 待测 32 26
A.该反应中甲、丙、丁的质量比为1:16:13 B.乙在该反应中一定是催化剂
C.该反应是分解反应 D.待测质量一定为4g
14.实验室用过氧化氢溶液和二氧化锰制取氧气,有关该实验的说法错误的是
A.二氧化锰是反应物 B.可用实验室制取二氧化碳的装置
C.可用向上排空气法收集 D.可用带火星的木条检验二氧化碳
15.某同学在实验室制取二氧化碳的过程中,进行制取、收集、检验、验满的四步操作如”下图所示,其中正确的是
A.制取 B.收集 C.检验 D.验满
二、填空题(每空1分,共37分)
16.请用化学用语填写下列空白:
(1)+5价的磷元素__________________。
(2)2个氢氧根离子____________。
(3)氯化钾_______________。
(4)3个五氧化二磷分子________________。
17.下列物质中属于混合物的是______________,属于纯净物的是________________(均填序号)。
①海水 ②铜 ③食盐水 ④洁净的空气 ⑤液氧 ⑥二氧化碳 ⑦冰水混合物
18.现有:①氧气 ②石墨 ③一氧化碳 ④二氧化碳,请根据题意回答问题__________(填序号)。
(1)能供给呼吸的是:___________________。
(3)能使燃着的木条熄灭的是:___________________。
(4)能使氧化铜变成铜的氧化物是:___________________。
19.在2Mg+O22MgO中镁、氧气和氧化镁的质量比为________________。
20.在A+B=C+D的反应中,如果生成物C和D的质量比为3:5,参加反应的A和B的质量总和为160g,则生成D的质量为_______________。
21.下图是用来表示某物质发生化学变化的微观示意图。图中●和分别表示两种元素的原子,仔细观察图,回答下列问题:
(1)C物质属于______ ( 填“混合物”、“单质"或“化合物”)。
(2)该反应的基本反应类型为____________。
(3)若A、B、C为初中化学中的常见物质,写出符合该反应的化学方程式______________。
(4)根据上述示意图,你能得到哪些化学变化的信息 ___________(请写一条)
22.碳及其化合物的综合利用是世界关注的热点。
(一)认识“碳”
(1)石墨与金刚石互称为同素异形体,从微观角度看两者物理性质差异的主要原因是_____________;CO2与CO的化学性质不同,是因为________________。
(2)金刚石用于裁玻璃是因为金刚石__________, 石墨用来作电极体现石墨有良好的_______性。
(3)制糖工业中利用活性炭脱色制白糖,体现活性炭的______性。
(4)我国古代书法家、画家用墨(用炭黑等制成)书写或绘制的字画能够保存很长时间而不褪色,是因为______________。
(二)“碳”排放
(5)煤、________和天然气等化石燃料的燃烧会产生大量CO2,过多的CO2排放会导致加剧__________。
(6)提倡“低碳生活”是当今社会的生活理念,以下建议可行的是___________。
A.减少使用一次性餐具 B.推广使用太阳能发电
C.提倡使用可循环购物袋 D.禁止使用化石燃料
23.随着经济的发展,能源与环境成为人们日益关注的问题。
(1)燃烧是人类最早利用的化学反应之一,火善用之为福,不善用之为祸。生活中遇到油锅着火时,通常用锅盖盖灭,利用的灭火原理是__________________;纸箱着火用水浇灭利用的灭火原理是____________。
(2)《易经》中记载:“泽中有火”,“上火下泽”,描述的是沼气的燃烧现象,写出沼气的主要成分甲烧完全燃烧的化学方程式:____________________。
(3)液氢常用作航天飞机的燃料,氢能源的优点是_______ (任写一条即可)。
24.根据图示回答问题:
(1)如图是探究燃烧条件的部分图示。实验一是探究燃烧 需要______;实验二中原来在热水里不燃烧的白磷,在通入氧气后燃烧了,说明燃烧还需要_______________。
(2)图3实验中铜片上的白磷燃烧而红磷不燃烧,说明了可燃物燃烧满足的条件是_________;烧杯中热水的作用是_________________。
25. A-H都是初中化学常用的物质。其中B、E、H是单质,B、C、F为气体,C通过光合作用转化可得到B;它们相互间的转化关系如下图所示(部分反应物、生成物及反应条件已路去)。
请回答下列问题:
(1)写出物质A、F的化学式: A_______, F_____。
(2)写出反应C→F的化学方程式:_________________,该反应是__________反应(填“放热”或“吸热”)。
三、实验题(每空1分,共21分)
26.实验室利用下图实验装置进行有关的化学实验,请回答下列问题:
(1)请你写出仪器乙的名称:__________________。
(2)实验室制取二氧化碳,发生装置可选择图中的_________(填序号), 写出该反应的化学反应方程式______________。
(3)实验室制取二氧化碳选用装置C作为发生装置,优点是__________;利用向上排空气法用装置E收集二氧化碳,验满时燃着的木条应放在________(填“a”或“b”)端。
27.把刚烘干的木炭粉末和氧化铜粉末混合均匀,小心地铺放进试管,并把试管固定在铁架台上,试管口装有通入澄清石灰水的导管(如图)。用酒精灯给混合物加热,使其充分反应。
(1)图中酒精灯火焰上方加了一个金属网罩,这样做的好处是____________。
(2)被加热的试管中发生的化学反应方程式为_____________, 可观察到的现象为________________。
(3)刚开始加热时试管中有气泡冒出,澄清石灰水不变浑浊的原因是___________________。
(4)实验结束时,应先________(填“熄灭酒精灯”或“撤走导管”)。
(5)实验结束后,待试管冷却后再把试管里的粉末倒在纸上,原因是_________________。
28.为了探究二氧化碳能与水发生反应生成具有酸性的物质,A、B两同学分别设计了探究实验方案。A同学的方案是将二氧化碳通入紫色石蕊试剂中(紫色石蕊试剂遇酸变红色),观察溶液的颜色变化,如图甲所示,B同学的实验方案是取四朵用石蕊试液染成紫色的干燥小花,按图乙中的步骤Ⅰ~ Ⅳ依次进行实验,观察小花颜色变化。
请对A、B两同学的实验探究方案进行评价后回答下列问题:
(1)哪个同学的方案合理_____________,理由是_________________。
(2) B同学的方案中观察到纸花的颜色变化是:
Ⅰ.纸花变红 Ⅱ. 纸花不变红 Ⅲ.纸花不变色 Ⅳ.______________。
(3)B同学进行的Ⅰ、Ⅱ两项实验,说明了什么__________________。
(4)写出B同学方案中实验IV中发生反应的化学方程式______________。
29.为探究燃烧的条件,某同学进行如图所示的实验:
(1)实验Ⅰ能验证可燃物燃烧需要氧气的现象是_______________,化学方程式是______________。
(2)设计实验Ⅱ的目的是_______________。
(3)铜片上的红磷没有燃烧的原因是______________。
(4)实验中水的作用是_______________。
四、计算题(共12分)
30.最近,科学家研究确认,一些油炸食品含有致癌物质丙烯酰胺(C3H5ON)。回答并计算(不要求写计算过程):
(1)丙烯酰胺由_____________种元素组成,1个丙烯酰胺分子由____个原子构成;
(2)丙烯酰胺的相对分子质量为______________;
(3)丙烯酰胺中碳、氢、氧、氮四种元索的质量比为_____________;
(4)丙烯酰胺中氮元素的质量分数为______________。
31.实验室加热氯酸钾与二氧化锰的混合物制取氧气,加热28g此混合物至不再产生气体为止,冷却后测得剩余固体质量为18.4g。试计算:
(1)生成的氧气的质量____________。
(2)原混合物中二氧化锰的质量____________。.
参考答案:
1.B 2.B 3.D 4.A 5.A 6.A 7.D 8.A 9.D 10.C 11.C 12.C 13.C 14.AD 15.C
16.(1);(2)2OH-;(3)KCl;(4)3P2O5
17.①③④;②⑤⑥⑦
18.(1)①;(2)②;(3)④;(4)③
19.3:2:5
20.100g
21.(1)化合物;(2)化合反应(3);(4)在化学反应前后元素的种类不变
22.(1)碳原子的排列方式不同 ;分子构成不同;(2)硬度大;导电;(3)吸附;(4)常温下碳的化学性质稳定;(5)石油 ;温室效应;(6)ABC
23.(1)隔绝氧气/空气;降低温度到可燃物着火点以下
(2)CH4+2O2CO2+2H2O
(3)无污染、热值高等
24.(1)可燃物;氧气;O2
(2)温度达到着火点;提供热量、隔绝氧气
25.(1)CuO;CO;(2) ;吸热
26.(1)锥形瓶
(2)B;C;D;
(3)随时控制反应的发生与停止;b
27. (1)集中火焰,提高温度;(2);黑色粉末变为红色;(3)刚开始加热时逸出的气体是空气;(4)撤走导管;(5)防止热的铜与空气中的氧气反应重新生成氧化铜
28. B;无法证明是二氧化碳使石蕊试液变红,还是二氧化碳和水反应生成的碳酸使石蕊试液变红;湿润的纸花变红;酸能使石蕊变红,而水不能使石蕊变红;H2O+CO2=H2CO3
29.(1)①铜片上的白磷燃烧,热水中的白磷不燃烧; ②;(2)探究燃烧需要氧气;(3)温度没有达到红磷的着火点;(4)提供热量、隔绝氧气
30. (1) 4;10;(2)71;(3)36︰5︰16︰14;(4)19.7 %
31. (1)9.6g;根据质量守恒定律,反应生成氧气的质量为28g-18.4g=9.6g;
(2)3.5g
解:设原混合物中氯酸钾的质量为x,
故混合物中二氧化锰质量为28g-24.5g=3.5g;
答:生成的氧气的质量为9.6g;原混合物中二氧化锰的质量为3.5g。
同课章节目录
