期末复习综合训练(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3
文档属性
| 名称 | 期末复习综合训练(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3 |
|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-15 00:00:00 | ||
图片预览

文档简介
期末复习综合训练
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.M是一种含有热塑性聚氨脂结构的物质。X和Y是可合成M的单体,其合成反应如下:
下列说法不正确的是。
A.单体Y的化学式为
B.单体X分子中的所有碳原子一定共平面
C.形成聚合物的过程中发生了加成反应
D.该聚合物在一定条件下可降解
2.中成药连花清瘟胶囊在防治新冠肺炎中起到重要作用,其有效成分绿原酸结构简式如图所示。下列说法正确的是
A.绿原酸的分子式为
B.每个绿原酸分子中含有6个手性碳原子
C.绿原酸与足量反应,可消耗
D.绿原酸与足量溶液反应,最多消耗
3.下列有关高分子材料的说法不正确的是
A.为了防止淀粉—聚丙烯酸钠材料溶于水,可以使用交联剂对其进行改性处理
B.聚乙烯材料具有一定的弹性是因为化学键在拉伸过程中会断裂,除去外力后会恢复
C.用于制作烹任器具手柄的酚醛树脂是一种网状高分子材料
D.乳酸和均可用于制备可降解材料,有助于减轻温室效应、消除“白色污染”
4.药物吗替麦考酚酯有强大的抑制淋巴细胞增殖的作用,可通过如下反应制得:
下列叙述正确的是
A.化合物X中含有手性碳原子
B.化合物Y的分子式为
C.可用溴水检验是否有化合物Z生成
D.1mol化合物Z最多与反应
5.“达芦那韦”是一种蛋白酶抑制剂,其合成路线中的某片段如图所示:
下列说法正确的是
A.a的一氯代物有3种 B.b与有机物含有的官能团相同
C.c能发生取代反应、加成反应 D.d的分子式为
6.下列实验装置能达到目的的是
A.装置甲实验室制乙酸乙酯 B.装置乙实验室制硝基苯
C.装置丙实验室制乙炔 D.装置丁实验室制乙烯
7.2021年初,我国自主研发的创新药“奥布替尼”上市。“奥布替尼”的结构简式为
下列说法正确的是
A.“奥布替尼”分子中的单键碳原子均有手性
B.一定条件下“奥布替尼”能与盐酸发生水解反应产生羧酸和铵盐
C.“奥布替尼”的分子式为
D.是合成该药物的前体,其分子中所有原子可能在同一平面上
8.近年来科学家制造出大量的新物质。对下列四种物质的相关描述错误的是
A.石墨烯具有良好的导电性 B.石墨炔、石墨烯均能发生加成反应
C.碳纳米管属于无机非金属材料 D.上述四种物质均属于碳的单质
9.我国自主研发对二甲苯的绿色合成路线取得新进展,其合成示意图如图。下列说法正确的是
A.过程①发生了取代反应
B.中间产物M的结构简式为
C.1mol对二甲苯可以与3mol H2加成,其加成产物的一氯代物有2种
D.该合成路线原子利用率为100%,最终得到的产物易分离
10.有机物X可以作为药物合成中间体,其结构简式如图所示。有关X说法错误的是
A.分子式为C10H12O4
B.分子中含有3个手性碳原子
C.1molX最多可与3molBr2发生加成反应
D.一定条件下,能发生加聚反应,也能发生缩聚反应
11.在10%稀碱溶液催化下,醛分子间能发生如下反应:RCHO+R'CH2CHO。苯甲醛和乙醛发生上述反应生成的是
A. B.
C. D.
12.光刻胶(主要成分是)是大规模集成电路印刷电路版技术中的关键材料,某一光刻胶的主要成分如图所示,下列有关说法正确的是
A.合成此高聚物的单体的化学式为C11H10O2
B.发生加成反应时1mol该物质可消耗4molH2
C.该物质可稳定存在于碱性溶液中
D.该物质可经过缩聚反应制得
13.有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图的一系列反应。则下列说法不正确的是
A.根据图示可推知D为苯酚
B.G的同分异构体中属于酯且能发生银镜反应的只有2种
C.上述各物质中能发生水解反应的有A、B、C、F、G
D.A的结构中含2种官能团
14.莲花清瘟胶囊对于治疗新冠肺炎有确切的疗效,其有效成分绿原酸的结构简式如下图所示。下列有关绿原酸说法正确的是
A.所有碳原子均可能共平面
B.绿原酸与足量反应,最多可消耗
C.与等量绿原酸反应时,所需、的物质的量之比是
D.能发生酯化、加成、消去、氧化、加聚反应
15.光刻胶是制造芯片、集成电路的关键材料。某新型的光刻胶(高分子化合物e),可以由芳香族化合物a、有机物b(丙酮)为原料制备,其合成路线如下:
其中a、c均含有-COOH。下列说法错误的是
A.反应①为加成反应 B.有机物c脱水成烯的产物可能有2种
C.反应②为酯化 D.反应③为缩聚反应
二、实验题
16.乙酰苯胺()作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺()和冰醋酸反应制得,该反应是放热的可逆反应。
已知:I.苯胺在空气中易被氧化。
II.可能用到的有关性质如下:
名称 熔点/℃ 沸点/℃ 溶解度/g(20℃)
水 乙醇
苯胺 184 3.4 任意比混合
冰醋酸 16.6 118 任意比混合 任意比混合
乙酰苯胺 114.3 304 0.46 36.9
(温度高溶解度大)
制备乙酰苯胺的具体流程如下:
回答下列问题:
(1)写出制备乙酰苯胺的化学方程式___________。
(2)①加入的锌粒的作用是___________(写两条)。
②加入的冰醋酸要过量的目的___________。
(3)步骤1所用装置如图所示。
①a处使用的仪器为___________(填“A”、“B”或“C”),该仪器的名称是___________。
②反应体系的温度控制在100℃~105℃,目的是___________。
③判断反应基本完全的现象是___________。
(4)步骤3中洗涤乙酰苯胺粗产品最合适的试剂是___________(填标号)。A.冰水 B.热水 C.15%的乙醇溶液 D.NaOH溶液
(5)步骤4中重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→___________→冷却结晶→过滤→洗涤→干燥。
17.苯乙酮( )可用作制造香料,可由苯和乙酸酐制备,其反应原理为:
已知:
名称 相对分子质量 沸点/℃ 密度() 溶解性
苯 78 80.1 0.88 不溶于水,易溶于有机溶剂
苯乙酮 120 203 1.03 微溶于水,易溶于有机溶剂
乙酸酐 102 139 1.08 溶于水生成乙酸,易溶于有机溶剂
133.5 178(升华) 2.44 遇水易水解
请回答下列问题:
Ⅰ.催化剂无水的制备
下图是实验室制取并收集少量无水的相关实验仪器和药品。
(1)B中发生反应的化学方程式为_______。
(2)制备无水时导管接口顺序为c→_______(填序号,装置不可重复使用),其中装置E的作用是_______。
Ⅱ.苯乙酮的制备
步骤一:向三颈烧瓶中加入14.0g苯和6.0g无水,在搅拌下滴加10.2g乙酸酐,在70~80℃下加热45min,反应装置如图(省略部分装置)。
步骤二:冷却后,将三颈烧瓶中的物质全部倒入25.0g冰水中,有白色胶状沉淀生成;水层用苯萃取,合并苯层溶液,再依次用15mL 5% NaOH溶液和15mL水洗涤,分离出苯层。
步骤三:向苯层中加入无水硫酸镁,放置一段时间后,收集产品苯乙酮并回收苯。
(3)仪器N的名称为_______,其作用有:①平衡气压;②_______。
(4)步骤二中用NaOH溶液洗涤的目的是_______。
(5)实验中制得5.6g苯乙酮,则苯乙酮的产率为_______%(保留一位小数)。
三、结构与性质
18.钛、锌、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。铁的基态原子价电子排布式为_______。
(2)黄铜是人类最早使用的合金之一,主要由和组成。第一电离能I1(Zn) _______I1(Cu) (填“大于”或“小于”)。原因是_______。
(3)《中华本草》等中医典籍中,记载了炉甘石()入药,可用于治疗皮肤炎症或表面创伤。中,阴离子空间构型为_______,原子的杂化形式为_______。
(4)与酚类物质的显色反应常用于其离子检验,已知遇邻苯二酚()和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是_______;已知,利用该离子方程式可以检验溶液中的。中键、键数目之比为_______。
(5)和的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
①该晶体的化学式为_______。
②已知该晶胞的摩尔质量为,密度为。设为阿伏加德罗常数的值,则该晶胞的边长是_______(用含、、的代数式表示)。
四、有机推断题
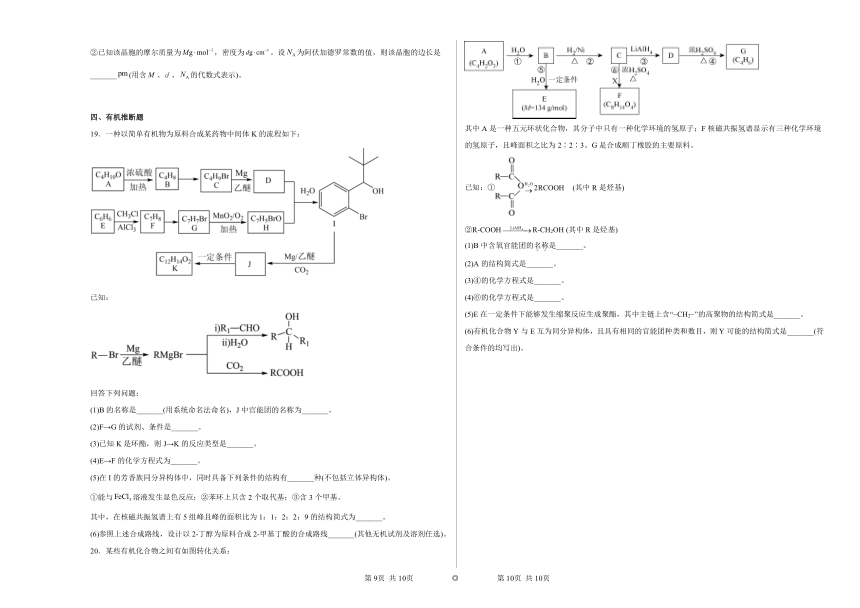
19.一种以简单有机物为原料合成某药物中间体K的流程如下:
已知:
回答下列问题:
(1)B的名称是_______(用系统命名法命名),J中官能团的名称为_______。
(2)F→G的试剂、条件是_______。
(3)已知K是环酯,则J→K的反应类型是_______。
(4)E→F的化学方程式为_______。
(5)在I的芳香族同分异构体中,同时具备下列条件的结构有_______种(不包括立体异构体)。
①能与溶液发生显色反应;②苯环上只含2个取代基;③含3个甲基。
其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:9的结构简式为_______。
(6)参照上述合成路线,设计以2-丁醇为原料合成2-甲基丁酸的合成路线_______(其他无机试剂及溶剂任选)。
20.某些有机化合物之间有如图转化关系:
其中A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F核磁共振氢谱显示有三种化学环境的氢原子,且峰面积之比为2∶2∶3。G是合成顺丁橡胶的主要原料。
已知:①2RCOOH (其中R是烃基)
②R-COOHR-CH2OH (其中R是烃基)
(1)B中含氧官能团的名称是_______。
(2)A的结构简式是_______。
(3)④的化学方程式是_______。
(4)⑥的化学方程式是_______。
(5)E在一定条件下能够发生缩聚反应生成聚酯,其中主链上含“ CH2 ”的高聚物的结构简式是_______。
(6)有机化合物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y可能的结构简式是_______(符合条件的均写出)。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】A.根据Y的结构简式可判断单体Y的化学式为,A正确;
B.由于单键可以旋转,所以单体X分子中的所有碳原子不一定共平面,B错误;
C.形成聚合物的过程中碳氮双键变为碳氮单键,因此发生了加成反应,C正确;
D.该聚合物中含有酯基、肽键等,因此在一定条件下可降解,D正确;
答案选B。
2.D
【详解】A.由结构可知,绿原酸分子含有16个碳原子、9个氧原子,不饱和度为8,分子中氢原子数目为,故其分子式为,A错误;
B.连4个不同基团的碳原子为手性碳原子,每个绿原酸分子中含有4个手性碳原子,B错误;
C.绿原酸中有1个苯环和1个碳碳双键可与H2反应,则绿原酸与足量反应,可消耗,C错误;
D.绿原酸含有1个羧基、1个酯基(羧酸与醇形成)、2个酚羟基,因此绿原酸与足量溶液反应,最多消耗,D正确;
故答案为D。
3.B
【详解】A.使用交联剂,增加特殊聚合物的耐溶性,描述正确,不符题意;
B.聚乙烯材料具有一定的弹性是因为分子结构中碳链可折叠,描述错误,符合题意;
C.酚醛树脂是热固性塑料,其聚合形成的高聚物呈网状结构,描述正确,不符题意;
D.乳酸在一定条件下可以缩聚成聚乳酸酯,CO2与环氧化物在一定条件下可以制备聚碳酸酯,消耗CO2减轻温室效应,可降解塑料可减少“白色污染”,描述正确,不符题意;
综上,本题选B。
4.D
【详解】A.连接4个不同原子或原子团的碳原子为手性碳原子,X中不含手性碳原子,故A错误;
B.Y中C、H、O、N原子个数依次是6、13、2、1,分子式为C6H13NO2,故B错误;
C.碳碳双键能和溴水发生加成反应而使溴水褪色,X、Z中都含有碳碳双键,都能和溴水发生加成反应而使溴水褪色,所以不能用溴水检验是否含有Z,故C错误;
D.酚羟基、酯基水解生成的羧基都能和NaOH以1:1反应,Z中含有1个酚羟基、2个酯基水解生成2个羧基,所以1molZ最多消耗3molNaOH,故D正确;
故选D。
5.C
【详解】A.a分子中的氢原子有5种,一氯代物有5种,A错误;
B.b含有醛基,有机物含有酯基,含有的官能团不相同,B错误;
C.c含有苯环,因此能发生取代反应、加成反应,C正确;
D.根据d的结构简式可知分子式为,D错误;
答案选C。
6.B
【详解】A.装置甲实验室装置甲实验室制乙酸乙酯,应在制备装置后连接收集产物的装置(试管中加饱和碳酸钠溶液),A错误;
B.制备硝基苯,水浴加热,温度计测定水温,图中制备装置合理,能够达到实验目的,B正确;
C.装置丙实验室制乙炔,不能使用启普发生器,电石是粉末状的,会从启普发生器中间的间隙中漏到食盐水中,不会达到随时停止的状况,且反应剧烈,C错误;
D.装置丁制取乙烯的条件是迅速加热到170℃,图中缺少温度计,D错误;
故答案为:B。
7.B
【详解】A.以单键连接四个不同原子或原子团的碳原子才是手性碳,故A错误;
B.分子中的肽键能与盐酸发生水解反应产生羧酸和铵盐,故B正确;
C.分子式为,故C错误;
D.含饱和碳原子,所有原子不可能都共面,故D错误;故选B。
8.D
【详解】A.石墨烯具有良好的导电性,A项正确,故A不符合题意;
B.石墨炔、石墨烯都含有不饱和碳碳键,均能发生加成反应,B正确,故B不符合题意;
C.碳纳米管属于无机非金属材料,C项正确,故C不符合题意;
D.石墨炔、石墨烯、碳纳米管三种物质均属于碳的单质,而金刚烷属于烃类物质,不属于碳的单质,D错误,故D符合题意;
答案为:D。
9.B
【详解】A.过程①中异戊二烯与丙烯醛发生加成反应生成M,A错误;
B.由M的球棍模型知,M的结构简式为,B正确;
C.1mol对二甲苯可以与3mol H2加成,其加成产物只有3种氢原子,故其一氯代物只有3种,C错误;
D.过程①的原子利用率为100%,但过程②除生成对二甲苯外,还生成了水,原子利用率小于100%,D错误;
答案为B。
10.B
【详解】A.根据结构简式可判断分子式为C10H12O4,A正确;
B.分子中含有2个手性碳原子,即,B错误;
C.分子中含有3个碳碳双键,1molX最多可与3molBr2发生加成反应,C正确;
D.分子中含有碳碳双键、羧基和羟基,一定条件下,能发生加聚反应,也能发生缩聚反应,D正确;
答案选B。
11.D
【详解】根据题给信息知,醛分子与醛分子反应的实质是一个醛分子中与醛基相连的碳原子上脱去一个氢原子然后和剩余基团加成到另一个醛分子的碳氧双键上,形成羟基并加长碳链,之后羟基发生消去反应形成碳碳双键;苯甲醛为,乙醛为CH3CHO,乙醛可以将苯甲醛中的醛基加成得到,醇羟基的碳原子的邻位碳原子上含有氢的可以发生消去反应,得到碳碳双键,故选D。
12.A
【详解】A.根据结构简式知,该高聚物( )的单体是苯丙烯酸乙烯酯,分子式为C11H10O2,故A正确;
B.该物质为高分子化合物,聚合度为n,发生加成反应时1mol该物质可消耗4nmolH2,故B错误;
C.该物质存在-COOC-,在碱性溶液中能发生水解反应,不能稳定存在,故C错误;
D.该高分子化合物的直链中只有2个碳原子,可通过加聚反应制得的,故D错误;
故选A。
【点睛】本题的易错点为B,要注意该物质为高聚物。
13.D
【分析】B能和二氧化碳、水反应生成D,D能和溴水发生取代反应生成白色沉淀,说明D中含有酚羟基,所以A中含有苯环,A的不饱和度=(8×2+2-8)/2=5,则A中还含有一个不饱和键,A能和氢氧化钠的水溶液发生水解反应生成B和C,则A中含有酯基,C酸化后生成E,E是羧酸,E和乙醇发生酯化反应生成G,G的分子式为C4H8O2,则E的结构简式为CH3COOH,C为CH3COONa,G的结构简式为CH3COOCH2CH3,结合A的分子式可知,B为,D为,F为三溴苯酚,A为,以此解答该题。
【详解】A.由上述分析可知,D为苯酚,故A正确;
B.G的结构简式为CH3COOCH2CH3,它的同分异构体中属于酯且能发生银镜反应,应是甲酸形成的酯,相应的醇有1-丙醇,2-丙醇,有2种,故B正确;
C.A、G属于酯类,B是苯酚钠,C是醋酸钠,F是三溴苯酚,因此上述各物质中能发生水解反应的有A、B、C、F、G,故C正确;
D.A为,只有一种官能团酯基,故D错误;
故选D。
14.D
【详解】A.分子结构中含有饱和碳原子,饱和碳原子是四面体结构,因此左边的六元碳环上的碳原子一定不共面,故A错误;
B.分子结构中只有碳碳双键和苯环能够与氢气发生加成反应,羧基和酯基不能,绿原酸与足量反应,最多可消耗,故B错误;
C.羟基和羟基均能与钠反应放出氢气,所以1mol绿原酸消耗6molNa;只有羧基能和碳酸氢钠以1:1反应,该分子中含有1个羧基,所以1mol绿原酸消耗1molNaHCO3,与等量绿原酸反应时,所需、的物质的量之比是,故C错误;
D.羧基和羟基能发生酯化反应、苯环和碳碳双键能发生加成反应、碳碳双键和酚羟基能发生氧化反应、醇羟基能发生消去反应,碳碳双键能发生加聚反应,故D正确;
故选D。
15.D
【分析】根据流程采用逆合成分析,e为d的加聚产物,由e的结构可得d为,a、c均含有-COOH,d由c反应得到,且c、d组成相差一分子水,由d结构分析可知,c应为,c由a、b反应制得,结合a的分子式以及b的结构可推出a为,据此分析解答。
【详解】A.根据以上分析,反应①为羰基的加成反应,故A正确;
B.c为,含有醇羟基,可发生消去反应,且羟基所连碳上有两种邻位碳、氢存在,可得到两种消去产物,故B正确;
C.根据以上分析,反应②为分子内的酯化反应形成酯基,故C正确;
D.反应③是d中碳碳双键发生加聚反应产生e,不是缩聚反应,故D错误;
故选D。
16.(1)
(2) 防止液体暴沸,防止苯胺被氧化 提高苯胺的利用率
(3) A 直形冷凝管 有利于水蒸气馏出,减少乙酸等馏出 尾接管中不再有液滴滴下
(4)A
(5)趁热过滤
【分析】苯胺和冰醋酸及锌粒存在下共热,控制反应温度100℃~105℃,能蒸出产物中的水,使该反应平衡正向移动,又不会把其它反应物蒸出,可以提高苯胺利用率。
(1)
苯胺()和冰醋酸发生取代反应生成乙酰苯胺,制备乙酰苯胺的化学方程式为 。
(2)
①加入的锌粒的作用有可防止液体暴沸,已知苯胺在空气中易被氧化,锌与醋酸反应生成氢气,形成氢气环境,可防止苯胺被氧化。
②加入过量的冰醋酸,能促进反应正向进行,可提高苯胺的利用率。
(3)
①a处使用的仪器为A,该仪器的名称是直形冷凝管,用于冷凝蒸气,便于馏分流出。
②冰醋酸具有挥发性,温度过高,冰醋酸蒸出,降低了反应物的利用率,温度过低,不利于蒸出水,故反应体系的温度控制在100℃~105℃,目的是有利于水蒸气馏出,减少乙酸馏出。
③尾接管中不再有液滴滴下时说明反应基本完全。
(4)
温度越高,乙酰苯胺在水中的溶解度越大,故不能用热水洗涤,应用冰水洗涤;乙酰苯胺易溶于乙醇,且在碱性条件下易水解,故不能用15%的乙醇溶液或NaOH溶液洗涤,故选A。
(5)
因为乙酰苯胺的溶解度随温度升高而增大,重结晶时,应趁热过滤,以除去难溶物,再冷却结晶。
17.(1)MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
(2) f→g→e→d→a→b→h→i 处理尾气,防止污染环境,防止空气中水蒸气进入
(3) 球形冷凝管 冷凝回流苯等物质
(4)除去产品中的乙酸
(5)46.7%
【分析】无水的制备是氯气和铝在加热条件下反应,实验室用B装置制备氯气,用D装置除掉氯气中的氯化氢气体,再用C装置干燥氯气,再铜A装置制备氯化铝,再用E装置除掉尾气。向三颈烧瓶中加入14.0g苯和6.0g无水,在搅拌下滴加10.2g乙酸酐,在水浴条件下加热45min,冷却后,倒入25.0g冰水中,有白色胶状沉淀生成;水层用苯萃取,合并苯层溶液,再依次用15mL 5% NaOH溶液和15mL水洗涤,分离出苯层,加入无水硫酸镁干燥,在蒸馏得到苯乙酮并回收苯。
(1)
B中是二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,其发生反应的化学方程式为MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O;故答案为:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O。
(2)
A装置是制备氯化铝,B是制备氯气,C是干燥氯气,D是除掉氯气中氯化氢气体,E是除掉尾气,防止空气中水蒸气进入,因此制备无水时导管接口顺序为c→f→g→e→d→a→b→h→i,其中装置E的作用是处理尾气,防止污染环境,防止空气中水蒸气进入;故答案为:f→g→e→d→a→b→h→i;处理尾气,防止污染环境,防止空气中水蒸气进入。
(3)
苯等物质沸点不高,受热易挥发,通过球形冷凝管充分冷凝回流可提高苯等物质的利用率,仪器N的名称为球形冷凝管,其作用有:①平衡气压;②冷凝回流苯等物质;故答案为:球形冷凝管;冷凝回流苯等物质。
(4)
苯中溶解有苯乙酮、乙酸等物质,乙酸能与碱反应,可选用NaOH溶液洗涤粗品,以除去七中溶解的乙酸,因此步骤二中用NaOH溶液洗涤的目的是除去产品中的乙酸;故答案为:除去产品中的乙酸。
(5)
14.0g苯物质的量为,10.2g乙酸酐物质的量为,根据方程式分析得到乙酸酐不足,由反应可知,参加反应的苯、乙酸酐和生成的苯乙酮的物质的量相等,所以苯乙酮理论产量为0.1mol,则苯乙酮的产率为;故答案为:46.7%。
18.(1)
(2) 大于 核外电子排布为全满稳定结构,较难失电子
(3) 平面三角形
(4) 邻苯二酚易形成分子内氢键,对苯二酚易形成分子间氢键,故邻苯二酚的熔沸点比对苯二酚低 1:1
(5)
【详解】(1)铁为26号元素,其基态原子价电子排布式为。
(2)的第一电离能高于的第一电离能,原因是的核外电子排布已经达到了每个能级都是全满的稳定结构,所以失电子比较困难。
(3)中碳原子的价层电子对数=中心原子原子的键数+中心原子上的孤电子对数,所以阴离子中碳属于杂化,没有孤对电子,是平面三角形结构。
(4)易形成分子内氢键,易形成分子间氢键,形成分子间氢键的物质熔沸点更高,因此邻苯二酚的熔沸点比对苯二酚低;键和键数均为12,键、键数目之比为。
(5)①位于晶胞的顶点,晶胞实际占有的个数为,位于面上和内部,晶胞实际占有的个数是,因此化学式为;②晶胞的质量为,根据密度的定义,晶胞的体积为,该晶胞的边长是。
19.(1) 2-甲基丙烯 羟基、羧基
(2)Br2(l)(或液溴),FeBr3(或Fe)
(3)酯化反应(或取代反应)
(4)+CH3Cl+HCl
(5) 12
(6)
【分析】本题突破口是Ⅰ的结构简式,由Ⅰ逆推可知:A为或,B为,C为,D为,E为苯,F为甲苯,G为,H为,J为,结合K的分子式,K为,据此解答。
【详解】(1)B为,B的名称是2-甲基丙烯,J为,J中官能团的名称为羟基、羧基。
(2)F→G是苯环上引入溴原子,则反应的试剂、条件是Br2(l)(或液溴),FeBr3(或Fe)。
(3)已知K是环酯,说明是分子内羟基和羧基的酯化反应,则J→K的反应类型是酯化反应(或取代反应)。
(4)E→F是苯环上引入甲基,则反应的化学方程式为+CH3Cl+HCl。
(5)①能与溶液发生显色反应;②苯环上只含2个取代基;③含3个甲基,说明苯环上含1个羟基、1个溴戊基。含3个甲基的溴戊基有4种:、、、(—R表示苯基),溴戊基与羟基位于邻、间、对三种,共12种同分异构体,其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:9的结构简式为。
(6)2-丁醇首先和溴化氢发生取代反应生成2-溴丁烷,然后2-溴丁烷转化为,最后和二氧化碳反应转化为,则合成2-甲基丁酸的合成路线为。
20.(1)羧基
(2)
(3)HOCH2CH2CH2CH2OHCH2=CHCH=CH2+2H2O
(4)HOOCCH2CH2COOH+2CH3CH2OHCH3CH2OOCCH2CH2COOCH2CH3+2H2O
(5)
(6),
【分析】A是一种五元环状化合物,其分子中只有一种化学环境的氢原子,结合信息①,可知A中还含有一个碳碳双键,故A的结构简式是,A→B是酸酐水解,则B是HOOCCH=CHCOOH,B与氢气发生加成反应生成C,则C是HOOCCH2CH2COOH,根据信息②,可知反应③是还原反应,故D是HOCH2CH2CH2CH2OH,由D与G的分子可知,反应④是消去反应,且G为合成顺丁橡胶的主要原料,所以G为CH2=CHCH=CH2,由B与E的相对分子质量,可知反应⑤是碳碳双键与H2O发生的加成反应,故E为HOOCCH2CHOHCOOH,C(丁二酸)分子内含有两种不同化学环境的氢原子,根据反应条件,可知反应⑥为酯化反应,又结合C和F的分子式和结构知,X为乙醇,反应后生成F为CH3CH2OOCCH2CH2COOCH2CH3。据此解答。
(1)
B是HOOCCH=CHCOOH,含氧官能团为羧基,故答案为:羧基;
(2)
由上述分析可知,A的结构简式是,故答案为:;
(3)
反应④的化学方程式是HOCH2CH2CH2CH2OHCH2=CHCH=CH2+2H2O,故答案为:HOCH2CH2CH2CH2OHCH2=CHCH=CH2+2H2O;
(4)
反应⑥的化学方程式为HOOCCH2CH2COOH+2CH3CH2OHCH3CH2OOCCH2CH2COOCH2CH3+2H2O,故答案为HOOCCH2CH2COOH+2CH3CH2OHCH3CH2OOCCH2CH2COOCH2CH3+2H2O;
(5)
HOOCCH2CHOHCOOH在一定条件下能够发生缩聚反应,其中主链上含“ CH2 ”的高聚物的结构简式是,故答案为: ;
(6)
有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,Y有两个-COOH,一个-OH,把E的主链上碳原子缩减为3个,则会出现2种结构,即 ,,故答案为: ,。
答案第1页,共2页
答案第1页,共2页
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.M是一种含有热塑性聚氨脂结构的物质。X和Y是可合成M的单体,其合成反应如下:
下列说法不正确的是。
A.单体Y的化学式为
B.单体X分子中的所有碳原子一定共平面
C.形成聚合物的过程中发生了加成反应
D.该聚合物在一定条件下可降解
2.中成药连花清瘟胶囊在防治新冠肺炎中起到重要作用,其有效成分绿原酸结构简式如图所示。下列说法正确的是
A.绿原酸的分子式为
B.每个绿原酸分子中含有6个手性碳原子
C.绿原酸与足量反应,可消耗
D.绿原酸与足量溶液反应,最多消耗
3.下列有关高分子材料的说法不正确的是
A.为了防止淀粉—聚丙烯酸钠材料溶于水,可以使用交联剂对其进行改性处理
B.聚乙烯材料具有一定的弹性是因为化学键在拉伸过程中会断裂,除去外力后会恢复
C.用于制作烹任器具手柄的酚醛树脂是一种网状高分子材料
D.乳酸和均可用于制备可降解材料,有助于减轻温室效应、消除“白色污染”
4.药物吗替麦考酚酯有强大的抑制淋巴细胞增殖的作用,可通过如下反应制得:
下列叙述正确的是
A.化合物X中含有手性碳原子
B.化合物Y的分子式为
C.可用溴水检验是否有化合物Z生成
D.1mol化合物Z最多与反应
5.“达芦那韦”是一种蛋白酶抑制剂,其合成路线中的某片段如图所示:
下列说法正确的是
A.a的一氯代物有3种 B.b与有机物含有的官能团相同
C.c能发生取代反应、加成反应 D.d的分子式为
6.下列实验装置能达到目的的是
A.装置甲实验室制乙酸乙酯 B.装置乙实验室制硝基苯
C.装置丙实验室制乙炔 D.装置丁实验室制乙烯
7.2021年初,我国自主研发的创新药“奥布替尼”上市。“奥布替尼”的结构简式为
下列说法正确的是
A.“奥布替尼”分子中的单键碳原子均有手性
B.一定条件下“奥布替尼”能与盐酸发生水解反应产生羧酸和铵盐
C.“奥布替尼”的分子式为
D.是合成该药物的前体,其分子中所有原子可能在同一平面上
8.近年来科学家制造出大量的新物质。对下列四种物质的相关描述错误的是
A.石墨烯具有良好的导电性 B.石墨炔、石墨烯均能发生加成反应
C.碳纳米管属于无机非金属材料 D.上述四种物质均属于碳的单质
9.我国自主研发对二甲苯的绿色合成路线取得新进展,其合成示意图如图。下列说法正确的是
A.过程①发生了取代反应
B.中间产物M的结构简式为
C.1mol对二甲苯可以与3mol H2加成,其加成产物的一氯代物有2种
D.该合成路线原子利用率为100%,最终得到的产物易分离
10.有机物X可以作为药物合成中间体,其结构简式如图所示。有关X说法错误的是
A.分子式为C10H12O4
B.分子中含有3个手性碳原子
C.1molX最多可与3molBr2发生加成反应
D.一定条件下,能发生加聚反应,也能发生缩聚反应
11.在10%稀碱溶液催化下,醛分子间能发生如下反应:RCHO+R'CH2CHO。苯甲醛和乙醛发生上述反应生成的是
A. B.
C. D.
12.光刻胶(主要成分是)是大规模集成电路印刷电路版技术中的关键材料,某一光刻胶的主要成分如图所示,下列有关说法正确的是
A.合成此高聚物的单体的化学式为C11H10O2
B.发生加成反应时1mol该物质可消耗4molH2
C.该物质可稳定存在于碱性溶液中
D.该物质可经过缩聚反应制得
13.有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图的一系列反应。则下列说法不正确的是
A.根据图示可推知D为苯酚
B.G的同分异构体中属于酯且能发生银镜反应的只有2种
C.上述各物质中能发生水解反应的有A、B、C、F、G
D.A的结构中含2种官能团
14.莲花清瘟胶囊对于治疗新冠肺炎有确切的疗效,其有效成分绿原酸的结构简式如下图所示。下列有关绿原酸说法正确的是
A.所有碳原子均可能共平面
B.绿原酸与足量反应,最多可消耗
C.与等量绿原酸反应时,所需、的物质的量之比是
D.能发生酯化、加成、消去、氧化、加聚反应
15.光刻胶是制造芯片、集成电路的关键材料。某新型的光刻胶(高分子化合物e),可以由芳香族化合物a、有机物b(丙酮)为原料制备,其合成路线如下:
其中a、c均含有-COOH。下列说法错误的是
A.反应①为加成反应 B.有机物c脱水成烯的产物可能有2种
C.反应②为酯化 D.反应③为缩聚反应
二、实验题
16.乙酰苯胺()作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺()和冰醋酸反应制得,该反应是放热的可逆反应。
已知:I.苯胺在空气中易被氧化。
II.可能用到的有关性质如下:
名称 熔点/℃ 沸点/℃ 溶解度/g(20℃)
水 乙醇
苯胺 184 3.4 任意比混合
冰醋酸 16.6 118 任意比混合 任意比混合
乙酰苯胺 114.3 304 0.46 36.9
(温度高溶解度大)
制备乙酰苯胺的具体流程如下:
回答下列问题:
(1)写出制备乙酰苯胺的化学方程式___________。
(2)①加入的锌粒的作用是___________(写两条)。
②加入的冰醋酸要过量的目的___________。
(3)步骤1所用装置如图所示。
①a处使用的仪器为___________(填“A”、“B”或“C”),该仪器的名称是___________。
②反应体系的温度控制在100℃~105℃,目的是___________。
③判断反应基本完全的现象是___________。
(4)步骤3中洗涤乙酰苯胺粗产品最合适的试剂是___________(填标号)。A.冰水 B.热水 C.15%的乙醇溶液 D.NaOH溶液
(5)步骤4中重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→___________→冷却结晶→过滤→洗涤→干燥。
17.苯乙酮( )可用作制造香料,可由苯和乙酸酐制备,其反应原理为:
已知:
名称 相对分子质量 沸点/℃ 密度() 溶解性
苯 78 80.1 0.88 不溶于水,易溶于有机溶剂
苯乙酮 120 203 1.03 微溶于水,易溶于有机溶剂
乙酸酐 102 139 1.08 溶于水生成乙酸,易溶于有机溶剂
133.5 178(升华) 2.44 遇水易水解
请回答下列问题:
Ⅰ.催化剂无水的制备
下图是实验室制取并收集少量无水的相关实验仪器和药品。
(1)B中发生反应的化学方程式为_______。
(2)制备无水时导管接口顺序为c→_______(填序号,装置不可重复使用),其中装置E的作用是_______。
Ⅱ.苯乙酮的制备
步骤一:向三颈烧瓶中加入14.0g苯和6.0g无水,在搅拌下滴加10.2g乙酸酐,在70~80℃下加热45min,反应装置如图(省略部分装置)。
步骤二:冷却后,将三颈烧瓶中的物质全部倒入25.0g冰水中,有白色胶状沉淀生成;水层用苯萃取,合并苯层溶液,再依次用15mL 5% NaOH溶液和15mL水洗涤,分离出苯层。
步骤三:向苯层中加入无水硫酸镁,放置一段时间后,收集产品苯乙酮并回收苯。
(3)仪器N的名称为_______,其作用有:①平衡气压;②_______。
(4)步骤二中用NaOH溶液洗涤的目的是_______。
(5)实验中制得5.6g苯乙酮,则苯乙酮的产率为_______%(保留一位小数)。
三、结构与性质
18.钛、锌、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。铁的基态原子价电子排布式为_______。
(2)黄铜是人类最早使用的合金之一,主要由和组成。第一电离能I1(Zn) _______I1(Cu) (填“大于”或“小于”)。原因是_______。
(3)《中华本草》等中医典籍中,记载了炉甘石()入药,可用于治疗皮肤炎症或表面创伤。中,阴离子空间构型为_______,原子的杂化形式为_______。
(4)与酚类物质的显色反应常用于其离子检验,已知遇邻苯二酚()和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是_______;已知,利用该离子方程式可以检验溶液中的。中键、键数目之比为_______。
(5)和的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
①该晶体的化学式为_______。
②已知该晶胞的摩尔质量为,密度为。设为阿伏加德罗常数的值,则该晶胞的边长是_______(用含、、的代数式表示)。
四、有机推断题
19.一种以简单有机物为原料合成某药物中间体K的流程如下:
已知:
回答下列问题:
(1)B的名称是_______(用系统命名法命名),J中官能团的名称为_______。
(2)F→G的试剂、条件是_______。
(3)已知K是环酯,则J→K的反应类型是_______。
(4)E→F的化学方程式为_______。
(5)在I的芳香族同分异构体中,同时具备下列条件的结构有_______种(不包括立体异构体)。
①能与溶液发生显色反应;②苯环上只含2个取代基;③含3个甲基。
其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:9的结构简式为_______。
(6)参照上述合成路线,设计以2-丁醇为原料合成2-甲基丁酸的合成路线_______(其他无机试剂及溶剂任选)。
20.某些有机化合物之间有如图转化关系:
其中A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F核磁共振氢谱显示有三种化学环境的氢原子,且峰面积之比为2∶2∶3。G是合成顺丁橡胶的主要原料。
已知:①2RCOOH (其中R是烃基)
②R-COOHR-CH2OH (其中R是烃基)
(1)B中含氧官能团的名称是_______。
(2)A的结构简式是_______。
(3)④的化学方程式是_______。
(4)⑥的化学方程式是_______。
(5)E在一定条件下能够发生缩聚反应生成聚酯,其中主链上含“ CH2 ”的高聚物的结构简式是_______。
(6)有机化合物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y可能的结构简式是_______(符合条件的均写出)。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】A.根据Y的结构简式可判断单体Y的化学式为,A正确;
B.由于单键可以旋转,所以单体X分子中的所有碳原子不一定共平面,B错误;
C.形成聚合物的过程中碳氮双键变为碳氮单键,因此发生了加成反应,C正确;
D.该聚合物中含有酯基、肽键等,因此在一定条件下可降解,D正确;
答案选B。
2.D
【详解】A.由结构可知,绿原酸分子含有16个碳原子、9个氧原子,不饱和度为8,分子中氢原子数目为,故其分子式为,A错误;
B.连4个不同基团的碳原子为手性碳原子,每个绿原酸分子中含有4个手性碳原子,B错误;
C.绿原酸中有1个苯环和1个碳碳双键可与H2反应,则绿原酸与足量反应,可消耗,C错误;
D.绿原酸含有1个羧基、1个酯基(羧酸与醇形成)、2个酚羟基,因此绿原酸与足量溶液反应,最多消耗,D正确;
故答案为D。
3.B
【详解】A.使用交联剂,增加特殊聚合物的耐溶性,描述正确,不符题意;
B.聚乙烯材料具有一定的弹性是因为分子结构中碳链可折叠,描述错误,符合题意;
C.酚醛树脂是热固性塑料,其聚合形成的高聚物呈网状结构,描述正确,不符题意;
D.乳酸在一定条件下可以缩聚成聚乳酸酯,CO2与环氧化物在一定条件下可以制备聚碳酸酯,消耗CO2减轻温室效应,可降解塑料可减少“白色污染”,描述正确,不符题意;
综上,本题选B。
4.D
【详解】A.连接4个不同原子或原子团的碳原子为手性碳原子,X中不含手性碳原子,故A错误;
B.Y中C、H、O、N原子个数依次是6、13、2、1,分子式为C6H13NO2,故B错误;
C.碳碳双键能和溴水发生加成反应而使溴水褪色,X、Z中都含有碳碳双键,都能和溴水发生加成反应而使溴水褪色,所以不能用溴水检验是否含有Z,故C错误;
D.酚羟基、酯基水解生成的羧基都能和NaOH以1:1反应,Z中含有1个酚羟基、2个酯基水解生成2个羧基,所以1molZ最多消耗3molNaOH,故D正确;
故选D。
5.C
【详解】A.a分子中的氢原子有5种,一氯代物有5种,A错误;
B.b含有醛基,有机物含有酯基,含有的官能团不相同,B错误;
C.c含有苯环,因此能发生取代反应、加成反应,C正确;
D.根据d的结构简式可知分子式为,D错误;
答案选C。
6.B
【详解】A.装置甲实验室装置甲实验室制乙酸乙酯,应在制备装置后连接收集产物的装置(试管中加饱和碳酸钠溶液),A错误;
B.制备硝基苯,水浴加热,温度计测定水温,图中制备装置合理,能够达到实验目的,B正确;
C.装置丙实验室制乙炔,不能使用启普发生器,电石是粉末状的,会从启普发生器中间的间隙中漏到食盐水中,不会达到随时停止的状况,且反应剧烈,C错误;
D.装置丁制取乙烯的条件是迅速加热到170℃,图中缺少温度计,D错误;
故答案为:B。
7.B
【详解】A.以单键连接四个不同原子或原子团的碳原子才是手性碳,故A错误;
B.分子中的肽键能与盐酸发生水解反应产生羧酸和铵盐,故B正确;
C.分子式为,故C错误;
D.含饱和碳原子,所有原子不可能都共面,故D错误;故选B。
8.D
【详解】A.石墨烯具有良好的导电性,A项正确,故A不符合题意;
B.石墨炔、石墨烯都含有不饱和碳碳键,均能发生加成反应,B正确,故B不符合题意;
C.碳纳米管属于无机非金属材料,C项正确,故C不符合题意;
D.石墨炔、石墨烯、碳纳米管三种物质均属于碳的单质,而金刚烷属于烃类物质,不属于碳的单质,D错误,故D符合题意;
答案为:D。
9.B
【详解】A.过程①中异戊二烯与丙烯醛发生加成反应生成M,A错误;
B.由M的球棍模型知,M的结构简式为,B正确;
C.1mol对二甲苯可以与3mol H2加成,其加成产物只有3种氢原子,故其一氯代物只有3种,C错误;
D.过程①的原子利用率为100%,但过程②除生成对二甲苯外,还生成了水,原子利用率小于100%,D错误;
答案为B。
10.B
【详解】A.根据结构简式可判断分子式为C10H12O4,A正确;
B.分子中含有2个手性碳原子,即,B错误;
C.分子中含有3个碳碳双键,1molX最多可与3molBr2发生加成反应,C正确;
D.分子中含有碳碳双键、羧基和羟基,一定条件下,能发生加聚反应,也能发生缩聚反应,D正确;
答案选B。
11.D
【详解】根据题给信息知,醛分子与醛分子反应的实质是一个醛分子中与醛基相连的碳原子上脱去一个氢原子然后和剩余基团加成到另一个醛分子的碳氧双键上,形成羟基并加长碳链,之后羟基发生消去反应形成碳碳双键;苯甲醛为,乙醛为CH3CHO,乙醛可以将苯甲醛中的醛基加成得到,醇羟基的碳原子的邻位碳原子上含有氢的可以发生消去反应,得到碳碳双键,故选D。
12.A
【详解】A.根据结构简式知,该高聚物( )的单体是苯丙烯酸乙烯酯,分子式为C11H10O2,故A正确;
B.该物质为高分子化合物,聚合度为n,发生加成反应时1mol该物质可消耗4nmolH2,故B错误;
C.该物质存在-COOC-,在碱性溶液中能发生水解反应,不能稳定存在,故C错误;
D.该高分子化合物的直链中只有2个碳原子,可通过加聚反应制得的,故D错误;
故选A。
【点睛】本题的易错点为B,要注意该物质为高聚物。
13.D
【分析】B能和二氧化碳、水反应生成D,D能和溴水发生取代反应生成白色沉淀,说明D中含有酚羟基,所以A中含有苯环,A的不饱和度=(8×2+2-8)/2=5,则A中还含有一个不饱和键,A能和氢氧化钠的水溶液发生水解反应生成B和C,则A中含有酯基,C酸化后生成E,E是羧酸,E和乙醇发生酯化反应生成G,G的分子式为C4H8O2,则E的结构简式为CH3COOH,C为CH3COONa,G的结构简式为CH3COOCH2CH3,结合A的分子式可知,B为,D为,F为三溴苯酚,A为,以此解答该题。
【详解】A.由上述分析可知,D为苯酚,故A正确;
B.G的结构简式为CH3COOCH2CH3,它的同分异构体中属于酯且能发生银镜反应,应是甲酸形成的酯,相应的醇有1-丙醇,2-丙醇,有2种,故B正确;
C.A、G属于酯类,B是苯酚钠,C是醋酸钠,F是三溴苯酚,因此上述各物质中能发生水解反应的有A、B、C、F、G,故C正确;
D.A为,只有一种官能团酯基,故D错误;
故选D。
14.D
【详解】A.分子结构中含有饱和碳原子,饱和碳原子是四面体结构,因此左边的六元碳环上的碳原子一定不共面,故A错误;
B.分子结构中只有碳碳双键和苯环能够与氢气发生加成反应,羧基和酯基不能,绿原酸与足量反应,最多可消耗,故B错误;
C.羟基和羟基均能与钠反应放出氢气,所以1mol绿原酸消耗6molNa;只有羧基能和碳酸氢钠以1:1反应,该分子中含有1个羧基,所以1mol绿原酸消耗1molNaHCO3,与等量绿原酸反应时,所需、的物质的量之比是,故C错误;
D.羧基和羟基能发生酯化反应、苯环和碳碳双键能发生加成反应、碳碳双键和酚羟基能发生氧化反应、醇羟基能发生消去反应,碳碳双键能发生加聚反应,故D正确;
故选D。
15.D
【分析】根据流程采用逆合成分析,e为d的加聚产物,由e的结构可得d为,a、c均含有-COOH,d由c反应得到,且c、d组成相差一分子水,由d结构分析可知,c应为,c由a、b反应制得,结合a的分子式以及b的结构可推出a为,据此分析解答。
【详解】A.根据以上分析,反应①为羰基的加成反应,故A正确;
B.c为,含有醇羟基,可发生消去反应,且羟基所连碳上有两种邻位碳、氢存在,可得到两种消去产物,故B正确;
C.根据以上分析,反应②为分子内的酯化反应形成酯基,故C正确;
D.反应③是d中碳碳双键发生加聚反应产生e,不是缩聚反应,故D错误;
故选D。
16.(1)
(2) 防止液体暴沸,防止苯胺被氧化 提高苯胺的利用率
(3) A 直形冷凝管 有利于水蒸气馏出,减少乙酸等馏出 尾接管中不再有液滴滴下
(4)A
(5)趁热过滤
【分析】苯胺和冰醋酸及锌粒存在下共热,控制反应温度100℃~105℃,能蒸出产物中的水,使该反应平衡正向移动,又不会把其它反应物蒸出,可以提高苯胺利用率。
(1)
苯胺()和冰醋酸发生取代反应生成乙酰苯胺,制备乙酰苯胺的化学方程式为 。
(2)
①加入的锌粒的作用有可防止液体暴沸,已知苯胺在空气中易被氧化,锌与醋酸反应生成氢气,形成氢气环境,可防止苯胺被氧化。
②加入过量的冰醋酸,能促进反应正向进行,可提高苯胺的利用率。
(3)
①a处使用的仪器为A,该仪器的名称是直形冷凝管,用于冷凝蒸气,便于馏分流出。
②冰醋酸具有挥发性,温度过高,冰醋酸蒸出,降低了反应物的利用率,温度过低,不利于蒸出水,故反应体系的温度控制在100℃~105℃,目的是有利于水蒸气馏出,减少乙酸馏出。
③尾接管中不再有液滴滴下时说明反应基本完全。
(4)
温度越高,乙酰苯胺在水中的溶解度越大,故不能用热水洗涤,应用冰水洗涤;乙酰苯胺易溶于乙醇,且在碱性条件下易水解,故不能用15%的乙醇溶液或NaOH溶液洗涤,故选A。
(5)
因为乙酰苯胺的溶解度随温度升高而增大,重结晶时,应趁热过滤,以除去难溶物,再冷却结晶。
17.(1)MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
(2) f→g→e→d→a→b→h→i 处理尾气,防止污染环境,防止空气中水蒸气进入
(3) 球形冷凝管 冷凝回流苯等物质
(4)除去产品中的乙酸
(5)46.7%
【分析】无水的制备是氯气和铝在加热条件下反应,实验室用B装置制备氯气,用D装置除掉氯气中的氯化氢气体,再用C装置干燥氯气,再铜A装置制备氯化铝,再用E装置除掉尾气。向三颈烧瓶中加入14.0g苯和6.0g无水,在搅拌下滴加10.2g乙酸酐,在水浴条件下加热45min,冷却后,倒入25.0g冰水中,有白色胶状沉淀生成;水层用苯萃取,合并苯层溶液,再依次用15mL 5% NaOH溶液和15mL水洗涤,分离出苯层,加入无水硫酸镁干燥,在蒸馏得到苯乙酮并回收苯。
(1)
B中是二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,其发生反应的化学方程式为MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O;故答案为:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O。
(2)
A装置是制备氯化铝,B是制备氯气,C是干燥氯气,D是除掉氯气中氯化氢气体,E是除掉尾气,防止空气中水蒸气进入,因此制备无水时导管接口顺序为c→f→g→e→d→a→b→h→i,其中装置E的作用是处理尾气,防止污染环境,防止空气中水蒸气进入;故答案为:f→g→e→d→a→b→h→i;处理尾气,防止污染环境,防止空气中水蒸气进入。
(3)
苯等物质沸点不高,受热易挥发,通过球形冷凝管充分冷凝回流可提高苯等物质的利用率,仪器N的名称为球形冷凝管,其作用有:①平衡气压;②冷凝回流苯等物质;故答案为:球形冷凝管;冷凝回流苯等物质。
(4)
苯中溶解有苯乙酮、乙酸等物质,乙酸能与碱反应,可选用NaOH溶液洗涤粗品,以除去七中溶解的乙酸,因此步骤二中用NaOH溶液洗涤的目的是除去产品中的乙酸;故答案为:除去产品中的乙酸。
(5)
14.0g苯物质的量为,10.2g乙酸酐物质的量为,根据方程式分析得到乙酸酐不足,由反应可知,参加反应的苯、乙酸酐和生成的苯乙酮的物质的量相等,所以苯乙酮理论产量为0.1mol,则苯乙酮的产率为;故答案为:46.7%。
18.(1)
(2) 大于 核外电子排布为全满稳定结构,较难失电子
(3) 平面三角形
(4) 邻苯二酚易形成分子内氢键,对苯二酚易形成分子间氢键,故邻苯二酚的熔沸点比对苯二酚低 1:1
(5)
【详解】(1)铁为26号元素,其基态原子价电子排布式为。
(2)的第一电离能高于的第一电离能,原因是的核外电子排布已经达到了每个能级都是全满的稳定结构,所以失电子比较困难。
(3)中碳原子的价层电子对数=中心原子原子的键数+中心原子上的孤电子对数,所以阴离子中碳属于杂化,没有孤对电子,是平面三角形结构。
(4)易形成分子内氢键,易形成分子间氢键,形成分子间氢键的物质熔沸点更高,因此邻苯二酚的熔沸点比对苯二酚低;键和键数均为12,键、键数目之比为。
(5)①位于晶胞的顶点,晶胞实际占有的个数为,位于面上和内部,晶胞实际占有的个数是,因此化学式为;②晶胞的质量为,根据密度的定义,晶胞的体积为,该晶胞的边长是。
19.(1) 2-甲基丙烯 羟基、羧基
(2)Br2(l)(或液溴),FeBr3(或Fe)
(3)酯化反应(或取代反应)
(4)+CH3Cl+HCl
(5) 12
(6)
【分析】本题突破口是Ⅰ的结构简式,由Ⅰ逆推可知:A为或,B为,C为,D为,E为苯,F为甲苯,G为,H为,J为,结合K的分子式,K为,据此解答。
【详解】(1)B为,B的名称是2-甲基丙烯,J为,J中官能团的名称为羟基、羧基。
(2)F→G是苯环上引入溴原子,则反应的试剂、条件是Br2(l)(或液溴),FeBr3(或Fe)。
(3)已知K是环酯,说明是分子内羟基和羧基的酯化反应,则J→K的反应类型是酯化反应(或取代反应)。
(4)E→F是苯环上引入甲基,则反应的化学方程式为+CH3Cl+HCl。
(5)①能与溶液发生显色反应;②苯环上只含2个取代基;③含3个甲基,说明苯环上含1个羟基、1个溴戊基。含3个甲基的溴戊基有4种:、、、(—R表示苯基),溴戊基与羟基位于邻、间、对三种,共12种同分异构体,其中,在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:9的结构简式为。
(6)2-丁醇首先和溴化氢发生取代反应生成2-溴丁烷,然后2-溴丁烷转化为,最后和二氧化碳反应转化为,则合成2-甲基丁酸的合成路线为。
20.(1)羧基
(2)
(3)HOCH2CH2CH2CH2OHCH2=CHCH=CH2+2H2O
(4)HOOCCH2CH2COOH+2CH3CH2OHCH3CH2OOCCH2CH2COOCH2CH3+2H2O
(5)
(6),
【分析】A是一种五元环状化合物,其分子中只有一种化学环境的氢原子,结合信息①,可知A中还含有一个碳碳双键,故A的结构简式是,A→B是酸酐水解,则B是HOOCCH=CHCOOH,B与氢气发生加成反应生成C,则C是HOOCCH2CH2COOH,根据信息②,可知反应③是还原反应,故D是HOCH2CH2CH2CH2OH,由D与G的分子可知,反应④是消去反应,且G为合成顺丁橡胶的主要原料,所以G为CH2=CHCH=CH2,由B与E的相对分子质量,可知反应⑤是碳碳双键与H2O发生的加成反应,故E为HOOCCH2CHOHCOOH,C(丁二酸)分子内含有两种不同化学环境的氢原子,根据反应条件,可知反应⑥为酯化反应,又结合C和F的分子式和结构知,X为乙醇,反应后生成F为CH3CH2OOCCH2CH2COOCH2CH3。据此解答。
(1)
B是HOOCCH=CHCOOH,含氧官能团为羧基,故答案为:羧基;
(2)
由上述分析可知,A的结构简式是,故答案为:;
(3)
反应④的化学方程式是HOCH2CH2CH2CH2OHCH2=CHCH=CH2+2H2O,故答案为:HOCH2CH2CH2CH2OHCH2=CHCH=CH2+2H2O;
(4)
反应⑥的化学方程式为HOOCCH2CH2COOH+2CH3CH2OHCH3CH2OOCCH2CH2COOCH2CH3+2H2O,故答案为HOOCCH2CH2COOH+2CH3CH2OHCH3CH2OOCCH2CH2COOCH2CH3+2H2O;
(5)
HOOCCH2CHOHCOOH在一定条件下能够发生缩聚反应,其中主链上含“ CH2 ”的高聚物的结构简式是,故答案为: ;
(6)
有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,Y有两个-COOH,一个-OH,把E的主链上碳原子缩减为3个,则会出现2种结构,即 ,,故答案为: ,。
答案第1页,共2页
答案第1页,共2页
