专题4第二单元醛 羧酸 同步练习(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题4第二单元醛 羧酸 同步练习(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 460.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-15 00:00:00 | ||
图片预览




文档简介
专题4第二单元醛 羧酸同步练习
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.具有解热镇痛及抗生素作用的药物“芬必得”主要成分的结构简式如图,它属于
①芳香族化合物②脂肪族化合物③有机羧酸④有机高分子化合物⑤芳香烃
A.③⑤ B.②③ C.①③ D.①④
2.人造海绵的主要成分是聚氨酯,合成方法如图,下列说法不正确的是
+nHOCH2CH2OH→
A.M的分子式为C15H10N2O2
B.聚氨酯和蛋白质分子的某些化学性质相似
C.聚氨酯在一定条件下能发生水解反应
D.合成聚氨酯的反应属于缩聚反应
3.已知。现有A、B、C、D、E、F六种有机物有如下转化关系,其中A的分子式为C4H8O3。下列判断正确的是
A.有机物A结构可能有四种
B.反应①属于氧化反应
C.有机物B、D的最简式相同
D.有机物E是交警检测酒驾的重要物证
4.用括号内的试剂和分离方法除去下列物质中的少量杂质,不正确的是
A.乙酸乙酯中混有乙酸(饱和溶液,分液)
B.乙醇中混有乙酸(NaOH溶液,蒸馏)
C.甲烷中混有乙烯(溴的四氯化碳溶液,分液)
D.溴苯中混有溴(NaOH溶液,分液)
5.下列5种有机化合物中,能够发生酯化、加成和氧化3种类型反应的是
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH3CH2CH2OH ⑤CH3CH(OH)CH2CHO
A.①③④ B.②④⑤ C.①③⑤ D.①②⑤
6.PBT是最坚韧的工程热塑性塑料之一,它是半结晶材料,有非常好的化学稳定性、机械强度、电绝缘性和热稳定性,其结构简式为,下列叙述错误的是
A.PBT可以反复加热熔融加工
B.PBT的单体是对苯二甲酸和1,4-丁二醇
C.由单体合成PBT的反应属于缩聚反应
D.1mol PBT与NaOH 溶液反应时,最多可消耗2mol NaOH溶液
7.实验室用乙酸、乙醇和浓硫酸制取乙酸乙酯的装置如图。下列说法中,不正确的是
A.右侧试管中导管不伸入液面下,是为了防止倒吸
B.实验前先加入浓硫酸,再缓缓加入乙醇和冰醋酸
C.及时将乙酸乙酯蒸出,促进平衡向正反应方向移动
D.饱和Na2CO3溶液可除去产品中混有的乙酸、乙醇
8.下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏;
③除去苯中混有的少量甲苯:加入浓溴水后分液;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A.①② B.②④ C.③④ D.②③
9.下列物质中不属于羧酸类有机物的是
A. B. C. D.
10.茉莉醛具有浓郁的茉莉花香,其结构简式如图所示,下列叙述正确的是
A.茉莉醛与苯甲醛互为同系物
B.在一定条件下,1 mol茉莉醛最多可以与4 mol H2发生加成反应
C.茉莉醛的分子式为C14H18O,一定条件下可以发生氧化反应、还原反应、酯化反应等
D.理论上,202 g茉莉醛能与足量的银氨溶液反应生成216 g单质银
11.某甲酸溶液中可能含有少量甲醛,用下列方法可以证明的是
A.加入新制的并加热,有砖红色沉淀产生,则含甲醛
B.加入银氨溶液并水浴加热,若能产生银镜,则含甲醛
C.先将试液充分进行酯化反应,收集生成物进行银镜反应,若有银镜产生,则含甲醛
D.将该溶液与足量溶液混合后蒸馏,若其蒸馏产物可发生银镜反应,则含甲醛
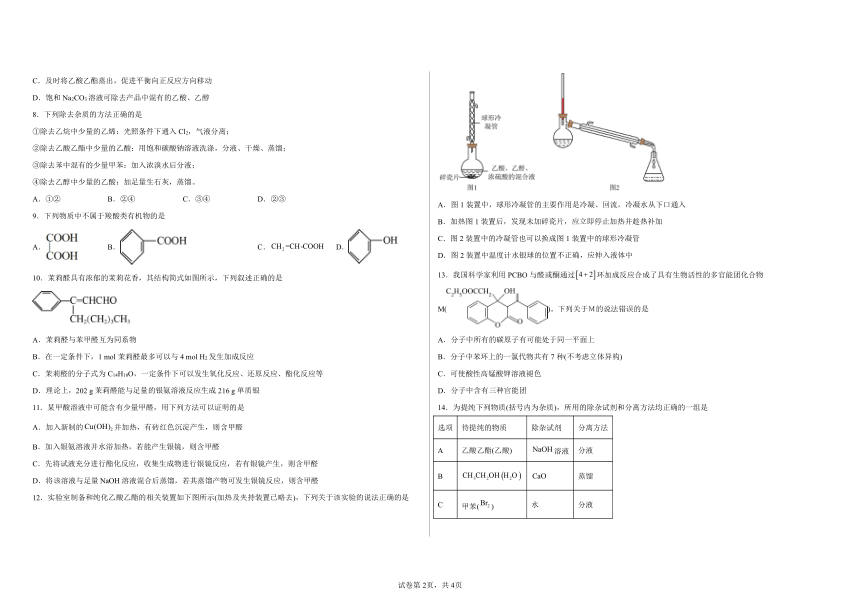
12.实验室制备和纯化乙酸乙酯的相关装置如下图所示(加热及夹持装置已略去),下列关于该实验的说法正确的是
A.图1装置中,球形冷凝管的主要作用是冷凝、回流,冷凝水从下口通入
B.加热图1装置后,发现未加碎瓷片,应立即停止加热并趁热补加
C.图2装置中的冷凝管也可以换成图1装置中的球形冷凝管
D.图2装置中温度计水银球的位置不正确,应伸入液体中
13.我国科学家利用PCBO与醛或酮通过环加成反应合成了具有生物活性的多官能团化合物M()。下列关于M的说法错误的是
A.分子中所有的碳原子有可能处于同一平面上
B.分子中苯环上的一氯代物共有7种(不考虑立体异构)
C.可使酸性高锰酸钾溶液褪色
D.分子中含有三种官能团
14.为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法均正确的一组是
选项 待提纯的物质 除杂试剂 分离方法
A 乙酸乙酯(乙酸) 溶液 分液
B 蒸馏
C 甲苯() 水 分液
D () 萃取
A.A B.B C.C D.D
15.取一定量的有机物和足量反应得到,取另一份等物质的量的同种有机物和足量反应得到,若在同温同压下,,则该有机物可能是
①②HOOC-COOH③CH3CH2COOH④⑤
A.② B.②③④ C.④ D.①
二、填空题
16.由于甲酸的特殊结构(下图),使其表现特有的性质,完成下面各小题:
(1)蜂、蝎子都会分泌蚁酸,被蜂、蝎子蛰咬可涂抹稀氨水、小苏打水缓解疼痛,上述反应的化学方程式为_________、_________。
(2)甲酸中加入新制氢氧化铜溶液,可能的现象:_____,反应的化学方程式:______。
(3)若在新制氢氧化铜溶液中滴入少量甲酸并加热,产生砖红色沉淀,其原因_________,反应的化学方程式:_________。
(4)写出甲酸与银氨溶液反应的化学方程式:_________。
(5)某甲酸溶液中可能存在着甲醛,下列操作能正确说明的是 。
A.加入新制的Cu(OH)2加热,有砖红色沉淀生成,证明一定存在甲醛
B.能发生银镜反应,证明含甲醛
C.试液与足量NaOH溶液混合,其蒸馏产物可发生银镜反应,则有甲醛
D.先将试液充分进行酯化反应,收集生成物进行银镜反应,有银镜产生,则含甲醛
17.某有机化合物A的结构简式如下:
(1)A的分子式是_________。
(2)A在溶液中加热反应得到B和C,C分子含有苯环。B和C的结构简式是:B_________,C_________。该反应属于_________反应。
(3)室温下,C用稀盐酸酸化得到E,E的结构简式是_________。
(4)下列物质中,不能与E发生化学反应的是_________(填写序号)。
①酸性溶液 ②溶液 ③溶液 ④丁烷
三、计算题
18.现有一些只含C、H、O三种元素的有机物,它们燃烧时消耗的O2和生成的CO2的体积比是3:4。
(1)这些有机物中,相对分子质量最小的化合物的分子式是_______________。
(2)某两种碳原子数相同的上述有机物,若它们的相对分子质量分别为a和b(a(3)在这些有机物中有一种化合物,它含有两个羧基。取0.2625g该化合物恰好能跟25.00mL0.1000moL·L-1NaOH溶液完全中和。由此可以得知该化合物的相对分子质量应是______,并可推导出它的分子式应是____________。
四、实验题
19.乙酸乙酯是一种用途广泛的精细化工产品。某课外小组设计实验室制取乙酸乙酯的方案如下:
已知:①无水氯化钙可与乙醇形成CaCl2·6C2H5OH。
②有关有机物的沸点:
有机物 乙醚 乙醇 乙酸 乙酸乙酯
沸点/℃ 34.5 79 118 77.1
③2CH3CH2OHCH3CH2OCH2CH3+H2O。
制备过程:
装置如图所示,A中盛有浓硫酸,B中盛有9.5 mL无水乙醇和6 mL冰醋酸,D中盛有饱和碳酸钠溶液。
(1)写出乙酸与乙醇发生酯化反应的化学方程式:_______。
(2)实验过程中滴加大约3 mL浓硫酸,B的容积最合适的是_______(填字母)。A.25 mL B.50 mL C.250 mL D.500 mL
(3)球形干燥管的主要作用是_______。
(4)预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是_______。
20.醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
可能用到的有关数据如下:
相对分子质量 密度/ g·cm-3 沸点/℃ 溶解性
环己醇 100 0.961 8 161 微溶于水
环己烯 82 0.810 2 83 难溶于水
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是_______。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_______ (填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为_______。
(4)分液漏斗在使用前须清洗干净并_______;在本实验分离过程中,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是_______。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有_______(填字母,下同)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是_______。A.41% B.50% C.61% D.70%
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】由题给结构可知,该有机物含苯环、-COOH,其余结构饱和。
①该有机物含苯环,属于芳香族化合物,①正确;
②含苯环的有机物不属于脂肪族化合物,②错误;
③该有机物含-COOH,属于有机羧酸,③正确;
④该有机物相对分子质量不够大,不属于有机高分子化合物,④错误;
⑤该有机物含O,不属于芳香烃,⑤错误;
综上所述,①③正确,故答案选C。
2.D
【详解】A.根据M的结构简式,其分子式为C15H10N2O2,A正确;
B.聚氨酯和蛋白质分子中均含有酰胺基,则某些化学性质相似,如水解,B正确;
C.聚氨酯中含有酯基和酰胺基,在一定条件下能发生水解反应,C正确;
D.合成聚氨酯的反应中,M中的碳氮双键与乙二醇中羟基的H原子、O原子发生加成反应,属于加成聚合反应,D错误;
故选D。
3.D
【分析】由B与新制反应生成C,再结合A的分子式可推知B为、C为、D为、E为;由B的结构简式、题给已知反应,结合A的分子式C4H8O3,可知A为。
【详解】A.A为,只有一种结构,A错误;
B.反应①中,CH3CHO发生还原反应生成,B错误;
C.和的最简式不同,C错误;
D.检测酒驾就是检测的含量,D正确;
故选D。
4.C
【详解】A.用饱和Na2CO3溶液除去乙酸乙酯中的乙酸,然后使用分液的方法分离有机层和水层,A正确;
B.氢氧化钠和乙醇不反应,和乙酸生成乙酸钠,然后利用乙醇沸点较低的性质,蒸馏得到乙醇,B正确;
C.溴可以和乙烯反应而进入溶液,甲烷为气体逸出,不需分液,C错误;
D.氢氧化钠和溴苯不反应、和溴反应生成盐溶液,然后使用分液的方法分离有机层和水层,D正确;
故选C。
5.C
【详解】①CH2=CHCOOH中含碳碳双键可发生氧化、加成反应,含-COOH可发生酯化反应,故选;
②CH2=CHCOOCH3中含碳碳双键可发生氧化、加成反应,不能发生酯化反应,故不选;
③CH2=CHCH2OH中含碳碳双键可发生氧化、加成反应,含-OH可发生酯化反应,故选;
④CH3CH2CH2OH不能发生加成反应,故不选;
⑤CH3CH(OH)CH2CHO中含-CHO可发生氧化、加成反应,含-OH可发生酯化反应,故选;
故选C。
6.D
【详解】A.由于该塑料属于线性结构,故PBT具有热塑性,受热会熔化,A正确;
B.PBT 的单体有对苯二甲酸和1,4-丁二醇HOCH2CH2CH2CH2OH两种,B正确;
C.和HOCH2CH2CH2CH2OH生成和水,属于缩聚反应,C正确;
D.由题干的结构简式可知,1 mol PBT与NaOH溶液反应时,最多可消耗2n mol NaOH溶液,D错误;
故答案为:D。
7.B
【详解】A.制取的乙酸乙酯中常常混有乙醇、乙酸,产物通入饱和碳酸钠溶液中以除去,但乙酸与碳酸钠较快反应、乙醇极易溶于水,会发生倒吸,所以试管中导管不伸入液面下,故A正确;
B.浓硫酸密度较大、吸水放热,所以混合时先加密度小的乙醇,再加密度大的浓硫酸,且最后加冰醋酸,试剂顺序不能颠倒,故B错误;
C.乙醇、乙酸转化为乙酸乙酯的反应为可逆反应,及时将乙酸乙酯蒸出,促进平衡向正反应方向移动,提高产率,故C正确;
D.饱和碳酸钠作用是吸收乙醇、除去乙酸,使乙酸乙酯分层,然后采用分液法将乙酸乙酯从混合物中分离出来,故D正确;
故选B。
8.B
【详解】①光照条件下通入Cl2,会和乙烷反应,无法除去乙烷中的乙烯,错误;
②饱和碳酸钠溶液可以和乙酸反应,而且乙酸乙酯在其中溶解度很小,所以可以用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏除去乙酸乙酯中的乙酸,正确;
③甲苯和浓溴水反应生成的三溴甲苯会溶于苯,无法分液除去,错误;
④乙酸和生石灰反应生成乙酸钙,然后蒸馏出乙醇,故可除去乙醇中的乙酸,正确;
综上,故选B。
9.D
【详解】乙二酸、苯甲酸和丙烯酸中均含有羧基,属于羧酸类,苯酚属于酚类,故选D。
10.D
【详解】A.茉莉醛中含有的官能团为碳碳双键、醛基,苯甲醛中含有的官能团为醛基,二者含有的官能团不完全相同,二者的结构不相似,因此二者不能互为同系物,A错误;
B.茉莉醛中分子中含有一个苯环、一个碳碳双键、一个醛基都能与氢气发生加成反应,1 mol茉莉醛最多能与3 mol+1 mol+1 mol=5 mol的H2发生加成反应,B错误;
C.由结构简式可知茉莉醛的分子式为C14H18O,其分子中含醛基,因此该物质能够发生氧化反应;也可以与氢气发生还原反应;物质分子中无羟基或羧基,因此不能发生酯化反应,C错误;
D.202 g茉莉醛的物质的量,物质分子中含有1 mol醛基,可与银氨溶液反应得到2 mol Ag,即生成单质银的质量为m(Ag)=2 mol×108 g/mol=216 g,D正确;
故合理选项是D。
11.D
【详解】甲酸和甲醛都含有醛基,则直接加入新制的氢氧化铜或银氨溶液不能证明是否含有甲醛,应先加入足量溶液,甲酸与氢氧化钠溶液反应生成难挥发的甲酸钠,然后蒸馏,将可能存在的甲醛蒸出,再用银氨溶液或新制的氢氧化铜检验蒸馏出的产物,故选D。
12.A
【详解】A.乙酸、乙醇等有机物均易挥发,则图1装置中,球形冷凝管的主要作用是冷凝、回流,冷凝水从下口通入,故A正确;
B.加热题图1装置后,发现未加碎瓷片,应立即停止加热,待冷却后,再补加碎瓷片,故B错误;
C.若题图2装置中的直形冷凝管换成球形冷凝管,不利于冷凝液体顺利流下进入锥形瓶,故C错误;
D.蒸馏时温度计水银球应在蒸馏烧瓶支管口处,故D错误;
答案选A。
13.A
【详解】A.M分子中存在连有3个碳原子的饱和碳原子,因此所有的碳原子不可能处于同一平面上,A项错误;
B.M分子中苯环上有7种不同化学环境的氢原子,如图:,故其苯环上的一氯代物共有7种,B项正确;
C.M中含有碳碳双键,能使酸性高锰酸钾溶液褪色,C项正确;
D.由M的结构可知,其分子中含有酯基、羟基、碳碳双键三种官能团,D项正确;
答案选A。
14.B
【详解】A.乙酸乙酯也能和氢氧化钠溶液反应,应该用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,A项错误;
B.氧化钙和水反应生成氢氧化钙,然后蒸馏即可得到乙醇,B项正确;
C.溴单质易溶于有机溶剂,应该用氢氧化钠溶液除去甲苯中的溴单质,C项错误;
D.溴单质和苯都易溶于四氯化碳,应该用氢氧化钠溶液除去苯中的溴单质,D项错误;
答案选B。
15.D
【详解】只能与反应产生;既能与反应产生,又能与反应产生,题中四种物质各取时分别与足量或反应所得气体的物质的量如表:
物质() 与足量反应生产的量() 与足量反应生产的量()
① 1 1
② 1 2
③ 0.5 1
④ 1.5 2
⑤ 1 0
故答案为:D。
16.(1)
(2) 蓝色的悬浊液变为蓝色溶液
(3) 甲酸中含有醛基,具有还原性,将新制氢氧化铜还原为砖红色的沉淀
(4)
(5)C
【详解】(1)中含有,与氨水发生酸碱中和反应,与反应生成,发生反应的方程式分别为:和;
(2)中含有,加入新制氢氧化铜溶液,可以发生酸碱中和反应,现象为蓝色的悬浊液变为蓝色溶液,反应的化学方程式为:;
(3)中含有,甲酸中含有醛基,具有还原性,将新制氢氧化铜还原为砖红色的沉淀,反应方程式为:;
(4)中含有,与银氨溶液发生银镜反应,反应方程式为:;
(5)A.甲酸与甲醛均含有醛基,与新制的反应产生砖红色沉淀,A错误;
B.甲酸与甲醛均含有醛基,二者均可发生银镜,B错误;
C.试液与足量溶液反应,生成沸点高的甲酸钠溶液,这时蒸馏,得到低沸点的甲醛,可用银氨溶液或新制的加以鉴定,C正确;
D.将试液进行酯化反应,由于酯化反应是可逆反应,生成物中还是含有甲酸,并且生成的甲酸酯中也含有醛基,因而无法鉴别,D错误;
故选C。
17.(1)C17H23NO5
(2) 取代反应(水解反应)
(3)
(4)②④
【详解】(1)由A的结构可知,A的分子式为C17H23NO5;
(2)A中含有酯基,在NaOH水溶液中加热发生水解反应得到B和C,C是芳香化合物,则B的结构简式为,C的结构简;
(3)C用稀盐酸酸化得到E,则C中-COONa转化为-COOH,则E的结构简式为;
(4)E的结构为,含有羧基、羟基,KMnO4可以氧化醇羟基,羧基具有酸性,可与Na2CO3反应生成CO2和H2O,因此②④不发生反应,故选②④。
18. C2H2O2 18 210 C6H10O8
【分析】有机物的碳和氢燃烧后生成CO2和H2O,所以两种有机物在分子组成上相差n个“CO2”或“H2O”原子团时,完全燃烧的耗氧量是相同的。
C、H、O元素组成的有机物,燃烧时耗O2和生成CO2的体积比为3:4,即有机物和3O2反应可以得到4CO2,相当于4个碳原子需要氧气分子提供6个氧原子,则有机物自身需要提供8-6=2个氧原子,也就是相当于有机物中每2个碳原子自身提供1氧原子,故则这类有机物的通式可写为[(C2O)m(H2O)n],据此分析可得结论。
【详解】(1)相对分子质量最小的物质应是通式中m=1,n=1的物质,此时其分子式为:C2H2O2;故答案为C2H2O2;
(2)若两有机物碳原子数相同,则在通式中m值相同,若其相对分子质量不同,必是n不同;若a(3)此化合物有两个羧基,则为二元酸,因1mol二元酸可中和2molNaOH,根据此类关系式可求得二元酸物质的量为:n=25.00×10-3L×0.1000 moL·L-1÷2=1.250×10-3mol。则此二元羧酸的相对分子质量为M==210;
在通式中(C2O)的式量为40,(H2O)的式量为18,即:210=40m+18n;则(H2O)n中只有当n=5时,m才能是正整数,令n=5时,m=(210-90)÷40=3,得此二元羧酸的分子式为[(C2O)3,(H2O)5],即:C6H10O8。故答案为210、C6Hl0O8。
19.(1)CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O。
(2)B
(3)防止倒吸
(4)吸收乙酸,溶解乙醇。降低乙酸乙酯的溶解度,也便于观察液体分层
【解析】(1)
乙酸与乙醇 在浓硫酸存在的条件下加热发生酯化反应,生成乙酸乙酯和水,其反应的方程式为:CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,故答案:CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O。
(2)
实验过程中圆底烧瓶需要加热,烧瓶内液体的总体积约为18.5mL,根据圆底烧瓶盛液量一般不少于不超过其容积的关系可知B的容积最合适的是50mL,故答案:50mL。
(3)
球形干燥管的主要作用是防止倒吸,故答案:防止倒吸。
(4)
预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是为了吸收乙酸,溶解乙醇。降低乙酸乙酯的溶解度,也便于观察液体分层。故答案:吸收乙酸,溶解乙醇。降低乙酸乙酯的溶解度,也便于观察液体分层。
20.(1)直形冷凝管
(2) 防止暴沸 B
(3)
(4) 检漏 上口倒出
(5)干燥(或除水除醇)
(6)CD
(7)C
【分析】(1)
装置b的名称是直形冷凝管,可用于冷凝回流。故答案为:直形冷凝管;
(2)
加入碎瓷片的作用是防止有机物在加热时发生暴沸。如果在加热时发现忘记加碎瓷片,这时必须停止加热,待冷却后补加碎瓷片。故答案为:防止暴沸;B;
(3)
醇分子间最容易发生脱水反应生成醚类化合物,本实验中最容易产生的副产物的结构简式为。故答案为:;
(4)
分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”)。故答案为:检漏;上口倒出;
(5)
加入无水氯化钙的目的:除去水(做干燥剂)和除去环己醇(因为乙醇可以和氯化钙反应,类比推知,环己醇和氯化钙也可以反应)。分离提纯过程中加入无水氯化钙的目的是干燥(或除水除醇)。故答案为:干燥(或除水除醇);
(6)
观察题中实验装置图知蒸馏过程中不可能用到吸滤瓶及球形冷凝管。故答案为:CD;
(7)
20 g环己醇的物质的量为=0.2 mol,理论上生成环己烯的物质的量为0.2 mol,环己烯的质量为0.2 mol×82 g·mol-1=16.4 g,实际得到环己烯的质量为10 g,则产率为×100%≈61%。故答案为:C。
答案第1页,共2页
答案第1页,共2页
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.具有解热镇痛及抗生素作用的药物“芬必得”主要成分的结构简式如图,它属于
①芳香族化合物②脂肪族化合物③有机羧酸④有机高分子化合物⑤芳香烃
A.③⑤ B.②③ C.①③ D.①④
2.人造海绵的主要成分是聚氨酯,合成方法如图,下列说法不正确的是
+nHOCH2CH2OH→
A.M的分子式为C15H10N2O2
B.聚氨酯和蛋白质分子的某些化学性质相似
C.聚氨酯在一定条件下能发生水解反应
D.合成聚氨酯的反应属于缩聚反应
3.已知。现有A、B、C、D、E、F六种有机物有如下转化关系,其中A的分子式为C4H8O3。下列判断正确的是
A.有机物A结构可能有四种
B.反应①属于氧化反应
C.有机物B、D的最简式相同
D.有机物E是交警检测酒驾的重要物证
4.用括号内的试剂和分离方法除去下列物质中的少量杂质,不正确的是
A.乙酸乙酯中混有乙酸(饱和溶液,分液)
B.乙醇中混有乙酸(NaOH溶液,蒸馏)
C.甲烷中混有乙烯(溴的四氯化碳溶液,分液)
D.溴苯中混有溴(NaOH溶液,分液)
5.下列5种有机化合物中,能够发生酯化、加成和氧化3种类型反应的是
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH3CH2CH2OH ⑤CH3CH(OH)CH2CHO
A.①③④ B.②④⑤ C.①③⑤ D.①②⑤
6.PBT是最坚韧的工程热塑性塑料之一,它是半结晶材料,有非常好的化学稳定性、机械强度、电绝缘性和热稳定性,其结构简式为,下列叙述错误的是
A.PBT可以反复加热熔融加工
B.PBT的单体是对苯二甲酸和1,4-丁二醇
C.由单体合成PBT的反应属于缩聚反应
D.1mol PBT与NaOH 溶液反应时,最多可消耗2mol NaOH溶液
7.实验室用乙酸、乙醇和浓硫酸制取乙酸乙酯的装置如图。下列说法中,不正确的是
A.右侧试管中导管不伸入液面下,是为了防止倒吸
B.实验前先加入浓硫酸,再缓缓加入乙醇和冰醋酸
C.及时将乙酸乙酯蒸出,促进平衡向正反应方向移动
D.饱和Na2CO3溶液可除去产品中混有的乙酸、乙醇
8.下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏;
③除去苯中混有的少量甲苯:加入浓溴水后分液;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A.①② B.②④ C.③④ D.②③
9.下列物质中不属于羧酸类有机物的是
A. B. C. D.
10.茉莉醛具有浓郁的茉莉花香,其结构简式如图所示,下列叙述正确的是
A.茉莉醛与苯甲醛互为同系物
B.在一定条件下,1 mol茉莉醛最多可以与4 mol H2发生加成反应
C.茉莉醛的分子式为C14H18O,一定条件下可以发生氧化反应、还原反应、酯化反应等
D.理论上,202 g茉莉醛能与足量的银氨溶液反应生成216 g单质银
11.某甲酸溶液中可能含有少量甲醛,用下列方法可以证明的是
A.加入新制的并加热,有砖红色沉淀产生,则含甲醛
B.加入银氨溶液并水浴加热,若能产生银镜,则含甲醛
C.先将试液充分进行酯化反应,收集生成物进行银镜反应,若有银镜产生,则含甲醛
D.将该溶液与足量溶液混合后蒸馏,若其蒸馏产物可发生银镜反应,则含甲醛
12.实验室制备和纯化乙酸乙酯的相关装置如下图所示(加热及夹持装置已略去),下列关于该实验的说法正确的是
A.图1装置中,球形冷凝管的主要作用是冷凝、回流,冷凝水从下口通入
B.加热图1装置后,发现未加碎瓷片,应立即停止加热并趁热补加
C.图2装置中的冷凝管也可以换成图1装置中的球形冷凝管
D.图2装置中温度计水银球的位置不正确,应伸入液体中
13.我国科学家利用PCBO与醛或酮通过环加成反应合成了具有生物活性的多官能团化合物M()。下列关于M的说法错误的是
A.分子中所有的碳原子有可能处于同一平面上
B.分子中苯环上的一氯代物共有7种(不考虑立体异构)
C.可使酸性高锰酸钾溶液褪色
D.分子中含有三种官能团
14.为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法均正确的一组是
选项 待提纯的物质 除杂试剂 分离方法
A 乙酸乙酯(乙酸) 溶液 分液
B 蒸馏
C 甲苯() 水 分液
D () 萃取
A.A B.B C.C D.D
15.取一定量的有机物和足量反应得到,取另一份等物质的量的同种有机物和足量反应得到,若在同温同压下,,则该有机物可能是
①②HOOC-COOH③CH3CH2COOH④⑤
A.② B.②③④ C.④ D.①
二、填空题
16.由于甲酸的特殊结构(下图),使其表现特有的性质,完成下面各小题:
(1)蜂、蝎子都会分泌蚁酸,被蜂、蝎子蛰咬可涂抹稀氨水、小苏打水缓解疼痛,上述反应的化学方程式为_________、_________。
(2)甲酸中加入新制氢氧化铜溶液,可能的现象:_____,反应的化学方程式:______。
(3)若在新制氢氧化铜溶液中滴入少量甲酸并加热,产生砖红色沉淀,其原因_________,反应的化学方程式:_________。
(4)写出甲酸与银氨溶液反应的化学方程式:_________。
(5)某甲酸溶液中可能存在着甲醛,下列操作能正确说明的是 。
A.加入新制的Cu(OH)2加热,有砖红色沉淀生成,证明一定存在甲醛
B.能发生银镜反应,证明含甲醛
C.试液与足量NaOH溶液混合,其蒸馏产物可发生银镜反应,则有甲醛
D.先将试液充分进行酯化反应,收集生成物进行银镜反应,有银镜产生,则含甲醛
17.某有机化合物A的结构简式如下:
(1)A的分子式是_________。
(2)A在溶液中加热反应得到B和C,C分子含有苯环。B和C的结构简式是:B_________,C_________。该反应属于_________反应。
(3)室温下,C用稀盐酸酸化得到E,E的结构简式是_________。
(4)下列物质中,不能与E发生化学反应的是_________(填写序号)。
①酸性溶液 ②溶液 ③溶液 ④丁烷
三、计算题
18.现有一些只含C、H、O三种元素的有机物,它们燃烧时消耗的O2和生成的CO2的体积比是3:4。
(1)这些有机物中,相对分子质量最小的化合物的分子式是_______________。
(2)某两种碳原子数相同的上述有机物,若它们的相对分子质量分别为a和b(a
四、实验题
19.乙酸乙酯是一种用途广泛的精细化工产品。某课外小组设计实验室制取乙酸乙酯的方案如下:
已知:①无水氯化钙可与乙醇形成CaCl2·6C2H5OH。
②有关有机物的沸点:
有机物 乙醚 乙醇 乙酸 乙酸乙酯
沸点/℃ 34.5 79 118 77.1
③2CH3CH2OHCH3CH2OCH2CH3+H2O。
制备过程:
装置如图所示,A中盛有浓硫酸,B中盛有9.5 mL无水乙醇和6 mL冰醋酸,D中盛有饱和碳酸钠溶液。
(1)写出乙酸与乙醇发生酯化反应的化学方程式:_______。
(2)实验过程中滴加大约3 mL浓硫酸,B的容积最合适的是_______(填字母)。A.25 mL B.50 mL C.250 mL D.500 mL
(3)球形干燥管的主要作用是_______。
(4)预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是_______。
20.醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
可能用到的有关数据如下:
相对分子质量 密度/ g·cm-3 沸点/℃ 溶解性
环己醇 100 0.961 8 161 微溶于水
环己烯 82 0.810 2 83 难溶于水
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是_______。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_______ (填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为_______。
(4)分液漏斗在使用前须清洗干净并_______;在本实验分离过程中,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是_______。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有_______(填字母,下同)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是_______。A.41% B.50% C.61% D.70%
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】由题给结构可知,该有机物含苯环、-COOH,其余结构饱和。
①该有机物含苯环,属于芳香族化合物,①正确;
②含苯环的有机物不属于脂肪族化合物,②错误;
③该有机物含-COOH,属于有机羧酸,③正确;
④该有机物相对分子质量不够大,不属于有机高分子化合物,④错误;
⑤该有机物含O,不属于芳香烃,⑤错误;
综上所述,①③正确,故答案选C。
2.D
【详解】A.根据M的结构简式,其分子式为C15H10N2O2,A正确;
B.聚氨酯和蛋白质分子中均含有酰胺基,则某些化学性质相似,如水解,B正确;
C.聚氨酯中含有酯基和酰胺基,在一定条件下能发生水解反应,C正确;
D.合成聚氨酯的反应中,M中的碳氮双键与乙二醇中羟基的H原子、O原子发生加成反应,属于加成聚合反应,D错误;
故选D。
3.D
【分析】由B与新制反应生成C,再结合A的分子式可推知B为、C为、D为、E为;由B的结构简式、题给已知反应,结合A的分子式C4H8O3,可知A为。
【详解】A.A为,只有一种结构,A错误;
B.反应①中,CH3CHO发生还原反应生成,B错误;
C.和的最简式不同,C错误;
D.检测酒驾就是检测的含量,D正确;
故选D。
4.C
【详解】A.用饱和Na2CO3溶液除去乙酸乙酯中的乙酸,然后使用分液的方法分离有机层和水层,A正确;
B.氢氧化钠和乙醇不反应,和乙酸生成乙酸钠,然后利用乙醇沸点较低的性质,蒸馏得到乙醇,B正确;
C.溴可以和乙烯反应而进入溶液,甲烷为气体逸出,不需分液,C错误;
D.氢氧化钠和溴苯不反应、和溴反应生成盐溶液,然后使用分液的方法分离有机层和水层,D正确;
故选C。
5.C
【详解】①CH2=CHCOOH中含碳碳双键可发生氧化、加成反应,含-COOH可发生酯化反应,故选;
②CH2=CHCOOCH3中含碳碳双键可发生氧化、加成反应,不能发生酯化反应,故不选;
③CH2=CHCH2OH中含碳碳双键可发生氧化、加成反应,含-OH可发生酯化反应,故选;
④CH3CH2CH2OH不能发生加成反应,故不选;
⑤CH3CH(OH)CH2CHO中含-CHO可发生氧化、加成反应,含-OH可发生酯化反应,故选;
故选C。
6.D
【详解】A.由于该塑料属于线性结构,故PBT具有热塑性,受热会熔化,A正确;
B.PBT 的单体有对苯二甲酸和1,4-丁二醇HOCH2CH2CH2CH2OH两种,B正确;
C.和HOCH2CH2CH2CH2OH生成和水,属于缩聚反应,C正确;
D.由题干的结构简式可知,1 mol PBT与NaOH溶液反应时,最多可消耗2n mol NaOH溶液,D错误;
故答案为:D。
7.B
【详解】A.制取的乙酸乙酯中常常混有乙醇、乙酸,产物通入饱和碳酸钠溶液中以除去,但乙酸与碳酸钠较快反应、乙醇极易溶于水,会发生倒吸,所以试管中导管不伸入液面下,故A正确;
B.浓硫酸密度较大、吸水放热,所以混合时先加密度小的乙醇,再加密度大的浓硫酸,且最后加冰醋酸,试剂顺序不能颠倒,故B错误;
C.乙醇、乙酸转化为乙酸乙酯的反应为可逆反应,及时将乙酸乙酯蒸出,促进平衡向正反应方向移动,提高产率,故C正确;
D.饱和碳酸钠作用是吸收乙醇、除去乙酸,使乙酸乙酯分层,然后采用分液法将乙酸乙酯从混合物中分离出来,故D正确;
故选B。
8.B
【详解】①光照条件下通入Cl2,会和乙烷反应,无法除去乙烷中的乙烯,错误;
②饱和碳酸钠溶液可以和乙酸反应,而且乙酸乙酯在其中溶解度很小,所以可以用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏除去乙酸乙酯中的乙酸,正确;
③甲苯和浓溴水反应生成的三溴甲苯会溶于苯,无法分液除去,错误;
④乙酸和生石灰反应生成乙酸钙,然后蒸馏出乙醇,故可除去乙醇中的乙酸,正确;
综上,故选B。
9.D
【详解】乙二酸、苯甲酸和丙烯酸中均含有羧基,属于羧酸类,苯酚属于酚类,故选D。
10.D
【详解】A.茉莉醛中含有的官能团为碳碳双键、醛基,苯甲醛中含有的官能团为醛基,二者含有的官能团不完全相同,二者的结构不相似,因此二者不能互为同系物,A错误;
B.茉莉醛中分子中含有一个苯环、一个碳碳双键、一个醛基都能与氢气发生加成反应,1 mol茉莉醛最多能与3 mol+1 mol+1 mol=5 mol的H2发生加成反应,B错误;
C.由结构简式可知茉莉醛的分子式为C14H18O,其分子中含醛基,因此该物质能够发生氧化反应;也可以与氢气发生还原反应;物质分子中无羟基或羧基,因此不能发生酯化反应,C错误;
D.202 g茉莉醛的物质的量,物质分子中含有1 mol醛基,可与银氨溶液反应得到2 mol Ag,即生成单质银的质量为m(Ag)=2 mol×108 g/mol=216 g,D正确;
故合理选项是D。
11.D
【详解】甲酸和甲醛都含有醛基,则直接加入新制的氢氧化铜或银氨溶液不能证明是否含有甲醛,应先加入足量溶液,甲酸与氢氧化钠溶液反应生成难挥发的甲酸钠,然后蒸馏,将可能存在的甲醛蒸出,再用银氨溶液或新制的氢氧化铜检验蒸馏出的产物,故选D。
12.A
【详解】A.乙酸、乙醇等有机物均易挥发,则图1装置中,球形冷凝管的主要作用是冷凝、回流,冷凝水从下口通入,故A正确;
B.加热题图1装置后,发现未加碎瓷片,应立即停止加热,待冷却后,再补加碎瓷片,故B错误;
C.若题图2装置中的直形冷凝管换成球形冷凝管,不利于冷凝液体顺利流下进入锥形瓶,故C错误;
D.蒸馏时温度计水银球应在蒸馏烧瓶支管口处,故D错误;
答案选A。
13.A
【详解】A.M分子中存在连有3个碳原子的饱和碳原子,因此所有的碳原子不可能处于同一平面上,A项错误;
B.M分子中苯环上有7种不同化学环境的氢原子,如图:,故其苯环上的一氯代物共有7种,B项正确;
C.M中含有碳碳双键,能使酸性高锰酸钾溶液褪色,C项正确;
D.由M的结构可知,其分子中含有酯基、羟基、碳碳双键三种官能团,D项正确;
答案选A。
14.B
【详解】A.乙酸乙酯也能和氢氧化钠溶液反应,应该用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,A项错误;
B.氧化钙和水反应生成氢氧化钙,然后蒸馏即可得到乙醇,B项正确;
C.溴单质易溶于有机溶剂,应该用氢氧化钠溶液除去甲苯中的溴单质,C项错误;
D.溴单质和苯都易溶于四氯化碳,应该用氢氧化钠溶液除去苯中的溴单质,D项错误;
答案选B。
15.D
【详解】只能与反应产生;既能与反应产生,又能与反应产生,题中四种物质各取时分别与足量或反应所得气体的物质的量如表:
物质() 与足量反应生产的量() 与足量反应生产的量()
① 1 1
② 1 2
③ 0.5 1
④ 1.5 2
⑤ 1 0
故答案为:D。
16.(1)
(2) 蓝色的悬浊液变为蓝色溶液
(3) 甲酸中含有醛基,具有还原性,将新制氢氧化铜还原为砖红色的沉淀
(4)
(5)C
【详解】(1)中含有,与氨水发生酸碱中和反应,与反应生成,发生反应的方程式分别为:和;
(2)中含有,加入新制氢氧化铜溶液,可以发生酸碱中和反应,现象为蓝色的悬浊液变为蓝色溶液,反应的化学方程式为:;
(3)中含有,甲酸中含有醛基,具有还原性,将新制氢氧化铜还原为砖红色的沉淀,反应方程式为:;
(4)中含有,与银氨溶液发生银镜反应,反应方程式为:;
(5)A.甲酸与甲醛均含有醛基,与新制的反应产生砖红色沉淀,A错误;
B.甲酸与甲醛均含有醛基,二者均可发生银镜,B错误;
C.试液与足量溶液反应,生成沸点高的甲酸钠溶液,这时蒸馏,得到低沸点的甲醛,可用银氨溶液或新制的加以鉴定,C正确;
D.将试液进行酯化反应,由于酯化反应是可逆反应,生成物中还是含有甲酸,并且生成的甲酸酯中也含有醛基,因而无法鉴别,D错误;
故选C。
17.(1)C17H23NO5
(2) 取代反应(水解反应)
(3)
(4)②④
【详解】(1)由A的结构可知,A的分子式为C17H23NO5;
(2)A中含有酯基,在NaOH水溶液中加热发生水解反应得到B和C,C是芳香化合物,则B的结构简式为,C的结构简;
(3)C用稀盐酸酸化得到E,则C中-COONa转化为-COOH,则E的结构简式为;
(4)E的结构为,含有羧基、羟基,KMnO4可以氧化醇羟基,羧基具有酸性,可与Na2CO3反应生成CO2和H2O,因此②④不发生反应,故选②④。
18. C2H2O2 18 210 C6H10O8
【分析】有机物的碳和氢燃烧后生成CO2和H2O,所以两种有机物在分子组成上相差n个“CO2”或“H2O”原子团时,完全燃烧的耗氧量是相同的。
C、H、O元素组成的有机物,燃烧时耗O2和生成CO2的体积比为3:4,即有机物和3O2反应可以得到4CO2,相当于4个碳原子需要氧气分子提供6个氧原子,则有机物自身需要提供8-6=2个氧原子,也就是相当于有机物中每2个碳原子自身提供1氧原子,故则这类有机物的通式可写为[(C2O)m(H2O)n],据此分析可得结论。
【详解】(1)相对分子质量最小的物质应是通式中m=1,n=1的物质,此时其分子式为:C2H2O2;故答案为C2H2O2;
(2)若两有机物碳原子数相同,则在通式中m值相同,若其相对分子质量不同,必是n不同;若a
在通式中(C2O)的式量为40,(H2O)的式量为18,即:210=40m+18n;则(H2O)n中只有当n=5时,m才能是正整数,令n=5时,m=(210-90)÷40=3,得此二元羧酸的分子式为[(C2O)3,(H2O)5],即:C6H10O8。故答案为210、C6Hl0O8。
19.(1)CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O。
(2)B
(3)防止倒吸
(4)吸收乙酸,溶解乙醇。降低乙酸乙酯的溶解度,也便于观察液体分层
【解析】(1)
乙酸与乙醇 在浓硫酸存在的条件下加热发生酯化反应,生成乙酸乙酯和水,其反应的方程式为:CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,故答案:CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O。
(2)
实验过程中圆底烧瓶需要加热,烧瓶内液体的总体积约为18.5mL,根据圆底烧瓶盛液量一般不少于不超过其容积的关系可知B的容积最合适的是50mL,故答案:50mL。
(3)
球形干燥管的主要作用是防止倒吸,故答案:防止倒吸。
(4)
预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是为了吸收乙酸,溶解乙醇。降低乙酸乙酯的溶解度,也便于观察液体分层。故答案:吸收乙酸,溶解乙醇。降低乙酸乙酯的溶解度,也便于观察液体分层。
20.(1)直形冷凝管
(2) 防止暴沸 B
(3)
(4) 检漏 上口倒出
(5)干燥(或除水除醇)
(6)CD
(7)C
【分析】(1)
装置b的名称是直形冷凝管,可用于冷凝回流。故答案为:直形冷凝管;
(2)
加入碎瓷片的作用是防止有机物在加热时发生暴沸。如果在加热时发现忘记加碎瓷片,这时必须停止加热,待冷却后补加碎瓷片。故答案为:防止暴沸;B;
(3)
醇分子间最容易发生脱水反应生成醚类化合物,本实验中最容易产生的副产物的结构简式为。故答案为:;
(4)
分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”)。故答案为:检漏;上口倒出;
(5)
加入无水氯化钙的目的:除去水(做干燥剂)和除去环己醇(因为乙醇可以和氯化钙反应,类比推知,环己醇和氯化钙也可以反应)。分离提纯过程中加入无水氯化钙的目的是干燥(或除水除醇)。故答案为:干燥(或除水除醇);
(6)
观察题中实验装置图知蒸馏过程中不可能用到吸滤瓶及球形冷凝管。故答案为:CD;
(7)
20 g环己醇的物质的量为=0.2 mol,理论上生成环己烯的物质的量为0.2 mol,环己烯的质量为0.2 mol×82 g·mol-1=16.4 g,实际得到环己烯的质量为10 g,则产率为×100%≈61%。故答案为:C。
答案第1页,共2页
答案第1页,共2页
