专题5第三单元 有机合成设计 同步练习(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题5第三单元 有机合成设计 同步练习(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-15 00:00:00 | ||
图片预览



文档简介
专题5第三单元有机合成设计同步练习
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.某届奥运会上,有个别运动员因服用兴奋剂被取消参赛资格。如图是检测出兴奋剂的某种同系物X的结构,下列关于X的说法正确的是
A.1molX与NaOH溶液反应最多消耗4molNaOH
B.X能使酸性KMnO4溶液褪色,可证明其分子中含有碳碳双键
C.1molX与足量的饱和溴水反应,最多消耗4molBr2
D.X可与NH4HCO3溶液作用产生气泡
2.水杨酸环己酯具有花香气味,可作为香精配方,其合成路线如下:
++H2O
下列说法不正确的是
A.水杨酸的核磁共振氢谱有6组峰
B.水杨酸、水杨酸环己酯都能与FeCl3溶液发生显色反应
C.1 mol水杨酸与浓溴水反应时,最多消耗2 mol Br2
D.1 mol水杨酸环己酯在NaOH溶液中水解时,最多消耗3 mol NaOH
3.香兰素是重要的香料之一,它可由丁香酚经多步反应合成。有关两种化合物的说法错误的是
A.常温下,1mol的丁香酚和香兰素均能与1molBr2发生取代反应
B.两种分子均与Na2CO3溶液反应
C.1mol香兰素最多能与4mol氢气发生加成反应
D.可用高锰酸钾溶液分别检验两种物质中碳碳双键和酚羟基的存在
4.已知:醛或酮可与格氏试剂(R′MgX):
由乙醇合成CH3CH=CHCH3(2-丁烯)的流程如下:
下列说法错误的是
A.③发生氧化反应,⑥发生消去反应
B.M的结构简式为CH3CH2X
C.P的分子式为C4H10O
D.2-丁烯与Br2以1∶1加成可得三种不同产物
5.下图是以秸秆为原料制备某种高分子化合物W的合成路线:
下列有关说法正确的是
A.X具有两种不同的含氧官能团
B.Y可以发生酯化反应和加成反应
C.Y和1,4-丁二醇通过加聚反应生成W
D.W的分子式为C10nH16n+2O4n+1
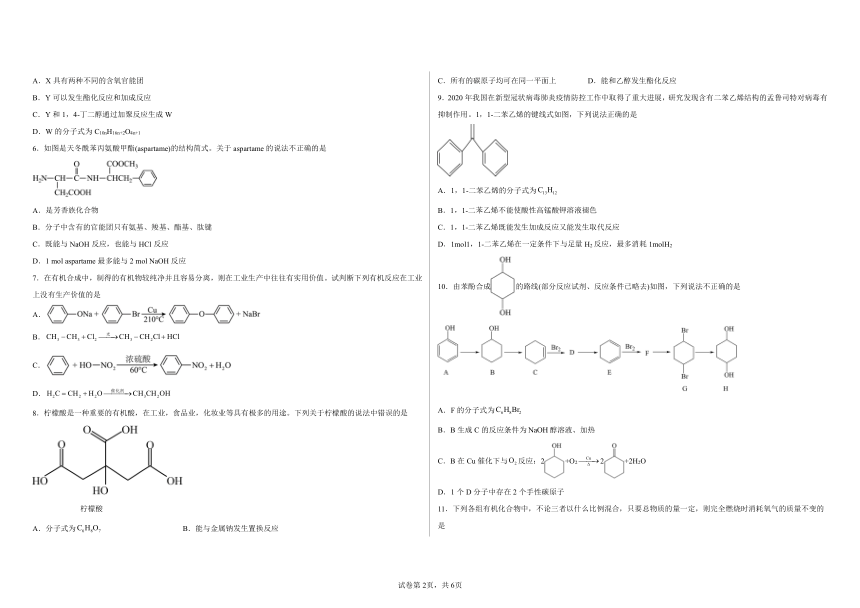
6.如图是天冬酰苯丙氨酸甲酯(aspartame)的结构简式。关于aspartame的说法不正确的是
A.是芳香族化合物
B.分子中含有的官能团只有氨基、羧基、酯基、肽键
C.既能与NaOH反应,也能与HCl反应
D.1 mol aspartame最多能与2 mol NaOH反应
7.在有机合成中,制得的有机物较纯净并且容易分离,则在工业生产中往往有实用价值。试判断下列有机反应在工业上没有生产价值的是
A.
B.
C.
D.
8.柠檬酸是一种重要的有机酸,在工业,食品业,化妆业等具有极多的用途。下列关于柠檬酸的说法中错误的是
柠檬酸
A.分子式为 B.能与金属钠发生置换反应
C.所有的碳原子均可在同一平面上 D.能和乙醇发生酯化反应
9.2020年我国在新型冠状病毒肺炎疫情防控工作中取得了重大进展,研究发现含有二苯乙烯结构的孟鲁司特对病毒有抑制作用。1,1-二苯乙烯的键线式如图,下列说法正确的是
A.1,1-二苯乙烯的分子式为
B.1,1-二苯乙烯不能使酸性高锰酸钾溶液褪色
C.1,1-二苯乙烯既能发生加成反应又能发生取代反应
D.1mol1,1-二苯乙烯在一定条件下与足量H2反应,最多消耗1molH2
10.由苯酚合成的路线(部分反应试剂、反应条件已略去)如图,下列说法不正确的是
A.F的分子式为
B.B生成C的反应条件为醇溶液、加热
C.B在Cu催化下与反应:2+O22+2H2O
D.1个D分子中存在2个手性碳原子
11.下列各组有机化合物中,不论三者以什么比例混合,只要总物质的量一定,则完全燃烧时消耗氧气的质量不变的是
A.,, B.,,
C.,, D.,,
12.MMA()是合成有机玻璃的单体,下面是MMA的两条合成路线(部分反应条件已略去)。
路线一:①+HCN→
②+CH3OH+H2SO4→+NH4HSO4
路线二:
下列有关说法中不正确的是
A.路线一中的副产物对设备具有腐蚀性
B.路线一中涉及的反应全部为加成反应
C.路线二中原子利用率理论上为100%
D.MMA在一定条件下能发生取代反应
13.某有机物A的结构简式如图所示,下列有关叙述正确的是
A.1A最多可以与1发生加成反应
B.一个A分子中最多有12个碳原子在同一平面上
C.1A与足量的溶液反应,最多可以消耗3
D.A能发生消去反应和取代反应,不能发生加成反应
14.波立维是国家引进的新药,它给中风、心肌梗死等疾病患者带来福音。波立维属于硫酸氢盐,它的结构如图所示。下列关于它的说法正确的是
A.该物质的化学式为
B.1该物质最多可与6氢气反应
C.波立维能发生水解反应
D.该有机物可以发生氧化、还原、加成、取代、消去反应
15.已知:①+3Fe+6HCl→ +3FeCl2+2H2O,苯胺极易被氧化;②+CH3Cl+HCl(烷基化反应);③-CH3为邻、对位定位取代基,-NO2、-COOH为间位定位取代基。以苯为原料合成对氨基苯甲酸()理的步骤是
A.苯XYZ对氨基苯甲酸
B.苯XYZ对氨基苯甲酸
C.苯XYZ对氨基苯甲酸
D.苯XYZ对氨基苯甲酸
二、填空题
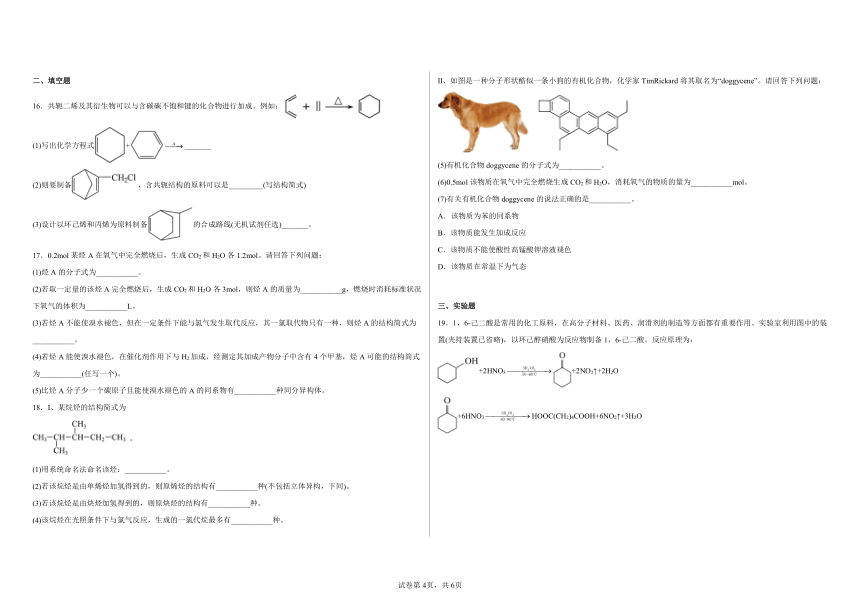
16.共轭二烯及其衍生物可以与含碳碳不饱和键的化合物进行加成。例如:
(1)写出化学方程式+_______
(2)则要制备,含共轭结构的原料可以是_________(写结构简式)
(3)设计以环己烯和丙烯为原料制备的合成路线(无机试剂任选)_______。
17.0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol。请回答下列问题:
(1)烃A的分子式为___________。
(2)若取一定量的该烃A完全燃烧后,生成CO2和H2O各3mol,则烃A的质量为___________g,燃烧时消耗标准状况下氧气的体积为___________L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为___________。
(4)若烃A能使溴水褪色,在催化剂作用下与H2加成,经测定其加成产物分子中含有4个甲基,烃A可能的结构简式为___________(任写一个)。
(5)比烃A分子少一个碳原子且能使溴水褪色的A的同系物有___________种同分异构体。
18.Ⅰ、某烷烃的结构简式为
。
(1)用系统命名法命名该烃:___________。
(2)若该烷烃是由单烯烃加氢得到的,则原烯烃的结构有___________种(不包括立体异构,下同)。
(3)若该烷烃是由炔烃加氢得到的,则原炔烃的结构有___________种。
(4)该烷烃在光照条件下与氯气反应,生成的一氯代烷最多有___________种。
Ⅱ、如图是一种分子形状酷似一条小狗的有机化合物,化学家TimRickard将其取名为“doggycene”。请回答下列问题:
(5)有机化合物doggycene的分子式为___________。
(6)0.5mol该物质在氧气中完全燃烧生成CO2和H2O,消耗氧气的物质的量为___________mol。
(7)有关有机化合物doggycene的说法正确的是___________。
A.该物质为苯的同系物
B.该物质能发生加成反应
C.该物质不能使酸性高锰酸钾溶液褪色
D.该物质在常温下为气态
三、实验题
19.1,6-己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇硝酸为反应物制备1,6-己二酸。反应原理为:
+2HNO3+2NO2↑+2H2O
+6HNO3HOOC(CH2)4COOH+6NO2↑+3H2O
相关物质的物理性质见下表:
试剂 相对分子质量 密度/(g mL-1) 熔点/℃ 沸点/℃ 溶解性
环己醇 100 0.962 25.9 161.8 可溶于水、乙醇、乙醚
1,6-己二酸 146 1.360 152 330.5 微溶于冷水,易溶于乙醇
NH4VO3 117 2.326 210(分解) —— 微溶于冷水,易溶于热水
实验步骤如下:
I.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇。
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕。
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,_______,干燥,得到粗产品。
Ⅳ.1,6-己二酸粗产品的提纯
(1)仪器A的名称为_______,其作用是_______
(2)B中发生反应的离子方程式为_______(其中一种产物为亚硝酸盐)
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为_______。滴加环己醇的过程中,若温度过高,可用冷水浴冷却维持50~60℃,说明该反应的 H_______0(填“>”或“<”)。
(4)将步骤Ⅲ补充完整:_______。步骤IV提纯方法的名称为_______。如图为1,6-己二酸在水中的溶解度曲线,80℃时1,6-己二酸水溶液的密度为ρg mL-1;该溶液的物质的量浓度为_______。
(5)最终得到1,6-己二酸产品4.810g,则1,6-己二酸的产率为_______。
A.46.07% B.57. 08% C.63.03% D.74. 61%
四、有机推断题
20.航天员的航天服采用了很多新型超高性能复合材料。其中聚酰胺纤维M就是一种新型超高性能纤维,它的防热和防火性能十分出色。聚酰胺纤维M的结构简式为
。
下面是聚酰胺纤维M的一种合成路线(部分反应未注明条件):
AB→CDEFM
(1)写出下列反应的反应类型A→B:_______;G+H→M:_______。
(2)生成B的同时还可能生成B的一种同分异构体,其结构简式为_______。
(3)写出E→F的化学方程式:_______。
(4)聚酯纤维P是一种无毒的玩具内充物,其结构简式为。聚酯纤维P可用A和乙烯为原料合成,请你设计并写出其合成路线_______。
提示:①;
②合成过程中无机试剂任选。
21.按下列步骤可由合成(部分试剂和反应条件已略去)。
请回答下列问题:
(1)B、D的结构简式:B_______,D_______。
(2)反应①~⑦中属于消去反应的是_______(填代号)。
(3)根据+Br2,写出在同样条件下CH2=CH—CH=CH2与等物质的量的Br2发生上述加成反应的化学方程式:_______。
(4)写出C→的化学方程式(有机化合物写结构简式,注明反应条件):_______。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A.1 mol X含有3 mol酚羟基,能与3 mol NaOH反应,1 mol Cl水解消耗1 mol NaOH,且生成1 mol酚羟基,又消耗1 mol NaOH,共消耗5 mol NaOH,错误;
B.酚羟基也能使酸性KMnO4溶液褪色,无法证明其分子中含有碳碳双键,错误;
C.苯酚中苯环上的邻对位上的氢易被溴取代,碳碳双键能够与溴发生加成反应;所以1 mol X与足量的饱和溴水反应,最多消耗4 mol Br2,正确;
D.酚羟基与NH4HCO3不反应,错误;
故选C。
2.D
【详解】A.水杨酸中含有6种不同类型的氢原子,故其在核磁共振氢谱中应有6组峰,A正确;
B.水杨酸、水杨酸环己酯均含有酚羟基,可与FeCl3溶液发生显色反应,B正确;
C.溴与水杨酸发生取代时,取代的位置是苯环上酚羟基的邻位和对位,水杨酸的酚羟基邻位与对位能被取代的只有两个位置,所以1mol水杨酸跟足量浓溴水反应时,最多消耗2mol Br2,故C正确;
D.水杨酸中含有1个羧基和一个酚羟基,1 mol水杨酸环己酯水解最多消耗2 mol NaOH,D错误;
故选D。
3.D
【详解】A.苯环上,处于酚羟基的邻对位上的氢易被溴取代,1mol丁香酚和香兰素能发生取代反应需要1mol,A正确;
B.两种分子都含有酚羟基,能与溶液反应(但注意不能生成),正确;
C.1mol香兰素中的苯环与3mol氢气发生加成反应,其中的醛基还要消耗1mol氢气,故最多能与4mol氢气发生加成反应,C正确;
D.香兰素含有羟基和醛基,丁香酚含有羟基和碳碳双键,这些官能团都能使高锰酸钾褪色,D错误;
故选D。
4.D
【分析】依据信息可知,M应为CH3CH2X,N应为CH3CHO,从而得出P为,据此分析解答。
【详解】A.反应③中,CH3CH2OH转化为CH3CHO,发生氧化反应,反应⑥中,转化为CH3CH=CHCH3,发生消去反应,A正确;
B.由以上分析可知,M的结构简式为CH3CH2X,B正确;
C.P的结构简式为,分子式为C4H10O,C正确;
D.2-丁烯与Br2以1∶1加成,只能生成一种产物,D错误;
故选D。
5.D
【详解】A.X中的含氧官能团只有羧基一种,A错误;
B.Y中含有羧基,可以发生酯化反应,但不能发生加成反应,B错误;
C.Y和1,4-丁二醇通过缩聚反应生成W,C错误;
D.据W的结构简式可知其分子式为,D正确;
故选D。
6.D
【详解】A.由于分子中含有苯环,所以属芳香族化合物,A项正确;
B.分子中含有氨基、羧基、酯基和肽键四种官能团,B项正确;
C.羧基能与NaOH反应,氨基能与HCl反应,C项正确;
D.羧基、酯基和肽键都能与NaOH反应,1 mol aspartame最多能与3 mol NaOH反应,D错误;
故选D。
7.B
【详解】A.该反应中生成物较纯净,且容易与NaBr分离,具有生产价值,A错误;
B.该反应中氯气可能与CH3CH2Cl进一步取代生成1,2-二氯乙烷等副产物,产物不纯净,且不易与副产物分离,不具有生产价值,B正确;
C.该反应生成物较为纯净,且容易与H2O分离,具有生产价值,C错误;
D.该反应为加成反应,生成物较为纯净,产物单一,具有生产价值,D错误;
故答案选B。
8.C
【详解】A.该有机物分子中含有6个C原子、7个O原子,不饱和度为3,则分子式为,A正确;
B.该有机物分子中含有的羧基和醇羟基,都能与金属钠发生置换反应,B正确;
C.依据甲烷的结构分析,与醇羟基相连的碳原子,与周围3个碳原子直接相连,4个碳原子中最多只能有3个碳原子共平面,C错误;
D.该有机物分子中含有3个羧基,都能和乙醇发生酯化反应,D正确;
故选C。
9.C
【详解】A.由1,1-二苯乙烯的键线式可知其分子式为,A错误;
B.1,1-二苯乙烯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色,B错误;
C.1,1-二苯乙烯分子中含有碳碳双键和苯环,既能发生加成反应又能发生苯环上的取代反应,C正确;
D.1mol1,1-二苯乙烯在一定条件下与足量H2反应,最多消耗7molH2,D错误;
故选C。
10.B
【分析】A发生加成反应得到B,B发生消去反应得到C,C发生加成反应得到D:;D发生消去反应得到E;E发生1,4-加成反应得到F: ,F与氢气加成得到G,G水解得到H。
【详解】A.F为,分子式为:,A正确;
B.B生成C为醇的消去反应,条件为浓硫酸、加热,B错误;
C.B中与羟基直接相连的碳原子上有1个氢原子,被氧化成羰基,方程式正确,C正确;
D.D为,与溴原子直接相连的碳原子为手性碳原子,共2个,D正确;
故选B。
11.B
【分析】有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为;有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为,有机物总物质的量一定,完全燃烧时消耗氧气的质量不变,说明有机物()分子的与有机物()分子的相同,据此分析判断。
【详解】A.的,的,的,A不符合题意;
B.的,的,的,B符合题意;
C.的,的,的,C不符合题意;
D.的,的,的,D不符合题意;
答案选B。
12.B
【详解】A.路线一中的副产物为,在水溶液中可电离出,显酸性,可腐蚀设备,A正确;
B.线路一中①为加成反应,②中产物不止一种,不是加成反应,B错误;
C.原子利用率100%指反应没有副产物,所有原子均转入目标产物中,路线二无副产物,C正确;
D.MMA中含有酯基,可在酸性或碱性条件下水解,发生取代反应,D正确;
故选B。
13.A
【详解】A.由有机物的结构简式可知,1A中含有1碳碳双键,故最多可以与1发生加成反应,A正确;
B.根据苯环上12原子共平面,乙烯6原子共平面,碳碳单键可以旋转,则一个A分子中最多有11个碳原子在同一平面上,B错误;
C.A分子中含有酚羟基、酚酯基、碳氯键,故1A与足量的溶液反应,最多可以消耗5,C错误;
D.由有机物的结构简式可知,A中含有苯环和碳碳双键,故可以发生加成反应,D错误。
答案选A。
14.C
【详解】A.由题图结构知化学式为,A错误;
B.酯基不能与氢气反应,所以1该物质最多可与5氢气反应,B错误;
C.波立维分子中含有酯基、碳氯键,两种官能团均能发生水解反应,C正确;
D.该有机物不能发生消去反应,D错误;
答案选C。
15.C
【详解】若苯先发生硝化反应,由于硝基是间位定位取代基,再引入甲基时会进入硝基的间位,故应先发生烷基化反应,得到的甲苯发生硝化反应,生成对硝基甲苯;对硝基甲苯先发生氧化反应,将甲基氧化为羧基,若先将硝基还原为氨基,则氧化甲基时氨基容易被氧化。最后再将硝基还原为氨基。所以合理步骤为:苯甲苯对硝基甲苯对硝基苯甲酸对氨基苯甲酸,故选C。
16.(1)
(2)或
(3)
【详解】(1)根据已知反应,共轭双键与双键发生1,4加成,所以+;
(2)根据已知反应,要制备,含共轭结构的原料可能为:或;
(3)根据已知反应,共轭双键与双键发生1,4加成,倒推法,要生成,需要和,苯乙烯为原料,发生反应,总体的合成路线为:。
17.(1)C6H12
(2) 42 100.8
(3)
(4)(CH3)2CHC(CH3)=CH2或
(CH3)2C=C(CH3)2或(CH3)3CCH=CH2
(5)6
【详解】(1)0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol,根据原子守恒确定A分子中C原子数目为6,H原子数目为12,故烃A分子式为C6H12。
(2)根据C原子守恒可知参加反应的烃A的物质的量为0.5mol,故参加反应的烃A的质量为0.5mol×84g·mol-1=42g,故消耗氧气的物质的量为0.5mol×(6+)=4.5mol,标准状况下氧气的体积为4.5mol×22.4L·mol-1=100.8L。
(3)烃A分子式为C6H12,烃A不能使溴水褪色,不含不饱和键,在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,A为环己烷,结构简式为 。
(4)烃A能使溴水褪色,则分子中含有1个碳碳双键,在催化剂作用下与H2加成的产物分子中含有4个甲基,故加成产物的结构简式为 或。若加成产物为,对应的A的结构为(CH3)2CHC(CH3)=CH2或(CH3)2C=C(CH3)2;若加成产物为,对应的A的结构为(CH3)3CCH=CH2。
(5)比烃A分子少一个碳原子且能使溴水褪色的A的同系物的分子式为C5H10,分子中含有1个碳碳双键,符合条件的同分异构体为CH3CH2CH2CH=CH2、CH3CH2CH=CHCH3(存在顺反异构)、CH2=C(CH3)CH2CH3、(CH3)2C=CHCH3、(CH3)2CHCH=CH2,共6种。
18.(1)2,3-二甲基戊烷
(2)5
(3)1
(4)6
(5)C26H26
(6)16.25
(7)B
【详解】(1)该烷烃的系统命名为2,3-二甲基戊烷。
(2)若该烷烃是由单烯烃加氢得到的,则加氢后原双键两端的碳原子上至少各含有1个氢原子,故碳碳双键可能的位置为 ,共有5种。
(3)若该烷烃是由炔烃加氢后得到的,则加氢后原碳碳三键两端的碳原子上至少各含有2个氢原子,故原炔烃只能为 ,只有1种。
(4)由该分子的结构可看出,左端两个甲基连在同一个碳原子上,两个甲基上的氢原子是等效氢原子,其他位置上的氢原子均不等效,故其一氯代烷共有6种。
(5)由doggycene分子的结构简式可知其分子式为C26H26。
(6)由doggycene的分子式为C26H26可得,0.5mol该物质在氧气中完全燃烧生成CO2和H2O,消耗氧气的物质的量为0.5mol×(26+)=16.25mol。
(7)A.因doggycene的分子结构中含有苯环,且只含有C、H元素,因此该物质属于芳香烃,但根据同系物的定义可判断,该物质不属于苯的同系物,A错误;
B.其为不饱和烃,且苯环上有烷基,故其能发生加成反应,B正确;
C.与苯环相连的C上有H,能被高锰酸钾氧化为羧基,从而使酸性高锰酸钾溶液褪色,C错误;
D.因doggycene分子含有26个碳原子,常温下不可能为气态,D错误。
故选B。
19. 球形冷凝管 冷凝回流,减少反应物损失,导出气体 2NO2+2OH =++ H2O 浓硝酸在加热时分解生成NO2 < 用冷水洗涤晶体2~3次 重结晶 2.89ρmol L-1 B
【分析】向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),为了让完全反应,向恒压滴液漏斗中加入6mL环己醇。将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,发生反应:+2HNO3+2NO2↑+2H2O,开始慢慢加入余下的环己醇,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕,将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,发生反应+6HNO3HOOC(CH2)4COOH+6NO2↑+3H2O,实验中的尾气为二氧化氮,用氢氧化钠溶液来吸收,用倒扣的漏斗防止倒吸,由此分析。
【详解】(1)根据仪器A的形状可知,仪器A的名称为球形冷凝管,其作用是冷凝回流,减少反应物损失,导出气体;
(2)B中发生反应为二氧化氮和氢氧化钠的反应,生成硝酸钠、亚硝酸钠和水,离子方程式为2NO2+2OH =++ H2O;
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为浓硝酸具有不稳定性,在加热时分解生成NO2、水和氧气;
滴加环己醇的过程中,若温度过高,可用冷水浴冷却维持50~60℃,说明该反应放热, H<0;
(4)由于1,6-己二酸微溶于冷水,用冷水洗涤晶体2~3次,减少洗涤时的损耗;
将1,6-己二酸粗产品进行提纯提纯,由于1,6-己二酸在冰水中的溶解度小于常温下的水,为了减小损失,步骤IV提纯方法的名称为重结晶;
根据图中1,6-己二酸在水中的溶解度曲线,80℃时1,6-己二酸的溶解度为0.73g,根据质量分数为=42.2%,溶液的密度为ρg mL-1;该溶液的物质的量浓度为=2.89ρmol L-1;
(5)由表中数据可知,6mL环己醇的密度为0.962g mL-1,摩尔质量为100,得到质量为6mL×0.962g mL-1≈5.772g,根据+2HNO3+2NO2↑+2H2O,+6HNO3HOOC(CH2)4COOH+6NO2↑+3H2O,得到~~HOOC(CH2)4COOH,设HOOC(CH2)4COOH的质量的x,,计算得到HOOC(CH2)4COOH的理论质量为8.427g,最终得到1,6-己二酸产品4.810g,则1,6-己二酸的产率为≈57. 08%。
【点睛】80℃时1,6-己二酸的溶解度为0.73g,计算质量分数时=42.2%,为易错点,要仔细观察题中有效信息。
20.(1) 取代反应 缩聚反应
(2)
(3)+6NaOH+2NaCl+4H2O
(4)
【分析】根据路线D被氧化生成,可以推出A为,与在光照条件下发生取代反应生成B,结构简式为:,在溶液中水解生成C,结构简式为:,在发生氧化生成D,结构简式为:,被氧化生成,与发生取代反应生成E:,在氢氧化钠溶液中发生水解反应和中和反应,最后得到产品M。
【详解】(1)A为,与在光照条件下发生取代反应生成B,结构简式为:;
(2)A→B的转化过程中Cl2有可能与同一个甲基上的氢原子发生二取代,故生成的B的同分异构体的结构简式为;
(3)由M的结构简式可知,E为,由氯代烃在NaOH溶液中发生取代反应和羧酸及酚羟基的性质可写出E→F的化学方程式;
(4)由聚酯纤维P的结构简式可知,它是由乙二醇和对苯二甲酸两种单体发生缩聚反应得到的,结合提示,可利用对二甲苯(原料A)在酸性高锰酸钾溶液条件下氧化生成对苯二甲酸,利用乙烯与卤素单质发生加成反应生成卤代烃,然后水解生成乙二醇,最后由对苯二甲酸与乙二醇缩聚得到聚酯纤维P,合成路线为。
21.(1)
(2)②④
(3)CH2=CH—CH=CH2+Br2
(4)+2NaOH+2NaBr+2H2O
【分析】。
【详解】(1)苯酚先与H2加成变成醇A(),A发生消去反应得到B(),B与Br2发生加成反应得到C(),C发生消去反应生成,在一定条件下与Br2反应生成,再与H2发生加成反应得到D(),D在NaOH的水溶液中发生水解反应得到;
故答案为:;。
(2)根据分析可知②④为消去反应;
故答案为:②④。
(3)根据+Br2,可知CH2=CH—CH=CH2与等物质的量的Br2发生上述加成反应的化学方程式CH2=CH—CH=CH2+Br2;
故答案为:CH2=CH—CH=CH2+Br2。
(4)C→的化学方程式+2NaOH+2NaBr+2H2O;
故答案为:+2NaOH+2NaBr+2H2O。
答案第1页,共2页
答案第1页,共2页
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.某届奥运会上,有个别运动员因服用兴奋剂被取消参赛资格。如图是检测出兴奋剂的某种同系物X的结构,下列关于X的说法正确的是
A.1molX与NaOH溶液反应最多消耗4molNaOH
B.X能使酸性KMnO4溶液褪色,可证明其分子中含有碳碳双键
C.1molX与足量的饱和溴水反应,最多消耗4molBr2
D.X可与NH4HCO3溶液作用产生气泡
2.水杨酸环己酯具有花香气味,可作为香精配方,其合成路线如下:
++H2O
下列说法不正确的是
A.水杨酸的核磁共振氢谱有6组峰
B.水杨酸、水杨酸环己酯都能与FeCl3溶液发生显色反应
C.1 mol水杨酸与浓溴水反应时,最多消耗2 mol Br2
D.1 mol水杨酸环己酯在NaOH溶液中水解时,最多消耗3 mol NaOH
3.香兰素是重要的香料之一,它可由丁香酚经多步反应合成。有关两种化合物的说法错误的是
A.常温下,1mol的丁香酚和香兰素均能与1molBr2发生取代反应
B.两种分子均与Na2CO3溶液反应
C.1mol香兰素最多能与4mol氢气发生加成反应
D.可用高锰酸钾溶液分别检验两种物质中碳碳双键和酚羟基的存在
4.已知:醛或酮可与格氏试剂(R′MgX):
由乙醇合成CH3CH=CHCH3(2-丁烯)的流程如下:
下列说法错误的是
A.③发生氧化反应,⑥发生消去反应
B.M的结构简式为CH3CH2X
C.P的分子式为C4H10O
D.2-丁烯与Br2以1∶1加成可得三种不同产物
5.下图是以秸秆为原料制备某种高分子化合物W的合成路线:
下列有关说法正确的是
A.X具有两种不同的含氧官能团
B.Y可以发生酯化反应和加成反应
C.Y和1,4-丁二醇通过加聚反应生成W
D.W的分子式为C10nH16n+2O4n+1
6.如图是天冬酰苯丙氨酸甲酯(aspartame)的结构简式。关于aspartame的说法不正确的是
A.是芳香族化合物
B.分子中含有的官能团只有氨基、羧基、酯基、肽键
C.既能与NaOH反应,也能与HCl反应
D.1 mol aspartame最多能与2 mol NaOH反应
7.在有机合成中,制得的有机物较纯净并且容易分离,则在工业生产中往往有实用价值。试判断下列有机反应在工业上没有生产价值的是
A.
B.
C.
D.
8.柠檬酸是一种重要的有机酸,在工业,食品业,化妆业等具有极多的用途。下列关于柠檬酸的说法中错误的是
柠檬酸
A.分子式为 B.能与金属钠发生置换反应
C.所有的碳原子均可在同一平面上 D.能和乙醇发生酯化反应
9.2020年我国在新型冠状病毒肺炎疫情防控工作中取得了重大进展,研究发现含有二苯乙烯结构的孟鲁司特对病毒有抑制作用。1,1-二苯乙烯的键线式如图,下列说法正确的是
A.1,1-二苯乙烯的分子式为
B.1,1-二苯乙烯不能使酸性高锰酸钾溶液褪色
C.1,1-二苯乙烯既能发生加成反应又能发生取代反应
D.1mol1,1-二苯乙烯在一定条件下与足量H2反应,最多消耗1molH2
10.由苯酚合成的路线(部分反应试剂、反应条件已略去)如图,下列说法不正确的是
A.F的分子式为
B.B生成C的反应条件为醇溶液、加热
C.B在Cu催化下与反应:2+O22+2H2O
D.1个D分子中存在2个手性碳原子
11.下列各组有机化合物中,不论三者以什么比例混合,只要总物质的量一定,则完全燃烧时消耗氧气的质量不变的是
A.,, B.,,
C.,, D.,,
12.MMA()是合成有机玻璃的单体,下面是MMA的两条合成路线(部分反应条件已略去)。
路线一:①+HCN→
②+CH3OH+H2SO4→+NH4HSO4
路线二:
下列有关说法中不正确的是
A.路线一中的副产物对设备具有腐蚀性
B.路线一中涉及的反应全部为加成反应
C.路线二中原子利用率理论上为100%
D.MMA在一定条件下能发生取代反应
13.某有机物A的结构简式如图所示,下列有关叙述正确的是
A.1A最多可以与1发生加成反应
B.一个A分子中最多有12个碳原子在同一平面上
C.1A与足量的溶液反应,最多可以消耗3
D.A能发生消去反应和取代反应,不能发生加成反应
14.波立维是国家引进的新药,它给中风、心肌梗死等疾病患者带来福音。波立维属于硫酸氢盐,它的结构如图所示。下列关于它的说法正确的是
A.该物质的化学式为
B.1该物质最多可与6氢气反应
C.波立维能发生水解反应
D.该有机物可以发生氧化、还原、加成、取代、消去反应
15.已知:①+3Fe+6HCl→ +3FeCl2+2H2O,苯胺极易被氧化;②+CH3Cl+HCl(烷基化反应);③-CH3为邻、对位定位取代基,-NO2、-COOH为间位定位取代基。以苯为原料合成对氨基苯甲酸()理的步骤是
A.苯XYZ对氨基苯甲酸
B.苯XYZ对氨基苯甲酸
C.苯XYZ对氨基苯甲酸
D.苯XYZ对氨基苯甲酸
二、填空题
16.共轭二烯及其衍生物可以与含碳碳不饱和键的化合物进行加成。例如:
(1)写出化学方程式+_______
(2)则要制备,含共轭结构的原料可以是_________(写结构简式)
(3)设计以环己烯和丙烯为原料制备的合成路线(无机试剂任选)_______。
17.0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol。请回答下列问题:
(1)烃A的分子式为___________。
(2)若取一定量的该烃A完全燃烧后,生成CO2和H2O各3mol,则烃A的质量为___________g,燃烧时消耗标准状况下氧气的体积为___________L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为___________。
(4)若烃A能使溴水褪色,在催化剂作用下与H2加成,经测定其加成产物分子中含有4个甲基,烃A可能的结构简式为___________(任写一个)。
(5)比烃A分子少一个碳原子且能使溴水褪色的A的同系物有___________种同分异构体。
18.Ⅰ、某烷烃的结构简式为
。
(1)用系统命名法命名该烃:___________。
(2)若该烷烃是由单烯烃加氢得到的,则原烯烃的结构有___________种(不包括立体异构,下同)。
(3)若该烷烃是由炔烃加氢得到的,则原炔烃的结构有___________种。
(4)该烷烃在光照条件下与氯气反应,生成的一氯代烷最多有___________种。
Ⅱ、如图是一种分子形状酷似一条小狗的有机化合物,化学家TimRickard将其取名为“doggycene”。请回答下列问题:
(5)有机化合物doggycene的分子式为___________。
(6)0.5mol该物质在氧气中完全燃烧生成CO2和H2O,消耗氧气的物质的量为___________mol。
(7)有关有机化合物doggycene的说法正确的是___________。
A.该物质为苯的同系物
B.该物质能发生加成反应
C.该物质不能使酸性高锰酸钾溶液褪色
D.该物质在常温下为气态
三、实验题
19.1,6-己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇硝酸为反应物制备1,6-己二酸。反应原理为:
+2HNO3+2NO2↑+2H2O
+6HNO3HOOC(CH2)4COOH+6NO2↑+3H2O
相关物质的物理性质见下表:
试剂 相对分子质量 密度/(g mL-1) 熔点/℃ 沸点/℃ 溶解性
环己醇 100 0.962 25.9 161.8 可溶于水、乙醇、乙醚
1,6-己二酸 146 1.360 152 330.5 微溶于冷水,易溶于乙醇
NH4VO3 117 2.326 210(分解) —— 微溶于冷水,易溶于热水
实验步骤如下:
I.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇。
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕。
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,_______,干燥,得到粗产品。
Ⅳ.1,6-己二酸粗产品的提纯
(1)仪器A的名称为_______,其作用是_______
(2)B中发生反应的离子方程式为_______(其中一种产物为亚硝酸盐)
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为_______。滴加环己醇的过程中,若温度过高,可用冷水浴冷却维持50~60℃,说明该反应的 H_______0(填“>”或“<”)。
(4)将步骤Ⅲ补充完整:_______。步骤IV提纯方法的名称为_______。如图为1,6-己二酸在水中的溶解度曲线,80℃时1,6-己二酸水溶液的密度为ρg mL-1;该溶液的物质的量浓度为_______。
(5)最终得到1,6-己二酸产品4.810g,则1,6-己二酸的产率为_______。
A.46.07% B.57. 08% C.63.03% D.74. 61%
四、有机推断题
20.航天员的航天服采用了很多新型超高性能复合材料。其中聚酰胺纤维M就是一种新型超高性能纤维,它的防热和防火性能十分出色。聚酰胺纤维M的结构简式为
。
下面是聚酰胺纤维M的一种合成路线(部分反应未注明条件):
AB→CDEFM
(1)写出下列反应的反应类型A→B:_______;G+H→M:_______。
(2)生成B的同时还可能生成B的一种同分异构体,其结构简式为_______。
(3)写出E→F的化学方程式:_______。
(4)聚酯纤维P是一种无毒的玩具内充物,其结构简式为。聚酯纤维P可用A和乙烯为原料合成,请你设计并写出其合成路线_______。
提示:①;
②合成过程中无机试剂任选。
21.按下列步骤可由合成(部分试剂和反应条件已略去)。
请回答下列问题:
(1)B、D的结构简式:B_______,D_______。
(2)反应①~⑦中属于消去反应的是_______(填代号)。
(3)根据+Br2,写出在同样条件下CH2=CH—CH=CH2与等物质的量的Br2发生上述加成反应的化学方程式:_______。
(4)写出C→的化学方程式(有机化合物写结构简式,注明反应条件):_______。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A.1 mol X含有3 mol酚羟基,能与3 mol NaOH反应,1 mol Cl水解消耗1 mol NaOH,且生成1 mol酚羟基,又消耗1 mol NaOH,共消耗5 mol NaOH,错误;
B.酚羟基也能使酸性KMnO4溶液褪色,无法证明其分子中含有碳碳双键,错误;
C.苯酚中苯环上的邻对位上的氢易被溴取代,碳碳双键能够与溴发生加成反应;所以1 mol X与足量的饱和溴水反应,最多消耗4 mol Br2,正确;
D.酚羟基与NH4HCO3不反应,错误;
故选C。
2.D
【详解】A.水杨酸中含有6种不同类型的氢原子,故其在核磁共振氢谱中应有6组峰,A正确;
B.水杨酸、水杨酸环己酯均含有酚羟基,可与FeCl3溶液发生显色反应,B正确;
C.溴与水杨酸发生取代时,取代的位置是苯环上酚羟基的邻位和对位,水杨酸的酚羟基邻位与对位能被取代的只有两个位置,所以1mol水杨酸跟足量浓溴水反应时,最多消耗2mol Br2,故C正确;
D.水杨酸中含有1个羧基和一个酚羟基,1 mol水杨酸环己酯水解最多消耗2 mol NaOH,D错误;
故选D。
3.D
【详解】A.苯环上,处于酚羟基的邻对位上的氢易被溴取代,1mol丁香酚和香兰素能发生取代反应需要1mol,A正确;
B.两种分子都含有酚羟基,能与溶液反应(但注意不能生成),正确;
C.1mol香兰素中的苯环与3mol氢气发生加成反应,其中的醛基还要消耗1mol氢气,故最多能与4mol氢气发生加成反应,C正确;
D.香兰素含有羟基和醛基,丁香酚含有羟基和碳碳双键,这些官能团都能使高锰酸钾褪色,D错误;
故选D。
4.D
【分析】依据信息可知,M应为CH3CH2X,N应为CH3CHO,从而得出P为,据此分析解答。
【详解】A.反应③中,CH3CH2OH转化为CH3CHO,发生氧化反应,反应⑥中,转化为CH3CH=CHCH3,发生消去反应,A正确;
B.由以上分析可知,M的结构简式为CH3CH2X,B正确;
C.P的结构简式为,分子式为C4H10O,C正确;
D.2-丁烯与Br2以1∶1加成,只能生成一种产物,D错误;
故选D。
5.D
【详解】A.X中的含氧官能团只有羧基一种,A错误;
B.Y中含有羧基,可以发生酯化反应,但不能发生加成反应,B错误;
C.Y和1,4-丁二醇通过缩聚反应生成W,C错误;
D.据W的结构简式可知其分子式为,D正确;
故选D。
6.D
【详解】A.由于分子中含有苯环,所以属芳香族化合物,A项正确;
B.分子中含有氨基、羧基、酯基和肽键四种官能团,B项正确;
C.羧基能与NaOH反应,氨基能与HCl反应,C项正确;
D.羧基、酯基和肽键都能与NaOH反应,1 mol aspartame最多能与3 mol NaOH反应,D错误;
故选D。
7.B
【详解】A.该反应中生成物较纯净,且容易与NaBr分离,具有生产价值,A错误;
B.该反应中氯气可能与CH3CH2Cl进一步取代生成1,2-二氯乙烷等副产物,产物不纯净,且不易与副产物分离,不具有生产价值,B正确;
C.该反应生成物较为纯净,且容易与H2O分离,具有生产价值,C错误;
D.该反应为加成反应,生成物较为纯净,产物单一,具有生产价值,D错误;
故答案选B。
8.C
【详解】A.该有机物分子中含有6个C原子、7个O原子,不饱和度为3,则分子式为,A正确;
B.该有机物分子中含有的羧基和醇羟基,都能与金属钠发生置换反应,B正确;
C.依据甲烷的结构分析,与醇羟基相连的碳原子,与周围3个碳原子直接相连,4个碳原子中最多只能有3个碳原子共平面,C错误;
D.该有机物分子中含有3个羧基,都能和乙醇发生酯化反应,D正确;
故选C。
9.C
【详解】A.由1,1-二苯乙烯的键线式可知其分子式为,A错误;
B.1,1-二苯乙烯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色,B错误;
C.1,1-二苯乙烯分子中含有碳碳双键和苯环,既能发生加成反应又能发生苯环上的取代反应,C正确;
D.1mol1,1-二苯乙烯在一定条件下与足量H2反应,最多消耗7molH2,D错误;
故选C。
10.B
【分析】A发生加成反应得到B,B发生消去反应得到C,C发生加成反应得到D:;D发生消去反应得到E;E发生1,4-加成反应得到F: ,F与氢气加成得到G,G水解得到H。
【详解】A.F为,分子式为:,A正确;
B.B生成C为醇的消去反应,条件为浓硫酸、加热,B错误;
C.B中与羟基直接相连的碳原子上有1个氢原子,被氧化成羰基,方程式正确,C正确;
D.D为,与溴原子直接相连的碳原子为手性碳原子,共2个,D正确;
故选B。
11.B
【分析】有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为;有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为,有机物总物质的量一定,完全燃烧时消耗氧气的质量不变,说明有机物()分子的与有机物()分子的相同,据此分析判断。
【详解】A.的,的,的,A不符合题意;
B.的,的,的,B符合题意;
C.的,的,的,C不符合题意;
D.的,的,的,D不符合题意;
答案选B。
12.B
【详解】A.路线一中的副产物为,在水溶液中可电离出,显酸性,可腐蚀设备,A正确;
B.线路一中①为加成反应,②中产物不止一种,不是加成反应,B错误;
C.原子利用率100%指反应没有副产物,所有原子均转入目标产物中,路线二无副产物,C正确;
D.MMA中含有酯基,可在酸性或碱性条件下水解,发生取代反应,D正确;
故选B。
13.A
【详解】A.由有机物的结构简式可知,1A中含有1碳碳双键,故最多可以与1发生加成反应,A正确;
B.根据苯环上12原子共平面,乙烯6原子共平面,碳碳单键可以旋转,则一个A分子中最多有11个碳原子在同一平面上,B错误;
C.A分子中含有酚羟基、酚酯基、碳氯键,故1A与足量的溶液反应,最多可以消耗5,C错误;
D.由有机物的结构简式可知,A中含有苯环和碳碳双键,故可以发生加成反应,D错误。
答案选A。
14.C
【详解】A.由题图结构知化学式为,A错误;
B.酯基不能与氢气反应,所以1该物质最多可与5氢气反应,B错误;
C.波立维分子中含有酯基、碳氯键,两种官能团均能发生水解反应,C正确;
D.该有机物不能发生消去反应,D错误;
答案选C。
15.C
【详解】若苯先发生硝化反应,由于硝基是间位定位取代基,再引入甲基时会进入硝基的间位,故应先发生烷基化反应,得到的甲苯发生硝化反应,生成对硝基甲苯;对硝基甲苯先发生氧化反应,将甲基氧化为羧基,若先将硝基还原为氨基,则氧化甲基时氨基容易被氧化。最后再将硝基还原为氨基。所以合理步骤为:苯甲苯对硝基甲苯对硝基苯甲酸对氨基苯甲酸,故选C。
16.(1)
(2)或
(3)
【详解】(1)根据已知反应,共轭双键与双键发生1,4加成,所以+;
(2)根据已知反应,要制备,含共轭结构的原料可能为:或;
(3)根据已知反应,共轭双键与双键发生1,4加成,倒推法,要生成,需要和,苯乙烯为原料,发生反应,总体的合成路线为:。
17.(1)C6H12
(2) 42 100.8
(3)
(4)(CH3)2CHC(CH3)=CH2或
(CH3)2C=C(CH3)2或(CH3)3CCH=CH2
(5)6
【详解】(1)0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol,根据原子守恒确定A分子中C原子数目为6,H原子数目为12,故烃A分子式为C6H12。
(2)根据C原子守恒可知参加反应的烃A的物质的量为0.5mol,故参加反应的烃A的质量为0.5mol×84g·mol-1=42g,故消耗氧气的物质的量为0.5mol×(6+)=4.5mol,标准状况下氧气的体积为4.5mol×22.4L·mol-1=100.8L。
(3)烃A分子式为C6H12,烃A不能使溴水褪色,不含不饱和键,在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,A为环己烷,结构简式为 。
(4)烃A能使溴水褪色,则分子中含有1个碳碳双键,在催化剂作用下与H2加成的产物分子中含有4个甲基,故加成产物的结构简式为 或。若加成产物为,对应的A的结构为(CH3)2CHC(CH3)=CH2或(CH3)2C=C(CH3)2;若加成产物为,对应的A的结构为(CH3)3CCH=CH2。
(5)比烃A分子少一个碳原子且能使溴水褪色的A的同系物的分子式为C5H10,分子中含有1个碳碳双键,符合条件的同分异构体为CH3CH2CH2CH=CH2、CH3CH2CH=CHCH3(存在顺反异构)、CH2=C(CH3)CH2CH3、(CH3)2C=CHCH3、(CH3)2CHCH=CH2,共6种。
18.(1)2,3-二甲基戊烷
(2)5
(3)1
(4)6
(5)C26H26
(6)16.25
(7)B
【详解】(1)该烷烃的系统命名为2,3-二甲基戊烷。
(2)若该烷烃是由单烯烃加氢得到的,则加氢后原双键两端的碳原子上至少各含有1个氢原子,故碳碳双键可能的位置为 ,共有5种。
(3)若该烷烃是由炔烃加氢后得到的,则加氢后原碳碳三键两端的碳原子上至少各含有2个氢原子,故原炔烃只能为 ,只有1种。
(4)由该分子的结构可看出,左端两个甲基连在同一个碳原子上,两个甲基上的氢原子是等效氢原子,其他位置上的氢原子均不等效,故其一氯代烷共有6种。
(5)由doggycene分子的结构简式可知其分子式为C26H26。
(6)由doggycene的分子式为C26H26可得,0.5mol该物质在氧气中完全燃烧生成CO2和H2O,消耗氧气的物质的量为0.5mol×(26+)=16.25mol。
(7)A.因doggycene的分子结构中含有苯环,且只含有C、H元素,因此该物质属于芳香烃,但根据同系物的定义可判断,该物质不属于苯的同系物,A错误;
B.其为不饱和烃,且苯环上有烷基,故其能发生加成反应,B正确;
C.与苯环相连的C上有H,能被高锰酸钾氧化为羧基,从而使酸性高锰酸钾溶液褪色,C错误;
D.因doggycene分子含有26个碳原子,常温下不可能为气态,D错误。
故选B。
19. 球形冷凝管 冷凝回流,减少反应物损失,导出气体 2NO2+2OH =++ H2O 浓硝酸在加热时分解生成NO2 < 用冷水洗涤晶体2~3次 重结晶 2.89ρmol L-1 B
【分析】向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),为了让完全反应,向恒压滴液漏斗中加入6mL环己醇。将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,发生反应:+2HNO3+2NO2↑+2H2O,开始慢慢加入余下的环己醇,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕,将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,发生反应+6HNO3HOOC(CH2)4COOH+6NO2↑+3H2O,实验中的尾气为二氧化氮,用氢氧化钠溶液来吸收,用倒扣的漏斗防止倒吸,由此分析。
【详解】(1)根据仪器A的形状可知,仪器A的名称为球形冷凝管,其作用是冷凝回流,减少反应物损失,导出气体;
(2)B中发生反应为二氧化氮和氢氧化钠的反应,生成硝酸钠、亚硝酸钠和水,离子方程式为2NO2+2OH =++ H2O;
(3)若步骤Ⅱ中控制水浴温度不当,未滴加环己醇前就会观察到红棕色气体生成,原因为浓硝酸具有不稳定性,在加热时分解生成NO2、水和氧气;
滴加环己醇的过程中,若温度过高,可用冷水浴冷却维持50~60℃,说明该反应放热, H<0;
(4)由于1,6-己二酸微溶于冷水,用冷水洗涤晶体2~3次,减少洗涤时的损耗;
将1,6-己二酸粗产品进行提纯提纯,由于1,6-己二酸在冰水中的溶解度小于常温下的水,为了减小损失,步骤IV提纯方法的名称为重结晶;
根据图中1,6-己二酸在水中的溶解度曲线,80℃时1,6-己二酸的溶解度为0.73g,根据质量分数为=42.2%,溶液的密度为ρg mL-1;该溶液的物质的量浓度为=2.89ρmol L-1;
(5)由表中数据可知,6mL环己醇的密度为0.962g mL-1,摩尔质量为100,得到质量为6mL×0.962g mL-1≈5.772g,根据+2HNO3+2NO2↑+2H2O,+6HNO3HOOC(CH2)4COOH+6NO2↑+3H2O,得到~~HOOC(CH2)4COOH,设HOOC(CH2)4COOH的质量的x,,计算得到HOOC(CH2)4COOH的理论质量为8.427g,最终得到1,6-己二酸产品4.810g,则1,6-己二酸的产率为≈57. 08%。
【点睛】80℃时1,6-己二酸的溶解度为0.73g,计算质量分数时=42.2%,为易错点,要仔细观察题中有效信息。
20.(1) 取代反应 缩聚反应
(2)
(3)+6NaOH+2NaCl+4H2O
(4)
【分析】根据路线D被氧化生成,可以推出A为,与在光照条件下发生取代反应生成B,结构简式为:,在溶液中水解生成C,结构简式为:,在发生氧化生成D,结构简式为:,被氧化生成,与发生取代反应生成E:,在氢氧化钠溶液中发生水解反应和中和反应,最后得到产品M。
【详解】(1)A为,与在光照条件下发生取代反应生成B,结构简式为:;
(2)A→B的转化过程中Cl2有可能与同一个甲基上的氢原子发生二取代,故生成的B的同分异构体的结构简式为;
(3)由M的结构简式可知,E为,由氯代烃在NaOH溶液中发生取代反应和羧酸及酚羟基的性质可写出E→F的化学方程式;
(4)由聚酯纤维P的结构简式可知,它是由乙二醇和对苯二甲酸两种单体发生缩聚反应得到的,结合提示,可利用对二甲苯(原料A)在酸性高锰酸钾溶液条件下氧化生成对苯二甲酸,利用乙烯与卤素单质发生加成反应生成卤代烃,然后水解生成乙二醇,最后由对苯二甲酸与乙二醇缩聚得到聚酯纤维P,合成路线为。
21.(1)
(2)②④
(3)CH2=CH—CH=CH2+Br2
(4)+2NaOH+2NaBr+2H2O
【分析】。
【详解】(1)苯酚先与H2加成变成醇A(),A发生消去反应得到B(),B与Br2发生加成反应得到C(),C发生消去反应生成,在一定条件下与Br2反应生成,再与H2发生加成反应得到D(),D在NaOH的水溶液中发生水解反应得到;
故答案为:;。
(2)根据分析可知②④为消去反应;
故答案为:②④。
(3)根据+Br2,可知CH2=CH—CH=CH2与等物质的量的Br2发生上述加成反应的化学方程式CH2=CH—CH=CH2+Br2;
故答案为:CH2=CH—CH=CH2+Br2。
(4)C→的化学方程式+2NaOH+2NaBr+2H2O;
故答案为:+2NaOH+2NaBr+2H2O。
答案第1页,共2页
答案第1页,共2页
