专题5第一单元 卤代烃 同步练习(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题5第一单元 卤代烃 同步练习(含解析)2022——2023学年高中化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 768.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-15 00:00:00 | ||
图片预览




文档简介
专题5第一单元卤代烃同步练习
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.要检验卤代烃中是否含有溴元素,正确的实验方法是
A.加入氯水振荡,观察上层是否有橙色
B.滴加硝酸酸化的AgNO3溶液,观察有无浅黄色沉淀生成
C.滴加NaOH水溶液,加热,然后加入稀硝酸酸化,再滴加AgNO3溶液,观察有无浅黄色沉淀生成
D.滴加NaOH水溶液,然后滴加AgNO3溶液,观察有无浅黄色沉淀生成
2.下列化合物中,既能发生水解反应,又能发生消去反应,且消去反应生成的烯烃只有一种的是
A.CH3Br B.
C. D.
3.下列有关化合物X(结构如图)的叙述正确的是
A.X分子式为
B.X最多可与7mol发生加成反应
C.X在酸性条件下水解的产物均可与溶液反应
D.X可发生消去反应
4.卤代烃在一定条件下可发生消去反应生成烯烃,下图为2-溴丁烷在乙醇钠存在的条件下发生消去反应的产物情况。下列说法不正确的是
A.此条件下的消去反应,生成的2-丁烯的量比1-丁烯多
B.产物A和B互为顺反异构体
C.产物A、B与发生加成反应得到结构相同的产物
D.2-溴丙烷在相同条件下发生消去反应也会有不同结构的产物生成
5.氟利昂-12是甲烷的氯、氟代物,结构式为,下列有关叙述正确的是
A.它只有一种结构 B.它的空间构型是正四面体
C.它常温下是无色液体 D.它溶于水可以电离出氟离子和氯离子
6.用有机物甲可制备环己二烯(),其合成路线如图所示:
甲乙丙
下列有关判断不正确的是
A.甲的分子式为C6H12
B.乙与环己二烯互为同系物
C.反应①②③分别为取代反应、消去反应、加成反应
D.丙的同分异构体中含有六元碳环结构的还有3种
7.从溴乙烷制取1,2 二溴乙烷,下列制备方案中最好的是
A.CH3CH2BrCH3CH2OHCH2=CH2CH2BrCH2Br
B.CH3CH2BrCH2BrCH2Br
C.CH3CH2BrCH2=CH2CH3CH2BrCH2BrCH2Br
D.CH3CH2BrCH2=CH2CH2BrCH2Br
8.已知某有机物的结构如下图所示,下列分析正确的是
A.1 mol该有机物中含有1 mol碳溴键
B.该有机物能发生加成、取代、消去反应
C.1 mol该有机物的单体最多可消耗2mol NaOH
D.该有机物分子中不存在手性碳原子
9.卤代烃能够发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列有机物可以与钠反应合成环丁烷的是
A. B.
C. D.
10.为鉴别卤代烃中所含卤素原子,现有下列实验操作步骤,正确的顺序是
①加入AgNO3溶液 ②加入少许卤代烃试样 ③加热 ④加入5 mL 4 mol·L-1 NaOH溶液 ⑤加入5 mL 4 mol·L-1 HNO3溶液
A.②④③①⑤ B.②③①④⑤ C.②④③⑤① D.②⑤③①④
11.下列“类比”结果正确的是
A.MgCl2溶液低温蒸干得到Mg(OH)2,则FeCl2溶液低温蒸干得到Fe(OH)2
B.NH3与足量盐酸反应生成NH4Cl,则N2H4与足量盐酸反应生成N2H6Cl2
C.少量CO2通入Ca(ClO)2溶液生成CaCO3,则少量CO2通入NaClO溶液生成Na2CO3
D.消去反应条件为浓硫酸,加热,则消去反应条件也为浓硫酸,加热
12.有机物O(2—溴—2—甲基丁烷)存在如图转化关系(P分子中含有两个甲基),下列说法正确的是
A.O的同分异构体中,发生消去反应所得产物有6种
B.P分子中,含有5种不同化学环境的氢原子
C.Q的同分异构体中,含有两个甲基的醇有4种
D.Q的同分异构体中,能被氧化为醛的醇有3种
13.以乙醇、过氧化氢、碘化钠和原料1制备联苯衍生物2的一种反应机理如图。下列说法不正确的是
A.反应过程的催化剂是 B.涉及的有机反应只有取代、消去、还原
C.化合物4和5互为同分异构体 D.反应过程中反应液可能保持不变
14.用如图装置探究1—溴丁烷在氢氧化钠溶液中发生的反应,观察到高锰酸钾酸性溶液褪色。下列分析不正确的是
A.推断烧瓶中可能生成了1—丁醇或1—丁烯
B.用红外光谱可检验在该条件下反应生成有机物中的官能团
C.通过检验反应后烧瓶内溶液中的溴离子,可确定烧瓶内发生的反应类型
D.将试管中溶液改为溴水,若溴水褪色,则烧瓶中一定有消去反应发生
15.称为环氧乙烷,它在一定条件下,能与氢化物发生加成反应,氢原子加到氧原子上,其他部分加到碳原子上。对下面环氧乙烷的衍生物的叙述中,不正确的是
A.在一定条件下能与水反应生成
B.在一定条件下能与水反应生成
C.在一定条件下可以合成甘油
D.加入AgNO3溶液能生成难溶于HNO3的白色沉淀
二、填空题
16.滴滴涕(DDT)是20世纪60年代以前广为应用的一种杀虫剂,它可由氯苯制得,其结构简式为,因其性质稳定、脂溶性好、药效强、适用性广而被大量生产,普遍使用,以致最终造成环境污染。为了杀灭对人类有害的昆虫,而又避免或减少环境污染、破坏生态平衡,化学工作者进行了不懈的努力,研制出多种新型杀虫剂,以代替DDT等农药。例如化合物A就是其中一种,其分子结构如图所示。
请完成下列各题:
(1)化合物A的分子式为_______。
(2)化合物A中的官能团有_______(写名称)。
(3)下列关于DDT的说法中,错误的是_______(填字母)。
A.DDT在杀死害虫的同时,也能杀死有益的生物
B.DDT是一种难溶于水,易溶于有机溶剂的物质
C.DDT的分子式为
D.DDT用于蔬菜杀虫时,在蔬菜中残留时间短,对人体无害
17.体育比赛中,当运动员肌肉挫伤或扭伤时,队医立即对准运动员的受伤部位喷射药剂——氯乙烷(CH3CH2Cl,沸点为12.27℃)进行局部冷冻麻醉应急处理。
(1)写出由乙烯制取氯乙烷的反应的化学方程式:_______。
(2)氯乙烷能用于冷冻麻醉应急处理的原因是_______。
三、实验题
18.某学习小组探究溴乙烷的消去反应并验证产物。
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)实验原理:___________。
(2)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因:____________。
(3)丙同学认为只要对实验装置进行适当改进,即可避免对乙烯气体检验的干扰,改进方法:________。
19.如图是实验室制备溴乙烷的装置(已知溴乙烷的沸点38.4℃)。步骤如下:
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。
请回答下列问题:
(1)已知烧瓶中制备溴乙烷时包含两个反应,写出反应②:
①NaBr+H2SO4=HBr+NaHSO4
②_______________
(2)溴乙烷的水溶性______(填“大于”“等于”或“小于)乙醇的水溶性,其原因是___________。
(3)反应时若温度过高,会有多种有机副产物生成,,写出相应的化学方程式________(任写一个)
(4)反应结束后,U形管中制得的溴乙烷呈棕黄色。为了除去产品中的杂质,可选择下列试剂中的_____填序号)。
A.H2O B.Na2SO3溶液 C.CC14 D.NaOH溶液
除杂所需的主要玻璃仪器是_______(填仪器名称)
(5)检验溴乙烷中溴元素:取少量溴乙烷,然后_______(按正确的操作顺序填序号)。
①加热:②加入AgNO3溶液:③加入稀HNO3酸化; ④冷却;⑤加入NaOH溶液
四、有机推断题
20.化合物G是制备抗HIV药物阿扎那韦的关键中间体,其一种合成路线如图:
已知:BoC-表示。
(1)A分子中含有的官能团名称为____。
(2)E→F的反应类型为____。
(3)G每个分子中含有手性碳原子的数目为____。
(4)设计以为原料制备的合成路线(无机试剂和上述合成路线中的有机试剂任用,合成路线示例见本题题干)____。
21.根据题中信息回答问题:
(1)有机物A的实验式为C2H4O,质谱图和主要碎片的归属如图所示。则有机物A的相对分子质量是___,该有机物的结构简式为___。
(2)某有机物结构简式如图所示,则用足量的Na、NaOH、NaHCO3、浓溴水分别与等物质的量的该有机物反应时,消耗Na、NaOH、NaHCO3和Br2的物质的量之比为___。
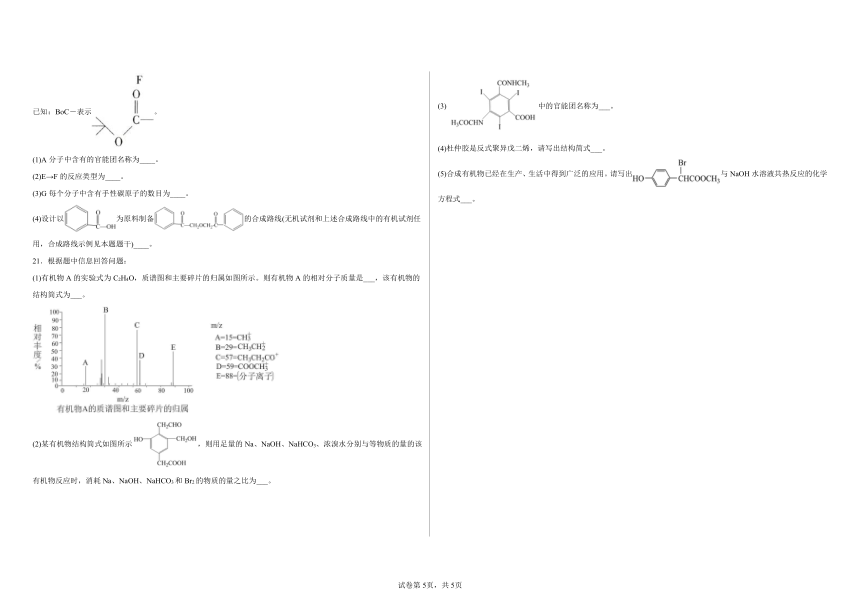
(3) 中的官能团名称为___。
(4)杜仲胶是反式聚异戊二烯,请写出结构简式___。
(5)合成有机物已经在生产、生活中得到广泛的应用。请写出与NaOH水溶液共热反应的化学方程式___。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A.卤代烃为非电解质,不能电离出卤素离子,因此溴代烃不能直接与氯水发生反应,故A错误;
B.卤代烃不能直接与硝酸银溶液发生反应,故B错误;
C.溴代烃在碱性条件下发生水解生成溴化钠,然后加硝酸中和过量的NaOH后再加硝酸银溶液,若出现浅黄色沉淀说明含有溴元素,故C正确;
D.NaOH能与硝酸银发生反应生成沉淀,因此在加硝酸银前应先加硝酸酸化,故D错误;
故选:C。
2.B
【详解】A.该有机物只有一个碳原子,不能发生消去反应,A错误;
B.该有机物可以发生水解反应,生成醇,也可以发生消去反应,产物只有一种如右图所示,,B正确;
C.该有机物中与卤原子相连的碳原子的相邻碳原子上没有氢原子,不能发生消去反应,C错误;
D.该有机物发生消去反应会有两种产物如右图,和,D错误;
故本题选B。
3.D
【详解】A.依据化合物X的结构图,可数出C原子数目为21,O原子数目为4,Br原子数目为2,不饱和度为10,则H原子数目为,则X分子式为,A错误;
B.化合物X有两个苯环,一个羰基,一个酯基,最多可与8mol发生加成反应,B错误;
C.X在酸性条件下,酯基发生水解反应,生成羧酸与醇,其中只有生成的羧酸可与溶液反应,C错误;
D.化合物X有一个羟基,且与之相连的C原子的邻位C上有H,可发生醇的消去反应;化合物X有两个Br原子,其中与Br原子相连的烃基C的邻位C上有H,可发生卤代烃的消去反应,D正确;
故合理选项为D。
4.D
【详解】A.依据题意,2-溴丁烷在乙醇钠存在的条件下发生消去反应的主要产物为A(顺-2-丁烯),次要产物为B(反-2-丁烯),而C(1-丁烯)只有少量生成,表明A(顺-2-丁烯)和B(反-2-丁烯)的总量比C(1-丁烯)的量多,A正确;
B.有机物A和B的分子中均含有4个C、8个H,但是有机物A中的两个甲基在碳碳双键的两边,而有机物B的两个甲基在碳碳双键的同一侧,所以A和B互为顺反异构体,B正确;
C.产物A和B与溴单质发生加成反应,得到的产物均为2,3-二溴丁烷,C正确;
D.2-溴丙烷在相同条件下发生消去反应,只能生成丙烯一种产物,D错误;
故合理选项为D。
5.A
【详解】A.由于CH4是正四面体结构,CF2Cl2是CH4分子中2个H原子被2个Cl原子取代,2个H原子被2个F原子取代产生的物质,由于分子中任何两个化学键都相邻,因此结构式为 ,只有一种结构,A正确;
B.由于CF2Cl2分子中的C-F、C-Cl键键长不同,因此它的空间构型是四面体,但不是正四面体,B错误;
C.氟利昂-12在常温下是无色气体,而不是无色液体物质,C错误;
D.卤代烃是由CF2Cl2分子构成的物质,它不溶于水,也不能发生电离,产生自由移动的氟离子和氯离子,D错误;
故合理选项是A。
6.B
【详解】由流程图可知,甲与Cl2在光照条件下发生取代反应生成,则甲为 ; 与氢氧化钠的醇溶液共热发生消去反应生成乙,则乙为 ;乙与Br2的CCl4溶液发生加成反应生成丙,则丙为 ;丙发生消去反应生成。
A.甲为 ,其分子式为C6H12,选项A正确;
B.乙为 ,与环己二烯的结构不相似,二者不互为同系物,选项B不正确;
C.反应①为取代反应,反应②为消去反应,反应③为加成反应,选项C正确;
D.丙的同分异构体中含有六元碳环结构的有,共3种,选项D正确;
答案选B。
7.D
【分析】在有机物的制备反应中,应选择的合成路线是步骤尽量少,合成产率尽量高,据此解答即可。
【详解】A.前两步可以合并成一步,即CH3CH2Br在NaOH醇溶液中发生消去反应制乙烯,反应步骤过于复杂,故A错误;
B.在CH3CH2Br CH2BrCH2Br的转化中发生取代反应的产物较多,难以得到单一的有机取代产物,引入杂质,且反应不易控制,故B错误;
C.CH2BrCH3与溴发生取代反应的生成物太复杂,不能保证CH2BrCH3和Br2发生取代反应时只生成1,2-二溴乙烷,且生成物不易分离,故C错误;
D.转化中发生消去、加成两步转化,节约原料、转化率高、操作简单、产物纯净,故D正确;
故答案为D。
8.C
【详解】A.1 mol该有机物中含有n mol碳溴键,A错误;
B.该有机物含有苯环,可与氢气发生加成反应,含碳溴键,可与NaOH水溶液发生取代反应,不能发生消去反应,B错误;
C.1 mol该有机物的单体含1mol碳溴键,与1molNaOH溶液发生水解反应得到酚羟基,具有弱酸性,再消耗1molNaOH溶液,则1 mol该有机物的单体最多可消耗2mol NaOH,C正确;
D.连接4个不同的原子或原子团的碳原子为手性碳原子,根据图知,与苯环相连的碳原子是手性碳原子,故D错误;
故选:C。
9.A
【分析】根据题目信息:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,可知反应的原理为:碳溴键发生断裂,溴原子与钠形成溴化钠,与溴原子相连的碳相连形成新的碳碳键,若形成环状结构,分子中一定含有两个溴原子,据此完成解答。
【详解】A.CH2BrCH2CH2CH2Br分子中含有两个溴原子,与钠发生反应可以生成环丁烷和NaBr,A符合题意;
B.CH3CH2CHBrCH2Br和钠以1:2反应生成1,4-二乙基环丁烷,B不符题意;
C.CH3CHBrCHBrCH2Br分子中含有3个溴原子,不能和钠反应生成环丁烷,C不符题意;
D.CH3CH2CH2CH2Br与金属钠反应后生成的是CH3CH2CH2CH2CH2CH2CH2CH3,D不符题意;
故合理选项是A。
10.C
【详解】卤代烃不溶于水,也不能电离出卤素离子,所以鉴定卤代烃中所含卤素原子时,可先使卤代烃水解生成相应的卤素离子,再加入HNO3中和碱,最后加入AgNO3溶液检验出卤素离子。即操作顺序为②④③⑤①,故选:C。
11.B
【详解】A.氯化亚铁在溶液低温蒸干时铁元素会被空气中的氧气氧化,最终生成氢氧化铁,故A错误;
B.由氨气能与足量盐酸反应生成氯化铵可知,联氨与足量盐酸反应生成N2H6Cl2,故B正确;
C.少量二氧化碳与次氯酸钠溶液反应生成碳酸氢钠,故C错误;
D.在氢氧化钠醇溶液中共热发生消去反应,故D错误;
答案选B。
12.C
【分析】由题干信息可知,O为2—溴—2—甲基丁烷其结构简式为:(CH3)2CBrCH2CH3,O在氢氧化钠乙醇溶液中加热发生消去反应,生成P的结构简式为CH2=C(CH3)CH2CH3或者(CH3)2C=CHCH3,P与水发生加成反应生成Q其结构简式为(CH3)2C(OH)CH2CH3,Q与HBr加热生成O,据此分析解题。
【详解】A.O的同分异构体有:CH3CH2CH2CH2CH2Br、CH3CH2CH2CHBrCH3、CH3CH2CHBrCH2CH3,CH2BrCH(CH3)CH2CH3、(CH3)2CHCHBrCH3、(CH3)2CHCH2CH2Br和(CH3)3CCH2Br,它们发生消去反应的产物分别有:1种、1种、0种、1种、2种、0种和0种,故发生消去反应所得产物有5种,A错误;
B.由分析可知,P分子的结构简式为CH2=C(CH3)CH2CH3或者(CH3)2C=CHCH3,分别含有4种、3种不同化学环境的氢原子,B错误;
C.由分析可知,Q的结构简式为:(CH3)2C(OH)CH2CH3,其含有两个甲基的醇类同分异构体有CH3CH(OH)CH2CH2CH3、CH3CH2CH(OH)CH2CH3、(CH3)2CHCH2CH2OH、HOCH2CH(CH3)CH2CH3共4种,C正确;
D.由分析可知,Q的结构简式为:(CH3)2C(OH)CH2CH3,其能被氧化为醛的醇类同分异构体有CH3CH2CH2CH2CH2OH、HOCH2CH(CH3)CH2CH3、(CH3)2CHCH2CH2OH ,(CH3)3CCH2OH共4种,D错误;
故答案为:C。
13.B
【详解】A.由图可知,碘化钠开始加入,最终未被消耗,则在反应过程的催化剂是,A项正确;
B.该过程中化合物1转化为化合物3为取代反应,化合物3转化为化合物4为消去反应,化合物4、5互为同分异构体,化合物4、5之间的转化为异构化反应,化合物5转化为化合物2为取代反应,乙醇与HI发生取代反应生成C2H5I,B项错误;
C.化合物4和5的分子式相同,但结构不同,互为同分异构体,C项正确;
D.反应过程中,生成的氢氧化钠和碘化氢均会被消耗,则反应液可能保持不变,D项正确;
答案选B。
14.C
【分析】1—溴丁烷在氢氧化钠溶液中共热发生水解反应生成1—丁醇、溴化钠,当1—丁醇浓度过大时,1—溴丁烷在氢氧化钠醇溶液中共热发生消去反应生成1—丁烯、溴化钠和水,1—丁醇和1—丁烯都能使高锰酸钾酸性溶液褪色,但1—丁醇不能与溴水反应,则将试管中高锰酸钾酸性溶液改为溴水,可以判断烧瓶中是否有消去反应发生。
【详解】A.由分析可知,烧瓶中可能发生水解反应生成了1—丁醇,也可能发生消去反应了1—丁烯,故A正确;
B.1—丁醇和1—丁烯的官能团不同,红外光谱的谱图不同,则用红外光谱可检验在该条件下反应生成有机物中的官能团,故B正确;
C.由分析可知,1—溴丁烷无论是发生水解反应,还是发生消去反应,都有溴化钠生成,则通过检验反应后烧瓶内溶液中的溴离子,不能确定烧瓶内发生的反应类型,故C错误;
D.由分析可知,1—丁烯能与溴水发生加成反应使溴水褪色,1—丁醇不能与溴水反应,则将试管中高锰酸钾酸性溶液改为溴水,可以判断烧瓶中是否有消去反应发生,故D正确;
故选C。
15.D
【详解】A.与水加成反应可生成,A正确;
B.在氢氧化钠溶液中加热水解就可以生成,B正确;
C.与水加成反应可生成,再在氢氧化钠溶液中加热水解就可以生成甘油,C正确;
D.是一种共价化合物,不可能电离出Cl-,因此不能与AgNO3溶液反应,D错误;
故选D。
16.(1)C15H22O3
(2)碳碳双键、醛基、羟基
(3)D
【详解】(1)化合物A的分子式为:C15H22O3。
(2)化合物A的官能团有:碳碳双键、醛基、羟基。
(3)A.DDT“药效强”、“最终造成环境污染”,在杀死害虫的同时,也能杀死有益的生物,A正确;
B.DDT“脂溶性好”说明其难溶于水,易溶于有机溶剂,B正确;
C.DDT的分子式为C14H9Cl5,C正确;
D.DDT“性质稳定”,杀虫时在蔬菜中残留时间长;“药效强”,进入人体后会对身体造成危害,D错误;
故选D。
17.(1)CH2=CH2+HClCH3CH2Cl
(2)氯乙烷的沸点低,易挥发,挥发时吸收热量起到降温的作用
【详解】(1)在催化剂作用下,乙烯能与氯化氢发生加成反应生成氯乙烷,反应的化学方程式:CH2=CH2+HClCH3CH2Cl。答案为:CH2=CH2+HClCH3CH2Cl;
(2)氯乙烷的沸点低,常温下易挥发,挥发时,会带走周围环境中的热量,从而使周围环境温度降低,能减轻伤员的痛感,所以氯乙烷能用于冷冻麻醉应急处理的原因是:氯乙烷的沸点低,易挥发,挥发时吸收热量起到降温的作用。答案为:氯乙烷的沸点低,易挥发,挥发时吸收热量起到降温的作用。
18. CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O 乙醇易挥发,挥发出来的乙醇也可以使酸性KMnO4溶液褪色 在小试管之前增加一个盛有冷水的洗气瓶
【分析】溴乙烷在强碱的醇溶液中发生消去反应生成乙烯,生成的乙烯和试管中的酸性高锰酸钾溶液反应使溶液褪色,但因为乙醇具有挥发性,所以从反应装置出来的气体除了生成的乙烯外还有挥发出来的乙醇,乙烯和乙醇都可以使酸性KMnO4溶液颜色褪去,以此解答。
【详解】(1)溴乙烷在强碱的醇溶液中发生消去反应生成乙烯,实验原理为:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O,故答案为:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O;
(2)因为乙醇具有挥发性,所以从反应装置出来的气体除了生成的乙烯外还有挥发出来的乙醇,乙烯和乙醇都可以使酸性KMnO4溶液颜色褪去,故不一定是产生的乙烯,故答案为:乙醇易挥发,挥发出来的乙醇也可以使酸性KMnO4溶液褪色;
(3)根据(2)的分析,只要在通入酸性KMnO4溶液之前除去乙醇就可以证明乙烯的生成了,除去乙醇最简单的方法就是通入水中而且又不影响乙烯,故答案为:在小试管之前增加一个盛有冷水的洗气瓶。
19. CH3CH2OH+HBrCH3CH2Br+H2O 小于 乙醇可与 H2O 分子间形成氢键,而溴乙烷不能 CH3CH2OH CH2=CH2↑+H2O或 2CH3CH2OH CH3CH2OCH2CH3+H2O B 分液漏斗 ⑤①④③②
【分析】烧瓶中NaBr和硫酸反应产生HBr,HBr和CH3CH2OH反应产生CH3CH2Br,CH3CH2Br挥发,在U形管中冷凝为液态CH3CH2Br;反应结束后,U形管中制得的溴乙烷呈棕黄色可知,得到的液态CH3CH2Br中混有溴,可加入Na2SO3溶液将溴还原,然后分液除去水层得较纯的溴乙烷,据此分析解答。
【详解】(1)溴化钠、浓硫酸混合加热生成HBr,HBr和CH3CH2OH发生取代反应制得CH3CH2Br,化学方程式为CH3CH2OH+HBrCH3CH2Br+H2O,故答案为:CH3CH2OH+HBrCH3CH2Br+H2O;
(2)由于乙醇可与H2O分子间形成氢键,而溴乙烷不能,所以溴乙烷的水溶性小于乙醇的水溶性,故答案为:小于;乙醇可与 H2O 分子间形成氢键,而溴乙烷不能;
(3)温度过高会发生副反应产生乙烯或乙醚,即CH3CH2OH CH2=CH2↑+H2O或 2CH3CH2OH CH3CH2OCH2CH3+H2O,故答案为:CH3CH2OH CH2=CH2↑+H2O或 2CH3CH2OH CH3CH2OCH2CH3+H2O;
(4)粗制的溴乙烷呈棕黄色,从元素角度分析可知含有单质溴杂质,可加入某种试剂后进行分液:
A.溴在溴乙烷中的溶解度比在水中大,加水不能除去溴乙烷中的溴,A错误;
B.Na2SO3与溴发生氧化还原反应,Na2SO3溶液可除去溴,B正确;
C.溴和溴乙烷都易溶于四氯化碳,不能将二者分离,C错误;
D.溴、溴乙烷都能够与氢氧化钠反应,不能用NaOH溶液除去溴,D错误;
综上所述,答案选B;
分液使用的主要仪器是分液漏斗,故答案为:B;分液漏斗;
(5)检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,所以操作顺序为⑤①④③②,故答案为:⑤①④③②。
20.(1)氨基、羧基
(2)还原反应
(3)2
(4)
【分析】a与(Boc)2O发生取代反应生成B和,B与SOCl2发生取代反应生成C,C中氯原子转化甲基生成D,D中甲基上氢原子被氯原子替代生成E,E中羰基被还原为羟基生成F:,F→G可以理解为:氯原子水解引入羟基,羟基之间再脱去1分子水成环而生成G。
(1)
由A的结构简式可知:A分子中含有的官能团为氨基、羧基;
(2)
E→F的过程中羰基与H2发生加成反应转化为羟基,组成上加氢的反应类型为还原反应;
(3)
连接4个不同原子或原子团的碳原子是手性碳原子,G中如图所示标有“*”的为手性碳原子:,G分子含有2个手性碳原子;
(4)
由F→G的转化可知,由与在碱性条件下反应生成,而在碱性条件下水解生成,由B→C→D→E的转化可知:与SOCl2在DMF条件下生成,然后经过①M个CHOH、②CH2(COO(C2H5)2)2、③H+/H2O生成,再与HCl作用生成,故合成路线为。
21. 88 CH3CH2COOCH3 3∶2∶1∶3 羧基、酰胺键(或肽键)和碳碘键 +3NaOH+CH3OH+NaBr+H2O
【详解】(1)由质荷比可知有机物的相对分子质量为88;有机物A的最简式为C2H4O,相对分子质量为88,则A的分子式为C4H8O2,B和D的碎片加起来的质量刚好等于88,则该有机物的结构简式为CH3CH2COOCH3;
(2)有机物中含酚-OH、醇-OH、-CHO、-COOH,酚-OH、醇-OH、-COOH均与Na反应,酚-OH、-COOH与NaOH反应,只有-COOH与NaHCO3反应,醛基与酚羟基的邻、对位苯环C上的H能够与浓溴水反应,则等物质的量的该有机物完全反应时,消耗Na、NaOH、NaHCO3和Br2的物质的量之比为3:2:1:3,
(3) 官能团名称为羧基、酰胺键(或肽键)和碳碘键;
(4)反式聚异戊二烯的结构简式为;
(5) 能与NaOH水溶液反应的官能团有酚羟基、溴原子、酯基,反应的化学方程式+3NaOH+CH3OH+NaBr+H2O。
答案第1页,共2页
答案第1页,共2页
2022——2023学年高中化学苏教版(2019)选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.要检验卤代烃中是否含有溴元素,正确的实验方法是
A.加入氯水振荡,观察上层是否有橙色
B.滴加硝酸酸化的AgNO3溶液,观察有无浅黄色沉淀生成
C.滴加NaOH水溶液,加热,然后加入稀硝酸酸化,再滴加AgNO3溶液,观察有无浅黄色沉淀生成
D.滴加NaOH水溶液,然后滴加AgNO3溶液,观察有无浅黄色沉淀生成
2.下列化合物中,既能发生水解反应,又能发生消去反应,且消去反应生成的烯烃只有一种的是
A.CH3Br B.
C. D.
3.下列有关化合物X(结构如图)的叙述正确的是
A.X分子式为
B.X最多可与7mol发生加成反应
C.X在酸性条件下水解的产物均可与溶液反应
D.X可发生消去反应
4.卤代烃在一定条件下可发生消去反应生成烯烃,下图为2-溴丁烷在乙醇钠存在的条件下发生消去反应的产物情况。下列说法不正确的是
A.此条件下的消去反应,生成的2-丁烯的量比1-丁烯多
B.产物A和B互为顺反异构体
C.产物A、B与发生加成反应得到结构相同的产物
D.2-溴丙烷在相同条件下发生消去反应也会有不同结构的产物生成
5.氟利昂-12是甲烷的氯、氟代物,结构式为,下列有关叙述正确的是
A.它只有一种结构 B.它的空间构型是正四面体
C.它常温下是无色液体 D.它溶于水可以电离出氟离子和氯离子
6.用有机物甲可制备环己二烯(),其合成路线如图所示:
甲乙丙
下列有关判断不正确的是
A.甲的分子式为C6H12
B.乙与环己二烯互为同系物
C.反应①②③分别为取代反应、消去反应、加成反应
D.丙的同分异构体中含有六元碳环结构的还有3种
7.从溴乙烷制取1,2 二溴乙烷,下列制备方案中最好的是
A.CH3CH2BrCH3CH2OHCH2=CH2CH2BrCH2Br
B.CH3CH2BrCH2BrCH2Br
C.CH3CH2BrCH2=CH2CH3CH2BrCH2BrCH2Br
D.CH3CH2BrCH2=CH2CH2BrCH2Br
8.已知某有机物的结构如下图所示,下列分析正确的是
A.1 mol该有机物中含有1 mol碳溴键
B.该有机物能发生加成、取代、消去反应
C.1 mol该有机物的单体最多可消耗2mol NaOH
D.该有机物分子中不存在手性碳原子
9.卤代烃能够发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列有机物可以与钠反应合成环丁烷的是
A. B.
C. D.
10.为鉴别卤代烃中所含卤素原子,现有下列实验操作步骤,正确的顺序是
①加入AgNO3溶液 ②加入少许卤代烃试样 ③加热 ④加入5 mL 4 mol·L-1 NaOH溶液 ⑤加入5 mL 4 mol·L-1 HNO3溶液
A.②④③①⑤ B.②③①④⑤ C.②④③⑤① D.②⑤③①④
11.下列“类比”结果正确的是
A.MgCl2溶液低温蒸干得到Mg(OH)2,则FeCl2溶液低温蒸干得到Fe(OH)2
B.NH3与足量盐酸反应生成NH4Cl,则N2H4与足量盐酸反应生成N2H6Cl2
C.少量CO2通入Ca(ClO)2溶液生成CaCO3,则少量CO2通入NaClO溶液生成Na2CO3
D.消去反应条件为浓硫酸,加热,则消去反应条件也为浓硫酸,加热
12.有机物O(2—溴—2—甲基丁烷)存在如图转化关系(P分子中含有两个甲基),下列说法正确的是
A.O的同分异构体中,发生消去反应所得产物有6种
B.P分子中,含有5种不同化学环境的氢原子
C.Q的同分异构体中,含有两个甲基的醇有4种
D.Q的同分异构体中,能被氧化为醛的醇有3种
13.以乙醇、过氧化氢、碘化钠和原料1制备联苯衍生物2的一种反应机理如图。下列说法不正确的是
A.反应过程的催化剂是 B.涉及的有机反应只有取代、消去、还原
C.化合物4和5互为同分异构体 D.反应过程中反应液可能保持不变
14.用如图装置探究1—溴丁烷在氢氧化钠溶液中发生的反应,观察到高锰酸钾酸性溶液褪色。下列分析不正确的是
A.推断烧瓶中可能生成了1—丁醇或1—丁烯
B.用红外光谱可检验在该条件下反应生成有机物中的官能团
C.通过检验反应后烧瓶内溶液中的溴离子,可确定烧瓶内发生的反应类型
D.将试管中溶液改为溴水,若溴水褪色,则烧瓶中一定有消去反应发生
15.称为环氧乙烷,它在一定条件下,能与氢化物发生加成反应,氢原子加到氧原子上,其他部分加到碳原子上。对下面环氧乙烷的衍生物的叙述中,不正确的是
A.在一定条件下能与水反应生成
B.在一定条件下能与水反应生成
C.在一定条件下可以合成甘油
D.加入AgNO3溶液能生成难溶于HNO3的白色沉淀
二、填空题
16.滴滴涕(DDT)是20世纪60年代以前广为应用的一种杀虫剂,它可由氯苯制得,其结构简式为,因其性质稳定、脂溶性好、药效强、适用性广而被大量生产,普遍使用,以致最终造成环境污染。为了杀灭对人类有害的昆虫,而又避免或减少环境污染、破坏生态平衡,化学工作者进行了不懈的努力,研制出多种新型杀虫剂,以代替DDT等农药。例如化合物A就是其中一种,其分子结构如图所示。
请完成下列各题:
(1)化合物A的分子式为_______。
(2)化合物A中的官能团有_______(写名称)。
(3)下列关于DDT的说法中,错误的是_______(填字母)。
A.DDT在杀死害虫的同时,也能杀死有益的生物
B.DDT是一种难溶于水,易溶于有机溶剂的物质
C.DDT的分子式为
D.DDT用于蔬菜杀虫时,在蔬菜中残留时间短,对人体无害
17.体育比赛中,当运动员肌肉挫伤或扭伤时,队医立即对准运动员的受伤部位喷射药剂——氯乙烷(CH3CH2Cl,沸点为12.27℃)进行局部冷冻麻醉应急处理。
(1)写出由乙烯制取氯乙烷的反应的化学方程式:_______。
(2)氯乙烷能用于冷冻麻醉应急处理的原因是_______。
三、实验题
18.某学习小组探究溴乙烷的消去反应并验证产物。
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)实验原理:___________。
(2)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因:____________。
(3)丙同学认为只要对实验装置进行适当改进,即可避免对乙烯气体检验的干扰,改进方法:________。
19.如图是实验室制备溴乙烷的装置(已知溴乙烷的沸点38.4℃)。步骤如下:
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。
请回答下列问题:
(1)已知烧瓶中制备溴乙烷时包含两个反应,写出反应②:
①NaBr+H2SO4=HBr+NaHSO4
②_______________
(2)溴乙烷的水溶性______(填“大于”“等于”或“小于)乙醇的水溶性,其原因是___________。
(3)反应时若温度过高,会有多种有机副产物生成,,写出相应的化学方程式________(任写一个)
(4)反应结束后,U形管中制得的溴乙烷呈棕黄色。为了除去产品中的杂质,可选择下列试剂中的_____填序号)。
A.H2O B.Na2SO3溶液 C.CC14 D.NaOH溶液
除杂所需的主要玻璃仪器是_______(填仪器名称)
(5)检验溴乙烷中溴元素:取少量溴乙烷,然后_______(按正确的操作顺序填序号)。
①加热:②加入AgNO3溶液:③加入稀HNO3酸化; ④冷却;⑤加入NaOH溶液
四、有机推断题
20.化合物G是制备抗HIV药物阿扎那韦的关键中间体,其一种合成路线如图:
已知:BoC-表示。
(1)A分子中含有的官能团名称为____。
(2)E→F的反应类型为____。
(3)G每个分子中含有手性碳原子的数目为____。
(4)设计以为原料制备的合成路线(无机试剂和上述合成路线中的有机试剂任用,合成路线示例见本题题干)____。
21.根据题中信息回答问题:
(1)有机物A的实验式为C2H4O,质谱图和主要碎片的归属如图所示。则有机物A的相对分子质量是___,该有机物的结构简式为___。
(2)某有机物结构简式如图所示,则用足量的Na、NaOH、NaHCO3、浓溴水分别与等物质的量的该有机物反应时,消耗Na、NaOH、NaHCO3和Br2的物质的量之比为___。
(3) 中的官能团名称为___。
(4)杜仲胶是反式聚异戊二烯,请写出结构简式___。
(5)合成有机物已经在生产、生活中得到广泛的应用。请写出与NaOH水溶液共热反应的化学方程式___。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A.卤代烃为非电解质,不能电离出卤素离子,因此溴代烃不能直接与氯水发生反应,故A错误;
B.卤代烃不能直接与硝酸银溶液发生反应,故B错误;
C.溴代烃在碱性条件下发生水解生成溴化钠,然后加硝酸中和过量的NaOH后再加硝酸银溶液,若出现浅黄色沉淀说明含有溴元素,故C正确;
D.NaOH能与硝酸银发生反应生成沉淀,因此在加硝酸银前应先加硝酸酸化,故D错误;
故选:C。
2.B
【详解】A.该有机物只有一个碳原子,不能发生消去反应,A错误;
B.该有机物可以发生水解反应,生成醇,也可以发生消去反应,产物只有一种如右图所示,,B正确;
C.该有机物中与卤原子相连的碳原子的相邻碳原子上没有氢原子,不能发生消去反应,C错误;
D.该有机物发生消去反应会有两种产物如右图,和,D错误;
故本题选B。
3.D
【详解】A.依据化合物X的结构图,可数出C原子数目为21,O原子数目为4,Br原子数目为2,不饱和度为10,则H原子数目为,则X分子式为,A错误;
B.化合物X有两个苯环,一个羰基,一个酯基,最多可与8mol发生加成反应,B错误;
C.X在酸性条件下,酯基发生水解反应,生成羧酸与醇,其中只有生成的羧酸可与溶液反应,C错误;
D.化合物X有一个羟基,且与之相连的C原子的邻位C上有H,可发生醇的消去反应;化合物X有两个Br原子,其中与Br原子相连的烃基C的邻位C上有H,可发生卤代烃的消去反应,D正确;
故合理选项为D。
4.D
【详解】A.依据题意,2-溴丁烷在乙醇钠存在的条件下发生消去反应的主要产物为A(顺-2-丁烯),次要产物为B(反-2-丁烯),而C(1-丁烯)只有少量生成,表明A(顺-2-丁烯)和B(反-2-丁烯)的总量比C(1-丁烯)的量多,A正确;
B.有机物A和B的分子中均含有4个C、8个H,但是有机物A中的两个甲基在碳碳双键的两边,而有机物B的两个甲基在碳碳双键的同一侧,所以A和B互为顺反异构体,B正确;
C.产物A和B与溴单质发生加成反应,得到的产物均为2,3-二溴丁烷,C正确;
D.2-溴丙烷在相同条件下发生消去反应,只能生成丙烯一种产物,D错误;
故合理选项为D。
5.A
【详解】A.由于CH4是正四面体结构,CF2Cl2是CH4分子中2个H原子被2个Cl原子取代,2个H原子被2个F原子取代产生的物质,由于分子中任何两个化学键都相邻,因此结构式为 ,只有一种结构,A正确;
B.由于CF2Cl2分子中的C-F、C-Cl键键长不同,因此它的空间构型是四面体,但不是正四面体,B错误;
C.氟利昂-12在常温下是无色气体,而不是无色液体物质,C错误;
D.卤代烃是由CF2Cl2分子构成的物质,它不溶于水,也不能发生电离,产生自由移动的氟离子和氯离子,D错误;
故合理选项是A。
6.B
【详解】由流程图可知,甲与Cl2在光照条件下发生取代反应生成,则甲为 ; 与氢氧化钠的醇溶液共热发生消去反应生成乙,则乙为 ;乙与Br2的CCl4溶液发生加成反应生成丙,则丙为 ;丙发生消去反应生成。
A.甲为 ,其分子式为C6H12,选项A正确;
B.乙为 ,与环己二烯的结构不相似,二者不互为同系物,选项B不正确;
C.反应①为取代反应,反应②为消去反应,反应③为加成反应,选项C正确;
D.丙的同分异构体中含有六元碳环结构的有,共3种,选项D正确;
答案选B。
7.D
【分析】在有机物的制备反应中,应选择的合成路线是步骤尽量少,合成产率尽量高,据此解答即可。
【详解】A.前两步可以合并成一步,即CH3CH2Br在NaOH醇溶液中发生消去反应制乙烯,反应步骤过于复杂,故A错误;
B.在CH3CH2Br CH2BrCH2Br的转化中发生取代反应的产物较多,难以得到单一的有机取代产物,引入杂质,且反应不易控制,故B错误;
C.CH2BrCH3与溴发生取代反应的生成物太复杂,不能保证CH2BrCH3和Br2发生取代反应时只生成1,2-二溴乙烷,且生成物不易分离,故C错误;
D.转化中发生消去、加成两步转化,节约原料、转化率高、操作简单、产物纯净,故D正确;
故答案为D。
8.C
【详解】A.1 mol该有机物中含有n mol碳溴键,A错误;
B.该有机物含有苯环,可与氢气发生加成反应,含碳溴键,可与NaOH水溶液发生取代反应,不能发生消去反应,B错误;
C.1 mol该有机物的单体含1mol碳溴键,与1molNaOH溶液发生水解反应得到酚羟基,具有弱酸性,再消耗1molNaOH溶液,则1 mol该有机物的单体最多可消耗2mol NaOH,C正确;
D.连接4个不同的原子或原子团的碳原子为手性碳原子,根据图知,与苯环相连的碳原子是手性碳原子,故D错误;
故选:C。
9.A
【分析】根据题目信息:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,可知反应的原理为:碳溴键发生断裂,溴原子与钠形成溴化钠,与溴原子相连的碳相连形成新的碳碳键,若形成环状结构,分子中一定含有两个溴原子,据此完成解答。
【详解】A.CH2BrCH2CH2CH2Br分子中含有两个溴原子,与钠发生反应可以生成环丁烷和NaBr,A符合题意;
B.CH3CH2CHBrCH2Br和钠以1:2反应生成1,4-二乙基环丁烷,B不符题意;
C.CH3CHBrCHBrCH2Br分子中含有3个溴原子,不能和钠反应生成环丁烷,C不符题意;
D.CH3CH2CH2CH2Br与金属钠反应后生成的是CH3CH2CH2CH2CH2CH2CH2CH3,D不符题意;
故合理选项是A。
10.C
【详解】卤代烃不溶于水,也不能电离出卤素离子,所以鉴定卤代烃中所含卤素原子时,可先使卤代烃水解生成相应的卤素离子,再加入HNO3中和碱,最后加入AgNO3溶液检验出卤素离子。即操作顺序为②④③⑤①,故选:C。
11.B
【详解】A.氯化亚铁在溶液低温蒸干时铁元素会被空气中的氧气氧化,最终生成氢氧化铁,故A错误;
B.由氨气能与足量盐酸反应生成氯化铵可知,联氨与足量盐酸反应生成N2H6Cl2,故B正确;
C.少量二氧化碳与次氯酸钠溶液反应生成碳酸氢钠,故C错误;
D.在氢氧化钠醇溶液中共热发生消去反应,故D错误;
答案选B。
12.C
【分析】由题干信息可知,O为2—溴—2—甲基丁烷其结构简式为:(CH3)2CBrCH2CH3,O在氢氧化钠乙醇溶液中加热发生消去反应,生成P的结构简式为CH2=C(CH3)CH2CH3或者(CH3)2C=CHCH3,P与水发生加成反应生成Q其结构简式为(CH3)2C(OH)CH2CH3,Q与HBr加热生成O,据此分析解题。
【详解】A.O的同分异构体有:CH3CH2CH2CH2CH2Br、CH3CH2CH2CHBrCH3、CH3CH2CHBrCH2CH3,CH2BrCH(CH3)CH2CH3、(CH3)2CHCHBrCH3、(CH3)2CHCH2CH2Br和(CH3)3CCH2Br,它们发生消去反应的产物分别有:1种、1种、0种、1种、2种、0种和0种,故发生消去反应所得产物有5种,A错误;
B.由分析可知,P分子的结构简式为CH2=C(CH3)CH2CH3或者(CH3)2C=CHCH3,分别含有4种、3种不同化学环境的氢原子,B错误;
C.由分析可知,Q的结构简式为:(CH3)2C(OH)CH2CH3,其含有两个甲基的醇类同分异构体有CH3CH(OH)CH2CH2CH3、CH3CH2CH(OH)CH2CH3、(CH3)2CHCH2CH2OH、HOCH2CH(CH3)CH2CH3共4种,C正确;
D.由分析可知,Q的结构简式为:(CH3)2C(OH)CH2CH3,其能被氧化为醛的醇类同分异构体有CH3CH2CH2CH2CH2OH、HOCH2CH(CH3)CH2CH3、(CH3)2CHCH2CH2OH ,(CH3)3CCH2OH共4种,D错误;
故答案为:C。
13.B
【详解】A.由图可知,碘化钠开始加入,最终未被消耗,则在反应过程的催化剂是,A项正确;
B.该过程中化合物1转化为化合物3为取代反应,化合物3转化为化合物4为消去反应,化合物4、5互为同分异构体,化合物4、5之间的转化为异构化反应,化合物5转化为化合物2为取代反应,乙醇与HI发生取代反应生成C2H5I,B项错误;
C.化合物4和5的分子式相同,但结构不同,互为同分异构体,C项正确;
D.反应过程中,生成的氢氧化钠和碘化氢均会被消耗,则反应液可能保持不变,D项正确;
答案选B。
14.C
【分析】1—溴丁烷在氢氧化钠溶液中共热发生水解反应生成1—丁醇、溴化钠,当1—丁醇浓度过大时,1—溴丁烷在氢氧化钠醇溶液中共热发生消去反应生成1—丁烯、溴化钠和水,1—丁醇和1—丁烯都能使高锰酸钾酸性溶液褪色,但1—丁醇不能与溴水反应,则将试管中高锰酸钾酸性溶液改为溴水,可以判断烧瓶中是否有消去反应发生。
【详解】A.由分析可知,烧瓶中可能发生水解反应生成了1—丁醇,也可能发生消去反应了1—丁烯,故A正确;
B.1—丁醇和1—丁烯的官能团不同,红外光谱的谱图不同,则用红外光谱可检验在该条件下反应生成有机物中的官能团,故B正确;
C.由分析可知,1—溴丁烷无论是发生水解反应,还是发生消去反应,都有溴化钠生成,则通过检验反应后烧瓶内溶液中的溴离子,不能确定烧瓶内发生的反应类型,故C错误;
D.由分析可知,1—丁烯能与溴水发生加成反应使溴水褪色,1—丁醇不能与溴水反应,则将试管中高锰酸钾酸性溶液改为溴水,可以判断烧瓶中是否有消去反应发生,故D正确;
故选C。
15.D
【详解】A.与水加成反应可生成,A正确;
B.在氢氧化钠溶液中加热水解就可以生成,B正确;
C.与水加成反应可生成,再在氢氧化钠溶液中加热水解就可以生成甘油,C正确;
D.是一种共价化合物,不可能电离出Cl-,因此不能与AgNO3溶液反应,D错误;
故选D。
16.(1)C15H22O3
(2)碳碳双键、醛基、羟基
(3)D
【详解】(1)化合物A的分子式为:C15H22O3。
(2)化合物A的官能团有:碳碳双键、醛基、羟基。
(3)A.DDT“药效强”、“最终造成环境污染”,在杀死害虫的同时,也能杀死有益的生物,A正确;
B.DDT“脂溶性好”说明其难溶于水,易溶于有机溶剂,B正确;
C.DDT的分子式为C14H9Cl5,C正确;
D.DDT“性质稳定”,杀虫时在蔬菜中残留时间长;“药效强”,进入人体后会对身体造成危害,D错误;
故选D。
17.(1)CH2=CH2+HClCH3CH2Cl
(2)氯乙烷的沸点低,易挥发,挥发时吸收热量起到降温的作用
【详解】(1)在催化剂作用下,乙烯能与氯化氢发生加成反应生成氯乙烷,反应的化学方程式:CH2=CH2+HClCH3CH2Cl。答案为:CH2=CH2+HClCH3CH2Cl;
(2)氯乙烷的沸点低,常温下易挥发,挥发时,会带走周围环境中的热量,从而使周围环境温度降低,能减轻伤员的痛感,所以氯乙烷能用于冷冻麻醉应急处理的原因是:氯乙烷的沸点低,易挥发,挥发时吸收热量起到降温的作用。答案为:氯乙烷的沸点低,易挥发,挥发时吸收热量起到降温的作用。
18. CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O 乙醇易挥发,挥发出来的乙醇也可以使酸性KMnO4溶液褪色 在小试管之前增加一个盛有冷水的洗气瓶
【分析】溴乙烷在强碱的醇溶液中发生消去反应生成乙烯,生成的乙烯和试管中的酸性高锰酸钾溶液反应使溶液褪色,但因为乙醇具有挥发性,所以从反应装置出来的气体除了生成的乙烯外还有挥发出来的乙醇,乙烯和乙醇都可以使酸性KMnO4溶液颜色褪去,以此解答。
【详解】(1)溴乙烷在强碱的醇溶液中发生消去反应生成乙烯,实验原理为:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O,故答案为:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O;
(2)因为乙醇具有挥发性,所以从反应装置出来的气体除了生成的乙烯外还有挥发出来的乙醇,乙烯和乙醇都可以使酸性KMnO4溶液颜色褪去,故不一定是产生的乙烯,故答案为:乙醇易挥发,挥发出来的乙醇也可以使酸性KMnO4溶液褪色;
(3)根据(2)的分析,只要在通入酸性KMnO4溶液之前除去乙醇就可以证明乙烯的生成了,除去乙醇最简单的方法就是通入水中而且又不影响乙烯,故答案为:在小试管之前增加一个盛有冷水的洗气瓶。
19. CH3CH2OH+HBrCH3CH2Br+H2O 小于 乙醇可与 H2O 分子间形成氢键,而溴乙烷不能 CH3CH2OH CH2=CH2↑+H2O或 2CH3CH2OH CH3CH2OCH2CH3+H2O B 分液漏斗 ⑤①④③②
【分析】烧瓶中NaBr和硫酸反应产生HBr,HBr和CH3CH2OH反应产生CH3CH2Br,CH3CH2Br挥发,在U形管中冷凝为液态CH3CH2Br;反应结束后,U形管中制得的溴乙烷呈棕黄色可知,得到的液态CH3CH2Br中混有溴,可加入Na2SO3溶液将溴还原,然后分液除去水层得较纯的溴乙烷,据此分析解答。
【详解】(1)溴化钠、浓硫酸混合加热生成HBr,HBr和CH3CH2OH发生取代反应制得CH3CH2Br,化学方程式为CH3CH2OH+HBrCH3CH2Br+H2O,故答案为:CH3CH2OH+HBrCH3CH2Br+H2O;
(2)由于乙醇可与H2O分子间形成氢键,而溴乙烷不能,所以溴乙烷的水溶性小于乙醇的水溶性,故答案为:小于;乙醇可与 H2O 分子间形成氢键,而溴乙烷不能;
(3)温度过高会发生副反应产生乙烯或乙醚,即CH3CH2OH CH2=CH2↑+H2O或 2CH3CH2OH CH3CH2OCH2CH3+H2O,故答案为:CH3CH2OH CH2=CH2↑+H2O或 2CH3CH2OH CH3CH2OCH2CH3+H2O;
(4)粗制的溴乙烷呈棕黄色,从元素角度分析可知含有单质溴杂质,可加入某种试剂后进行分液:
A.溴在溴乙烷中的溶解度比在水中大,加水不能除去溴乙烷中的溴,A错误;
B.Na2SO3与溴发生氧化还原反应,Na2SO3溶液可除去溴,B正确;
C.溴和溴乙烷都易溶于四氯化碳,不能将二者分离,C错误;
D.溴、溴乙烷都能够与氢氧化钠反应,不能用NaOH溶液除去溴,D错误;
综上所述,答案选B;
分液使用的主要仪器是分液漏斗,故答案为:B;分液漏斗;
(5)检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,所以操作顺序为⑤①④③②,故答案为:⑤①④③②。
20.(1)氨基、羧基
(2)还原反应
(3)2
(4)
【分析】a与(Boc)2O发生取代反应生成B和,B与SOCl2发生取代反应生成C,C中氯原子转化甲基生成D,D中甲基上氢原子被氯原子替代生成E,E中羰基被还原为羟基生成F:,F→G可以理解为:氯原子水解引入羟基,羟基之间再脱去1分子水成环而生成G。
(1)
由A的结构简式可知:A分子中含有的官能团为氨基、羧基;
(2)
E→F的过程中羰基与H2发生加成反应转化为羟基,组成上加氢的反应类型为还原反应;
(3)
连接4个不同原子或原子团的碳原子是手性碳原子,G中如图所示标有“*”的为手性碳原子:,G分子含有2个手性碳原子;
(4)
由F→G的转化可知,由与在碱性条件下反应生成,而在碱性条件下水解生成,由B→C→D→E的转化可知:与SOCl2在DMF条件下生成,然后经过①M个CHOH、②CH2(COO(C2H5)2)2、③H+/H2O生成,再与HCl作用生成,故合成路线为。
21. 88 CH3CH2COOCH3 3∶2∶1∶3 羧基、酰胺键(或肽键)和碳碘键 +3NaOH+CH3OH+NaBr+H2O
【详解】(1)由质荷比可知有机物的相对分子质量为88;有机物A的最简式为C2H4O,相对分子质量为88,则A的分子式为C4H8O2,B和D的碎片加起来的质量刚好等于88,则该有机物的结构简式为CH3CH2COOCH3;
(2)有机物中含酚-OH、醇-OH、-CHO、-COOH,酚-OH、醇-OH、-COOH均与Na反应,酚-OH、-COOH与NaOH反应,只有-COOH与NaHCO3反应,醛基与酚羟基的邻、对位苯环C上的H能够与浓溴水反应,则等物质的量的该有机物完全反应时,消耗Na、NaOH、NaHCO3和Br2的物质的量之比为3:2:1:3,
(3) 官能团名称为羧基、酰胺键(或肽键)和碳碘键;
(4)反式聚异戊二烯的结构简式为;
(5) 能与NaOH水溶液反应的官能团有酚羟基、溴原子、酯基,反应的化学方程式+3NaOH+CH3OH+NaBr+H2O。
答案第1页,共2页
答案第1页,共2页
