化学人教版(2019)必修第二册7.2.1乙烯(共28张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.2.1乙烯(共28张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 20.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-16 00:00:00 | ||
图片预览





文档简介
(共28张PPT)
碳在地壳中的含量很低,但是含有碳元素的有机化合物却分布极广。有机化合物不仅构成了生机勃勃的生命世界,也是燃料、材料、食品和药物的主要来源。
与无机化合物相比,有机化合物的组成元素并不复杂,但化合物数量众多,性质各异。对有机化合物的研究,需要在了解碳原子成键规律的基础上,认识有机化合物的分子结构,以及决定其分类与性质的特征基团。进而认识有机化学反应,实现有机化合物之间的转化,合成新的物质。
●认识有机化合物
●乙烯与有机高分子材料
●乙醇与乙酸
●基本营养物质
组织建设
第二节 乙烯与有机高分子材料
(第1课时 乙烯)
第七章 有机化合物
生活小窍门
把未熟的青香蕉和熟苹果放在同一个塑料袋里,系紧袋口,放置一段时间,你会发现?
震惊!青香蕉熟了
成熟的苹果会产生乙烯, 果实中乙烯含量增加时, 可促进其中有机物质的转化,加速成熟,故可以催熟香蕉。
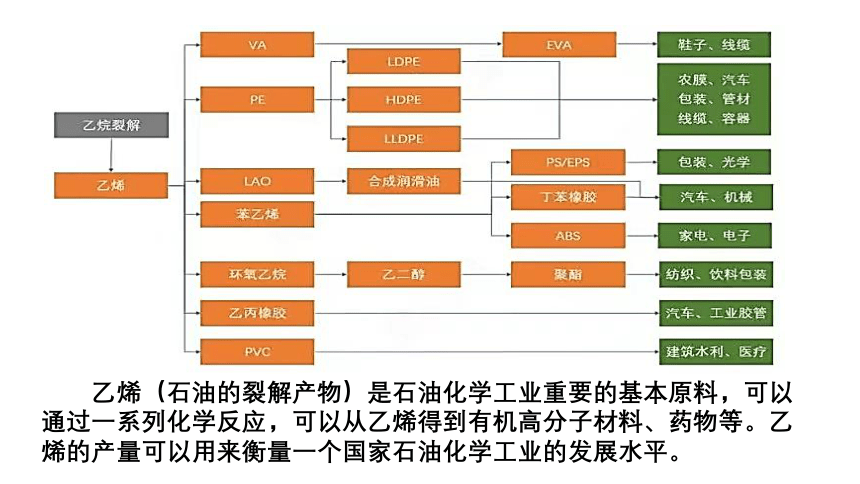
乙烯(石油的裂解产物)是石油化学工业重要的基本原料,可以通过一系列化学反应,可以从乙烯得到有机高分子材料、药物等。乙烯的产量可以用来衡量一个国家石油化学工业的发展水平。
一、乙烯的组成和结构
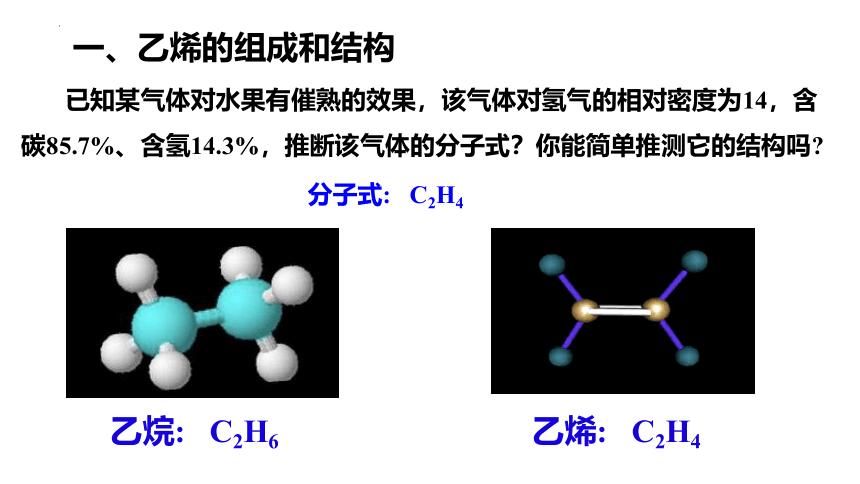
已知某气体对水果有催熟的效果,该气体对氢气的相对密度为14,含碳85.7%、含氢14.3%,推断该气体的分子式?你能简单推测它的结构吗
分子式: C2H4
乙烷: C2H6
乙烯: C2H4
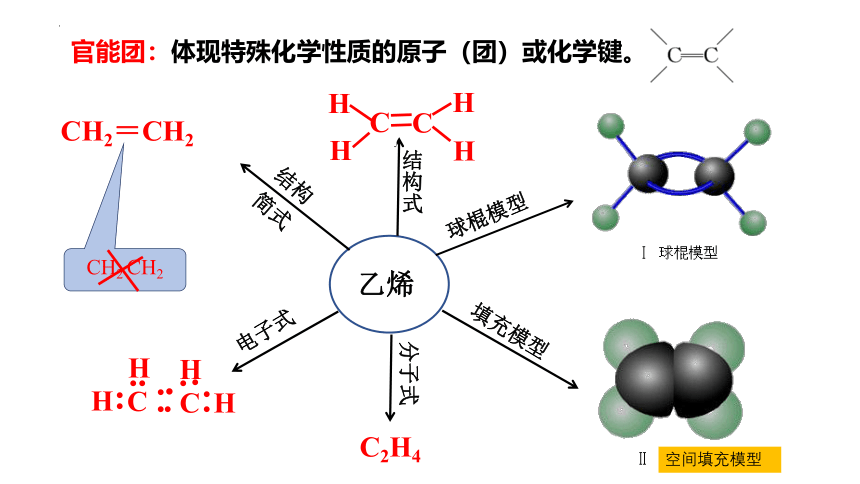
乙烯
分子式
电子式
球棍模型
填充模型
结构式
C2H4
CH2=CH2
C
C
H
H
H
H
C
C
H
H
H
H
CH2 CH2
结构
简式
空间填充模型
官能团:体现特殊化学性质的原子(团)或化学键。
乙烯的空间结构
共平面
6原子共平面
C
C
H
H
H
H
345 kJ mol—1
265 kJ mol—1
不可旋转
不是两个 的简单组合, 中有一个键比较特殊,比通常的 键能小,比较活泼,键容易断裂。
【小试牛刀】下列说法正确的是( )
A.乙烯的结构简式可书写为CH2CH2
B.乙烯的充填模型为
C.乙烯分子中所有原子共平面,可推断丙稀(CH2=CH—CH3)所有原子也共平面
D.乙烯分子中的价键没有全部被氢原子“饱和”,因此乙烯属于不饱和烃
D
二、乙烯的物理性质
无色
稍有气味
难溶于水
排水法
密度:
气味 :
收集方法:
颜色 :
水溶性:
状态 :
气体
比空气略小(相对分子质量28)
三、乙烯的化学性质
1.氧化反应
(1)在空气中燃烧 【实验7-1】(1)
乙烯在空气中燃烧、火焰明亮且伴有黑烟,生成二氧化碳和水,同时放出大量热。
C2H4+3O2 2CO2+2H2O
点燃
产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光。乙烯中含有碳碳双键,含碳量比甲烷高。
(2)与酸性高锰酸钾溶液反应【实验7-1】(2)
5CH2=CH2+12KMnO4+18H2SO4=
12MnSO4+10CO2+28H2O+6K2SO4
5CH2=CH2+12MnO4-+36H+=12Mn2++10CO2+28H2O
紫红色褪去
2.加成反应
【实验7-3】与溴的四氯化碳溶液反应
【实验7-3】将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
现象:乙烯使溴的四氯化碳溶液或溴水褪色
2.加成反应
乙烯通入溴的CCl4溶液时,乙烯双键中一个键断裂,两个溴原子分别加在两个价健不饱和的碳原子上,生成无色的1,2-二溴乙烷液体
CH2=CH2+Br2 CH2Br-CH2Br
1,2 – 二溴乙烷
H—C=C—H
H H
Br Br
Br Br
H—C C—H
H H
同时断键
乙烯与烷烃鉴别、除杂
(无色油状液体)
乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应。
2.加成反应
(溴水、溴的CCl4溶液)
有机物分子中的不饱和键(双键 或 三键)两端的碳原子与其他原子或原子团直接结合成新化合物的反应叫加成反应。
CH2=CH2 + Cl2 CH2ClCH2Cl
CH2=CH2 + H2 CH3CH3
催化剂
CH2=CH2 + HCl CH3CH2Cl
催化剂
1, 2 - 二氯乙烷,无色液体
乙烷,无色气体
氯乙烷,无色液体
乙醇,无色液体
CH2=CH2 + H2O CH3CH2OH
催化剂
加热,加压
工业上可利用乙烯与水的加成反应制取乙醇
我是溴分子
2.加成反应
我是乙烯分子
【小试牛刀】判断下列反应类型
(1)CH3CH3 +Br2 CH3CH2Br+HBr
(2)CH3CH2OH +HBr CH3CH2Br +H2O
取代反应
(3)CH2=CH2 +HBr CH3CH2Br
催化剂
(4)CH3CCH3 +H2 CH3CHCH3
催化剂
O
OH
(5)C2H4 +3O2 2CO2+2H2O
点燃
取代反应
加成反应
加成反应
氧化反应
类型 取代反应 加成反应
反应物结构特征
生成物种类
碳碳键变化情况
结构变化形式
含有易被取代的原子或原子团
不饱和有机化合物
两种
(有机物+无机物)
一种(有机物)
无变化
不饱和键打开
等价替换式
开键加合式
小结:取代反应和加成反应的对比
【小试牛刀】在一定条件下乙烷和乙烯都能制备氯乙烷CH3CH2Cl。试回答:
①乙烷制氯乙烷的化学方程式是
_____________________________________;该反应类型是___________。
②乙烯制备氯乙烷的化学方程式是
___________________________________;该反应类型是_________。
③比较两种方法,________方法制备氯乙烷更好,原因是_______________________________________________________________
______________________________。
CH3CH3+ Cl2 CH3CH2Cl + HCl
光照
取代反应
加成反应
第2种
乙烷与Cl2发生取代反应,产物中有多种卤代烃;而乙烯与HCl发生加成
反应,产物单一。
CH2=CH2 + HCl
CH3-CH2Cl
催化剂
△
【再来一刀】已知:丙烯的结构简式为CH3-CH=CH2。请依据所学知识,回答下列问题:
(1)联想甲烷和乙烯,推测丙烯可能发生哪些类型的化学反应?
(2)丙烯若与HCl发生加成反应, 可能会生成哪些物质?
结构特点: 甲 烷 乙 烯
可能的化学反应:取代反应、氧化反应、加成反应
3.聚合反应——加聚反应
在适当的温度、压强和催化剂存在的条件下,乙烯分子中碳碳双键中的一个键断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物聚乙烯。
CH2=CH2+CH2=CH2+CH2=CH2+......
像这样,由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。聚合反应在有机高分子材料的生产中有着广泛的应用。乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
3.聚合反应
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
链节
聚合度
单体
单体:聚合成高分子化合物的小分子化合物,如CH2=CH2;
链节:高分子化合物中的最小重复单元,如 — CH2 — CH2 —;
聚合度:高分子化合物中的链节数,如聚乙烯中的n。
注意 (1)单烯烃的聚合物中碳碳之间是单键,不存在碳碳双键,不具备碳碳双键的性质。
(2)高分子化合物虽被称为“化合物”,但由于高分子化合物中的n不同,所以高分子化合物均为混合物,而不是纯净物。
【小试牛刀】仿照乙烯的加聚反应,写出丙烯的加聚反应方程式 。
其中链节为 ,聚合度是 ,单体是 。
—CH2—CH—
|
CH3
n
CH2=CH-CH3
nCH2=CH-CH3
催化剂
[ CH2—CH ]n
|
CH3
聚丙烯 (PP)
【再来一刀】①氯乙烯的加聚反应 。
②聚苯乙烯:
③有机玻璃:
nCH2=CHCl
催化剂
—CH2-CH—
|
Cl
[ ]n
(PVC)
催化剂
(PS)
nCH2=CH-COOCH3
催化剂
[ ]n
COOCH3
|
(PMMA)
—CH2-CH—
四、乙烯的用途
1.重要的基本化工原料,可制取酒精、橡胶、塑料等
2.植物生长调节剂和水果的催熟剂。
乙烯
乙烯
石油经过分馏、裂化、裂解,可以得到乙烯。
乙烯的产量可以用来衡量一个国家的石油化工水平。
五.乙烯的来源
归纳总结
分子结构
化学性质
物理性质
用途
决定
决定
乙烯
决定
氧化反应
加成反应
聚合反应
平面型
有碳碳双键
无色气体
略有气味
难溶于水
ρ乙烯<ρ空气
产量衡量一个国家化工产业的发展水平
植物生长调节剂
碳在地壳中的含量很低,但是含有碳元素的有机化合物却分布极广。有机化合物不仅构成了生机勃勃的生命世界,也是燃料、材料、食品和药物的主要来源。
与无机化合物相比,有机化合物的组成元素并不复杂,但化合物数量众多,性质各异。对有机化合物的研究,需要在了解碳原子成键规律的基础上,认识有机化合物的分子结构,以及决定其分类与性质的特征基团。进而认识有机化学反应,实现有机化合物之间的转化,合成新的物质。
●认识有机化合物
●乙烯与有机高分子材料
●乙醇与乙酸
●基本营养物质
组织建设
第二节 乙烯与有机高分子材料
(第1课时 乙烯)
第七章 有机化合物
生活小窍门
把未熟的青香蕉和熟苹果放在同一个塑料袋里,系紧袋口,放置一段时间,你会发现?
震惊!青香蕉熟了
成熟的苹果会产生乙烯, 果实中乙烯含量增加时, 可促进其中有机物质的转化,加速成熟,故可以催熟香蕉。
乙烯(石油的裂解产物)是石油化学工业重要的基本原料,可以通过一系列化学反应,可以从乙烯得到有机高分子材料、药物等。乙烯的产量可以用来衡量一个国家石油化学工业的发展水平。
一、乙烯的组成和结构
已知某气体对水果有催熟的效果,该气体对氢气的相对密度为14,含碳85.7%、含氢14.3%,推断该气体的分子式?你能简单推测它的结构吗
分子式: C2H4
乙烷: C2H6
乙烯: C2H4
乙烯
分子式
电子式
球棍模型
填充模型
结构式
C2H4
CH2=CH2
C
C
H
H
H
H
C
C
H
H
H
H
CH2 CH2
结构
简式
空间填充模型
官能团:体现特殊化学性质的原子(团)或化学键。
乙烯的空间结构
共平面
6原子共平面
C
C
H
H
H
H
345 kJ mol—1
265 kJ mol—1
不可旋转
不是两个 的简单组合, 中有一个键比较特殊,比通常的 键能小,比较活泼,键容易断裂。
【小试牛刀】下列说法正确的是( )
A.乙烯的结构简式可书写为CH2CH2
B.乙烯的充填模型为
C.乙烯分子中所有原子共平面,可推断丙稀(CH2=CH—CH3)所有原子也共平面
D.乙烯分子中的价键没有全部被氢原子“饱和”,因此乙烯属于不饱和烃
D
二、乙烯的物理性质
无色
稍有气味
难溶于水
排水法
密度:
气味 :
收集方法:
颜色 :
水溶性:
状态 :
气体
比空气略小(相对分子质量28)
三、乙烯的化学性质
1.氧化反应
(1)在空气中燃烧 【实验7-1】(1)
乙烯在空气中燃烧、火焰明亮且伴有黑烟,生成二氧化碳和水,同时放出大量热。
C2H4+3O2 2CO2+2H2O
点燃
产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光。乙烯中含有碳碳双键,含碳量比甲烷高。
(2)与酸性高锰酸钾溶液反应【实验7-1】(2)
5CH2=CH2+12KMnO4+18H2SO4=
12MnSO4+10CO2+28H2O+6K2SO4
5CH2=CH2+12MnO4-+36H+=12Mn2++10CO2+28H2O
紫红色褪去
2.加成反应
【实验7-3】与溴的四氯化碳溶液反应
【实验7-3】将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
现象:乙烯使溴的四氯化碳溶液或溴水褪色
2.加成反应
乙烯通入溴的CCl4溶液时,乙烯双键中一个键断裂,两个溴原子分别加在两个价健不饱和的碳原子上,生成无色的1,2-二溴乙烷液体
CH2=CH2+Br2 CH2Br-CH2Br
1,2 – 二溴乙烷
H—C=C—H
H H
Br Br
Br Br
H—C C—H
H H
同时断键
乙烯与烷烃鉴别、除杂
(无色油状液体)
乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应。
2.加成反应
(溴水、溴的CCl4溶液)
有机物分子中的不饱和键(双键 或 三键)两端的碳原子与其他原子或原子团直接结合成新化合物的反应叫加成反应。
CH2=CH2 + Cl2 CH2ClCH2Cl
CH2=CH2 + H2 CH3CH3
催化剂
CH2=CH2 + HCl CH3CH2Cl
催化剂
1, 2 - 二氯乙烷,无色液体
乙烷,无色气体
氯乙烷,无色液体
乙醇,无色液体
CH2=CH2 + H2O CH3CH2OH
催化剂
加热,加压
工业上可利用乙烯与水的加成反应制取乙醇
我是溴分子
2.加成反应
我是乙烯分子
【小试牛刀】判断下列反应类型
(1)CH3CH3 +Br2 CH3CH2Br+HBr
(2)CH3CH2OH +HBr CH3CH2Br +H2O
取代反应
(3)CH2=CH2 +HBr CH3CH2Br
催化剂
(4)CH3CCH3 +H2 CH3CHCH3
催化剂
O
OH
(5)C2H4 +3O2 2CO2+2H2O
点燃
取代反应
加成反应
加成反应
氧化反应
类型 取代反应 加成反应
反应物结构特征
生成物种类
碳碳键变化情况
结构变化形式
含有易被取代的原子或原子团
不饱和有机化合物
两种
(有机物+无机物)
一种(有机物)
无变化
不饱和键打开
等价替换式
开键加合式
小结:取代反应和加成反应的对比
【小试牛刀】在一定条件下乙烷和乙烯都能制备氯乙烷CH3CH2Cl。试回答:
①乙烷制氯乙烷的化学方程式是
_____________________________________;该反应类型是___________。
②乙烯制备氯乙烷的化学方程式是
___________________________________;该反应类型是_________。
③比较两种方法,________方法制备氯乙烷更好,原因是_______________________________________________________________
______________________________。
CH3CH3+ Cl2 CH3CH2Cl + HCl
光照
取代反应
加成反应
第2种
乙烷与Cl2发生取代反应,产物中有多种卤代烃;而乙烯与HCl发生加成
反应,产物单一。
CH2=CH2 + HCl
CH3-CH2Cl
催化剂
△
【再来一刀】已知:丙烯的结构简式为CH3-CH=CH2。请依据所学知识,回答下列问题:
(1)联想甲烷和乙烯,推测丙烯可能发生哪些类型的化学反应?
(2)丙烯若与HCl发生加成反应, 可能会生成哪些物质?
结构特点: 甲 烷 乙 烯
可能的化学反应:取代反应、氧化反应、加成反应
3.聚合反应——加聚反应
在适当的温度、压强和催化剂存在的条件下,乙烯分子中碳碳双键中的一个键断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物聚乙烯。
CH2=CH2+CH2=CH2+CH2=CH2+......
像这样,由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。聚合反应在有机高分子材料的生产中有着广泛的应用。乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
3.聚合反应
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
链节
聚合度
单体
单体:聚合成高分子化合物的小分子化合物,如CH2=CH2;
链节:高分子化合物中的最小重复单元,如 — CH2 — CH2 —;
聚合度:高分子化合物中的链节数,如聚乙烯中的n。
注意 (1)单烯烃的聚合物中碳碳之间是单键,不存在碳碳双键,不具备碳碳双键的性质。
(2)高分子化合物虽被称为“化合物”,但由于高分子化合物中的n不同,所以高分子化合物均为混合物,而不是纯净物。
【小试牛刀】仿照乙烯的加聚反应,写出丙烯的加聚反应方程式 。
其中链节为 ,聚合度是 ,单体是 。
—CH2—CH—
|
CH3
n
CH2=CH-CH3
nCH2=CH-CH3
催化剂
[ CH2—CH ]n
|
CH3
聚丙烯 (PP)
【再来一刀】①氯乙烯的加聚反应 。
②聚苯乙烯:
③有机玻璃:
nCH2=CHCl
催化剂
—CH2-CH—
|
Cl
[ ]n
(PVC)
催化剂
(PS)
nCH2=CH-COOCH3
催化剂
[ ]n
COOCH3
|
(PMMA)
—CH2-CH—
四、乙烯的用途
1.重要的基本化工原料,可制取酒精、橡胶、塑料等
2.植物生长调节剂和水果的催熟剂。
乙烯
乙烯
石油经过分馏、裂化、裂解,可以得到乙烯。
乙烯的产量可以用来衡量一个国家的石油化工水平。
五.乙烯的来源
归纳总结
分子结构
化学性质
物理性质
用途
决定
决定
乙烯
决定
氧化反应
加成反应
聚合反应
平面型
有碳碳双键
无色气体
略有气味
难溶于水
ρ乙烯<ρ空气
产量衡量一个国家化工产业的发展水平
植物生长调节剂
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
