浙江省2023年中考科学模拟题知识点分类汇编-07金属(含解析)
文档属性
| 名称 | 浙江省2023年中考科学模拟题知识点分类汇编-07金属(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 689.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-05-17 00:00:00 | ||
图片预览



文档简介
浙江省2023年中考科学模拟题知识点分类汇编-07金属
一、选择题
1.(2023·浙江·一模)第19届亚运会将于2023年9月23日起在杭州举行,下列说法错误的是( )
A.奥体主体育场屋面采用的新材料铝镁锰板,属于金属材料
B.主体育场的“花瓣”钢结构造型采用压弯成型技术,利用了金属的延展性
C.亚运火炬“薪火”的燃料是生物质燃气(主要成分、CO),利用了它们的可燃性
D.奥体游泳馆内的水经循环过滤、消毒、杀菌后,水质达到饮用水标准,属于纯净物
2.(2023·浙江·一模)将一定量的锌粉加入含有硝酸铜和硝酸银的废液中,充分反应后过滤,得到滤渣和滤液,下列说法错误的是( )
A.若向滤渣中滴加稀盐酸没有气泡,则滤渣中一定有银,可能有铜
B.若向滤渣中滴加稀盐酸有气泡,则滤渣中一定有锌、铜和银
C.若滤液呈蓝色,则滤液中的溶质一定有硝酸铜
D.若滤液呈无色,则滤液中的溶质有硝酸锌和硝酸银
3.(2023·浙江·一模)重建后的雷峰塔是中国第一座彩色铜雕塔,其斗拱部分的材料为铜、锌组成的黄铜,黄铜这种材料属于( )
A.金属材料 B.非金属材料
C.有机合成材料 D.陶瓷材料
4.(2023·浙江·一模)2022年10月一项报告显示今年会有53亿只手机成为电子垃圾。为了回收手机中的铁与银,某公司向含有硝酸亚铁、硝酸银的浸泡液中逐渐加入锌粒,溶液质量变化如图,下列说法错误的是( )
A.b点对应的溶液颜色为浅绿色
B.d点存在两种溶质
C.向e点的对应的物质中加入盐酸,不会有气泡产生
D.ac段发生的反应为
5.(2023·浙江·一模)科学应基于证据与逻辑得出结论。关于下列四个实验的有关证据和结论的说法正确的是( )
A. ①中生成黄色沉淀是结论,硝酸铅与碘化钾发生了化学反应是证据
B. ②中根据生成物不能被磁铁吸引的证据,得出金属都能与非金属反应的结论
C. ③中得出某血管是小动脉的结论,基于的证据是观察到血管中的血液是鲜红色的
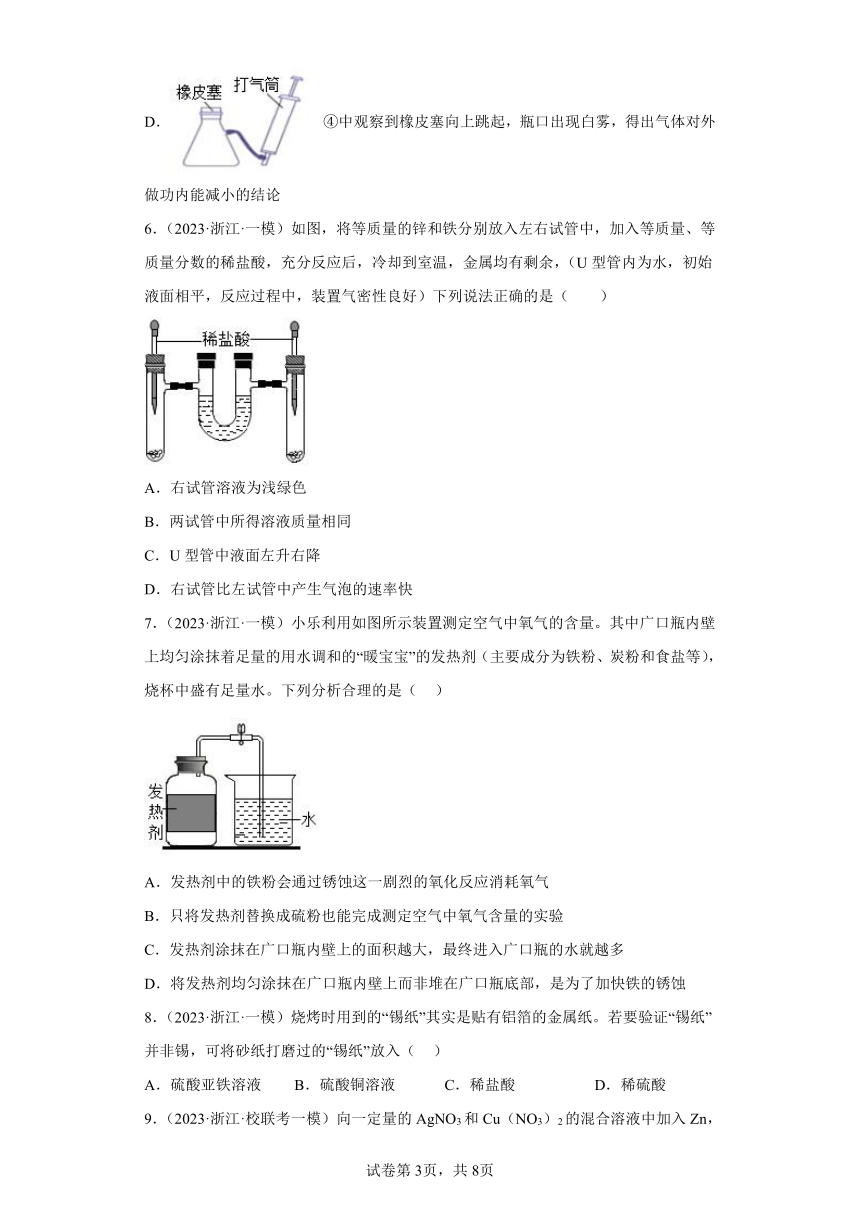
D. ④中观察到橡皮塞向上跳起,瓶口出现白雾,得出气体对外做功内能减小的结论
6.(2023·浙江·一模)如图,将等质量的锌和铁分别放入左右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中,装置气密性良好)下列说法正确的是( )
A.右试管溶液为浅绿色
B.两试管中所得溶液质量相同
C.U型管中液面左升右降
D.右试管比左试管中产生气泡的速率快
7.(2023·浙江·一模)小乐利用如图所示装置测定空气中氧气的含量。其中广口瓶内壁上均匀涂抹着足量的用水调和的“暖宝宝”的发热剂(主要成分为铁粉、炭粉和食盐等),烧杯中盛有足量水。下列分析合理的是( )
A.发热剂中的铁粉会通过锈蚀这一剧烈的氧化反应消耗氧气
B.只将发热剂替换成硫粉也能完成测定空气中氧气含量的实验
C.发热剂涂抹在广口瓶内壁上的面积越大,最终进入广口瓶的水就越多
D.将发热剂均匀涂抹在广口瓶内壁上而非堆在广口瓶底部,是为了加快铁的锈蚀
8.(2023·浙江·一模)烧烤时用到的“锡纸”其实是贴有铝箔的金属纸。若要验证“锡纸”并非锡,可将砂纸打磨过的“锡纸”放入( )
A.硫酸亚铁溶液 B.硫酸铜溶液 C.稀盐酸 D.稀硫酸
9.(2023·浙江·校联考一模)向一定量的AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如下图所示,下列说法正确的是( )
A.a点溶液中有2种阳离子
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段溶液,滴加稀盐酸,会产生白色沉淀
D.若取d点固体,有反应生成的铜与银,加入稀盐酸则无气泡产生
10.(2023·浙江·一模)在5.6g铁粉中,先逐滴加入一定量的Cu(NO3)2溶液,充分反应后再逐滴加入AgNO3溶液,剩余固体质量与所加溶液总质量的关系如图所示。下列说法正确的是( )
A.所加溶液质量为M1g时,生成Cu的质量为m1g
B.bc段发生的是Cu和AgNO3溶液的反应
C.m3的值为21.6
D.e点溶液中不含Cu(NO3)2
11.(2023·浙江·校联考一模)如图是一款变色眼镜,它的镜片内含有溴化银和氧化铜。在强光照射下,溴化银分解成单质溴和银,镜片颜色变深:当光线变暗时在氧化铜催化作用下,又立即化合成溴化银,镜片颜色变浅。有关该眼镜的说法错误的是( )
A.塑料是有机合成材料
B.钛合金属于化合物
C.溴化银分解后,银元素的化合价降低
D.溴和银化合成溴化银前后,氧化铜化学性质不变
二、探究题
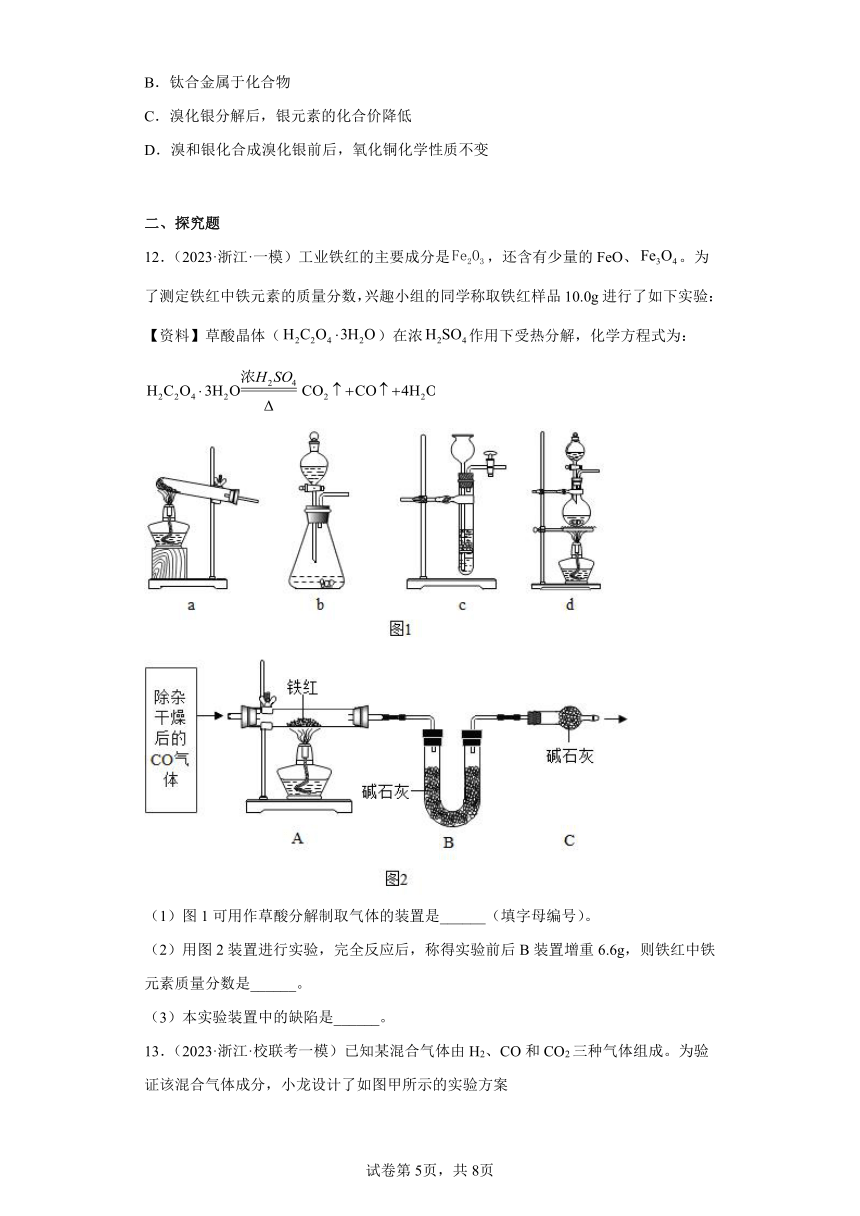
12.(2023·浙江·一模)工业铁红的主要成分是,还含有少量的FeO、。为了测定铁红中铁元素的质量分数,兴趣小组的同学称取铁红样品10.0g进行了如下实验:
【资料】草酸晶体()在浓作用下受热分解,化学方程式为:
(1)图1可用作草酸分解制取气体的装置是______(填字母编号)。
(2)用图2装置进行实验,完全反应后,称得实验前后B装置增重6.6g,则铁红中铁元素质量分数是______。
(3)本实验装置中的缺陷是______。
13.(2023·浙江·校联考一模)已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,小龙设计了如图甲所示的实验方案
根据方案回答下列问题
(1)装置A、C、F装的都是澄清石灰水,但它们的作用各不相同。装置F在实验中的作用是______。
(2)小港认为CD装置之间还应增加一个气体干燥装置,你是否赞成他的想法,请说明理由:______。
(3)图甲方案B装置可用来吸收二氧化碳但没有现象。为证明CO2和NaOH能发生反应,小龙又设计了图乙所示的方案。则图乙方案中所加的X试剂应该是NaOH和______的混合溶液。
三、简答题
14.(2023·浙江·一模)小金用如图所示的实验装置模拟工业炼铁,选用CO和氧化铁样品(含少量杂质)进行反应。
(1)实验开始时应______(填序号)。
A.先加热,再通入一氧化碳 B.先通一氧化碳,再加热
(2)装置B的作用除吸收外,还起到的作用是______。
(3)小金取氧化铁样品20g,若经过充分反应,测量反应前、后装置A处大玻璃管的质量减少了4.8g,则该氧化铁样品中氧化铁的质量分数为______。
15.(2023·浙江·二模)据报道,每年因锈蚀而报废的铁制品约占当年产量的20%-40%。
(1)铁制品生锈的条件是___________。
(2)现从铁锈中得到氧化铁,让其与足量一氧化碳充分反应,可得到铁的质量是多少g?___________
四、填空题
16.(2023·浙江·一模)地球表面的70%以上是海洋,开发利用海洋前景广阔。
潮汐发电:人们在靠近海的河口或海湾深处建挡海大坝,在大坝中间装上水轮发电机,涨潮时,海水通过大坝流进河口,带动水轮发电机发电,如图甲所示;退潮时,海水又流回海洋,从相反方向带动水轮发电机发电。
海水淡化:人们利用人造纤维制成“人工膜”进行海水淡化。预处理的海水加压后,水分子可通过“人工膜”,而海水中的其他微粒则无法通过,从而得到淡水和浓盐水。浓盐水中含大量MgCl2,又可用于制备金属镁,其工艺流程如图乙所示。
(1)潮汐发电是将海水的______能转化为电能,水轮发电机是应用______原理制成的;
(2)“人工膜”是受细胞膜的启发而制造出来的,它模拟了细胞膜的______(填写功能);
(3)制备金属镁的步骤①使用石灰乳,而不用澄清石灰水的原因是______;浓盐水经过步骤①和②两步反应后又获得了MgCl2,设计这两个步骤的目的是______。
17.(2023·浙江·一模)向盛有足量稀盐酸的烧杯中加入一定量的黄铜(铜和锌的合金)粉末,充分反应后过滤、并对滤渣进行洗涤。
(1)稀盐酸和黄铜粉末反应前后,烧杯中溶液里的离子种类如图所示,“”表示的离子是______(填写离子符号)。
(2)若要检验滤渣是否洗涤干净,可向最后一次洗涤液中滴入适量______溶液和足量稀硝酸,观察是否有沉淀生成。
18.(2023·浙江·二模)向盛有X溶液的烧杯中加入Y物质(过量)后发生化学反应,反应前后烧杯中溶液里的离子及比例关系如图所示,则烧杯中反应的化学方程式是___________;反应后溶液的质量___________(选填“增加”“减少”或“不变”)。
参考答案:
1.D
【详解】A、金属材料包括纯金属和合金,奥体主体育场屋面采用的新材料铝镁锰板,属于金属材料 ,说法正确;
B、主体育场的“花瓣”钢结构造型采用压弯成型技术,利用了金属的延展性,说法正确;
C、 亚运火炬“薪火”的燃料是生物质燃气(主要成分 H2 、CO),利用了它们的可燃性,说法正确;
D、 奥体游泳馆内的水经循环过滤、消毒、杀菌后,水质达到饮用水标准,在此过程中没有除去水中可溶性杂质,属于混合物,不属于纯净物,说法错误。
故选D。
2.D
【分析】锌、铜、银三种金属的活动性由强到弱的顺序是锌、铜、银,将一定量的锌粉加入含有硝酸铜和硝酸银的废液中,锌先与硝酸银反应生成硝酸锌和银,硝酸银完全反应后,剩余的锌再与硝酸铜反应生成硝酸锌和铜。
【详解】A、滤渣中加入稀盐酸无气泡产生,即滤渣中不含锌,锌完全反应,将一定量的锌粉加入含有硝酸铜和硝酸银的废液中,锌先与硝酸银反应生成硝酸锌和银,硝酸银完全反应后,剩余的锌再与硝酸铜反应生成硝酸锌和铜,滤渣中一定有银,可能有铜,说法正确;
B、滤渣中加入稀盐酸有气泡产生,即反应后锌有剩余,硝酸铜与硝酸银完全反应,则滤渣中一定有锌、铜和银,说法正确;
C、过滤后的滤液为蓝色,即滤液中含有硝酸铜,说法正确;
D、过滤后的滤液为无色,即硝酸银与硝酸铜完全反应,则滤液中的溶质一定有硝酸锌,一定没有硝酸银,说法错误。
故选D。
3.A
【详解】金属材料包括合金和纯金属,黄铜是铜锌合金,属于金属材料 。
故选A。
4.C
【详解】A、ac段的反应是锌和硝酸银反应生成硝酸锌和银,硝酸亚铁还没参与反应,则b点对应的溶液颜色为浅绿色,故选项说法正确;
B、d点时硝酸银已经完全反应,硝酸亚铁还没反应完,则d点存在生成的硝酸锌和没反应完的硝酸亚铁两种溶质,故选项说法正确;
C、e点时锌和硝酸银、硝酸亚铁恰好完全反应,对应物质中有生成的铁、银,铁和盐酸反应会生成氢气,则向e点的对应的物质中加入盐酸,会有气泡产生,故选项说法错误;
D、ac段是锌和硝酸银反应,发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag,故选项说法正确。
故选C。
5.D
【详解】A、①硝酸铅和碘化钾发生反应,产生硝酸钾和碘化铅,碘化铅是金黄色的沉淀,所以①中生成黄色沉淀是实验现象,硝酸铅与碘化钾发生了化学反应是实验过程,故A错误;
B、②加热铁粉和硫磺粉混合,铁粉与硫磺反应生成硫化亚铁,而硫化亚铁是一种新物质,它不具有铁的性质,不会被磁铁吸引,不能得出金属与非金属反应的结论,比如,金属铂、金等很稳定,跟许多非金属都不反应,故B错误;
C、③判断小鱼尾部小动脉的依据是血液流动的方向,是由主干流向分支,而不是血液的颜色,故C错误;
D、④橡皮塞向上跳起,瓶口出现白雾,因为瓶内气压达到一定程度,气体对外做功,内能转化成机械能,塞子获得了机械能向上跳起,同时气体的内能减少,温度降低,瓶口周围的气体液化成小水滴,这些小水滴就是看到的白雾,得出气体对外做功内能减小的结论,故D正确。
故选D。
6.A
【分析】锌和稀盐酸反应生成氯化锌和氢气,铁和稀盐酸反应生成氯化亚铁和氢气,氯化亚铁溶液是浅绿色的;金属均有剩余,说明稀盐酸不足,进一步说明两个反应中生成的氢气质量相等。
【详解】A、铁与稀盐酸反应生成氯化亚铁和氢气,氯化亚铁溶液是浅绿色的,故右试管中的现象是产生大量的气泡,溶液由无色变成浅绿色,正确;
B、根据化学方程式Zn+ 2HCl = ZnCl2 + H2↑、Fe + 2HC = FeCl2 + H2↑ 可知,每65份质量锌与73质量的盐酸能生成2份质量氢气,每56份质量铁与73质量的盐酸能生成2份质量氢气,等质量、等质量分数的稀盐酸分别与足量的锌、铁反应,生成氢气的质量相等,但消耗的锌的质量更多,故左边试管中溶液的质量更大,错误;
C、选项B的分析可知,生成的氢气的质量相等,即左右两边的压强相等,那么U型管中液面持平,错误;
D、锌比铁活泼,故与稀盐酸反应的速率更快,即左试管中产生的气泡速率快,错误。
故选A。
【点睛】等质量的金属(生成物中金属的化合价相同)与相同的酸反应,若酸过量,那么金属的相对原子质量越小,生成的氢气的质量越多;若金属过量,那么生成的氢气的质量相等。
7.D
【详解】A、铁锈蚀过程速度较慢,属于缓慢氧化,发热剂中的铁粉会通过锈蚀这一缓慢的氧化反应消耗氧气,错误;
B、 只将发热剂替换成硫粉不能完成测定空气中氧气含量的实验 ,原因硫在空气中燃烧生二氧化硫气体,瓶内气压不变小,水不能倒流,不能确定空气中氧气的含量,错误;
C、空气中氧气含量是一定的,发热剂涂抹在广口瓶内壁上的面积越大,最终进入广口瓶的水不会越多,错误;
D、 将发热剂均匀涂抹在广口瓶内壁上而非堆在广口瓶底部,增大发热剂与空气的接触面积,是为了加快铁的锈蚀,正确。
故选D。
8.A
【详解】A、硫酸亚铁只与铝反应,和锡不反应,能证明,符合题意;
B、两种金属都能置换出硫酸铜中的铜,不能证明,不符合题意;
C、铝和锡都能和稀盐酸反应,不能证明,不符合题意;
D、铝和锡都能和稀硫酸反应,不能证明,不符合题意。
故选A。
9.B
【分析】当锌和硝酸银反应,由于进入溶液的锌的质量小于析出银的质量,所以溶液质量是减小的,即ab段。当锌和硝酸铜反应时,由于进入溶液锌的质量大于析出铜的质量,所以溶液质量是增大的,即bc段。当硝酸铜完全反应后,锌不再参加反应,因此溶液的质量保持不变,即cd段。
【详解】A.a点时,锌正在和硝酸银反应,而硝酸铜还为开始反应,则此时溶液中的阳离子为Zn2+,Cu2+和没有反应完的Ag+,故A错误;
B.c点时,硝酸银和硝酸铜恰好完全反应,此时的溶质只有反应产物硝酸锌,故B正确;
C.b~c段,锌再和硝酸铜反应,此时溶质为硝酸锌和硝酸铜,如果滴加稀盐酸,那么不会产生沉淀,故C错误;
D.d点时,加入的锌过量,此时固体为锌、铜和银,加入稀盐酸后,锌会和稀盐酸反应生成氢气,故D错误。
故选B。
10.C
【分析】首先,ab段,铁粉与硝酸铜发生置换反应,M1点时,硝酸铜被完全消耗,之后bc段铁粉与硝酸银发生置换反应,直到M2点时铁粉消耗完毕,然后cd段之前生成的铜与硝酸银发生置换反应,直至M3点时,铜被完全消耗;
【详解】A、设有质量为x的铁粉与硝酸铜反应,并生成质量为y的铜,
解方程组得y=8(m1-5.6)g,不符合题意。
B、bc段是铁粉与硝酸银发生置换反应,不符合题意。
C、M3点时铁粉被完全消耗,沉淀完全是Ag,整体反应过程相当于铁粉与硝酸银发生置换反应,设生成Ag的质量为x,则有:
解得x=21.6g,符合题意。
D、cd段之前生成的铜与硝酸银发生置换反应生成了银单质和硝酸铜溶液,后面在滴加硝酸银也不会与硝酸铜反应,因此e点含有硝酸铜存在,不符合题意。
故选C。
【点睛】bc的斜率大于cd的斜率,而相对原子质量是Ag>Cu>Fe,在结合题干和所学知识,可以得出b点的转折是因为硝酸铜被完全消耗,而不是铁粉被完全消耗。
11.B
【详解】A、塑料属于三大高分子合成材料之一,故选项说法正确;
B、钛合金含有多种物质,属于混合物,故选项说法错误;
C、在强光照射下,溴化银分解成单质溴和银,银元素的化合价由+1价变为0价,化合价降低,故选项说法正确;
D、溴和银在氧化铜催化作用下,又立即化合成溴化银,氧化铜作催化剂,反应前后氧化铜化学性质不变,故选项说法正确。
故选B。
12. d 76% 缺少尾气处理装置
【详解】(1)草酸晶体(H2C2O4 3H2O)在浓硫酸作用下受热分解,该反应的反应物状态是固体和液体,反应条件是加热,因此选用d装置;
(2)铁的氧化物与一氧化碳在高温条件反应生成铁和二氧化碳,碱石灰能吸收二氧化碳,B装置增重6.6g,那么反应生成的二氧化碳是6.6g,氧元素的质量=,因为4.8g氧元素的质量一半来自于一氧化碳,一半来自于铁的氧化物,那么铁红中氧元素的质量是4.8g÷2=2.4g,则铁红中铁的质量分数=;
(3)实验装置的一个明显缺陷是没有处理一氧化碳,一氧化碳进入空气中会污染环境。
13. 检验装置D中是否生成CO2(或“检验混合气体中是否存在“CO”也可) 赞成,装置E可以根据白色硫酸铜粉末是否变蓝检验水蒸气的存在,但该水蒸气可能是氢气与氧化铜反应产生,也可能是从装置C中带入的 氯化钡
【详解】(1)根据可用澄清石灰水检验二氧化碳气体知,装置A是为了检验混合气体中是否有二氧化碳;装置C在实验中的作用是检验二氧化碳气体是否除尽;装置F在实验中的作用是检验是否有二氧化碳生成。
(2)赞成小港的想法,因为装置E可以根据白色硫酸铜粉末是否变蓝检验水蒸气的存在,但该水蒸气可能是氢气与氧化铜反应产生,也可能是从装置C中带入的。
(3)二氧化碳与氯化钡不发生反应,当二氧化碳通入BaCl2和NaOH的混合溶液,二氧化碳与氢氧化钠先反应生成碳酸钠和水,碳酸钠与氯化钡反应生成碳酸钡沉淀,即可证明。
14. B 收集一氧化碳 80%
【详解】(1)一氧化碳是可燃性气体,与氧气或空气混合达到一定程度时遇明火会发生爆炸,为防止发生爆炸,实验开始时应先通一氧化碳,排尽空气,再加热。
故选B;
(2)一氧化碳密度小于氢氧化钠溶液的密度,装置B的作用除吸收外,还起到的作用是收集一氧化碳;
(3)根据化学方程式可知,后装置A处大玻璃管的质量减少了4.8g为氧化铁中氧元素的质量,则氧化铁的质量为
则该氧化铁样品中氧化铁的质量分数。
答:该氧化铁样品中氧化铁的质量分数80%。
15. 铁与氧气和水接触 5.6
【详解】(1)铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。铁制品生锈的条件是:铁与氧气和水接触;
(2)设:可得到铁的质量是x。
x=5.6g
答:可得到铁的质量是5.6g。
16. 机械 电磁感应 选择透过性 使用石灰乳,可以使镁离子充分反应,澄清石灰水中的氢氧化钙含量少,不能全部反应 减少镁的损失
【详解】(1)[1]潮汐发电是运用海水的运动带动水轮机转动来发电,所以是将海水的机械能转化为电能。
[2]水轮发电机中的线圈切割磁感线,产生感应电流,所以是运用电磁感应原理制成的。
(2)[3]由于细胞具有选择透过性,对细胞有用的物质可以进入,对细胞有害的物质不能进入,所以“人工膜”也是有选择的使有益的物质通过,模拟了细胞膜的选择透过性。
(3)[4]由于海水中有大量的镁离子,氢氧化钙微溶于水,所以澄清石灰水不能使海水中的镁离子全部发生反应,故使用石灰乳而不使用澄清石灰水。
[5]经过步骤①和②两步反应后,海水中的镁离子基本反应完成,能有效的减少镁的流失。
17. Zn2+ 硝酸银/ AgNO3
【详解】(1)在金属活动顺序中,锌排在氢之前,能与稀盐酸反应生成氯化锌和氢气,铜排在氢之后,不能与稀盐酸反应,稀盐酸和黄铜粉末反应前后,烧杯中溶液里的离子种类如图所示,“” 表示的离子是氯离子,“” 表示的离子是氢离子,“”表示的离子是锌离子,其离子符号为:Zn2+;
(2)若要检验滤渣是否洗涤干净,只要检验最后一次洗涤液中是否存在氯离子,氯离子能与硝酸银中银离子结合生成不溶于稀硝酸的氯化银白色沉淀,可向最后一次洗涤液中滴入适量硝酸银(AgNO3)溶液和足量稀硝酸,观察是否有沉淀生成。
18. Fe+CuCl2═FeCl2+Cu, 减少
【详解】由图中信息可知,反应前是氯化铜,反应后是氯化亚铁,说明铁和氯化铜反应生成了氯化亚铁和铜,反应的化学方程式是Fe+CuCl2═FeCl2+Cu,根据化学方程式可知,56份质量的铁反应生成64份质量的铜,反应后溶液质量减小。
试卷第1页,共3页
试卷第1页,共3页
一、选择题
1.(2023·浙江·一模)第19届亚运会将于2023年9月23日起在杭州举行,下列说法错误的是( )
A.奥体主体育场屋面采用的新材料铝镁锰板,属于金属材料
B.主体育场的“花瓣”钢结构造型采用压弯成型技术,利用了金属的延展性
C.亚运火炬“薪火”的燃料是生物质燃气(主要成分、CO),利用了它们的可燃性
D.奥体游泳馆内的水经循环过滤、消毒、杀菌后,水质达到饮用水标准,属于纯净物
2.(2023·浙江·一模)将一定量的锌粉加入含有硝酸铜和硝酸银的废液中,充分反应后过滤,得到滤渣和滤液,下列说法错误的是( )
A.若向滤渣中滴加稀盐酸没有气泡,则滤渣中一定有银,可能有铜
B.若向滤渣中滴加稀盐酸有气泡,则滤渣中一定有锌、铜和银
C.若滤液呈蓝色,则滤液中的溶质一定有硝酸铜
D.若滤液呈无色,则滤液中的溶质有硝酸锌和硝酸银
3.(2023·浙江·一模)重建后的雷峰塔是中国第一座彩色铜雕塔,其斗拱部分的材料为铜、锌组成的黄铜,黄铜这种材料属于( )
A.金属材料 B.非金属材料
C.有机合成材料 D.陶瓷材料
4.(2023·浙江·一模)2022年10月一项报告显示今年会有53亿只手机成为电子垃圾。为了回收手机中的铁与银,某公司向含有硝酸亚铁、硝酸银的浸泡液中逐渐加入锌粒,溶液质量变化如图,下列说法错误的是( )
A.b点对应的溶液颜色为浅绿色
B.d点存在两种溶质
C.向e点的对应的物质中加入盐酸,不会有气泡产生
D.ac段发生的反应为
5.(2023·浙江·一模)科学应基于证据与逻辑得出结论。关于下列四个实验的有关证据和结论的说法正确的是( )
A. ①中生成黄色沉淀是结论,硝酸铅与碘化钾发生了化学反应是证据
B. ②中根据生成物不能被磁铁吸引的证据,得出金属都能与非金属反应的结论
C. ③中得出某血管是小动脉的结论,基于的证据是观察到血管中的血液是鲜红色的
D. ④中观察到橡皮塞向上跳起,瓶口出现白雾,得出气体对外做功内能减小的结论
6.(2023·浙江·一模)如图,将等质量的锌和铁分别放入左右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中,装置气密性良好)下列说法正确的是( )
A.右试管溶液为浅绿色
B.两试管中所得溶液质量相同
C.U型管中液面左升右降
D.右试管比左试管中产生气泡的速率快
7.(2023·浙江·一模)小乐利用如图所示装置测定空气中氧气的含量。其中广口瓶内壁上均匀涂抹着足量的用水调和的“暖宝宝”的发热剂(主要成分为铁粉、炭粉和食盐等),烧杯中盛有足量水。下列分析合理的是( )
A.发热剂中的铁粉会通过锈蚀这一剧烈的氧化反应消耗氧气
B.只将发热剂替换成硫粉也能完成测定空气中氧气含量的实验
C.发热剂涂抹在广口瓶内壁上的面积越大,最终进入广口瓶的水就越多
D.将发热剂均匀涂抹在广口瓶内壁上而非堆在广口瓶底部,是为了加快铁的锈蚀
8.(2023·浙江·一模)烧烤时用到的“锡纸”其实是贴有铝箔的金属纸。若要验证“锡纸”并非锡,可将砂纸打磨过的“锡纸”放入( )
A.硫酸亚铁溶液 B.硫酸铜溶液 C.稀盐酸 D.稀硫酸
9.(2023·浙江·校联考一模)向一定量的AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如下图所示,下列说法正确的是( )
A.a点溶液中有2种阳离子
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段溶液,滴加稀盐酸,会产生白色沉淀
D.若取d点固体,有反应生成的铜与银,加入稀盐酸则无气泡产生
10.(2023·浙江·一模)在5.6g铁粉中,先逐滴加入一定量的Cu(NO3)2溶液,充分反应后再逐滴加入AgNO3溶液,剩余固体质量与所加溶液总质量的关系如图所示。下列说法正确的是( )
A.所加溶液质量为M1g时,生成Cu的质量为m1g
B.bc段发生的是Cu和AgNO3溶液的反应
C.m3的值为21.6
D.e点溶液中不含Cu(NO3)2
11.(2023·浙江·校联考一模)如图是一款变色眼镜,它的镜片内含有溴化银和氧化铜。在强光照射下,溴化银分解成单质溴和银,镜片颜色变深:当光线变暗时在氧化铜催化作用下,又立即化合成溴化银,镜片颜色变浅。有关该眼镜的说法错误的是( )
A.塑料是有机合成材料
B.钛合金属于化合物
C.溴化银分解后,银元素的化合价降低
D.溴和银化合成溴化银前后,氧化铜化学性质不变
二、探究题
12.(2023·浙江·一模)工业铁红的主要成分是,还含有少量的FeO、。为了测定铁红中铁元素的质量分数,兴趣小组的同学称取铁红样品10.0g进行了如下实验:
【资料】草酸晶体()在浓作用下受热分解,化学方程式为:
(1)图1可用作草酸分解制取气体的装置是______(填字母编号)。
(2)用图2装置进行实验,完全反应后,称得实验前后B装置增重6.6g,则铁红中铁元素质量分数是______。
(3)本实验装置中的缺陷是______。
13.(2023·浙江·校联考一模)已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,小龙设计了如图甲所示的实验方案
根据方案回答下列问题
(1)装置A、C、F装的都是澄清石灰水,但它们的作用各不相同。装置F在实验中的作用是______。
(2)小港认为CD装置之间还应增加一个气体干燥装置,你是否赞成他的想法,请说明理由:______。
(3)图甲方案B装置可用来吸收二氧化碳但没有现象。为证明CO2和NaOH能发生反应,小龙又设计了图乙所示的方案。则图乙方案中所加的X试剂应该是NaOH和______的混合溶液。
三、简答题
14.(2023·浙江·一模)小金用如图所示的实验装置模拟工业炼铁,选用CO和氧化铁样品(含少量杂质)进行反应。
(1)实验开始时应______(填序号)。
A.先加热,再通入一氧化碳 B.先通一氧化碳,再加热
(2)装置B的作用除吸收外,还起到的作用是______。
(3)小金取氧化铁样品20g,若经过充分反应,测量反应前、后装置A处大玻璃管的质量减少了4.8g,则该氧化铁样品中氧化铁的质量分数为______。
15.(2023·浙江·二模)据报道,每年因锈蚀而报废的铁制品约占当年产量的20%-40%。
(1)铁制品生锈的条件是___________。
(2)现从铁锈中得到氧化铁,让其与足量一氧化碳充分反应,可得到铁的质量是多少g?___________
四、填空题
16.(2023·浙江·一模)地球表面的70%以上是海洋,开发利用海洋前景广阔。
潮汐发电:人们在靠近海的河口或海湾深处建挡海大坝,在大坝中间装上水轮发电机,涨潮时,海水通过大坝流进河口,带动水轮发电机发电,如图甲所示;退潮时,海水又流回海洋,从相反方向带动水轮发电机发电。
海水淡化:人们利用人造纤维制成“人工膜”进行海水淡化。预处理的海水加压后,水分子可通过“人工膜”,而海水中的其他微粒则无法通过,从而得到淡水和浓盐水。浓盐水中含大量MgCl2,又可用于制备金属镁,其工艺流程如图乙所示。
(1)潮汐发电是将海水的______能转化为电能,水轮发电机是应用______原理制成的;
(2)“人工膜”是受细胞膜的启发而制造出来的,它模拟了细胞膜的______(填写功能);
(3)制备金属镁的步骤①使用石灰乳,而不用澄清石灰水的原因是______;浓盐水经过步骤①和②两步反应后又获得了MgCl2,设计这两个步骤的目的是______。
17.(2023·浙江·一模)向盛有足量稀盐酸的烧杯中加入一定量的黄铜(铜和锌的合金)粉末,充分反应后过滤、并对滤渣进行洗涤。
(1)稀盐酸和黄铜粉末反应前后,烧杯中溶液里的离子种类如图所示,“”表示的离子是______(填写离子符号)。
(2)若要检验滤渣是否洗涤干净,可向最后一次洗涤液中滴入适量______溶液和足量稀硝酸,观察是否有沉淀生成。
18.(2023·浙江·二模)向盛有X溶液的烧杯中加入Y物质(过量)后发生化学反应,反应前后烧杯中溶液里的离子及比例关系如图所示,则烧杯中反应的化学方程式是___________;反应后溶液的质量___________(选填“增加”“减少”或“不变”)。
参考答案:
1.D
【详解】A、金属材料包括纯金属和合金,奥体主体育场屋面采用的新材料铝镁锰板,属于金属材料 ,说法正确;
B、主体育场的“花瓣”钢结构造型采用压弯成型技术,利用了金属的延展性,说法正确;
C、 亚运火炬“薪火”的燃料是生物质燃气(主要成分 H2 、CO),利用了它们的可燃性,说法正确;
D、 奥体游泳馆内的水经循环过滤、消毒、杀菌后,水质达到饮用水标准,在此过程中没有除去水中可溶性杂质,属于混合物,不属于纯净物,说法错误。
故选D。
2.D
【分析】锌、铜、银三种金属的活动性由强到弱的顺序是锌、铜、银,将一定量的锌粉加入含有硝酸铜和硝酸银的废液中,锌先与硝酸银反应生成硝酸锌和银,硝酸银完全反应后,剩余的锌再与硝酸铜反应生成硝酸锌和铜。
【详解】A、滤渣中加入稀盐酸无气泡产生,即滤渣中不含锌,锌完全反应,将一定量的锌粉加入含有硝酸铜和硝酸银的废液中,锌先与硝酸银反应生成硝酸锌和银,硝酸银完全反应后,剩余的锌再与硝酸铜反应生成硝酸锌和铜,滤渣中一定有银,可能有铜,说法正确;
B、滤渣中加入稀盐酸有气泡产生,即反应后锌有剩余,硝酸铜与硝酸银完全反应,则滤渣中一定有锌、铜和银,说法正确;
C、过滤后的滤液为蓝色,即滤液中含有硝酸铜,说法正确;
D、过滤后的滤液为无色,即硝酸银与硝酸铜完全反应,则滤液中的溶质一定有硝酸锌,一定没有硝酸银,说法错误。
故选D。
3.A
【详解】金属材料包括合金和纯金属,黄铜是铜锌合金,属于金属材料 。
故选A。
4.C
【详解】A、ac段的反应是锌和硝酸银反应生成硝酸锌和银,硝酸亚铁还没参与反应,则b点对应的溶液颜色为浅绿色,故选项说法正确;
B、d点时硝酸银已经完全反应,硝酸亚铁还没反应完,则d点存在生成的硝酸锌和没反应完的硝酸亚铁两种溶质,故选项说法正确;
C、e点时锌和硝酸银、硝酸亚铁恰好完全反应,对应物质中有生成的铁、银,铁和盐酸反应会生成氢气,则向e点的对应的物质中加入盐酸,会有气泡产生,故选项说法错误;
D、ac段是锌和硝酸银反应,发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag,故选项说法正确。
故选C。
5.D
【详解】A、①硝酸铅和碘化钾发生反应,产生硝酸钾和碘化铅,碘化铅是金黄色的沉淀,所以①中生成黄色沉淀是实验现象,硝酸铅与碘化钾发生了化学反应是实验过程,故A错误;
B、②加热铁粉和硫磺粉混合,铁粉与硫磺反应生成硫化亚铁,而硫化亚铁是一种新物质,它不具有铁的性质,不会被磁铁吸引,不能得出金属与非金属反应的结论,比如,金属铂、金等很稳定,跟许多非金属都不反应,故B错误;
C、③判断小鱼尾部小动脉的依据是血液流动的方向,是由主干流向分支,而不是血液的颜色,故C错误;
D、④橡皮塞向上跳起,瓶口出现白雾,因为瓶内气压达到一定程度,气体对外做功,内能转化成机械能,塞子获得了机械能向上跳起,同时气体的内能减少,温度降低,瓶口周围的气体液化成小水滴,这些小水滴就是看到的白雾,得出气体对外做功内能减小的结论,故D正确。
故选D。
6.A
【分析】锌和稀盐酸反应生成氯化锌和氢气,铁和稀盐酸反应生成氯化亚铁和氢气,氯化亚铁溶液是浅绿色的;金属均有剩余,说明稀盐酸不足,进一步说明两个反应中生成的氢气质量相等。
【详解】A、铁与稀盐酸反应生成氯化亚铁和氢气,氯化亚铁溶液是浅绿色的,故右试管中的现象是产生大量的气泡,溶液由无色变成浅绿色,正确;
B、根据化学方程式Zn+ 2HCl = ZnCl2 + H2↑、Fe + 2HC = FeCl2 + H2↑ 可知,每65份质量锌与73质量的盐酸能生成2份质量氢气,每56份质量铁与73质量的盐酸能生成2份质量氢气,等质量、等质量分数的稀盐酸分别与足量的锌、铁反应,生成氢气的质量相等,但消耗的锌的质量更多,故左边试管中溶液的质量更大,错误;
C、选项B的分析可知,生成的氢气的质量相等,即左右两边的压强相等,那么U型管中液面持平,错误;
D、锌比铁活泼,故与稀盐酸反应的速率更快,即左试管中产生的气泡速率快,错误。
故选A。
【点睛】等质量的金属(生成物中金属的化合价相同)与相同的酸反应,若酸过量,那么金属的相对原子质量越小,生成的氢气的质量越多;若金属过量,那么生成的氢气的质量相等。
7.D
【详解】A、铁锈蚀过程速度较慢,属于缓慢氧化,发热剂中的铁粉会通过锈蚀这一缓慢的氧化反应消耗氧气,错误;
B、 只将发热剂替换成硫粉不能完成测定空气中氧气含量的实验 ,原因硫在空气中燃烧生二氧化硫气体,瓶内气压不变小,水不能倒流,不能确定空气中氧气的含量,错误;
C、空气中氧气含量是一定的,发热剂涂抹在广口瓶内壁上的面积越大,最终进入广口瓶的水不会越多,错误;
D、 将发热剂均匀涂抹在广口瓶内壁上而非堆在广口瓶底部,增大发热剂与空气的接触面积,是为了加快铁的锈蚀,正确。
故选D。
8.A
【详解】A、硫酸亚铁只与铝反应,和锡不反应,能证明,符合题意;
B、两种金属都能置换出硫酸铜中的铜,不能证明,不符合题意;
C、铝和锡都能和稀盐酸反应,不能证明,不符合题意;
D、铝和锡都能和稀硫酸反应,不能证明,不符合题意。
故选A。
9.B
【分析】当锌和硝酸银反应,由于进入溶液的锌的质量小于析出银的质量,所以溶液质量是减小的,即ab段。当锌和硝酸铜反应时,由于进入溶液锌的质量大于析出铜的质量,所以溶液质量是增大的,即bc段。当硝酸铜完全反应后,锌不再参加反应,因此溶液的质量保持不变,即cd段。
【详解】A.a点时,锌正在和硝酸银反应,而硝酸铜还为开始反应,则此时溶液中的阳离子为Zn2+,Cu2+和没有反应完的Ag+,故A错误;
B.c点时,硝酸银和硝酸铜恰好完全反应,此时的溶质只有反应产物硝酸锌,故B正确;
C.b~c段,锌再和硝酸铜反应,此时溶质为硝酸锌和硝酸铜,如果滴加稀盐酸,那么不会产生沉淀,故C错误;
D.d点时,加入的锌过量,此时固体为锌、铜和银,加入稀盐酸后,锌会和稀盐酸反应生成氢气,故D错误。
故选B。
10.C
【分析】首先,ab段,铁粉与硝酸铜发生置换反应,M1点时,硝酸铜被完全消耗,之后bc段铁粉与硝酸银发生置换反应,直到M2点时铁粉消耗完毕,然后cd段之前生成的铜与硝酸银发生置换反应,直至M3点时,铜被完全消耗;
【详解】A、设有质量为x的铁粉与硝酸铜反应,并生成质量为y的铜,
解方程组得y=8(m1-5.6)g,不符合题意。
B、bc段是铁粉与硝酸银发生置换反应,不符合题意。
C、M3点时铁粉被完全消耗,沉淀完全是Ag,整体反应过程相当于铁粉与硝酸银发生置换反应,设生成Ag的质量为x,则有:
解得x=21.6g,符合题意。
D、cd段之前生成的铜与硝酸银发生置换反应生成了银单质和硝酸铜溶液,后面在滴加硝酸银也不会与硝酸铜反应,因此e点含有硝酸铜存在,不符合题意。
故选C。
【点睛】bc的斜率大于cd的斜率,而相对原子质量是Ag>Cu>Fe,在结合题干和所学知识,可以得出b点的转折是因为硝酸铜被完全消耗,而不是铁粉被完全消耗。
11.B
【详解】A、塑料属于三大高分子合成材料之一,故选项说法正确;
B、钛合金含有多种物质,属于混合物,故选项说法错误;
C、在强光照射下,溴化银分解成单质溴和银,银元素的化合价由+1价变为0价,化合价降低,故选项说法正确;
D、溴和银在氧化铜催化作用下,又立即化合成溴化银,氧化铜作催化剂,反应前后氧化铜化学性质不变,故选项说法正确。
故选B。
12. d 76% 缺少尾气处理装置
【详解】(1)草酸晶体(H2C2O4 3H2O)在浓硫酸作用下受热分解,该反应的反应物状态是固体和液体,反应条件是加热,因此选用d装置;
(2)铁的氧化物与一氧化碳在高温条件反应生成铁和二氧化碳,碱石灰能吸收二氧化碳,B装置增重6.6g,那么反应生成的二氧化碳是6.6g,氧元素的质量=,因为4.8g氧元素的质量一半来自于一氧化碳,一半来自于铁的氧化物,那么铁红中氧元素的质量是4.8g÷2=2.4g,则铁红中铁的质量分数=;
(3)实验装置的一个明显缺陷是没有处理一氧化碳,一氧化碳进入空气中会污染环境。
13. 检验装置D中是否生成CO2(或“检验混合气体中是否存在“CO”也可) 赞成,装置E可以根据白色硫酸铜粉末是否变蓝检验水蒸气的存在,但该水蒸气可能是氢气与氧化铜反应产生,也可能是从装置C中带入的 氯化钡
【详解】(1)根据可用澄清石灰水检验二氧化碳气体知,装置A是为了检验混合气体中是否有二氧化碳;装置C在实验中的作用是检验二氧化碳气体是否除尽;装置F在实验中的作用是检验是否有二氧化碳生成。
(2)赞成小港的想法,因为装置E可以根据白色硫酸铜粉末是否变蓝检验水蒸气的存在,但该水蒸气可能是氢气与氧化铜反应产生,也可能是从装置C中带入的。
(3)二氧化碳与氯化钡不发生反应,当二氧化碳通入BaCl2和NaOH的混合溶液,二氧化碳与氢氧化钠先反应生成碳酸钠和水,碳酸钠与氯化钡反应生成碳酸钡沉淀,即可证明。
14. B 收集一氧化碳 80%
【详解】(1)一氧化碳是可燃性气体,与氧气或空气混合达到一定程度时遇明火会发生爆炸,为防止发生爆炸,实验开始时应先通一氧化碳,排尽空气,再加热。
故选B;
(2)一氧化碳密度小于氢氧化钠溶液的密度,装置B的作用除吸收外,还起到的作用是收集一氧化碳;
(3)根据化学方程式可知,后装置A处大玻璃管的质量减少了4.8g为氧化铁中氧元素的质量,则氧化铁的质量为
则该氧化铁样品中氧化铁的质量分数。
答:该氧化铁样品中氧化铁的质量分数80%。
15. 铁与氧气和水接触 5.6
【详解】(1)铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。铁制品生锈的条件是:铁与氧气和水接触;
(2)设:可得到铁的质量是x。
x=5.6g
答:可得到铁的质量是5.6g。
16. 机械 电磁感应 选择透过性 使用石灰乳,可以使镁离子充分反应,澄清石灰水中的氢氧化钙含量少,不能全部反应 减少镁的损失
【详解】(1)[1]潮汐发电是运用海水的运动带动水轮机转动来发电,所以是将海水的机械能转化为电能。
[2]水轮发电机中的线圈切割磁感线,产生感应电流,所以是运用电磁感应原理制成的。
(2)[3]由于细胞具有选择透过性,对细胞有用的物质可以进入,对细胞有害的物质不能进入,所以“人工膜”也是有选择的使有益的物质通过,模拟了细胞膜的选择透过性。
(3)[4]由于海水中有大量的镁离子,氢氧化钙微溶于水,所以澄清石灰水不能使海水中的镁离子全部发生反应,故使用石灰乳而不使用澄清石灰水。
[5]经过步骤①和②两步反应后,海水中的镁离子基本反应完成,能有效的减少镁的流失。
17. Zn2+ 硝酸银/ AgNO3
【详解】(1)在金属活动顺序中,锌排在氢之前,能与稀盐酸反应生成氯化锌和氢气,铜排在氢之后,不能与稀盐酸反应,稀盐酸和黄铜粉末反应前后,烧杯中溶液里的离子种类如图所示,“” 表示的离子是氯离子,“” 表示的离子是氢离子,“”表示的离子是锌离子,其离子符号为:Zn2+;
(2)若要检验滤渣是否洗涤干净,只要检验最后一次洗涤液中是否存在氯离子,氯离子能与硝酸银中银离子结合生成不溶于稀硝酸的氯化银白色沉淀,可向最后一次洗涤液中滴入适量硝酸银(AgNO3)溶液和足量稀硝酸,观察是否有沉淀生成。
18. Fe+CuCl2═FeCl2+Cu, 减少
【详解】由图中信息可知,反应前是氯化铜,反应后是氯化亚铁,说明铁和氯化铜反应生成了氯化亚铁和铜,反应的化学方程式是Fe+CuCl2═FeCl2+Cu,根据化学方程式可知,56份质量的铁反应生成64份质量的铜,反应后溶液质量减小。
试卷第1页,共3页
试卷第1页,共3页
