专题7初识酸、碱和盐检测题(含答案)--2022-2023学年九年级化学仁爱版下册
文档属性
| 名称 | 专题7初识酸、碱和盐检测题(含答案)--2022-2023学年九年级化学仁爱版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 169.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-16 00:00:00 | ||
图片预览

文档简介
专题7《初识酸、碱和盐》检测题
一、单选题
1.化学概念在逻辑上存在交叉、包含、并列等关系,以下概念符合如图所示关系的是( )
选项 X Y Z
A 化合反应 氧化反应 化学反应
B 有机物 化合物 纯净物
C 酸 碱 化合物
D 钠盐 碳酸盐 盐
A.A B.B C.C D.D
2.山区农业是保障山区人民正常生活的重要部分,山区的春秋两季风势较强,为增强农作物抗倒伏能力,建议施用的化肥是( )
A.KCl B.CO(NH2)2 C.Ca(H2PO4)2 D.KOH
3.下列水果中酸性最强的是
A.菠萝pH=4.1 B.柠檬pH=2.3
C.草莓pH=3.2 D.木瓜pH=5.0
4.一种含氯消毒剂的制备反应为:2NaOH+Cl2=NaCl+NaClO+H2O。下列说法正确的是
A.NaOH属于盐 B.Cl2是单质 C.NaCl是消毒剂 D.NaClO是氧化物
5.下列有关实验现象的描述正确的是
A.木炭在氧气中剧烈燃烧,生成二氧化碳气体
B.将铜片放入装有稀硫酸的试管中,有气泡产生
C.研磨氢氧化钙和氯化铵的混合物,有刺激性气味产生
D.打开浓盐酸瓶塞,瓶口有白烟冒出,一段时间后,溶液质量增大
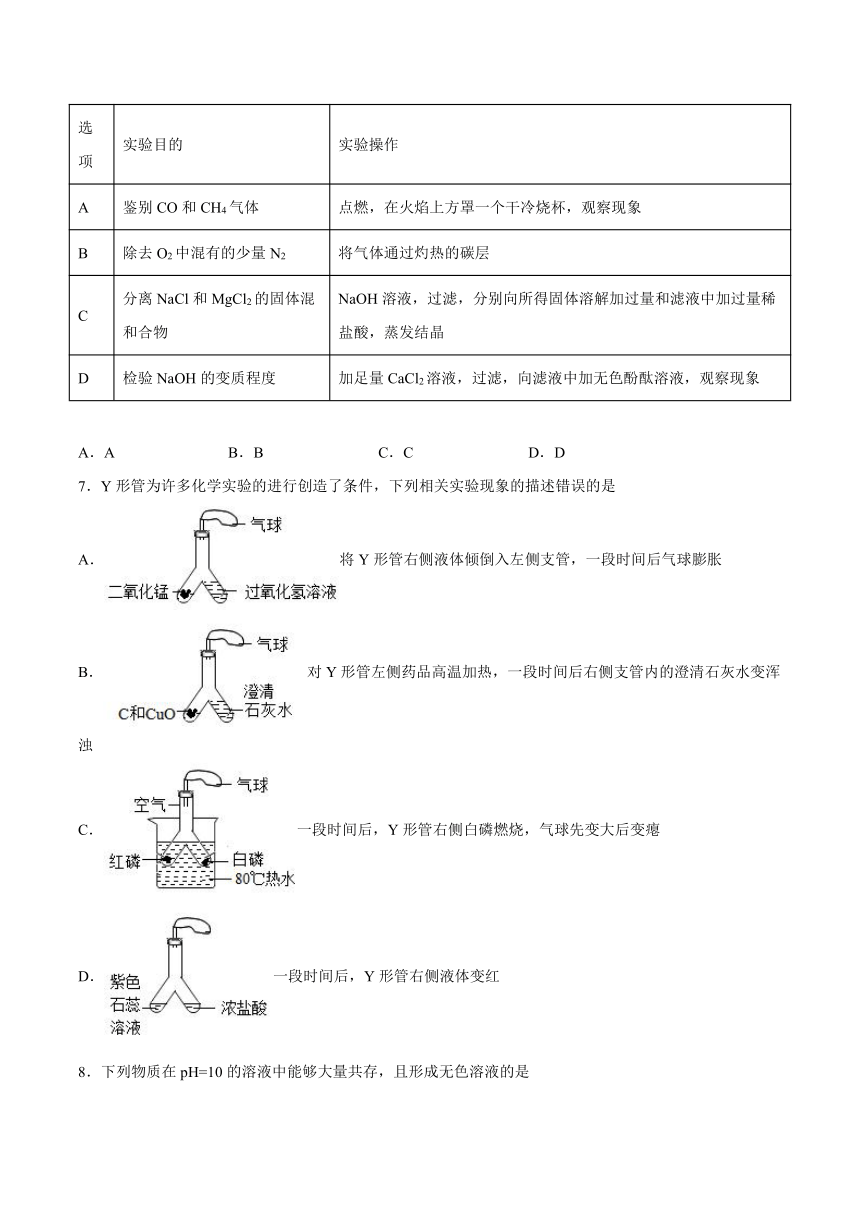
6.下列实验操作不能达到相应实验目的的是选项 实验目的 实验操作
选项 实验目的 实验操作
A 鉴别CO和CH4气体 点燃,在火焰上方罩一个干冷烧杯,观察现象
B 除去O2中混有的少量N2 将气体通过灼热的碳层
C 分离NaCl和MgCl2的固体混和合物 NaOH溶液,过滤,分别向所得固体溶解加过量和滤液中加过量稀盐酸,蒸发结晶
D 检验NaOH的变质程度 加足量CaCl2溶液,过滤,向滤液中加无色酚酞溶液,观察现象
A.A B.B C.C D.D
7.Y形管为许多化学实验的进行创造了条件,下列相关实验现象的描述错误的是
A.将Y形管右侧液体倾倒入左侧支管,一段时间后气球膨胀
B.对Y形管左侧药品高温加热,一段时间后右侧支管内的澄清石灰水变浑浊
C.一段时间后,Y形管右侧白磷燃烧,气球先变大后变瘪
D.一段时间后,Y形管右侧液体变红
8.下列物质在pH=10的溶液中能够大量共存,且形成无色溶液的是
A.FeCl3, KCl, NH4 NO3, Na2 SO4 B.NaHCO3, H2SO4, KCl, NaNO3
C.CaCl2, NaOH,KNO3, BaCl2 D.CaCl2, Na2SO4, NH4Cl, KNO3
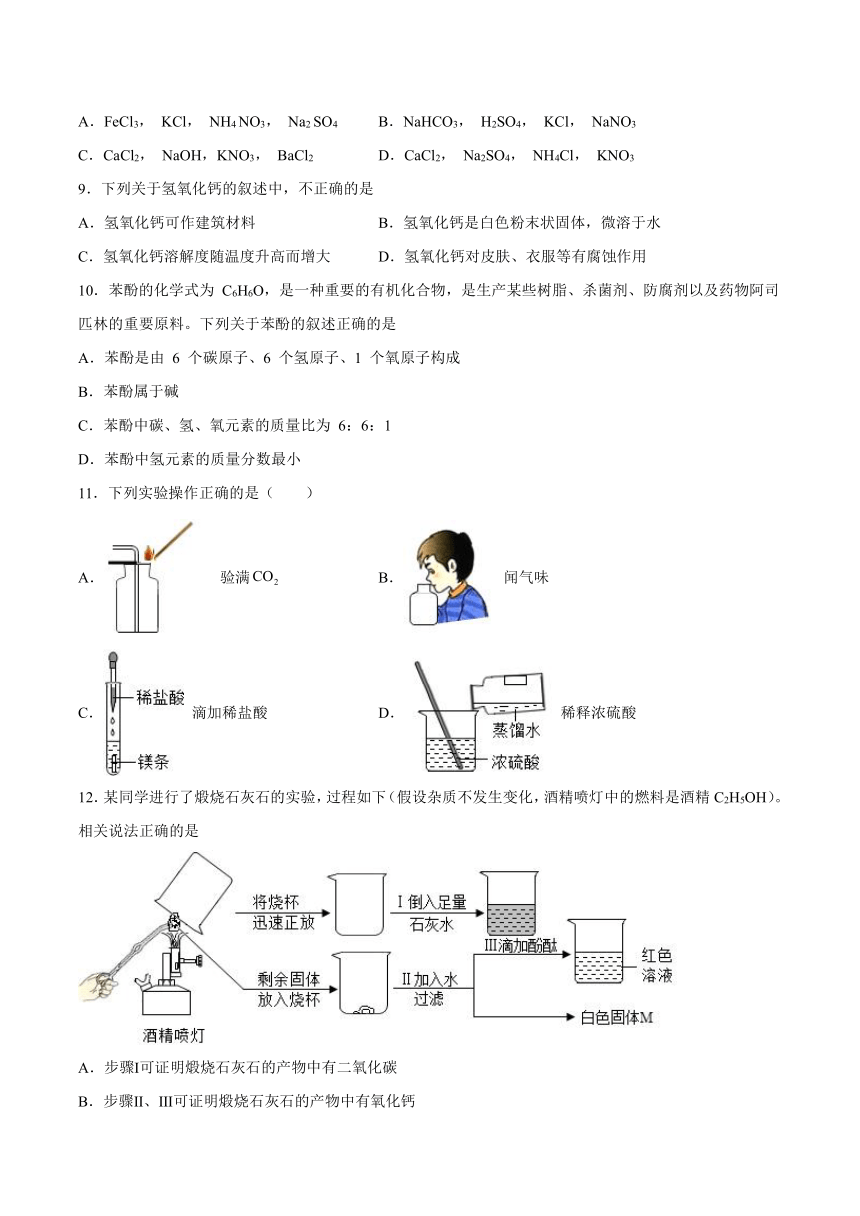
9.下列关于氢氧化钙的叙述中,不正确的是
A.氢氧化钙可作建筑材料 B.氢氧化钙是白色粉末状固体,微溶于水
C.氢氧化钙溶解度随温度升高而增大 D.氢氧化钙对皮肤、衣服等有腐蚀作用
10.苯酚的化学式为 C6H6O,是一种重要的有机化合物,是生产某些树脂、杀菌剂、防腐剂以及药物阿司匹林的重要原料。下列关于苯酚的叙述正确的是
A.苯酚是由 6 个碳原子、6 个氢原子、1 个氧原子构成
B.苯酚属于碱
C.苯酚中碳、氢、氧元素的质量比为 6:6:1
D.苯酚中氢元素的质量分数最小
11.下列实验操作正确的是( )
A. 验满 B. 闻气味
C. 滴加稀盐酸 D. 稀释浓硫酸
12.某同学进行了煅烧石灰石的实验,过程如下(假设杂质不发生变化,酒精喷灯中的燃料是酒精C2H5OH)。相关说法正确的是
A.步骤Ⅰ可证明煅烧石灰石的产物中有二氧化碳
B.步骤Ⅱ、Ⅲ可证明煅烧石灰石的产物中有氧化钙
C.白色固体M是氢氧化钙和碳酸钙的混合物
D.白色固体M中钙元素的质量等于煅烧前石灰石中钙元素的质量
二、填空题
13.生活中处处有化学。
(1)体温计中的液体金属化学式为___________。
(2)玻璃的主要成分是SiO2,SiO2读作___________。
(3)生石灰常用作食品干燥剂,其干燥原理是___________(用化学方程式表示)。
(4)医用消毒酒精中酒精的化学式为C2H5OH,碳、氢元素原子个数比为___________。0.1mol酒精的质量为___________g ,含有___________个氢原子。
14.某无色混合气体中可能含有H2、CO、CO2、HCl、NH3及水蒸气中的两种或多种,当混合气体依次通过下列物质中:
(1)澄清石灰水(无浑浊现象);(2)氢氧化钡溶液(有浑浊现象);(3)浓硫酸;(4)灼热氧化铜(变红色);(5)无水硫酸铜(变蓝色)。
试分析该混合气体中肯定含有_____________;肯定不含有_____________;可能含有______________。
15.在学习了常见的酸和碱后,某化学兴趣小组的同学围绕“酸碱中和反应”,在老师引导下开展实验探究活动,请你参与下列活动。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将_______(填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中 b.稀硫酸滴入氢氧化钾溶液中
三、实验题
16.补全实验报告。
实验方法 1.二氧化碳的性质两支试管中分别加少量水,然后各滴入紫色石蕊溶液,向其中一支通入二氧化碳。 2.燃烧的条件从乒乓球和滤纸上各剪下一小片分开放在薄铜片两侧,加热铜片中部
现象分析 通入二氧化碳试管中的紫色石蕊溶液变成_________色 乒乓球片先燃烧,滤纸片后燃烧。说明燃烧条件之一是___________
四、推断题
17.A、B、C、E均含有组成化合物种类最多的元素,其中A是单质;D、E均含有人体中含量最高的金属元素,其中E中该元素的质量分数为40%.它们之间的转化关系如图所示(“-”表示相连的物质能发生反应“→”表示一种物质能生成另一种物质,部分物质和反应条件已略去)。E的化学式为______;由C转化为B的反应条件是______,由D转化为E的化学方程式为______。
18.A、B、C、D是初中化学常见的物质,且由H、C、O、S、Cl、Na、Ca等7种元素中的一种或几种组成,它们之间的关系如下图所示。(图中“—”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件均已略去)。
(1)若A~D均含一种相同元素,且A、B、D均为氧化物, C是空气中的主要成分之一,B的化学式为 ____________ , A与C反应的化学方程式为 __________________________ 。
(2)若A~D均为化合物,且D、B、A、C相对分子质量依次增大,B和D在生活中常用于灭火,B的化学式为 ______ ,A与C反应的化学方程式为 __________________________ 。
(3)若A~D均由三种元素组成,且有如右图所示的实验,C、D含有相同的金属元素。若关闭K2打开K1,将D中溶液滴入A中,可观察到产生大量气泡, B中溶液变浑浊;此时关闭K1、打开K2,可观察到广口瓶中液体进入C中,发生反应但无明显现象。则D为 _________ ,B→C的化学方程式为 ______________________________ 。
五、计算题
19.在实验室中,小明发现了一瓶氢氧化钙粉末试剂瓶盖有破损,取部分粉末作为样品对其变质情况进行分析,实验室温度20℃查阅氢氧化钙的溶解度并进行如下实验。
氢氧化钙溶解度表
温度℃ 0 10 20 30 40 50 60 70
溶解度g 0.185 0.176 0.165 0.153 0.141 0.138 0.116 0.106
(1)取1g样品溶于100g水中,出现浑浊现象。小明认为该固体已经变质。你觉得这种说法是否正确?______(填“正确”或“不正确”)。理由是:______。
(2)小明另取2g样品于大烧杯中,加足量水充分溶解配制成1850g溶液,并通入CO2.溶液的质量与反应的CO2质量关系如图所示。请计算:该样品中氢氧化钙的质量分数。
(3)配制的氢氧化钙溶液浓度为______。
参考答案:
1.C 2.A 3.B 4.B 5.C 6.B 7.D 8.C 9.C 10.D 11.A 12.B
13. Hg 二氧化硅 CaO+H2O=Ca(OH)2 2:6或1:3 4.6 3.612×1023
14. H2、CO2、HCl NH3 CO、水蒸气
15.a
16. 红 温度达到可燃物的着火点
17. CaCO3 高温 CO2+Ca(OH)2=CaCO3↓+H2O
18. )H2O或H2O2 CO2 Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑ Na2CO3 Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH
19.(1)不正确;因为氢氧化钙的溶解度很小,导致不能完全溶液而浑浊;(2)92.5%;(3)0.1%
一、单选题
1.化学概念在逻辑上存在交叉、包含、并列等关系,以下概念符合如图所示关系的是( )
选项 X Y Z
A 化合反应 氧化反应 化学反应
B 有机物 化合物 纯净物
C 酸 碱 化合物
D 钠盐 碳酸盐 盐
A.A B.B C.C D.D
2.山区农业是保障山区人民正常生活的重要部分,山区的春秋两季风势较强,为增强农作物抗倒伏能力,建议施用的化肥是( )
A.KCl B.CO(NH2)2 C.Ca(H2PO4)2 D.KOH
3.下列水果中酸性最强的是
A.菠萝pH=4.1 B.柠檬pH=2.3
C.草莓pH=3.2 D.木瓜pH=5.0
4.一种含氯消毒剂的制备反应为:2NaOH+Cl2=NaCl+NaClO+H2O。下列说法正确的是
A.NaOH属于盐 B.Cl2是单质 C.NaCl是消毒剂 D.NaClO是氧化物
5.下列有关实验现象的描述正确的是
A.木炭在氧气中剧烈燃烧,生成二氧化碳气体
B.将铜片放入装有稀硫酸的试管中,有气泡产生
C.研磨氢氧化钙和氯化铵的混合物,有刺激性气味产生
D.打开浓盐酸瓶塞,瓶口有白烟冒出,一段时间后,溶液质量增大
6.下列实验操作不能达到相应实验目的的是选项 实验目的 实验操作
选项 实验目的 实验操作
A 鉴别CO和CH4气体 点燃,在火焰上方罩一个干冷烧杯,观察现象
B 除去O2中混有的少量N2 将气体通过灼热的碳层
C 分离NaCl和MgCl2的固体混和合物 NaOH溶液,过滤,分别向所得固体溶解加过量和滤液中加过量稀盐酸,蒸发结晶
D 检验NaOH的变质程度 加足量CaCl2溶液,过滤,向滤液中加无色酚酞溶液,观察现象
A.A B.B C.C D.D
7.Y形管为许多化学实验的进行创造了条件,下列相关实验现象的描述错误的是
A.将Y形管右侧液体倾倒入左侧支管,一段时间后气球膨胀
B.对Y形管左侧药品高温加热,一段时间后右侧支管内的澄清石灰水变浑浊
C.一段时间后,Y形管右侧白磷燃烧,气球先变大后变瘪
D.一段时间后,Y形管右侧液体变红
8.下列物质在pH=10的溶液中能够大量共存,且形成无色溶液的是
A.FeCl3, KCl, NH4 NO3, Na2 SO4 B.NaHCO3, H2SO4, KCl, NaNO3
C.CaCl2, NaOH,KNO3, BaCl2 D.CaCl2, Na2SO4, NH4Cl, KNO3
9.下列关于氢氧化钙的叙述中,不正确的是
A.氢氧化钙可作建筑材料 B.氢氧化钙是白色粉末状固体,微溶于水
C.氢氧化钙溶解度随温度升高而增大 D.氢氧化钙对皮肤、衣服等有腐蚀作用
10.苯酚的化学式为 C6H6O,是一种重要的有机化合物,是生产某些树脂、杀菌剂、防腐剂以及药物阿司匹林的重要原料。下列关于苯酚的叙述正确的是
A.苯酚是由 6 个碳原子、6 个氢原子、1 个氧原子构成
B.苯酚属于碱
C.苯酚中碳、氢、氧元素的质量比为 6:6:1
D.苯酚中氢元素的质量分数最小
11.下列实验操作正确的是( )
A. 验满 B. 闻气味
C. 滴加稀盐酸 D. 稀释浓硫酸
12.某同学进行了煅烧石灰石的实验,过程如下(假设杂质不发生变化,酒精喷灯中的燃料是酒精C2H5OH)。相关说法正确的是
A.步骤Ⅰ可证明煅烧石灰石的产物中有二氧化碳
B.步骤Ⅱ、Ⅲ可证明煅烧石灰石的产物中有氧化钙
C.白色固体M是氢氧化钙和碳酸钙的混合物
D.白色固体M中钙元素的质量等于煅烧前石灰石中钙元素的质量
二、填空题
13.生活中处处有化学。
(1)体温计中的液体金属化学式为___________。
(2)玻璃的主要成分是SiO2,SiO2读作___________。
(3)生石灰常用作食品干燥剂,其干燥原理是___________(用化学方程式表示)。
(4)医用消毒酒精中酒精的化学式为C2H5OH,碳、氢元素原子个数比为___________。0.1mol酒精的质量为___________g ,含有___________个氢原子。
14.某无色混合气体中可能含有H2、CO、CO2、HCl、NH3及水蒸气中的两种或多种,当混合气体依次通过下列物质中:
(1)澄清石灰水(无浑浊现象);(2)氢氧化钡溶液(有浑浊现象);(3)浓硫酸;(4)灼热氧化铜(变红色);(5)无水硫酸铜(变蓝色)。
试分析该混合气体中肯定含有_____________;肯定不含有_____________;可能含有______________。
15.在学习了常见的酸和碱后,某化学兴趣小组的同学围绕“酸碱中和反应”,在老师引导下开展实验探究活动,请你参与下列活动。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将_______(填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中 b.稀硫酸滴入氢氧化钾溶液中
三、实验题
16.补全实验报告。
实验方法 1.二氧化碳的性质两支试管中分别加少量水,然后各滴入紫色石蕊溶液,向其中一支通入二氧化碳。 2.燃烧的条件从乒乓球和滤纸上各剪下一小片分开放在薄铜片两侧,加热铜片中部
现象分析 通入二氧化碳试管中的紫色石蕊溶液变成_________色 乒乓球片先燃烧,滤纸片后燃烧。说明燃烧条件之一是___________
四、推断题
17.A、B、C、E均含有组成化合物种类最多的元素,其中A是单质;D、E均含有人体中含量最高的金属元素,其中E中该元素的质量分数为40%.它们之间的转化关系如图所示(“-”表示相连的物质能发生反应“→”表示一种物质能生成另一种物质,部分物质和反应条件已略去)。E的化学式为______;由C转化为B的反应条件是______,由D转化为E的化学方程式为______。
18.A、B、C、D是初中化学常见的物质,且由H、C、O、S、Cl、Na、Ca等7种元素中的一种或几种组成,它们之间的关系如下图所示。(图中“—”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件均已略去)。
(1)若A~D均含一种相同元素,且A、B、D均为氧化物, C是空气中的主要成分之一,B的化学式为 ____________ , A与C反应的化学方程式为 __________________________ 。
(2)若A~D均为化合物,且D、B、A、C相对分子质量依次增大,B和D在生活中常用于灭火,B的化学式为 ______ ,A与C反应的化学方程式为 __________________________ 。
(3)若A~D均由三种元素组成,且有如右图所示的实验,C、D含有相同的金属元素。若关闭K2打开K1,将D中溶液滴入A中,可观察到产生大量气泡, B中溶液变浑浊;此时关闭K1、打开K2,可观察到广口瓶中液体进入C中,发生反应但无明显现象。则D为 _________ ,B→C的化学方程式为 ______________________________ 。
五、计算题
19.在实验室中,小明发现了一瓶氢氧化钙粉末试剂瓶盖有破损,取部分粉末作为样品对其变质情况进行分析,实验室温度20℃查阅氢氧化钙的溶解度并进行如下实验。
氢氧化钙溶解度表
温度℃ 0 10 20 30 40 50 60 70
溶解度g 0.185 0.176 0.165 0.153 0.141 0.138 0.116 0.106
(1)取1g样品溶于100g水中,出现浑浊现象。小明认为该固体已经变质。你觉得这种说法是否正确?______(填“正确”或“不正确”)。理由是:______。
(2)小明另取2g样品于大烧杯中,加足量水充分溶解配制成1850g溶液,并通入CO2.溶液的质量与反应的CO2质量关系如图所示。请计算:该样品中氢氧化钙的质量分数。
(3)配制的氢氧化钙溶液浓度为______。
参考答案:
1.C 2.A 3.B 4.B 5.C 6.B 7.D 8.C 9.C 10.D 11.A 12.B
13. Hg 二氧化硅 CaO+H2O=Ca(OH)2 2:6或1:3 4.6 3.612×1023
14. H2、CO2、HCl NH3 CO、水蒸气
15.a
16. 红 温度达到可燃物的着火点
17. CaCO3 高温 CO2+Ca(OH)2=CaCO3↓+H2O
18. )H2O或H2O2 CO2 Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑ Na2CO3 Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH
19.(1)不正确;因为氢氧化钙的溶解度很小,导致不能完全溶液而浑浊;(2)92.5%;(3)0.1%
