第12章盐检测题(含答案)--2022-2023学年九年级化学京改版(2013)下册
文档属性
| 名称 | 第12章盐检测题(含答案)--2022-2023学年九年级化学京改版(2013)下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 96.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-16 00:00:00 | ||
图片预览



文档简介
第12章《盐》检测题
一、单选题
1.碳酸氢钠受热易分解2NaHCO3═Na2CO3+CO2↑+H2O现将12克碳酸钠和碳酸氢钠的混合物完全加热后,剩余固体8.9克,则原混合物中碳酸氢钠的质量为
A.7g B.8.4g C.11.8 g D.10.9g
2.下列化学反应中,属于复分解反应的是
A.Fe + 2HCl=FeCl2 + H2↑ B.2H2+O22H2O
C.HCl+ NaOH=NaCl+H2O D.2H2O2H2↑+ O2↑
3.西彭一农技站货架上待售的化肥有、、,其中缺少的肥料品种是
A.氨肥 B.钾肥 C.磷肥 D.复合肥料
4.物质的性质在很大程度上决定了物质的用途,物质的用途体现了物质的性质,下列物质的用途体现了物质的化学性质的是( )
A.干冰用于人工降雨 B.修车师傅用汽油除去油污
C.生石灰用作食品干燥剂 D.下雪后用氯化钠融雪
5.化学实验室通常将药品分类存放,现存放的部分药品如下:
药品柜 甲 乙 丙 丁
药品 硫酸硝酸 食盐氯化钡 氢氧化钠氢氧化镁 汽油酒精
实验室新购进的浓盐酸应放入的药品柜编号是
A.甲 B.乙 C.丙 D.丁
6.除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是
选项 物质(括号内为杂质) 选用试剂 操作方法
A CO2(CO) 适量O2 点燃
B NaCl溶液(Na2CO3) 过量CaCl2溶液 过滤
C KNO3溶液(K2SO4溶液) 适量Ba(NO3)2溶液 过滤
D KC1溶液(CuCl2溶液) 足量NaOH溶液 过滤
A.A B.B C.C D.D
7.化学肥料对农业的高产丰收具有重要作用,下列关于农作物和化肥的说法正确的是
A.为保证农作物高产,应大量施用化肥
B.农作物所必需的营养元素只有氮、磷和钾三种
C.磷肥能使作物根系发达,耐寒耐旱
D.铵态氮肥与熟石灰混合施用可以明显提高肥效
8.推理是一种重要的思维方法,下列推理合理的是
A.纯碱溶液的PH>7,说明纯碱溶液显碱性,纯碱属于碱
B.化合物含有不同种元素,所以含有不同种元素的物质都是化合物
C.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D.化学反应伴随能量变化,所以铁生锈过程中一定伴随能量变化
9.下列物质的名称、俗名对应正确的是
A.乙醇——白酒 B.硫酸铜晶体——胆矾 C.碳酸氢钠——苏打 D.氧化钙——熟石灰
10.下列说法合理的有( )
①随着铁制品的不断锈蚀,自然界中铁元素的含量会减少
②某固体可能由硫酸钠、氯化钡、氯化镁、硫酸钾中的一种或几种组成。取少量该固体,加入足量的稀氢氧化钠溶液,产生白色沉淀,过滤,向沉淀中加入足量稀硝酸,沉淀全部溶解。则该固体的组成有4种情况
③炼铁高炉中的主要原料为铁矿石、焦炭和石灰石,石灰石的主要作用是吸收二氧化碳
④将一定量的镁粉和铝粉加入含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生,则滤液的组成有3种情况
⑤除去锌粉中混有的少量铁粉,可加入足量氯化锌溶液充分反应后过滤
A.1个 B.2个 C.3个 D.4个
11.下列各组离子在指定的溶液中,能大量共存的一组是
A.无色溶液中:K+、Na+、、Cu2+
B.pH=11的溶液中:、Ba2+、、Cl-
C.酸性溶液中:Mg2+、Na+、、Cl-
D.含有大量Ba2+的溶液中:K+、Al3+、、
12.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
物质 所含杂质 除去杂质的方法
A CO2 CO 通入氧气,点燃
B NH3 H2O 通过浓硫酸洗气
C NaOH Na2CO3 加入过量的氢氧化钙溶液,过滤
D NaCl 泥沙 溶解、过滤、蒸发结晶
A.A B.B C.C D.D
二、填空题
13.从铁、二氧化碳、高锰酸钾、氯化铁溶液、水、氢氧化钠溶液、稀盐酸中选出适当物质,分别写出符合下列要求的化学反应方程式,每种物质只能用一次。
(1)化合反应_____________________________;
(2)分解反应_____________________________ ;
(3)置换反应_____________________________;
(4)复分解反应_____________________________。
14.化学与我们的生活有着密切的联系。现有氧气、一氧化碳、食盐、二氧化碳、氦气、二氧化硫,请用化学式按下列要求填空:
(1)可充填灯泡的保护气是______;
(2)与人体血红蛋白结合的有毒气体是_______;
(3)引起温室效应的气体是_______;
(4)造成酸雨的气体是______;
(5)潜水员需要携带的气体是______;
(6)厨房中作调味品的是______;
三、实验题
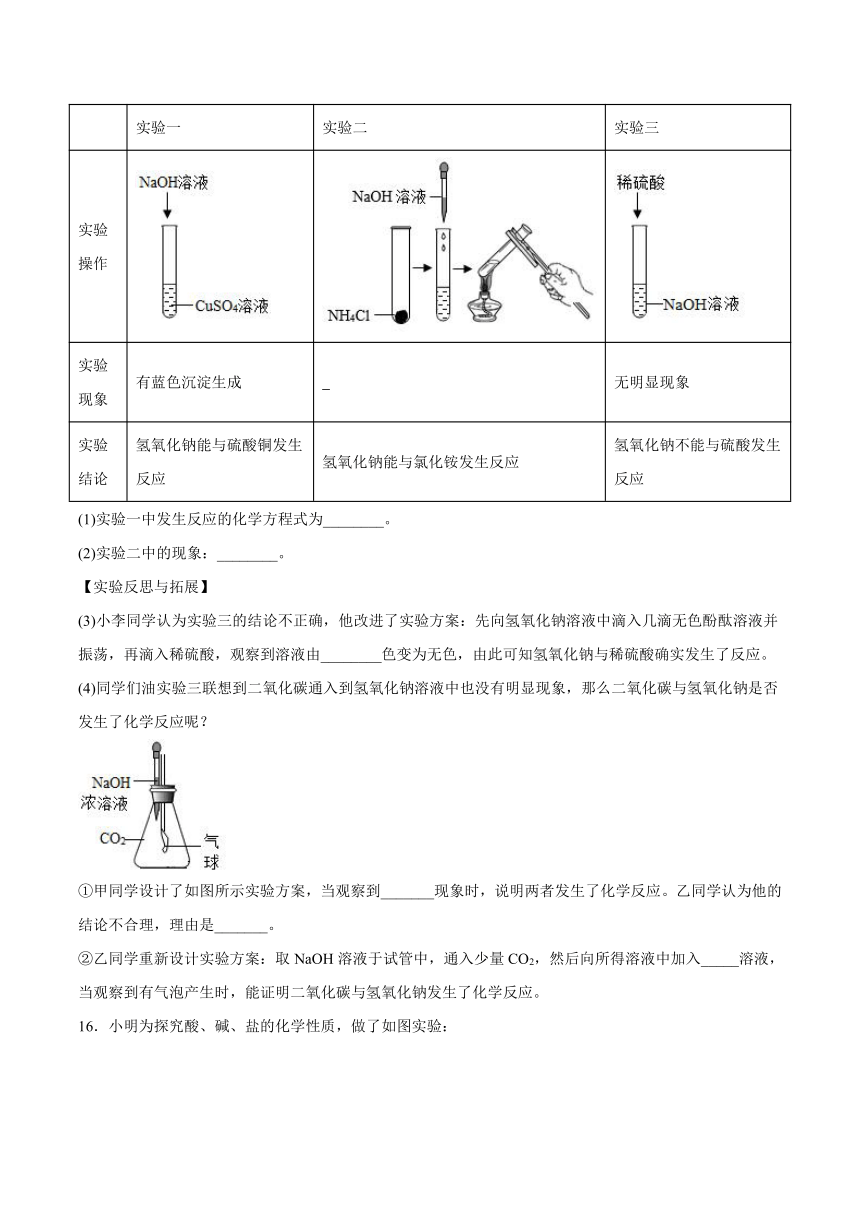
15.化学兴趣小组同学通过实验来探究氢氧化钠的性质,设计过程如下,请你和他们一起完成。
【实验过程与分析】
实验一 实验二 实验三
实验操作
实验现象 有蓝色沉淀生成 无明显现象
实验结论 氢氧化钠能与硫酸铜发生反应 氢氧化钠能与氯化铵发生反应 氢氧化钠不能与硫酸发生反应
(1)实验一中发生反应的化学方程式为________。
(2)实验二中的现象:________。
【实验反思与拓展】
(3)小李同学认为实验三的结论不正确,他改进了实验方案:先向氢氧化钠溶液中滴入几滴无色酚酞溶液并振荡,再滴入稀硫酸,观察到溶液由________色变为无色,由此可知氢氧化钠与稀硫酸确实发生了反应。
(4)同学们油实验三联想到二氧化碳通入到氢氧化钠溶液中也没有明显现象,那么二氧化碳与氢氧化钠是否发生了化学反应呢?
①甲同学设计了如图所示实验方案,当观察到_______现象时,说明两者发生了化学反应。乙同学认为他的结论不合理,理由是_______。
②乙同学重新设计实验方案:取NaOH溶液于试管中,通入少量CO2,然后向所得溶液中加入_____溶液,当观察到有气泡产生时,能证明二氧化碳与氢氧化钠发生了化学反应。
16.小明为探究酸、碱、盐的化学性质,做了如图实验:
(1)实验后液体颜色变红的试管是_______;
(2)反应后试管C的溶液中一定有的阳离子是_______;
(3)小明把D、E反应后的液体倒入一个洁净的烧杯中,观察到只有白色沉淀生成,过滤后得到白色沉淀和无色滤液,小明分别对试管D、E反应时的反应物用量有如下描述,正确的是_______。
A 试管D:氢氧化钙溶液一定过量
B 试管D:稀盐酸可能不足
C 试管E:碳酸钠一定过量
D 试管E:稀盐酸一定过量
四、推断题
17.A、B、C、D是初中化学常见的物质,物质之间的转化关系如图所示。
(1)若A、C是氧化物,D是相对分子量为100的一种白色固体,其中金属元素所占质量分数为40%,则反应的化学方程式为______。
(2)若A、C属于碱,D是白色沉淀,则反应的化学方程式为______。
(3)若A、C是元素组成相同的气态化合物,则A、C化学性质不同的原因是______。
18.下图表示的是物质A—F相互间的关系(“→”表示物质间的转化关系,“—”表示两端的物质能发生化学反应)。A—E属于不同种类(单质、氧化物、酸、碱、盐)的物质,气体C常用于灭火,F是一种蓝色溶液,E与F用于配制农药波尔多液。请你回答:
(1)C的化学式__________;
(2)反应①的属于基本反应类型_________反应;
(3)反应③的化学方程式为________;
(4)D物质属于_______(选填“单质”、“氧化物”、“酸”、“碱”、“盐”)。
五、计算题
19.维C泡腾片是一种常见的补充维生素C的保健品。某品牌维C泡腾片的主要成分如图1所示。
(1)将本品一片投入蒸馏水中,有气泡产生,反应原理为:H3C6H5O2+3NaHCO3=Na3C6H5O2+3CO2↑+3______(填化学式)。
(2)维C泡腾片中碳酸氢钠质量分数的测定:称量相关实验用品质量,将本品一片投入蒸馏水中,待不再产生气体后,称量锥形瓶及瓶内所有物质的总质量。装置如图2所示。相关数据如表:
物品 反应前 反应后
锥形瓶 蒸馏水 维C泡腾片 锥形瓶及瓶内所有物质
质量/g 71.75 50.00 4.00 125.53
①生成二氧化碳质量为________克。
②根据以上数据计算本品中碳酸氢钠的质量分数_____(写出计算过程,结果精确到0.1%)。
参考答案:
1.B 2.C 3.D 4.C 5.A 6.C 7.C 8.D 9.B 10.A 11.C 12.D
13.(1)
(2)
(3)
(4)
14.(1)He
(2)CO
(3)CO2
(4)SO2
(5)O2
(6)NaCl
15.(1)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
(2)有刺激性气味气体产生
(3)红
(4) 气球膨胀 二氧化碳能和水反应,且能溶于水 稀盐酸(合理即可)
16. A Fe3+ BC
17.(1)CO2+Ca(OH)2=CaCO3↓+H2O
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(或Ba(OH)2+Na2SO4=BaSO4↓+2NaOH)
(3)分子构成不同
18. CO2 置换反应 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 盐
19.(1)H2O
(2) 0.22 设样品中碳酸氢钠的质量为x,则
解得x=0.42g
则本品中碳酸氢钠的质量分数为
答:本品中碳酸氢钠的质量分数为10.58%
一、单选题
1.碳酸氢钠受热易分解2NaHCO3═Na2CO3+CO2↑+H2O现将12克碳酸钠和碳酸氢钠的混合物完全加热后,剩余固体8.9克,则原混合物中碳酸氢钠的质量为
A.7g B.8.4g C.11.8 g D.10.9g
2.下列化学反应中,属于复分解反应的是
A.Fe + 2HCl=FeCl2 + H2↑ B.2H2+O22H2O
C.HCl+ NaOH=NaCl+H2O D.2H2O2H2↑+ O2↑
3.西彭一农技站货架上待售的化肥有、、,其中缺少的肥料品种是
A.氨肥 B.钾肥 C.磷肥 D.复合肥料
4.物质的性质在很大程度上决定了物质的用途,物质的用途体现了物质的性质,下列物质的用途体现了物质的化学性质的是( )
A.干冰用于人工降雨 B.修车师傅用汽油除去油污
C.生石灰用作食品干燥剂 D.下雪后用氯化钠融雪
5.化学实验室通常将药品分类存放,现存放的部分药品如下:
药品柜 甲 乙 丙 丁
药品 硫酸硝酸 食盐氯化钡 氢氧化钠氢氧化镁 汽油酒精
实验室新购进的浓盐酸应放入的药品柜编号是
A.甲 B.乙 C.丙 D.丁
6.除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是
选项 物质(括号内为杂质) 选用试剂 操作方法
A CO2(CO) 适量O2 点燃
B NaCl溶液(Na2CO3) 过量CaCl2溶液 过滤
C KNO3溶液(K2SO4溶液) 适量Ba(NO3)2溶液 过滤
D KC1溶液(CuCl2溶液) 足量NaOH溶液 过滤
A.A B.B C.C D.D
7.化学肥料对农业的高产丰收具有重要作用,下列关于农作物和化肥的说法正确的是
A.为保证农作物高产,应大量施用化肥
B.农作物所必需的营养元素只有氮、磷和钾三种
C.磷肥能使作物根系发达,耐寒耐旱
D.铵态氮肥与熟石灰混合施用可以明显提高肥效
8.推理是一种重要的思维方法,下列推理合理的是
A.纯碱溶液的PH>7,说明纯碱溶液显碱性,纯碱属于碱
B.化合物含有不同种元素,所以含有不同种元素的物质都是化合物
C.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D.化学反应伴随能量变化,所以铁生锈过程中一定伴随能量变化
9.下列物质的名称、俗名对应正确的是
A.乙醇——白酒 B.硫酸铜晶体——胆矾 C.碳酸氢钠——苏打 D.氧化钙——熟石灰
10.下列说法合理的有( )
①随着铁制品的不断锈蚀,自然界中铁元素的含量会减少
②某固体可能由硫酸钠、氯化钡、氯化镁、硫酸钾中的一种或几种组成。取少量该固体,加入足量的稀氢氧化钠溶液,产生白色沉淀,过滤,向沉淀中加入足量稀硝酸,沉淀全部溶解。则该固体的组成有4种情况
③炼铁高炉中的主要原料为铁矿石、焦炭和石灰石,石灰石的主要作用是吸收二氧化碳
④将一定量的镁粉和铝粉加入含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生,则滤液的组成有3种情况
⑤除去锌粉中混有的少量铁粉,可加入足量氯化锌溶液充分反应后过滤
A.1个 B.2个 C.3个 D.4个
11.下列各组离子在指定的溶液中,能大量共存的一组是
A.无色溶液中:K+、Na+、、Cu2+
B.pH=11的溶液中:、Ba2+、、Cl-
C.酸性溶液中:Mg2+、Na+、、Cl-
D.含有大量Ba2+的溶液中:K+、Al3+、、
12.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
物质 所含杂质 除去杂质的方法
A CO2 CO 通入氧气,点燃
B NH3 H2O 通过浓硫酸洗气
C NaOH Na2CO3 加入过量的氢氧化钙溶液,过滤
D NaCl 泥沙 溶解、过滤、蒸发结晶
A.A B.B C.C D.D
二、填空题
13.从铁、二氧化碳、高锰酸钾、氯化铁溶液、水、氢氧化钠溶液、稀盐酸中选出适当物质,分别写出符合下列要求的化学反应方程式,每种物质只能用一次。
(1)化合反应_____________________________;
(2)分解反应_____________________________ ;
(3)置换反应_____________________________;
(4)复分解反应_____________________________。
14.化学与我们的生活有着密切的联系。现有氧气、一氧化碳、食盐、二氧化碳、氦气、二氧化硫,请用化学式按下列要求填空:
(1)可充填灯泡的保护气是______;
(2)与人体血红蛋白结合的有毒气体是_______;
(3)引起温室效应的气体是_______;
(4)造成酸雨的气体是______;
(5)潜水员需要携带的气体是______;
(6)厨房中作调味品的是______;
三、实验题
15.化学兴趣小组同学通过实验来探究氢氧化钠的性质,设计过程如下,请你和他们一起完成。
【实验过程与分析】
实验一 实验二 实验三
实验操作
实验现象 有蓝色沉淀生成 无明显现象
实验结论 氢氧化钠能与硫酸铜发生反应 氢氧化钠能与氯化铵发生反应 氢氧化钠不能与硫酸发生反应
(1)实验一中发生反应的化学方程式为________。
(2)实验二中的现象:________。
【实验反思与拓展】
(3)小李同学认为实验三的结论不正确,他改进了实验方案:先向氢氧化钠溶液中滴入几滴无色酚酞溶液并振荡,再滴入稀硫酸,观察到溶液由________色变为无色,由此可知氢氧化钠与稀硫酸确实发生了反应。
(4)同学们油实验三联想到二氧化碳通入到氢氧化钠溶液中也没有明显现象,那么二氧化碳与氢氧化钠是否发生了化学反应呢?
①甲同学设计了如图所示实验方案,当观察到_______现象时,说明两者发生了化学反应。乙同学认为他的结论不合理,理由是_______。
②乙同学重新设计实验方案:取NaOH溶液于试管中,通入少量CO2,然后向所得溶液中加入_____溶液,当观察到有气泡产生时,能证明二氧化碳与氢氧化钠发生了化学反应。
16.小明为探究酸、碱、盐的化学性质,做了如图实验:
(1)实验后液体颜色变红的试管是_______;
(2)反应后试管C的溶液中一定有的阳离子是_______;
(3)小明把D、E反应后的液体倒入一个洁净的烧杯中,观察到只有白色沉淀生成,过滤后得到白色沉淀和无色滤液,小明分别对试管D、E反应时的反应物用量有如下描述,正确的是_______。
A 试管D:氢氧化钙溶液一定过量
B 试管D:稀盐酸可能不足
C 试管E:碳酸钠一定过量
D 试管E:稀盐酸一定过量
四、推断题
17.A、B、C、D是初中化学常见的物质,物质之间的转化关系如图所示。
(1)若A、C是氧化物,D是相对分子量为100的一种白色固体,其中金属元素所占质量分数为40%,则反应的化学方程式为______。
(2)若A、C属于碱,D是白色沉淀,则反应的化学方程式为______。
(3)若A、C是元素组成相同的气态化合物,则A、C化学性质不同的原因是______。
18.下图表示的是物质A—F相互间的关系(“→”表示物质间的转化关系,“—”表示两端的物质能发生化学反应)。A—E属于不同种类(单质、氧化物、酸、碱、盐)的物质,气体C常用于灭火,F是一种蓝色溶液,E与F用于配制农药波尔多液。请你回答:
(1)C的化学式__________;
(2)反应①的属于基本反应类型_________反应;
(3)反应③的化学方程式为________;
(4)D物质属于_______(选填“单质”、“氧化物”、“酸”、“碱”、“盐”)。
五、计算题
19.维C泡腾片是一种常见的补充维生素C的保健品。某品牌维C泡腾片的主要成分如图1所示。
(1)将本品一片投入蒸馏水中,有气泡产生,反应原理为:H3C6H5O2+3NaHCO3=Na3C6H5O2+3CO2↑+3______(填化学式)。
(2)维C泡腾片中碳酸氢钠质量分数的测定:称量相关实验用品质量,将本品一片投入蒸馏水中,待不再产生气体后,称量锥形瓶及瓶内所有物质的总质量。装置如图2所示。相关数据如表:
物品 反应前 反应后
锥形瓶 蒸馏水 维C泡腾片 锥形瓶及瓶内所有物质
质量/g 71.75 50.00 4.00 125.53
①生成二氧化碳质量为________克。
②根据以上数据计算本品中碳酸氢钠的质量分数_____(写出计算过程,结果精确到0.1%)。
参考答案:
1.B 2.C 3.D 4.C 5.A 6.C 7.C 8.D 9.B 10.A 11.C 12.D
13.(1)
(2)
(3)
(4)
14.(1)He
(2)CO
(3)CO2
(4)SO2
(5)O2
(6)NaCl
15.(1)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
(2)有刺激性气味气体产生
(3)红
(4) 气球膨胀 二氧化碳能和水反应,且能溶于水 稀盐酸(合理即可)
16. A Fe3+ BC
17.(1)CO2+Ca(OH)2=CaCO3↓+H2O
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(或Ba(OH)2+Na2SO4=BaSO4↓+2NaOH)
(3)分子构成不同
18. CO2 置换反应 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 盐
19.(1)H2O
(2) 0.22 设样品中碳酸氢钠的质量为x,则
解得x=0.42g
则本品中碳酸氢钠的质量分数为
答:本品中碳酸氢钠的质量分数为10.58%
