安徽省亳州市二完中2022-2023学年高二下学期期中考试化学试题(含解析)
文档属性
| 名称 | 安徽省亳州市二完中2022-2023学年高二下学期期中考试化学试题(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 651.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-17 00:00:00 | ||
图片预览




文档简介
亳州市二完中2022-2023学年高二下学期期中考试
化 学 试 题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100,时间75分钟,请在答题卷上作答。
第Ⅰ卷 选择题
一、选择题(本题共10题,每题3分,共30分。在每小题给出的四个选项中,只有一项是最符合题意要求的。)
1.下列说法正确的是( )
A.甲苯、乙醇都是烃的衍生物
B.有机化合物都是从动物体内提取出来的
C.组成差一个或若干个的有机化合物互称同系物
D.化学家维勒首次在实验室用无机物合成有机物尿素,打破了无机物与有机物的界限
2.由CH3CH3→CH3CH2Cl→CH2 = CH2→CH3CH2OH的转化过程中,经过的反应是( )
A.取代→加成→氧化 B.裂解→取代→消去
C.取代→消去→加成 D.取代→消去→水解
3.有关化学用语正确的是( )
A.乙烯的实验式:C2H4 B.乙醇的分子式:CH3CH2OH
C.四氯化碳的电子式: D.间羟基苯甲酸的结构简式:
4.异丙苯一种无色有特殊芳香气味的液体,主要用于生产苯酚和丙酮。已知异丙苯的结构简式如下图,下列说法错误的是( )
A.异丙苯中碳原子可能都处于同一平面 B.异丙苯的沸点比苯的高
C.异丙苯属于芳香烃 D.异丙苯可发生加成反应
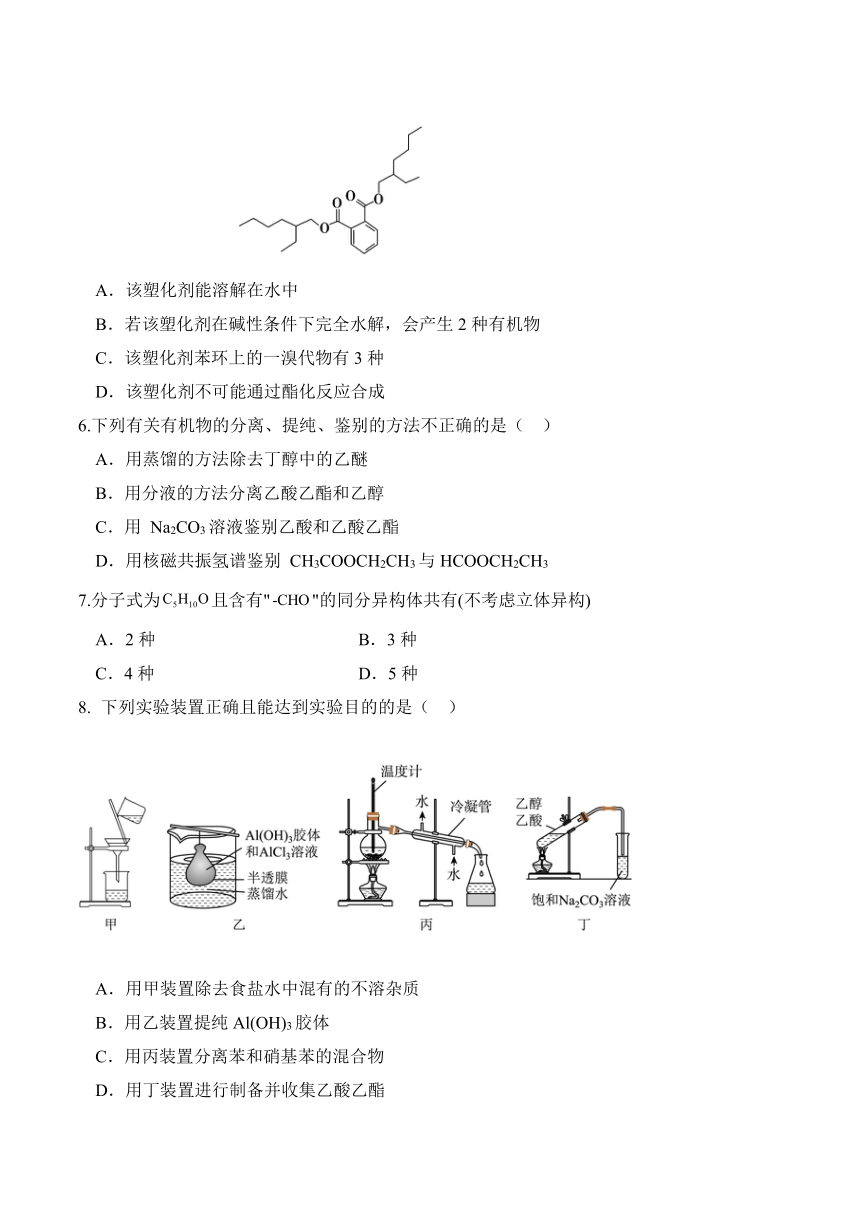
5.塑化剂的种类很多,其中一种塑化剂的结构简式如右图所示。
下列有关说法正确的是( )
A.该塑化剂能溶解在水中
B.若该塑化剂在碱性条件下完全水解,会产生2种有机物
C.该塑化剂苯环上的一溴代物有3种
D.该塑化剂不可能通过酯化反应合成
6.下列有关有机物的分离、提纯、鉴别的方法不正确的是( )
A.用蒸馏的方法除去丁醇中的乙醚
B.用分液的方法分离乙酸乙酯和乙醇
C.用 Na2CO3溶液鉴别乙酸和乙酸乙酯
D.用核磁共振氢谱鉴别 CH3COOCH2CH3与HCOOCH2CH3
7.分子式为且含有""的同分异构体共有(不考虑立体异构)
A.2种 B.3种
C.4种 D.5种
下列实验装置正确且能达到实验目的的是( )
A.用甲装置除去食盐水中混有的不溶杂质
B.用乙装置提纯Al(OH)3胶体
C.用丙装置分离苯和硝基苯的混合物
D.用丁装置进行制备并收集乙酸乙酯
烯烃被氧化的部位 CH2= RCH=
对应的氧化产物 CO2 RCOOH
9.烯烃或炔烃在酸性高锰酸钾溶液作用下,分子中的不饱和键完全断裂,此法可用于减短碳链。已知:
现有某烯烃与酸性溶液作用后得到的氧化产物有、乙二酸()和丙酮( ),则该烯烃的结构简式可能是( )
A. B.
C.CH2=CH-CH=CHCH2CH3 D.
10.2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质, 5-羧基荧光素与5-羧基二乙酸荧光素在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等。
下列说法不正确的是 ( )
A.5-FAM转变为5-CFDA属于取代反应
B.5-FAM的分子式为C21H12O7
C.5-FAM和5-CFDA 各1mol分别与足量NaOH溶液反应,5-CFDA消耗NaOH 的量多
D.实验室鉴别5-FAM与5-CFDA可用NaHCO3 溶液
二、选择题(本题共5题,每题3分,共15分。在每小题给出的四个选项中,有一到两个选项项符合题意要求的,全对得3分,选对但不全的得1.5分,有错的得0分。)
11.在卤代烃R—CH2—CH2—X 中化学键如图所示:(①为 C—X ,②③为C—H,④为C—R) 则下列说法正确的是 ( )
A.发生水解反应时,被破坏的键是①
B.发生水解反应时,被破坏的键是①和②
C.发生消去反应时,被破坏的键是①和③
D.发生消去反应时,被破坏的键是①和④
12.2020年以来,新型冠状病毒肺炎席卷全世界,中国传统中药“莲花清瘟胶囊”助力世界抗疫。莲花清瘟胶囊配方中含传统中药金银花,绿原酸是金银花主要抗菌、抗病毒有效药理成分之一,结构简式如下图所示,关于绿原酸的下列推测不合理的是( )
A.1mol绿原酸最多可和1mol碳酸钠反应
B.可溶于水也可溶于乙醇
C.分子中有4个手性碳原子
D.结构中含有3种含氧官能团
13..下列反应方程式书写错误的是( )
A.2CH3CH2OH+O2 2CH3CHO+2H2O
B.+NaHCO3 +CO2↑+H2O
C.HCHO+2Cu(OH)2+NaOHHCOONa+Cu2O↓+3H2O
D.+Cl2+HCl
14.下列说法不正确的是( )
A.乙烯基乙炔(CH2=CHC≡CH)分子中所有原子位于同一平面
B.苯酚久置于空气中或遇到FeCl3溶液,都会变为紫色
C.从有机物的红外光谱图可以获得分子中含有何种化学键或官能团的信息
D.如图分别是实验室制取乙炔和乙酸乙酯的装置图,X、Y都是饱和食盐水
15.药物Z可用于治疗哮喘、系统性红斑狼疮等,可由X(咖啡酸)和Y(1,4-环己二酮单乙二醇缩酮)为原料合成(如图)。下列说法中正确的是的( )
A.可用FeCl3溶液检验此反应中是否有Z生成
B.X和Y生成Z的反应属于加成反应
C.1molZ与NaOH溶液反应,最多消耗3molNaOH
D.X中最多有9个碳原子共面
第Ⅱ卷 非选择题
非选择题(4题,共55分)
书写方程式(12分)
苯的硝化反应:___________________
用甲苯制取烈性炸药TNT:___________________
2﹣氯丙烷()的消去反应:___________________
向苯酚钠溶液里通入足量的CO2:___________________
苯酚与溴水的反应:__________________
乙醛与银氨溶液的反应:__________________
(14分)烃A(结构简式:)是有机化学工业的基本原料,可从石油中获得。烃A可发生如下图所示的一系列化学反应。
请回答下列问题:
(1)B的分子式为_______,③的反应类型是_______。
(2)E的名称是_______,可鉴别A、E两种物质的试剂是_______(填一种)。
(3)C是A通过加聚反应制得的有机高分子材料,其结构简式为_______。
(4)G的官能团是_______(填名称),F的结构简式是_______。
18.(16分))下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯。
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,该反应的化学方程式为______________________________________。
[装置设计]甲、乙、丙三位同学分别设计了如下图所示三套实验装置:
若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是________(填“甲”或“乙”)。乙中导管a的作用为________________________。丙同学将甲装置中的玻璃管改成了球形的干燥管,除了起上述作用外,另一重要作用是_______________。
[实验步骤]A.按所选择的装置组装仪器,在试管①中先加入3mL体积分数为95%的乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸。
B.将试管固定在铁架台上。
C.在试管②中加入5mL饱和Na2CO3溶液。
D.用酒精灯对试管①加热。
E.当观察到试管②中有明显现象时停止实验。
[问题讨论]
(1)步骤A组装好实验装置,加入样品前还应检查__________________________。
(2)试管②中观察到的现象是_____________________________。
(3)试管②中饱和Na2CO3溶液的作用是________________________,饱和Na2CO3溶液________(填“能”或“不能”)用NaOH溶液代替,其原因是_________________。
19.(13分)实验室用溴和乙醇制备1,2-二溴乙烷的装置如图所示,反应原理如下:
CH3CH2OH CH2=CH2 +H2O
CH2=CH2 +Br2 BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140°C脱水生成乙醚。
有关数据列表如下:
乙醇 1,2-二溴乙烷 乙醚
状态 无色液体 无色液体 无色液体
密度/ g·cm-3 0.79 2.2 0.71
沸点/°C 78.5 132 34.6
熔点/°C -130 9 -116
回答下列问题:
(1)在此制备实验中,要迅速地把反应温度提高到170°C左右,其最主要目的是___________。
(2)在装置C中应加入___________,其目的是吸收反应中可能生成的酸性气体。
A.水 B.浓硫酸
C.氢氧化钠溶液 D.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是___________。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中,加水并充分振荡,静置后液体分层,产物应在___________层(填“上”、“下”)。(1分)
(5)若产物中有少量未反应的Br2,最好用___________洗涤除去。
A.水 B.Na2SO3溶液
C.碘化钠溶液 D.乙醇
(6)若产物中有少量副产物乙醚可用___________的方法除去,反应过程中应用冷水冷却装置D,其主要目的是___________ 。
参考答案:
D
2. C
3. D
【详解】A.乙烯的实验式(最简式)为CH2,
B.乙醇的结构简式为C2H5OH或CH3CH2OH,
C.四氯化碳的电子式为,
4. A
5. B
6. B
【详解】A.丁醇、乙醚互溶,但沸点不同,则蒸馏可分离,
B.乙酸乙酯和乙醇互溶,不能分液分离,应选蒸馏法,
C.乙酸与碳酸钠反应生成气体,乙酸乙酯与碳酸钠溶液分层,现象不同可鉴别,
D.CH3COOCH2CH3与HCOOCH2CH3中均含3种H,但二者的核磁共振氢谱中峰的面积比不相同,可以用核磁共振氢谱来鉴别。
7. C
8. B
【详解】A.过滤时应该遵循一贴二低三靠,图中漏斗下端未紧靠烧杯内壁,不能悬空放置,
B.胶体粒子不能透过半透膜,分子、离子可以透过半透膜,图中渗析法可提纯胶体
C.蒸馏时温度计测定馏分的温度,应该放置蒸馏烧瓶支管口附近,
D.酯化反应需要浓硫酸作催化剂、吸水剂,图中未加浓硫酸,也未加碎瓷片以防止暴沸现象的发生,液体体积超过试管容积的
9. A
10. D
【详解】A. 5-FAM转变为5-CFDA,羟基上的H被乙酰基取代,属于取代反应,
B. 5-FAM的分子式为C21H12O7,
C. 5-FAM和5-CFDA 各1mol分别与足量NaOH溶液反应,消耗的NaOH 物质的量分别为4mol和6mol,5-CFDA消耗的NaOH 物质的量多,
D. 5-FAM与5-CFDA分子中都有羧基,都可与NaHCO3 溶液反应生成二氧化碳,所以不能用NaHCO3溶液鉴别它们。
11. AC
12. A
【详解】A.酚羟基、羧基都可以和Na2CO3反应,所以1mol绿原酸最多消耗3mol Na2CO3
B.该分子含有多个羟基,可和水分子、乙醇分子形成分子间氢键,可溶与水也可溶于乙醇
C.连接四个不同原子或原子团的碳原子为手性碳,该物质含有如图所示4个手性碳原子
D.结构中含氧官能团有羟基、酯基、羧基,
13. BC
14. BD
【详解】A. 乙烯是平面型分子、乙炔是直线型分子,双键碳和与之直接相连的6个原子共平面、叁键碳及与之直接相连的原子共线,故乙烯基乙炔(CH2=CHC≡CH)分子中所有原子位于同一平面
苯酚久置于空气中变粉红色,遇到FeCl3溶液,会变为紫色,
C.通过分析有机物的红外光谱图,可以知道分子中含有何种化学键或官能团,
D. 电石中加饱和食盐水可用于实验室制取乙炔,制取乙酸乙酯时试管Y中是饱和碳酸钠,
15. CD
【详解】A.X、Z分子中均含酚羟基,不能用FeCl3溶液检验此反应中是否有Z生成
B.1个加成反应的原子利用率为100%,该反应中O原子利用率小于100%,故该反应不是加成反应
Z分子中含一个酯基,2个酚羟基,因此1molZ与NaOH溶液反应,最多消耗3molNaOH
D苯环、乙烯是平面型分子,如图,图中两个方框内的C原子分别共面,两个平面共用两个点(C),因此这个两个平面可能共面,则X中最多有9个C原子共面。
16.书写方程式(12分,每空2分)
苯的硝化反应:,+HNO3(浓) +H2O;
烈性炸药TNT的制取:+3HNO3 + 3H2O
2﹣氯丙烷消去反应:+NaOHCH3CH=CH2↑+H2O+NaCl
向苯酚钠溶液里通入足量的CO2:+CO2+H2O→+NaHCO3
(5)苯酚与溴水的反应: +3Br2→ ↓+3HBr
(6)乙醛与银氨溶液的反应: CH3CHO+2Ag(NH3)2OH2Ag↓+CH3COONH4+3NH3+H2O
17.(14分,每空2分)
(1) C3H6Br2 加成反应
(2) 丙烷 溴水或溴的CCl4溶液或酸性高锰酸钾溶液
(3)
(4) 碳碳双键、酯基 CH2=CH2COOH
【分析】CH2=CHCH3经过反应①与溴发生加成反应,生成B(1,2-二溴丙烷),经过反应②发生加聚反应,生成C(聚丙烯),经过反应③与水发生加成反应,生成D(1-丙醇),经过反应④与氢气加成,生成E(丙烷),D和F发生酯化反应生成丙烯酸丙酯,可知F为丙烯酸。
(2)E是CH2=CHCH3经过反应④与氢气发生加成反应生成的丙烷,要鉴别丙烯和丙烷可以用溴水(或溴的CCl4溶液或酸性高锰酸钾溶液)。
(3)CH2=CHCH3经过反应②发生加聚反应,生成聚丙烯,其结构简式为
(4)从G结构简式中可以推知其中含有的官能团为:碳碳双键、酯基;D与F即1-丙醇与丙烯酸发生酯化反应生成丙烯酸丙酯,
(16分,除备注处1分其余每空2分)
CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O 乙(1分) 冷凝 防止倒吸
(1)装置气密性 (2) 液体分为两层且能闻到香味 (3)溶解乙醇、反应乙酸、降低乙酸乙酯的溶解度 不能(1分) NaOH和乙酸乙酯反应,促进乙酸乙酯的水解
【分析】实验室制取乙酸乙酯,利用乙酸、乙醇、浓硫酸共热发生酯化反应,生成乙酸乙酯和水;收集乙酸乙酯时用饱和碳酸钠溶液,可以起到溶解乙醇,中和乙酸,降低乙酸乙酯的溶解度的作用;长导管不能深入液面以下,防止倒吸,也可以使用干燥管,由此分析。
【详解】[实验原理]乙醇、乙酸与浓硫酸发生酯化反应,酸失去羟基醇失去羟基上的氢原子,生成乙酸乙酯和水,化学方程式为:CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O;
[装置设计]若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是乙,甲装置会引起倒吸,收集不到乙酸乙酯,乙中导管a的作用为冷凝;
丙同学将甲装置中的玻璃管改成了球形的干燥管,球形干燥管可以增大气体与液体的接触面积,可以防止倒吸;
[问题讨论](1)步骤A组装好实验装置,加入样品前还应检查装置的气密性,否则将导致实验失败;
(2)乙酸乙酯是有香味的密度比水小的油状液体,故试管②中观察到的现象是液体分为两层且能闻到香味;
(3)乙醇、乙酸与浓硫酸发生酯化反应,酸失去羟基醇失去羟基上的氢原子,生成乙酸乙酯和水,试管②中饱和Na2CO3溶液的作用是溶解乙醇、中和乙酸、降低乙酸乙酯的溶解度,饱和Na2CO3溶液不能用NaOH溶液代替,其原因是NaOH和乙酸乙酯反应,促进乙酸乙酯的水解,降低乙酸乙酯的产率。
【点睛】乙醇和乙酸制取乙酸乙酯的实验中,反应原理是酸失去羟基,醇失去羟基上的氢原子,属于酯化反应,也属于取代反应,酯在氢氧化钠存在条件下要发生水解,为易错点,饱和碳酸钠溶液的作用是难点。
(13分,除备注处1分其余每空2分)
(1)减少副产物乙醚生成
(2)C
(3)观察D中颜色是否完全褪去
(4)下(1分)
(5)B
(6) 蒸馏 避免溴大量挥发
【分析】实验室制备1,2-二溴乙烷:三颈烧瓶A中发生反应是乙醇在浓硫酸的作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应方程式为:CH3CH2OHCH2=CH2↑+H2O,如果D中导气管发生堵塞事故,A中产生的乙烯气体会导致装置B中压强增大,长导管液面会上升,所以装置B中长玻璃管可判断装置是否堵塞,装置B起缓冲作用,浓硫酸具有脱水性、吸水性和强氧化性,能氧化乙醇,CH3CH2OH+4H2SO4(浓)4SO2↑+CO2↑+7H2O+C,可能生成的酸性气体为二氧化硫、二氧化碳,装置C中放氢氧化钠溶液,发生反应SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH═Na2CO3+H2O,除去杂质气体,乙烯含有不饱和键C=C双键,能卤素单质发生加成反应,D中乙烯和溴加成生成1,2-二溴乙烷,反应为:CH2=CH2+Br-Br→CH2Br-CH2Br,制得1,2-二溴乙烷,据此分析解题。
(1)由题干信息可知,乙醇在140℃时发生取代反应生成乙醚,导致生成乙烯的量减少,
(2)由分析可知,浓硫酸具有脱水性、吸水性和强氧化性,能氧化乙醇,CH3CH2OH+4H2SO4(浓)4SO2↑+CO2↑+7H2O+C,可能生成的酸性气体为二氧化硫、二氧化碳,装置C中放氢氧化钠溶液,发生反应SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH═Na2CO3+H2O,除去杂质气体,故答案为:C;
(3)乙烯和溴发生加成反应而使溴水褪色,如果观察到D中颜色完全褪去就说明该制备反应已经结束,故答案为:观察D中颜色是否完全褪去;
(4)由题干信息可知,1,2-二溴乙烷的密度比水的要大,故将1,2-二溴乙烷粗产品置于分液漏斗中,加水并充分振荡,静置后液体分层,产物应在下层,故答案为:下;
(5)溴在水中的溶解度较小,但易溶于1,2-二溴乙烷,用水无法除溴;溴具有强氧化性,能氧化还原性物质,亚硫酸钠能被溴氧化转化为可溶性硫酸钠,可以除去溴;NaI也能被溴氧化但生成新的杂质I2,碘易溶于有机物,不能除去溴;酒精与1,2-二溴乙烷互溶,不能除去溴,故答案为:B;
(6)由题干信息可知,乙醚和1,2-二溴乙烷的沸点相差很大,故若产物中有少量副产物乙醚,可用蒸馏的方法除去,溴有毒且易挥发,所以反应过程中应用冷水冷却装置D,产品1,2一二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管。
化 学 试 题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100,时间75分钟,请在答题卷上作答。
第Ⅰ卷 选择题
一、选择题(本题共10题,每题3分,共30分。在每小题给出的四个选项中,只有一项是最符合题意要求的。)
1.下列说法正确的是( )
A.甲苯、乙醇都是烃的衍生物
B.有机化合物都是从动物体内提取出来的
C.组成差一个或若干个的有机化合物互称同系物
D.化学家维勒首次在实验室用无机物合成有机物尿素,打破了无机物与有机物的界限
2.由CH3CH3→CH3CH2Cl→CH2 = CH2→CH3CH2OH的转化过程中,经过的反应是( )
A.取代→加成→氧化 B.裂解→取代→消去
C.取代→消去→加成 D.取代→消去→水解
3.有关化学用语正确的是( )
A.乙烯的实验式:C2H4 B.乙醇的分子式:CH3CH2OH
C.四氯化碳的电子式: D.间羟基苯甲酸的结构简式:
4.异丙苯一种无色有特殊芳香气味的液体,主要用于生产苯酚和丙酮。已知异丙苯的结构简式如下图,下列说法错误的是( )
A.异丙苯中碳原子可能都处于同一平面 B.异丙苯的沸点比苯的高
C.异丙苯属于芳香烃 D.异丙苯可发生加成反应
5.塑化剂的种类很多,其中一种塑化剂的结构简式如右图所示。
下列有关说法正确的是( )
A.该塑化剂能溶解在水中
B.若该塑化剂在碱性条件下完全水解,会产生2种有机物
C.该塑化剂苯环上的一溴代物有3种
D.该塑化剂不可能通过酯化反应合成
6.下列有关有机物的分离、提纯、鉴别的方法不正确的是( )
A.用蒸馏的方法除去丁醇中的乙醚
B.用分液的方法分离乙酸乙酯和乙醇
C.用 Na2CO3溶液鉴别乙酸和乙酸乙酯
D.用核磁共振氢谱鉴别 CH3COOCH2CH3与HCOOCH2CH3
7.分子式为且含有""的同分异构体共有(不考虑立体异构)
A.2种 B.3种
C.4种 D.5种
下列实验装置正确且能达到实验目的的是( )
A.用甲装置除去食盐水中混有的不溶杂质
B.用乙装置提纯Al(OH)3胶体
C.用丙装置分离苯和硝基苯的混合物
D.用丁装置进行制备并收集乙酸乙酯
烯烃被氧化的部位 CH2= RCH=
对应的氧化产物 CO2 RCOOH
9.烯烃或炔烃在酸性高锰酸钾溶液作用下,分子中的不饱和键完全断裂,此法可用于减短碳链。已知:
现有某烯烃与酸性溶液作用后得到的氧化产物有、乙二酸()和丙酮( ),则该烯烃的结构简式可能是( )
A. B.
C.CH2=CH-CH=CHCH2CH3 D.
10.2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质, 5-羧基荧光素与5-羧基二乙酸荧光素在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等。
下列说法不正确的是 ( )
A.5-FAM转变为5-CFDA属于取代反应
B.5-FAM的分子式为C21H12O7
C.5-FAM和5-CFDA 各1mol分别与足量NaOH溶液反应,5-CFDA消耗NaOH 的量多
D.实验室鉴别5-FAM与5-CFDA可用NaHCO3 溶液
二、选择题(本题共5题,每题3分,共15分。在每小题给出的四个选项中,有一到两个选项项符合题意要求的,全对得3分,选对但不全的得1.5分,有错的得0分。)
11.在卤代烃R—CH2—CH2—X 中化学键如图所示:(①为 C—X ,②③为C—H,④为C—R) 则下列说法正确的是 ( )
A.发生水解反应时,被破坏的键是①
B.发生水解反应时,被破坏的键是①和②
C.发生消去反应时,被破坏的键是①和③
D.发生消去反应时,被破坏的键是①和④
12.2020年以来,新型冠状病毒肺炎席卷全世界,中国传统中药“莲花清瘟胶囊”助力世界抗疫。莲花清瘟胶囊配方中含传统中药金银花,绿原酸是金银花主要抗菌、抗病毒有效药理成分之一,结构简式如下图所示,关于绿原酸的下列推测不合理的是( )
A.1mol绿原酸最多可和1mol碳酸钠反应
B.可溶于水也可溶于乙醇
C.分子中有4个手性碳原子
D.结构中含有3种含氧官能团
13..下列反应方程式书写错误的是( )
A.2CH3CH2OH+O2 2CH3CHO+2H2O
B.+NaHCO3 +CO2↑+H2O
C.HCHO+2Cu(OH)2+NaOHHCOONa+Cu2O↓+3H2O
D.+Cl2+HCl
14.下列说法不正确的是( )
A.乙烯基乙炔(CH2=CHC≡CH)分子中所有原子位于同一平面
B.苯酚久置于空气中或遇到FeCl3溶液,都会变为紫色
C.从有机物的红外光谱图可以获得分子中含有何种化学键或官能团的信息
D.如图分别是实验室制取乙炔和乙酸乙酯的装置图,X、Y都是饱和食盐水
15.药物Z可用于治疗哮喘、系统性红斑狼疮等,可由X(咖啡酸)和Y(1,4-环己二酮单乙二醇缩酮)为原料合成(如图)。下列说法中正确的是的( )
A.可用FeCl3溶液检验此反应中是否有Z生成
B.X和Y生成Z的反应属于加成反应
C.1molZ与NaOH溶液反应,最多消耗3molNaOH
D.X中最多有9个碳原子共面
第Ⅱ卷 非选择题
非选择题(4题,共55分)
书写方程式(12分)
苯的硝化反应:___________________
用甲苯制取烈性炸药TNT:___________________
2﹣氯丙烷()的消去反应:___________________
向苯酚钠溶液里通入足量的CO2:___________________
苯酚与溴水的反应:__________________
乙醛与银氨溶液的反应:__________________
(14分)烃A(结构简式:)是有机化学工业的基本原料,可从石油中获得。烃A可发生如下图所示的一系列化学反应。
请回答下列问题:
(1)B的分子式为_______,③的反应类型是_______。
(2)E的名称是_______,可鉴别A、E两种物质的试剂是_______(填一种)。
(3)C是A通过加聚反应制得的有机高分子材料,其结构简式为_______。
(4)G的官能团是_______(填名称),F的结构简式是_______。
18.(16分))下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯。
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,该反应的化学方程式为______________________________________。
[装置设计]甲、乙、丙三位同学分别设计了如下图所示三套实验装置:
若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是________(填“甲”或“乙”)。乙中导管a的作用为________________________。丙同学将甲装置中的玻璃管改成了球形的干燥管,除了起上述作用外,另一重要作用是_______________。
[实验步骤]A.按所选择的装置组装仪器,在试管①中先加入3mL体积分数为95%的乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸。
B.将试管固定在铁架台上。
C.在试管②中加入5mL饱和Na2CO3溶液。
D.用酒精灯对试管①加热。
E.当观察到试管②中有明显现象时停止实验。
[问题讨论]
(1)步骤A组装好实验装置,加入样品前还应检查__________________________。
(2)试管②中观察到的现象是_____________________________。
(3)试管②中饱和Na2CO3溶液的作用是________________________,饱和Na2CO3溶液________(填“能”或“不能”)用NaOH溶液代替,其原因是_________________。
19.(13分)实验室用溴和乙醇制备1,2-二溴乙烷的装置如图所示,反应原理如下:
CH3CH2OH CH2=CH2 +H2O
CH2=CH2 +Br2 BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140°C脱水生成乙醚。
有关数据列表如下:
乙醇 1,2-二溴乙烷 乙醚
状态 无色液体 无色液体 无色液体
密度/ g·cm-3 0.79 2.2 0.71
沸点/°C 78.5 132 34.6
熔点/°C -130 9 -116
回答下列问题:
(1)在此制备实验中,要迅速地把反应温度提高到170°C左右,其最主要目的是___________。
(2)在装置C中应加入___________,其目的是吸收反应中可能生成的酸性气体。
A.水 B.浓硫酸
C.氢氧化钠溶液 D.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是___________。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中,加水并充分振荡,静置后液体分层,产物应在___________层(填“上”、“下”)。(1分)
(5)若产物中有少量未反应的Br2,最好用___________洗涤除去。
A.水 B.Na2SO3溶液
C.碘化钠溶液 D.乙醇
(6)若产物中有少量副产物乙醚可用___________的方法除去,反应过程中应用冷水冷却装置D,其主要目的是___________ 。
参考答案:
D
2. C
3. D
【详解】A.乙烯的实验式(最简式)为CH2,
B.乙醇的结构简式为C2H5OH或CH3CH2OH,
C.四氯化碳的电子式为,
4. A
5. B
6. B
【详解】A.丁醇、乙醚互溶,但沸点不同,则蒸馏可分离,
B.乙酸乙酯和乙醇互溶,不能分液分离,应选蒸馏法,
C.乙酸与碳酸钠反应生成气体,乙酸乙酯与碳酸钠溶液分层,现象不同可鉴别,
D.CH3COOCH2CH3与HCOOCH2CH3中均含3种H,但二者的核磁共振氢谱中峰的面积比不相同,可以用核磁共振氢谱来鉴别。
7. C
8. B
【详解】A.过滤时应该遵循一贴二低三靠,图中漏斗下端未紧靠烧杯内壁,不能悬空放置,
B.胶体粒子不能透过半透膜,分子、离子可以透过半透膜,图中渗析法可提纯胶体
C.蒸馏时温度计测定馏分的温度,应该放置蒸馏烧瓶支管口附近,
D.酯化反应需要浓硫酸作催化剂、吸水剂,图中未加浓硫酸,也未加碎瓷片以防止暴沸现象的发生,液体体积超过试管容积的
9. A
10. D
【详解】A. 5-FAM转变为5-CFDA,羟基上的H被乙酰基取代,属于取代反应,
B. 5-FAM的分子式为C21H12O7,
C. 5-FAM和5-CFDA 各1mol分别与足量NaOH溶液反应,消耗的NaOH 物质的量分别为4mol和6mol,5-CFDA消耗的NaOH 物质的量多,
D. 5-FAM与5-CFDA分子中都有羧基,都可与NaHCO3 溶液反应生成二氧化碳,所以不能用NaHCO3溶液鉴别它们。
11. AC
12. A
【详解】A.酚羟基、羧基都可以和Na2CO3反应,所以1mol绿原酸最多消耗3mol Na2CO3
B.该分子含有多个羟基,可和水分子、乙醇分子形成分子间氢键,可溶与水也可溶于乙醇
C.连接四个不同原子或原子团的碳原子为手性碳,该物质含有如图所示4个手性碳原子
D.结构中含氧官能团有羟基、酯基、羧基,
13. BC
14. BD
【详解】A. 乙烯是平面型分子、乙炔是直线型分子,双键碳和与之直接相连的6个原子共平面、叁键碳及与之直接相连的原子共线,故乙烯基乙炔(CH2=CHC≡CH)分子中所有原子位于同一平面
苯酚久置于空气中变粉红色,遇到FeCl3溶液,会变为紫色,
C.通过分析有机物的红外光谱图,可以知道分子中含有何种化学键或官能团,
D. 电石中加饱和食盐水可用于实验室制取乙炔,制取乙酸乙酯时试管Y中是饱和碳酸钠,
15. CD
【详解】A.X、Z分子中均含酚羟基,不能用FeCl3溶液检验此反应中是否有Z生成
B.1个加成反应的原子利用率为100%,该反应中O原子利用率小于100%,故该反应不是加成反应
Z分子中含一个酯基,2个酚羟基,因此1molZ与NaOH溶液反应,最多消耗3molNaOH
D苯环、乙烯是平面型分子,如图,图中两个方框内的C原子分别共面,两个平面共用两个点(C),因此这个两个平面可能共面,则X中最多有9个C原子共面。
16.书写方程式(12分,每空2分)
苯的硝化反应:,+HNO3(浓) +H2O;
烈性炸药TNT的制取:+3HNO3 + 3H2O
2﹣氯丙烷消去反应:+NaOHCH3CH=CH2↑+H2O+NaCl
向苯酚钠溶液里通入足量的CO2:+CO2+H2O→+NaHCO3
(5)苯酚与溴水的反应: +3Br2→ ↓+3HBr
(6)乙醛与银氨溶液的反应: CH3CHO+2Ag(NH3)2OH2Ag↓+CH3COONH4+3NH3+H2O
17.(14分,每空2分)
(1) C3H6Br2 加成反应
(2) 丙烷 溴水或溴的CCl4溶液或酸性高锰酸钾溶液
(3)
(4) 碳碳双键、酯基 CH2=CH2COOH
【分析】CH2=CHCH3经过反应①与溴发生加成反应,生成B(1,2-二溴丙烷),经过反应②发生加聚反应,生成C(聚丙烯),经过反应③与水发生加成反应,生成D(1-丙醇),经过反应④与氢气加成,生成E(丙烷),D和F发生酯化反应生成丙烯酸丙酯,可知F为丙烯酸。
(2)E是CH2=CHCH3经过反应④与氢气发生加成反应生成的丙烷,要鉴别丙烯和丙烷可以用溴水(或溴的CCl4溶液或酸性高锰酸钾溶液)。
(3)CH2=CHCH3经过反应②发生加聚反应,生成聚丙烯,其结构简式为
(4)从G结构简式中可以推知其中含有的官能团为:碳碳双键、酯基;D与F即1-丙醇与丙烯酸发生酯化反应生成丙烯酸丙酯,
(16分,除备注处1分其余每空2分)
CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O 乙(1分) 冷凝 防止倒吸
(1)装置气密性 (2) 液体分为两层且能闻到香味 (3)溶解乙醇、反应乙酸、降低乙酸乙酯的溶解度 不能(1分) NaOH和乙酸乙酯反应,促进乙酸乙酯的水解
【分析】实验室制取乙酸乙酯,利用乙酸、乙醇、浓硫酸共热发生酯化反应,生成乙酸乙酯和水;收集乙酸乙酯时用饱和碳酸钠溶液,可以起到溶解乙醇,中和乙酸,降低乙酸乙酯的溶解度的作用;长导管不能深入液面以下,防止倒吸,也可以使用干燥管,由此分析。
【详解】[实验原理]乙醇、乙酸与浓硫酸发生酯化反应,酸失去羟基醇失去羟基上的氢原子,生成乙酸乙酯和水,化学方程式为:CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O;
[装置设计]若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是乙,甲装置会引起倒吸,收集不到乙酸乙酯,乙中导管a的作用为冷凝;
丙同学将甲装置中的玻璃管改成了球形的干燥管,球形干燥管可以增大气体与液体的接触面积,可以防止倒吸;
[问题讨论](1)步骤A组装好实验装置,加入样品前还应检查装置的气密性,否则将导致实验失败;
(2)乙酸乙酯是有香味的密度比水小的油状液体,故试管②中观察到的现象是液体分为两层且能闻到香味;
(3)乙醇、乙酸与浓硫酸发生酯化反应,酸失去羟基醇失去羟基上的氢原子,生成乙酸乙酯和水,试管②中饱和Na2CO3溶液的作用是溶解乙醇、中和乙酸、降低乙酸乙酯的溶解度,饱和Na2CO3溶液不能用NaOH溶液代替,其原因是NaOH和乙酸乙酯反应,促进乙酸乙酯的水解,降低乙酸乙酯的产率。
【点睛】乙醇和乙酸制取乙酸乙酯的实验中,反应原理是酸失去羟基,醇失去羟基上的氢原子,属于酯化反应,也属于取代反应,酯在氢氧化钠存在条件下要发生水解,为易错点,饱和碳酸钠溶液的作用是难点。
(13分,除备注处1分其余每空2分)
(1)减少副产物乙醚生成
(2)C
(3)观察D中颜色是否完全褪去
(4)下(1分)
(5)B
(6) 蒸馏 避免溴大量挥发
【分析】实验室制备1,2-二溴乙烷:三颈烧瓶A中发生反应是乙醇在浓硫酸的作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应方程式为:CH3CH2OHCH2=CH2↑+H2O,如果D中导气管发生堵塞事故,A中产生的乙烯气体会导致装置B中压强增大,长导管液面会上升,所以装置B中长玻璃管可判断装置是否堵塞,装置B起缓冲作用,浓硫酸具有脱水性、吸水性和强氧化性,能氧化乙醇,CH3CH2OH+4H2SO4(浓)4SO2↑+CO2↑+7H2O+C,可能生成的酸性气体为二氧化硫、二氧化碳,装置C中放氢氧化钠溶液,发生反应SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH═Na2CO3+H2O,除去杂质气体,乙烯含有不饱和键C=C双键,能卤素单质发生加成反应,D中乙烯和溴加成生成1,2-二溴乙烷,反应为:CH2=CH2+Br-Br→CH2Br-CH2Br,制得1,2-二溴乙烷,据此分析解题。
(1)由题干信息可知,乙醇在140℃时发生取代反应生成乙醚,导致生成乙烯的量减少,
(2)由分析可知,浓硫酸具有脱水性、吸水性和强氧化性,能氧化乙醇,CH3CH2OH+4H2SO4(浓)4SO2↑+CO2↑+7H2O+C,可能生成的酸性气体为二氧化硫、二氧化碳,装置C中放氢氧化钠溶液,发生反应SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH═Na2CO3+H2O,除去杂质气体,故答案为:C;
(3)乙烯和溴发生加成反应而使溴水褪色,如果观察到D中颜色完全褪去就说明该制备反应已经结束,故答案为:观察D中颜色是否完全褪去;
(4)由题干信息可知,1,2-二溴乙烷的密度比水的要大,故将1,2-二溴乙烷粗产品置于分液漏斗中,加水并充分振荡,静置后液体分层,产物应在下层,故答案为:下;
(5)溴在水中的溶解度较小,但易溶于1,2-二溴乙烷,用水无法除溴;溴具有强氧化性,能氧化还原性物质,亚硫酸钠能被溴氧化转化为可溶性硫酸钠,可以除去溴;NaI也能被溴氧化但生成新的杂质I2,碘易溶于有机物,不能除去溴;酒精与1,2-二溴乙烷互溶,不能除去溴,故答案为:B;
(6)由题干信息可知,乙醚和1,2-二溴乙烷的沸点相差很大,故若产物中有少量副产物乙醚,可用蒸馏的方法除去,溴有毒且易挥发,所以反应过程中应用冷水冷却装置D,产品1,2一二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管。
同课章节目录
