【备考2023】浙教版科学“冲刺重高”压轴训练(二十三):化学基础(含解析)
文档属性
| 名称 | 【备考2023】浙教版科学“冲刺重高”压轴训练(二十三):化学基础(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 173.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-05-18 00:00:00 | ||
图片预览

文档简介
1.2月15日,科技部生物中心主任张新民在新闻发布会中提到,针对新型冠状病毒,科学家们已经进行了多次药物筛选,逐渐聚焦于磷酸氯喹、瑞德西韦等药物;两天后,也就是2月17日,科技部生物中心副主任孙燕荣再次在新闻发布会中提到磷酸氯喹{C18H26ClN3 2(H3PO4)}——研究显示,它对新冠肺炎的治疗有效。以下关于磷酸氯喹的说法中,正确的是( )
A.每个磷酸氯喹分子中含有二个磷酸分子
B.磷酸氯喹的相对分子质量为515.87克
C.磷酸氯喹共含有6种元素
D.磷酸氯喹是一种特效药,我们可以多吃一些以预防流感
2.如果用符号“●”表示氧原子,用符号“○”表示氢原子,则下列模型表示化合物的是( )
4.某同学认为“O2”表示意义有以下几种: ①表示氧元素;②表示氧气这种物质;③表示1个氧分子;④表示2个氧原子;⑤表示氧气是一种无色气体;⑥表示1个氧分子里有2个氧原子。其中正确的是( )
A.②④⑤ B.②③⑥ C.②③④⑤ D.②③⑤⑥
3.国际上有铟等7种元素的相对原子质量采用了我国科学家张青莲测的数据。由图可知铟元素( )
A.是非金属元素
B.质子数为49
C.相对原子质量是114.8g
D.与其他元素根本区别是中子数不同
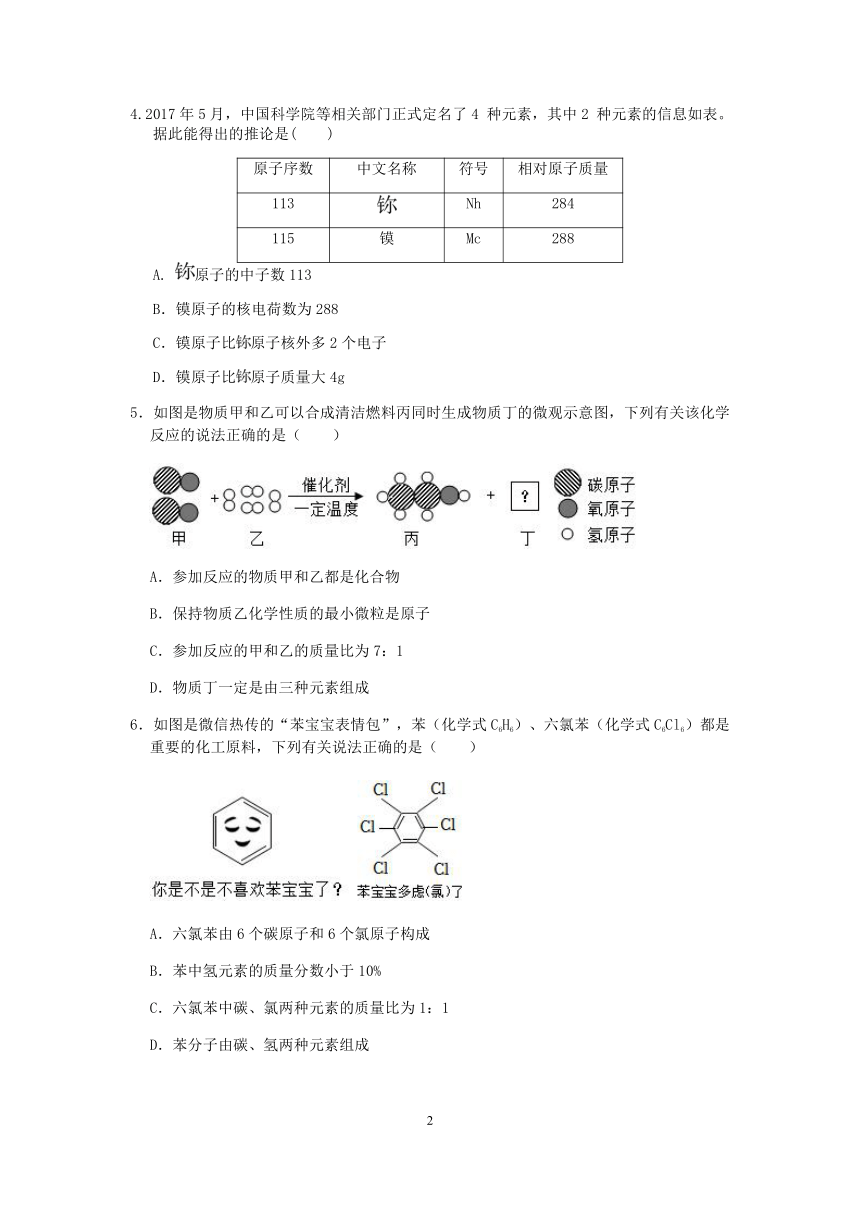
4.2017年5月,中国科学院等相关部门正式定名了4 种元素,其中2 种元素的信息如表。据此能得出的推论是( )
原子序数 中文名称 符号 相对原子质量
113 Nh 284
115 镆 Mc 288
A. 原子的中子数113
B.镆原子的核电荷数为288
C.镆原子比原子核外多2个电子
D.镆原子比原子质量大4g
5.如图是物质甲和乙可以合成清洁燃料丙同时生成物质丁的微观示意图,下列有关该化学反应的说法正确的是( )
A.参加反应的物质甲和乙都是化合物
B.保持物质乙化学性质的最小微粒是原子
C.参加反应的甲和乙的质量比为7:1
D.物质丁一定是由三种元素组成
6.如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是( )
A.六氯苯由6个碳原子和6个氯原子构成
B.苯中氢元素的质量分数小于10%
C.六氯苯中碳、氯两种元素的质量比为1:1
D.苯分子由碳、氢两种元素组成
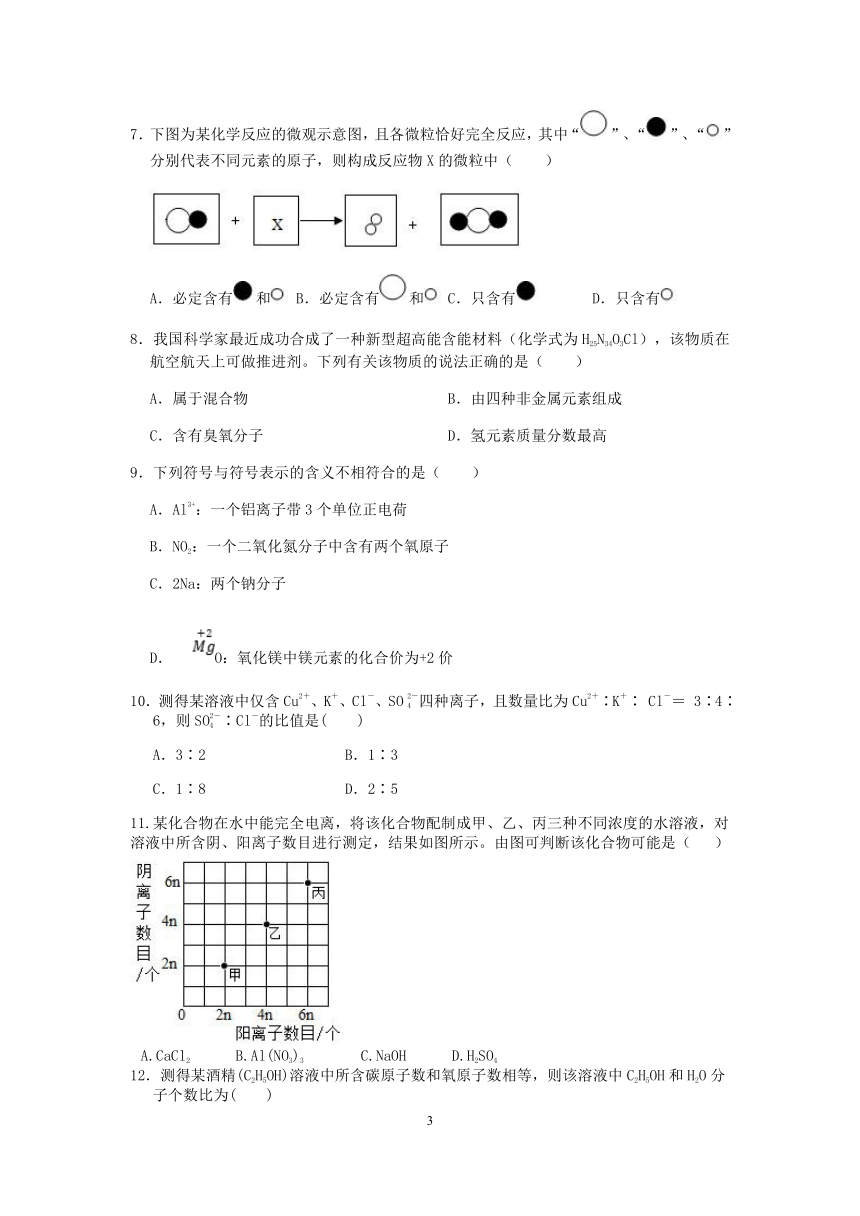
7.下图为某化学反应的微观示意图,且各微粒恰好完全反应,其中“”、“”、“”分别代表不同元素的原子,则构成反应物X的微粒中( )
A.必定含有和 B.必定含有和 C.只含有 D.只含有
8.我国科学家最近成功合成了一种新型超高能含能材料(化学式为H25N34O3Cl),该物质在航空航天上可做推进剂。下列有关该物质的说法正确的是( )
A.属于混合物 B.由四种非金属元素组成
C.含有臭氧分子 D.氢元素质量分数最高
9.下列符号与符号表示的含义不相符合的是( )
A.Al3+:一个铝离子带3个单位正电荷
B.NO2:一个二氧化氮分子中含有两个氧原子
C.2Na:两个钠分子
D.O:氧化镁中镁元素的化合价为+2价
10.测得某溶液中仅含Cu2+、K+、Cl-、SO四种离子,且数量比为Cu2+∶K+∶ Cl-= 3∶4∶6,则SO∶Cl-的比值是( )
A.3∶2 B.1∶3
C.1∶8 D.2∶5
11.某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( )
A.CaCl2 B.Al(NO3)3 C.NaOH D.H2SO4
12.测得某酒精(C2H5OH)溶液中所含碳原子数和氧原子数相等,则该溶液中C2H5OH和H2O分子个数比为( )
A.1∶1 B.1∶2
C.1∶3 D.1∶4
13.某固体混合物由硫化钠(Na2S)和亚硫酸钠(Na2SO3)两种物质组成。已知该固体混合物中氧元素的质量分数为22%。则该固体混合物中钠元素的质量分数为( )
A.23% B.46%
C.50% D.78%
14.A、B、C为三种元素的符号,A、B2-、C+三种微粒都具有10个核外电子,A的元素符号为____,C2B的化学式为____,B元素与氢元素组成的化合物的化学式为____(写出一种即可)。
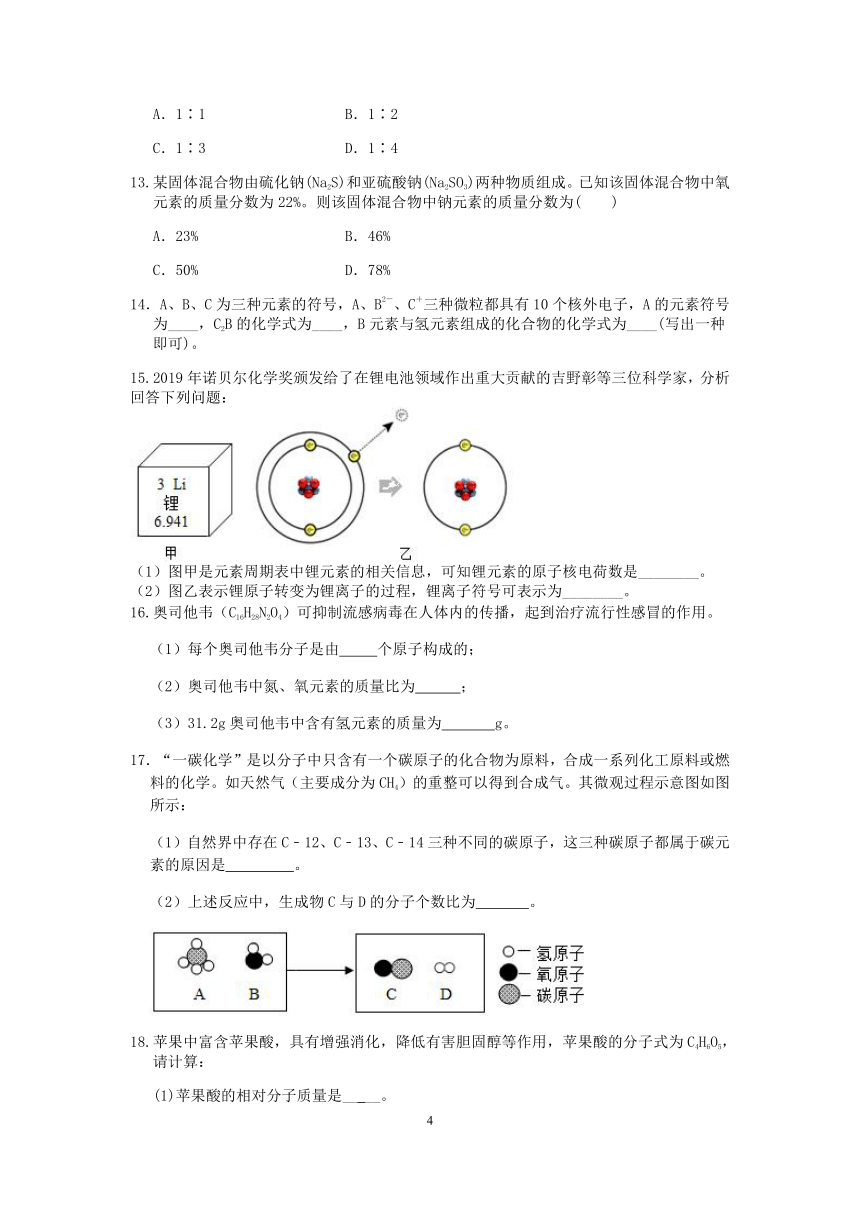
15.2019年诺贝尔化学奖颁发给了在锂电池领域作出重大贡献的吉野彰等三位科学家,分析回答下列问题:
(1)图甲是元素周期表中锂元素的相关信息,可知锂元素的原子核电荷数是________。
(2)图乙表示锂原子转变为锂离子的过程,锂离子符号可表示为________。
16.奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播,起到治疗流行性感冒的作用。
(1)每个奥司他韦分子是由 个原子构成的;
(2)奥司他韦中氮、氧元素的质量比为 ;
(3)31.2g奥司他韦中含有氢元素的质量为 g。
17.“一碳化学”是以分子中只含有一个碳原子的化合物为原料,合成一系列化工原料或燃料的化学。如天然气(主要成分为CH4)的重整可以得到合成气。其微观过程示意图如图所示:
(1)自然界中存在C﹣12、C﹣13、C﹣14三种不同的碳原子,这三种碳原子都属于碳元素的原因是 。
(2)上述反应中,生成物C与D的分子个数比为 。
18.苹果中富含苹果酸,具有增强消化,降低有害胆固醇等作用,苹果酸的分子式为C4H6O5,请计算:
(1)苹果酸的相对分子质量是__ __。
(2)苹果酸中碳、氢、氧三种元素的质量比是__ _(最简整数比)。
(3)13.4g苹果酸中含C元素质量多少克?(写出计算过程,答案精确到0.1)。
19.我国科学家屠呦呦由于成功提取出青蒿素,获得了 2015年诺贝尔生理学或医学奖。青蒿 素的化学式为 C15H22O5。试计算:
(1)青蒿素的相对分子质量为____。
(2)青蒿素中,各元素质量的最简整数比为 m(C)∶m(H)∶m(O)=____。
20.某晶体是一种结晶水合物,其相对分子质量为126,化学式可用CxHyOz·nH2O来表示。取12.6g该晶体,100℃加热失去结晶水后称得固体质量为9g,又测得在无水物CxHyOz中,碳、氢、氧的质量分数分别为26.7%、2.2%、71.1%,通过计算确定该晶体的化学式。
参考答案
1.解:A、磷酸氯喹是由磷酸氯喹分子构成,不含有磷酸分子,说法错误;
B、相对分子质量的单位是“1”,不是“g”,说法错误;
C、磷酸氯喹共含有6种元素,说法正确;
D、磷酸氯喹是一种特效药,对新冠肺炎的治疗有效,但不能预防流感,说法错误;
故选:C。
2.A
【解析】A图中每一个粒子(水分子)都是由一个氧原子和两个氢原子构成,表示化合物。B图表示水和氢气的混合物。C图表示氢气和氧气的混合物。D图表示氢气单质。
4.B
【解析】化学式的含义:(1)表示该种物质;(2)表示该物质的组成;(3)表示该物质的一个分子;(4)表示该物质的一个分子的构成。
3.B
【解析】该元素的名称是铟,汉字名称的偏旁“钅”,属于金属元素。铟原子中质子数为49。该元素的相对原子质量为114.8,相对原子质量单位符号是“1”,不是“g”,省略不写。铟与其他元素根本区别是质子数不同。
4.C
【解析】原子核内的中子数为相对原子质量与原子序数的差,所以原子的中子数为171;原子的核电荷数等于原子序数即核内质子数,所以镆原子的核电荷数为115;原子的核外电子数就等于核电荷数,所以镆原子比原子核外多2 个电子;镆原子的相对原子质量比原子大4。
5.解:甲物质的化学式为CO、乙物质的化学式为H2、丙物质的化学式为C2H6O,结合质量守恒定律化学反应前后原子的种类和个数都不变可知丁的化学式为H2O,因此反应的方程式为:2CO+4H2C2H6O+H2O,因此:
A、由物质的组成可知,参加反应的物质甲是化合物,物质乙是单质,故说法错误;
B、由微粒的构成可知,乙是由分子构成的,保持物质乙化学性质的最小微粒是分子,故说法错误;
C、由方程式可知,参加反应的甲和乙的质量比为(28×2):(2×4)=7:1,故说法正确;
D、由上述分析可知,丁物质是水,是由氢、氧两种元素组成的化合物,故D说法错误。
故选:C。
6.解:A、六氯苯是由六氯苯分子构成的,而不是由原子直接构成的,故错误;
B、苯中氢元素的质量分数为100%≈7.7%<10%,故正确;
C、由六氯苯的化学式C6Cl6可知,其中碳元素和氯元素的质量比为:(12×6):(35.5×6)=12:35.5,故错误;
D、苯是由苯分子构成的,苯是由碳元素与氢元素组成的,故错误。
故选:B。
7.解:由化学反应的微观示意图,且各微粒恰好完全反应可知,反应前有一个“”、“”原子。反应后有两个原子、一个原子、两个,根据质量守恒定律反应前后原子的种类及数目不变可推出构成反应物X的微粒中必定含有和.所以A正确。
故选:A。
8.解:A.由全氮阴离子盐(化学式为H25N34O3Cl)的化学式可知,该物质是由一种物质组成的,属于纯净物,故选项说法错误。
B.全氮阴离子盐是由氢、氮、氧、氯四种非金属元素组成的,故选项说法正确。
C.分子是由原子构成的,1个全氮阴离子盐分子是由25个氢原子、34个氮原子、3个氧原子和1个氯原子构成的,不含臭氧分子,故选项说法错误。
D.H25N34O3Cl中,氢、氮、氧、氯四种元素的质量比为:(1×25):(14×34):(16×3):35.5=25:476:48:35.5,可见其中氮元素的质量分数最高,故选项说法错误。
故选:B。
9.解:A、Al3+中的3表示一个铝离子带3个单位正电荷,正确;
B、NO2中的2表示一个二氧化氮分子中含有两个氧原子,正确;
C、2Na中的2表示两个钠原子,不是分子,错误;
D、O中的2表示氧化镁中镁元素的化合价为+2价,正确;
故选:C。
10.B
【解析】整个溶液呈电中性,即四种离子所带正、负电荷数相等。设离子的数量比Cu2+∶K+∶Cl-∶SO=3∶4∶6∶n,则+2×3+1×4-1×6-2×n=0,解得:n=2,所以离子数量比SO∶Cl-=2∶6=1∶3。
11.C
【解析】根据图像可知,无论溶液的浓度如何,该化合物的阴、阳离子的个数之比为:2n:2n=1:1;4n:4n=1:1;6n:6n=1:1。在四种物质中,只有NaOH的阴、阳离子的个数之比为1:1,故C正确,而A、B、D错误。
12.测得某酒精(C2H5OH)溶液中所含碳原子数和氧原子数相等,则该溶液中C2H5OH和H2O分子个数比为( )
A.1∶1 B.1∶2
C.1∶3 D.1∶4
【答案】A
【解析】设C2H5OH和H2O的分子个数比为x∶y,2x∶(x+y)=1∶1,则x∶y=1∶1。
13.B
【解析】在Na2S、Na2SO3两种物质组成的混合物中一共有三种元素,其中氧元素含量为22%,则钠元素和硫元素的含量共为78%;由化学式分析可知在混合物中钠元素和硫元素的质量比为(23×2)∶32=23∶16;所以硫元素的质量分数为23/(23+16)×78%=46%。
14.Ne Na2O H2O(或H2O2)
【解析】A不带电荷,所以A为原子,核外有10个电子,则A为10号元素氖(Ne)。B2-是B得到2个电子后形成的离子,该离子核外电子数也为10,所以B为8号元素氧(O)。C失去一个电子后形成C+,其核外电子也为10,所以C为11号元素钠(Na)。
15.(1)3 (2)Li+
【解析】(1)在元素周期表中,元素名称左上角的数字就是原子序数,而原子序数=质子数=核电荷数;
(2)在原子变成离子过程中,失去电子带正电荷,得到电子带负电荷,所带电荷数与得失电子的个数有关。
【解答】(1)根据甲图可知,锂元素的原子序数为3;根据核电荷数=原子序数得到,锂元素的原子核电荷数为3.
(2)根据乙图可知,锂原子失去一个电子得到锂离子,因此锂离子带一个单位的正电荷,那么符号为: Li+ 。
16.解:(1)由化学式可知,1个奥司他韦分子是由16个碳原子、28个氢原子、2个氮原子和4个氧原子构成的,共含50个原子;故填:50;
(2)奥司他韦中氮、氧元素的质量比为(14×2):(16×4)=7:16;故填:7:16;
(3)31.2g奥司他韦中含有氢元素的质量为31.2g2.8g;故填:2.8。
17.解:(1)C﹣12、C﹣13、C﹣14三种不同的碳原子都属于碳元素是因为它们的质子数相同,故填:它们的质子数相同;
(2)根据微观模型图可以看出,该反应的化学方程式为:CH4+H2O=CO+3H2,故C和D的分子个数比为1:3,故填:1:3。
18.(3)13.4g苹果酸中含C元素质量为: 13.4g××100%=4.8g。
【解析】(1)苹果酸的相对分子质量为12×4+1×6+16×5=134。(2)苹果酸中碳、氢、氧三种元素的质量比是(12×4)∶(1×6)∶(16×5)=24∶3∶40。
19.282 90∶11∶40
【解析】(1)青蒿素的相对分子质量为12×15+1×22+16×5=282。(2)青蒿素中碳、氢、氧三种元素的质量比为:(12×15)∶(1×22)∶(16×5)=90∶11∶40。
20.晶体的化学式为C2H2O4·2H2O。
【解析】由题意可知,结晶水的质量为12.6g-9g=3.6g,从化学式(CxHyOz·nH2O)求算含水量算式为H2O%===,
解得:n=2,
CxHyOz的相对分子质量为126-2×18=90,
C%===26.7%,x=2,
H%===2.2%,y=2,
O%===71.1%,z=4,
晶体的化学式为C2H2O4·2H2O。
化学基础
A.每个磷酸氯喹分子中含有二个磷酸分子
B.磷酸氯喹的相对分子质量为515.87克
C.磷酸氯喹共含有6种元素
D.磷酸氯喹是一种特效药,我们可以多吃一些以预防流感
2.如果用符号“●”表示氧原子,用符号“○”表示氢原子,则下列模型表示化合物的是( )
4.某同学认为“O2”表示意义有以下几种: ①表示氧元素;②表示氧气这种物质;③表示1个氧分子;④表示2个氧原子;⑤表示氧气是一种无色气体;⑥表示1个氧分子里有2个氧原子。其中正确的是( )
A.②④⑤ B.②③⑥ C.②③④⑤ D.②③⑤⑥
3.国际上有铟等7种元素的相对原子质量采用了我国科学家张青莲测的数据。由图可知铟元素( )
A.是非金属元素
B.质子数为49
C.相对原子质量是114.8g
D.与其他元素根本区别是中子数不同
4.2017年5月,中国科学院等相关部门正式定名了4 种元素,其中2 种元素的信息如表。据此能得出的推论是( )
原子序数 中文名称 符号 相对原子质量
113 Nh 284
115 镆 Mc 288
A. 原子的中子数113
B.镆原子的核电荷数为288
C.镆原子比原子核外多2个电子
D.镆原子比原子质量大4g
5.如图是物质甲和乙可以合成清洁燃料丙同时生成物质丁的微观示意图,下列有关该化学反应的说法正确的是( )
A.参加反应的物质甲和乙都是化合物
B.保持物质乙化学性质的最小微粒是原子
C.参加反应的甲和乙的质量比为7:1
D.物质丁一定是由三种元素组成
6.如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是( )
A.六氯苯由6个碳原子和6个氯原子构成
B.苯中氢元素的质量分数小于10%
C.六氯苯中碳、氯两种元素的质量比为1:1
D.苯分子由碳、氢两种元素组成
7.下图为某化学反应的微观示意图,且各微粒恰好完全反应,其中“”、“”、“”分别代表不同元素的原子,则构成反应物X的微粒中( )
A.必定含有和 B.必定含有和 C.只含有 D.只含有
8.我国科学家最近成功合成了一种新型超高能含能材料(化学式为H25N34O3Cl),该物质在航空航天上可做推进剂。下列有关该物质的说法正确的是( )
A.属于混合物 B.由四种非金属元素组成
C.含有臭氧分子 D.氢元素质量分数最高
9.下列符号与符号表示的含义不相符合的是( )
A.Al3+:一个铝离子带3个单位正电荷
B.NO2:一个二氧化氮分子中含有两个氧原子
C.2Na:两个钠分子
D.O:氧化镁中镁元素的化合价为+2价
10.测得某溶液中仅含Cu2+、K+、Cl-、SO四种离子,且数量比为Cu2+∶K+∶ Cl-= 3∶4∶6,则SO∶Cl-的比值是( )
A.3∶2 B.1∶3
C.1∶8 D.2∶5
11.某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( )
A.CaCl2 B.Al(NO3)3 C.NaOH D.H2SO4
12.测得某酒精(C2H5OH)溶液中所含碳原子数和氧原子数相等,则该溶液中C2H5OH和H2O分子个数比为( )
A.1∶1 B.1∶2
C.1∶3 D.1∶4
13.某固体混合物由硫化钠(Na2S)和亚硫酸钠(Na2SO3)两种物质组成。已知该固体混合物中氧元素的质量分数为22%。则该固体混合物中钠元素的质量分数为( )
A.23% B.46%
C.50% D.78%
14.A、B、C为三种元素的符号,A、B2-、C+三种微粒都具有10个核外电子,A的元素符号为____,C2B的化学式为____,B元素与氢元素组成的化合物的化学式为____(写出一种即可)。
15.2019年诺贝尔化学奖颁发给了在锂电池领域作出重大贡献的吉野彰等三位科学家,分析回答下列问题:
(1)图甲是元素周期表中锂元素的相关信息,可知锂元素的原子核电荷数是________。
(2)图乙表示锂原子转变为锂离子的过程,锂离子符号可表示为________。
16.奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播,起到治疗流行性感冒的作用。
(1)每个奥司他韦分子是由 个原子构成的;
(2)奥司他韦中氮、氧元素的质量比为 ;
(3)31.2g奥司他韦中含有氢元素的质量为 g。
17.“一碳化学”是以分子中只含有一个碳原子的化合物为原料,合成一系列化工原料或燃料的化学。如天然气(主要成分为CH4)的重整可以得到合成气。其微观过程示意图如图所示:
(1)自然界中存在C﹣12、C﹣13、C﹣14三种不同的碳原子,这三种碳原子都属于碳元素的原因是 。
(2)上述反应中,生成物C与D的分子个数比为 。
18.苹果中富含苹果酸,具有增强消化,降低有害胆固醇等作用,苹果酸的分子式为C4H6O5,请计算:
(1)苹果酸的相对分子质量是__ __。
(2)苹果酸中碳、氢、氧三种元素的质量比是__ _(最简整数比)。
(3)13.4g苹果酸中含C元素质量多少克?(写出计算过程,答案精确到0.1)。
19.我国科学家屠呦呦由于成功提取出青蒿素,获得了 2015年诺贝尔生理学或医学奖。青蒿 素的化学式为 C15H22O5。试计算:
(1)青蒿素的相对分子质量为____。
(2)青蒿素中,各元素质量的最简整数比为 m(C)∶m(H)∶m(O)=____。
20.某晶体是一种结晶水合物,其相对分子质量为126,化学式可用CxHyOz·nH2O来表示。取12.6g该晶体,100℃加热失去结晶水后称得固体质量为9g,又测得在无水物CxHyOz中,碳、氢、氧的质量分数分别为26.7%、2.2%、71.1%,通过计算确定该晶体的化学式。
参考答案
1.解:A、磷酸氯喹是由磷酸氯喹分子构成,不含有磷酸分子,说法错误;
B、相对分子质量的单位是“1”,不是“g”,说法错误;
C、磷酸氯喹共含有6种元素,说法正确;
D、磷酸氯喹是一种特效药,对新冠肺炎的治疗有效,但不能预防流感,说法错误;
故选:C。
2.A
【解析】A图中每一个粒子(水分子)都是由一个氧原子和两个氢原子构成,表示化合物。B图表示水和氢气的混合物。C图表示氢气和氧气的混合物。D图表示氢气单质。
4.B
【解析】化学式的含义:(1)表示该种物质;(2)表示该物质的组成;(3)表示该物质的一个分子;(4)表示该物质的一个分子的构成。
3.B
【解析】该元素的名称是铟,汉字名称的偏旁“钅”,属于金属元素。铟原子中质子数为49。该元素的相对原子质量为114.8,相对原子质量单位符号是“1”,不是“g”,省略不写。铟与其他元素根本区别是质子数不同。
4.C
【解析】原子核内的中子数为相对原子质量与原子序数的差,所以原子的中子数为171;原子的核电荷数等于原子序数即核内质子数,所以镆原子的核电荷数为115;原子的核外电子数就等于核电荷数,所以镆原子比原子核外多2 个电子;镆原子的相对原子质量比原子大4。
5.解:甲物质的化学式为CO、乙物质的化学式为H2、丙物质的化学式为C2H6O,结合质量守恒定律化学反应前后原子的种类和个数都不变可知丁的化学式为H2O,因此反应的方程式为:2CO+4H2C2H6O+H2O,因此:
A、由物质的组成可知,参加反应的物质甲是化合物,物质乙是单质,故说法错误;
B、由微粒的构成可知,乙是由分子构成的,保持物质乙化学性质的最小微粒是分子,故说法错误;
C、由方程式可知,参加反应的甲和乙的质量比为(28×2):(2×4)=7:1,故说法正确;
D、由上述分析可知,丁物质是水,是由氢、氧两种元素组成的化合物,故D说法错误。
故选:C。
6.解:A、六氯苯是由六氯苯分子构成的,而不是由原子直接构成的,故错误;
B、苯中氢元素的质量分数为100%≈7.7%<10%,故正确;
C、由六氯苯的化学式C6Cl6可知,其中碳元素和氯元素的质量比为:(12×6):(35.5×6)=12:35.5,故错误;
D、苯是由苯分子构成的,苯是由碳元素与氢元素组成的,故错误。
故选:B。
7.解:由化学反应的微观示意图,且各微粒恰好完全反应可知,反应前有一个“”、“”原子。反应后有两个原子、一个原子、两个,根据质量守恒定律反应前后原子的种类及数目不变可推出构成反应物X的微粒中必定含有和.所以A正确。
故选:A。
8.解:A.由全氮阴离子盐(化学式为H25N34O3Cl)的化学式可知,该物质是由一种物质组成的,属于纯净物,故选项说法错误。
B.全氮阴离子盐是由氢、氮、氧、氯四种非金属元素组成的,故选项说法正确。
C.分子是由原子构成的,1个全氮阴离子盐分子是由25个氢原子、34个氮原子、3个氧原子和1个氯原子构成的,不含臭氧分子,故选项说法错误。
D.H25N34O3Cl中,氢、氮、氧、氯四种元素的质量比为:(1×25):(14×34):(16×3):35.5=25:476:48:35.5,可见其中氮元素的质量分数最高,故选项说法错误。
故选:B。
9.解:A、Al3+中的3表示一个铝离子带3个单位正电荷,正确;
B、NO2中的2表示一个二氧化氮分子中含有两个氧原子,正确;
C、2Na中的2表示两个钠原子,不是分子,错误;
D、O中的2表示氧化镁中镁元素的化合价为+2价,正确;
故选:C。
10.B
【解析】整个溶液呈电中性,即四种离子所带正、负电荷数相等。设离子的数量比Cu2+∶K+∶Cl-∶SO=3∶4∶6∶n,则+2×3+1×4-1×6-2×n=0,解得:n=2,所以离子数量比SO∶Cl-=2∶6=1∶3。
11.C
【解析】根据图像可知,无论溶液的浓度如何,该化合物的阴、阳离子的个数之比为:2n:2n=1:1;4n:4n=1:1;6n:6n=1:1。在四种物质中,只有NaOH的阴、阳离子的个数之比为1:1,故C正确,而A、B、D错误。
12.测得某酒精(C2H5OH)溶液中所含碳原子数和氧原子数相等,则该溶液中C2H5OH和H2O分子个数比为( )
A.1∶1 B.1∶2
C.1∶3 D.1∶4
【答案】A
【解析】设C2H5OH和H2O的分子个数比为x∶y,2x∶(x+y)=1∶1,则x∶y=1∶1。
13.B
【解析】在Na2S、Na2SO3两种物质组成的混合物中一共有三种元素,其中氧元素含量为22%,则钠元素和硫元素的含量共为78%;由化学式分析可知在混合物中钠元素和硫元素的质量比为(23×2)∶32=23∶16;所以硫元素的质量分数为23/(23+16)×78%=46%。
14.Ne Na2O H2O(或H2O2)
【解析】A不带电荷,所以A为原子,核外有10个电子,则A为10号元素氖(Ne)。B2-是B得到2个电子后形成的离子,该离子核外电子数也为10,所以B为8号元素氧(O)。C失去一个电子后形成C+,其核外电子也为10,所以C为11号元素钠(Na)。
15.(1)3 (2)Li+
【解析】(1)在元素周期表中,元素名称左上角的数字就是原子序数,而原子序数=质子数=核电荷数;
(2)在原子变成离子过程中,失去电子带正电荷,得到电子带负电荷,所带电荷数与得失电子的个数有关。
【解答】(1)根据甲图可知,锂元素的原子序数为3;根据核电荷数=原子序数得到,锂元素的原子核电荷数为3.
(2)根据乙图可知,锂原子失去一个电子得到锂离子,因此锂离子带一个单位的正电荷,那么符号为: Li+ 。
16.解:(1)由化学式可知,1个奥司他韦分子是由16个碳原子、28个氢原子、2个氮原子和4个氧原子构成的,共含50个原子;故填:50;
(2)奥司他韦中氮、氧元素的质量比为(14×2):(16×4)=7:16;故填:7:16;
(3)31.2g奥司他韦中含有氢元素的质量为31.2g2.8g;故填:2.8。
17.解:(1)C﹣12、C﹣13、C﹣14三种不同的碳原子都属于碳元素是因为它们的质子数相同,故填:它们的质子数相同;
(2)根据微观模型图可以看出,该反应的化学方程式为:CH4+H2O=CO+3H2,故C和D的分子个数比为1:3,故填:1:3。
18.(3)13.4g苹果酸中含C元素质量为: 13.4g××100%=4.8g。
【解析】(1)苹果酸的相对分子质量为12×4+1×6+16×5=134。(2)苹果酸中碳、氢、氧三种元素的质量比是(12×4)∶(1×6)∶(16×5)=24∶3∶40。
19.282 90∶11∶40
【解析】(1)青蒿素的相对分子质量为12×15+1×22+16×5=282。(2)青蒿素中碳、氢、氧三种元素的质量比为:(12×15)∶(1×22)∶(16×5)=90∶11∶40。
20.晶体的化学式为C2H2O4·2H2O。
【解析】由题意可知,结晶水的质量为12.6g-9g=3.6g,从化学式(CxHyOz·nH2O)求算含水量算式为H2O%===,
解得:n=2,
CxHyOz的相对分子质量为126-2×18=90,
C%===26.7%,x=2,
H%===2.2%,y=2,
O%===71.1%,z=4,
晶体的化学式为C2H2O4·2H2O。
化学基础
同课章节目录
