2.1.1有机物中碳原子成键特点及结构的表示方法-高中化学课件(共48张PPT)(苏教版2019选择性必修3)
文档属性
| 名称 | 2.1.1有机物中碳原子成键特点及结构的表示方法-高中化学课件(共48张PPT)(苏教版2019选择性必修3) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-20 00:00:00 | ||
图片预览








文档简介
(共48张PPT)
2.1.1有机物中碳原子成键特点及结构的表示方法
专
题
二
学习目标
01
了解有机物中碳原子的成键特点
02
分析有机物中的原子共面问题(难点)
03
学会有机物结构的表示方法(重点)
01
有机物中碳原子的成键特点
PART ONE
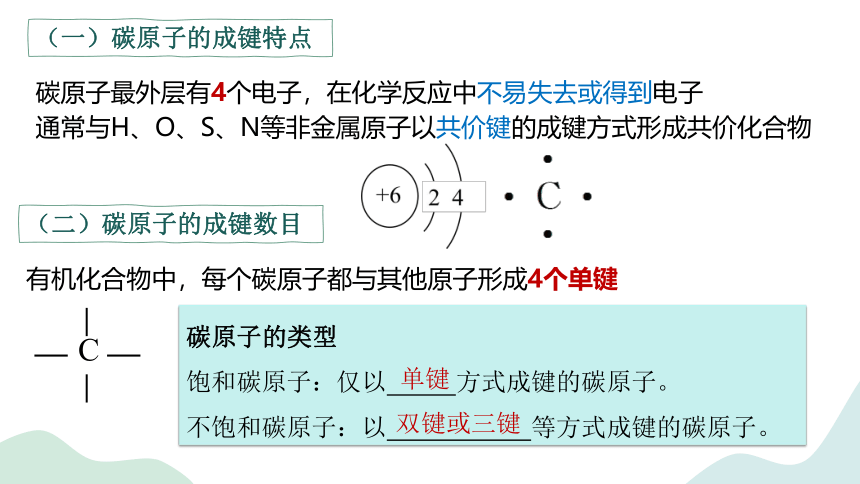
(一)碳原子的成键特点
碳原子最外层有4个电子,在化学反应中不易失去或得到电子
通常与H、O、S、N等非金属原子以共价键的成键方式形成共价化合物
(二)碳原子的成键数目
有机化合物中,每个碳原子都与其他原子形成4个单键
C
碳原子的类型
饱和碳原子:仅以 方式成键的碳原子。
不饱和碳原子:以 等方式成键的碳原子。
单键
双键或三键
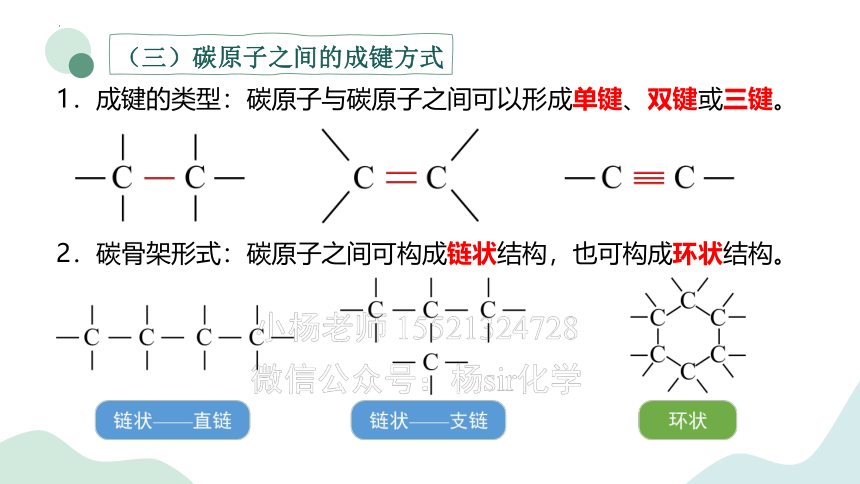
(三)碳原子之间的成键方式
1.成键的类型:碳原子与碳原子之间可以形成单键、双键或三键。
2.碳骨架形式:碳原子之间可构成链状结构,也可构成环状结构。
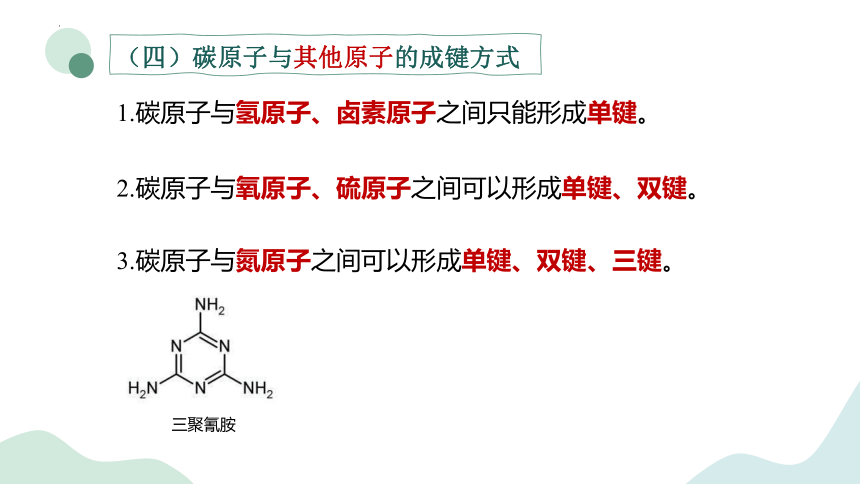
(四)碳原子与其他原子的成键方式
1.碳原子与氢原子、卤素原子之间只能形成单键。
2.碳原子与氧原子、硫原子之间可以形成单键、双键。
3.碳原子与氮原子之间可以形成单键、双键、三键。
三聚氰胺
题组例练
(以下选择题有1个或2个选项符合题意)
1.下列说法正确的是( )
A.碳原子的最外层有4个电子,故只能形成4条单键
B.破坏碳碳双键和三键所需要的能量分别是破坏碳碳单键所需能量的2倍和3倍
C.CH3—CH3中只存在共价键
D.乙醇和乙酸中均含有羟基(—OH),但两者性质不同
CD
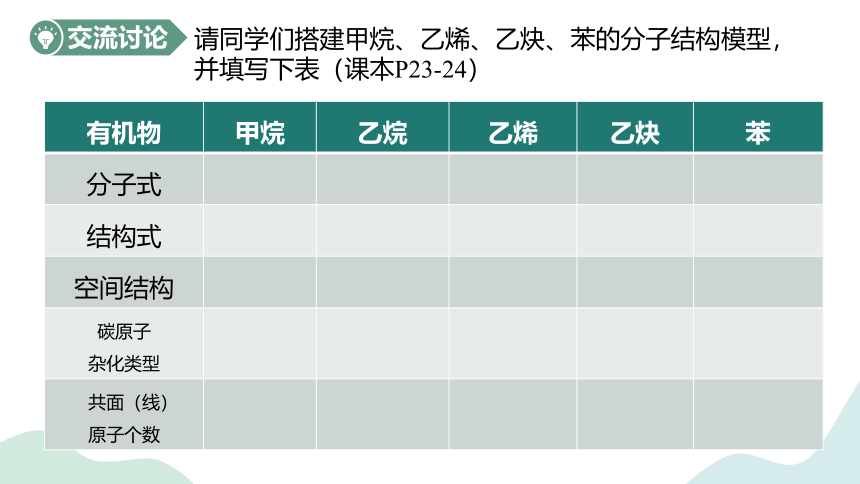
交流讨论
请同学们搭建甲烷、乙烯、乙炔、苯的分子结构模型,并填写下表(课本P23-24)
有机物 甲烷 乙烷 乙烯 乙炔 苯
分子式
结构式
空间结构
碳原子 杂化类型
共面(线) 原子个数
碳原子的成键方式与空间结构
1. 4个单键:碳原子与其他4个原子形成四面体结构,分子中所有原子可能同时不共面,如甲烷,乙烷。
2.双键:形成双键的碳原子跟与其直接相连的原子处于同一平面上,分子中至少有6个原子同时共面,如乙烯。
3.三键:形成三键的碳原子跟与其直接相连的原子处于同一直线上,分子中至少有4个原子同时共线,如乙炔。
4.苯环:有机物分子中含有一个苯环,至少有12个原子共面,如苯。
题组例练
3.在①丙烯、②氯乙烯、③苯、④甲苯四种有机化合物中,分子内所有原子均在同一平面的是( )
A.①② B.②③ C.③④ D.②④
B
02
有机物结构的表示方法
PART TWO
有机物结构的表示方法
1.结构式
2.结构简式
3.键线式
(一)结构式
1.概念:
优点:能完整地表示出有机物分子中每个原子的成键情况
缺点:书写比较麻烦
例1. 写出乙烷、乙醇、丙酸的结构式。
将分子中每对共用电子对都用一条短线表示的式子。(完整)
(二)结构简式
1.概念:
在结构式的基础上,省略碳氢键,也可省略碳碳单键,还可合并相同的部分。
注意事项:
1.表示单键的“—”:C-H一般省略;其它单键可以省略;上下连接“│”不能省略。
2.表示双键和三键的“=”和“≡”:C=C和C≡C不能省略;C=O可以省略。
3.准确表示分子中原子成键的情况(原子间连接情况)
(二)结构简式
结构简式:
CH3
CH2
CH2
CH2
CH3
CH3
CH2
CH2
CH2
CH3
CH3
(CH2)3
CH3
C
C
C
C
C
H
H
H
H
H
H
H
H
H
H
H
H
结构式:
(二)结构简式
C
C
C
H
H
H
H
C
H
H
H
H
CH2
CH
CH2
CH3
CH2
CH
CH2
CH3
结构简式:
结构式:
分子式: C4H8
(三)键线式
1.概念:
省略掉C、H原子,仅将(碳碳)键用短线表示
例3. 戊烷、1-丁烯、乙酸、葡萄糖
注意:每个拐点、交点和端点均表示一个碳原子。
CH3
CH2
CH2
CH2
CH3
分子式: C5H12
键线式:
结构简式:
(三)键线式
CH2
CH
CH2
CH3
分子式: C4H8
键线式:
结构简式:
(三)键线式
CH3
C
O
O
H
O
OH
分子式: C2H4O2
键线式:
结构简式:
键线式书写注意事项
①省去C、H元素符号,只要求表示出碳碳键(单键、双键、三键)及与碳原子相连的基团.
② —OH、—CHO、—COOH、—X等官能团不省
③端点、拐点、交叉点是C。
写出下列有机物对应的键线式或结构简式
学以致用
CH3 – CH – C = CH – CHO
OH
CH2CH3
Cl
O
O
=
有机物分子组成和结构的表示方法
分子式
最简式
电子式
结构式
结构简式
键线式
碳骨架式
球棍模型
空间填充模型
只表示分子的组成,不能反映物质的结构.
只表示分子的部分组成,不能反映物质的结构.
既能表示分子的组成,
又能反映物质的结构.
但书写麻烦!
既能表示分子的组成,
又能反映物质的结构.
只能表示碳原子的连接方式,不能表示分子组成!
既能表示分子的组成,
又能反映物质的结构.
一般只用于题目分析,正规的书写表达时不用!
常用
03
不饱和度的计算与应用
PART THREE
(一)不饱和度的计算
不饱和度又称缺氢指数,有机物分子与碳原子数目相等的链状烷烃相比较,每减少2个氢原子,则有机物不饱和度增加1,通常用Ω表示。
基团 少氢数 不饱和度
碳碳双键 少2H 1
碳环 少2H 1
碳氧双键 少2H 1
碳碳三键 少4H 2
苯环 少8H 4
(一)不饱和度的计算
(二)不饱和度的应用
1.已知分子式,推测结构
2.分子式为C6H9Br的有机化合物,其结构不可能是( )
A.含有一个双键的直链有机化合物
B.含有两个双键的直链有机化合物
C.含有一个双键的环状有机化合物
D.含有两个环的环状有机化合物
在判断有机物结构时,可以把卤素看作是氢原子被取代。
接着找有机物对应的烷烃,计算不饱和度,猜测可能结构。
A
(二)不饱和度的应用
2.通过不饱和度计算分子式
CHO
C6H12O
C8H8
C14H10
(二)不饱和度的应用
2.通过不饱和度计算分子式
C26H26
04
有机物原子共线共面问题
PART FOUR
先将被分析对象分解成下述几种常用的结构模板,最后综合分析不同结构间的交叉关系确定结果。
基本方法
结构 四面体形 平面形 直线形
模板 5个原子构成四面体,有3个原子共面 6个原子共面; 12个原子共面 a —C≡C—b:
4个原子共直线;苯环上处于对角位置的4个原子共直线
对照模板确定共线、共面原子数目
需要结合相关的几何知识进行分析:如不共线的任意三点可确定一个平面;一条直线与某平面有两个交点时,则这条直线上的所有点都在相应的平面内;同时要注意问题中的限定性词语(如最多、至少、可能、一定等)。
1
结构中每出现一个碳碳三键:至少有4个原子共线或共面。
结构中每出现一个饱和碳原子,则整个分子中所有原子不可能全部共面。
结构中每出现一个苯环:至少有12个原子共面
结构中每出现一个碳碳双键:至少有6个原子共面。
2
3
4
(一)共线共面的一般规律
结构不同的基团连接后原子共面分析
1、直线与平面连接:
直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2==CH—C≡CH,其空间结构为
中间两个碳原子既在乙烯平面上,
又在乙炔直线上,所以直线在平面上,所有原子共平面。
结构不同的基团连接后原子共面分析
2、平面与平面连接:
如果两个平面结构通过单键(σ键)相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
如苯乙烯分子
共平面原子最多 个
16
结构不同的基团连接后原子共面分析
3、平面与立体连接:
如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。
如丙烯分子
共平面原子最多 个
7
4、直线、平面与立体连接:
如图所示的分子中共平面原子最多 个。
19
①先看碳原子1连2、1连3、1连4的面线问题,再看如何尽可能共面的问题;
②单链烷基上-CnH2n+1最多有n+1个原子在同一平面
注意:
结构不同的基团连接后原子共面分析
题组例练
4.已知某有机物分子结构为
有关该分子下列说法正确的是( )
A.分子中甲基(—CH3)上的氢原子有可能都与苯环共平面
B.—CHF2基团中两个F原子可能同时与双键共平面
C.最多有18个原子共平面
D.分子中至多有6个碳原子共线
D
课时作业
B
课时作业
B
6.下列有关有机化合物结构的说法不正确的是( )
A.以碳原子和化学键为立足点,若氢原子被其他原子所代替,其键角基本不变
B.若两个平面结构的基团之间以单键相连,这个单键可以旋转,则两个平面可能共面,但不是“一定”
C.若两个苯环共边,则两个苯环不一定共面
D.若甲基与一个平面结构相连,则甲基上的氢原子最多有一个与其共面;若一个碳原子以四个单键与其他原子直接相连,则这四个原子为四面体结构,不可能共面
课时作业
C
课时作业
D
课时作业
A
12.某有机化合物结构如图,分析其结构并完成下列问题。
课时作业
(1)写出其分子式: 。
(2)其中含有 个不饱和碳原子。
(3)分子中的饱和碳原子有 个;一定与苯环处于同一平面的碳原子有 个(不包括苯环碳原子)。
13.大气污染物氟利昂-12的化学式是CF2Cl2,下面关于氟利昂-12的说法正确的是( )
A.没有固定的熔、沸点
B.分子中的碳原子是饱和的
C.具有正四面体的空间结构
D.只有1种结构
课时作业
BD
15.科学家在-100 ℃的低温下合成了一种烃X,该分子的球棍模型如图所示。下列说法中不正确的是( )
课时作业
D
课时作业
B
课时作业
感谢观看
2.1.1有机物中碳原子成键特点及结构的表示方法
专
题
二
学习目标
01
了解有机物中碳原子的成键特点
02
分析有机物中的原子共面问题(难点)
03
学会有机物结构的表示方法(重点)
01
有机物中碳原子的成键特点
PART ONE
(一)碳原子的成键特点
碳原子最外层有4个电子,在化学反应中不易失去或得到电子
通常与H、O、S、N等非金属原子以共价键的成键方式形成共价化合物
(二)碳原子的成键数目
有机化合物中,每个碳原子都与其他原子形成4个单键
C
碳原子的类型
饱和碳原子:仅以 方式成键的碳原子。
不饱和碳原子:以 等方式成键的碳原子。
单键
双键或三键
(三)碳原子之间的成键方式
1.成键的类型:碳原子与碳原子之间可以形成单键、双键或三键。
2.碳骨架形式:碳原子之间可构成链状结构,也可构成环状结构。
(四)碳原子与其他原子的成键方式
1.碳原子与氢原子、卤素原子之间只能形成单键。
2.碳原子与氧原子、硫原子之间可以形成单键、双键。
3.碳原子与氮原子之间可以形成单键、双键、三键。
三聚氰胺
题组例练
(以下选择题有1个或2个选项符合题意)
1.下列说法正确的是( )
A.碳原子的最外层有4个电子,故只能形成4条单键
B.破坏碳碳双键和三键所需要的能量分别是破坏碳碳单键所需能量的2倍和3倍
C.CH3—CH3中只存在共价键
D.乙醇和乙酸中均含有羟基(—OH),但两者性质不同
CD
交流讨论
请同学们搭建甲烷、乙烯、乙炔、苯的分子结构模型,并填写下表(课本P23-24)
有机物 甲烷 乙烷 乙烯 乙炔 苯
分子式
结构式
空间结构
碳原子 杂化类型
共面(线) 原子个数
碳原子的成键方式与空间结构
1. 4个单键:碳原子与其他4个原子形成四面体结构,分子中所有原子可能同时不共面,如甲烷,乙烷。
2.双键:形成双键的碳原子跟与其直接相连的原子处于同一平面上,分子中至少有6个原子同时共面,如乙烯。
3.三键:形成三键的碳原子跟与其直接相连的原子处于同一直线上,分子中至少有4个原子同时共线,如乙炔。
4.苯环:有机物分子中含有一个苯环,至少有12个原子共面,如苯。
题组例练
3.在①丙烯、②氯乙烯、③苯、④甲苯四种有机化合物中,分子内所有原子均在同一平面的是( )
A.①② B.②③ C.③④ D.②④
B
02
有机物结构的表示方法
PART TWO
有机物结构的表示方法
1.结构式
2.结构简式
3.键线式
(一)结构式
1.概念:
优点:能完整地表示出有机物分子中每个原子的成键情况
缺点:书写比较麻烦
例1. 写出乙烷、乙醇、丙酸的结构式。
将分子中每对共用电子对都用一条短线表示的式子。(完整)
(二)结构简式
1.概念:
在结构式的基础上,省略碳氢键,也可省略碳碳单键,还可合并相同的部分。
注意事项:
1.表示单键的“—”:C-H一般省略;其它单键可以省略;上下连接“│”不能省略。
2.表示双键和三键的“=”和“≡”:C=C和C≡C不能省略;C=O可以省略。
3.准确表示分子中原子成键的情况(原子间连接情况)
(二)结构简式
结构简式:
CH3
CH2
CH2
CH2
CH3
CH3
CH2
CH2
CH2
CH3
CH3
(CH2)3
CH3
C
C
C
C
C
H
H
H
H
H
H
H
H
H
H
H
H
结构式:
(二)结构简式
C
C
C
H
H
H
H
C
H
H
H
H
CH2
CH
CH2
CH3
CH2
CH
CH2
CH3
结构简式:
结构式:
分子式: C4H8
(三)键线式
1.概念:
省略掉C、H原子,仅将(碳碳)键用短线表示
例3. 戊烷、1-丁烯、乙酸、葡萄糖
注意:每个拐点、交点和端点均表示一个碳原子。
CH3
CH2
CH2
CH2
CH3
分子式: C5H12
键线式:
结构简式:
(三)键线式
CH2
CH
CH2
CH3
分子式: C4H8
键线式:
结构简式:
(三)键线式
CH3
C
O
O
H
O
OH
分子式: C2H4O2
键线式:
结构简式:
键线式书写注意事项
①省去C、H元素符号,只要求表示出碳碳键(单键、双键、三键)及与碳原子相连的基团.
② —OH、—CHO、—COOH、—X等官能团不省
③端点、拐点、交叉点是C。
写出下列有机物对应的键线式或结构简式
学以致用
CH3 – CH – C = CH – CHO
OH
CH2CH3
Cl
O
O
=
有机物分子组成和结构的表示方法
分子式
最简式
电子式
结构式
结构简式
键线式
碳骨架式
球棍模型
空间填充模型
只表示分子的组成,不能反映物质的结构.
只表示分子的部分组成,不能反映物质的结构.
既能表示分子的组成,
又能反映物质的结构.
但书写麻烦!
既能表示分子的组成,
又能反映物质的结构.
只能表示碳原子的连接方式,不能表示分子组成!
既能表示分子的组成,
又能反映物质的结构.
一般只用于题目分析,正规的书写表达时不用!
常用
03
不饱和度的计算与应用
PART THREE
(一)不饱和度的计算
不饱和度又称缺氢指数,有机物分子与碳原子数目相等的链状烷烃相比较,每减少2个氢原子,则有机物不饱和度增加1,通常用Ω表示。
基团 少氢数 不饱和度
碳碳双键 少2H 1
碳环 少2H 1
碳氧双键 少2H 1
碳碳三键 少4H 2
苯环 少8H 4
(一)不饱和度的计算
(二)不饱和度的应用
1.已知分子式,推测结构
2.分子式为C6H9Br的有机化合物,其结构不可能是( )
A.含有一个双键的直链有机化合物
B.含有两个双键的直链有机化合物
C.含有一个双键的环状有机化合物
D.含有两个环的环状有机化合物
在判断有机物结构时,可以把卤素看作是氢原子被取代。
接着找有机物对应的烷烃,计算不饱和度,猜测可能结构。
A
(二)不饱和度的应用
2.通过不饱和度计算分子式
CHO
C6H12O
C8H8
C14H10
(二)不饱和度的应用
2.通过不饱和度计算分子式
C26H26
04
有机物原子共线共面问题
PART FOUR
先将被分析对象分解成下述几种常用的结构模板,最后综合分析不同结构间的交叉关系确定结果。
基本方法
结构 四面体形 平面形 直线形
模板 5个原子构成四面体,有3个原子共面 6个原子共面; 12个原子共面 a —C≡C—b:
4个原子共直线;苯环上处于对角位置的4个原子共直线
对照模板确定共线、共面原子数目
需要结合相关的几何知识进行分析:如不共线的任意三点可确定一个平面;一条直线与某平面有两个交点时,则这条直线上的所有点都在相应的平面内;同时要注意问题中的限定性词语(如最多、至少、可能、一定等)。
1
结构中每出现一个碳碳三键:至少有4个原子共线或共面。
结构中每出现一个饱和碳原子,则整个分子中所有原子不可能全部共面。
结构中每出现一个苯环:至少有12个原子共面
结构中每出现一个碳碳双键:至少有6个原子共面。
2
3
4
(一)共线共面的一般规律
结构不同的基团连接后原子共面分析
1、直线与平面连接:
直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2==CH—C≡CH,其空间结构为
中间两个碳原子既在乙烯平面上,
又在乙炔直线上,所以直线在平面上,所有原子共平面。
结构不同的基团连接后原子共面分析
2、平面与平面连接:
如果两个平面结构通过单键(σ键)相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
如苯乙烯分子
共平面原子最多 个
16
结构不同的基团连接后原子共面分析
3、平面与立体连接:
如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。
如丙烯分子
共平面原子最多 个
7
4、直线、平面与立体连接:
如图所示的分子中共平面原子最多 个。
19
①先看碳原子1连2、1连3、1连4的面线问题,再看如何尽可能共面的问题;
②单链烷基上-CnH2n+1最多有n+1个原子在同一平面
注意:
结构不同的基团连接后原子共面分析
题组例练
4.已知某有机物分子结构为
有关该分子下列说法正确的是( )
A.分子中甲基(—CH3)上的氢原子有可能都与苯环共平面
B.—CHF2基团中两个F原子可能同时与双键共平面
C.最多有18个原子共平面
D.分子中至多有6个碳原子共线
D
课时作业
B
课时作业
B
6.下列有关有机化合物结构的说法不正确的是( )
A.以碳原子和化学键为立足点,若氢原子被其他原子所代替,其键角基本不变
B.若两个平面结构的基团之间以单键相连,这个单键可以旋转,则两个平面可能共面,但不是“一定”
C.若两个苯环共边,则两个苯环不一定共面
D.若甲基与一个平面结构相连,则甲基上的氢原子最多有一个与其共面;若一个碳原子以四个单键与其他原子直接相连,则这四个原子为四面体结构,不可能共面
课时作业
C
课时作业
D
课时作业
A
12.某有机化合物结构如图,分析其结构并完成下列问题。
课时作业
(1)写出其分子式: 。
(2)其中含有 个不饱和碳原子。
(3)分子中的饱和碳原子有 个;一定与苯环处于同一平面的碳原子有 个(不包括苯环碳原子)。
13.大气污染物氟利昂-12的化学式是CF2Cl2,下面关于氟利昂-12的说法正确的是( )
A.没有固定的熔、沸点
B.分子中的碳原子是饱和的
C.具有正四面体的空间结构
D.只有1种结构
课时作业
BD
15.科学家在-100 ℃的低温下合成了一种烃X,该分子的球棍模型如图所示。下列说法中不正确的是( )
课时作业
D
课时作业
B
课时作业
感谢观看
