1.2.2有机化合物组成、结构、反应的研究(共54张ppt)-高中化学课件(苏教版2019选择性必修3)
文档属性
| 名称 | 1.2.2有机化合物组成、结构、反应的研究(共54张ppt)-高中化学课件(苏教版2019选择性必修3) |

|
|
| 格式 | pptx | ||
| 文件大小 | 8.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-20 10:18:39 | ||
图片预览









文档简介
1.2.2有机化合物组成、结构、反应的研究
专
题
一
学习目标
01
掌握有机化合物组成的研究方法(重点)
02
了解有机物结构的研究方法
03
了解有机化学反应的研究
04
学会如何测定有机物的结构(难点)
有机化合物的研究步骤
分离、提纯
确定实验式
确定分子式
确定分子结构
元素分析
波谱分析
反应原理
实验式/最简式:有机物所含各元素原子个数的最简整数比
01
有机物组成的研究
元素分析
PART ONE
一、元素分析的原理
1.定性分析:
指用化学方法鉴定有机物的元素组成。
例如 有机物完全燃烧,生成物使无水CuSO4变蓝、澄清石灰水变浑浊,则该有机物中一定含有碳、氢元素,可能含有氧元素。
2.定量分析:
指确定分子中各元素的质量分数,从而确定最简式
思考探究
若已知以下的一组物理量,能否推到出有机物的最简式
1.有机物的质量,燃烧产物的质量
2.各元素的质量
3.各元素的质量比
4.各元素的质量分数
定性分析的常用方法
如:完全燃烧后,C生成 、H生成 、
S生成 、N生成 。
CO2
H2O
SO2
N2
(不能确定O元素是否存在)
1.燃烧法
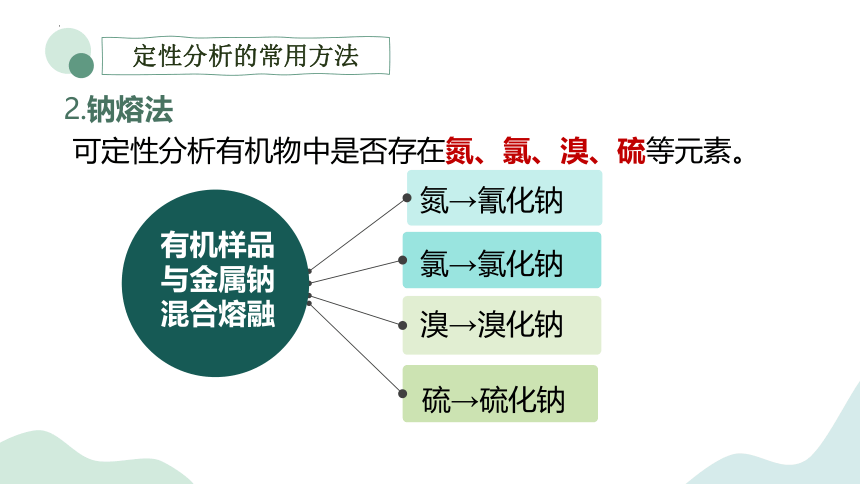
定性分析的常用方法
2.钠熔法
可定性分析有机物中是否存在氮、氯、溴、硫等元素。
溴→溴化钠
硫→硫化钠
氯→氯化钠
氮→氰化钠
有机样品与金属钠混合熔融
定性分析的常用方法
3.铜丝燃烧法
将一根纯铜丝加热至红热,蘸上试样,放在火焰上灼烧,若存在卤素,火焰则为绿色。
可定性分析有机物中是否存在卤素。
定量分析的常用方法
1.李比希元素分析法(测定C、H)
2.现代元素分析仪(精准度高,分析快)
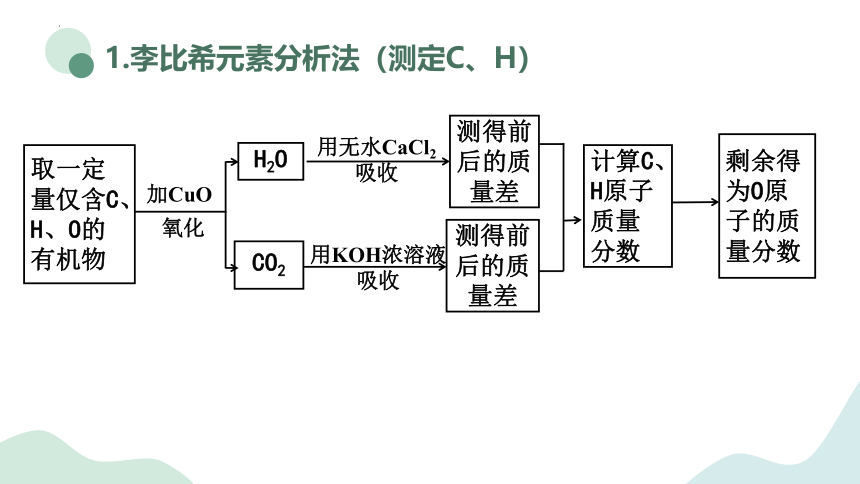
1.李比希元素分析法(测定C、H)
取一定量仅含C、H、O的有机物
加CuO
氧化
CO2
H2O
测得前后的质量差
用无水CaCl2
吸收
用KOH浓溶液吸收
计算C、H原子质量分数
剩余得为O原子的质量分数
测得前后的质量差
具体有机物各元素质量分数的方法
C、H元素的测定
N元素的测定
卤素元素的测定
O元素的测定
氧化铜高温氧化
测量产生CO2、H2O的质量
CO2气流中
加热氧化铜
测量产生N2的体积
加NaOH溶液
加AgNO3溶液
加稀硝酸酸化
测量产生卤化银的质量
用1-其他元素的质量分数
为0则不含氧元素,不为0则为氧的质量分数
例1.燃烧黄酒中有机化合物A 物质2.30g,生成2.24L(标况)CO2和2.7g H2O。求该有机物的实验式。
则实验式为:C2H6O
若要确定它的分子式,还需要什么条件?
相对分子质量
N(C):N(H):N(O)=0.1:0.3:0.05=2:6:1
n(CO2)= 2.24L÷22.4L·mol-1 = 0.1mol
n(H2O)= 2.7g÷18g·mol-1=0.15mol
n(C)= 0.1mol n(H)=0.3mol
n(O)=(2.3g-0.1×12-0.3×1)÷16= 0.05mol
二、确定有机物的分子式
元素定量分析
实验式
各组成原子的最简整数比
分子式
其中最精确、快捷的方法
相对分子质量
质谱法
质谱仪
确定有机物相对分子质量的常用方法如下:
①标准密度法:根据标准状况下气体的密度,求算该气体的相对分子质量:Mr=22.4×ρ。
②相对密度法:根据气体A相对于气体B的相对密度为D,求算该气体的相对分子质量:MA=D×MB。
③混合物的平均相对分子质量:M =????总????总。
④利用各类有机物的分子通式及相应的化学反应方程式
?
方法引导
28
(1)标准状况下0.56g某气态烃的体积为448ml;
(2)某有机物在相同状况下对空气的相对密度为4;
(3)某有机物的蒸气密度是相同状况下氢气密度的14倍;
29×4=116
14×2=28
学以致用
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
①直接法:
有机物的密度/相对密度→摩尔质量→1mol有机物中各原子的物质的量→分子式
《导与练》第16页 2.有机物分子式的确定
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
②最简式法:
各元素的质量分数→最简式 分子式
相对分子质量
1.确定最简式——百分量法
例:烃类最简式的求法
n(C):n(H) = ????(????)????(????): ????(????)????(????)?= a:b
则最简式为CaHb
?
2.分子式为最简式的n倍
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
②实验式法:
各元素的质量分数→实验式 分子式
相对分子质量
如果没有相对密度,能否依据最简式推出分子式呢?
可以依据烃类C、H的关系确定:
1.烃CnHm及烃的含氧衍生物CnHmOz中,H原子的数目小于或等于2n+2
2. 含氮的有机物,N原子数和H原子数同奇数同偶
3.不含氮的有机物,H原子数一定为偶数(卤素当氢处理)
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
③商余法:
用烃的相对分子质量除以14就可以确定分子中所含碳原子数,即n值
????????(C????H????)14=商(碳原子数)
余2???????????????????? 为烷烃除尽 为烯烃或环烷烃差2 为炔烃或二烯烃差6 为苯或苯的同系物
?
【题组例练】2.(2)燃烧某有机物A 1.50 g,生成1.12 L(标准状况)CO2和0.05 mol H2O。该有机物的蒸气对空气的相对密度是1.04,求该化合物的分子式。
【题组例练】2.(3)某有机化合物仅由碳、氢、氧三种元素组成,经测定其相对分子质量为90。取该有机物样品1.8 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08 g和2.64 g。,求该化合物的分子式。
④化学方程式法:
推出有机物的燃烧通式,将数据带入换算比例即可。
02
有机物结构的研究
波谱分析
PART TWO
测定有机化合物结构的基本流程
测定原理
有机物的结构特点
在有机化合物分子中,原子主要通过共价键结合在一起。原子之间结合方式或连接顺序的不同导致了所形成物质在性质上的差异。
基团理论是1838年德国化学家李比希提出的,常见的基团有羟基—OH、醛基—CHO、羧基—COOH、氨基—NH2、烃基—R等,不同的基团有不同的结构和性质特点。
尤斯图斯 · 冯 · 李比希
(J. von Liebig, 1803—1873)
有机化学之父
世界上最早的 60 位诺贝尔化学奖获得者其中有 42 位是他的学生,或者是他学生的学生。他一生从没有获得过诺贝尔化学奖,只是因为在他去世三十年后诺贝尔奖才刚刚创立。他是真正的有机化学之父,有史以来最伟大的化学教师,堪称有机化学的天才。
科学史话
1.核磁共振氢谱(H—NMR):
①用途:
②原理:
处在不同化学环境中的氢原子在谱图上出现的位置不同,而且吸收峰的面积与氢原子数成正比。
测定有机物分子中氢原子的种类和数目比
注意:不能确定H原子的总数
氢原子类型=吸收峰数目
不同氢原子的个数之比=峰面积之比
③等量关系:
A核磁共振氢谱
B核磁共振氢谱
分子式为C2H6O的有机物的核磁共振氢谱如图
CH3CH2OH
乙醇
CH3—O—CH3
二甲醚
核磁共振氢谱可快速确定有机物等效氢个数,是判断同分异构体、
确定有机物结构的一个重要依据!
等效氢法(对称法)
分子中等效氢原子有如下情况:
①分子中同一个碳原子上连接的氢原子等效。
②同一个碳原子上所连接的甲基上的氢原子等效。
③分子中处于对称位置上的氢原子是等效的。
等效氢的找法:
链画直线,环画平面,侧链看成球
下列有机物中有几种H原子?
CH3-CH-CH3
CH3
CH3-CH2-OH
问题探究
等效氢的找法:
链画直线,环画平面,侧链看成球
下列有机物中有几种H原子以及个数之比?
CH3-CH2-CH-CH3
C2H5
问题探究
CH3-C-CH2-CH-CH3
C2H5
CH3
CH3
H原子个数比:
主链看对称,支链看同碳;
主链不对称,从头数到尾
① CH3CH3
② CH3OH
判断下列核磁共振图谱对应哪种有机物?
A
B
学以致用
2.红外光谱:
①用途:
②原理:
利用有机物分子中不同基团的特征吸收频率不同,测试并记录有机物对一定波长范围的红外光谱吸收情况。
可获得分子中所含有的化学键或官能团的信息。
乙醇的红外吸收光谱图(可区分二甲醚)
3.质谱法:
①用途:
②原理:
用高能电子束轰击有机物分子,使之分离成带电的“碎片",这些不同离子具有不同的质量,质量不同的离子在磁场作用下达到检测器的时间有差异,其结果被记录为质谱图。
测定相对分子质量
③数据分析:
质核比的最大值=分子的相对分子质量
找出下列有机物的相对分子质量
学以致用
苯的质谱图
03
有机反应机理的研究
PART THREE
设计并合成新的有机化合物是有机化学的重要研究内容。通过有机化学反应,科学家们已经成功合成大量具有特殊功能的有机化合物。
在已颁发的诺贝尔化学奖中,有几十个获奖项目的研究内容涉及有机化合物的合成和有机化学反应的研究。
一、有机反应原理的基本概念
1.概念:
2.作用:
反应机理又称反应历程,指反应物转变为生成物所经历的过程。
有机化学的反应机理揭示了反应中化学键因基团的相互作用而发生断裂形成新化学键。
项目
基团
根
概念
有机化合物分子中失去一个原子或原子团剩余的部分
带电荷的原子团,是电解质电离的产物
电性
电中性
带电荷
稳定性
不稳定;不能独立存在
稳定;可独立存在于溶液中或熔融状态下
实例及其
电子式
—OH ·O······H
OH-
[··O······H]-
联系
“基团”与“根”两者可以相互转化,OH-失去1个电子,可转化为 —OH,而—OH获得1个电子,可转化为OH-
项目
基团
根
概念
有机化合物分子中失去一个原子或原子团剩余的部分
带电荷的原子团,是电解质电离的产物
电性
电中性
带电荷
稳定性
不稳定;不能独立存在
稳定;可独立存在于溶液中或熔融状态下
实例及其
电子式
联系
“基团”与“根”两者可以相互转化,OH-失去1个电子,可转化为 —OH,而—OH获得1个电子,可转化为OH-
甲烷与氯气取代反应的反应机理
1.自由基型链反应
二、有机反应原理的表示方法
同位素示踪法
三、有机反应原理的研究方法
18
O
CH3—C—OH +H—O—C2H5
18
O
CH3—C—O—C2H5+H2O
浓H2SO4
酸脱羟基醇脱氢
四、仪器在研究反应机理中的应用
乙烯和HBr加成反应的研究
利用质谱仪可以检测出反应过程中产生的中间体——乙烯碳正离子 ,推断该反应为离子型反应。
HBr→H++Br-
CH2=CH2+H+→CH3CH2
+
CH3CH2+Br-→CH3CH2Br
+
题组例练
B
作业布置
1.《导与练》P14 学业质量评价
2.《课时作业》P137-140
基础题组:2、5、6、7、9
能力题组:13
04
习题探究
PART FOUR
实验步骤
解释实验结论
测得A的蒸气密度是同状况下甲烷的4.375倍
(1)A的相对分子质量为?
将5.6 g A在足量氧气中燃烧,并将产物依次通过浓硫酸和碱石灰,分别增重7.2 g和17.6 g
(2)A的实验式为 ;?
A的分子式为 ?
A的核磁共振氢谱如下:
(3)综上所述,A的结构简式为
。
(4)结合上述分析,研究有机物的结构通常可采用哪些物理方法?
? 。?
(5)结合对第二单元的学习,归纳概括研究有机化合物的基本步骤(或流程)。
分离提纯→确定实验式→确定分子式→确定结构式
(4)红外光谱法、核磁共振波谱法
2.某有机化合物只含碳、氢、氧三种元素中的两种或三种,相对分子质量为74,完全燃烧时产生等物质的量的CO2和H2O。它的分子式可能为( )
A.C4H10O B.C4H4O2
C.C3H6O2 D.C4H8O2
C
课时作业
B
课时作业
D
课时作业
6.某有机化合物的1H核磁共振谱图中有6个特征峰,则该有机化合物可能是( )
7.某气态化合物X含C、H、O三种元素,现已知下列条件:①X中C的质量分数;②X中H的质量分数;③X在标准状况下的体积;④X对氢气的相对密度;⑤X的质量。欲确定化合物X的分子式,所需的最少条件是( )
A.①②④ B.②③④
C.①③⑤ D.①②
A
课时作业
9.按要求回答下列问题:
(1)有机物X的分子式为C4H8O2,其红外光谱如图所示:
则该有机物可能的结构为 (填字母)。?
A.CH3COOCH2CH3
B.CH3CH2COOCH3
C.HCOOCH2CH2CH3
D.(CH3)2CHCOOH
AB
9.按要求回答下列问题:
课时作业
13.下列装置中有机物样品在电炉中充分燃烧,通过测定生成的CO2和H2O的质量,来确定有机物的分子式。
感谢观看
专
题
一
学习目标
01
掌握有机化合物组成的研究方法(重点)
02
了解有机物结构的研究方法
03
了解有机化学反应的研究
04
学会如何测定有机物的结构(难点)
有机化合物的研究步骤
分离、提纯
确定实验式
确定分子式
确定分子结构
元素分析
波谱分析
反应原理
实验式/最简式:有机物所含各元素原子个数的最简整数比
01
有机物组成的研究
元素分析
PART ONE
一、元素分析的原理
1.定性分析:
指用化学方法鉴定有机物的元素组成。
例如 有机物完全燃烧,生成物使无水CuSO4变蓝、澄清石灰水变浑浊,则该有机物中一定含有碳、氢元素,可能含有氧元素。
2.定量分析:
指确定分子中各元素的质量分数,从而确定最简式
思考探究
若已知以下的一组物理量,能否推到出有机物的最简式
1.有机物的质量,燃烧产物的质量
2.各元素的质量
3.各元素的质量比
4.各元素的质量分数
定性分析的常用方法
如:完全燃烧后,C生成 、H生成 、
S生成 、N生成 。
CO2
H2O
SO2
N2
(不能确定O元素是否存在)
1.燃烧法
定性分析的常用方法
2.钠熔法
可定性分析有机物中是否存在氮、氯、溴、硫等元素。
溴→溴化钠
硫→硫化钠
氯→氯化钠
氮→氰化钠
有机样品与金属钠混合熔融
定性分析的常用方法
3.铜丝燃烧法
将一根纯铜丝加热至红热,蘸上试样,放在火焰上灼烧,若存在卤素,火焰则为绿色。
可定性分析有机物中是否存在卤素。
定量分析的常用方法
1.李比希元素分析法(测定C、H)
2.现代元素分析仪(精准度高,分析快)
1.李比希元素分析法(测定C、H)
取一定量仅含C、H、O的有机物
加CuO
氧化
CO2
H2O
测得前后的质量差
用无水CaCl2
吸收
用KOH浓溶液吸收
计算C、H原子质量分数
剩余得为O原子的质量分数
测得前后的质量差
具体有机物各元素质量分数的方法
C、H元素的测定
N元素的测定
卤素元素的测定
O元素的测定
氧化铜高温氧化
测量产生CO2、H2O的质量
CO2气流中
加热氧化铜
测量产生N2的体积
加NaOH溶液
加AgNO3溶液
加稀硝酸酸化
测量产生卤化银的质量
用1-其他元素的质量分数
为0则不含氧元素,不为0则为氧的质量分数
例1.燃烧黄酒中有机化合物A 物质2.30g,生成2.24L(标况)CO2和2.7g H2O。求该有机物的实验式。
则实验式为:C2H6O
若要确定它的分子式,还需要什么条件?
相对分子质量
N(C):N(H):N(O)=0.1:0.3:0.05=2:6:1
n(CO2)= 2.24L÷22.4L·mol-1 = 0.1mol
n(H2O)= 2.7g÷18g·mol-1=0.15mol
n(C)= 0.1mol n(H)=0.3mol
n(O)=(2.3g-0.1×12-0.3×1)÷16= 0.05mol
二、确定有机物的分子式
元素定量分析
实验式
各组成原子的最简整数比
分子式
其中最精确、快捷的方法
相对分子质量
质谱法
质谱仪
确定有机物相对分子质量的常用方法如下:
①标准密度法:根据标准状况下气体的密度,求算该气体的相对分子质量:Mr=22.4×ρ。
②相对密度法:根据气体A相对于气体B的相对密度为D,求算该气体的相对分子质量:MA=D×MB。
③混合物的平均相对分子质量:M =????总????总。
④利用各类有机物的分子通式及相应的化学反应方程式
?
方法引导
28
(1)标准状况下0.56g某气态烃的体积为448ml;
(2)某有机物在相同状况下对空气的相对密度为4;
(3)某有机物的蒸气密度是相同状况下氢气密度的14倍;
29×4=116
14×2=28
学以致用
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
①直接法:
有机物的密度/相对密度→摩尔质量→1mol有机物中各原子的物质的量→分子式
《导与练》第16页 2.有机物分子式的确定
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
②最简式法:
各元素的质量分数→最简式 分子式
相对分子质量
1.确定最简式——百分量法
例:烃类最简式的求法
n(C):n(H) = ????(????)????(????): ????(????)????(????)?= a:b
则最简式为CaHb
?
2.分子式为最简式的n倍
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
②实验式法:
各元素的质量分数→实验式 分子式
相对分子质量
如果没有相对密度,能否依据最简式推出分子式呢?
可以依据烃类C、H的关系确定:
1.烃CnHm及烃的含氧衍生物CnHmOz中,H原子的数目小于或等于2n+2
2. 含氮的有机物,N原子数和H原子数同奇数同偶
3.不含氮的有机物,H原子数一定为偶数(卤素当氢处理)
例2.实验测的某碳氢化合物A中含碳80%,含氢20%,又测得该化合物对氢气的相对密度为15,求该化合物的分子式。
③商余法:
用烃的相对分子质量除以14就可以确定分子中所含碳原子数,即n值
????????(C????H????)14=商(碳原子数)
余2???????????????????? 为烷烃除尽 为烯烃或环烷烃差2 为炔烃或二烯烃差6 为苯或苯的同系物
?
【题组例练】2.(2)燃烧某有机物A 1.50 g,生成1.12 L(标准状况)CO2和0.05 mol H2O。该有机物的蒸气对空气的相对密度是1.04,求该化合物的分子式。
【题组例练】2.(3)某有机化合物仅由碳、氢、氧三种元素组成,经测定其相对分子质量为90。取该有机物样品1.8 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08 g和2.64 g。,求该化合物的分子式。
④化学方程式法:
推出有机物的燃烧通式,将数据带入换算比例即可。
02
有机物结构的研究
波谱分析
PART TWO
测定有机化合物结构的基本流程
测定原理
有机物的结构特点
在有机化合物分子中,原子主要通过共价键结合在一起。原子之间结合方式或连接顺序的不同导致了所形成物质在性质上的差异。
基团理论是1838年德国化学家李比希提出的,常见的基团有羟基—OH、醛基—CHO、羧基—COOH、氨基—NH2、烃基—R等,不同的基团有不同的结构和性质特点。
尤斯图斯 · 冯 · 李比希
(J. von Liebig, 1803—1873)
有机化学之父
世界上最早的 60 位诺贝尔化学奖获得者其中有 42 位是他的学生,或者是他学生的学生。他一生从没有获得过诺贝尔化学奖,只是因为在他去世三十年后诺贝尔奖才刚刚创立。他是真正的有机化学之父,有史以来最伟大的化学教师,堪称有机化学的天才。
科学史话
1.核磁共振氢谱(H—NMR):
①用途:
②原理:
处在不同化学环境中的氢原子在谱图上出现的位置不同,而且吸收峰的面积与氢原子数成正比。
测定有机物分子中氢原子的种类和数目比
注意:不能确定H原子的总数
氢原子类型=吸收峰数目
不同氢原子的个数之比=峰面积之比
③等量关系:
A核磁共振氢谱
B核磁共振氢谱
分子式为C2H6O的有机物的核磁共振氢谱如图
CH3CH2OH
乙醇
CH3—O—CH3
二甲醚
核磁共振氢谱可快速确定有机物等效氢个数,是判断同分异构体、
确定有机物结构的一个重要依据!
等效氢法(对称法)
分子中等效氢原子有如下情况:
①分子中同一个碳原子上连接的氢原子等效。
②同一个碳原子上所连接的甲基上的氢原子等效。
③分子中处于对称位置上的氢原子是等效的。
等效氢的找法:
链画直线,环画平面,侧链看成球
下列有机物中有几种H原子?
CH3-CH-CH3
CH3
CH3-CH2-OH
问题探究
等效氢的找法:
链画直线,环画平面,侧链看成球
下列有机物中有几种H原子以及个数之比?
CH3-CH2-CH-CH3
C2H5
问题探究
CH3-C-CH2-CH-CH3
C2H5
CH3
CH3
H原子个数比:
主链看对称,支链看同碳;
主链不对称,从头数到尾
① CH3CH3
② CH3OH
判断下列核磁共振图谱对应哪种有机物?
A
B
学以致用
2.红外光谱:
①用途:
②原理:
利用有机物分子中不同基团的特征吸收频率不同,测试并记录有机物对一定波长范围的红外光谱吸收情况。
可获得分子中所含有的化学键或官能团的信息。
乙醇的红外吸收光谱图(可区分二甲醚)
3.质谱法:
①用途:
②原理:
用高能电子束轰击有机物分子,使之分离成带电的“碎片",这些不同离子具有不同的质量,质量不同的离子在磁场作用下达到检测器的时间有差异,其结果被记录为质谱图。
测定相对分子质量
③数据分析:
质核比的最大值=分子的相对分子质量
找出下列有机物的相对分子质量
学以致用
苯的质谱图
03
有机反应机理的研究
PART THREE
设计并合成新的有机化合物是有机化学的重要研究内容。通过有机化学反应,科学家们已经成功合成大量具有特殊功能的有机化合物。
在已颁发的诺贝尔化学奖中,有几十个获奖项目的研究内容涉及有机化合物的合成和有机化学反应的研究。
一、有机反应原理的基本概念
1.概念:
2.作用:
反应机理又称反应历程,指反应物转变为生成物所经历的过程。
有机化学的反应机理揭示了反应中化学键因基团的相互作用而发生断裂形成新化学键。
项目
基团
根
概念
有机化合物分子中失去一个原子或原子团剩余的部分
带电荷的原子团,是电解质电离的产物
电性
电中性
带电荷
稳定性
不稳定;不能独立存在
稳定;可独立存在于溶液中或熔融状态下
实例及其
电子式
—OH ·O······H
OH-
[··O······H]-
联系
“基团”与“根”两者可以相互转化,OH-失去1个电子,可转化为 —OH,而—OH获得1个电子,可转化为OH-
项目
基团
根
概念
有机化合物分子中失去一个原子或原子团剩余的部分
带电荷的原子团,是电解质电离的产物
电性
电中性
带电荷
稳定性
不稳定;不能独立存在
稳定;可独立存在于溶液中或熔融状态下
实例及其
电子式
联系
“基团”与“根”两者可以相互转化,OH-失去1个电子,可转化为 —OH,而—OH获得1个电子,可转化为OH-
甲烷与氯气取代反应的反应机理
1.自由基型链反应
二、有机反应原理的表示方法
同位素示踪法
三、有机反应原理的研究方法
18
O
CH3—C—OH +H—O—C2H5
18
O
CH3—C—O—C2H5+H2O
浓H2SO4
酸脱羟基醇脱氢
四、仪器在研究反应机理中的应用
乙烯和HBr加成反应的研究
利用质谱仪可以检测出反应过程中产生的中间体——乙烯碳正离子 ,推断该反应为离子型反应。
HBr→H++Br-
CH2=CH2+H+→CH3CH2
+
CH3CH2+Br-→CH3CH2Br
+
题组例练
B
作业布置
1.《导与练》P14 学业质量评价
2.《课时作业》P137-140
基础题组:2、5、6、7、9
能力题组:13
04
习题探究
PART FOUR
实验步骤
解释实验结论
测得A的蒸气密度是同状况下甲烷的4.375倍
(1)A的相对分子质量为?
将5.6 g A在足量氧气中燃烧,并将产物依次通过浓硫酸和碱石灰,分别增重7.2 g和17.6 g
(2)A的实验式为 ;?
A的分子式为 ?
A的核磁共振氢谱如下:
(3)综上所述,A的结构简式为
。
(4)结合上述分析,研究有机物的结构通常可采用哪些物理方法?
? 。?
(5)结合对第二单元的学习,归纳概括研究有机化合物的基本步骤(或流程)。
分离提纯→确定实验式→确定分子式→确定结构式
(4)红外光谱法、核磁共振波谱法
2.某有机化合物只含碳、氢、氧三种元素中的两种或三种,相对分子质量为74,完全燃烧时产生等物质的量的CO2和H2O。它的分子式可能为( )
A.C4H10O B.C4H4O2
C.C3H6O2 D.C4H8O2
C
课时作业
B
课时作业
D
课时作业
6.某有机化合物的1H核磁共振谱图中有6个特征峰,则该有机化合物可能是( )
7.某气态化合物X含C、H、O三种元素,现已知下列条件:①X中C的质量分数;②X中H的质量分数;③X在标准状况下的体积;④X对氢气的相对密度;⑤X的质量。欲确定化合物X的分子式,所需的最少条件是( )
A.①②④ B.②③④
C.①③⑤ D.①②
A
课时作业
9.按要求回答下列问题:
(1)有机物X的分子式为C4H8O2,其红外光谱如图所示:
则该有机物可能的结构为 (填字母)。?
A.CH3COOCH2CH3
B.CH3CH2COOCH3
C.HCOOCH2CH2CH3
D.(CH3)2CHCOOH
AB
9.按要求回答下列问题:
课时作业
13.下列装置中有机物样品在电炉中充分燃烧,通过测定生成的CO2和H2O的质量,来确定有机物的分子式。
感谢观看
