辽宁省沈阳市郊联体2022-2023学年高一下学期5月期中考试化学试题(含答案)
文档属性
| 名称 | 辽宁省沈阳市郊联体2022-2023学年高一下学期5月期中考试化学试题(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-22 10:10:28 | ||
图片预览



文档简介
沈阳市郊联体2022-2023学年高一下学期5月期中考试
化学
考试时间75分钟 试卷总分:100分
可能用到的相对原子质量 H 1 N 14 O 16 Fe 56 S 32
第Ⅰ卷 选择题(45分)
一、单选题(每小题只有一个正确选项,共15小题,每题3分,共45分)
1.下列发电站在发电过程中实现化学能转化为电能的是( )
A.天津双港垃圾焚烧发电厂 B.甘肃酒泉风电基地
C.大亚湾核电站 D.三峡水利发电站
2.下列说法正确的是( )
A.已知 ,在中和热的测定时实际加入的酸碱的量的多少会影响该反应的
B.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量.则
C.500℃、30MPa下,将0.5mol和1.5mol置于密闭的容器中充分反应生成,放热19.3kJ,其热化学方程式为:
D.相同条件下,在两个相同的恒容密闭容器中,2mol和6mol反应放出的热量是1mol和3mol反应放出的热量的2倍
3.下列说法正确的是( )
A.反应在低温下能自发进行,说明该反应的
B.的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为,则氢气燃烧的热化学方程式可表示为:
C.能自发进行的反应一定能迅速发生
D.增大反应物浓度,可增大活化分子百分数,从而增加有效碰撞的次数
4.一种太阳能电池的工作原理如图所示,电解质为铁氰化钾和亚铁氰化钾的混合溶液.下列说法不正确的是( )
A.移向催化剂b
B.催化剂a表面发生的化学反应:
C.在催化剂b表面被氧化
D.电解质溶液中的和浓度基本保持不变
5.HCl气体被氧气氧化的能量关系如图,下列叙述正确的是( )
A.该反应、
B.该反应的浓度平衡常数
C.用E表示键能,则该反应
D.反应
6.某化学兴趣小组用铝片与稀硫酸反应制取氢气,以下能够加快该反应速率的是( )
①用98%的浓硫酸代替稀硫酸 ②加热 ③改用铝粉 ④增大稀硫酸的体积 ⑤加水 ⑥加入少量硫酸铜
A.②③⑥ B.①②③ C.②③④⑥ D.全部
7.下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好
B.硫酸工业中,使用催化剂是为了提高转化为的转化率
C.合成氨工业中,将及时液化分离有利于氨的生产
D.硫酸工业中,的催化氧化不采用高压,是因为压强对转化率无影响
8.将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:,经5min后,测得D的浓度为,C的平均反应速率是,且此时A、B的物质的量之比为2∶3.下列说法不正确的是( )
A.x的值是3
B.5min内,B的平均反应速率为
C.开始时A的物质的量为2.8mol
D.5min时,容器中气体总的物质的量为3.6mol
9.下列说法正确的是( )
A.同温同压下,在光照和点燃的条件下不同
B.298K下,反应不能自发进行,则该反应的
C.当温度、压强一定时,在原料气(和的比例不变)中添加少量惰性气体,有利于提高反应气的平衡转化率
D.合成氨()在高温条件下进行符合勒夏特列原理
10.在密闭容器中的一定量混合气体发生反应:;平衡时测得A的浓度为0.45mol/L,保持温度不变,将容器的容积压缩到原来的一半,再达平衡时,测得A的浓度为0.9mol/L.下列有关判断正确的是( )
A.各物质的计量数一定满足:
B.若B为气体,压缩后B的体积分数增大,转化率降低
C.无论B为固体或气体,压缩后B的质量都不会改变
D.压缩时,平衡向逆反应方向移动,且正、逆反应速率都增大
11.多相催化反应是在催化剂表面通过吸附、解吸过程进行的.我国学者发现T℃时(各物质均为气态),甲醇()与水在铜基催化剂上的反应机理和能量图如图:
下列说法正确的是( )
A.反应Ⅱ的热化学方程式为:
B.在反应中生成又消耗,可认为是催化剂
C.1mol和1mol的总能量小于1mol和3mol的总能量
D.选择优良的催化剂可以降低反应Ⅰ和Ⅱ的活化能,减少过程中的能耗和反应的焓变
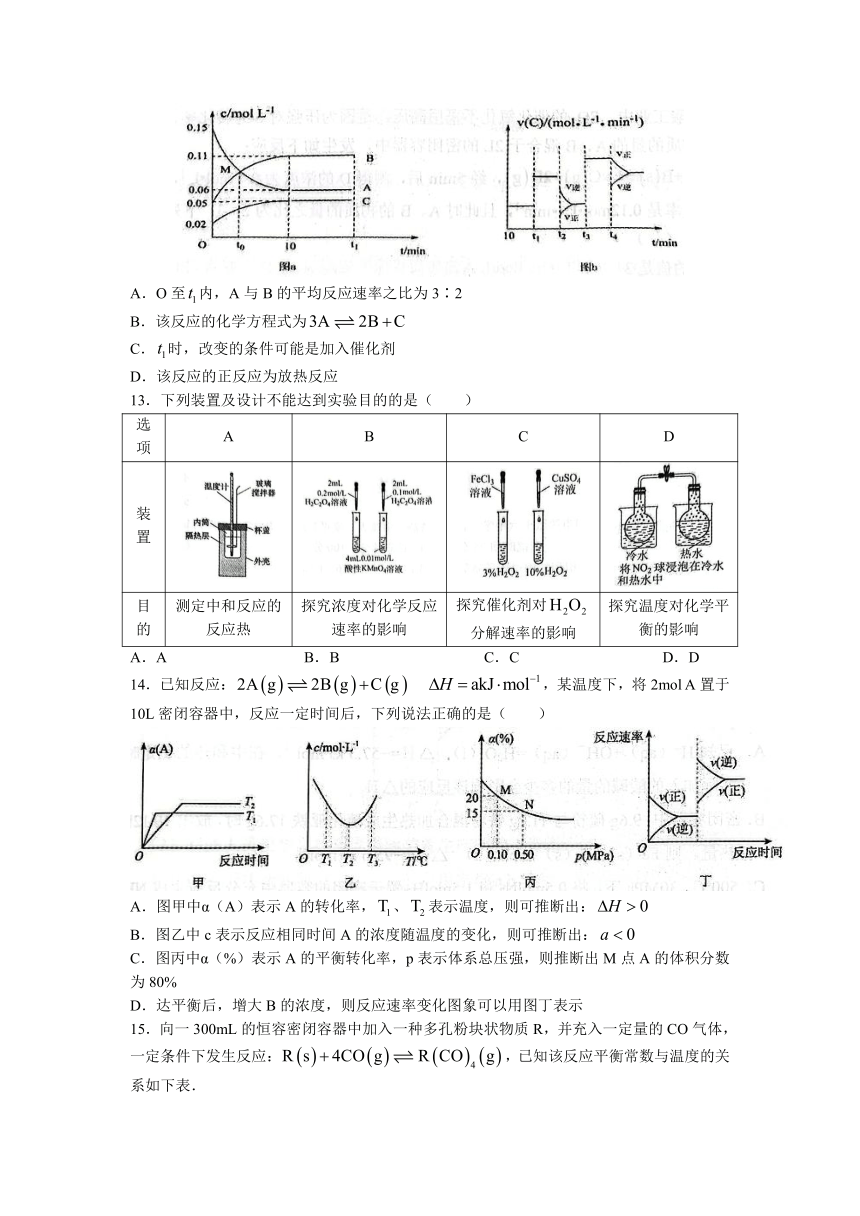
12.向一恒容密闭容器中充入A、B、C三种气体,在一定条件下发生反应,各物质的物质的量浓度随时间的变化如图a所示.若从时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b.下列说法不正确的是( )
A.O至内,A与B的平均反应速率之比为3∶2
B.该反应的化学方程式为
C.时,改变的条件可能是加入催化剂
D.该反应的正反应为放热反应
13.下列装置及设计不能达到实验目的的是( )
选项 A B C D
装置
目的 测定中和反应的反应热 探究浓度对化学反应速率的影响 探究催化剂对分解速率的影响 探究温度对化学平衡的影响
A.A B.B C.C D.D
14.已知反应: ,某温度下,将2mol A置于10L密闭容器中,反应一定时间后,下列说法正确的是( )
A.图甲中α(A)表示A的转化率,、表示温度,则可推断出:
B.图乙中c表示反应相同时间A的浓度随温度的变化,则可推断出:
C.图丙中α(%)表示A的平衡转化率,p表示体系总压强,则推断出M点A的体积分数为80%
D.达平衡后,增大B的浓度,则反应速率变化图象可以用图丁表示
15.向一300mL的恒容密闭容器中加入一种多孔粉块状物质R,并充入一定量的CO气体,一定条件下发生反应:,已知该反应平衡常数与温度的关系如下表.
温度/℃ 25 80 230
平衡常数 2
下列说法不正确的是( )
A.物质R做成多孔状可增大接触面积,加快化学反应速率
B.25℃时反应的平衡常数为
C.80℃时反应达到平衡,测得,则的平衡浓度为
D.80℃时,测得某时刻、CO的浓度均为,则此时
第Ⅱ卷非选择题(共55分)
16.(16分)如图表示298.15K时,、与的平均能量与合成氨反应的活化能的曲线图,据图回答下列问题:
(1)若反应中生成2mol氨,则反应______(填“吸热”或“放热”)______kJ.
(2)图中曲线______(填“a”或“b”)表示加入铁触媒(催化剂)的能量变化曲线,铁触媒能加快反应速率的原理是______.
(3)合成氨反应中平衡混合物中氨气的体积分数与压强、温度的关系如右图所示.若曲线a对应的温度为500℃,则曲线b对应的温度可能是______(填字母).
A.600℃ B.550℃ C.500℃ D.450℃
(4)合成氨所需的氢气可由甲烷与水反应制备.发生反应为.一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
t/min
0 0.2 0.3 0 0
2 0.3
3 0.3
4 0.09 0.19 x 0.33
①表中x=______;前2min内的平均反应速率为______.
②反应在3~4min之间,氢气的物质的量增多的原因可能是______(填字母).
A.充入水蒸气 B.缩小体积增大压强 C.升高温度 D.充入氢气
17.(9分)用活性炭还原法处理氮氧化物,有关反应为.某研究小组向某密闭的真空容器(假设容器体积不变)中加入NO和足量的活性炭,恒温()条件下反应.
(1)写出该反应的平衡常数的表达式______.
(2)若升高温度,发现NO体积分数减小,则该反应的______0.
(3)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率______(填“增大”“不变”或“减小”).
(4)某温度下,在一密闭容器中充入一定量发生反应 ,
下列对于该反应的说法正确的是______(填标号).
A.当混合气体颜色保持不变时,反应达到化学平衡状态
B.当的比值保持不变时,反应达到化学平衡状态
C.反应达到化学平衡状态时,每消耗0.1mol NO就会消耗0.05mol
D.反应达到平衡状态后,若降低温度,则混合气体的颜色变浅
E.反应达到平衡状态后,若减小压强,则混合气体的平均相对分子质量减小
18.(16分)肼()是一种应用广泛的化工原料.工业上先合成氨气: ,再进一步制备肼.完成下列填空:
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是______(填“A”或“B”或“C”)
(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
反应速率 平衡常数K
变化情况 ______ ______
(3)通常把拆开1mol某化学键所吸收的能量看成该化学键的键能.已知部分化学键的键能如下:
化学键 N—H N—N O==O N≡N O—H
键能(kJ/mol) 386 167 498 946 460
发射神舟飞船的长征火箭用了肼(,气态)为燃料,若它在氧气(气态)中燃烧,生成(气态)和(气态).该反应的热化学方程式为:______.
(4)氨主要用于生产化肥和硝酸.“十三五”期间,预计我国合成氨产量将保持稳中略增.下图是不同温度和不同压强下,反应达到平衡后,混合物中含量(体积%)的变化情况,已知初始时.判断、压强的大小关系,______(选填“>”、“<”或“=”).
(5)通过传感器可监测的含量,其工作原理如图.
①Pt电极是电源的______(填“正”或“负”)极上发生的是______反应(填“氧化”或“还原”).
②写出NiO电极上的电极反应式:______.
19.(14分)已知炼铁过程中发生
回答下列问题:
(1)时,向容积为2L的恒容密闭容器中加入3mol 和3mol CO发生反应,5min时达到平衡,平衡时测得混合气体中的体积分数为80%.
①0~5min内反应的平均速率______.
②该温度下反应的平衡常数为______.
③下列选项中能够说明该反应已经达到平衡状态的是______(填字母)
a.的物质的量不再变化 b.体系的压强保持不变
c.混合气体的平均摩尔质量保持不变 d.单位时间内消耗CO和生成的物质的量相等
④若平衡后再向容器中加入1mol 、1mol CO、2mol Fe和1mol ,判断此时、的大小关系为:______(填“>”、“=”或“<”).
(2)一定条件下,正向反应速率与时间的关系如右图所示,时刻改变了一个外界条件,可能是______.
(3)科研人员设想用如图原电池装置生产硫酸(设通入的气体完全参与反应).
导线中电子移动方向为______(用字母a,b填写)负极发生的电极反应为______.
沈阳市郊联体2022-2023学年高一下学期5月期中考试
化学答案
一.单选题:(每小题3分,共45分)
1-5 ABACD 6-10 ACBBC 11-15 CDCBD
二.填空题共55分,每空两分(除特殊标明的)
16.(16分)(1)放热 92
(2)b 改变了反应的历程,降低了合成氨反应的活化能
(3)D
(4)0.11 C
17.(9分)(1)
(2)> (3)不变 (4)ACE(3分)(每对一个选项得一分,有错的不得分)
18.(16分)A 增大 减小 <
正 还原
19.(14分)(1)0.24 64 ac(每对一个选项得一分,有错的不得分) >
(2)恒压条件下充入一定量
(3)a→b
化学
考试时间75分钟 试卷总分:100分
可能用到的相对原子质量 H 1 N 14 O 16 Fe 56 S 32
第Ⅰ卷 选择题(45分)
一、单选题(每小题只有一个正确选项,共15小题,每题3分,共45分)
1.下列发电站在发电过程中实现化学能转化为电能的是( )
A.天津双港垃圾焚烧发电厂 B.甘肃酒泉风电基地
C.大亚湾核电站 D.三峡水利发电站
2.下列说法正确的是( )
A.已知 ,在中和热的测定时实际加入的酸碱的量的多少会影响该反应的
B.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量.则
C.500℃、30MPa下,将0.5mol和1.5mol置于密闭的容器中充分反应生成,放热19.3kJ,其热化学方程式为:
D.相同条件下,在两个相同的恒容密闭容器中,2mol和6mol反应放出的热量是1mol和3mol反应放出的热量的2倍
3.下列说法正确的是( )
A.反应在低温下能自发进行,说明该反应的
B.的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为,则氢气燃烧的热化学方程式可表示为:
C.能自发进行的反应一定能迅速发生
D.增大反应物浓度,可增大活化分子百分数,从而增加有效碰撞的次数
4.一种太阳能电池的工作原理如图所示,电解质为铁氰化钾和亚铁氰化钾的混合溶液.下列说法不正确的是( )
A.移向催化剂b
B.催化剂a表面发生的化学反应:
C.在催化剂b表面被氧化
D.电解质溶液中的和浓度基本保持不变
5.HCl气体被氧气氧化的能量关系如图,下列叙述正确的是( )
A.该反应、
B.该反应的浓度平衡常数
C.用E表示键能,则该反应
D.反应
6.某化学兴趣小组用铝片与稀硫酸反应制取氢气,以下能够加快该反应速率的是( )
①用98%的浓硫酸代替稀硫酸 ②加热 ③改用铝粉 ④增大稀硫酸的体积 ⑤加水 ⑥加入少量硫酸铜
A.②③⑥ B.①②③ C.②③④⑥ D.全部
7.下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好
B.硫酸工业中,使用催化剂是为了提高转化为的转化率
C.合成氨工业中,将及时液化分离有利于氨的生产
D.硫酸工业中,的催化氧化不采用高压,是因为压强对转化率无影响
8.将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:,经5min后,测得D的浓度为,C的平均反应速率是,且此时A、B的物质的量之比为2∶3.下列说法不正确的是( )
A.x的值是3
B.5min内,B的平均反应速率为
C.开始时A的物质的量为2.8mol
D.5min时,容器中气体总的物质的量为3.6mol
9.下列说法正确的是( )
A.同温同压下,在光照和点燃的条件下不同
B.298K下,反应不能自发进行,则该反应的
C.当温度、压强一定时,在原料气(和的比例不变)中添加少量惰性气体,有利于提高反应气的平衡转化率
D.合成氨()在高温条件下进行符合勒夏特列原理
10.在密闭容器中的一定量混合气体发生反应:;平衡时测得A的浓度为0.45mol/L,保持温度不变,将容器的容积压缩到原来的一半,再达平衡时,测得A的浓度为0.9mol/L.下列有关判断正确的是( )
A.各物质的计量数一定满足:
B.若B为气体,压缩后B的体积分数增大,转化率降低
C.无论B为固体或气体,压缩后B的质量都不会改变
D.压缩时,平衡向逆反应方向移动,且正、逆反应速率都增大
11.多相催化反应是在催化剂表面通过吸附、解吸过程进行的.我国学者发现T℃时(各物质均为气态),甲醇()与水在铜基催化剂上的反应机理和能量图如图:
下列说法正确的是( )
A.反应Ⅱ的热化学方程式为:
B.在反应中生成又消耗,可认为是催化剂
C.1mol和1mol的总能量小于1mol和3mol的总能量
D.选择优良的催化剂可以降低反应Ⅰ和Ⅱ的活化能,减少过程中的能耗和反应的焓变
12.向一恒容密闭容器中充入A、B、C三种气体,在一定条件下发生反应,各物质的物质的量浓度随时间的变化如图a所示.若从时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b.下列说法不正确的是( )
A.O至内,A与B的平均反应速率之比为3∶2
B.该反应的化学方程式为
C.时,改变的条件可能是加入催化剂
D.该反应的正反应为放热反应
13.下列装置及设计不能达到实验目的的是( )
选项 A B C D
装置
目的 测定中和反应的反应热 探究浓度对化学反应速率的影响 探究催化剂对分解速率的影响 探究温度对化学平衡的影响
A.A B.B C.C D.D
14.已知反应: ,某温度下,将2mol A置于10L密闭容器中,反应一定时间后,下列说法正确的是( )
A.图甲中α(A)表示A的转化率,、表示温度,则可推断出:
B.图乙中c表示反应相同时间A的浓度随温度的变化,则可推断出:
C.图丙中α(%)表示A的平衡转化率,p表示体系总压强,则推断出M点A的体积分数为80%
D.达平衡后,增大B的浓度,则反应速率变化图象可以用图丁表示
15.向一300mL的恒容密闭容器中加入一种多孔粉块状物质R,并充入一定量的CO气体,一定条件下发生反应:,已知该反应平衡常数与温度的关系如下表.
温度/℃ 25 80 230
平衡常数 2
下列说法不正确的是( )
A.物质R做成多孔状可增大接触面积,加快化学反应速率
B.25℃时反应的平衡常数为
C.80℃时反应达到平衡,测得,则的平衡浓度为
D.80℃时,测得某时刻、CO的浓度均为,则此时
第Ⅱ卷非选择题(共55分)
16.(16分)如图表示298.15K时,、与的平均能量与合成氨反应的活化能的曲线图,据图回答下列问题:
(1)若反应中生成2mol氨,则反应______(填“吸热”或“放热”)______kJ.
(2)图中曲线______(填“a”或“b”)表示加入铁触媒(催化剂)的能量变化曲线,铁触媒能加快反应速率的原理是______.
(3)合成氨反应中平衡混合物中氨气的体积分数与压强、温度的关系如右图所示.若曲线a对应的温度为500℃,则曲线b对应的温度可能是______(填字母).
A.600℃ B.550℃ C.500℃ D.450℃
(4)合成氨所需的氢气可由甲烷与水反应制备.发生反应为.一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
t/min
0 0.2 0.3 0 0
2 0.3
3 0.3
4 0.09 0.19 x 0.33
①表中x=______;前2min内的平均反应速率为______.
②反应在3~4min之间,氢气的物质的量增多的原因可能是______(填字母).
A.充入水蒸气 B.缩小体积增大压强 C.升高温度 D.充入氢气
17.(9分)用活性炭还原法处理氮氧化物,有关反应为.某研究小组向某密闭的真空容器(假设容器体积不变)中加入NO和足量的活性炭,恒温()条件下反应.
(1)写出该反应的平衡常数的表达式______.
(2)若升高温度,发现NO体积分数减小,则该反应的______0.
(3)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率______(填“增大”“不变”或“减小”).
(4)某温度下,在一密闭容器中充入一定量发生反应 ,
下列对于该反应的说法正确的是______(填标号).
A.当混合气体颜色保持不变时,反应达到化学平衡状态
B.当的比值保持不变时,反应达到化学平衡状态
C.反应达到化学平衡状态时,每消耗0.1mol NO就会消耗0.05mol
D.反应达到平衡状态后,若降低温度,则混合气体的颜色变浅
E.反应达到平衡状态后,若减小压强,则混合气体的平均相对分子质量减小
18.(16分)肼()是一种应用广泛的化工原料.工业上先合成氨气: ,再进一步制备肼.完成下列填空:
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是______(填“A”或“B”或“C”)
(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
反应速率 平衡常数K
变化情况 ______ ______
(3)通常把拆开1mol某化学键所吸收的能量看成该化学键的键能.已知部分化学键的键能如下:
化学键 N—H N—N O==O N≡N O—H
键能(kJ/mol) 386 167 498 946 460
发射神舟飞船的长征火箭用了肼(,气态)为燃料,若它在氧气(气态)中燃烧,生成(气态)和(气态).该反应的热化学方程式为:______.
(4)氨主要用于生产化肥和硝酸.“十三五”期间,预计我国合成氨产量将保持稳中略增.下图是不同温度和不同压强下,反应达到平衡后,混合物中含量(体积%)的变化情况,已知初始时.判断、压强的大小关系,______(选填“>”、“<”或“=”).
(5)通过传感器可监测的含量,其工作原理如图.
①Pt电极是电源的______(填“正”或“负”)极上发生的是______反应(填“氧化”或“还原”).
②写出NiO电极上的电极反应式:______.
19.(14分)已知炼铁过程中发生
回答下列问题:
(1)时,向容积为2L的恒容密闭容器中加入3mol 和3mol CO发生反应,5min时达到平衡,平衡时测得混合气体中的体积分数为80%.
①0~5min内反应的平均速率______.
②该温度下反应的平衡常数为______.
③下列选项中能够说明该反应已经达到平衡状态的是______(填字母)
a.的物质的量不再变化 b.体系的压强保持不变
c.混合气体的平均摩尔质量保持不变 d.单位时间内消耗CO和生成的物质的量相等
④若平衡后再向容器中加入1mol 、1mol CO、2mol Fe和1mol ,判断此时、的大小关系为:______(填“>”、“=”或“<”).
(2)一定条件下,正向反应速率与时间的关系如右图所示,时刻改变了一个外界条件,可能是______.
(3)科研人员设想用如图原电池装置生产硫酸(设通入的气体完全参与反应).
导线中电子移动方向为______(用字母a,b填写)负极发生的电极反应为______.
沈阳市郊联体2022-2023学年高一下学期5月期中考试
化学答案
一.单选题:(每小题3分,共45分)
1-5 ABACD 6-10 ACBBC 11-15 CDCBD
二.填空题共55分,每空两分(除特殊标明的)
16.(16分)(1)放热 92
(2)b 改变了反应的历程,降低了合成氨反应的活化能
(3)D
(4)0.11 C
17.(9分)(1)
(2)> (3)不变 (4)ACE(3分)(每对一个选项得一分,有错的不得分)
18.(16分)A 增大 减小 <
正 还原
19.(14分)(1)0.24 64 ac(每对一个选项得一分,有错的不得分) >
(2)恒压条件下充入一定量
(3)a→b
同课章节目录
