福建省泉州市重点中学2022-2023学年高一下学期期中考试化学试题(含答案)
文档属性
| 名称 | 福建省泉州市重点中学2022-2023学年高一下学期期中考试化学试题(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 599.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-22 10:42:46 | ||
图片预览



文档简介
泉州市重点中学2022-2023学年高一下学期期中考试
化学试卷
考试时间:90分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Fe-56 Cu-64
一、选择题(本大题共14题,每小题3分,共42分,每小题只有一个选项符合题意。)
1.第24届冬奥会于2022年2月4日在北京开幕,许多核心技术为比赛保驾护航。下列说法不正确的是( )
A.大规模使用氢燃料电池车,行驶时只产生水,实现“零碳排放”
B.速滑馆“冰丝带”用干冰作为制冷剂,干冰升华过程中破坏了共价键
C.北京冬奥会的礼仪服采用石墨烯片聚热保暖,石墨烯与金刚石互为同素异形体
D.场馆选用了二氧化碳跨临界制冷系统,同时利用冷热联供一体化设计对制冷余热进行回收利用,比传统氟利昂制冷技术更节能、环保
2.下列表示相关微粒的化学用语正确的是( )F
A.次氯酸的结构式:H-O-Cl B.甲烷二氟代物的电子式为:
C.中子数为8的碳原子: D.分子的空间填充模型为:
3.下列溶液中能大量共存的离子组是( )
A.、、、 B.、、、
C.、、、 D.、、、
4.X、Y、Z、W均为两种元素组成的常见化合物,Y为淡黄色固体,W为常见液体;甲为单质,乙为红棕色气体;上述物质之间的转化关系如图所示(部分生成物已省略)。则下列说法中不正确的是( )
A.沸点:W>X B.Y中只含有离子键
C.Z中混有乙可用水洗涤再干燥除去 D.生成乙的方程式为:
5.一定温度下,在体积为1L的密闭容器中发生下列反应:,若由0.1降到0.08时,需要20S,那么生成0.02 所需反应的时间为( )
A.等于20S B.大于20S C.等于40S D.大于40S
6.下列反应方程式书写不正确的是( )
A.铝与NaOH溶液产生气泡:
B.用浓氨水检验氯气泄漏:
C.溶液与少量NaOH溶液反应:
D.向酸性溶液中加入足量溶液:
7.五种短周期元素X、Y、Z、M、W的原子序数与其一种常见化合价的关系如图所示,下列关系不正确的是( )
A.元素X可能为锂 B.原子半径大小:
C.中各原子均达到8电子稳定结构 D.元素的简单气态氢化物的稳定性:Y>M
8.实验室中某些气体的制取、收集及尾气处理装置如右图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 a中的物质 b中的物质 c中收集的气体 d中的物质
A 浓氨水 CaO
B 浓硫酸(70%) NaOH溶液
C 稀硝酸 Cu
D 浓盐酸 NaOH溶液
A.AB.BC.CD.D
9.如图是金属镁和卤素单质反应的能量变化示意图。下列说法正确的是( )
A.由制取Mg是放热过程
B.热稳定性:
C.金属镁和卤素单质(g)的反应都是放热反应
D.由图可知,此温度下(s)所含化学键的键能最大
10.《天工开物》记载:“凡火药以硝石、硫磺为主,草木灰为辅……而后火药成声”,涉及的主要反应为。设为阿伏加德罗常数的值,下列说法正确的是( )
A.和对应的晶体类型不同
B.常温常压下,4.4g 气体中含有的原子数为0.3
C.标准状况下,11.2L 中含有共价键的数目为
D.0.1 溶液中钾离子数为0.2
11.下列有关实验现象和解释或结论不正确的是( )
序号 实验操作 现象 解释或结论
① 将少量铁粉加入稀中,充分反应后,滴入KSCN溶液 溶液呈红色 稀将Fe氧化为
② 浓久置或光照 变黄色 不稳定易分解
③ 向某溶液中滴加溶液和稀 产生白色沉淀 溶液中一定含有
④ 用玻璃棒蘸取浓点到蓝色石蕊试纸上 试纸先变红色后褪色 浓具有酸性和强氧化性
A.① B.② C.③ D.④
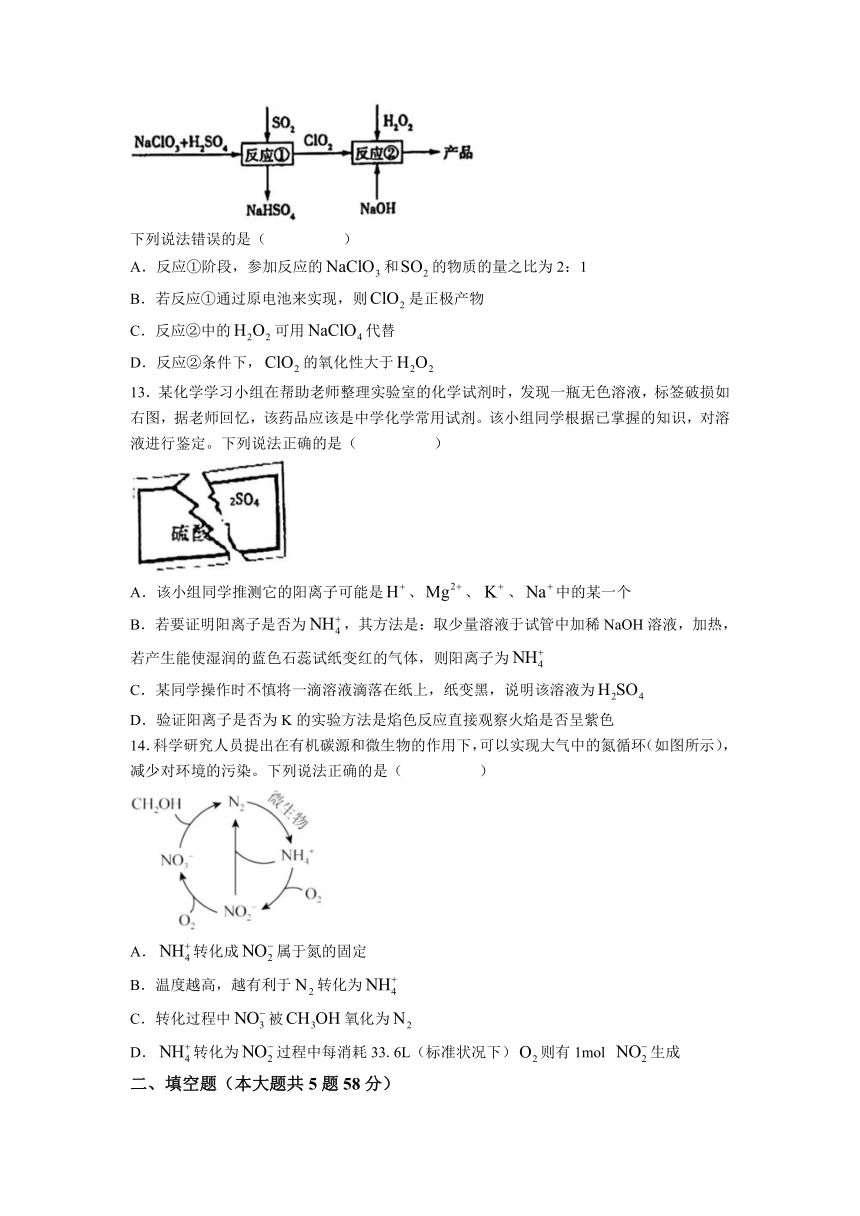
12.亚氯酸钠()是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊法制备亚氯酸钠的流程如下:
下列说法错误的是( )
A.反应①阶段,参加反应的和的物质的量之比为2:1
B.若反应①通过原电池来实现,则是正极产物
C.反应②中的可用代替
D.反应②条件下,的氧化性大于
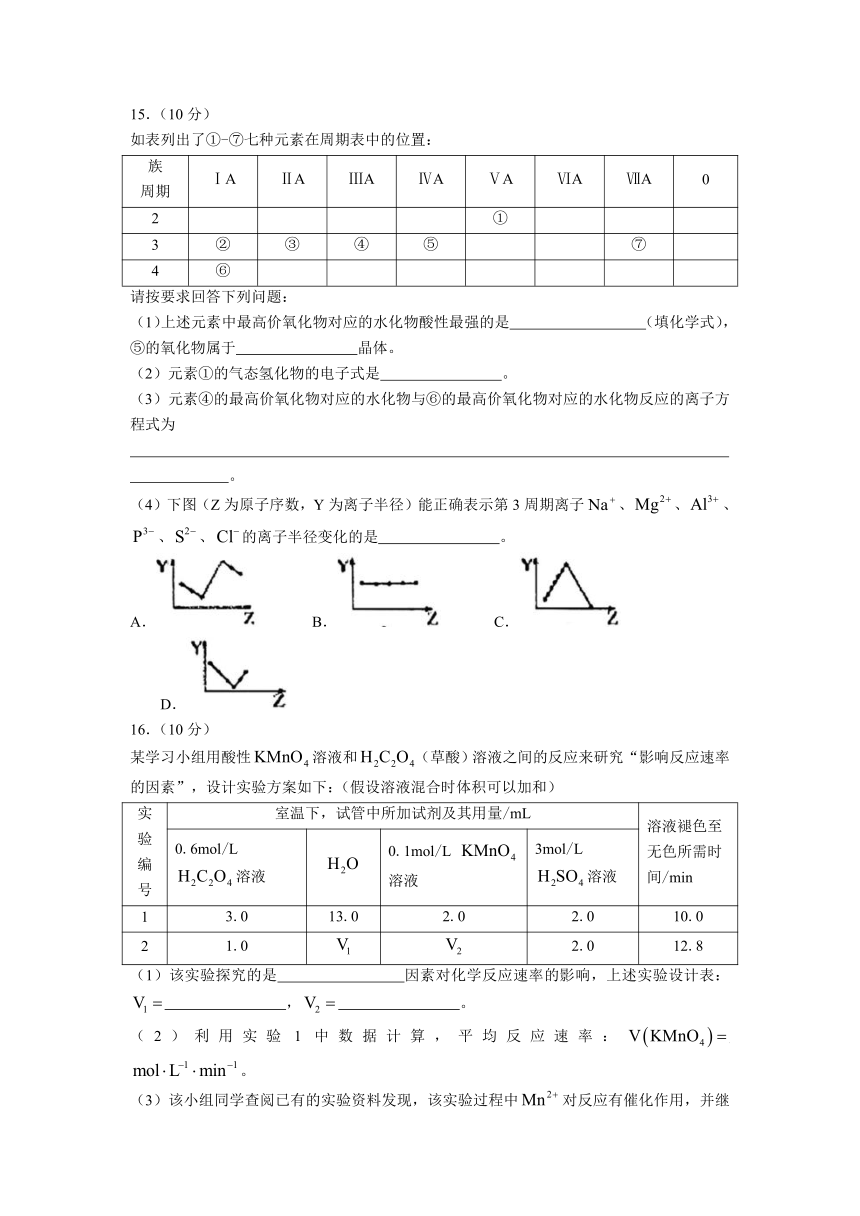
13.某化学学习小组在帮助老师整理实验室的化学试剂时,发现一瓶无色溶液,标签破损如右图,据老师回忆,该药品应该是中学化学常用试剂。该小组同学根据已掌握的知识,对溶液进行鉴定。下列说法正确的是( )
A.该小组同学推测它的阳离子可能是、、、中的某一个
B.若要证明阳离子是否为,其方法是:取少量溶液于试管中加稀NaOH溶液,加热,若产生能使湿润的蓝色石蕊试纸变红的气体,则阳离子为
C.某同学操作时不慎将一滴溶液滴落在纸上,纸变黑,说明该溶液为
D.验证阳离子是否为K的实验方法是焰色反应直接观察火焰是否呈紫色
14.科学研究人员提出在有机碳源和微生物的作用下,可以实现大气中的氮循环(如图所示),减少对环境的污染。下列说法正确的是( )
A.转化成属于氮的固定
B.温度越高,越有利于转化为
C.转化过程中被氧化为
D.转化为过程中每消耗33.6L(标准状况下)则有1mol 生成
二、填空题(本大题共5题58分)
15.(10分)
如表列出了①-⑦七种元素在周期表中的位置:
族 周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 ①
3 ② ③ ④ ⑤ ⑦
4 ⑥
请按要求回答下列问题:
(1)上述元素中最高价氧化物对应的水化物酸性最强的是 (填化学式),⑤的氧化物属于 晶体。
(2)元素①的气态氢化物的电子式是 。
(3)元素④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物反应的离子方程式为
。
(4)下图(Z为原子序数,Y为离子半径)能正确表示第3周期离子、、、、、的离子半径变化的是 。
A. B. C. D.
16.(10分)
某学习小组用酸性溶液和(草酸)溶液之间的反应来研究“影响反应速率的因素”,设计实验方案如下:(假设溶液混合时体积可以加和)
实验编号 室温下,试管中所加试剂及其用量/mL 溶液褪色至无色所需时间/min
0.6mol/L 溶液 0.1mol/L 溶液 3mol/L 溶液
1 3.0 13.0 2.0 2.0 10.0
2 1.0 2.0 12.8
(1)该实验探究的是 因素对化学反应速率的影响,上述实验设计表: , 。
(2)利用实验1中数据计算,平均反应速率: 。
(3)该小组同学查阅已有的实验资料发现,该实验过程中对反应有催化作用,并继续进行实验探究。请你帮助该小组同学完成实验方案。
所加试剂X最好选用
实验编号 室温下,试管中所加试剂及其用量/mL 少量 溶液褪色至无色所需时间/min
0.6mol/L 溶液 0.1mol/L 溶液 3mol/L 溶液
3 3.0 13.0 2.0 2.0 X t
A.0.1mol/L B.0.1mo1/L C.粉末 D.粉末
17.(9分)
汽车尾气中常含有CO、等气体,为减轻污染,一般汽车都加装了“催化净化器”,可将汽车尾气中的有毒气体转化为无污染的气体。
(1)已知NO和CO在催化剂作用下生成和,当有1mol NO完全反应时放出373kJ热量,请与出NO与CO反应的热化学方程式: 。
(2)在容积固定的绝热容器中发生反应,不能说明该反应已达到平衡状态的是
(填序号)。
A.容器内温度不再变化 B.容器内的气体压强保持不变.
C. D.容器内混合气体的密度保持不变
(3)利用下列反应:“设计一个原电池,请固答下列问题:
①负极材料为 。
②正极反应式为 。
18.(14分)
绿水青山就是金山银山,氮氧化合物和二氧化硫是引起雾霾重要物质,工业用多种方法来治理。某种综合处理含NH_{4+}废水和工业废气(主要含NO、CO、、、)的流程如图:
已知:、
(1)固体1的主要成分有、、 (填化学式)。
(2)捕获剂捕获的气体主要是 (填化学式)。
(3)若把气体2通入水中,发生反应的化学方程式为 。
(4)处理工业废气用石灰乳而不是烧碱的原因是 。
(5)向气体1中通入的空气不能过量,原因是 。
(6)与反应的离子方程式为: 。
(7)流程中生成的因外观和食盐相似,又有咸味,容易使人误食中毒。已知能发生如下反应:,可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别和NaCl固体。需选用的物质是 (填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
19.(15分)
氮的化合物在工业生产中有广泛的用途。
Ⅰ.实验室利用如图装置模拟工业生产制备少量硝酸。
(1)写出实验室用氯化铵和消石灰制备氨气的化学方程式 。
(2)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃。下列图示能够正确表示该反应过程中能量变化的是 (填序号)
A. B.
C.
(3)控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟,白烟的化学式是 。
(4)取上述制得的硝酸100ml与9.6g铜反应,硝酸的还原产物为NO,反应后溶液中含有0.1mol ,则硝酸的物质的量浓度为 mol/L。
Ⅱ.已知:
①室温下,
②酸性条件下,NO或都能与反应生成和。
现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示:
(5)装浓硝酸的仪器名称为 。
(6)B中Cu参与反应的离子方程式为 。
(7)装置C的作用是 。
(8)若无装置D,则E中产物除亚硝酸钠外,还有副产物 (填化学式)。
泉州市重点中学2022-2023学年高一下学期期中考试
化学试卷答案
一、选择题(本大题共14题,每小题3分,共42分,每小题只有一个选项符合题意。)
1.B 2.A 3.B 4.B 5.D 6.D 7.C 8.B 9.C 10.B 11.C 12.C
13.C 14.D
二、填空题(本大题共5题58分)
15.(10分)
(1) 共价
(2)
(3)
(4)A
16.(10分)
(1)浓度;15.0 2.0;
(2)0.001mol/(L·min);
(3)D
17.(8分)
(1)
(2)CD
(3)①Fe ②
18.(14分)
(1)
(2)CO
(3)
(4)石灰乳来源丰富,成本低
(5)空气过量时会将NO全部转化为,与NaOH溶液反应时不会将全部转化为导致处理含废水的效率降低
(6)
(7)①②⑤
19.(16分)
Ⅰ.
(1)
(2)A
(3)
(4)5
Ⅱ.
(5)分液漏斗
(6)
(7)防止倒吸
(8)、NaOH
化学试卷
考试时间:90分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Fe-56 Cu-64
一、选择题(本大题共14题,每小题3分,共42分,每小题只有一个选项符合题意。)
1.第24届冬奥会于2022年2月4日在北京开幕,许多核心技术为比赛保驾护航。下列说法不正确的是( )
A.大规模使用氢燃料电池车,行驶时只产生水,实现“零碳排放”
B.速滑馆“冰丝带”用干冰作为制冷剂,干冰升华过程中破坏了共价键
C.北京冬奥会的礼仪服采用石墨烯片聚热保暖,石墨烯与金刚石互为同素异形体
D.场馆选用了二氧化碳跨临界制冷系统,同时利用冷热联供一体化设计对制冷余热进行回收利用,比传统氟利昂制冷技术更节能、环保
2.下列表示相关微粒的化学用语正确的是( )F
A.次氯酸的结构式:H-O-Cl B.甲烷二氟代物的电子式为:
C.中子数为8的碳原子: D.分子的空间填充模型为:
3.下列溶液中能大量共存的离子组是( )
A.、、、 B.、、、
C.、、、 D.、、、
4.X、Y、Z、W均为两种元素组成的常见化合物,Y为淡黄色固体,W为常见液体;甲为单质,乙为红棕色气体;上述物质之间的转化关系如图所示(部分生成物已省略)。则下列说法中不正确的是( )
A.沸点:W>X B.Y中只含有离子键
C.Z中混有乙可用水洗涤再干燥除去 D.生成乙的方程式为:
5.一定温度下,在体积为1L的密闭容器中发生下列反应:,若由0.1降到0.08时,需要20S,那么生成0.02 所需反应的时间为( )
A.等于20S B.大于20S C.等于40S D.大于40S
6.下列反应方程式书写不正确的是( )
A.铝与NaOH溶液产生气泡:
B.用浓氨水检验氯气泄漏:
C.溶液与少量NaOH溶液反应:
D.向酸性溶液中加入足量溶液:
7.五种短周期元素X、Y、Z、M、W的原子序数与其一种常见化合价的关系如图所示,下列关系不正确的是( )
A.元素X可能为锂 B.原子半径大小:
C.中各原子均达到8电子稳定结构 D.元素的简单气态氢化物的稳定性:Y>M
8.实验室中某些气体的制取、收集及尾气处理装置如右图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 a中的物质 b中的物质 c中收集的气体 d中的物质
A 浓氨水 CaO
B 浓硫酸(70%) NaOH溶液
C 稀硝酸 Cu
D 浓盐酸 NaOH溶液
A.AB.BC.CD.D
9.如图是金属镁和卤素单质反应的能量变化示意图。下列说法正确的是( )
A.由制取Mg是放热过程
B.热稳定性:
C.金属镁和卤素单质(g)的反应都是放热反应
D.由图可知,此温度下(s)所含化学键的键能最大
10.《天工开物》记载:“凡火药以硝石、硫磺为主,草木灰为辅……而后火药成声”,涉及的主要反应为。设为阿伏加德罗常数的值,下列说法正确的是( )
A.和对应的晶体类型不同
B.常温常压下,4.4g 气体中含有的原子数为0.3
C.标准状况下,11.2L 中含有共价键的数目为
D.0.1 溶液中钾离子数为0.2
11.下列有关实验现象和解释或结论不正确的是( )
序号 实验操作 现象 解释或结论
① 将少量铁粉加入稀中,充分反应后,滴入KSCN溶液 溶液呈红色 稀将Fe氧化为
② 浓久置或光照 变黄色 不稳定易分解
③ 向某溶液中滴加溶液和稀 产生白色沉淀 溶液中一定含有
④ 用玻璃棒蘸取浓点到蓝色石蕊试纸上 试纸先变红色后褪色 浓具有酸性和强氧化性
A.① B.② C.③ D.④
12.亚氯酸钠()是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊法制备亚氯酸钠的流程如下:
下列说法错误的是( )
A.反应①阶段,参加反应的和的物质的量之比为2:1
B.若反应①通过原电池来实现,则是正极产物
C.反应②中的可用代替
D.反应②条件下,的氧化性大于
13.某化学学习小组在帮助老师整理实验室的化学试剂时,发现一瓶无色溶液,标签破损如右图,据老师回忆,该药品应该是中学化学常用试剂。该小组同学根据已掌握的知识,对溶液进行鉴定。下列说法正确的是( )
A.该小组同学推测它的阳离子可能是、、、中的某一个
B.若要证明阳离子是否为,其方法是:取少量溶液于试管中加稀NaOH溶液,加热,若产生能使湿润的蓝色石蕊试纸变红的气体,则阳离子为
C.某同学操作时不慎将一滴溶液滴落在纸上,纸变黑,说明该溶液为
D.验证阳离子是否为K的实验方法是焰色反应直接观察火焰是否呈紫色
14.科学研究人员提出在有机碳源和微生物的作用下,可以实现大气中的氮循环(如图所示),减少对环境的污染。下列说法正确的是( )
A.转化成属于氮的固定
B.温度越高,越有利于转化为
C.转化过程中被氧化为
D.转化为过程中每消耗33.6L(标准状况下)则有1mol 生成
二、填空题(本大题共5题58分)
15.(10分)
如表列出了①-⑦七种元素在周期表中的位置:
族 周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
2 ①
3 ② ③ ④ ⑤ ⑦
4 ⑥
请按要求回答下列问题:
(1)上述元素中最高价氧化物对应的水化物酸性最强的是 (填化学式),⑤的氧化物属于 晶体。
(2)元素①的气态氢化物的电子式是 。
(3)元素④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物反应的离子方程式为
。
(4)下图(Z为原子序数,Y为离子半径)能正确表示第3周期离子、、、、、的离子半径变化的是 。
A. B. C. D.
16.(10分)
某学习小组用酸性溶液和(草酸)溶液之间的反应来研究“影响反应速率的因素”,设计实验方案如下:(假设溶液混合时体积可以加和)
实验编号 室温下,试管中所加试剂及其用量/mL 溶液褪色至无色所需时间/min
0.6mol/L 溶液 0.1mol/L 溶液 3mol/L 溶液
1 3.0 13.0 2.0 2.0 10.0
2 1.0 2.0 12.8
(1)该实验探究的是 因素对化学反应速率的影响,上述实验设计表: , 。
(2)利用实验1中数据计算,平均反应速率: 。
(3)该小组同学查阅已有的实验资料发现,该实验过程中对反应有催化作用,并继续进行实验探究。请你帮助该小组同学完成实验方案。
所加试剂X最好选用
实验编号 室温下,试管中所加试剂及其用量/mL 少量 溶液褪色至无色所需时间/min
0.6mol/L 溶液 0.1mol/L 溶液 3mol/L 溶液
3 3.0 13.0 2.0 2.0 X t
A.0.1mol/L B.0.1mo1/L C.粉末 D.粉末
17.(9分)
汽车尾气中常含有CO、等气体,为减轻污染,一般汽车都加装了“催化净化器”,可将汽车尾气中的有毒气体转化为无污染的气体。
(1)已知NO和CO在催化剂作用下生成和,当有1mol NO完全反应时放出373kJ热量,请与出NO与CO反应的热化学方程式: 。
(2)在容积固定的绝热容器中发生反应,不能说明该反应已达到平衡状态的是
(填序号)。
A.容器内温度不再变化 B.容器内的气体压强保持不变.
C. D.容器内混合气体的密度保持不变
(3)利用下列反应:“设计一个原电池,请固答下列问题:
①负极材料为 。
②正极反应式为 。
18.(14分)
绿水青山就是金山银山,氮氧化合物和二氧化硫是引起雾霾重要物质,工业用多种方法来治理。某种综合处理含NH_{4+}废水和工业废气(主要含NO、CO、、、)的流程如图:
已知:、
(1)固体1的主要成分有、、 (填化学式)。
(2)捕获剂捕获的气体主要是 (填化学式)。
(3)若把气体2通入水中,发生反应的化学方程式为 。
(4)处理工业废气用石灰乳而不是烧碱的原因是 。
(5)向气体1中通入的空气不能过量,原因是 。
(6)与反应的离子方程式为: 。
(7)流程中生成的因外观和食盐相似,又有咸味,容易使人误食中毒。已知能发生如下反应:,可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别和NaCl固体。需选用的物质是 (填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
19.(15分)
氮的化合物在工业生产中有广泛的用途。
Ⅰ.实验室利用如图装置模拟工业生产制备少量硝酸。
(1)写出实验室用氯化铵和消石灰制备氨气的化学方程式 。
(2)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃。下列图示能够正确表示该反应过程中能量变化的是 (填序号)
A. B.
C.
(3)控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟,白烟的化学式是 。
(4)取上述制得的硝酸100ml与9.6g铜反应,硝酸的还原产物为NO,反应后溶液中含有0.1mol ,则硝酸的物质的量浓度为 mol/L。
Ⅱ.已知:
①室温下,
②酸性条件下,NO或都能与反应生成和。
现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示:
(5)装浓硝酸的仪器名称为 。
(6)B中Cu参与反应的离子方程式为 。
(7)装置C的作用是 。
(8)若无装置D,则E中产物除亚硝酸钠外,还有副产物 (填化学式)。
泉州市重点中学2022-2023学年高一下学期期中考试
化学试卷答案
一、选择题(本大题共14题,每小题3分,共42分,每小题只有一个选项符合题意。)
1.B 2.A 3.B 4.B 5.D 6.D 7.C 8.B 9.C 10.B 11.C 12.C
13.C 14.D
二、填空题(本大题共5题58分)
15.(10分)
(1) 共价
(2)
(3)
(4)A
16.(10分)
(1)浓度;15.0 2.0;
(2)0.001mol/(L·min);
(3)D
17.(8分)
(1)
(2)CD
(3)①Fe ②
18.(14分)
(1)
(2)CO
(3)
(4)石灰乳来源丰富,成本低
(5)空气过量时会将NO全部转化为,与NaOH溶液反应时不会将全部转化为导致处理含废水的效率降低
(6)
(7)①②⑤
19.(16分)
Ⅰ.
(1)
(2)A
(3)
(4)5
Ⅱ.
(5)分液漏斗
(6)
(7)防止倒吸
(8)、NaOH
同课章节目录
