2014高考全国新课标Ⅰ卷化学试题评价与解析(共57张PPT)
文档属性
| 名称 | 2014高考全国新课标Ⅰ卷化学试题评价与解析(共57张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-08-03 00:00:00 | ||
图片预览











文档简介
课件57张PPT。2014高考理综-化学试题分析 河北衡水中学 范灵丽 今年新课标Ⅰ卷理综的化学部分,在命题形式上继续突出课标要求,回归基础,与教材联系较为紧密。充分考查了考试大纲中要求掌握的基础知识、基本技能和应用基础知识、基本技能解决问题的能力。
试卷所涉及知识点覆盖面较广,试题难度整体来说比去年有所降低,但依然是以能力测试为主导,在测试学生学习基础知识、技能和方法的基础上,全面地检测了学生的化学学科素养。2014年新课标Ⅰ高考化学试卷评析选择题部分
试卷的选择题部分依次考查了同分异构体、化学与生活、化学反应速率、元素周期表、物质的溶解度、沉淀溶解平衡、化学实验基础、以及元素化学部分的知识。题目难度有所降低,着重增加了基础知识的考查。2014年新课标Ⅰ高考化学试卷评析必考题部分
新课标化学卷的非选择题一直是3+1的模式。3个必选题,考查的内容为有机化学实验;以元素化合物为载体,考查了分析应用信息的能力,弱电解质电离方程式的书写、氧化还原反应;以及选修4化学反应原理的综合应用。题目形式新颖,并且,今年也沿袭了前两年的特点,实验题扔是对有机合成的考查,而第27题则是属于化学试卷中的变化题型,在新课标卷中属于每一年都不重复的题型。2014年新课标Ⅰ高考化学试卷评析2014年新课标Ⅰ高考化学试卷评析选做题部分
选做题中,选修三的37题,物质结构与性质比去年难度有所降低。选修五的38题有机化学基础,与去年类似,属于给出信息进行推断的题目
在试题设计中除了每年必考的反应类型、结构简式、化学方程式的书写以及同分异构外,还对反应条件进行了重点考查。下面我把整套试题具体分析如下: 2014高考试题分析之选择7、下列化合物中同分异构体数目最少的是( A )
A. 戊烷 B. 戊醇
C. 戊烯 D. 乙酸乙酯 解析:点评:第7题延续了近几年对有机物同分异构体的考查方式,没有大的变化。题目难度较小 2014高考试题分析之选择8、化学与社会、生活密切相关。对下列现象或事实的
解释正确的是:( C )C.草木灰的有效成分K2CO3 水解显碱性,而NH4Cl水解显酸性,二者混合使用会使水解相互促进,产生氨气逸出而降低肥效 点评:第8题考查生活中的化学知识,意在考查考生利用所学知识解决实际问题的能力。知识来源于盐类的水解和氧化还原反应部分。纯碱去油污,漂白粉变质、铵态氮肥和草木灰不能混合使用,氯化铁和铜线路板反应等等,这些知识都来源于教材,难度小。 2014高考试题分析之选择 2014高考试题分析之选择9、已知分解1 mol H2O2 放出热量98kJ。在含少量I-的溶液中,H2O2分解的机理为:
H2O2+ I- →H2O +IO- 慢
H2O2+ IO-→H2O +O2+ I- 快
下列有关该反应的说法正确的是 ( A )
A. 反应速率与I-的浓度有关 B. IO-也是该反应的催化剂
C. 反应活化能等于98kJ·mol-1 D.v(H2O2)=v(H2O)=v(O2)【解析】决定化反应速率的主要是慢反应,所以I-浓度越大,则整个反应速率越快,A正确;
I-是该反应的催化剂 ,所以B错误;
98KJ/mol是该反应的△H,不是活化能,C 错误
把两个方程式合并得到:2H2O2=2H2O+O2
v(H2O2)=v(H2O)=2v(O2),D错误。 点评:第9题考查化学反应原理部分的基础知识,涉及内容包括催化原理、活化能与反应热的关系、化学反应速率的表示方法等等。
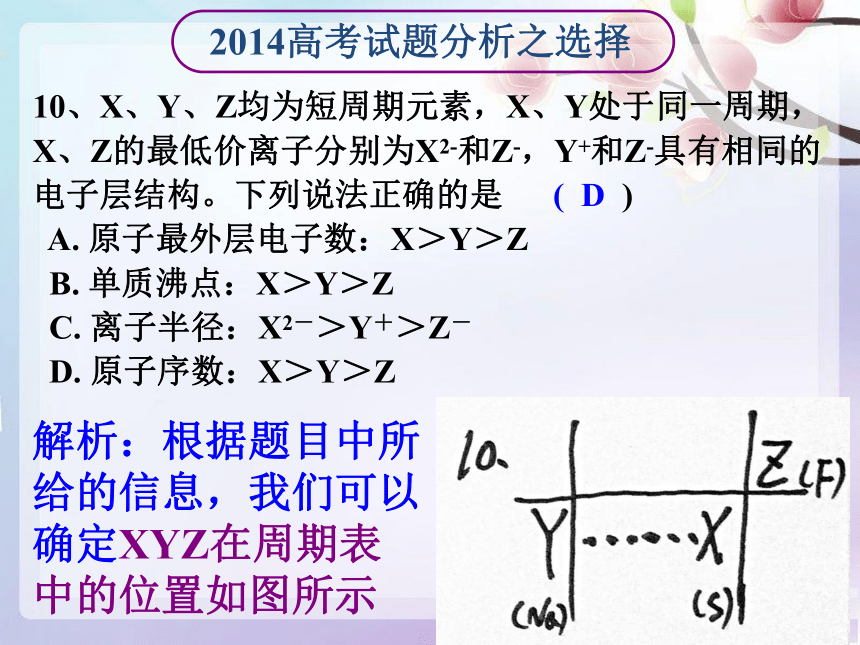
在历年高考题中均有考查,并且较以往的化学原理题来说,难度降低。 2014高考试题分析之选择 2014高考试题分析之选择10、X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是 ( D )
A. 原子最外层电子数:X>Y>Z
B. 单质沸点:X>Y>Z
C. 离子半径:X2->Y+>Z-
D. 原子序数:X>Y>Z解析:根据题目中所给的信息,我们可以确定XYZ在周期表中的位置如图所示 点评:第10题保留了近几年课表卷的必考题模式:元素周期表、元素周期律。更加注重基础知识,如:短周期、同一周期、最低(最高)价,电子层结构相同等等,考查的半径大小、熔沸点高低均为基本考查点。 2014高考试题分析之选择 2014高考试题分析之选择11、溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( A )A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,
可用重结晶方法提纯 2014高考试题分析之选择 点评:第11题考察了难溶电解质,与去年课标卷保持一致。
难溶电解质的沉淀溶解平衡是这几年高考化学中的重点知识。与去年的单纯利用公式进行计算不同,今年结合了难溶电解质的溶解度曲线,考查温度对物质溶解速率的影响以及Ksp、重结晶等知识。
这次结合溶解度曲线进行考察,虽然形势变化,但试题难度适中。 2014高考试题分析之选择12、下列有关仪器使用方法或实验操作正确的是( B )
A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B.酸式滴定管装标准液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以
减小实验误差
D用容量瓶配溶液时,若加水超过刻度线,
立即用滴管吸出多余液体【解析】容量瓶是对精度要求很高的仪器,不能高温烘干,以免影响其精度,A错误;
滴定管在盛装溶液前,都必须用待装溶液润洗,B正确
酸碱中和滴定实验中,锥形瓶不能润洗,否则会造成锥形瓶内的溶质增多,测定结果有误差,C 错误;
用容量瓶配制溶液时,若加水超过刻度线,只能放弃重配,若吸出溶液,会使配得溶液浓度偏低,D错。 2014高考试题分析之选择 点评:第12题考查了基本实验仪器的使用,重点考查了锥形瓶、容量瓶、滴定管的使用和注意事项,来源于高中化学的两个基础定量实验:配制一定物质的量浓度的溶液和酸碱中和滴定。
再次体现新课程标准的要求:回归教材,属于简单基础题。 2014高考试题分析之选择13、利用右图所示装置进行下列实验,能得出相应实验结论的是( B )【解析】 浓硫酸可使蔗糖碳化,并放出大量的热,体现浓硫酸的脱水性,生成的碳继续与浓硫酸反应生成SO2,使③中的溴水褪色,通过蔗糖变黑、溴水褪色可以得出浓硫酸具有脱水性、氧化性, B正确, 2014高考试题分析之选择 点评:第13题以基础实验为切入点,考查了元素化合物部分的知识。
四个选项中所涉及的知识均在历年高考试题中出现过。
本题中,有关氯化银和硫化银之间的沉淀转化,浓硫酸使蔗糖炭化脱水的实验等,均为对基础理论知识的考查。2014高考试题分析之必做题26.(13分)
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:实验步骤:
在A中加入4.4 g的异戊醇、6.0 g的乙酸、数滴浓硫酸和
2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)仪器B的名称是 。
(2)在洗涤操作中,第一次水洗的主要目的是 ,
第二次水洗的主要目的是 。
(3)在洗涤、分液操作中,应充分振荡,然后静置, 待分层后
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口 放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出【解析】(1)仪器B是球形冷凝管
(2)主要从物质的溶解性和存在的杂质考虑。
第一次水洗主要是洗掉浓硫酸和过量的乙酸。
第二次水洗则主要是洗去上一步加入的NaHCO3溶液。
(3)乙酸异戊酯密度比水小,它在上层,分液时下层必
须从下口放出,上层液体从上口倒出。所以选d。2014高考试题分析之必做题(4)本实验中加入过量乙酸的目的是 。
(5)实验中加入少量无水MgSO4的目的是 。【解析】
(4)由于乙酸的沸点较低,所以会有较多的
乙酸挥发损耗,加入过量的乙酸可以提
高异戊醇的转化率
(5)无水MgSO4有较快的吸水性,且不与
乙酸异戊酯反应,可以吸收水分,对乙酸
异戊酯进行干燥,便于下一步的蒸馏。 2014高考试题分析之必做题(6)在蒸馏操作中,仪器选择及安装都正确的
是 (填标号)。【解析】(6)a、d的温度计位置错误,
冷凝管应该用直形冷凝管,若用球形冷凝管,冷凝的液体不能全部流下,所以应该选b。2014高考试题分析之必做题(7)本实验的产率是 (填标号)。
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏 (填高或低) 原因 .【解析】
(7)从题目给的数据可以得出乙酸过量,则按异戊醇计算。异戊醇4.4g,为0.05mol,理论上可以生成乙酸异戊酯0.05mol,质量为6.5g。
则产率为:3.9g/6.5g×100%=60%.
(8) 从130 ℃开始收集,会使溶于乙酸异戊酯的异戊醇进入到产品中,所以使产率偏高, 2014高考试题分析之必做题 26、答案及评分标准 2014高考试题分析之必做题 2014高考试题分析之必做题 点评:第26题依然延续了连续三年的实验考查模式。以有机化合物的制备为切入点,考查基本仪器的识别和使用、基本物质的制备原理和制备流程、物质的分离和提纯等内容。
与往年的题目一样,来源于课本必修二的基本实验,稍作改变,难度较小。27.次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。
回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用
于化学镀银。 ①(H3PO2)中,P元素的化合价为 。
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质
的量之比为4︰1,则氧化产物为: (填化学式)。
③NaH2PO2为 (填“正盐”或“酸式盐”),
其溶液显 (填“弱酸性”、“中性”或“弱碱性”)。【解析】(1) 次磷酸一元酸,只发生一步电离,中强酸是弱电解质,电离时要用可逆符号 :
(2)①利用元素化合价代数和为零,得出P元素为+1价
②Ag+是氧化剂,H3PO2做还原剂,二者以4︰1反应,
则4Ag+总共降4价,1H3PO2中的P必须升4价,P元素
变为+5价,生成H3PO4。 ③由于H3PO2是一元酸,所以NaH2PO2是正盐,强碱弱酸盐水解显碱性。 2014高考试题分析之必做题(3)(H3PO2)的工业制法是:将白磷(P4)与Ba(OH)2溶
液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4
反应。写出白磷与Ba(OH)2溶液反应的化学方程式
。【解析】
(3)反应的反应物与产物都已经给出,这是
P元素的歧化反应,注意配平即可: 2014高考试题分析之必做题(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过): ①写出阳极的电极反应式: 。
②分析产品室可得到H3PO2的原因 : .
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”
中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与
产品室之间的阳膜,从而合并了阳极室与产品室。其缺点
是产品中混有 杂质,该杂质产生的原 因是 。 2014高考试题分析之必做题 2014高考试题分析之必做题27、答案及评分标准 2014高考试题分析之必做题 2014高考试题分析之必做题 评价:第27题与往年题目的情景设置有所不同,没有出现工艺流程图,但实际考查的知识没有发生变化,以次磷酸(H3PO2)为载体,考查了弱电解质电离方程式的书写、化合价的确定,氧化还原反应、盐类水解、以及电化学的相关知识
题目形式新颖,但实际上难度在降低,再次体现回归基础。28.乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯 (C2H5OSO3H),再水解生成乙醇。写出相应反应的化学方程式 。解析:
(1)乙烯与硫酸反应生成硫酸氢乙酯发生的是加成
反应,硫酸氢乙酯再水解得到乙醇。 2014高考试题分析之必做题(2)已知:甲醇脱水反应2CH3OH(g)=CH3OCH3(g)+H2O(g)
△H1=-23.9kJ/mol
甲醇制烯烃反应2CH3OH(g)=C2H4 (g)+2H2O(g)
△H2=-29.1kJ/mol
乙醇异构化反应CH3CH2OH(g)=CH3OCH3(g)
△H3=+50.7kJ/mol
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的
△H= kJ/mol。
与间接水合法相比,气相直接水合法的优点是 。解析:(2)考盖斯定律,用方程式①-②-③可得:
△H- △H1 - △H2 - △H3=—45.5KJ/mol
比较两种流程,可看出气相直接水合法减少反应步骤,增大产物的产率,同时减少污染物的排放;而且不用硫酸作反应物,减少对设备的腐蚀。 2014高考试题分析之必做题 2014高考试题分析之必做题 2014高考试题分析之必做题解析: 2014高考试题分析之必做题解析(3)28、答案及评分标准 2014高考试题分析之必做题 2014高考试题分析之必做题 第28题依然是考查化学反应原理的综合试题,重点考查了化学反应热效应、盖斯定律、化学平衡常数的概念以及计算。
试题设置的情景是以学生熟悉的乙醇和乙烯为载体,且测定的数据以图表的形式呈现,要求考生能够利用图表进行数据分析、判断、提取有效信息,突出了运用化学信息的能力的考查。
对这道题目的设计,大家的失分点在于化学平衡常数的计算部分,学生会由于不熟悉此类计算而失分,但实际上计算类型来源于2013年的高考原题新课标Ⅱ的28题。 2014高考试题分析之选做题36.[化学——选修2:化学与技术](15分)
磷矿石主要以磷酸钙[Ca3(PO4)2*H2O]和
磷灰石[Ca5F(PO4)3、Ca5(OH)(PO4)3]等形式存在。
图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。
图(b)是热法磷酸生成过程中由磷灰石制单质磷的流程。回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 %。
(2)以磷灰石为原料,湿法磷酸过程中Ca3F(PO4)3反应的化学方程式为: 。
现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85%的商品磷酸 吨 2014高考试题分析之选做题(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量
焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是:
(填化学式),冷凝塔1的主要沉积物是: .
冷凝塔2的主要沉积物是: 。 2014高考试题分析之选做题(4)尾气中主要含有 ,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去 ;再通入次氯酸钠溶液,可除去 (均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是: 。解析: 2014高考试题分析之选做题36、答案及评分标准 2014高考试题分析之选做题2014高考试题分析之选做题 评价:第36题是工艺流程题,以磷矿石制备磷酸为载体,涉及到基本化学反应在化工生产中的运用,考查基本知识比重较大,注重知识的迁移和综合运用。
我们在复习中应该加大对基础知识的总结,并提高知识的迁移、运用能力。37.[化学—选修3:物质结构与性质] (15分)
早期发现的一种天然二十面体准晶颗粒由三种Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置
序的独特晶体,可通过 方法区分晶体、
准晶体和非晶体。
(2)基态Fe原子有 个未成对电子,
Fe3+的电子排布式为 。
可用硫氰化钾检验Fe3+,形成的配合物的颜色为 。解析: 2014高考试题分析之选做题(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为 ,1mol乙醛分子中含有的σ键的数目为 。
乙酸的沸点明显高于乙醛,其主要原因是 。
Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。解析: 2014高考试题分析之选做题(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g/cm3(不必计算出结果)。解析: 2014高考试题分析之选做题37、答案及评分标准 2014高考试题分析之选做题 2014高考试题分析之选做题 评价:第37题以铝、铁、铜三种金属为载体,考查了晶体与非晶体的区别,原子的核外电子排布、配合物的相关知识、杂化轨道的知识、物质沸点与性质的关系、晶胞密度的相关计算等知识,以基本知识考查为主。
和历年试题比起来,增加了晶体知识的考查,角度较全面,但在计算方面难度有所降低。 2014高考试题分析之选做题 2014高考试题分析之选做题 2014高考试题分析之选做题38(4)F的同分异构体中含有苯环的还有 种(不考虑立体异构),其中核磁共振氢谱为4组峰,且面积比为6:2:2:1的是 (写出其中一种的结构简式)。 2014高考试题分析之选做题解析:38、答案及评分标准 2014高考试题分析之选做题2014高考试题分析之选做题 评价:第38题依然保持以陌生物质入手,考查有机合成的模式。所涉及的知识是有机化学中的基本知识,比如卤代烃的消去反应、苯的硝化反应,有机物化合物结构简式的确定,核磁共振氢谱、同分异构体等等。
命题形式依然延续了去年新课标Ⅰ卷中的形式,由两条线合成一种物质。给出必要的已知信息,而且已知信息中包含未学过的新知识,考查学生学习能力和知识迁移能力;同分异构体的考查、题型难度适中,基本延续去年模式。 2014年的化学试题再次指明了新课标模式下的高考备考方向:
①要回归教材,重视基础。
②重视学习能力、知识的迁移和运用能力
的培养。要学会利用图表进行数据分
析、判断、提取有效信息。
③重视化学学科素养的培养
④重视探究能力和创新思维品质 的培养2015年高考备考指导请多提宝贵意见
谢 谢!
试卷所涉及知识点覆盖面较广,试题难度整体来说比去年有所降低,但依然是以能力测试为主导,在测试学生学习基础知识、技能和方法的基础上,全面地检测了学生的化学学科素养。2014年新课标Ⅰ高考化学试卷评析选择题部分
试卷的选择题部分依次考查了同分异构体、化学与生活、化学反应速率、元素周期表、物质的溶解度、沉淀溶解平衡、化学实验基础、以及元素化学部分的知识。题目难度有所降低,着重增加了基础知识的考查。2014年新课标Ⅰ高考化学试卷评析必考题部分
新课标化学卷的非选择题一直是3+1的模式。3个必选题,考查的内容为有机化学实验;以元素化合物为载体,考查了分析应用信息的能力,弱电解质电离方程式的书写、氧化还原反应;以及选修4化学反应原理的综合应用。题目形式新颖,并且,今年也沿袭了前两年的特点,实验题扔是对有机合成的考查,而第27题则是属于化学试卷中的变化题型,在新课标卷中属于每一年都不重复的题型。2014年新课标Ⅰ高考化学试卷评析2014年新课标Ⅰ高考化学试卷评析选做题部分
选做题中,选修三的37题,物质结构与性质比去年难度有所降低。选修五的38题有机化学基础,与去年类似,属于给出信息进行推断的题目
在试题设计中除了每年必考的反应类型、结构简式、化学方程式的书写以及同分异构外,还对反应条件进行了重点考查。下面我把整套试题具体分析如下: 2014高考试题分析之选择7、下列化合物中同分异构体数目最少的是( A )
A. 戊烷 B. 戊醇
C. 戊烯 D. 乙酸乙酯 解析:点评:第7题延续了近几年对有机物同分异构体的考查方式,没有大的变化。题目难度较小 2014高考试题分析之选择8、化学与社会、生活密切相关。对下列现象或事实的
解释正确的是:( C )C.草木灰的有效成分K2CO3 水解显碱性,而NH4Cl水解显酸性,二者混合使用会使水解相互促进,产生氨气逸出而降低肥效 点评:第8题考查生活中的化学知识,意在考查考生利用所学知识解决实际问题的能力。知识来源于盐类的水解和氧化还原反应部分。纯碱去油污,漂白粉变质、铵态氮肥和草木灰不能混合使用,氯化铁和铜线路板反应等等,这些知识都来源于教材,难度小。 2014高考试题分析之选择 2014高考试题分析之选择9、已知分解1 mol H2O2 放出热量98kJ。在含少量I-的溶液中,H2O2分解的机理为:
H2O2+ I- →H2O +IO- 慢
H2O2+ IO-→H2O +O2+ I- 快
下列有关该反应的说法正确的是 ( A )
A. 反应速率与I-的浓度有关 B. IO-也是该反应的催化剂
C. 反应活化能等于98kJ·mol-1 D.v(H2O2)=v(H2O)=v(O2)【解析】决定化反应速率的主要是慢反应,所以I-浓度越大,则整个反应速率越快,A正确;
I-是该反应的催化剂 ,所以B错误;
98KJ/mol是该反应的△H,不是活化能,C 错误
把两个方程式合并得到:2H2O2=2H2O+O2
v(H2O2)=v(H2O)=2v(O2),D错误。 点评:第9题考查化学反应原理部分的基础知识,涉及内容包括催化原理、活化能与反应热的关系、化学反应速率的表示方法等等。
在历年高考题中均有考查,并且较以往的化学原理题来说,难度降低。 2014高考试题分析之选择 2014高考试题分析之选择10、X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是 ( D )
A. 原子最外层电子数:X>Y>Z
B. 单质沸点:X>Y>Z
C. 离子半径:X2->Y+>Z-
D. 原子序数:X>Y>Z解析:根据题目中所给的信息,我们可以确定XYZ在周期表中的位置如图所示 点评:第10题保留了近几年课表卷的必考题模式:元素周期表、元素周期律。更加注重基础知识,如:短周期、同一周期、最低(最高)价,电子层结构相同等等,考查的半径大小、熔沸点高低均为基本考查点。 2014高考试题分析之选择 2014高考试题分析之选择11、溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( A )A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,
可用重结晶方法提纯 2014高考试题分析之选择 点评:第11题考察了难溶电解质,与去年课标卷保持一致。
难溶电解质的沉淀溶解平衡是这几年高考化学中的重点知识。与去年的单纯利用公式进行计算不同,今年结合了难溶电解质的溶解度曲线,考查温度对物质溶解速率的影响以及Ksp、重结晶等知识。
这次结合溶解度曲线进行考察,虽然形势变化,但试题难度适中。 2014高考试题分析之选择12、下列有关仪器使用方法或实验操作正确的是( B )
A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B.酸式滴定管装标准液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以
减小实验误差
D用容量瓶配溶液时,若加水超过刻度线,
立即用滴管吸出多余液体【解析】容量瓶是对精度要求很高的仪器,不能高温烘干,以免影响其精度,A错误;
滴定管在盛装溶液前,都必须用待装溶液润洗,B正确
酸碱中和滴定实验中,锥形瓶不能润洗,否则会造成锥形瓶内的溶质增多,测定结果有误差,C 错误;
用容量瓶配制溶液时,若加水超过刻度线,只能放弃重配,若吸出溶液,会使配得溶液浓度偏低,D错。 2014高考试题分析之选择 点评:第12题考查了基本实验仪器的使用,重点考查了锥形瓶、容量瓶、滴定管的使用和注意事项,来源于高中化学的两个基础定量实验:配制一定物质的量浓度的溶液和酸碱中和滴定。
再次体现新课程标准的要求:回归教材,属于简单基础题。 2014高考试题分析之选择13、利用右图所示装置进行下列实验,能得出相应实验结论的是( B )【解析】 浓硫酸可使蔗糖碳化,并放出大量的热,体现浓硫酸的脱水性,生成的碳继续与浓硫酸反应生成SO2,使③中的溴水褪色,通过蔗糖变黑、溴水褪色可以得出浓硫酸具有脱水性、氧化性, B正确, 2014高考试题分析之选择 点评:第13题以基础实验为切入点,考查了元素化合物部分的知识。
四个选项中所涉及的知识均在历年高考试题中出现过。
本题中,有关氯化银和硫化银之间的沉淀转化,浓硫酸使蔗糖炭化脱水的实验等,均为对基础理论知识的考查。2014高考试题分析之必做题26.(13分)
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:实验步骤:
在A中加入4.4 g的异戊醇、6.0 g的乙酸、数滴浓硫酸和
2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)仪器B的名称是 。
(2)在洗涤操作中,第一次水洗的主要目的是 ,
第二次水洗的主要目的是 。
(3)在洗涤、分液操作中,应充分振荡,然后静置, 待分层后
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口 放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出【解析】(1)仪器B是球形冷凝管
(2)主要从物质的溶解性和存在的杂质考虑。
第一次水洗主要是洗掉浓硫酸和过量的乙酸。
第二次水洗则主要是洗去上一步加入的NaHCO3溶液。
(3)乙酸异戊酯密度比水小,它在上层,分液时下层必
须从下口放出,上层液体从上口倒出。所以选d。2014高考试题分析之必做题(4)本实验中加入过量乙酸的目的是 。
(5)实验中加入少量无水MgSO4的目的是 。【解析】
(4)由于乙酸的沸点较低,所以会有较多的
乙酸挥发损耗,加入过量的乙酸可以提
高异戊醇的转化率
(5)无水MgSO4有较快的吸水性,且不与
乙酸异戊酯反应,可以吸收水分,对乙酸
异戊酯进行干燥,便于下一步的蒸馏。 2014高考试题分析之必做题(6)在蒸馏操作中,仪器选择及安装都正确的
是 (填标号)。【解析】(6)a、d的温度计位置错误,
冷凝管应该用直形冷凝管,若用球形冷凝管,冷凝的液体不能全部流下,所以应该选b。2014高考试题分析之必做题(7)本实验的产率是 (填标号)。
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏 (填高或低) 原因 .【解析】
(7)从题目给的数据可以得出乙酸过量,则按异戊醇计算。异戊醇4.4g,为0.05mol,理论上可以生成乙酸异戊酯0.05mol,质量为6.5g。
则产率为:3.9g/6.5g×100%=60%.
(8) 从130 ℃开始收集,会使溶于乙酸异戊酯的异戊醇进入到产品中,所以使产率偏高, 2014高考试题分析之必做题 26、答案及评分标准 2014高考试题分析之必做题 2014高考试题分析之必做题 点评:第26题依然延续了连续三年的实验考查模式。以有机化合物的制备为切入点,考查基本仪器的识别和使用、基本物质的制备原理和制备流程、物质的分离和提纯等内容。
与往年的题目一样,来源于课本必修二的基本实验,稍作改变,难度较小。27.次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。
回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用
于化学镀银。 ①(H3PO2)中,P元素的化合价为 。
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质
的量之比为4︰1,则氧化产物为: (填化学式)。
③NaH2PO2为 (填“正盐”或“酸式盐”),
其溶液显 (填“弱酸性”、“中性”或“弱碱性”)。【解析】(1) 次磷酸一元酸,只发生一步电离,中强酸是弱电解质,电离时要用可逆符号 :
(2)①利用元素化合价代数和为零,得出P元素为+1价
②Ag+是氧化剂,H3PO2做还原剂,二者以4︰1反应,
则4Ag+总共降4价,1H3PO2中的P必须升4价,P元素
变为+5价,生成H3PO4。 ③由于H3PO2是一元酸,所以NaH2PO2是正盐,强碱弱酸盐水解显碱性。 2014高考试题分析之必做题(3)(H3PO2)的工业制法是:将白磷(P4)与Ba(OH)2溶
液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4
反应。写出白磷与Ba(OH)2溶液反应的化学方程式
。【解析】
(3)反应的反应物与产物都已经给出,这是
P元素的歧化反应,注意配平即可: 2014高考试题分析之必做题(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过): ①写出阳极的电极反应式: 。
②分析产品室可得到H3PO2的原因 : .
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”
中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与
产品室之间的阳膜,从而合并了阳极室与产品室。其缺点
是产品中混有 杂质,该杂质产生的原 因是 。 2014高考试题分析之必做题 2014高考试题分析之必做题27、答案及评分标准 2014高考试题分析之必做题 2014高考试题分析之必做题 评价:第27题与往年题目的情景设置有所不同,没有出现工艺流程图,但实际考查的知识没有发生变化,以次磷酸(H3PO2)为载体,考查了弱电解质电离方程式的书写、化合价的确定,氧化还原反应、盐类水解、以及电化学的相关知识
题目形式新颖,但实际上难度在降低,再次体现回归基础。28.乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯 (C2H5OSO3H),再水解生成乙醇。写出相应反应的化学方程式 。解析:
(1)乙烯与硫酸反应生成硫酸氢乙酯发生的是加成
反应,硫酸氢乙酯再水解得到乙醇。 2014高考试题分析之必做题(2)已知:甲醇脱水反应2CH3OH(g)=CH3OCH3(g)+H2O(g)
△H1=-23.9kJ/mol
甲醇制烯烃反应2CH3OH(g)=C2H4 (g)+2H2O(g)
△H2=-29.1kJ/mol
乙醇异构化反应CH3CH2OH(g)=CH3OCH3(g)
△H3=+50.7kJ/mol
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的
△H= kJ/mol。
与间接水合法相比,气相直接水合法的优点是 。解析:(2)考盖斯定律,用方程式①-②-③可得:
△H- △H1 - △H2 - △H3=—45.5KJ/mol
比较两种流程,可看出气相直接水合法减少反应步骤,增大产物的产率,同时减少污染物的排放;而且不用硫酸作反应物,减少对设备的腐蚀。 2014高考试题分析之必做题 2014高考试题分析之必做题 2014高考试题分析之必做题解析: 2014高考试题分析之必做题解析(3)28、答案及评分标准 2014高考试题分析之必做题 2014高考试题分析之必做题 第28题依然是考查化学反应原理的综合试题,重点考查了化学反应热效应、盖斯定律、化学平衡常数的概念以及计算。
试题设置的情景是以学生熟悉的乙醇和乙烯为载体,且测定的数据以图表的形式呈现,要求考生能够利用图表进行数据分析、判断、提取有效信息,突出了运用化学信息的能力的考查。
对这道题目的设计,大家的失分点在于化学平衡常数的计算部分,学生会由于不熟悉此类计算而失分,但实际上计算类型来源于2013年的高考原题新课标Ⅱ的28题。 2014高考试题分析之选做题36.[化学——选修2:化学与技术](15分)
磷矿石主要以磷酸钙[Ca3(PO4)2*H2O]和
磷灰石[Ca5F(PO4)3、Ca5(OH)(PO4)3]等形式存在。
图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。
图(b)是热法磷酸生成过程中由磷灰石制单质磷的流程。回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 %。
(2)以磷灰石为原料,湿法磷酸过程中Ca3F(PO4)3反应的化学方程式为: 。
现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85%的商品磷酸 吨 2014高考试题分析之选做题(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量
焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是:
(填化学式),冷凝塔1的主要沉积物是: .
冷凝塔2的主要沉积物是: 。 2014高考试题分析之选做题(4)尾气中主要含有 ,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去 ;再通入次氯酸钠溶液,可除去 (均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是: 。解析: 2014高考试题分析之选做题36、答案及评分标准 2014高考试题分析之选做题2014高考试题分析之选做题 评价:第36题是工艺流程题,以磷矿石制备磷酸为载体,涉及到基本化学反应在化工生产中的运用,考查基本知识比重较大,注重知识的迁移和综合运用。
我们在复习中应该加大对基础知识的总结,并提高知识的迁移、运用能力。37.[化学—选修3:物质结构与性质] (15分)
早期发现的一种天然二十面体准晶颗粒由三种Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置
序的独特晶体,可通过 方法区分晶体、
准晶体和非晶体。
(2)基态Fe原子有 个未成对电子,
Fe3+的电子排布式为 。
可用硫氰化钾检验Fe3+,形成的配合物的颜色为 。解析: 2014高考试题分析之选做题(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为 ,1mol乙醛分子中含有的σ键的数目为 。
乙酸的沸点明显高于乙醛,其主要原因是 。
Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。解析: 2014高考试题分析之选做题(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g/cm3(不必计算出结果)。解析: 2014高考试题分析之选做题37、答案及评分标准 2014高考试题分析之选做题 2014高考试题分析之选做题 评价:第37题以铝、铁、铜三种金属为载体,考查了晶体与非晶体的区别,原子的核外电子排布、配合物的相关知识、杂化轨道的知识、物质沸点与性质的关系、晶胞密度的相关计算等知识,以基本知识考查为主。
和历年试题比起来,增加了晶体知识的考查,角度较全面,但在计算方面难度有所降低。 2014高考试题分析之选做题 2014高考试题分析之选做题 2014高考试题分析之选做题38(4)F的同分异构体中含有苯环的还有 种(不考虑立体异构),其中核磁共振氢谱为4组峰,且面积比为6:2:2:1的是 (写出其中一种的结构简式)。 2014高考试题分析之选做题解析:38、答案及评分标准 2014高考试题分析之选做题2014高考试题分析之选做题 评价:第38题依然保持以陌生物质入手,考查有机合成的模式。所涉及的知识是有机化学中的基本知识,比如卤代烃的消去反应、苯的硝化反应,有机物化合物结构简式的确定,核磁共振氢谱、同分异构体等等。
命题形式依然延续了去年新课标Ⅰ卷中的形式,由两条线合成一种物质。给出必要的已知信息,而且已知信息中包含未学过的新知识,考查学生学习能力和知识迁移能力;同分异构体的考查、题型难度适中,基本延续去年模式。 2014年的化学试题再次指明了新课标模式下的高考备考方向:
①要回归教材,重视基础。
②重视学习能力、知识的迁移和运用能力
的培养。要学会利用图表进行数据分
析、判断、提取有效信息。
③重视化学学科素养的培养
④重视探究能力和创新思维品质 的培养2015年高考备考指导请多提宝贵意见
谢 谢!
同课章节目录
