【课堂新坐标,同步备课参考】2013-2014学年高中化学(苏教版)必修1综合检测1专题1 化学家眼中的物质世界
文档属性
| 名称 | 【课堂新坐标,同步备课参考】2013-2014学年高中化学(苏教版)必修1综合检测1专题1 化学家眼中的物质世界 |

|
|
| 格式 | zip | ||
| 文件大小 | 106.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-08-04 00:00:00 | ||
图片预览



文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
综合检测(一)
专题1 化学家眼中的物质世界
(时间:60分钟 分值:100分)
一、选择题(本题包括12小题,每小题4分,共计48分)
1.13C—NMR(核磁共振)、15N— ( http: / / www.21cnjy.com )NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtWü Thrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是( )21教育网
A.13C与15N有相同的中子数
B.13C与C60互为同素异形体
C.15N与14N互为同位素
D.15N的核外电子数与中子数相同
【解析】 13C与15N的中子数分别为13-6=7,15-7=8;同素异形体研究的是单质不是核素。
【答案】 C
2.若A+酸―→盐+水,则A不可能属于( )
A.氧化物 B.单质
C.碱 D.电解质
【解析】 本题考查各类物质之间的转化关系。 ( http: / / www.21cnjy.com )碱性氧化物能够和酸反应生成盐和水,如Na2O+2HCl===2NaCl+H2O,A选项符合;一般活泼金属单质能够和酸反应生成盐和氢气,而不能生成水,B选项不符合;碱和酸发生中和反应生成盐和水,如NaOH+HCl===NaCl+H2O,C选项符合;碱性氧化物和碱都属于电解质,所以D选项符合。21·cn·jy·com
【答案】 B
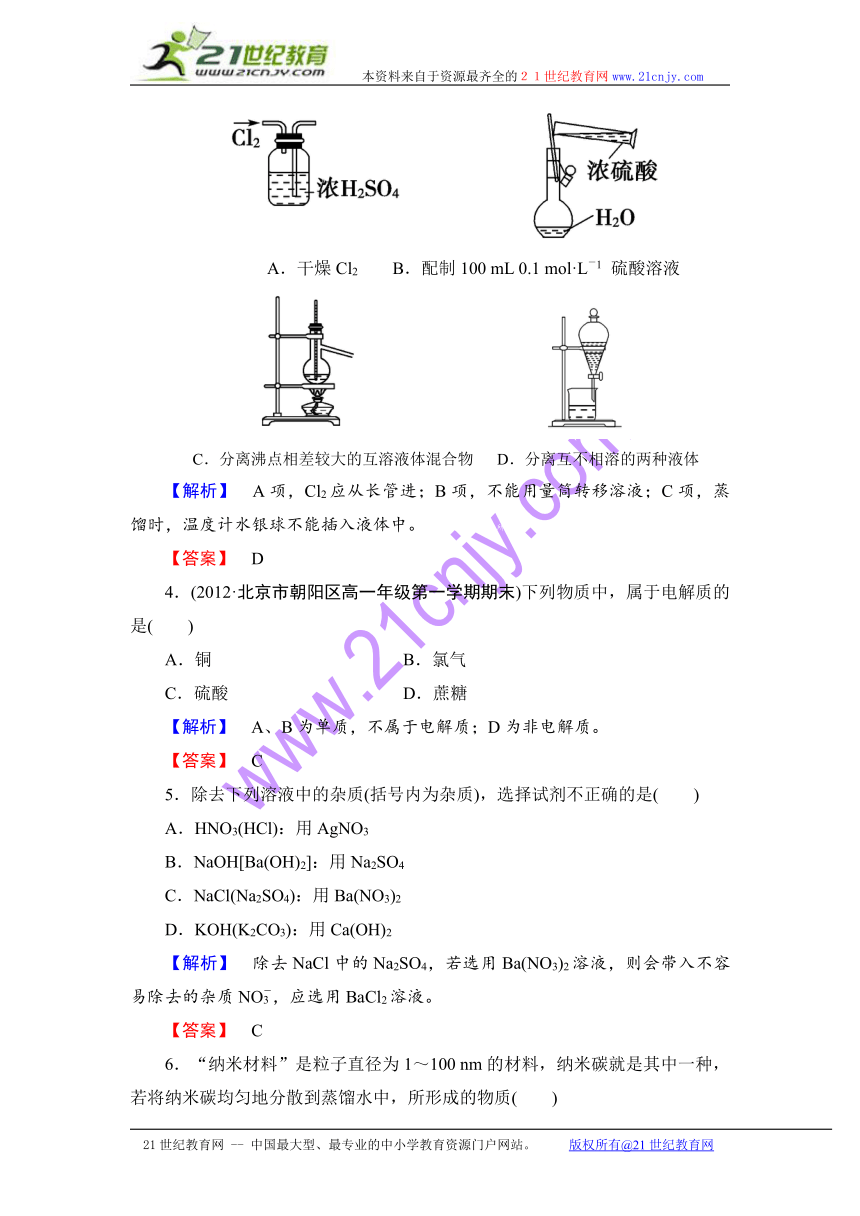
3.(2012·宁波市学年度第一学期期末)下列实验装置图所示的实验操作,正确的是( )
A.干燥Cl2 B.配制100 mL 0.1 mol·L-1 硫酸溶液
C.分离沸点相差较大的互溶液体混合物 D.分离互不相溶的两种液体
【解析】 A项,Cl2应从长管进;B项,不能用量筒转移溶液;C项,蒸馏时,温度计水银球不能插入液体中。21世纪教育网版权所有
【答案】 D
4.(2012·北京市朝阳区高一年级第一学期期末)下列物质中,属于电解质的是( )
A.铜 B.氯气
C.硫酸 D.蔗糖
【解析】 A、B为单质,不属于电解质;D为非电解质。
【答案】 C
5.除去下列溶液中的杂质(括号内为杂质),选择试剂不正确的是( )
A.HNO3(HCl):用AgNO3
B.NaOH[Ba(OH)2]:用Na2SO4
C.NaCl(Na2SO4):用Ba(NO3)2
D.KOH(K2CO3):用Ca(OH)2
【解析】 除去NaCl中的Na2SO4,若选用Ba(NO3)2溶液,则会带入不容易除去的杂质NO,应选用BaCl2溶液。www.21-cn-jy.com
【答案】 C
6.“纳米材料”是粒子直径为1~100 nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )21·世纪*教育网
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
A.①④⑤ B.②③④
C.②③⑤ D.①③④⑥
【解析】 纳米材料的粒子直径的范围和胶体粒 ( http: / / www.21cnjy.com )子直径大小范围相同,故纳米材料纳米碳分散到水中形成的分散系为胶体,能产生丁达尔效应,能透过滤纸,相对较稳定。【版权所有:21教育】
【答案】 B
7.(2012·台州市高一年级期末质量评估)用下图表示的一些物质或概念间的从属关系中正确的是( )21教育名师原创作品
X Y Z
A 雾 胶体 纯净物
B 金属氧化物 碱性氧化物 氧化物
C 碱 电解质 化合物
D 置换反应 氧化还原反应 离子反应
【解析】 胶体属于混合物;有的金属氧化物不是碱性氧化物;氧化还原反应与离子反应为交叉关系,不是从属关系。21cnjy.com
【答案】 C
8.(2012·武汉市江夏区部分中学高一期中联考)下列说法正确的是(NA表示阿伏加德罗常数)( )2·1·c·n·j·y
A.在常温常压下,11.2 升氯气含有的分子数为0.5NA
B.在常温常压下,1摩尔气体含有的原子数为NA
C.32 g氧气所含原子数目为2NA
D.在同温同压下,相同体积的任何气体单质所含原子数目相同
【解析】 A项,该条件下,11.2 L Cl2不是0.5 mol;
B项,气体不一定是单原子分子;
C项,N(O)=×NA=2NA;
D项,不同气体单质分子中含的原子个数不一定相同。
【答案】 C
9.等质量的CuO和MgO ( http: / / www.21cnjy.com )粉末分别溶于相同体积的硝酸中,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为a mol·L-1和b mol·L-1。则a与b的关系为( )
A.a=b B.a=2b
C.2a=b D.a=5b
【解析】 a=,b=,故2a=b。
【答案】 C
10.由硫酸钾、硫酸铝和硫酸组成的混合 ( http: / / www.21cnjy.com )溶液,其中c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c(SO)=0.8 mol·L-1,则c(K+)为( )
A.0.15 mol·L-1 B.0.2 mol·L-1
C.0.3 mol·L-1 D.0.4 mol·L-1
【解析】 根据电荷守恒知,c(K+)=c(SO)×2-c(H+)-c(Al3+)×3=0.3 mol·L-1【来源:21·世纪·教育·网】
【答案】 C
11.某非金属单质A和氧气发生化合 ( http: / / www.21cnjy.com )反应生成B。B为气体,其体积是反应掉氧气体积的两倍(同温同压)。以下对B分子组成的推测一定正确的是( )
A.有1个氧原子 B.有2个氧原子
C.有1个A原子 D.有2个A原子
【解析】 由题意知,B分子数为氧分子数的2倍,由氧元素守恒,则B分子中一定有1个氧原子。
【答案】 A
12.体积为V mL、密度为ρ g ( http: / / www.21cnjy.com )·cm-3的溶液,含有相对分子质量为M的溶质m g,其物质的量浓度为c mol·L-1,溶质的质量分数为W,下列表示式中不正确的是( )www-2-1-cnjy-com
A.c= B.m=
C.W%=% D.c=
【解析】 假设溶液为1 L,则c==,所以:W%=%,或c==。
【答案】 B
二、非选择题(共4小题,共52分)
13.(12分)(2012·台州市高一期末)硫酸是一重要化学试剂。
(1)实验时用18.4 mol·L-1的浓硫 ( http: / / www.21cnjy.com )酸,配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为______。(计算结果精确到小数点后一位)。
(2)下列操作中,容量瓶所具备的功能有______(填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来溶解固体溶质
D.常用来代替量筒量取一定体积的液体
(3)在下列配制过程示意图中,有错误的是(填写序号)______。
(4)下列说法正确的______。
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
【解析】 (1)根据稀释定律可知,
18.4 mol·L-1×V=1 mol·L-1×100 mL,
V=5.4 mL。
(2)容量瓶不能用来溶解且不能长期贮存溶液,容量瓶只有一个刻度,不能代替量筒使用。
(3)浓H2SO4稀释时应将浓H2SO4注入水中;定容应平视。
(4)转移前未冷却,所配浓度偏高;查漏时,应旋转180 ℃再倒置检查。
【答案】 (1)5.4 mL (2)A (3)①④ (4)AC
14.(12分)(2012·浙江宁波期末)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:2-1-c-n-j-y
( http: / / www.21cnjy.com )
已知:四氯化碳沸点是76.8 ℃,碘单质的沸点是184.35 ℃。
请填写下列空白:
(1)步骤③的实验操作名称 ( http: / / www.21cnjy.com )是______;步骤⑥的目的是从含碘四氯化碳溶液中分离出单质碘和回收四氯化碳,该步骤的实验操作名称是______。
(2)步骤③操作所需的玻璃仪器有烧杯____、____;
步骤⑤操作所需的玻璃仪器主要是________。
(3)步骤⑤中,某学生选择用四氯化碳来提取碘的理由是
__________________________________________________________。
(4)检验提取碘后的水溶液中是否还含有单质碘,可选用的试剂是______。
【解析】 (1)悬浊液得到溶液,需过滤;碘和CCl4的沸点不同,分离需用蒸馏。
(2)过滤所用玻璃仪器有烧杯、漏斗、玻璃棒,萃取分液主要用分液漏斗。
(3)CCl4与水不互溶,且I2在CCl4中溶解度比在水中大的多。
(4)I2可用淀粉检验。
【答案】 (1)过滤 蒸馏
(2)漏斗、玻璃棒 分液漏斗
(3)四氯化碳与水互不相溶;碘在四氯化碳中的溶解度比在水中大
(4)淀粉试液
15.(16分)(201 ( http: / / www.21cnjy.com )2·宁波市第一学期期末)有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的1/2,乙元素原子核内无中子,丙元素原子核内有8个质子。 21*cnjy*com
(1)写出丙元素的元素符号________,画出丙的原子结构示意图________;
(2)写出乙元素的三种核素符号分别为__________、________、________;
(3)乙、丙两种元素形成的化合物有________。(填化学式)
(4)写出甲、乙、丙三种元素组成的化合 ( http: / / www.21cnjy.com )物在水中的电离方程式__________________________________________________________。
(5)画出甲元素的离子结构示意图______。
【解析】 由题意知甲为Na ,乙为H,丙为O。H元素有三种核素H、H(或D)、H(或T)。【出处:21教育名师】
【答案】 (1)O
(2)H、H(或D)、H(或T)
(3)H2O、H2O2
(4)NaOH===Na++OH-
(5)
16.(12分)(2012·武汉市江夏 ( http: / / www.21cnjy.com )区部分中学高一期中联考)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则:【来源:21cnj*y.co*m】
(1)该气体在标准状况下的体积为________L。
(2)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为________。
(3)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_____mol·L-1。
(4)该气体在标准状况下的密度为________g·L-1。
【解析】 (1)V=×22.4 L
(2)w=×100%
(3)c==mol·L-1
(4)ρ= g·L-1
【答案】 (1) (2)×100%
(3) (4)
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
综合检测(一)
专题1 化学家眼中的物质世界
(时间:60分钟 分值:100分)
一、选择题(本题包括12小题,每小题4分,共计48分)
1.13C—NMR(核磁共振)、15N— ( http: / / www.21cnjy.com )NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtWü Thrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是( )21教育网
A.13C与15N有相同的中子数
B.13C与C60互为同素异形体
C.15N与14N互为同位素
D.15N的核外电子数与中子数相同
【解析】 13C与15N的中子数分别为13-6=7,15-7=8;同素异形体研究的是单质不是核素。
【答案】 C
2.若A+酸―→盐+水,则A不可能属于( )
A.氧化物 B.单质
C.碱 D.电解质
【解析】 本题考查各类物质之间的转化关系。 ( http: / / www.21cnjy.com )碱性氧化物能够和酸反应生成盐和水,如Na2O+2HCl===2NaCl+H2O,A选项符合;一般活泼金属单质能够和酸反应生成盐和氢气,而不能生成水,B选项不符合;碱和酸发生中和反应生成盐和水,如NaOH+HCl===NaCl+H2O,C选项符合;碱性氧化物和碱都属于电解质,所以D选项符合。21·cn·jy·com
【答案】 B
3.(2012·宁波市学年度第一学期期末)下列实验装置图所示的实验操作,正确的是( )
A.干燥Cl2 B.配制100 mL 0.1 mol·L-1 硫酸溶液
C.分离沸点相差较大的互溶液体混合物 D.分离互不相溶的两种液体
【解析】 A项,Cl2应从长管进;B项,不能用量筒转移溶液;C项,蒸馏时,温度计水银球不能插入液体中。21世纪教育网版权所有
【答案】 D
4.(2012·北京市朝阳区高一年级第一学期期末)下列物质中,属于电解质的是( )
A.铜 B.氯气
C.硫酸 D.蔗糖
【解析】 A、B为单质,不属于电解质;D为非电解质。
【答案】 C
5.除去下列溶液中的杂质(括号内为杂质),选择试剂不正确的是( )
A.HNO3(HCl):用AgNO3
B.NaOH[Ba(OH)2]:用Na2SO4
C.NaCl(Na2SO4):用Ba(NO3)2
D.KOH(K2CO3):用Ca(OH)2
【解析】 除去NaCl中的Na2SO4,若选用Ba(NO3)2溶液,则会带入不容易除去的杂质NO,应选用BaCl2溶液。www.21-cn-jy.com
【答案】 C
6.“纳米材料”是粒子直径为1~100 nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )21·世纪*教育网
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
A.①④⑤ B.②③④
C.②③⑤ D.①③④⑥
【解析】 纳米材料的粒子直径的范围和胶体粒 ( http: / / www.21cnjy.com )子直径大小范围相同,故纳米材料纳米碳分散到水中形成的分散系为胶体,能产生丁达尔效应,能透过滤纸,相对较稳定。【版权所有:21教育】
【答案】 B
7.(2012·台州市高一年级期末质量评估)用下图表示的一些物质或概念间的从属关系中正确的是( )21教育名师原创作品
X Y Z
A 雾 胶体 纯净物
B 金属氧化物 碱性氧化物 氧化物
C 碱 电解质 化合物
D 置换反应 氧化还原反应 离子反应
【解析】 胶体属于混合物;有的金属氧化物不是碱性氧化物;氧化还原反应与离子反应为交叉关系,不是从属关系。21cnjy.com
【答案】 C
8.(2012·武汉市江夏区部分中学高一期中联考)下列说法正确的是(NA表示阿伏加德罗常数)( )2·1·c·n·j·y
A.在常温常压下,11.2 升氯气含有的分子数为0.5NA
B.在常温常压下,1摩尔气体含有的原子数为NA
C.32 g氧气所含原子数目为2NA
D.在同温同压下,相同体积的任何气体单质所含原子数目相同
【解析】 A项,该条件下,11.2 L Cl2不是0.5 mol;
B项,气体不一定是单原子分子;
C项,N(O)=×NA=2NA;
D项,不同气体单质分子中含的原子个数不一定相同。
【答案】 C
9.等质量的CuO和MgO ( http: / / www.21cnjy.com )粉末分别溶于相同体积的硝酸中,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为a mol·L-1和b mol·L-1。则a与b的关系为( )
A.a=b B.a=2b
C.2a=b D.a=5b
【解析】 a=,b=,故2a=b。
【答案】 C
10.由硫酸钾、硫酸铝和硫酸组成的混合 ( http: / / www.21cnjy.com )溶液,其中c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c(SO)=0.8 mol·L-1,则c(K+)为( )
A.0.15 mol·L-1 B.0.2 mol·L-1
C.0.3 mol·L-1 D.0.4 mol·L-1
【解析】 根据电荷守恒知,c(K+)=c(SO)×2-c(H+)-c(Al3+)×3=0.3 mol·L-1【来源:21·世纪·教育·网】
【答案】 C
11.某非金属单质A和氧气发生化合 ( http: / / www.21cnjy.com )反应生成B。B为气体,其体积是反应掉氧气体积的两倍(同温同压)。以下对B分子组成的推测一定正确的是( )
A.有1个氧原子 B.有2个氧原子
C.有1个A原子 D.有2个A原子
【解析】 由题意知,B分子数为氧分子数的2倍,由氧元素守恒,则B分子中一定有1个氧原子。
【答案】 A
12.体积为V mL、密度为ρ g ( http: / / www.21cnjy.com )·cm-3的溶液,含有相对分子质量为M的溶质m g,其物质的量浓度为c mol·L-1,溶质的质量分数为W,下列表示式中不正确的是( )www-2-1-cnjy-com
A.c= B.m=
C.W%=% D.c=
【解析】 假设溶液为1 L,则c==,所以:W%=%,或c==。
【答案】 B
二、非选择题(共4小题,共52分)
13.(12分)(2012·台州市高一期末)硫酸是一重要化学试剂。
(1)实验时用18.4 mol·L-1的浓硫 ( http: / / www.21cnjy.com )酸,配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为______。(计算结果精确到小数点后一位)。
(2)下列操作中,容量瓶所具备的功能有______(填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来溶解固体溶质
D.常用来代替量筒量取一定体积的液体
(3)在下列配制过程示意图中,有错误的是(填写序号)______。
(4)下列说法正确的______。
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
【解析】 (1)根据稀释定律可知,
18.4 mol·L-1×V=1 mol·L-1×100 mL,
V=5.4 mL。
(2)容量瓶不能用来溶解且不能长期贮存溶液,容量瓶只有一个刻度,不能代替量筒使用。
(3)浓H2SO4稀释时应将浓H2SO4注入水中;定容应平视。
(4)转移前未冷却,所配浓度偏高;查漏时,应旋转180 ℃再倒置检查。
【答案】 (1)5.4 mL (2)A (3)①④ (4)AC
14.(12分)(2012·浙江宁波期末)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:2-1-c-n-j-y
( http: / / www.21cnjy.com )
已知:四氯化碳沸点是76.8 ℃,碘单质的沸点是184.35 ℃。
请填写下列空白:
(1)步骤③的实验操作名称 ( http: / / www.21cnjy.com )是______;步骤⑥的目的是从含碘四氯化碳溶液中分离出单质碘和回收四氯化碳,该步骤的实验操作名称是______。
(2)步骤③操作所需的玻璃仪器有烧杯____、____;
步骤⑤操作所需的玻璃仪器主要是________。
(3)步骤⑤中,某学生选择用四氯化碳来提取碘的理由是
__________________________________________________________。
(4)检验提取碘后的水溶液中是否还含有单质碘,可选用的试剂是______。
【解析】 (1)悬浊液得到溶液,需过滤;碘和CCl4的沸点不同,分离需用蒸馏。
(2)过滤所用玻璃仪器有烧杯、漏斗、玻璃棒,萃取分液主要用分液漏斗。
(3)CCl4与水不互溶,且I2在CCl4中溶解度比在水中大的多。
(4)I2可用淀粉检验。
【答案】 (1)过滤 蒸馏
(2)漏斗、玻璃棒 分液漏斗
(3)四氯化碳与水互不相溶;碘在四氯化碳中的溶解度比在水中大
(4)淀粉试液
15.(16分)(201 ( http: / / www.21cnjy.com )2·宁波市第一学期期末)有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的1/2,乙元素原子核内无中子,丙元素原子核内有8个质子。 21*cnjy*com
(1)写出丙元素的元素符号________,画出丙的原子结构示意图________;
(2)写出乙元素的三种核素符号分别为__________、________、________;
(3)乙、丙两种元素形成的化合物有________。(填化学式)
(4)写出甲、乙、丙三种元素组成的化合 ( http: / / www.21cnjy.com )物在水中的电离方程式__________________________________________________________。
(5)画出甲元素的离子结构示意图______。
【解析】 由题意知甲为Na ,乙为H,丙为O。H元素有三种核素H、H(或D)、H(或T)。【出处:21教育名师】
【答案】 (1)O
(2)H、H(或D)、H(或T)
(3)H2O、H2O2
(4)NaOH===Na++OH-
(5)
16.(12分)(2012·武汉市江夏 ( http: / / www.21cnjy.com )区部分中学高一期中联考)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则:【来源:21cnj*y.co*m】
(1)该气体在标准状况下的体积为________L。
(2)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为________。
(3)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_____mol·L-1。
(4)该气体在标准状况下的密度为________g·L-1。
【解析】 (1)V=×22.4 L
(2)w=×100%
(3)c==mol·L-1
(4)ρ= g·L-1
【答案】 (1) (2)×100%
(3) (4)
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
