5.3.1 无机非金属材料 课件(共108张PPT)-高中化学 人教版(2019) 必修二
文档属性
| 名称 | 5.3.1 无机非金属材料 课件(共108张PPT)-高中化学 人教版(2019) 必修二 |  | |
| 格式 | pptx | ||
| 文件大小 | 23.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-23 15:32:15 | ||
图片预览











文档简介
(共108张PPT)
第五章
化工生产中的重要非金属元素
第三节
无机非金属材料
[明确学习目标]
1.知道常见的硅酸盐材料玻璃、水泥、陶瓷及生产它们的主要原料。
2.了解高纯硅的制备原理。知道硅和二氧化硅的用途。
3.知道一些新型无机非金属材料如硅和二氧化硅、新型陶瓷和碳纳米材料等。
[核心素养对接]
1.通过对硅酸盐结构的了解培养学生宏观辨识与微观探析的能力。
2.通过对几种重要无机非金属材料生产及用途的学习,提高学生科学精神与社会责任。
课前篇
·
自主学习固基础
一、硅酸盐材料
[知识梳理]
1.硅酸盐
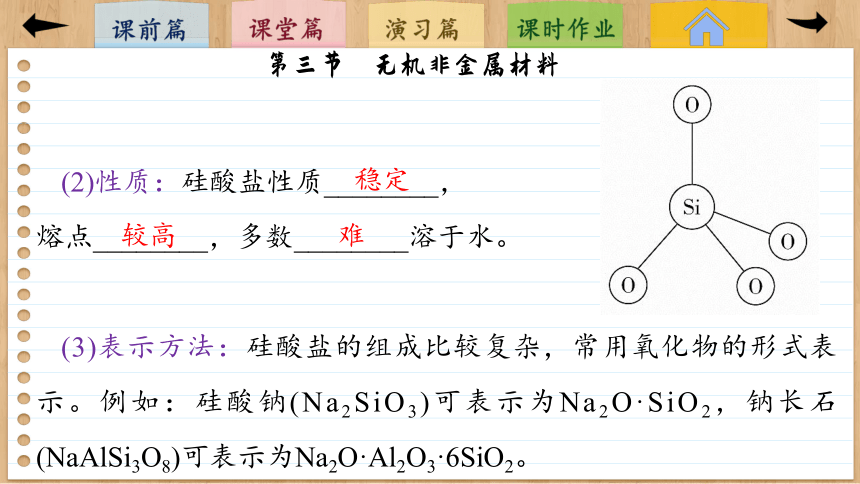
(1)结构:在硅酸盐中,Si和O构成了硅氧四面体,即以硅原子为中心,氧原子在四面体的4个顶角(如图所示),许多这样的四面体还可以通过顶角的O相连接,即每个Si与周围4个O结合,每个O与2个Si结合。硅氧四面体结构的特殊性,决定了硅酸盐材料的特殊性质。
(2)性质:硅酸盐性质________,
熔点________,多数________溶于水。
(3)表示方法:硅酸盐的组成比较复杂,常用氧化物的形式表示。例如:硅酸钠(Na2SiO3)可表示为Na2O·SiO2,钠长石(NaAlSi3O8)可表示为Na2O·Al2O3·6SiO2。
稳定
较高
难
(4) 最简单的硅酸盐——Na2SiO3
易
水玻璃
SiO32-+2H+===H2SiO3↓
2CO2+SiO32-+2H2O ===2HCO3-+H2SiO3↓
防火剂
2.传统的无机非金属材料——硅酸盐产品
玻璃 水泥 陶瓷
主要原料 ________、石灰石、________ ________、黏土 ________
主要设备 ________ ______________ 陶瓷窑
主要反应 __________________ __________________、 ________________ — —
纯碱
石英砂
石灰石
黏土
玻璃窑
水泥回转窑
SiO2+Na2CO3====Na2SiO3+CO2↑
高温
SiO2+CaCO3 ===== CaSiO3+CO2↑
高温
主要成分 普通玻璃 ________、________、 ________ ______________ 硅酸盐
Na2SiO3
CaSiO3
SiO2
硅酸三钙(3CaO·SiO2)、
硅酸二钙(2CaO·SiO2)、
铝酸三钙(3CaO·Al2O3)
二、新型无机非金属材料
1.硅和二氧化硅
(1)硅晶片是生产________的基础,属于________材料,是因为硅元素位于元素周期表第________周期,第________族,单质的导电性介于________和________之间。高纯硅广泛用于信息技术和新能源技术领域。
芯片
半导体
三
ⅣA
导体
绝缘体
(2)工业上制备高纯硅
①硅元素的存在:全部以化合态存在,主要以_________和氧化物(如水晶、玛瑙)形式存在。
②生产流程:石英砂——————→粗硅———→SiHCl3
———→高纯硅。
焦炭
1 800~2 000 ℃
HCl
300 ℃
H2
1 100 ℃
硅酸盐
写出其中涉及的主要化学反应的化学方程式:
___________________________________________________;
___________________________________________________;
___________________________________________________。
(3)光导纤维的生产需要________,优点:通信容量大,抗干扰性能好,传输信号不易衰减。
SiO2+2C ============ Si+2CO↑
1 800~2 000 ℃
Si+3HCl ======== SiHCl3+H2
300 ℃
SiHCl3+H2 ========= Si+3HCl
1 100 ℃
SiO2
[自我排查]
1.单质硅在常温下化学性质稳定,所以硅在自然界中以游离态存在,这种说法是否正确?为什么?
________________________________________________________________________________________________________________________________________________________
尝试解答
提示:不正确。硅属于亲氧元素,虽然在常温下稳定,但在漫长的地质年代中,硅元素和氧结合在一起,都以化合态存在,主要以二氧化硅及硅酸盐的形式存在。
2.实验室中盛放碱液的试剂瓶为什么用橡胶塞而不用磨口玻璃塞?
________________________________________________________________________________________________________________________________________________
提示:玻璃中含有SiO2,SiO2与碱反应生成具有黏合作用的硅酸盐,使瓶口和瓶塞黏结在一起而难以开启
课堂篇
·
重点难点要突破
研习1 硅、二氧化硅、硅酸盐
[重点讲解]
硅酸盐由于组成比较复杂,通常用氧化物的形式表示其组成,改写时的规律为:
(1)顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水;氧化物之间以“·”隔开。
一、硅酸盐氧化物形式的书写
(2)原则:各元素原子总个数比符合原来的组成,若出现分数应化为整数。
例如:钠长石(NaAlSi3O8)不能写成12Na2O·12Al2O3·3SiO2,应写成Na2O·Al2O3·6SiO2。
(3)各元素的化合价不能改变。
1.硅元素的存在
二、硅、二氧化硅
2.硅单质
(1)物理性质:熔点高、硬度大、不溶于水。
(2)化学性质
①常温下能与氟气、氢氟酸、强碱等反应。
Si+2F2===SiF4
Si+4HF===SiF4↑+2H2↑
Si+2NaOH+H2O===Na2SiO3+2H2↑
(Si+2NaOH+4H4e-2O===Na2SiO3+3H2O+2H2↑)
[特别提醒]
能与NaOH溶液反应的单质:Al、Si、S(加热)、Cl2。
② 加热时能与氧气、氯气、碳等反应。
Si+O2=====SiO2
Si+2Cl2=====SiCl4
Si+C=====SiC
△
△
高温
(3) 用途:半导体材料、芯片、太阳能电池。
3.二氧化硅
(1)存在
SiO2存在形态有结晶形和无定形两大类,统称硅石。石英、水晶、玛瑙、沙子、光导纤维的主要成分均是SiO2。
(2)结构
SiO2晶体是由Si和O按原子数之比为1∶2的比例组成的正四面体结构的晶体。每个硅原子周围结合4个O原子,每个O原子周围结合2个Si原子。
(3) 物理性质
熔点高,硬度大,不溶于水。
(4) 化学性质
(5)用途
①沙子是基本的建筑材料。
②纯净的SiO2是现代光学及光纤制品的基本材料,可以制作光导纤维。
③水晶和玛瑙用来制作饰物和工艺品。
④实验室中使用的石英坩埚。
4. 硅及其氧化物的特性
物质 一般规律 硅及其氧化物的特性
Si 硅的还原性比碳强 SiO2+2CSi+2CO↑
非金属单质与强碱反应一般不生成氢气 Si+2NaOH+H2O===Na2SiO3+2H2↑
非金属单质一般不与非氧化性酸反应 Si+4HF===SiF4↑+2H2↑
一般非金属单质为绝缘体 硅为半导体
物质 一般规律 硅及其氧化物的特性
SiO2 酸性氧化物一般与水反应生成相应的酸 SiO2不溶于水,也不与水反应
酸性氧化物一般不与酸发生复分解反应 SiO2+4HF===SiF4↑+2H2O
“较强酸制较弱酸”是复分解反应的一般规律,碳酸酸性大于硅酸 Na2SiO3+CO2(少量)+H2O===H2SiO3↓+Na2CO3,但在高温下Na2CO3+SiO2Na2SiO3+CO2↑
[联想质疑]
2018年3月5日,中国22岁的青年学者曹原在《自然》连刊两文介绍石墨烯超导重大发现,当将两层平行石墨烯堆成约1.1°的微妙角度,就会产生神奇的超导效应。2018年12月,《自然》杂志发布了2018年度影响世界的十大科学人物排行榜,曹原名列榜首。
石墨烯是一种由碳原子构成的六角型二维碳纳米材料,具有超高硬度、强度和导热系数等特性。
[问题探讨]
1.碳和硅的最外层电子数都是4,且碳元素的非金属性强于硅,但碳在自然界中有稳定的单质(如金刚石、石墨),而硅却没有,其原因是什么?
提示:硅是一种亲氧元素,硅与氧形成硅氧四面体的稳定结构,故自然界中无游离态的硅,而是以二氧化硅和硅酸盐的形式存在于自然界中。
2.工业上用焦炭和石英砂在高温下制备粗硅时,为什么要隔绝空气?写出工业上制备粗硅的化学方程式。
提示:因为高温下焦炭和空气中的O2发生反应,故制取粗硅时要隔绝空气,工业制取粗硅的化学方程式为
SiO2+2=======Si+2CO↑。
高温
3.已知:SiO2+4HF===SiF4↑+2H2O,SiO2既能与NaOH溶液发生反应,又能与氢氟酸发生反应,因此,SiO2属于两性氧化物,这种说法正确吗?
提示:不正确;SiO2尽管能与氢氟酸反应,但与其他强酸(如HCl、HNO3等)不反应,故SiO2不属于两性氧化物,属于酸性氧化物。
4.你知道的碳纳米材料有哪些?碳化硅陶瓷是传统无机非金属材料还是新型无机非金属材料?
提示:碳纳米材料主要有富勒烯、碳纳米管、石墨烯等。碳化硅陶瓷属于新型无机非金属材料。
[举一反三]
1.用氧化物的形式表示硅酸盐的组成,其中正确的是( )
A.钙沸石[Ca(Al2Si3O10)·3H2O]表示为Al2O3·CaO·3SiO2·3H2O
B.镁橄榄石(Mg2SiO4)表示为MgO·SiO2
C.钾云母(K2Al6Si6H4O24)表示为K2O·2H2O·3Al2O3·6SiO2
D.硅酸铜钡(BaCuSi2O6)表示为BaO·CuO·2SiO2
D
解析:A项,Ca(Al2Si3O10)·3H2O应改为CaO·Al2O3·3SiO2·3H2O
(排序错);B项,Mg2SiO4应改为2MgO·SiO2(不能在化学计量数中出现分数);C项,K2Al6Si6H4O24应改为K2O·3Al2O3·6SiO2·2H2O
(排序错)。
2.将过量的CO2分别通入:①CaCl2溶液;②浓Na2SiO3溶液;③Ca(OH)2溶液;④饱和Na2CO3溶液。最终溶液中有白色沉淀析出的是( )
A.①②③④ B.②④
C.①②③ D.②③
B
解析:CO2溶于水:CO2+H2O====H2CO3,H2CO3的酸性比盐酸弱,而比硅酸强。根据酸与盐反应的规律,CO2通入CaCl2溶液无明显现象;过量的CO2通入浓Na2SiO3溶液中有白色沉淀H2SiO3生成;CO2通入Ca(OH)2溶液中至过量,Ca(OH)2+CO2===CaCO3↓+H2O, CaCO3+H2O+CO2===Ca(HCO3)2,最终生成Ca(HCO3)2而无沉淀;过量CO2通入饱和Na2CO3溶液中:Na2CO3+H2O+CO2===2NaHCO3↓,生成的NaHCO3溶解度比Na2CO3溶解度小而析出结晶。
3.下列关于硅单质及其化合物的说法正确的是( )
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料
A.①② B.②③
C.①④ D.③④
C
解析:许多岩石和矿物中含有硅元素,①正确;水晶的主要成分是二氧化硅,所以水晶不是硅酸盐制品,②错误;光导纤维是由高纯度的二氧化硅制成的,③错误;陶瓷属于硅酸盐制品,④正确。
4.(双选)用石英砂制取高纯硅的主要化学反应如下:
①SiO2+2C=====Si(粗)+2CO↑
②Si(粗)+2Cl2=====SiCl4
③SiCl4+2H2=====Si(纯)+4HCl
高温
△
高温
关于上述反应的叙述不正确的是( )
A.①③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均弱于硅
C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子
D.高温下在炉子里将石英砂、焦炭、氯气、氢气按比例混合就能得到高纯硅
BD
解析:在氧化还原反应中,还原剂的还原性比还原产物的还原性强,B错误;根据元素化合价的变化,每消耗或生成28 g(1 mol)硅,均转移4 mol电子,C正确;题中的三个反应是在三个不同的反应器中发生的,D错误。
5.矿泉水一般是由岩石风化后,被地下水溶解其中的可溶部分生成的,此处所指的风化作用是指矿物与水和CO2同时作用的过程。例如钾长石(KAlSi3O8)风化生成高岭土[Al2Si2O5(OH)4],此反应的离子方程式为
2KAlSi3O8+2H2CO3+5H2O===2K++2HCO3-+4H2SiO3+Al2Si2O5(OH)4
(1) 将上述复杂硅酸盐改写成氧化物形式。
①KAlSi3O8______________________________。
②Al2Si2O5(OH)4______________________________。
(2)上述反应能够发生的原因是__________________________
_________________。
2KAlSi3O8+2H2CO3+5H2O===2K++2HCO3-+4H2SiO3+Al2Si2O5(OH)4
K2O·Al2O3·6SiO2
Al2O3·2SiO2·2H2O
H2CO3的酸性比H2SiO3强
解析:(1)将硅酸盐化学式写成氧化物形式时,需将氧以外的元素写成同价态的氧化物,并按活动性顺序排列,用“·”将它们连接起来,各种元素原子个数比符合原来的组成。
(2)此反应属于酸与盐发生的复分解反应,能发生的原因是酸性:H2CO3>H2SiO3。
演习篇
·
学业测试速达标
1.下列关于无机非金属材料的说法不正确的是( )
A.传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料克服了传统无机非金属材料的缺点,具有极大强度
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
D
解析:新型无机非金属材料不但克服了传统无机非金属材料易碎、强度不够等缺点,并且具有特殊结构、特殊功能;新型无机非金属材料的主要成分并不一定是硅酸盐,如氮化硅陶瓷、碳化硅陶瓷等。
2.在①浓硝酸、②水、③盐酸、④氢氟酸、⑤氢氧化钾溶液中,常温时能与二氧化硅起化学反应的有( )
A.①② B.②④
C.④⑤ D.③④
C
3.昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用二氧化硅和金属氧化物的形式可表示为( )
A.CaO·MgO·SiO2·H2O
B.2CaO·5MgO·8SiO2·H2O
C.2CaO·MgO·SiO2·2H2O
D.5CaO·2MgO·8SiO2·H2O
B
解析:根据昆仑玉的化学式,将Ca、Mg、Si、H分别写成氧化物的形式,按较活泼金属氧化物→较不活泼金属氧化物→SiO2→H2O的顺序排列,再调整各氧化物前的化学计量数并使其与昆仑玉化学式中一致,可得昆仑玉氧化物表示形式为2CaO·5MgO·8SiO2·H2O。
4.下列说法正确的是( )
A.CO2+H2O+Na2SiO3===H2SiO3↓+Na2CO3,说明酸性:H2CO3>H2SiO3
B.SiO2+Na2CO3=====Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
C.在复分解反应中必须是酸性强的生成酸性弱的
D.已知酸性:H2CO3>HClO>HCO3-,则CO2+H2O+2NaClO===Na2CO3+2HClO
A
高温
解析:由于H2CO3能与Na2SiO3反应生成H2SiO3,则说明H2CO3酸性大于H2SiO3,A正确;在B项中,由于在高温条件下反应,CO2为气体逸出,不能比较酸性强弱;在C项中,H2S+CuSO4===CuS↓+H2SO4,此反应为弱酸生成强酸;在D项中由于酸性:HClO>HCO3-,产物应为NaHCO3。
5.(双选)高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
下列说法正确的是( )
A.步骤①的化学方程式为SiO2+2C ===== Si+2CO↑
B.步骤①②③中每生成或反应1 mol Si,转移4 mol电子
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏(或分馏)可提纯SiHCl3
高温
AD
解析:A项,产物为CO,正确;B项,第②、③步中转移2 mol电子,错误;C项,硅可与氢氟酸反应生成四氟化硅和氢气,错误;D项,根据物质的沸点不同可用蒸馏的方法进行分离,正确。
6.某研究性学习小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si;
②Mg在点燃的条件下按质量比8∶5与SiO2反应生成一种白色固体化合物和另一种硅化物;
③金属硅化物与稀硫酸反应生成硫酸盐与SiH4;
④Si和SiO2均不能与稀H2SO4反应;
⑤SiH4在空气中自燃。
他们的研究报告中记载着“……选用合适的物质在适合的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量……用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期的63%左右。”请回答下列问题:
(1) 该小组“实验室制Si”的化学反应方程式是
____________________________________。
(2) 写出②的反应方程式:_______________________________。
2C+SiO2=====Si+2CO↑
高温
SiO2+4Mg=====2MgO+Mg2Si
点燃
(3)该过程中产率比预期低的原因是_______________________
______________________________________。
(4)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是什么?请用必要的文字和化学方程式予以说明:
_______________________________________________________________________________________。
部分硅与镁反应生成了硅化镁
SiH4能自燃,而有爆鸣声和火花就是由SiH4的自燃引起的,SiH4+2O2===SiO2+2H2O
解析:(1)碳可以在高温下还原SiO2制得Si。反应的化学方程式为2C+SiO2 ====== Si+2CO↑。
(2)Mg与SiO2反应类似于Mg与CO2的反应,先生成MgO和Si,Si再和Mg反应生成Mg2Si,故可生成MgO和Mg2Si。
高温
课时作业(七)
无机非金属材料
A篇·知识对点训练
1.下列物质中,不含有硅酸盐的是( )
A.水玻璃 B.硅芯片
C.黏土 D.普通水泥
B
解析:水玻璃是Na2SiO3的水溶液,黏土和普通水泥的主要成分都是硅酸盐,硅芯片的主要成分是硅单质。
2.下列说法错误的是( )
A.二氧化硅是光导纤维的主要原料
B.硅是信息技术的关键材料
C.陶瓷餐具所用材料为硅酸盐
D.水晶镜片所用原料为硅酸盐
D
解析:水晶、光导纤维的主要成分为SiO2。Si用于信息产业及太阳能电池。传统硅酸盐材料是陶瓷、水泥、玻璃。
3.下列有关硅及其化合物的说法正确的是( )
A.陶瓷、玻璃、水泥容器都能贮存氢氟酸
B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在具有磨口玻璃塞的试剂瓶中
C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2
D.由Na2CO3+SiO2=====CO2↑+Na2SiO3可知,硅酸的酸性强于碳酸
C
高温
解析:陶瓷、玻璃、水泥的主要成分都是硅酸盐,其含有的SiO2能与氢氟酸反应,A项错误;硅酸钠是一种黏合剂,能将玻璃塞和瓶体粘在一起,不便于打开,B项错误;D项中的反应能发生是因为生成的CO2气体不断逸出,不能说明硅酸的酸性强于碳酸。
4.下列说法正确的是( )
A.石英玻璃、玛瑙、水泥和餐桌上的瓷盘都是硅酸盐制品
B.红宝石、珍珠、水晶、钻石等装饰品的主要成分都是硅酸盐
C.氢氟酸能够雕刻玻璃
D.硅酸具有酸的通性,能使石蕊溶液变红
C
解析:石英玻璃、玛瑙的成分是SiO2,不属于硅酸盐,A不正确;红宝石的主要成分为三氧化二铝、珍珠的主要成分为CaCO3、水晶的主要成分为SiO2、钻石为碳单质,均不属于硅酸盐,B不正确;氢氟酸能与玻璃的成分之一SiO2发生反应:4HF+SiO2===SiF4↑+2H2O,C正确;硅酸具有酸的通性,例如能与碱反应,但其难溶于水,不能使石蕊溶液变色,D错。
5.制取下列物质不需要用石灰石作原料的是( )
A.硅酸 B.水泥
C.玻璃 D.生石灰
A
解析:硅酸由可溶性硅酸盐与酸反应制得。
6.下列关于无机非金属材料的说法中,不正确的是( )
A.高纯硅可用于制造半导体材料
B.氧化铝陶瓷属于新型无机非金属材料,它是生物陶瓷
C.氮化硅陶瓷属于新型无机非金属材料,可用于制造陶瓷发动机的受热面
D.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
D
解析:光导纤维不具有导电性,D不正确。
7.下列关于SiO2和CO2的说法中,不正确的是( )
A.CO2和SiO2都能与碱及碱性氧化物反应
B.CO2和SiO2都能与水反应生成相应的酸
C.CO2和SiO2都能与焦炭反应生成CO
D.SiO2可用于制光导纤维,干冰可用于人工降雨
B
解析:CO2能与水反应生成碳酸,但SiO2不能与水反应生成相应的酸,B错误。
8.二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等方面有着重要的用途。a~e是对①~⑤反应中SiO2所表现的化学性质或作用进行的判断,其中正确的是( )
①SiO2+2NaOH===Na2SiO3+H2O
②SiO2+2C ===== Si+2CO↑
③SiO2+4HF===SiF4↑+2H2O
④Na2CO3+SiO2======Na2SiO3+CO2↑
高温
高温
⑤SiO2+3C=======SiC+2CO↑
a.反应①中SiO2作为玻璃的成分被消耗,用于刻蚀玻璃
b.反应②中SiO2表现出氧化性
c.反应③中SiO2表现了酸性氧化物的通性
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的道理
e.反应⑤中SiO2未参加氧化还原反应
A.ace B.bde C.cde D.ab
高温
解析:通常用氢氟酸来刻蚀玻璃,与之对应的反应是③,因此a、c判断错误;反应②是一个置换反应,其中二氧化硅被还原,表现出氧化性,b判断正确;反应④是一个复分解反应,用难挥发的二氧化硅制取易挥发的二氧化碳,d判断正确;反应⑤中碳的化合价由0价变为-4和+2价,硅的化合价和氧的化合价都没有改变,因此二氧化硅没有参加氧化还原反应,e判断也正确。
9.二氧化硅气凝胶是一种世界上最轻的固体,可以经受住1 kg炸药的爆炸威力。下列有关说法正确的是( )
A.利用二氧化硅气凝胶能够开发导电材料
B.激光照射二氧化硅气凝胶可产生丁达尔效应
C.计算机芯片的主要成分是二氧化硅
D.二氧化硅气凝胶能溶于水
B
解析:二氧化硅不导电,A错误;二氧化硅气凝胶属于胶体,能产生丁达尔效应,B正确;计算机芯片的主要成分是单晶硅,C错误;二氧化硅不溶于水,D错误。
10.硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是________。
A.陶瓷 B.玻璃
C.水泥 D.生石灰
D
(2) SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_________________________________________,工艺师常用___________(填物质名称)来雕刻玻璃。
SiO2+2NaOH===Na2SiO3+H2O
氢氟酸
(3) 用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作________。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是________。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
防火剂
D
(4) 工业上常利用反应2C+SiO2 ===== Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是________(填化学式,下同),氧化剂是____________。
高温
C
SiO2
解析:(1)生石灰是CaO,为碱性氧化物且不含Si,不属于硅酸盐。
(2) SiO2与NaOH溶液反应的化学方程式为SiO2+2NaOH===
Na2SiO3+H2O。由于SiO2能溶于氢氟酸,因此工艺师常用氢氟酸来雕刻玻璃。
(3)Na2SiO3水溶液又称“水玻璃”,具有阻燃的功能,因此可用作防火剂。SiO2和Na2CO3在高温下反应生成Na2SiO3和CO2,故含SiO2的材料(普通玻璃、石英玻璃)以及Al2O3等都能与Na2CO3在高温下反应,故不能用以上材质的坩埚熔融纯碱。
(4)该反应中C被氧化,SiO2中+4价的硅被还原,因此SiO2作氧化剂。
B篇·综合提升训练
11.化学在生产生活和科学研究中具有重要的作用。下列说法正确的是( )
①石英的主要成分是二氧化硅
②三峡大坝使用了大量水泥,水泥是硅酸盐材料
③太阳能电池的主要成分是硅,太阳能电池在生活中的应用有利于环保、节能
④二氧化硅的熔点高,硬度大,所以可用来制造电子部件和光学器件
⑤水晶项链和餐桌上的瓷盘都是硅酸盐制品
A.①②③ B.②④⑤
C.③④⑤ D.①②③④
解析:石英的主要成分是二氧化硅;水泥属于传统硅酸盐产品;太阳能电池的主要成分是硅;水晶项链的主要成分是SiO2,餐桌上的瓷盘是硅酸盐制品;硅是半导体材料,可制造电子部件,二氧化硅光学性能优良,可制光学器件。综上所述,选A。
12.已知滑石粉的化学式为Mg3Si4O10(OH)2,色白、滑爽、柔软、耐火。下列有关说法不正确的是( )
A.滑石粉属于无机硅酸盐类物质
B.滑石粉组成可表示为3MgO·4SiO2·H2O
C.爽身粉中添加滑石粉是利用它的滑爽、柔软、耐火性
D.滑石粉可能会与氢氟酸、NaOH溶液发生反应
C
解析:硅酸盐是由硅、氧元素与其他元素组成的一类无机物的总称,故滑石粉属于无机硅酸盐类物质,A正确;可以将硅酸盐改写成氧化物的形式,B正确;爽身粉中添加滑石粉,主要是利用它的滑爽、柔软、干燥的特点,与耐火性无关,C错误;滑石粉中可能含有SiO2,可以与氢氟酸、NaOH溶液发生反应,D正确。
13.证明生石灰中既混有石英,又混有石灰石的正确方法是
( )
A.加入过量盐酸,观察是否有气泡冒出
B.加入过量烧碱溶液,观察是否有固体溶解
C.加热至高温,观察是否有气体冒出,是否有硅酸钙生成
D.加入过量盐酸搅拌,观察是否有不溶物剩余及气泡出现
D
解析:SiO2不溶于除氢氟酸以外的任何酸,CaO、CaCO3均可溶于盐酸,且CaCO3溶于盐酸有气泡生成。
14.(双选)下列说法正确的是( )
A.普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2
B.制玻璃的过程中发生反应Na2CO3+SiO2=====Na2SiO3+CO2↑,说明酸性H2SiO3>H2CO3
C.水晶玻璃、普通玻璃均属于硅酸盐产品
D.青花瓷胎体的原料为高岭土[Al2Si2O5(OH)4],用氧化物形式可表示为Al2O3·2SiO2·2H2O
AD
高温
解析:普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2,A项正确;反应Na2CO3+SiO2=====Na2SiO3+CO2↑能发生是因为生成的CO2不断逸出,且该反应不是在溶液中发生的,不能作为判断碳酸和硅酸酸性强弱的依据,事实上碳酸的酸性强于硅酸的酸性,B项错误;水晶玻璃的主要成分是二氧化硅,不属于硅酸盐产品,C项错误。
高温
15.(双选)下列说法正确的是( )
A.硅胶作袋装食品的干燥剂的过程中没有发生化学变化
B.酸性溶液中可能大量存在Na+、NH4+、SiO32-
C.向Na2SiO3溶液中滴加稀盐酸的离子方程式:SiO32-+2H+===H2SiO3↓
D.向Na2SiO3溶液中通入过量SO2的离子方程式:SiO32-+SO2+H2O===H2SiO3↓+SO32-
AC
解析:B项,酸性条件下,SiO32-不能大量存在;D项,应生成HSO3-。
16.硅铝合金具有熔点低、凝固时收缩率小等优点,适合铸造。现取试样10.0 g,放在纯净氧气中完全燃烧,燃烧后的固体经称量发现比原来试样增重9.23 g,由此计算硅铝合金中硅的质量分数约为( )
A.12.3% B.15.4%
C.13.4% D.17.0%
C
解析:铝、硅燃烧反应的化学方程式分别为4Al+3O2=====2Al2O3,Si+O2======SiO2。固体增重质量就是参加反应的氧气的质量。设Si的质量为x g,则Al的质量为(10-x) g,根据化学反应方程式知,铝消耗的氧气的质量为96(10-x) g÷108,硅消耗的氧气的质量为32x g÷28,96(10-x) g÷108+32x g÷28=9.23 g,解得x≈1.34,硅铝合金中硅的质量分数为1.34 g÷10.0 g×100%=13.4%。
点燃
点燃
17.A、B、C、D、E代表单质或化合物,它们之间的相互转化关系如图所示。A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。
请填空:
(1)组成A单质的元素的最高化合价为________。
(2)B的化学式为________,B和碳反应生成A和E的化学方程式为_______________________________________________。
+4价
SiO2
SiO2+2C ===== Si+2CO↑
高温
(3) C的化学式为___________,D的化学式为____________。
CaSiO3
Na2SiO3
解析:由本题题眼“A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似”,推知A为硅;根据框图B+碳―→Si+E,B既能与氧化钙反应又能与氢氧化钠反应,推知B为二氧化硅,进一步推知C为硅酸钙,D为硅酸钠,E为一氧化碳。
18.晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅。
②粗硅与干燥的Cl2反应制得SiCl4:Si+2Cl2=====SiCl4。
③SiCl4被过量的H2在1 000~1 100 ℃时还原制得纯硅。
△
某同学从资料中查知:SiCl4的熔点为-70 ℃,沸点为57.6 ℃,其在潮湿的空气中能与水发生反应而变质。该同学设计了以下制取纯硅的实验装置(热源及夹持装置略去)。
请回答下列问题:
(1)为使SiCl4从装置B中逸出与氢气混合,应采取的措施是__________________________________。
对装置B进行水浴加热
(2)盛放稀硫酸的仪器名称为________,装置A中发生反应的离子方程式为__________________________________________。
分液漏斗
Zn+2H+===Zn2++H2↑
(3)装置C能否采用普通玻璃管?________(选填“能”或“不能”),原因是_______________________________________。
不能
在1 000~1 100 ℃时普通玻璃管会软化
(4) 已知SiCl4在潮湿的空气中能与水发生反应生成氯化氢,为防止空气污染,含有SiCl4的尾气要通入盛有___________溶液的烧杯中。
NaOH
(5)为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度,还应对该装置进行的改进是______________________________________________________
_________________________________________________。
在装置A与装置B之间连接一盛有浓硫酸的洗气瓶(或盛有碱石灰的干燥管)
解析:(1)SiCl4的沸点较低(57.6 ℃),欲使其逸出烧瓶与装置C中的H2反应,需对装置B进行水浴加热。
(3)由于H2与SiCl4在1 000~1 100 ℃时反应制得纯硅,反应温度高,普通玻璃管在此温度下会软化,因此需要用石英管。
(5)为了防止装置A中的水蒸气进入装置B中,应在装置A、B之间加一干燥装置。
本课结束
This lesson is over
THANKS!
第五章
化工生产中的重要非金属元素
第三节
无机非金属材料
[明确学习目标]
1.知道常见的硅酸盐材料玻璃、水泥、陶瓷及生产它们的主要原料。
2.了解高纯硅的制备原理。知道硅和二氧化硅的用途。
3.知道一些新型无机非金属材料如硅和二氧化硅、新型陶瓷和碳纳米材料等。
[核心素养对接]
1.通过对硅酸盐结构的了解培养学生宏观辨识与微观探析的能力。
2.通过对几种重要无机非金属材料生产及用途的学习,提高学生科学精神与社会责任。
课前篇
·
自主学习固基础
一、硅酸盐材料
[知识梳理]
1.硅酸盐
(1)结构:在硅酸盐中,Si和O构成了硅氧四面体,即以硅原子为中心,氧原子在四面体的4个顶角(如图所示),许多这样的四面体还可以通过顶角的O相连接,即每个Si与周围4个O结合,每个O与2个Si结合。硅氧四面体结构的特殊性,决定了硅酸盐材料的特殊性质。
(2)性质:硅酸盐性质________,
熔点________,多数________溶于水。
(3)表示方法:硅酸盐的组成比较复杂,常用氧化物的形式表示。例如:硅酸钠(Na2SiO3)可表示为Na2O·SiO2,钠长石(NaAlSi3O8)可表示为Na2O·Al2O3·6SiO2。
稳定
较高
难
(4) 最简单的硅酸盐——Na2SiO3
易
水玻璃
SiO32-+2H+===H2SiO3↓
2CO2+SiO32-+2H2O ===2HCO3-+H2SiO3↓
防火剂
2.传统的无机非金属材料——硅酸盐产品
玻璃 水泥 陶瓷
主要原料 ________、石灰石、________ ________、黏土 ________
主要设备 ________ ______________ 陶瓷窑
主要反应 __________________ __________________、 ________________ — —
纯碱
石英砂
石灰石
黏土
玻璃窑
水泥回转窑
SiO2+Na2CO3====Na2SiO3+CO2↑
高温
SiO2+CaCO3 ===== CaSiO3+CO2↑
高温
主要成分 普通玻璃 ________、________、 ________ ______________ 硅酸盐
Na2SiO3
CaSiO3
SiO2
硅酸三钙(3CaO·SiO2)、
硅酸二钙(2CaO·SiO2)、
铝酸三钙(3CaO·Al2O3)
二、新型无机非金属材料
1.硅和二氧化硅
(1)硅晶片是生产________的基础,属于________材料,是因为硅元素位于元素周期表第________周期,第________族,单质的导电性介于________和________之间。高纯硅广泛用于信息技术和新能源技术领域。
芯片
半导体
三
ⅣA
导体
绝缘体
(2)工业上制备高纯硅
①硅元素的存在:全部以化合态存在,主要以_________和氧化物(如水晶、玛瑙)形式存在。
②生产流程:石英砂——————→粗硅———→SiHCl3
———→高纯硅。
焦炭
1 800~2 000 ℃
HCl
300 ℃
H2
1 100 ℃
硅酸盐
写出其中涉及的主要化学反应的化学方程式:
___________________________________________________;
___________________________________________________;
___________________________________________________。
(3)光导纤维的生产需要________,优点:通信容量大,抗干扰性能好,传输信号不易衰减。
SiO2+2C ============ Si+2CO↑
1 800~2 000 ℃
Si+3HCl ======== SiHCl3+H2
300 ℃
SiHCl3+H2 ========= Si+3HCl
1 100 ℃
SiO2
[自我排查]
1.单质硅在常温下化学性质稳定,所以硅在自然界中以游离态存在,这种说法是否正确?为什么?
________________________________________________________________________________________________________________________________________________________
尝试解答
提示:不正确。硅属于亲氧元素,虽然在常温下稳定,但在漫长的地质年代中,硅元素和氧结合在一起,都以化合态存在,主要以二氧化硅及硅酸盐的形式存在。
2.实验室中盛放碱液的试剂瓶为什么用橡胶塞而不用磨口玻璃塞?
________________________________________________________________________________________________________________________________________________
提示:玻璃中含有SiO2,SiO2与碱反应生成具有黏合作用的硅酸盐,使瓶口和瓶塞黏结在一起而难以开启
课堂篇
·
重点难点要突破
研习1 硅、二氧化硅、硅酸盐
[重点讲解]
硅酸盐由于组成比较复杂,通常用氧化物的形式表示其组成,改写时的规律为:
(1)顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水;氧化物之间以“·”隔开。
一、硅酸盐氧化物形式的书写
(2)原则:各元素原子总个数比符合原来的组成,若出现分数应化为整数。
例如:钠长石(NaAlSi3O8)不能写成12Na2O·12Al2O3·3SiO2,应写成Na2O·Al2O3·6SiO2。
(3)各元素的化合价不能改变。
1.硅元素的存在
二、硅、二氧化硅
2.硅单质
(1)物理性质:熔点高、硬度大、不溶于水。
(2)化学性质
①常温下能与氟气、氢氟酸、强碱等反应。
Si+2F2===SiF4
Si+4HF===SiF4↑+2H2↑
Si+2NaOH+H2O===Na2SiO3+2H2↑
(Si+2NaOH+4H4e-2O===Na2SiO3+3H2O+2H2↑)
[特别提醒]
能与NaOH溶液反应的单质:Al、Si、S(加热)、Cl2。
② 加热时能与氧气、氯气、碳等反应。
Si+O2=====SiO2
Si+2Cl2=====SiCl4
Si+C=====SiC
△
△
高温
(3) 用途:半导体材料、芯片、太阳能电池。
3.二氧化硅
(1)存在
SiO2存在形态有结晶形和无定形两大类,统称硅石。石英、水晶、玛瑙、沙子、光导纤维的主要成分均是SiO2。
(2)结构
SiO2晶体是由Si和O按原子数之比为1∶2的比例组成的正四面体结构的晶体。每个硅原子周围结合4个O原子,每个O原子周围结合2个Si原子。
(3) 物理性质
熔点高,硬度大,不溶于水。
(4) 化学性质
(5)用途
①沙子是基本的建筑材料。
②纯净的SiO2是现代光学及光纤制品的基本材料,可以制作光导纤维。
③水晶和玛瑙用来制作饰物和工艺品。
④实验室中使用的石英坩埚。
4. 硅及其氧化物的特性
物质 一般规律 硅及其氧化物的特性
Si 硅的还原性比碳强 SiO2+2CSi+2CO↑
非金属单质与强碱反应一般不生成氢气 Si+2NaOH+H2O===Na2SiO3+2H2↑
非金属单质一般不与非氧化性酸反应 Si+4HF===SiF4↑+2H2↑
一般非金属单质为绝缘体 硅为半导体
物质 一般规律 硅及其氧化物的特性
SiO2 酸性氧化物一般与水反应生成相应的酸 SiO2不溶于水,也不与水反应
酸性氧化物一般不与酸发生复分解反应 SiO2+4HF===SiF4↑+2H2O
“较强酸制较弱酸”是复分解反应的一般规律,碳酸酸性大于硅酸 Na2SiO3+CO2(少量)+H2O===H2SiO3↓+Na2CO3,但在高温下Na2CO3+SiO2Na2SiO3+CO2↑
[联想质疑]
2018年3月5日,中国22岁的青年学者曹原在《自然》连刊两文介绍石墨烯超导重大发现,当将两层平行石墨烯堆成约1.1°的微妙角度,就会产生神奇的超导效应。2018年12月,《自然》杂志发布了2018年度影响世界的十大科学人物排行榜,曹原名列榜首。
石墨烯是一种由碳原子构成的六角型二维碳纳米材料,具有超高硬度、强度和导热系数等特性。
[问题探讨]
1.碳和硅的最外层电子数都是4,且碳元素的非金属性强于硅,但碳在自然界中有稳定的单质(如金刚石、石墨),而硅却没有,其原因是什么?
提示:硅是一种亲氧元素,硅与氧形成硅氧四面体的稳定结构,故自然界中无游离态的硅,而是以二氧化硅和硅酸盐的形式存在于自然界中。
2.工业上用焦炭和石英砂在高温下制备粗硅时,为什么要隔绝空气?写出工业上制备粗硅的化学方程式。
提示:因为高温下焦炭和空气中的O2发生反应,故制取粗硅时要隔绝空气,工业制取粗硅的化学方程式为
SiO2+2=======Si+2CO↑。
高温
3.已知:SiO2+4HF===SiF4↑+2H2O,SiO2既能与NaOH溶液发生反应,又能与氢氟酸发生反应,因此,SiO2属于两性氧化物,这种说法正确吗?
提示:不正确;SiO2尽管能与氢氟酸反应,但与其他强酸(如HCl、HNO3等)不反应,故SiO2不属于两性氧化物,属于酸性氧化物。
4.你知道的碳纳米材料有哪些?碳化硅陶瓷是传统无机非金属材料还是新型无机非金属材料?
提示:碳纳米材料主要有富勒烯、碳纳米管、石墨烯等。碳化硅陶瓷属于新型无机非金属材料。
[举一反三]
1.用氧化物的形式表示硅酸盐的组成,其中正确的是( )
A.钙沸石[Ca(Al2Si3O10)·3H2O]表示为Al2O3·CaO·3SiO2·3H2O
B.镁橄榄石(Mg2SiO4)表示为MgO·SiO2
C.钾云母(K2Al6Si6H4O24)表示为K2O·2H2O·3Al2O3·6SiO2
D.硅酸铜钡(BaCuSi2O6)表示为BaO·CuO·2SiO2
D
解析:A项,Ca(Al2Si3O10)·3H2O应改为CaO·Al2O3·3SiO2·3H2O
(排序错);B项,Mg2SiO4应改为2MgO·SiO2(不能在化学计量数中出现分数);C项,K2Al6Si6H4O24应改为K2O·3Al2O3·6SiO2·2H2O
(排序错)。
2.将过量的CO2分别通入:①CaCl2溶液;②浓Na2SiO3溶液;③Ca(OH)2溶液;④饱和Na2CO3溶液。最终溶液中有白色沉淀析出的是( )
A.①②③④ B.②④
C.①②③ D.②③
B
解析:CO2溶于水:CO2+H2O====H2CO3,H2CO3的酸性比盐酸弱,而比硅酸强。根据酸与盐反应的规律,CO2通入CaCl2溶液无明显现象;过量的CO2通入浓Na2SiO3溶液中有白色沉淀H2SiO3生成;CO2通入Ca(OH)2溶液中至过量,Ca(OH)2+CO2===CaCO3↓+H2O, CaCO3+H2O+CO2===Ca(HCO3)2,最终生成Ca(HCO3)2而无沉淀;过量CO2通入饱和Na2CO3溶液中:Na2CO3+H2O+CO2===2NaHCO3↓,生成的NaHCO3溶解度比Na2CO3溶解度小而析出结晶。
3.下列关于硅单质及其化合物的说法正确的是( )
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料
A.①② B.②③
C.①④ D.③④
C
解析:许多岩石和矿物中含有硅元素,①正确;水晶的主要成分是二氧化硅,所以水晶不是硅酸盐制品,②错误;光导纤维是由高纯度的二氧化硅制成的,③错误;陶瓷属于硅酸盐制品,④正确。
4.(双选)用石英砂制取高纯硅的主要化学反应如下:
①SiO2+2C=====Si(粗)+2CO↑
②Si(粗)+2Cl2=====SiCl4
③SiCl4+2H2=====Si(纯)+4HCl
高温
△
高温
关于上述反应的叙述不正确的是( )
A.①③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均弱于硅
C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子
D.高温下在炉子里将石英砂、焦炭、氯气、氢气按比例混合就能得到高纯硅
BD
解析:在氧化还原反应中,还原剂的还原性比还原产物的还原性强,B错误;根据元素化合价的变化,每消耗或生成28 g(1 mol)硅,均转移4 mol电子,C正确;题中的三个反应是在三个不同的反应器中发生的,D错误。
5.矿泉水一般是由岩石风化后,被地下水溶解其中的可溶部分生成的,此处所指的风化作用是指矿物与水和CO2同时作用的过程。例如钾长石(KAlSi3O8)风化生成高岭土[Al2Si2O5(OH)4],此反应的离子方程式为
2KAlSi3O8+2H2CO3+5H2O===2K++2HCO3-+4H2SiO3+Al2Si2O5(OH)4
(1) 将上述复杂硅酸盐改写成氧化物形式。
①KAlSi3O8______________________________。
②Al2Si2O5(OH)4______________________________。
(2)上述反应能够发生的原因是__________________________
_________________。
2KAlSi3O8+2H2CO3+5H2O===2K++2HCO3-+4H2SiO3+Al2Si2O5(OH)4
K2O·Al2O3·6SiO2
Al2O3·2SiO2·2H2O
H2CO3的酸性比H2SiO3强
解析:(1)将硅酸盐化学式写成氧化物形式时,需将氧以外的元素写成同价态的氧化物,并按活动性顺序排列,用“·”将它们连接起来,各种元素原子个数比符合原来的组成。
(2)此反应属于酸与盐发生的复分解反应,能发生的原因是酸性:H2CO3>H2SiO3。
演习篇
·
学业测试速达标
1.下列关于无机非金属材料的说法不正确的是( )
A.传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料克服了传统无机非金属材料的缺点,具有极大强度
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
D
解析:新型无机非金属材料不但克服了传统无机非金属材料易碎、强度不够等缺点,并且具有特殊结构、特殊功能;新型无机非金属材料的主要成分并不一定是硅酸盐,如氮化硅陶瓷、碳化硅陶瓷等。
2.在①浓硝酸、②水、③盐酸、④氢氟酸、⑤氢氧化钾溶液中,常温时能与二氧化硅起化学反应的有( )
A.①② B.②④
C.④⑤ D.③④
C
3.昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用二氧化硅和金属氧化物的形式可表示为( )
A.CaO·MgO·SiO2·H2O
B.2CaO·5MgO·8SiO2·H2O
C.2CaO·MgO·SiO2·2H2O
D.5CaO·2MgO·8SiO2·H2O
B
解析:根据昆仑玉的化学式,将Ca、Mg、Si、H分别写成氧化物的形式,按较活泼金属氧化物→较不活泼金属氧化物→SiO2→H2O的顺序排列,再调整各氧化物前的化学计量数并使其与昆仑玉化学式中一致,可得昆仑玉氧化物表示形式为2CaO·5MgO·8SiO2·H2O。
4.下列说法正确的是( )
A.CO2+H2O+Na2SiO3===H2SiO3↓+Na2CO3,说明酸性:H2CO3>H2SiO3
B.SiO2+Na2CO3=====Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
C.在复分解反应中必须是酸性强的生成酸性弱的
D.已知酸性:H2CO3>HClO>HCO3-,则CO2+H2O+2NaClO===Na2CO3+2HClO
A
高温
解析:由于H2CO3能与Na2SiO3反应生成H2SiO3,则说明H2CO3酸性大于H2SiO3,A正确;在B项中,由于在高温条件下反应,CO2为气体逸出,不能比较酸性强弱;在C项中,H2S+CuSO4===CuS↓+H2SO4,此反应为弱酸生成强酸;在D项中由于酸性:HClO>HCO3-,产物应为NaHCO3。
5.(双选)高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
下列说法正确的是( )
A.步骤①的化学方程式为SiO2+2C ===== Si+2CO↑
B.步骤①②③中每生成或反应1 mol Si,转移4 mol电子
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏(或分馏)可提纯SiHCl3
高温
AD
解析:A项,产物为CO,正确;B项,第②、③步中转移2 mol电子,错误;C项,硅可与氢氟酸反应生成四氟化硅和氢气,错误;D项,根据物质的沸点不同可用蒸馏的方法进行分离,正确。
6.某研究性学习小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si;
②Mg在点燃的条件下按质量比8∶5与SiO2反应生成一种白色固体化合物和另一种硅化物;
③金属硅化物与稀硫酸反应生成硫酸盐与SiH4;
④Si和SiO2均不能与稀H2SO4反应;
⑤SiH4在空气中自燃。
他们的研究报告中记载着“……选用合适的物质在适合的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量……用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期的63%左右。”请回答下列问题:
(1) 该小组“实验室制Si”的化学反应方程式是
____________________________________。
(2) 写出②的反应方程式:_______________________________。
2C+SiO2=====Si+2CO↑
高温
SiO2+4Mg=====2MgO+Mg2Si
点燃
(3)该过程中产率比预期低的原因是_______________________
______________________________________。
(4)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是什么?请用必要的文字和化学方程式予以说明:
_______________________________________________________________________________________。
部分硅与镁反应生成了硅化镁
SiH4能自燃,而有爆鸣声和火花就是由SiH4的自燃引起的,SiH4+2O2===SiO2+2H2O
解析:(1)碳可以在高温下还原SiO2制得Si。反应的化学方程式为2C+SiO2 ====== Si+2CO↑。
(2)Mg与SiO2反应类似于Mg与CO2的反应,先生成MgO和Si,Si再和Mg反应生成Mg2Si,故可生成MgO和Mg2Si。
高温
课时作业(七)
无机非金属材料
A篇·知识对点训练
1.下列物质中,不含有硅酸盐的是( )
A.水玻璃 B.硅芯片
C.黏土 D.普通水泥
B
解析:水玻璃是Na2SiO3的水溶液,黏土和普通水泥的主要成分都是硅酸盐,硅芯片的主要成分是硅单质。
2.下列说法错误的是( )
A.二氧化硅是光导纤维的主要原料
B.硅是信息技术的关键材料
C.陶瓷餐具所用材料为硅酸盐
D.水晶镜片所用原料为硅酸盐
D
解析:水晶、光导纤维的主要成分为SiO2。Si用于信息产业及太阳能电池。传统硅酸盐材料是陶瓷、水泥、玻璃。
3.下列有关硅及其化合物的说法正确的是( )
A.陶瓷、玻璃、水泥容器都能贮存氢氟酸
B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在具有磨口玻璃塞的试剂瓶中
C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2
D.由Na2CO3+SiO2=====CO2↑+Na2SiO3可知,硅酸的酸性强于碳酸
C
高温
解析:陶瓷、玻璃、水泥的主要成分都是硅酸盐,其含有的SiO2能与氢氟酸反应,A项错误;硅酸钠是一种黏合剂,能将玻璃塞和瓶体粘在一起,不便于打开,B项错误;D项中的反应能发生是因为生成的CO2气体不断逸出,不能说明硅酸的酸性强于碳酸。
4.下列说法正确的是( )
A.石英玻璃、玛瑙、水泥和餐桌上的瓷盘都是硅酸盐制品
B.红宝石、珍珠、水晶、钻石等装饰品的主要成分都是硅酸盐
C.氢氟酸能够雕刻玻璃
D.硅酸具有酸的通性,能使石蕊溶液变红
C
解析:石英玻璃、玛瑙的成分是SiO2,不属于硅酸盐,A不正确;红宝石的主要成分为三氧化二铝、珍珠的主要成分为CaCO3、水晶的主要成分为SiO2、钻石为碳单质,均不属于硅酸盐,B不正确;氢氟酸能与玻璃的成分之一SiO2发生反应:4HF+SiO2===SiF4↑+2H2O,C正确;硅酸具有酸的通性,例如能与碱反应,但其难溶于水,不能使石蕊溶液变色,D错。
5.制取下列物质不需要用石灰石作原料的是( )
A.硅酸 B.水泥
C.玻璃 D.生石灰
A
解析:硅酸由可溶性硅酸盐与酸反应制得。
6.下列关于无机非金属材料的说法中,不正确的是( )
A.高纯硅可用于制造半导体材料
B.氧化铝陶瓷属于新型无机非金属材料,它是生物陶瓷
C.氮化硅陶瓷属于新型无机非金属材料,可用于制造陶瓷发动机的受热面
D.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
D
解析:光导纤维不具有导电性,D不正确。
7.下列关于SiO2和CO2的说法中,不正确的是( )
A.CO2和SiO2都能与碱及碱性氧化物反应
B.CO2和SiO2都能与水反应生成相应的酸
C.CO2和SiO2都能与焦炭反应生成CO
D.SiO2可用于制光导纤维,干冰可用于人工降雨
B
解析:CO2能与水反应生成碳酸,但SiO2不能与水反应生成相应的酸,B错误。
8.二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等方面有着重要的用途。a~e是对①~⑤反应中SiO2所表现的化学性质或作用进行的判断,其中正确的是( )
①SiO2+2NaOH===Na2SiO3+H2O
②SiO2+2C ===== Si+2CO↑
③SiO2+4HF===SiF4↑+2H2O
④Na2CO3+SiO2======Na2SiO3+CO2↑
高温
高温
⑤SiO2+3C=======SiC+2CO↑
a.反应①中SiO2作为玻璃的成分被消耗,用于刻蚀玻璃
b.反应②中SiO2表现出氧化性
c.反应③中SiO2表现了酸性氧化物的通性
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的道理
e.反应⑤中SiO2未参加氧化还原反应
A.ace B.bde C.cde D.ab
高温
解析:通常用氢氟酸来刻蚀玻璃,与之对应的反应是③,因此a、c判断错误;反应②是一个置换反应,其中二氧化硅被还原,表现出氧化性,b判断正确;反应④是一个复分解反应,用难挥发的二氧化硅制取易挥发的二氧化碳,d判断正确;反应⑤中碳的化合价由0价变为-4和+2价,硅的化合价和氧的化合价都没有改变,因此二氧化硅没有参加氧化还原反应,e判断也正确。
9.二氧化硅气凝胶是一种世界上最轻的固体,可以经受住1 kg炸药的爆炸威力。下列有关说法正确的是( )
A.利用二氧化硅气凝胶能够开发导电材料
B.激光照射二氧化硅气凝胶可产生丁达尔效应
C.计算机芯片的主要成分是二氧化硅
D.二氧化硅气凝胶能溶于水
B
解析:二氧化硅不导电,A错误;二氧化硅气凝胶属于胶体,能产生丁达尔效应,B正确;计算机芯片的主要成分是单晶硅,C错误;二氧化硅不溶于水,D错误。
10.硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是________。
A.陶瓷 B.玻璃
C.水泥 D.生石灰
D
(2) SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_________________________________________,工艺师常用___________(填物质名称)来雕刻玻璃。
SiO2+2NaOH===Na2SiO3+H2O
氢氟酸
(3) 用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作________。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是________。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
防火剂
D
(4) 工业上常利用反应2C+SiO2 ===== Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是________(填化学式,下同),氧化剂是____________。
高温
C
SiO2
解析:(1)生石灰是CaO,为碱性氧化物且不含Si,不属于硅酸盐。
(2) SiO2与NaOH溶液反应的化学方程式为SiO2+2NaOH===
Na2SiO3+H2O。由于SiO2能溶于氢氟酸,因此工艺师常用氢氟酸来雕刻玻璃。
(3)Na2SiO3水溶液又称“水玻璃”,具有阻燃的功能,因此可用作防火剂。SiO2和Na2CO3在高温下反应生成Na2SiO3和CO2,故含SiO2的材料(普通玻璃、石英玻璃)以及Al2O3等都能与Na2CO3在高温下反应,故不能用以上材质的坩埚熔融纯碱。
(4)该反应中C被氧化,SiO2中+4价的硅被还原,因此SiO2作氧化剂。
B篇·综合提升训练
11.化学在生产生活和科学研究中具有重要的作用。下列说法正确的是( )
①石英的主要成分是二氧化硅
②三峡大坝使用了大量水泥,水泥是硅酸盐材料
③太阳能电池的主要成分是硅,太阳能电池在生活中的应用有利于环保、节能
④二氧化硅的熔点高,硬度大,所以可用来制造电子部件和光学器件
⑤水晶项链和餐桌上的瓷盘都是硅酸盐制品
A.①②③ B.②④⑤
C.③④⑤ D.①②③④
解析:石英的主要成分是二氧化硅;水泥属于传统硅酸盐产品;太阳能电池的主要成分是硅;水晶项链的主要成分是SiO2,餐桌上的瓷盘是硅酸盐制品;硅是半导体材料,可制造电子部件,二氧化硅光学性能优良,可制光学器件。综上所述,选A。
12.已知滑石粉的化学式为Mg3Si4O10(OH)2,色白、滑爽、柔软、耐火。下列有关说法不正确的是( )
A.滑石粉属于无机硅酸盐类物质
B.滑石粉组成可表示为3MgO·4SiO2·H2O
C.爽身粉中添加滑石粉是利用它的滑爽、柔软、耐火性
D.滑石粉可能会与氢氟酸、NaOH溶液发生反应
C
解析:硅酸盐是由硅、氧元素与其他元素组成的一类无机物的总称,故滑石粉属于无机硅酸盐类物质,A正确;可以将硅酸盐改写成氧化物的形式,B正确;爽身粉中添加滑石粉,主要是利用它的滑爽、柔软、干燥的特点,与耐火性无关,C错误;滑石粉中可能含有SiO2,可以与氢氟酸、NaOH溶液发生反应,D正确。
13.证明生石灰中既混有石英,又混有石灰石的正确方法是
( )
A.加入过量盐酸,观察是否有气泡冒出
B.加入过量烧碱溶液,观察是否有固体溶解
C.加热至高温,观察是否有气体冒出,是否有硅酸钙生成
D.加入过量盐酸搅拌,观察是否有不溶物剩余及气泡出现
D
解析:SiO2不溶于除氢氟酸以外的任何酸,CaO、CaCO3均可溶于盐酸,且CaCO3溶于盐酸有气泡生成。
14.(双选)下列说法正确的是( )
A.普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2
B.制玻璃的过程中发生反应Na2CO3+SiO2=====Na2SiO3+CO2↑,说明酸性H2SiO3>H2CO3
C.水晶玻璃、普通玻璃均属于硅酸盐产品
D.青花瓷胎体的原料为高岭土[Al2Si2O5(OH)4],用氧化物形式可表示为Al2O3·2SiO2·2H2O
AD
高温
解析:普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2,A项正确;反应Na2CO3+SiO2=====Na2SiO3+CO2↑能发生是因为生成的CO2不断逸出,且该反应不是在溶液中发生的,不能作为判断碳酸和硅酸酸性强弱的依据,事实上碳酸的酸性强于硅酸的酸性,B项错误;水晶玻璃的主要成分是二氧化硅,不属于硅酸盐产品,C项错误。
高温
15.(双选)下列说法正确的是( )
A.硅胶作袋装食品的干燥剂的过程中没有发生化学变化
B.酸性溶液中可能大量存在Na+、NH4+、SiO32-
C.向Na2SiO3溶液中滴加稀盐酸的离子方程式:SiO32-+2H+===H2SiO3↓
D.向Na2SiO3溶液中通入过量SO2的离子方程式:SiO32-+SO2+H2O===H2SiO3↓+SO32-
AC
解析:B项,酸性条件下,SiO32-不能大量存在;D项,应生成HSO3-。
16.硅铝合金具有熔点低、凝固时收缩率小等优点,适合铸造。现取试样10.0 g,放在纯净氧气中完全燃烧,燃烧后的固体经称量发现比原来试样增重9.23 g,由此计算硅铝合金中硅的质量分数约为( )
A.12.3% B.15.4%
C.13.4% D.17.0%
C
解析:铝、硅燃烧反应的化学方程式分别为4Al+3O2=====2Al2O3,Si+O2======SiO2。固体增重质量就是参加反应的氧气的质量。设Si的质量为x g,则Al的质量为(10-x) g,根据化学反应方程式知,铝消耗的氧气的质量为96(10-x) g÷108,硅消耗的氧气的质量为32x g÷28,96(10-x) g÷108+32x g÷28=9.23 g,解得x≈1.34,硅铝合金中硅的质量分数为1.34 g÷10.0 g×100%=13.4%。
点燃
点燃
17.A、B、C、D、E代表单质或化合物,它们之间的相互转化关系如图所示。A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。
请填空:
(1)组成A单质的元素的最高化合价为________。
(2)B的化学式为________,B和碳反应生成A和E的化学方程式为_______________________________________________。
+4价
SiO2
SiO2+2C ===== Si+2CO↑
高温
(3) C的化学式为___________,D的化学式为____________。
CaSiO3
Na2SiO3
解析:由本题题眼“A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似”,推知A为硅;根据框图B+碳―→Si+E,B既能与氧化钙反应又能与氢氧化钠反应,推知B为二氧化硅,进一步推知C为硅酸钙,D为硅酸钠,E为一氧化碳。
18.晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅。
②粗硅与干燥的Cl2反应制得SiCl4:Si+2Cl2=====SiCl4。
③SiCl4被过量的H2在1 000~1 100 ℃时还原制得纯硅。
△
某同学从资料中查知:SiCl4的熔点为-70 ℃,沸点为57.6 ℃,其在潮湿的空气中能与水发生反应而变质。该同学设计了以下制取纯硅的实验装置(热源及夹持装置略去)。
请回答下列问题:
(1)为使SiCl4从装置B中逸出与氢气混合,应采取的措施是__________________________________。
对装置B进行水浴加热
(2)盛放稀硫酸的仪器名称为________,装置A中发生反应的离子方程式为__________________________________________。
分液漏斗
Zn+2H+===Zn2++H2↑
(3)装置C能否采用普通玻璃管?________(选填“能”或“不能”),原因是_______________________________________。
不能
在1 000~1 100 ℃时普通玻璃管会软化
(4) 已知SiCl4在潮湿的空气中能与水发生反应生成氯化氢,为防止空气污染,含有SiCl4的尾气要通入盛有___________溶液的烧杯中。
NaOH
(5)为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度,还应对该装置进行的改进是______________________________________________________
_________________________________________________。
在装置A与装置B之间连接一盛有浓硫酸的洗气瓶(或盛有碱石灰的干燥管)
解析:(1)SiCl4的沸点较低(57.6 ℃),欲使其逸出烧瓶与装置C中的H2反应,需对装置B进行水浴加热。
(3)由于H2与SiCl4在1 000~1 100 ℃时反应制得纯硅,反应温度高,普通玻璃管在此温度下会软化,因此需要用石英管。
(5)为了防止装置A中的水蒸气进入装置B中,应在装置A、B之间加一干燥装置。
本课结束
This lesson is over
THANKS!
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
