7.2.1 乙烯 课件(共69张PPT)
文档属性
| 名称 | 7.2.1 乙烯 课件(共69张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 18.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-23 15:45:55 | ||
图片预览










文档简介
(共69张PPT)
第七章
有机化合物
第二节
乙烯与有机高分子材料
第1课时
乙烯
[明确学习目标]
1.掌握乙烯的分子结构,初步体会其结构特点对性质的影响,了解乙烯的用途。
2.了解乙烯的物理性质,掌握其化学性质。
3.认识加成反应的特点,会书写乙烯发生加成反应的化学方程式。
[核心素养对接]
通过对乙烯结构与性质的学习,培养学生宏观辨识与微观探析的能力。
课前篇
·
自主学习固基础
一、乙烯
[知识梳理]
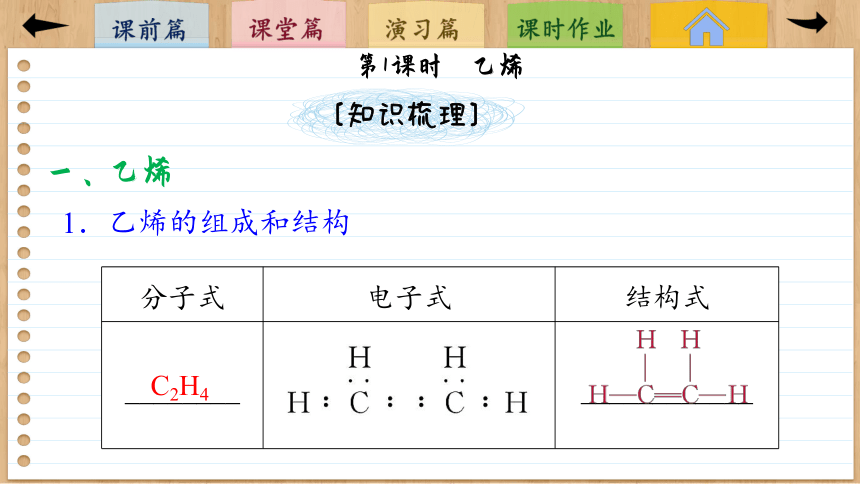
1.乙烯的组成和结构
分子式 电子式 结构式
________ ____________
C2H4
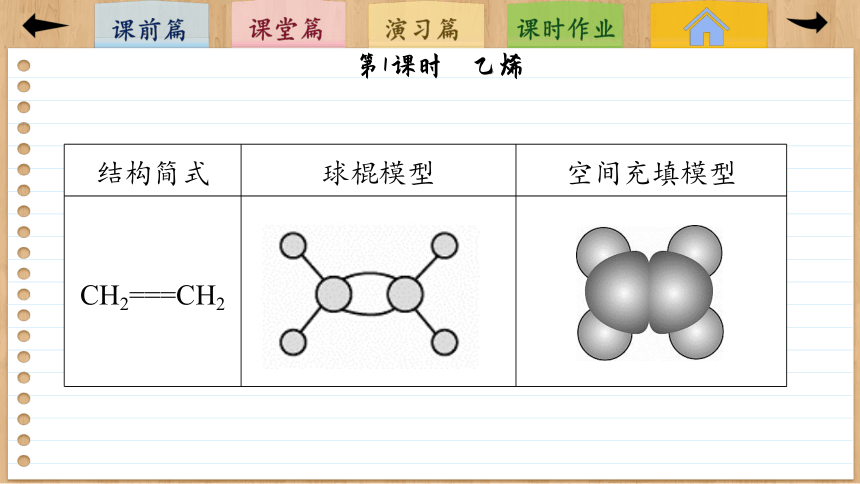
结构简式 球棍模型 空间充填模型
CH2===CH2
2.乙烯的物理性质
颜色 状态 气味 水溶性 密度
____色 ____体 稍有气味 ____溶于水 比空气略小
无
气
难
3.乙烯的化学性质
[实验7-2]
实验操作 实验现象
点燃乙烯 火焰明亮,伴有黑烟,放热有水珠生成
向酸性高锰酸钾溶液中通入乙烯 溶液由紫红色变成无色
(1) 氧化反应
火焰明亮且伴有黑烟
褪色
C2H4+3O2 ――→ 2CO2+2H2O
点燃
(2) 加成反应
[实验7-3]
实验操作 实验现象
向溴的四氯化碳溶液中通入乙烯 溴的四氯化碳溶液褪色
①概念:有机物分子中的不饱和碳原子与其他____________
_____________直接结合生成新的化合物的反应。
原子或原子团
② 乙烯的加成反应:
CH3CH3
CH3CH2Cl
CH3CH2OH
(3) 聚合反应
由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应,叫做聚合反应。由于发生加成反应而生成有机高分子化合物的聚合反应也叫加成聚合反应,简称加聚反应。乙烯能发生自身的加成反应生成高分子化合物聚乙烯,反应的化学方程式为
[ ] n
nCH2===CH2 ――→ ― CH2 ― CH2 ―
催化剂
聚乙烯
聚合反应生成的高分子是由较小的结构单元重复连接而成的。例如,聚乙烯分子可以用?CH2—CH2?来表示,其中重复的结构单元“—CH2—CH2—” 称为________,链节的数目n称为________。能合成高分子的小分子物质称为________,________就是聚乙烯的单体。
链节
聚合度
单体
乙烯
4.乙烯的用途
(1)重要的化工原料,用来制聚乙烯塑料、聚乙烯纤维、乙醇等。
(2)在农业生产中用作____________调节剂。
(3)乙烯的产量可以用来衡量一个国家的石油化工发展水平。
植物生长
二、烃
仅含________和________两种元素的有机物称为碳氢化合物,也称为________。
碳
氢
烃
CH3CH3
苯分子具有_____________结构,相邻碳原子之间的键______
________,其键长介于______________________的键长之间。
碳碳双键
CH2===CH2
碳碳三键
苯环
平面正六边形
完全相同
碳碳单键和碳碳双键
[自我排查]
(1) 烃 的分子式为C3H6,符合通式CnH2n,故该分子属于烯烃( )
(2) 某无色气体通入酸性KMnO4溶液中,溶液褪色,该气体一定是烯烃( )
一、微判断
(3)某无色气体能使溴水褪色,该气体可能是烯烃( )
(4)甲烷和乙烯都属于烃,前者属于烷烃,后者属于烯烃( )
(5)甲烷和乙烯都是可燃性气体,点燃之前必须验纯,而且燃烧时现象相同( )
(6)以石油为原料可以获得乙烯( )
(7)乙烯比乙烷的化学性质活泼( )
二、尝试解答
1.检验甲烷和乙烯气体可以采用什么方法?除去甲烷气体中的乙烯可以采用什么方法?________________________________________________________________________________________________________________________________________________________________________________________________________________________
提示:检验甲烷和乙烯可以选择溴水或酸性KMnO4溶液,出现褪色现象的为乙烯;但是除去甲烷中的乙烯只能用溴水,因为酸性KMnO4溶液可以将乙烯氧化成CO2气体而引入新的杂质。
2.C2H4和C3H6一定互为同系物吗?烯烃的通式是什么?_____________________________________________________________________________________________________________________________________________________________________________________________________________________
提示:不一定;因为无法确定C3H6为烯烃还是环烷烃,故不能确定C2H4和C3H6是不是同系物。烯烃的通式为CnH2n(n≥2)。
三、微训练
1.刚摘的猕猴桃往往青涩难吃,但将熟透的红苹果与它共同装入袋内,三天后就香甜可口了,原因是熟透的苹果挥发出的乙烯对猕猴桃起了催熟作用。下列有关乙烯的说法中不正确的是( )
A.乙烯分子为平面结构,分子中C—H键之间的键角约为120°
B.乙烯与溴发生加成反应后的产物中所有原子都共平面
C.乙烯的产量是衡量一个国家石油化工水平的标志
D.乙烯是一种植物生长的调节剂,也可作水果催熟剂
B
解析:乙烯分子中的6个原子共平面,但与溴发生加成反应后生成BrCH2CH2Br(1,2-二溴乙烷),其结构相当于乙烷分子中的两个H原子(位于不同的碳原子上)被Br原子代替,每个碳原子与其相连的4个原子构成四面体结构,1,2-二溴乙烷中的8个原子不共平面。
2.下列关于乙烯的叙述中,正确的是( )
A.乙烯的化学性质比乙烷活泼
B.甲烷和乙烯在一定条件下都可以与氯气反应,且反应类型相同
C.乙烯分子中所有原子不可能在同一平面上
D.乙烯分子的碳碳双键中的一个键易断裂,易发生加成反应和取代反应
A
解析:由乙烯可使酸性高锰酸钾溶液褪色而乙烷不能,可知乙烯比乙烷活泼,A正确;甲烷和氯气发生取代反应,而乙烯和氯气发生加成反应,B项不正确;乙烯分子中所有原子在同一平面上,C项不正确;乙烯分子的碳碳双键中的一个键易断裂,易发生加成反应,而不易发生取代反应,D不正确。
课堂篇
·
重点难点要突破
研习 乙烯 烯烃的性质
[重点讲解]
1.乙烯分子的结构特点
乙烯的结构简式不可以写成CH2CH2,而应写成CH2===CH2,即必须把其中的官能团碳碳双键体现出来,碳碳双键一定不能省略。
2.乙烯的化学性质
(1) 氧化反应
应用及注意事项
燃烧 C2H4+3O2 ――→ 2CO2+2H2O
①乙烯在点燃之前一定要验纯
②利用燃烧时的现象与甲烷不同,可用燃烧法鉴别甲烷和乙烯
③若反应中温度高于100 ℃,因H2O为气态,故反应前后气体体积不变
应用及注意事项
被酸性高锰酸钾溶液氧化 乙烯使酸性高锰酸钾溶液褪色
①利用该性质可鉴别甲烷(或烷烃)和乙烯(或烯烃)
②该反应中高锰酸钾将乙烯最终氧化为CO2,所以除去甲烷中的乙烯时不能用酸性高锰酸钾溶液
续表
(2) 加成反应
①乙烯与Br2反应
CH2===CH2+Br2―→CH2Br—CH2Br。
a.一般用溴水或溴的四氯化碳溶液,且生成的1,2 二溴乙烷为难溶于水的无色油状液体。
b.利用反应时溶液褪色的现象,既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯。
②乙烯与H2反应
CH2===CH2+H2 ―――→ CH3CH3。
③乙烯与HCl反应
CH2===CH2+HCl ―――→ CH3CH2Cl。
可利用该反应制取纯净的氯乙烷。
催化剂
△
催化剂
△
3.烯烃的性质
(1)烯烃的通式为CnH2n(n为正整数,n≥2),但具有这一通式的有机物不一定是烯烃。事实上,单环烷烃的通式也是CnH2n(n为正整数,n≥3)。
(2)双键只能是碳碳双键,不能是其他双键。若某分子中含有碳氧双键,则该分子不属于烃,更不是烯烃。
(3) 通常所说的烯烃严格地讲是单烯烃,分子内只能有1个碳碳双键。若某分子内有2个碳碳双键,则该烃应为二烯烃。
(4) 烯烃燃烧的通式为
CnH2n+O2――→nCO2+nH2O。
完全燃烧后产生的CO2和H2O的物质的量之比为1∶1。
点燃
(5) 烯烃的性质:与乙烯相似
②加成反应CH3—CH===CH2+Br2 ―→
(溴水褪色)
CnH2n+O2 ――→ nCO2+nH2O
同乙烯(现象)
使KMnO4(H+)褪色
①氧化反应燃烧
点燃
CH3—CH===CH2+H2 ―――→ CH3CH2CH3
CH3—CH===CH2+HCl ―――→ CH3CH2CH2Cl
或
催化剂
△
催化剂
△
CH3—CH===CH2+H2O ―――→ CH3CH2CH2OH
或
催化剂
③ 加聚反应nCH3—CH===CH2 ―――→
催化剂
nCH3—CH===CH—CH3 ―――→
催化剂
4.有机物分子中原子的共面情况
乙烯中的一个氢原子被其他原子或原子团替代后,只有与碳碳双键两端的碳原子直接相连的原子才与原有的原子共平面,
如丙烯 的—CH3中的碳原子一定在原平面上,
而另外3个氢原子中至多可以有1个在原平面上。
5.取代反应与加成反应比较
名称 比较 取代反应 加成反应
概念 有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应 有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应
反应特点 取而代之,有进有出 加之而成,有进无出
[探究活动]
[实验] 探究乙烯的化学性质
实验装置
实验现象 酸性KMnO4溶液紫色变成无色(或褪色) 红棕色溶液变成无色(或溴的CCl4溶液褪色)
[问题探讨]
1.乙烯使酸性KMnO4溶液褪色,体现了乙烯的什么性质?
提示:乙烯能被酸性KMnO4溶液氧化生成CO2,体现了乙烯的还原性。
2.乙烯能使溴的CCl4溶液褪色,褪色原理是什么?SO2使溴水褪色的原理又是什么?
提示:乙烯使溴的CCl4溶液褪色是由于乙烯与溴发生了加成反应;SO2使溴水褪色是由于SO2被溴水中的单质溴氧化。
3.如何鉴别乙烷和乙烯?除去乙烷中的乙烯气体能否用酸性KMnO4溶液?为什么?
提示:用溴水或酸性KMnO4溶液作鉴别试剂,其中使试剂褪色的是乙烯,不褪色的是乙烷;由于乙烯能被酸性KMnO4溶液氧化生成CO2,引入杂质CO2,故不能用酸性KMnO4溶液除去乙烷中的乙烯。
4.制取纯净的氯乙烷,是利用乙烷与氯气的取代反应,还是利用乙烯与氯化氢的加成反应?为什么?
提示:用乙烯与氯化氢的加成反应制取纯净的氯乙烷;原因是乙烯与氯化氢的加成产物只有一种,而乙烷与氯气的取代产物是多种氯代乙烷的混合物。
[举一反三]
1.(双选)由乙烯的结构和性质推测丙烯(CH2===CH—CH3)的结构或性质正确的是( )
A.能使酸性KMnO4溶液褪色
B.所有的原子都在同一平面内
C.能使溴的四氯化碳溶液褪色
D.与HCl在一定条件下能加成,并只得到一种产物
AC
解析:因丙烯分子中含有甲基(—CH3),故丙烯中所有原子不在同一平面内;因丙烯分子同乙烯分子一样含有碳碳双键,所以能被酸性KMnO4溶液氧化而使之褪色,能与溴加成而使溴的四氯化碳溶液褪色,能与HCl加成得到 或Cl—CH2CH2CH3两种产物。
2.0.5体积某气态烃只能与0.5体积氯气发生加成反应,生成氯代烷。0.5 mol此氯代烷可与3 mol氯气发生完全的取代反应,则该烃的结构简式为( )
A.CH2===CH2 B.CH3CH===CH2
C.CH3CH3 D.CH3CH2CH===CH2
B
解析:0.5体积气态烃只能与0.5体积氯气发生加成反应,说明该烃分子中含有1个碳碳双键;0.5 mol此氯代烷可与3 mol氯气发生完全的取代反应,说明该氯代烷分子中含有6个氢原子,即原烃分子中含有6个氢原子。
3.下列由乙烯推测丙烯的结构或性质中,正确的是( )
A.分子中3个碳原子在同一直线上
B.分子中所有原子都在同一平面上
C.分子中共价键的夹角均为120°
D.分子中共价键数为8,其中有一个碳碳双键
D
解析:由丙烯(CH2===CH—CH3)结构可看做是CH2===CH2结
构中一个氢原子被一个—CH3所替代。 中显然3个
碳原子不在同一条直线上。由于甲基中4个原子不在同一平面上,所以CH2===CH—CH3分子中所有原子不可能都在同一平面上。丙烯分子中—CH3上的碳氢键的夹角不是120°,故A、B、C三项错误。
4.下列分子中的所有原子均在同一平面上的是( )
A.C2H4 B.CHCl3
C.CH3CH===CH2 D.CH3—CH3
A
解析:C2H4为乙烯,属于平面形分子,A正确;CHCl3、CH3—CH3及CH3CH===CH2中的甲基碳原子均为饱和碳原子,与之紧邻的四个原子为四面体结构,故B、C、D错误。
5.(双选)下列说法正确的是( )
A.乙烯能使溴水和酸性高锰酸钾溶液褪色,其褪色原理相同
B.甲烷与氯气在光照条件下的反应属于取代反应
C.工业上可以通过乙烯与氯气发生加成反应制取氯乙烷
D.除去乙烷中的乙烯得到纯净的乙烷,可依次通过KMnO4(H+)溶液、NaOH溶液和浓H2SO4
BD
解析:乙烯能使溴水和酸性高锰酸钾溶液褪色,乙烯与Br2发生加成反应,与酸性高锰酸钾溶液发生氧化反应,其褪色原理不相同,A错误;甲烷与氯气在光照条件下的反应属于取代反应,B正确;乙烯与氯气发生加成反应生成1,2 二氯乙烷,C错误;酸性高锰酸钾溶液能把乙烯氧化为CO2,NaOH溶液能吸收CO2,经浓硫酸干燥后可得到纯净的乙烷,D正确。
演习篇
·
学业测试速达标
1.下列有关乙烯和乙烷的说法中,错误的是( )
A.乙烯的化学性质比乙烷的活泼
B.乙烯是平面分子,乙烷分子中并非所有原子都在同一平面上
C.溴的四氯化碳溶液和酸性KMnO4溶液都可以鉴别乙烯和乙烷
D.乙烯分子中的碳碳双键比乙烷分子中的碳碳单键更稳定
D
解析:A项,CH2===CH2分子中有碳碳双键,化学性质活泼,正确;B项,CH2===CH2分子中6个原子全部在一个平面上,CH3—CH3相当于两个—CH3结合,并非所有的原子都在同一个平面上,正确;C项,CH2===CH2可以使溴的四氯化碳溶液和酸性KMnO4溶液褪色,乙烷不能,可以鉴别,正确;D项,与乙烷分子中的碳碳单键比较,乙烯分子中的碳碳双键不稳定,易发生化学反应,错误。
2.已知乙烯能被酸性高锰酸钾溶液氧化成CO2。既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是
( )
A.通入酸性高锰酸钾溶液中
B.通入足量溴水中
C.通入水中
D.在空气中燃烧
B
解析:除去乙烷中混有的乙烯不能选用酸性高锰酸钾溶液,因为除去乙烯又会引入杂质CO2,也不能用水和燃烧的方法,故只有选项B符合题意。
3.高分子化合物 的单体是( )
D
A. B.CH2===CH2
C.CH3—CH2—CH2—CH3 D.CH3—CH===CH—CH3
解析:此高分子化合物是由CH3—CH===CH—CH3通过加聚反应生成的,故其单体为CH3—CH===CH—CH3,其链节
为 。
4.(双选)下列关于乙烯的用途叙述不正确的是( )
A.以乙烯为原料可以直接合成聚氯乙烯
B.乙烯可以用来制备1,2-二溴乙烷(Br—CH2—CH2—Br)
C.乙烯可以与水发生加成反应制备乙醇(CH3CH2OH)
D.乙烯可以与HBr发生加成反应制备1,1-二溴乙烷
AD
解析:乙烯分子中含有碳碳双键,能发生加聚反应生成聚乙烯,不能直接合成聚氯乙烯,A错误;乙烯与溴单质可发生加成反应生成1,2-二溴乙烷,B正确;乙烯在一定条件下可以与水发生加成反应生成乙醇(CH3CH2OH),C正确;乙烯与HBr发生加成反应生成溴乙烷(CH2BrCH3),D错误。
5.下列物质中,不能和乙烯发生加成反应的是( )
A.H2 B.H2O
C.KMnO4 D.Br2
C
解析:KMnO4与乙烯发生的是氧化还原反应。
6.能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢个数比为1∶2
B.乙烯完全燃烧生成的CO2和水的物质的量相等
C.乙烯能与Br2的CCl4溶液发生加成反应,且1 mol乙烯完全加成需消耗1 mol Br2
D.乙烯能使酸性高锰酸钾溶液褪色
C
解析:碳氢个数比为1∶2,是对乙烯的组成分析,而不是证明碳碳双键存在的事实,A不能证明;乙烯完全燃烧生成的CO2和水的物质的量相等,只能推断出乙烯分子中碳、氢原子个数比为1∶2,B不能证明;1 mol乙烯完全加成需要消耗1 mol Br2,说明乙烯分子中含有一个碳碳双键,C正确;能使酸性高锰酸钾溶液褪色只能证明有机物具有还原性或含有不饱和键,不一定含有碳碳双键和只含有一个碳碳双键,D不正确。
7.根据乙烯的性质填空:
(1) 乙烯通入酸性KMnO4溶液中观察到的现象是____________
_______________________,乙烯发生了________反应。
(2) 乙烯通入溴的CCl4溶液中观察到的现象是_______________
________________。乙烯发生了________反应,化学方程式为_____________________________________________________。
酸性KMnO4溶液褪色
氧化
溴的CCl4溶液褪色
加成
CH2===CH2+Br2―→CH2Br—CH2Br
(3)为了安全,点燃乙烯前应____________,乙烯燃烧时的实验现象是____________________________。
化学方程式为________________________________________。
检验纯度
火焰明亮且伴有黑烟
CH2===CH2+3O2――→2CO2+2H2O
点燃
本课结束
This lesson is over
THANKS!
第七章
有机化合物
第二节
乙烯与有机高分子材料
第1课时
乙烯
[明确学习目标]
1.掌握乙烯的分子结构,初步体会其结构特点对性质的影响,了解乙烯的用途。
2.了解乙烯的物理性质,掌握其化学性质。
3.认识加成反应的特点,会书写乙烯发生加成反应的化学方程式。
[核心素养对接]
通过对乙烯结构与性质的学习,培养学生宏观辨识与微观探析的能力。
课前篇
·
自主学习固基础
一、乙烯
[知识梳理]
1.乙烯的组成和结构
分子式 电子式 结构式
________ ____________
C2H4
结构简式 球棍模型 空间充填模型
CH2===CH2
2.乙烯的物理性质
颜色 状态 气味 水溶性 密度
____色 ____体 稍有气味 ____溶于水 比空气略小
无
气
难
3.乙烯的化学性质
[实验7-2]
实验操作 实验现象
点燃乙烯 火焰明亮,伴有黑烟,放热有水珠生成
向酸性高锰酸钾溶液中通入乙烯 溶液由紫红色变成无色
(1) 氧化反应
火焰明亮且伴有黑烟
褪色
C2H4+3O2 ――→ 2CO2+2H2O
点燃
(2) 加成反应
[实验7-3]
实验操作 实验现象
向溴的四氯化碳溶液中通入乙烯 溴的四氯化碳溶液褪色
①概念:有机物分子中的不饱和碳原子与其他____________
_____________直接结合生成新的化合物的反应。
原子或原子团
② 乙烯的加成反应:
CH3CH3
CH3CH2Cl
CH3CH2OH
(3) 聚合反应
由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应,叫做聚合反应。由于发生加成反应而生成有机高分子化合物的聚合反应也叫加成聚合反应,简称加聚反应。乙烯能发生自身的加成反应生成高分子化合物聚乙烯,反应的化学方程式为
[ ] n
nCH2===CH2 ――→ ― CH2 ― CH2 ―
催化剂
聚乙烯
聚合反应生成的高分子是由较小的结构单元重复连接而成的。例如,聚乙烯分子可以用?CH2—CH2?来表示,其中重复的结构单元“—CH2—CH2—” 称为________,链节的数目n称为________。能合成高分子的小分子物质称为________,________就是聚乙烯的单体。
链节
聚合度
单体
乙烯
4.乙烯的用途
(1)重要的化工原料,用来制聚乙烯塑料、聚乙烯纤维、乙醇等。
(2)在农业生产中用作____________调节剂。
(3)乙烯的产量可以用来衡量一个国家的石油化工发展水平。
植物生长
二、烃
仅含________和________两种元素的有机物称为碳氢化合物,也称为________。
碳
氢
烃
CH3CH3
苯分子具有_____________结构,相邻碳原子之间的键______
________,其键长介于______________________的键长之间。
碳碳双键
CH2===CH2
碳碳三键
苯环
平面正六边形
完全相同
碳碳单键和碳碳双键
[自我排查]
(1) 烃 的分子式为C3H6,符合通式CnH2n,故该分子属于烯烃( )
(2) 某无色气体通入酸性KMnO4溶液中,溶液褪色,该气体一定是烯烃( )
一、微判断
(3)某无色气体能使溴水褪色,该气体可能是烯烃( )
(4)甲烷和乙烯都属于烃,前者属于烷烃,后者属于烯烃( )
(5)甲烷和乙烯都是可燃性气体,点燃之前必须验纯,而且燃烧时现象相同( )
(6)以石油为原料可以获得乙烯( )
(7)乙烯比乙烷的化学性质活泼( )
二、尝试解答
1.检验甲烷和乙烯气体可以采用什么方法?除去甲烷气体中的乙烯可以采用什么方法?________________________________________________________________________________________________________________________________________________________________________________________________________________________
提示:检验甲烷和乙烯可以选择溴水或酸性KMnO4溶液,出现褪色现象的为乙烯;但是除去甲烷中的乙烯只能用溴水,因为酸性KMnO4溶液可以将乙烯氧化成CO2气体而引入新的杂质。
2.C2H4和C3H6一定互为同系物吗?烯烃的通式是什么?_____________________________________________________________________________________________________________________________________________________________________________________________________________________
提示:不一定;因为无法确定C3H6为烯烃还是环烷烃,故不能确定C2H4和C3H6是不是同系物。烯烃的通式为CnH2n(n≥2)。
三、微训练
1.刚摘的猕猴桃往往青涩难吃,但将熟透的红苹果与它共同装入袋内,三天后就香甜可口了,原因是熟透的苹果挥发出的乙烯对猕猴桃起了催熟作用。下列有关乙烯的说法中不正确的是( )
A.乙烯分子为平面结构,分子中C—H键之间的键角约为120°
B.乙烯与溴发生加成反应后的产物中所有原子都共平面
C.乙烯的产量是衡量一个国家石油化工水平的标志
D.乙烯是一种植物生长的调节剂,也可作水果催熟剂
B
解析:乙烯分子中的6个原子共平面,但与溴发生加成反应后生成BrCH2CH2Br(1,2-二溴乙烷),其结构相当于乙烷分子中的两个H原子(位于不同的碳原子上)被Br原子代替,每个碳原子与其相连的4个原子构成四面体结构,1,2-二溴乙烷中的8个原子不共平面。
2.下列关于乙烯的叙述中,正确的是( )
A.乙烯的化学性质比乙烷活泼
B.甲烷和乙烯在一定条件下都可以与氯气反应,且反应类型相同
C.乙烯分子中所有原子不可能在同一平面上
D.乙烯分子的碳碳双键中的一个键易断裂,易发生加成反应和取代反应
A
解析:由乙烯可使酸性高锰酸钾溶液褪色而乙烷不能,可知乙烯比乙烷活泼,A正确;甲烷和氯气发生取代反应,而乙烯和氯气发生加成反应,B项不正确;乙烯分子中所有原子在同一平面上,C项不正确;乙烯分子的碳碳双键中的一个键易断裂,易发生加成反应,而不易发生取代反应,D不正确。
课堂篇
·
重点难点要突破
研习 乙烯 烯烃的性质
[重点讲解]
1.乙烯分子的结构特点
乙烯的结构简式不可以写成CH2CH2,而应写成CH2===CH2,即必须把其中的官能团碳碳双键体现出来,碳碳双键一定不能省略。
2.乙烯的化学性质
(1) 氧化反应
应用及注意事项
燃烧 C2H4+3O2 ――→ 2CO2+2H2O
①乙烯在点燃之前一定要验纯
②利用燃烧时的现象与甲烷不同,可用燃烧法鉴别甲烷和乙烯
③若反应中温度高于100 ℃,因H2O为气态,故反应前后气体体积不变
应用及注意事项
被酸性高锰酸钾溶液氧化 乙烯使酸性高锰酸钾溶液褪色
①利用该性质可鉴别甲烷(或烷烃)和乙烯(或烯烃)
②该反应中高锰酸钾将乙烯最终氧化为CO2,所以除去甲烷中的乙烯时不能用酸性高锰酸钾溶液
续表
(2) 加成反应
①乙烯与Br2反应
CH2===CH2+Br2―→CH2Br—CH2Br。
a.一般用溴水或溴的四氯化碳溶液,且生成的1,2 二溴乙烷为难溶于水的无色油状液体。
b.利用反应时溶液褪色的现象,既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯。
②乙烯与H2反应
CH2===CH2+H2 ―――→ CH3CH3。
③乙烯与HCl反应
CH2===CH2+HCl ―――→ CH3CH2Cl。
可利用该反应制取纯净的氯乙烷。
催化剂
△
催化剂
△
3.烯烃的性质
(1)烯烃的通式为CnH2n(n为正整数,n≥2),但具有这一通式的有机物不一定是烯烃。事实上,单环烷烃的通式也是CnH2n(n为正整数,n≥3)。
(2)双键只能是碳碳双键,不能是其他双键。若某分子中含有碳氧双键,则该分子不属于烃,更不是烯烃。
(3) 通常所说的烯烃严格地讲是单烯烃,分子内只能有1个碳碳双键。若某分子内有2个碳碳双键,则该烃应为二烯烃。
(4) 烯烃燃烧的通式为
CnH2n+O2――→nCO2+nH2O。
完全燃烧后产生的CO2和H2O的物质的量之比为1∶1。
点燃
(5) 烯烃的性质:与乙烯相似
②加成反应CH3—CH===CH2+Br2 ―→
(溴水褪色)
CnH2n+O2 ――→ nCO2+nH2O
同乙烯(现象)
使KMnO4(H+)褪色
①氧化反应燃烧
点燃
CH3—CH===CH2+H2 ―――→ CH3CH2CH3
CH3—CH===CH2+HCl ―――→ CH3CH2CH2Cl
或
催化剂
△
催化剂
△
CH3—CH===CH2+H2O ―――→ CH3CH2CH2OH
或
催化剂
③ 加聚反应nCH3—CH===CH2 ―――→
催化剂
nCH3—CH===CH—CH3 ―――→
催化剂
4.有机物分子中原子的共面情况
乙烯中的一个氢原子被其他原子或原子团替代后,只有与碳碳双键两端的碳原子直接相连的原子才与原有的原子共平面,
如丙烯 的—CH3中的碳原子一定在原平面上,
而另外3个氢原子中至多可以有1个在原平面上。
5.取代反应与加成反应比较
名称 比较 取代反应 加成反应
概念 有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应 有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应
反应特点 取而代之,有进有出 加之而成,有进无出
[探究活动]
[实验] 探究乙烯的化学性质
实验装置
实验现象 酸性KMnO4溶液紫色变成无色(或褪色) 红棕色溶液变成无色(或溴的CCl4溶液褪色)
[问题探讨]
1.乙烯使酸性KMnO4溶液褪色,体现了乙烯的什么性质?
提示:乙烯能被酸性KMnO4溶液氧化生成CO2,体现了乙烯的还原性。
2.乙烯能使溴的CCl4溶液褪色,褪色原理是什么?SO2使溴水褪色的原理又是什么?
提示:乙烯使溴的CCl4溶液褪色是由于乙烯与溴发生了加成反应;SO2使溴水褪色是由于SO2被溴水中的单质溴氧化。
3.如何鉴别乙烷和乙烯?除去乙烷中的乙烯气体能否用酸性KMnO4溶液?为什么?
提示:用溴水或酸性KMnO4溶液作鉴别试剂,其中使试剂褪色的是乙烯,不褪色的是乙烷;由于乙烯能被酸性KMnO4溶液氧化生成CO2,引入杂质CO2,故不能用酸性KMnO4溶液除去乙烷中的乙烯。
4.制取纯净的氯乙烷,是利用乙烷与氯气的取代反应,还是利用乙烯与氯化氢的加成反应?为什么?
提示:用乙烯与氯化氢的加成反应制取纯净的氯乙烷;原因是乙烯与氯化氢的加成产物只有一种,而乙烷与氯气的取代产物是多种氯代乙烷的混合物。
[举一反三]
1.(双选)由乙烯的结构和性质推测丙烯(CH2===CH—CH3)的结构或性质正确的是( )
A.能使酸性KMnO4溶液褪色
B.所有的原子都在同一平面内
C.能使溴的四氯化碳溶液褪色
D.与HCl在一定条件下能加成,并只得到一种产物
AC
解析:因丙烯分子中含有甲基(—CH3),故丙烯中所有原子不在同一平面内;因丙烯分子同乙烯分子一样含有碳碳双键,所以能被酸性KMnO4溶液氧化而使之褪色,能与溴加成而使溴的四氯化碳溶液褪色,能与HCl加成得到 或Cl—CH2CH2CH3两种产物。
2.0.5体积某气态烃只能与0.5体积氯气发生加成反应,生成氯代烷。0.5 mol此氯代烷可与3 mol氯气发生完全的取代反应,则该烃的结构简式为( )
A.CH2===CH2 B.CH3CH===CH2
C.CH3CH3 D.CH3CH2CH===CH2
B
解析:0.5体积气态烃只能与0.5体积氯气发生加成反应,说明该烃分子中含有1个碳碳双键;0.5 mol此氯代烷可与3 mol氯气发生完全的取代反应,说明该氯代烷分子中含有6个氢原子,即原烃分子中含有6个氢原子。
3.下列由乙烯推测丙烯的结构或性质中,正确的是( )
A.分子中3个碳原子在同一直线上
B.分子中所有原子都在同一平面上
C.分子中共价键的夹角均为120°
D.分子中共价键数为8,其中有一个碳碳双键
D
解析:由丙烯(CH2===CH—CH3)结构可看做是CH2===CH2结
构中一个氢原子被一个—CH3所替代。 中显然3个
碳原子不在同一条直线上。由于甲基中4个原子不在同一平面上,所以CH2===CH—CH3分子中所有原子不可能都在同一平面上。丙烯分子中—CH3上的碳氢键的夹角不是120°,故A、B、C三项错误。
4.下列分子中的所有原子均在同一平面上的是( )
A.C2H4 B.CHCl3
C.CH3CH===CH2 D.CH3—CH3
A
解析:C2H4为乙烯,属于平面形分子,A正确;CHCl3、CH3—CH3及CH3CH===CH2中的甲基碳原子均为饱和碳原子,与之紧邻的四个原子为四面体结构,故B、C、D错误。
5.(双选)下列说法正确的是( )
A.乙烯能使溴水和酸性高锰酸钾溶液褪色,其褪色原理相同
B.甲烷与氯气在光照条件下的反应属于取代反应
C.工业上可以通过乙烯与氯气发生加成反应制取氯乙烷
D.除去乙烷中的乙烯得到纯净的乙烷,可依次通过KMnO4(H+)溶液、NaOH溶液和浓H2SO4
BD
解析:乙烯能使溴水和酸性高锰酸钾溶液褪色,乙烯与Br2发生加成反应,与酸性高锰酸钾溶液发生氧化反应,其褪色原理不相同,A错误;甲烷与氯气在光照条件下的反应属于取代反应,B正确;乙烯与氯气发生加成反应生成1,2 二氯乙烷,C错误;酸性高锰酸钾溶液能把乙烯氧化为CO2,NaOH溶液能吸收CO2,经浓硫酸干燥后可得到纯净的乙烷,D正确。
演习篇
·
学业测试速达标
1.下列有关乙烯和乙烷的说法中,错误的是( )
A.乙烯的化学性质比乙烷的活泼
B.乙烯是平面分子,乙烷分子中并非所有原子都在同一平面上
C.溴的四氯化碳溶液和酸性KMnO4溶液都可以鉴别乙烯和乙烷
D.乙烯分子中的碳碳双键比乙烷分子中的碳碳单键更稳定
D
解析:A项,CH2===CH2分子中有碳碳双键,化学性质活泼,正确;B项,CH2===CH2分子中6个原子全部在一个平面上,CH3—CH3相当于两个—CH3结合,并非所有的原子都在同一个平面上,正确;C项,CH2===CH2可以使溴的四氯化碳溶液和酸性KMnO4溶液褪色,乙烷不能,可以鉴别,正确;D项,与乙烷分子中的碳碳单键比较,乙烯分子中的碳碳双键不稳定,易发生化学反应,错误。
2.已知乙烯能被酸性高锰酸钾溶液氧化成CO2。既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是
( )
A.通入酸性高锰酸钾溶液中
B.通入足量溴水中
C.通入水中
D.在空气中燃烧
B
解析:除去乙烷中混有的乙烯不能选用酸性高锰酸钾溶液,因为除去乙烯又会引入杂质CO2,也不能用水和燃烧的方法,故只有选项B符合题意。
3.高分子化合物 的单体是( )
D
A. B.CH2===CH2
C.CH3—CH2—CH2—CH3 D.CH3—CH===CH—CH3
解析:此高分子化合物是由CH3—CH===CH—CH3通过加聚反应生成的,故其单体为CH3—CH===CH—CH3,其链节
为 。
4.(双选)下列关于乙烯的用途叙述不正确的是( )
A.以乙烯为原料可以直接合成聚氯乙烯
B.乙烯可以用来制备1,2-二溴乙烷(Br—CH2—CH2—Br)
C.乙烯可以与水发生加成反应制备乙醇(CH3CH2OH)
D.乙烯可以与HBr发生加成反应制备1,1-二溴乙烷
AD
解析:乙烯分子中含有碳碳双键,能发生加聚反应生成聚乙烯,不能直接合成聚氯乙烯,A错误;乙烯与溴单质可发生加成反应生成1,2-二溴乙烷,B正确;乙烯在一定条件下可以与水发生加成反应生成乙醇(CH3CH2OH),C正确;乙烯与HBr发生加成反应生成溴乙烷(CH2BrCH3),D错误。
5.下列物质中,不能和乙烯发生加成反应的是( )
A.H2 B.H2O
C.KMnO4 D.Br2
C
解析:KMnO4与乙烯发生的是氧化还原反应。
6.能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢个数比为1∶2
B.乙烯完全燃烧生成的CO2和水的物质的量相等
C.乙烯能与Br2的CCl4溶液发生加成反应,且1 mol乙烯完全加成需消耗1 mol Br2
D.乙烯能使酸性高锰酸钾溶液褪色
C
解析:碳氢个数比为1∶2,是对乙烯的组成分析,而不是证明碳碳双键存在的事实,A不能证明;乙烯完全燃烧生成的CO2和水的物质的量相等,只能推断出乙烯分子中碳、氢原子个数比为1∶2,B不能证明;1 mol乙烯完全加成需要消耗1 mol Br2,说明乙烯分子中含有一个碳碳双键,C正确;能使酸性高锰酸钾溶液褪色只能证明有机物具有还原性或含有不饱和键,不一定含有碳碳双键和只含有一个碳碳双键,D不正确。
7.根据乙烯的性质填空:
(1) 乙烯通入酸性KMnO4溶液中观察到的现象是____________
_______________________,乙烯发生了________反应。
(2) 乙烯通入溴的CCl4溶液中观察到的现象是_______________
________________。乙烯发生了________反应,化学方程式为_____________________________________________________。
酸性KMnO4溶液褪色
氧化
溴的CCl4溶液褪色
加成
CH2===CH2+Br2―→CH2Br—CH2Br
(3)为了安全,点燃乙烯前应____________,乙烯燃烧时的实验现象是____________________________。
化学方程式为________________________________________。
检验纯度
火焰明亮且伴有黑烟
CH2===CH2+3O2――→2CO2+2H2O
点燃
本课结束
This lesson is over
THANKS!
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
