【备考2023】浙江中考科学考前易错点查漏补缺(七):物质组成与结构(含解析)
文档属性
| 名称 | 【备考2023】浙江中考科学考前易错点查漏补缺(七):物质组成与结构(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 205.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-05-24 00:00:00 | ||
图片预览


文档简介
1.2022年冬奥会闭幕式上放满了中国红灯笼,全硼富勒烯团簇(B40)的分子结构像中国红灯笼。B40中的40表示一个分子中有40个( )
A.原子 B.质子 C.离子 D.电子
2.为减少温室气体排放,人们积极寻找不含碳的燃料,其中NH3燃烧前后分子种类变化的微观示意图如图。下列说法正确的是( )
A.该反应属于置换反应
B.NH3中氮元素的化合价为+3价
C.17g甲完全燃烧至少需要32g乙
D.生成的丙与丁的分子个数比为1:1
3.某家庭式空气净化器在工作时会释放出臭氧(O3),利用其强氧化性杀菌消毒并转化为无污染的氧气(O2)。下列分析合理的是( )
A.O3的强氧化性是由O3分子结构决定的
B.相同质量的O3与O2所含的分子个数相同
C.相同分子个数的O3与O2中,所含氧原子的个数相同
D.O3与O2都由氧元素组成,它们的化学性质完全相同
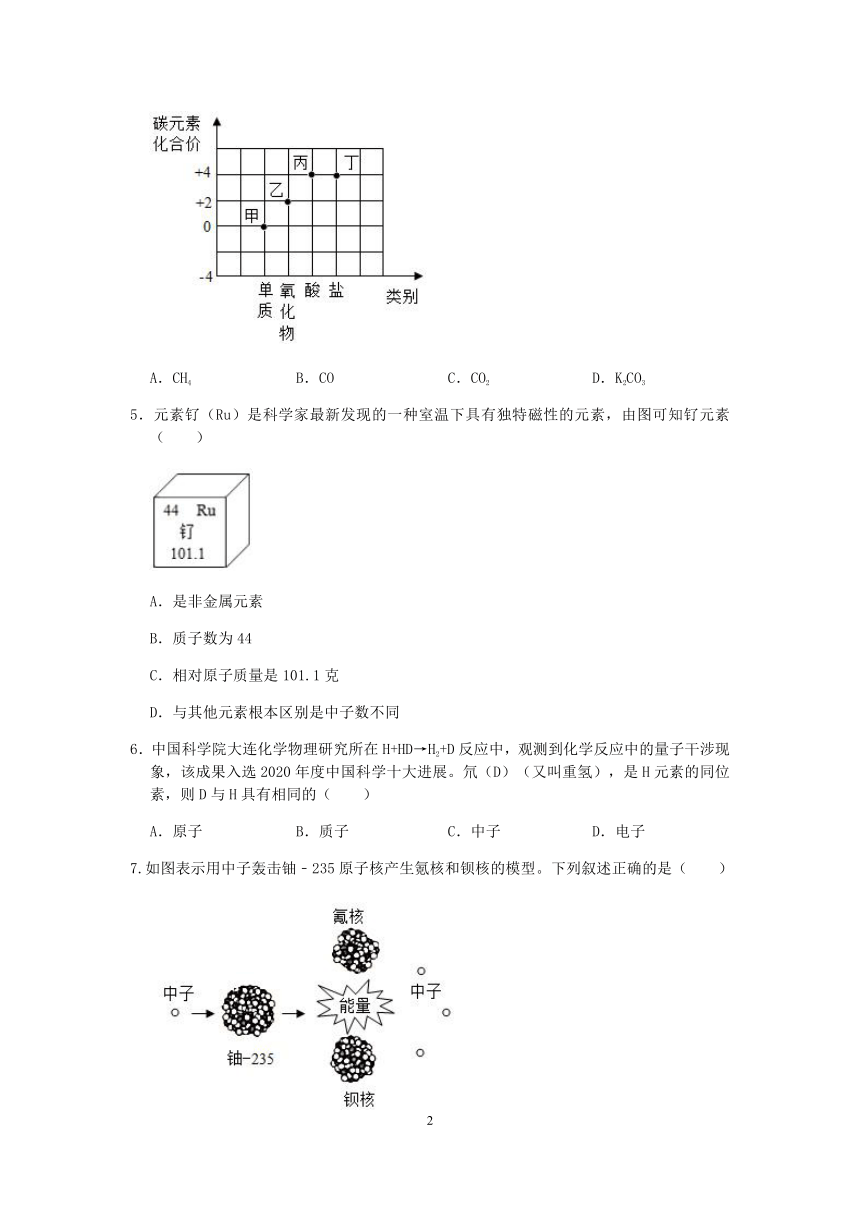
4.类价图反映的是元素的化合价与物质类别之间的关系。如图是碳元素的类价图,图中物质“乙”是( )
A.CH4 B.CO C.CO2 D.K2CO3
5.元素钌(Ru)是科学家最新发现的一种室温下具有独特磁性的元素,由图可知钌元素( )
A.是非金属元素
B.质子数为44
C.相对原子质量是101.1克
D.与其他元素根本区别是中子数不同
6.中国科学院大连化学物理研究所在H+HD→H2+D反应中,观测到化学反应中的量子干涉现象,该成果入选2020年度中国科学十大进展。氘(D)(又叫重氢),是H元素的同位素,则D与H具有相同的( )
A.原子 B.质子 C.中子 D.电子
7.如图表示用中子轰击铀﹣235原子核产生氪核和钡核的模型。下列叙述正确的是( )
A.该模型表示的是核聚变
B.该反应产生的中子可继续轰击其他铀核形成链式反应
C.该反应不会产生放射性物质
D.不能用该反应获得能量的方式来发电
8.市售的加碘食盐是在食盐中加入一定量的碘酸钾(KIO3),碘酸钾中碘元素的化合价是( )
A.﹣2 B.﹣3 C.+1 D.+5
9.“超临界水”(H2O)因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的状态,用“〇”表示氢原子,“”表示氧原子,下列模型能表示“超临界水”分子的是( )
A. B. C. D.
10.有3种不同的原子,甲原子核内有6个质子和6个中子,乙原子核内有6个质子和8个中子,丙原子核内有7个质子和7个中子。下列说法正确的是( )
A.甲和乙是同一种元素 B.甲和乙的核电荷数不同
C.乙和丙核外电子数相等 D.乙和丙互为同位素原子
11.最新科技报道,夏威夷联合天文中心的科学家在宇宙深处发现H3+离子和H3分子,以下关于它们的说法不正确的是( )
A.H3+和H3都是构成物质的微粒
B.H3是单质
C.一个H3+中含有3个电子
D.一个H3中含有3个质子
12.武阳春雨是我市名茶之一,叶底纤细多芽,为茶中真品。茶叶中的
咖啡因能使中枢神经系统兴奋。咖啡因的化学式为C8H10N4O2,下列说法中错误的是( )
A.茶叶树的根向地生长是植物对地球引力刺激作出的反应
B.茶叶树根吸收的水分主要参与枝叶的生长和花果的发育
C.茶叶树相邻的叶总是不重叠,增大光照面积是对光合作用的适应
D.咖啡因中含碳、氢、氮、氧四种元素
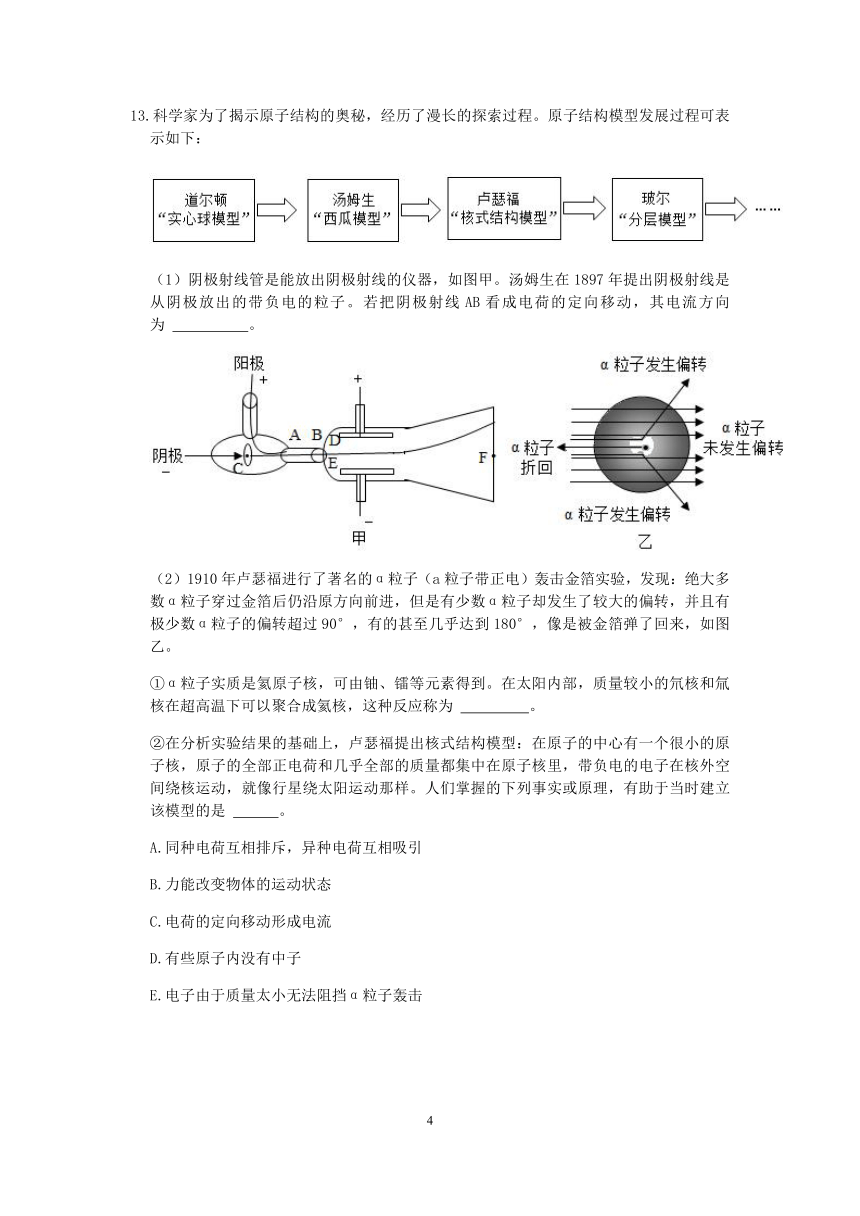
13.科学家为了揭示原子结构的奥秘,经历了漫长的探索过程。原子结构模型发展过程可表示如下:
(1)阴极射线管是能放出阴极射线的仪器,如图甲。汤姆生在1897年提出阴极射线是从阴极放出的带负电的粒子。若把阴极射线AB看成电荷的定向移动,其电流方向为 。
(2)1910年卢瑟福进行了著名的α粒子(a粒子带正电)轰击金箔实验,发现:绝大多数α粒子穿过金箔后仍沿原方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来,如图乙。
①α粒子实质是氦原子核,可由铀、镭等元素得到。在太阳内部,质量较小的氘核和氚核在超高温下可以聚合成氦核,这种反应称为 。
②在分析实验结果的基础上,卢瑟福提出核式结构模型:在原子的中心有一个很小的原子核,原子的全部正电荷和几乎全部的质量都集中在原子核里,带负电的电子在核外空间绕核运动,就像行星绕太阳运动那样。人们掌握的下列事实或原理,有助于当时建立该模型的是 。
A.同种电荷互相排斥,异种电荷互相吸引
B.力能改变物体的运动状态
C.电荷的定向移动形成电流
D.有些原子内没有中子
E.电子由于质量太小无法阻挡α粒子轰击
14.考古时常用死亡生物体内碳﹣14的含量减少一半所需的时间来推测生物的死亡年代。
(1)碳﹣14与碳﹣12属于同位素原子,它们的原子核内 不相同。
(2)大气中的氮﹣14在宇宙射线的作用下会变成碳﹣14,使地球上碳﹣14总量能基本保持不变。从氮﹣14变成碳﹣14,其原子核内部粒子的变化情况
。
15.通过已学习知识的对比和归纳,可以得出一些十分有趣的规律.这些规律可以帮助我们掌握学习化学的方法.请你仔细阅读表中内容,并回答相应的问题.
常见的几种离子 H+ Na+ Mg+ O2﹣
对应元素及原子团在化合物中的化合价
所能形成化合物的化学式 Na2O,MgO,H2O HNO3,H2CO3 MgCO3,NaNO3
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 相等;
(2)由后两行内容对照可得出书写化学式依据的原则是: .
16.平安和健康是幸福生活的前提,科技可以帮助我们更好地保持平安和健康。
(1)某些汽车配置的安全气囊内有叠氮化钠(NaN3)。它是由钠离子和叠氮根离子构成。据此写出叠氮化铜的化学式 ;
(2)在抗疫一线,卫生部使用了负压救护车。负压就是利用技术手段,使车内气压低于外界大气压,所以空气在自由流动时只能由车外向内流动。下列例子中,同样处于负压状态的是 。
A.充完气的轮胎 B.高空飞行中的飞机机舱
C.正在工作的吸尘器 D.烧煮食物的高压锅
参考答案
1.解:化学式右下角的数字表示该物质的一个分子中所含该原子的数目,因此B40中的40表示一个分子中有40个硼原子。
故选:A。
2.解:由反应的结构示意图和模型表示的原子种类,可判断甲为NH3,乙为O2,丙为N2,丁为H2O,反应的化学方程式为:4NH3+3O22N2+6H2O;
A、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,由化学方程式可知,该反应属于置换反应,故A正确;
B、NH3中氢元素的化合价为+1价,则氮元素的化合价为﹣3价,故B错误;
C、由化学方程式可知,反应中甲、乙的质量比:(4×17):(3×32)=17:24;故17g甲完全燃烧至少需要24g乙,故C错误;
D、由化学方程式可知,生成的丙与丁的分子个数比为1:3;故D错误;
故选:A。
3.解:A、物质的组成决定物质的性质,故O3的强氧化性是由O3结构决定的,合理,符合题意;
B、臭氧和氧气的分子含有的氧原子个数不同,等质量的臭氧和氧气含有不同分子数臭氧和氧气的分子含有的氧原子个数不同,等质量的臭氧和氧气含有不同分子数,不合理,不符合题意;
C、相同分子个数的O3与O2中,所含氧原子的个数不同,不合理,不符合题意;
D、构成它们的分子不同,化学性质不同,不合理,不符合题意;
故选:A。
4.解:A、CH4不是氧化物,选项错误;
B、CO是氧化物,碳元素化合价为+2价,选项正确;
C、CO2是氧化物,碳元素化合价为+4价,选项错误;
D、K2CO3是盐,选项错误;
故选:B。
5.解:A、钌元素是金属元素,该选项说法不正确;
B、钌元素质子数是44,该选项说法正确;
C、钌元素相对原子质量是101.1,单位不是g,该选项说法不正确;
D、钌元素与其他元素根本区别是质子数不同,该选项说法不正确。
故选:B。
6.解:同位素为同种元素的不同原子,即D与H属于同种元素,都是氢元素,核内质子数都是1.
故选:B。
7.解:A、该模型表示的是核裂变,该选项说法不正确;
B、该反应产生的中子可继续轰击其他铀核形成链式反应,该选项说法正确;
C、过程中产生的氪原子具有放射性,该选项说法不正确;
D、可以通过核裂变来发电,例如核电站是利用核裂变发电,该选项说法不正确。
故选:B。
8.解:钾元素显+1价,氧元素显﹣2价,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)×3=0,则x=+5价。
故选:D。
9.解:“超临界水”(H2O)是水的液态和气态完全交融在一起的状态,还是属于水,所以分子模型就是水分子模型。
故选:C。
10.解:A.质子数相同的原子属于同一种元素,由题中甲和乙原子的质子数都是6,所以甲和乙是同一种元素,故 A正确;
B.在原子中质子数等于核电荷数,由甲和乙质子数相等可知甲和乙的核电荷数相同,故B不正确;
C.在原子中质子数等于核外电子数,由题中乙和丙质子数不同,所以二者的核外电子数不同,故C不正确;
D.质子数相同中子数不同的原子互为同位素原子,由题中乙和丙的质子数不同,所以乙和丙不是互为同位素,故D不正确。
故选:A。
11.解:A、分子和离子均是构成物质的粒子,H3+和H3都是构成物质的微粒,故选项说法正确。
B、H3是由一种元素组成的纯净物,属于单质,故选项说法正确。
C、一个H3+是1个H3分子失去1个电子得到的,1个H3分子中含有1×3=3个电子,则一个H3+中含有2个电子,故选项说法错误。
D、1个H3分子中含有3个氢原子,一个H3中含有1×3=3个质子,故选项说法正确。
故选:C。
12.解:A、根向地生长是水稻对地球引力刺激作出的反应,A正确;
B、蒸腾作用是根吸水的动力,促进了水和无机盐的运输,蒸腾作用还能降低温度,植物的蒸腾作用散失的水分约占植物吸收水的99%以上。因此,蒸腾作用还能增加大气湿度,增加降水,降低大气温度,调节气候。促进了地球的水循环。因此,茶树从根系吸收进来的大量水分主要用于蒸腾作用。B错误;
C、合理密植,有利于充分利用光能,提高光合效率。种植过密,植物叶片相互遮盖,只有上部叶片进行光合作用,种植过稀,部分光能得不到利用,光能利用率低。因此,种植茶树时要注意合理密植,能提高总产量,C正确;
D、咖啡因的化学式为C8H10N4O2,可见咖啡因中含碳、氢、氮、氧四种元素。D正确。
故选:B。
13.解:(1)电流的方向与带负电荷的粒子定向移动方向相反,因此该实验中电流方向为B→A;
(2)①根据“质量较小的氘核和氚核在超高温下可以聚合成氦核”,可知这种反应称为核聚变;
②A、由带正电的a粒子被带正电荷的原子核推离了原来的运动方向,可知带同种电荷互相排斥,异种电荷互相吸引,故正确;
B、由于带正电的a粒子被带正电荷的原子核推离了原来的运动方向,可知力能改变物体的运动状态,故正确;
C、本实验没有产生电流,因此无法确定电流的方向,故错误;
D、本实验中原子核没有被破坏,不能得出原子核的结构,故错误;
E、电子的质量远小于a粒子,由于原子核外的电子没有改变a粒子的运动方向,因此电子质量太小无法阻挡α粒子轰击,故正确。
故选:ABE。
故答案为:(1)B→A;(2)①核聚变; ②ABE。
14.解:(1)碳﹣14与碳﹣12属于同位素原子,它们的原子核内质子数相同,中子数不相同。
(2)氮﹣14变成碳﹣14,质子数和中子数之和不变,氮原子的质子数为7,碳原子的质子数为6,则其原子核内部粒子的变化情况是质子数减少,中子数增加。
故答案为:
(1)中子数;
(2)质子数减少,中子数增加。
15.解:(1)对比离子符号与其化合价可知:化合价数值与离子数值相同,其符号即正负也相同.
(2)化学式的书写主要是利用化学式书写的一般规律,正价在前负价在后排列,并保证化合价代数和为零.
故答案分别是:(1)电荷数;
(2)化合物中各种元素化合价的代数和等于零.
16.解:(1)叠氮化钠(NaN3)是由钠离子和叠氮根离子构成,叠氮根离子为﹣1价,则形成叠氮化铜的化学式为:Cu(N3)2,故填:Cu(N3)2。
(2)A.充完气的汽车轮胎内的气压大于大气压,不处于负压状态,故错误;
B.高空飞行中的飞机机舱外气体流速大、压强小,小于机舱内的气压,不处于负压状态,故错误;
C.正在工作的吸尘器,内部压强减小,小于外界的大气压,处于负压状态,故正确;
D.烧煮食物的高压锅的气压大于大气压,不处于负压状态,故错误。
故选C。
物质组成与结构
A.原子 B.质子 C.离子 D.电子
2.为减少温室气体排放,人们积极寻找不含碳的燃料,其中NH3燃烧前后分子种类变化的微观示意图如图。下列说法正确的是( )
A.该反应属于置换反应
B.NH3中氮元素的化合价为+3价
C.17g甲完全燃烧至少需要32g乙
D.生成的丙与丁的分子个数比为1:1
3.某家庭式空气净化器在工作时会释放出臭氧(O3),利用其强氧化性杀菌消毒并转化为无污染的氧气(O2)。下列分析合理的是( )
A.O3的强氧化性是由O3分子结构决定的
B.相同质量的O3与O2所含的分子个数相同
C.相同分子个数的O3与O2中,所含氧原子的个数相同
D.O3与O2都由氧元素组成,它们的化学性质完全相同
4.类价图反映的是元素的化合价与物质类别之间的关系。如图是碳元素的类价图,图中物质“乙”是( )
A.CH4 B.CO C.CO2 D.K2CO3
5.元素钌(Ru)是科学家最新发现的一种室温下具有独特磁性的元素,由图可知钌元素( )
A.是非金属元素
B.质子数为44
C.相对原子质量是101.1克
D.与其他元素根本区别是中子数不同
6.中国科学院大连化学物理研究所在H+HD→H2+D反应中,观测到化学反应中的量子干涉现象,该成果入选2020年度中国科学十大进展。氘(D)(又叫重氢),是H元素的同位素,则D与H具有相同的( )
A.原子 B.质子 C.中子 D.电子
7.如图表示用中子轰击铀﹣235原子核产生氪核和钡核的模型。下列叙述正确的是( )
A.该模型表示的是核聚变
B.该反应产生的中子可继续轰击其他铀核形成链式反应
C.该反应不会产生放射性物质
D.不能用该反应获得能量的方式来发电
8.市售的加碘食盐是在食盐中加入一定量的碘酸钾(KIO3),碘酸钾中碘元素的化合价是( )
A.﹣2 B.﹣3 C.+1 D.+5
9.“超临界水”(H2O)因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的状态,用“〇”表示氢原子,“”表示氧原子,下列模型能表示“超临界水”分子的是( )
A. B. C. D.
10.有3种不同的原子,甲原子核内有6个质子和6个中子,乙原子核内有6个质子和8个中子,丙原子核内有7个质子和7个中子。下列说法正确的是( )
A.甲和乙是同一种元素 B.甲和乙的核电荷数不同
C.乙和丙核外电子数相等 D.乙和丙互为同位素原子
11.最新科技报道,夏威夷联合天文中心的科学家在宇宙深处发现H3+离子和H3分子,以下关于它们的说法不正确的是( )
A.H3+和H3都是构成物质的微粒
B.H3是单质
C.一个H3+中含有3个电子
D.一个H3中含有3个质子
12.武阳春雨是我市名茶之一,叶底纤细多芽,为茶中真品。茶叶中的
咖啡因能使中枢神经系统兴奋。咖啡因的化学式为C8H10N4O2,下列说法中错误的是( )
A.茶叶树的根向地生长是植物对地球引力刺激作出的反应
B.茶叶树根吸收的水分主要参与枝叶的生长和花果的发育
C.茶叶树相邻的叶总是不重叠,增大光照面积是对光合作用的适应
D.咖啡因中含碳、氢、氮、氧四种元素
13.科学家为了揭示原子结构的奥秘,经历了漫长的探索过程。原子结构模型发展过程可表示如下:
(1)阴极射线管是能放出阴极射线的仪器,如图甲。汤姆生在1897年提出阴极射线是从阴极放出的带负电的粒子。若把阴极射线AB看成电荷的定向移动,其电流方向为 。
(2)1910年卢瑟福进行了著名的α粒子(a粒子带正电)轰击金箔实验,发现:绝大多数α粒子穿过金箔后仍沿原方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来,如图乙。
①α粒子实质是氦原子核,可由铀、镭等元素得到。在太阳内部,质量较小的氘核和氚核在超高温下可以聚合成氦核,这种反应称为 。
②在分析实验结果的基础上,卢瑟福提出核式结构模型:在原子的中心有一个很小的原子核,原子的全部正电荷和几乎全部的质量都集中在原子核里,带负电的电子在核外空间绕核运动,就像行星绕太阳运动那样。人们掌握的下列事实或原理,有助于当时建立该模型的是 。
A.同种电荷互相排斥,异种电荷互相吸引
B.力能改变物体的运动状态
C.电荷的定向移动形成电流
D.有些原子内没有中子
E.电子由于质量太小无法阻挡α粒子轰击
14.考古时常用死亡生物体内碳﹣14的含量减少一半所需的时间来推测生物的死亡年代。
(1)碳﹣14与碳﹣12属于同位素原子,它们的原子核内 不相同。
(2)大气中的氮﹣14在宇宙射线的作用下会变成碳﹣14,使地球上碳﹣14总量能基本保持不变。从氮﹣14变成碳﹣14,其原子核内部粒子的变化情况
。
15.通过已学习知识的对比和归纳,可以得出一些十分有趣的规律.这些规律可以帮助我们掌握学习化学的方法.请你仔细阅读表中内容,并回答相应的问题.
常见的几种离子 H+ Na+ Mg+ O2﹣
对应元素及原子团在化合物中的化合价
所能形成化合物的化学式 Na2O,MgO,H2O HNO3,H2CO3 MgCO3,NaNO3
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 相等;
(2)由后两行内容对照可得出书写化学式依据的原则是: .
16.平安和健康是幸福生活的前提,科技可以帮助我们更好地保持平安和健康。
(1)某些汽车配置的安全气囊内有叠氮化钠(NaN3)。它是由钠离子和叠氮根离子构成。据此写出叠氮化铜的化学式 ;
(2)在抗疫一线,卫生部使用了负压救护车。负压就是利用技术手段,使车内气压低于外界大气压,所以空气在自由流动时只能由车外向内流动。下列例子中,同样处于负压状态的是 。
A.充完气的轮胎 B.高空飞行中的飞机机舱
C.正在工作的吸尘器 D.烧煮食物的高压锅
参考答案
1.解:化学式右下角的数字表示该物质的一个分子中所含该原子的数目,因此B40中的40表示一个分子中有40个硼原子。
故选:A。
2.解:由反应的结构示意图和模型表示的原子种类,可判断甲为NH3,乙为O2,丙为N2,丁为H2O,反应的化学方程式为:4NH3+3O22N2+6H2O;
A、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,由化学方程式可知,该反应属于置换反应,故A正确;
B、NH3中氢元素的化合价为+1价,则氮元素的化合价为﹣3价,故B错误;
C、由化学方程式可知,反应中甲、乙的质量比:(4×17):(3×32)=17:24;故17g甲完全燃烧至少需要24g乙,故C错误;
D、由化学方程式可知,生成的丙与丁的分子个数比为1:3;故D错误;
故选:A。
3.解:A、物质的组成决定物质的性质,故O3的强氧化性是由O3结构决定的,合理,符合题意;
B、臭氧和氧气的分子含有的氧原子个数不同,等质量的臭氧和氧气含有不同分子数臭氧和氧气的分子含有的氧原子个数不同,等质量的臭氧和氧气含有不同分子数,不合理,不符合题意;
C、相同分子个数的O3与O2中,所含氧原子的个数不同,不合理,不符合题意;
D、构成它们的分子不同,化学性质不同,不合理,不符合题意;
故选:A。
4.解:A、CH4不是氧化物,选项错误;
B、CO是氧化物,碳元素化合价为+2价,选项正确;
C、CO2是氧化物,碳元素化合价为+4价,选项错误;
D、K2CO3是盐,选项错误;
故选:B。
5.解:A、钌元素是金属元素,该选项说法不正确;
B、钌元素质子数是44,该选项说法正确;
C、钌元素相对原子质量是101.1,单位不是g,该选项说法不正确;
D、钌元素与其他元素根本区别是质子数不同,该选项说法不正确。
故选:B。
6.解:同位素为同种元素的不同原子,即D与H属于同种元素,都是氢元素,核内质子数都是1.
故选:B。
7.解:A、该模型表示的是核裂变,该选项说法不正确;
B、该反应产生的中子可继续轰击其他铀核形成链式反应,该选项说法正确;
C、过程中产生的氪原子具有放射性,该选项说法不正确;
D、可以通过核裂变来发电,例如核电站是利用核裂变发电,该选项说法不正确。
故选:B。
8.解:钾元素显+1价,氧元素显﹣2价,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)×3=0,则x=+5价。
故选:D。
9.解:“超临界水”(H2O)是水的液态和气态完全交融在一起的状态,还是属于水,所以分子模型就是水分子模型。
故选:C。
10.解:A.质子数相同的原子属于同一种元素,由题中甲和乙原子的质子数都是6,所以甲和乙是同一种元素,故 A正确;
B.在原子中质子数等于核电荷数,由甲和乙质子数相等可知甲和乙的核电荷数相同,故B不正确;
C.在原子中质子数等于核外电子数,由题中乙和丙质子数不同,所以二者的核外电子数不同,故C不正确;
D.质子数相同中子数不同的原子互为同位素原子,由题中乙和丙的质子数不同,所以乙和丙不是互为同位素,故D不正确。
故选:A。
11.解:A、分子和离子均是构成物质的粒子,H3+和H3都是构成物质的微粒,故选项说法正确。
B、H3是由一种元素组成的纯净物,属于单质,故选项说法正确。
C、一个H3+是1个H3分子失去1个电子得到的,1个H3分子中含有1×3=3个电子,则一个H3+中含有2个电子,故选项说法错误。
D、1个H3分子中含有3个氢原子,一个H3中含有1×3=3个质子,故选项说法正确。
故选:C。
12.解:A、根向地生长是水稻对地球引力刺激作出的反应,A正确;
B、蒸腾作用是根吸水的动力,促进了水和无机盐的运输,蒸腾作用还能降低温度,植物的蒸腾作用散失的水分约占植物吸收水的99%以上。因此,蒸腾作用还能增加大气湿度,增加降水,降低大气温度,调节气候。促进了地球的水循环。因此,茶树从根系吸收进来的大量水分主要用于蒸腾作用。B错误;
C、合理密植,有利于充分利用光能,提高光合效率。种植过密,植物叶片相互遮盖,只有上部叶片进行光合作用,种植过稀,部分光能得不到利用,光能利用率低。因此,种植茶树时要注意合理密植,能提高总产量,C正确;
D、咖啡因的化学式为C8H10N4O2,可见咖啡因中含碳、氢、氮、氧四种元素。D正确。
故选:B。
13.解:(1)电流的方向与带负电荷的粒子定向移动方向相反,因此该实验中电流方向为B→A;
(2)①根据“质量较小的氘核和氚核在超高温下可以聚合成氦核”,可知这种反应称为核聚变;
②A、由带正电的a粒子被带正电荷的原子核推离了原来的运动方向,可知带同种电荷互相排斥,异种电荷互相吸引,故正确;
B、由于带正电的a粒子被带正电荷的原子核推离了原来的运动方向,可知力能改变物体的运动状态,故正确;
C、本实验没有产生电流,因此无法确定电流的方向,故错误;
D、本实验中原子核没有被破坏,不能得出原子核的结构,故错误;
E、电子的质量远小于a粒子,由于原子核外的电子没有改变a粒子的运动方向,因此电子质量太小无法阻挡α粒子轰击,故正确。
故选:ABE。
故答案为:(1)B→A;(2)①核聚变; ②ABE。
14.解:(1)碳﹣14与碳﹣12属于同位素原子,它们的原子核内质子数相同,中子数不相同。
(2)氮﹣14变成碳﹣14,质子数和中子数之和不变,氮原子的质子数为7,碳原子的质子数为6,则其原子核内部粒子的变化情况是质子数减少,中子数增加。
故答案为:
(1)中子数;
(2)质子数减少,中子数增加。
15.解:(1)对比离子符号与其化合价可知:化合价数值与离子数值相同,其符号即正负也相同.
(2)化学式的书写主要是利用化学式书写的一般规律,正价在前负价在后排列,并保证化合价代数和为零.
故答案分别是:(1)电荷数;
(2)化合物中各种元素化合价的代数和等于零.
16.解:(1)叠氮化钠(NaN3)是由钠离子和叠氮根离子构成,叠氮根离子为﹣1价,则形成叠氮化铜的化学式为:Cu(N3)2,故填:Cu(N3)2。
(2)A.充完气的汽车轮胎内的气压大于大气压,不处于负压状态,故错误;
B.高空飞行中的飞机机舱外气体流速大、压强小,小于机舱内的气压,不处于负压状态,故错误;
C.正在工作的吸尘器,内部压强减小,小于外界的大气压,处于负压状态,故正确;
D.烧煮食物的高压锅的气压大于大气压,不处于负压状态,故错误。
故选C。
物质组成与结构
同课章节目录
