人教版(2019)必修一 2.2.1 氯气 课件(共21张PPT)
文档属性
| 名称 | 人教版(2019)必修一 2.2.1 氯气 课件(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 17.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-26 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
新人教版 化学 必修一
第二章 海水中的重要元素
————钠和氯
第二节 氯及其化合物
第1课时:氯气的性质
物理性质
颜色、状态
气味
水溶性
毒性
密度
沸点
黄绿色气体
有刺激性气味
有毒
比空气大
能溶于水
沸点低
水溶液称为氯水
易液化,液态称为液氯
钢瓶
Cl2与Fe不反应吗
化学性质
与金属单质反应
现象
剧烈燃烧
Fe
棕红色的烟
常温下铁与氯气不反应
2Fe+3Cl2 2FeCl3
△
化学性质
与金属单质反应
Na
现象
剧烈燃烧
白色的烟
2Na+Cl2 2NaCl
△
Fe
棕红色的烟
2Fe+3Cl2 2FeCl3
△
化学性质
与金属单质反应
Cu
现象
剧烈燃烧
棕黄色的烟
Na
白色的烟
2Na+Cl2 2NaCl
△
Fe
棕红色的烟
2Fe+3Cl2 2FeCl3
△
Cu+Cl2 CuCl2
△
化学性质
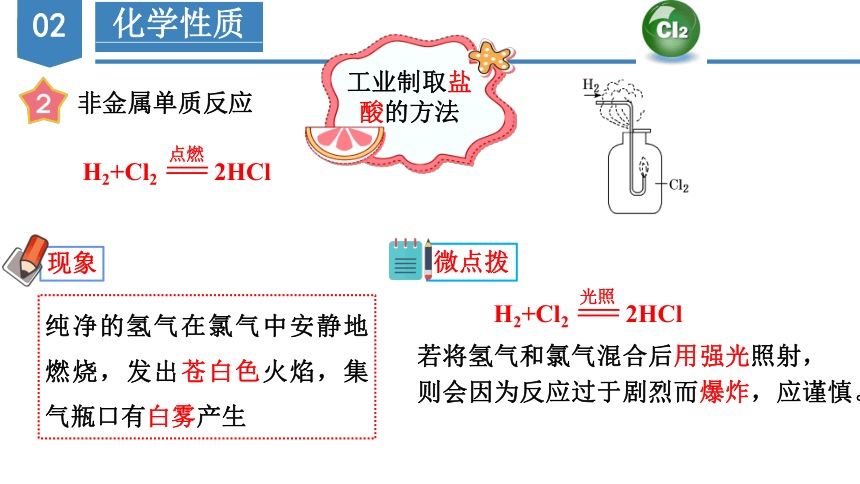
非金属单质反应
纯净的氢气在氯气中安静地燃烧,发出苍白色火焰,集气瓶口有白雾产生
现象
微点拨
若将氢气和氯气混合后用强光照射,
则会因为反应过于剧烈而爆炸,应谨慎。
H2+Cl2 2HCl
点燃
H2+Cl2 2HCl
光照
工业制取盐酸的方法
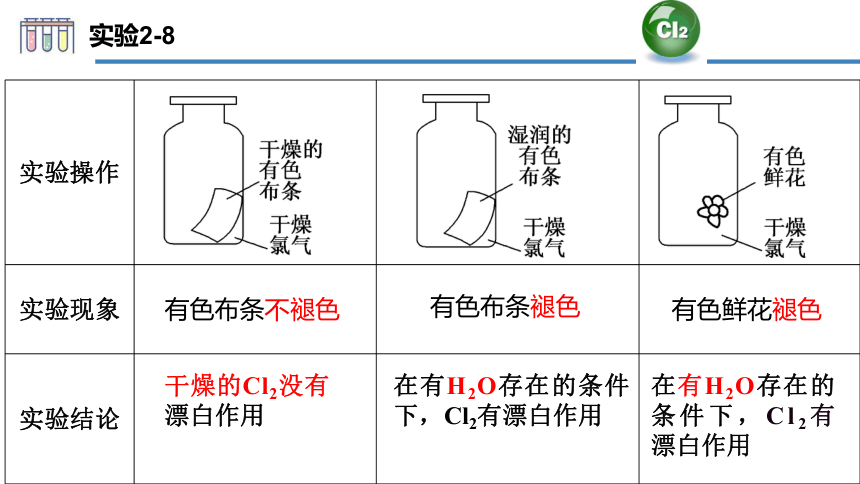
实验2-8
实验操作
实验现象
实验结论
有色布条不褪色
有色布条褪色
有色鲜花褪色
干燥的Cl2没有漂白作用
在有H2O存在的条件下,Cl2有漂白作用
在有H2O存在的条件下,Cl2有漂白作用
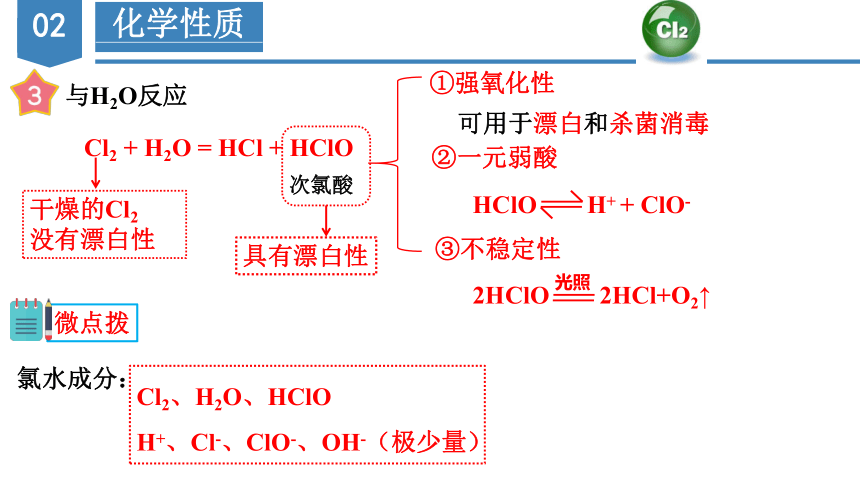
化学性质
与H2O反应
Cl2 + H2O = HCl + HClO
次氯酸
①强氧化性
可用于漂白和杀菌消毒
②一元弱酸
HClO H+ + ClO-
③不稳定性
2HClO 2HCl+O2↑
光照
微点拨
Cl2、H2O、HClO
H+、Cl-、ClO-、OH-(极少量)
氯水成分:
具有漂白性
干燥的Cl2
没有漂白性
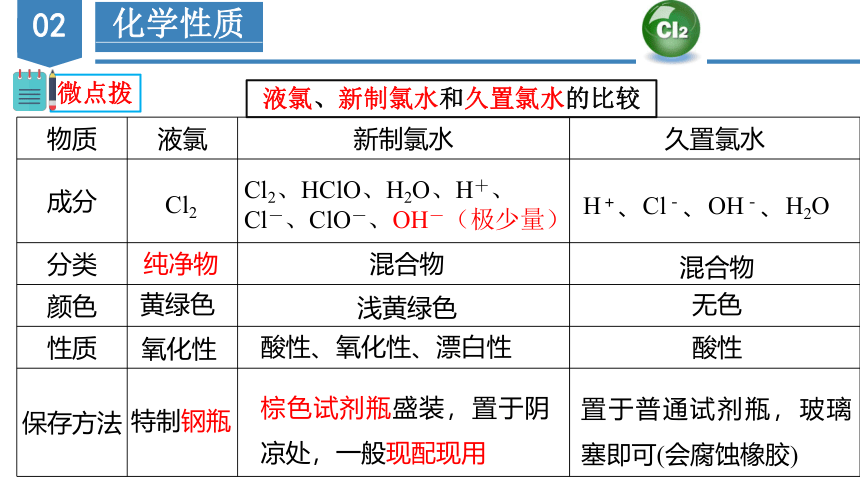
化学性质
物质 液氯 新制氯水 久置氯水
成分
分类
颜色
性质
保存方法
液氯、新制氯水和久置氯水的比较
微点拨
Cl2
Cl2、HClO、H2O、H+、
Cl-、ClO-、OH-(极少量)
H+、Cl-、OH-、H2O
纯净物
混合物
混合物
黄绿色
浅黄绿色
无色
氧化性
酸性、氧化性、漂白性
酸性
特制钢瓶
棕色试剂瓶盛装,置于阴凉处,一般现配现用
置于普通试剂瓶,玻璃塞即可(会腐蚀橡胶)
化学性质
与碱反应
Cl2+2NaOH===NaCl+NaClO+H2O
2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(工业上制取漂白液原理)
(工业上制取漂白粉原理)
(1)Cl2与NaOH溶液反应
(2)氯气通入冷的石灰乳
有效成分
有效成分
(工业上制取漂粉精原理)
充分反应
主要成分
氯气的尾气处理
化学性质
与碱反应
Cl2+2NaOH===NaCl+NaClO+H2O
(1)Cl2与NaOH溶液反应
Cl2+2OH- === Cl-+ClO-+H2O
Cl2的尾气处理
制漂白液
2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(2)氯气通入冷的石灰乳
Cl2+Ca(OH)2===Ca2++Cl-+ClO-+H2O
制漂白粉和漂粉精
化学性质
Ca(ClO)2 + CO2 + H2O = CaCO3↓ + 2HClO
(1)漂白粉的漂白原理
微点拨
(2)漂白粉的失效原理
Ca(ClO)2 + CO2 + H2O = CaCO3↓ + 2HClO
2HClO 2HCl+O2↑
光照
化学性质
与还原性物质反应
I-
Br -
S2-
SO2
Fe2+
Cl2+2Br- === 2Cl-+Br2
Cl2+2Fe2+ === 2Cl-+2Fe3+
Cl2+2I- === 2Cl-+I2
Cl2+S2- === 2Cl-+S
Cl2+SO2+2H2O === 4H+ + 2Cl-+SO42-
存在与用途
在自然界中除了以 MgCl2 、 NaCl 、 CaCl2等形式
大量存在于海水中,还存在于陆地的盐湖和盐矿中。
1.存在
氯是一种重要的“成盐元素”
存在与用途
氯气是一种重要的化工原料,大量用于制造盐酸、 有机溶剂 、
农药 、染料和 药品 等。
氯气用于自来水消毒时,因与水中的有机物反应,生成的有机氯化物可能对人体有害,所以要严格控制饮用水中余氯的含量,并开始使用二氧化氯(ClO2)、 臭氧(O3) 等新的自来水消毒剂。
2.用途
1.某城市以“液氯泄漏”作应急预警演习,演习时,下列防护措施合理的是
①及时向上风口和地势较高处转移疏散人群;
②及时戴上用浓烧碱溶液湿润过的口罩;
③用高压水枪向泄露口附近喷洒稀碱液并设法控制氯气泄漏;
④及时戴上用稀纯碱溶液湿润过的口罩;
⑤及时用毛巾包裹活性炭捂住口鼻;
⑥就近向地下商场转移。
A.②③④⑤ B.①②④⑤ C.①③④⑤ D.①③④⑥
C
2.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是
①氯气 ②液氯 ③新制氯水 ④盐酸
A.①② B.①②③ C.③ D.③④
C
3.下列有关氯气及其性质、用途的叙述中不正确的是( )
A.氯气分子是由两个氯原子构成的双原子分子
B.通常情况下,氯气呈黄绿色,有刺激性气味,比空气重,能溶于水
C.氯气能与大多数金属单质直接化合,生成金属氯化物
D.工业上常用氢气在氯气中燃烧来制备氯化氢
C
4.某同学误用氯气消毒的自来水配制下列溶液:①Na2S;②KI;③FeCl3;④FeSO4;⑤AgNO3;⑥稀盐酸,可能导致溶液变质的有( )
A.4种 B.3种 C.2种 D.1种
A
5.下列反应的离子方程式书写不正确的是( )
A.氯气溶于水:Cl2+ H2O=H+ +Cl- + HClOB.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2OC.钠与水反应:Na+2H2O=Na++2OH- +H2↑D.过氧化钠投入水中:2Na2O2+2H2O =O2↑+4Na+ +4OH-
C
氯气的
物理性质
01
氯气的
化学性质
02
与金属单质反应
与非金属单质反应
与水反应
与碱反应
与还原性物质反应
存在与用途
03
新人教版 化学 必修一
第二章 海水中的重要元素
————钠和氯
第二节 氯及其化合物
第1课时:氯气的性质
物理性质
颜色、状态
气味
水溶性
毒性
密度
沸点
黄绿色气体
有刺激性气味
有毒
比空气大
能溶于水
沸点低
水溶液称为氯水
易液化,液态称为液氯
钢瓶
Cl2与Fe不反应吗
化学性质
与金属单质反应
现象
剧烈燃烧
Fe
棕红色的烟
常温下铁与氯气不反应
2Fe+3Cl2 2FeCl3
△
化学性质
与金属单质反应
Na
现象
剧烈燃烧
白色的烟
2Na+Cl2 2NaCl
△
Fe
棕红色的烟
2Fe+3Cl2 2FeCl3
△
化学性质
与金属单质反应
Cu
现象
剧烈燃烧
棕黄色的烟
Na
白色的烟
2Na+Cl2 2NaCl
△
Fe
棕红色的烟
2Fe+3Cl2 2FeCl3
△
Cu+Cl2 CuCl2
△
化学性质
非金属单质反应
纯净的氢气在氯气中安静地燃烧,发出苍白色火焰,集气瓶口有白雾产生
现象
微点拨
若将氢气和氯气混合后用强光照射,
则会因为反应过于剧烈而爆炸,应谨慎。
H2+Cl2 2HCl
点燃
H2+Cl2 2HCl
光照
工业制取盐酸的方法
实验2-8
实验操作
实验现象
实验结论
有色布条不褪色
有色布条褪色
有色鲜花褪色
干燥的Cl2没有漂白作用
在有H2O存在的条件下,Cl2有漂白作用
在有H2O存在的条件下,Cl2有漂白作用
化学性质
与H2O反应
Cl2 + H2O = HCl + HClO
次氯酸
①强氧化性
可用于漂白和杀菌消毒
②一元弱酸
HClO H+ + ClO-
③不稳定性
2HClO 2HCl+O2↑
光照
微点拨
Cl2、H2O、HClO
H+、Cl-、ClO-、OH-(极少量)
氯水成分:
具有漂白性
干燥的Cl2
没有漂白性
化学性质
物质 液氯 新制氯水 久置氯水
成分
分类
颜色
性质
保存方法
液氯、新制氯水和久置氯水的比较
微点拨
Cl2
Cl2、HClO、H2O、H+、
Cl-、ClO-、OH-(极少量)
H+、Cl-、OH-、H2O
纯净物
混合物
混合物
黄绿色
浅黄绿色
无色
氧化性
酸性、氧化性、漂白性
酸性
特制钢瓶
棕色试剂瓶盛装,置于阴凉处,一般现配现用
置于普通试剂瓶,玻璃塞即可(会腐蚀橡胶)
化学性质
与碱反应
Cl2+2NaOH===NaCl+NaClO+H2O
2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(工业上制取漂白液原理)
(工业上制取漂白粉原理)
(1)Cl2与NaOH溶液反应
(2)氯气通入冷的石灰乳
有效成分
有效成分
(工业上制取漂粉精原理)
充分反应
主要成分
氯气的尾气处理
化学性质
与碱反应
Cl2+2NaOH===NaCl+NaClO+H2O
(1)Cl2与NaOH溶液反应
Cl2+2OH- === Cl-+ClO-+H2O
Cl2的尾气处理
制漂白液
2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(2)氯气通入冷的石灰乳
Cl2+Ca(OH)2===Ca2++Cl-+ClO-+H2O
制漂白粉和漂粉精
化学性质
Ca(ClO)2 + CO2 + H2O = CaCO3↓ + 2HClO
(1)漂白粉的漂白原理
微点拨
(2)漂白粉的失效原理
Ca(ClO)2 + CO2 + H2O = CaCO3↓ + 2HClO
2HClO 2HCl+O2↑
光照
化学性质
与还原性物质反应
I-
Br -
S2-
SO2
Fe2+
Cl2+2Br- === 2Cl-+Br2
Cl2+2Fe2+ === 2Cl-+2Fe3+
Cl2+2I- === 2Cl-+I2
Cl2+S2- === 2Cl-+S
Cl2+SO2+2H2O === 4H+ + 2Cl-+SO42-
存在与用途
在自然界中除了以 MgCl2 、 NaCl 、 CaCl2等形式
大量存在于海水中,还存在于陆地的盐湖和盐矿中。
1.存在
氯是一种重要的“成盐元素”
存在与用途
氯气是一种重要的化工原料,大量用于制造盐酸、 有机溶剂 、
农药 、染料和 药品 等。
氯气用于自来水消毒时,因与水中的有机物反应,生成的有机氯化物可能对人体有害,所以要严格控制饮用水中余氯的含量,并开始使用二氧化氯(ClO2)、 臭氧(O3) 等新的自来水消毒剂。
2.用途
1.某城市以“液氯泄漏”作应急预警演习,演习时,下列防护措施合理的是
①及时向上风口和地势较高处转移疏散人群;
②及时戴上用浓烧碱溶液湿润过的口罩;
③用高压水枪向泄露口附近喷洒稀碱液并设法控制氯气泄漏;
④及时戴上用稀纯碱溶液湿润过的口罩;
⑤及时用毛巾包裹活性炭捂住口鼻;
⑥就近向地下商场转移。
A.②③④⑤ B.①②④⑤ C.①③④⑤ D.①③④⑥
C
2.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是
①氯气 ②液氯 ③新制氯水 ④盐酸
A.①② B.①②③ C.③ D.③④
C
3.下列有关氯气及其性质、用途的叙述中不正确的是( )
A.氯气分子是由两个氯原子构成的双原子分子
B.通常情况下,氯气呈黄绿色,有刺激性气味,比空气重,能溶于水
C.氯气能与大多数金属单质直接化合,生成金属氯化物
D.工业上常用氢气在氯气中燃烧来制备氯化氢
C
4.某同学误用氯气消毒的自来水配制下列溶液:①Na2S;②KI;③FeCl3;④FeSO4;⑤AgNO3;⑥稀盐酸,可能导致溶液变质的有( )
A.4种 B.3种 C.2种 D.1种
A
5.下列反应的离子方程式书写不正确的是( )
A.氯气溶于水:Cl2+ H2O=H+ +Cl- + HClOB.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2OC.钠与水反应:Na+2H2O=Na++2OH- +H2↑D.过氧化钠投入水中:2Na2O2+2H2O =O2↑+4Na+ +4OH-
C
氯气的
物理性质
01
氯气的
化学性质
02
与金属单质反应
与非金属单质反应
与水反应
与碱反应
与还原性物质反应
存在与用途
03
