化学人教版(2019)必修第二册7.3.2乙酸(共15张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3.2乙酸(共15张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 193.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-26 00:00:00 | ||
图片预览





文档简介
人教版必修第二册
第七章 有机化合物
第三节 乙醇与乙酸
第2课时 乙酸
【学习目标与核心素养】
搭建乙酸的球棍模型,与乙醇和水对比,认识乙酸的物理性质和化学性质。
PART
01
PART
02
PART
03
认识乙酸的官能团——羧基的性质,知道酯化反应的原理
知道官能团是辨识有机化合物类别与决定有机化合物特性的特征基团
【情景引入】饮食中的有机物——乙酸
任务一 认识乙酸的物理性质
活动1 通过观察乙酸的颜色和状态,闻一闻乙酸的气味(扇闻法)
(参照资料卡片和生活经验)
无色
颜色:
液体
状态:
强烈刺激性
气味:
易挥发
挥发性:
易溶于水和乙醇
溶解性:
熔点:
16.6℃
1.乙酸的物理性质
注意:温度低于16.6℃时,乙酸会凝结成冰一样的晶体,因此纯净的乙酸又称为冰醋酸
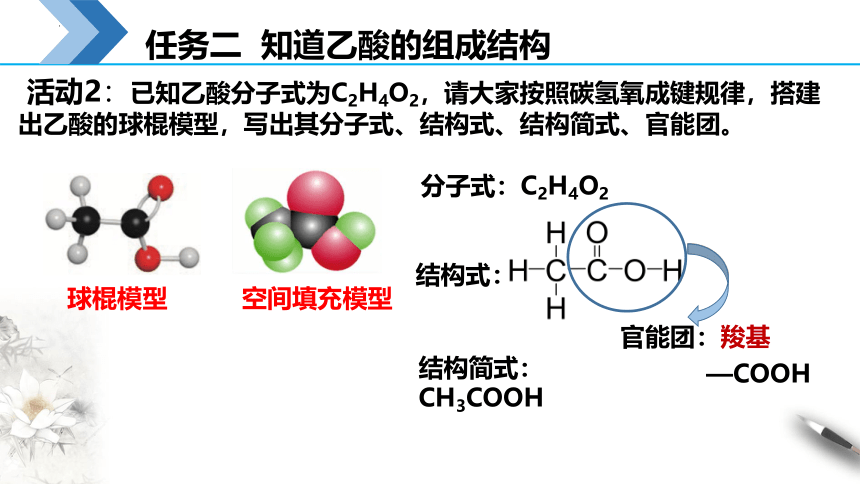
任务二 知道乙酸的组成结构
活动2:已知乙酸分子式为C2H4O2,请大家按照碳氢氧成键规律,搭建出乙酸的球棍模型,写出其分子式、结构式、结构简式、官能团。
球棍模型
空间填充模型
分子式:C2H4O2
结构式:
结构简式:CH3COOH
官能团:羧基
—COOH
任务三 乙酸的化学性质
活动1 设计实验,证明乙酸具有酸的通性
可选试剂:乙酸溶液、镁条、Na2CO3粉末、NaOH溶液、石蕊、酚酞等
可行的方案:
1.乙酸溶液中加入石蕊
2.取一小段镁条,加入乙酸溶液
3.取1mL NaOH溶液,加入几滴酚酞,再加入乙酸溶液
4.取一定量Na2CO3粉末,加入1mL 乙酸溶液
学以致用——如何像葛优一样优雅地剥生鸡蛋?
实验用品:
乙酸溶液、鹌鹑蛋、小烧杯。
分组实验:注意观察实验现象。
【思考与讨论】这利用了乙酸的什么性质?请写出有关反应方程式。醋酸和碳酸的酸性强弱?
2CH3COOH + CaCO3 = (CH3COO)2Ca +H2O+CO2↑
酸性强弱: CH3COOH>H2CO3
名称
乙酸
水
乙醇
碳酸
分子结构
CH3COOH
H—OH
C2H5OH
?
遇石蕊溶液
变红
不变红
不变红
变红
与Na
反应
反应
反应
反应
与NaOH
与Na2CO3
反应
?
不反应
反应
羟基氢的活泼性强弱
CH3COOH>H2CO3>H2O>C2H5OH
乙酸、水、乙醇、碳酸的性质比较
含羟基
酸性
不仅有酸性,且酸性大于碳酸
任务四 探究乙酸的酯化反应
俗话说:“姜是老的辣,酒是陈的香。”
厨师烧鱼时常加醋并加点酒,
这样鱼的味道就变得香醇,特别鲜美
这是为什么呢
活动1:【实验7-4】观看乙酸和乙醇反应视频,观察并记录实验现象
任务四 探究乙酸的酯化反应
任务四 探究乙酸的酯化反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}宏观现象
化学键的变化
反应机理/实质
溶液分层,上层有无色油状液体生成,可闻到香味。
断CO-OH键、醇中的O-H键,酸和醇形成了-COO-键(酯基)。
酸脱羟基醇脱氢
活动1 探究酯化反应的原理
活动2 使用球棍模型模拟酯化反应
同位素原子示踪法
探究化学反应机理的重要方法
任务四 探究乙酸的酯化反应
浓硫酸作用:催化剂,吸水剂
加物顺序:乙醇→浓硫酸→乙酸
碎瓷片防暴沸
饱和Na2CO3作用:
①溶解乙醇;
②中和乙酸;
③降低乙酸乙酯的溶解度,利于酯的析出
长导管冷凝、回流、导气作用
导管在饱和Na2CO3液面上:防止倒吸
问题1:如何分离提纯产物?
问题2:如何从减少反应物挥发的角度改进装置,提高反应物的转化率?
冷凝回流
分液
任务五 乙酸的用途
有机化工原料
农药
染料
醋酸纤维
香料
喷漆溶剂
医药
合成纤维
乙酸
归纳整合——建立结构化知识网络
结构
性质
用途
决定
决定
反映
反映
官能团:
物理性质:易挥发
酯化反应
弱酸性
化学性质
练习与评价
1.如图是某种有机物的简易球棍模型,该有机物中只含有C、H、O三种元素。下列有关于该有机物的说法中不正确的是( )
A.分子式是C3H6O2 B.不能和NaOH溶液反应
C.能发生酯化反应 D.能使紫色石蕊溶液变红
2、写出甲醇和丙醇与乙酸反应的方程式
CH3COOH + CH3CH2CH2OH CH3COOCH2CH2CH3 + H2O
甲醇与乙酸反应:
CH3COOH+ CH3OH CH3COOCH3 + H2O
浓H2SO4
浓H2SO4
Δ
Δ
丙醇与乙酸反应:
第七章 有机化合物
第三节 乙醇与乙酸
第2课时 乙酸
【学习目标与核心素养】
搭建乙酸的球棍模型,与乙醇和水对比,认识乙酸的物理性质和化学性质。
PART
01
PART
02
PART
03
认识乙酸的官能团——羧基的性质,知道酯化反应的原理
知道官能团是辨识有机化合物类别与决定有机化合物特性的特征基团
【情景引入】饮食中的有机物——乙酸
任务一 认识乙酸的物理性质
活动1 通过观察乙酸的颜色和状态,闻一闻乙酸的气味(扇闻法)
(参照资料卡片和生活经验)
无色
颜色:
液体
状态:
强烈刺激性
气味:
易挥发
挥发性:
易溶于水和乙醇
溶解性:
熔点:
16.6℃
1.乙酸的物理性质
注意:温度低于16.6℃时,乙酸会凝结成冰一样的晶体,因此纯净的乙酸又称为冰醋酸
任务二 知道乙酸的组成结构
活动2:已知乙酸分子式为C2H4O2,请大家按照碳氢氧成键规律,搭建出乙酸的球棍模型,写出其分子式、结构式、结构简式、官能团。
球棍模型
空间填充模型
分子式:C2H4O2
结构式:
结构简式:CH3COOH
官能团:羧基
—COOH
任务三 乙酸的化学性质
活动1 设计实验,证明乙酸具有酸的通性
可选试剂:乙酸溶液、镁条、Na2CO3粉末、NaOH溶液、石蕊、酚酞等
可行的方案:
1.乙酸溶液中加入石蕊
2.取一小段镁条,加入乙酸溶液
3.取1mL NaOH溶液,加入几滴酚酞,再加入乙酸溶液
4.取一定量Na2CO3粉末,加入1mL 乙酸溶液
学以致用——如何像葛优一样优雅地剥生鸡蛋?
实验用品:
乙酸溶液、鹌鹑蛋、小烧杯。
分组实验:注意观察实验现象。
【思考与讨论】这利用了乙酸的什么性质?请写出有关反应方程式。醋酸和碳酸的酸性强弱?
2CH3COOH + CaCO3 = (CH3COO)2Ca +H2O+CO2↑
酸性强弱: CH3COOH>H2CO3
名称
乙酸
水
乙醇
碳酸
分子结构
CH3COOH
H—OH
C2H5OH
?
遇石蕊溶液
变红
不变红
不变红
变红
与Na
反应
反应
反应
反应
与NaOH
与Na2CO3
反应
?
不反应
反应
羟基氢的活泼性强弱
CH3COOH>H2CO3>H2O>C2H5OH
乙酸、水、乙醇、碳酸的性质比较
含羟基
酸性
不仅有酸性,且酸性大于碳酸
任务四 探究乙酸的酯化反应
俗话说:“姜是老的辣,酒是陈的香。”
厨师烧鱼时常加醋并加点酒,
这样鱼的味道就变得香醇,特别鲜美
这是为什么呢
活动1:【实验7-4】观看乙酸和乙醇反应视频,观察并记录实验现象
任务四 探究乙酸的酯化反应
任务四 探究乙酸的酯化反应
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}宏观现象
化学键的变化
反应机理/实质
溶液分层,上层有无色油状液体生成,可闻到香味。
断CO-OH键、醇中的O-H键,酸和醇形成了-COO-键(酯基)。
酸脱羟基醇脱氢
活动1 探究酯化反应的原理
活动2 使用球棍模型模拟酯化反应
同位素原子示踪法
探究化学反应机理的重要方法
任务四 探究乙酸的酯化反应
浓硫酸作用:催化剂,吸水剂
加物顺序:乙醇→浓硫酸→乙酸
碎瓷片防暴沸
饱和Na2CO3作用:
①溶解乙醇;
②中和乙酸;
③降低乙酸乙酯的溶解度,利于酯的析出
长导管冷凝、回流、导气作用
导管在饱和Na2CO3液面上:防止倒吸
问题1:如何分离提纯产物?
问题2:如何从减少反应物挥发的角度改进装置,提高反应物的转化率?
冷凝回流
分液
任务五 乙酸的用途
有机化工原料
农药
染料
醋酸纤维
香料
喷漆溶剂
医药
合成纤维
乙酸
归纳整合——建立结构化知识网络
结构
性质
用途
决定
决定
反映
反映
官能团:
物理性质:易挥发
酯化反应
弱酸性
化学性质
练习与评价
1.如图是某种有机物的简易球棍模型,该有机物中只含有C、H、O三种元素。下列有关于该有机物的说法中不正确的是( )
A.分子式是C3H6O2 B.不能和NaOH溶液反应
C.能发生酯化反应 D.能使紫色石蕊溶液变红
2、写出甲醇和丙醇与乙酸反应的方程式
CH3COOH + CH3CH2CH2OH CH3COOCH2CH2CH3 + H2O
甲醇与乙酸反应:
CH3COOH+ CH3OH CH3COOCH3 + H2O
浓H2SO4
浓H2SO4
Δ
Δ
丙醇与乙酸反应:
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
