化学人教版(2019)必修第二册7.3.2乙酸(共24张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3.2乙酸(共24张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 20.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-28 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
醋的来历
酉
廿
一
日
相传古代的时候醋是酒圣杜康的儿子黑塔发明的。
杜康发明了酒,他儿子黑塔在作坊里提水、搬缸什么都干,慢慢也学会了酿酒技术。后来,黑塔酿酒后觉得酒糟扔掉可惜,就存放起来,在缸里浸泡。
到了二十一日的酉时,一开缸,一股从来没有闻过的香气扑鼻而来。在浓郁的香味诱惑下,黑塔尝了一口,酸甜兼备,味道很美,便贮藏着作为“调味浆”。
黑塔把二十一日加“酉”字来命名这种调料叫“醋”。
第七章 有机化合物
第二课时 乙酸
第三节 乙醇和乙酸
必修第二册
一、乙酸的物理性质
1. 乙酸的物理性质
俗 称:
色态味:
挥发性:
沸 点:
熔 点:
溶解性:
醋酸
无色强烈刺激性气味液体
易挥发
16.6℃
易溶于水和乙醇
117.9℃
当温度低于16.6℃时,乙酸就凝结为类似于冰一样的晶体,
所以纯净的乙酸又称冰醋酸。
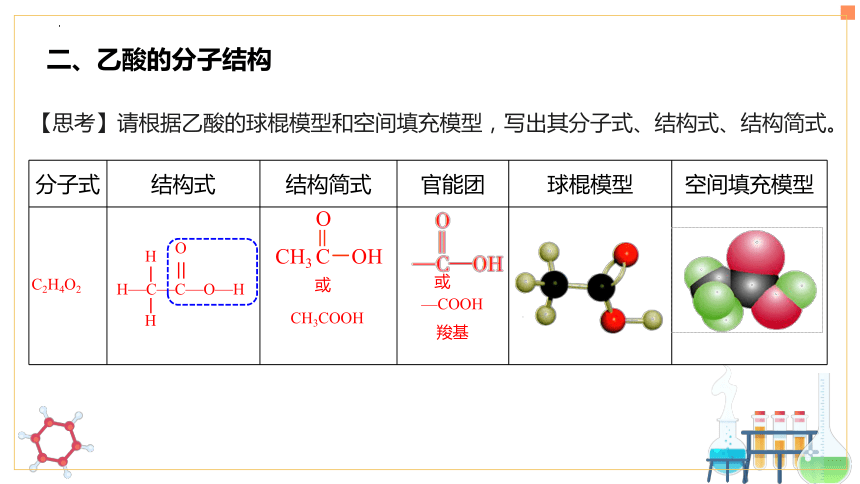
分子式 结构式 结构简式 官能团 球棍模型 空间填充模型
C2H4O2
羧基
CH3COOH
O
CH3 C-OH
或
H
O
H
H—C—C—O—H
【思考】请根据乙酸的球棍模型和空间填充模型,写出其分子式、结构式、结构简式。
—COOH
或
二、乙酸的分子结构
三、乙酸的化学性质
1. 酸性
乙酸是一元弱酸,具有酸的通性。
1)与指示剂反应
2)与金属反应(Na)
3)与金属氧化物反应(Na2O)
4)与碱作用(NaOH)
5)与盐作用(Na2CO3)
电离方程式:
CH3COOH CH3COO- + H+
2CH3COOH+2Na→2CH3COONa+H2↑
CH3COOH+NaOH→CH3COONa+H2O
2CH3COOH+Na2O→2CH3COONa+H2O
2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
使紫色石蕊溶液变红
食醋可以清除水壶中的少量水垢(主要成分是碳酸钙),这是利用了乙酸的什么性质?请写出相关反应的化学方程式。
酸性,2CH3COOH + CaCO3 === (CH3COO)2Ca +H2O+CO2↑
酸性强弱: CH3COOH>H2CO3
思考讨论
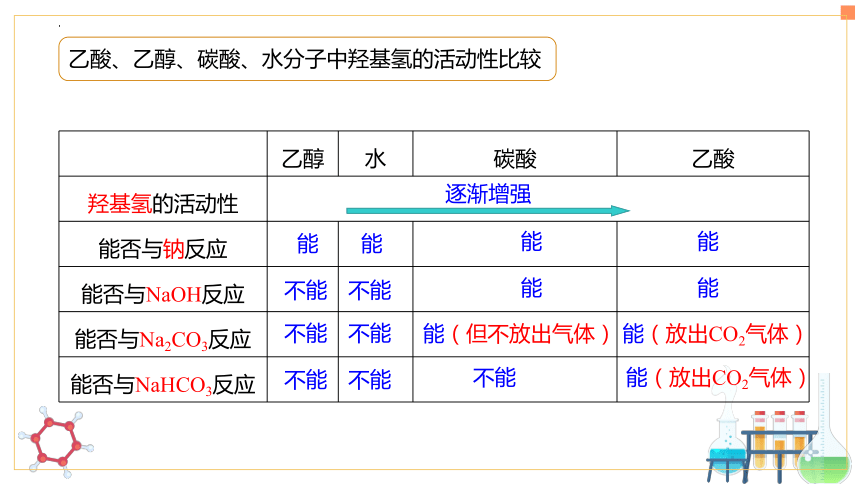
乙酸、乙醇、碳酸、水分子中羟基氢的活动性比较
乙醇 水 碳酸 乙酸
羟基氢的活动性 能否与钠反应
能否与NaOH反应
能否与Na2CO3反应
能否与NaHCO3反应
逐渐增强
能
能
能
能
能
能
能(放出CO2气体)
不能
不能
不能
不能
能(但不放出气体)
不能
不能
不能
能(放出CO2气体)
(1)在标准状况下醋酸是一种无色有强烈刺激性气味的液体( )
(2)乙酸中含有双键,因此属于不饱和烃( )
(3)乙酸分子中含有4个H原子,故为四元酸( )
(4)乙酸分子中含有 和—OH两种官能团( )
(5)乙酸的结构简式可以写成CH3COOH或COOHCH3( )
(6)乙酸可以和碳酸盐反应生成二氧化碳( )
×
√
×
×
×
×
提示 醋酸的熔点为16.6 ℃,在标准状况下,醋酸为无色晶体。
提示 乙酸分子中只有—COOH中的氢原子可以电离,故为一元酸。
判断正误
在做鱼时会加醋和酒,这样鱼会更香醇鲜美,你知道为什么吗?
【实验7-6】在一支试管中加入3mL乙醇,然后边振荡试管边慢慢加入2 mL浓硫酸和2 mL乙酸,再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和Na2CO3溶液的液面上,观察现象。
2. 酯化反应
实验探究
现象:液面分层,液面上层有无色透明不溶于水的油状液体产生,并可以闻到香味。
结论: 在浓硫酸、加热的条件下,乙酸和乙醇发生反应,生成无色、透明、不溶于水、有香味的油状液体。该油状液体是乙酸乙酯。
浓硫酸
CH3COOH + HOC2H5 CH3COOC2H5+H2O
碎瓷片防暴沸
导管在饱和Na2CO3液面上:防止倒吸
长导管冷凝、回流、导气作用
加物顺序:乙醇→浓硫酸→乙酸
饱和Na2CO3作用
①溶解乙醇;
②中和乙酸;
③降低乙酸乙酯的溶解度,利于酯的析出
浓硫酸:催化剂、吸水剂
沸点:
乙酸乙酯(77.1)
乙醇(78.3 ℃ )
乙酸(118℃)
酯化反应注意事项
小心加热:减少乙酸、乙醇的挥发。
加热:加快反应速率,蒸出乙酸乙酯,提高乙酸转化率。
分离碳酸钠和乙酸乙酯:分液
O
CH3—C—O—H+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓硫酸
CH3—C—O—H+H—O—C2H5 CH3—C—O—C2H5 +H2O
浓硫酸
=
=
O
O
乙酸和乙醇可能是以怎样的方式相互结合形成乙酸乙酯的?
思考探索
浓硫酸
CH3COOH + HOC2H5 CH3COOC2H5+H2O
=
O
18O
18O
同位素示踪法
CH3—C—OH + H—18O—C2H5
浓硫酸
=
O
CH3—C—18O—C2H5 + H2O
=
O
CH3COOH + HOCH3
浓硫酸
CH3COOCH3 + H2O
乙酸甲酯
HCOOH + HOCH2CH3
浓硫酸
HCOOCH2CH3 + H2O
甲酸乙酯
酯化反应实质:酸脱羟基,醇脱氢
酯化反应
——取代反应
定义:
酸跟醇起作用,生成酯和水的反应
实质:
酸脱羟基、醇脱氢 (羟基氢)
O
CH3—C—OH + H—18O—C2H5
浓硫酸
△
H2O
+ CH3—C— 18O—C2H5
O
乙酸乙酯(香味)
可逆反应
酯基
2. 酯化反应
很多鲜花和水果的香味都来自酯,如草莓中含有乙酸乙酯和乙酸异戊酯,苹果中含有戊酸戊酯等。
这些分子中碳原子数少、相对分子质量较小的低级酯具有一定的挥发性,有芳香气味,难溶于水,可用作饮料、糖果、化妆品中的香料和有机溶剂。
酯类广泛存在于自然界中
酒是陈的香
有机酸 + 醇 → 酯
有特殊香味
O
CH3—C—O—H
①
②
①弱酸性,具有酸的通性;酸性比碳酸强。
②酯化反应
浓硫酸
结构
性质
决定
归纳总结
有机化工原料
农药
染料
醋酸纤维
香料
喷漆溶剂
医药
合成纤维
四、乙酸的用途
1. 某有机物的结构简式如图,下列关于该有机物的说法正确的是( )
B
A.分子式为C7H6O5
B.1 mol该物质能与4 mol Na发生反应
C.分子中含有两种官能团
D.在水溶液中羧基和羟基均能电离出H+
A.其分子式为C15H20O4
B.该物质不能使酸性KMnO4溶液褪色
C.能发生加成反应、取代反应、氧化反应、酯化反应
D.1 mol该物质与足量NaOH溶液反应,最多消耗1 mol NaOH
2. 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开。S-诱抗素的分子结构如图所示,下列关于该分子的说法不正确的是
B
3. 1 mol 分别与Na、NaOH、NaHCO3、Na2CO3完全反应时,
消耗的Na、NaOH、NaHCO3、Na2CO3的物质的量之比为多少
4∶2∶2∶1
醋的来历
酉
廿
一
日
相传古代的时候醋是酒圣杜康的儿子黑塔发明的。
杜康发明了酒,他儿子黑塔在作坊里提水、搬缸什么都干,慢慢也学会了酿酒技术。后来,黑塔酿酒后觉得酒糟扔掉可惜,就存放起来,在缸里浸泡。
到了二十一日的酉时,一开缸,一股从来没有闻过的香气扑鼻而来。在浓郁的香味诱惑下,黑塔尝了一口,酸甜兼备,味道很美,便贮藏着作为“调味浆”。
黑塔把二十一日加“酉”字来命名这种调料叫“醋”。
第七章 有机化合物
第二课时 乙酸
第三节 乙醇和乙酸
必修第二册
一、乙酸的物理性质
1. 乙酸的物理性质
俗 称:
色态味:
挥发性:
沸 点:
熔 点:
溶解性:
醋酸
无色强烈刺激性气味液体
易挥发
16.6℃
易溶于水和乙醇
117.9℃
当温度低于16.6℃时,乙酸就凝结为类似于冰一样的晶体,
所以纯净的乙酸又称冰醋酸。
分子式 结构式 结构简式 官能团 球棍模型 空间填充模型
C2H4O2
羧基
CH3COOH
O
CH3 C-OH
或
H
O
H
H—C—C—O—H
【思考】请根据乙酸的球棍模型和空间填充模型,写出其分子式、结构式、结构简式。
—COOH
或
二、乙酸的分子结构
三、乙酸的化学性质
1. 酸性
乙酸是一元弱酸,具有酸的通性。
1)与指示剂反应
2)与金属反应(Na)
3)与金属氧化物反应(Na2O)
4)与碱作用(NaOH)
5)与盐作用(Na2CO3)
电离方程式:
CH3COOH CH3COO- + H+
2CH3COOH+2Na→2CH3COONa+H2↑
CH3COOH+NaOH→CH3COONa+H2O
2CH3COOH+Na2O→2CH3COONa+H2O
2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
使紫色石蕊溶液变红
食醋可以清除水壶中的少量水垢(主要成分是碳酸钙),这是利用了乙酸的什么性质?请写出相关反应的化学方程式。
酸性,2CH3COOH + CaCO3 === (CH3COO)2Ca +H2O+CO2↑
酸性强弱: CH3COOH>H2CO3
思考讨论
乙酸、乙醇、碳酸、水分子中羟基氢的活动性比较
乙醇 水 碳酸 乙酸
羟基氢的活动性 能否与钠反应
能否与NaOH反应
能否与Na2CO3反应
能否与NaHCO3反应
逐渐增强
能
能
能
能
能
能
能(放出CO2气体)
不能
不能
不能
不能
能(但不放出气体)
不能
不能
不能
能(放出CO2气体)
(1)在标准状况下醋酸是一种无色有强烈刺激性气味的液体( )
(2)乙酸中含有双键,因此属于不饱和烃( )
(3)乙酸分子中含有4个H原子,故为四元酸( )
(4)乙酸分子中含有 和—OH两种官能团( )
(5)乙酸的结构简式可以写成CH3COOH或COOHCH3( )
(6)乙酸可以和碳酸盐反应生成二氧化碳( )
×
√
×
×
×
×
提示 醋酸的熔点为16.6 ℃,在标准状况下,醋酸为无色晶体。
提示 乙酸分子中只有—COOH中的氢原子可以电离,故为一元酸。
判断正误
在做鱼时会加醋和酒,这样鱼会更香醇鲜美,你知道为什么吗?
【实验7-6】在一支试管中加入3mL乙醇,然后边振荡试管边慢慢加入2 mL浓硫酸和2 mL乙酸,再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和Na2CO3溶液的液面上,观察现象。
2. 酯化反应
实验探究
现象:液面分层,液面上层有无色透明不溶于水的油状液体产生,并可以闻到香味。
结论: 在浓硫酸、加热的条件下,乙酸和乙醇发生反应,生成无色、透明、不溶于水、有香味的油状液体。该油状液体是乙酸乙酯。
浓硫酸
CH3COOH + HOC2H5 CH3COOC2H5+H2O
碎瓷片防暴沸
导管在饱和Na2CO3液面上:防止倒吸
长导管冷凝、回流、导气作用
加物顺序:乙醇→浓硫酸→乙酸
饱和Na2CO3作用
①溶解乙醇;
②中和乙酸;
③降低乙酸乙酯的溶解度,利于酯的析出
浓硫酸:催化剂、吸水剂
沸点:
乙酸乙酯(77.1)
乙醇(78.3 ℃ )
乙酸(118℃)
酯化反应注意事项
小心加热:减少乙酸、乙醇的挥发。
加热:加快反应速率,蒸出乙酸乙酯,提高乙酸转化率。
分离碳酸钠和乙酸乙酯:分液
O
CH3—C—O—H+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓硫酸
CH3—C—O—H+H—O—C2H5 CH3—C—O—C2H5 +H2O
浓硫酸
=
=
O
O
乙酸和乙醇可能是以怎样的方式相互结合形成乙酸乙酯的?
思考探索
浓硫酸
CH3COOH + HOC2H5 CH3COOC2H5+H2O
=
O
18O
18O
同位素示踪法
CH3—C—OH + H—18O—C2H5
浓硫酸
=
O
CH3—C—18O—C2H5 + H2O
=
O
CH3COOH + HOCH3
浓硫酸
CH3COOCH3 + H2O
乙酸甲酯
HCOOH + HOCH2CH3
浓硫酸
HCOOCH2CH3 + H2O
甲酸乙酯
酯化反应实质:酸脱羟基,醇脱氢
酯化反应
——取代反应
定义:
酸跟醇起作用,生成酯和水的反应
实质:
酸脱羟基、醇脱氢 (羟基氢)
O
CH3—C—OH + H—18O—C2H5
浓硫酸
△
H2O
+ CH3—C— 18O—C2H5
O
乙酸乙酯(香味)
可逆反应
酯基
2. 酯化反应
很多鲜花和水果的香味都来自酯,如草莓中含有乙酸乙酯和乙酸异戊酯,苹果中含有戊酸戊酯等。
这些分子中碳原子数少、相对分子质量较小的低级酯具有一定的挥发性,有芳香气味,难溶于水,可用作饮料、糖果、化妆品中的香料和有机溶剂。
酯类广泛存在于自然界中
酒是陈的香
有机酸 + 醇 → 酯
有特殊香味
O
CH3—C—O—H
①
②
①弱酸性,具有酸的通性;酸性比碳酸强。
②酯化反应
浓硫酸
结构
性质
决定
归纳总结
有机化工原料
农药
染料
醋酸纤维
香料
喷漆溶剂
医药
合成纤维
四、乙酸的用途
1. 某有机物的结构简式如图,下列关于该有机物的说法正确的是( )
B
A.分子式为C7H6O5
B.1 mol该物质能与4 mol Na发生反应
C.分子中含有两种官能团
D.在水溶液中羧基和羟基均能电离出H+
A.其分子式为C15H20O4
B.该物质不能使酸性KMnO4溶液褪色
C.能发生加成反应、取代反应、氧化反应、酯化反应
D.1 mol该物质与足量NaOH溶液反应,最多消耗1 mol NaOH
2. 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开。S-诱抗素的分子结构如图所示,下列关于该分子的说法不正确的是
B
3. 1 mol 分别与Na、NaOH、NaHCO3、Na2CO3完全反应时,
消耗的Na、NaOH、NaHCO3、Na2CO3的物质的量之比为多少
4∶2∶2∶1
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
