沪教版化学九年级上册 第五章 基础实验4 常见金属的性质 教案(表格式)
文档属性
| 名称 | 沪教版化学九年级上册 第五章 基础实验4 常见金属的性质 教案(表格式) |
|
|
| 格式 | docx | ||
| 文件大小 | 53.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-28 00:00:00 | ||
图片预览



文档简介
第五章 金属的冶炼与利用
基础实验4 常见金属的性质
一、【教学目标】
1、认识生活中常见金属的物理性质,能利用简单的方法区分常见的金属;
2、实验探究金属的化学性质,初步理解金属活动性强弱;
3、探究钢铁锈蚀的条件,了解在生产和生活中怎样防止钢铁生锈。
二、【教学重点】
1、认识金属的主要物理性质;
2、能通过比较金属与氧气、酸反应的难易程度和反应剧烈程度判断金属的活动性;
3、会探究钢铁锈蚀的条件。
三、【教学难点】
1、通过控制变量法研究不同金属化学性质的差异;
2、会设计对比实验探究影响钢铁生锈的因素。
四、【教学方法】
情境导入法,实验探究法,对比实验法等。
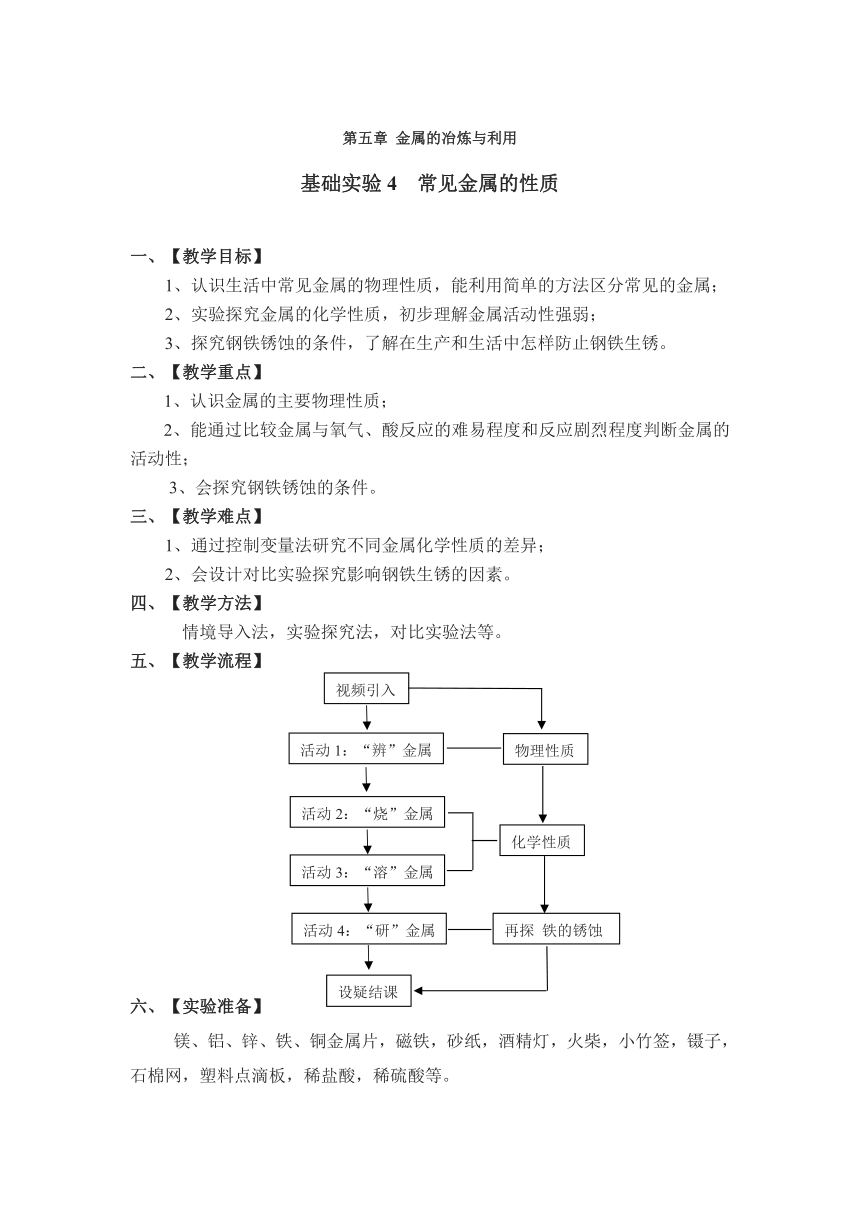
五、【教学流程】
六、【实验准备】
镁、铝、锌、铁、铜金属片,磁铁,砂纸,酒精灯,火柴,小竹签,镊子,石棉网,塑料点滴板,稀盐酸,稀硫酸等。
七、教学过程
教 学 环 节 教师活动 学生活动 设计意图
一、导入 【视频导入】 这就是举世瞩目的港珠澳大桥,被誉为“新世界七大奇迹之一”下面我们通过一段视频来走近奇迹。 【设疑】 港珠澳大桥的建成离不开哪一类材料? 【讲解】 不仅仅在桥梁上,金属材料在生产生活中的应用也十分广泛,那么金属都有什么样的性质呢?本节课我们一起学习常见金属的性质。 欣赏视频 钢材料(金属材料) 利用关于港珠澳大桥的新闻引入本节课,从而带领学生走近港珠澳大桥
二、 物理性质 活动一: “辨” 金 属 三、 化学性质 活动二: “烧” 金 属 活动三: “溶” 金 属 四、 再探 铁的锈蚀 活动四: “研” 金 属 【活动一:“辨”金属】 限时:2min 首先,老师考考大家,能否借助合适的器材,利用最简单的方法区分出常见的金属(镁、锌、铁、铜)。请在小组内进行实验。 注:小组讨论后,完成任务卡讨论结束后,请一个小组派代表阐述区分过程。 【设疑】 金属一般具有哪些物理性质呢?我们邀请两位同学通过游戏来PK一下。 【设疑】 左边都是金属的物理性质的正确描述,你能说说这些性质在生活中的具体应用吗? 你能说一说右边错在哪里吗?能否举例说明? 正确答案错误答案具有金属光泽常温下都为固体有良好的导电性都是银白色有良好的延展性不具有导电性硬度都很大
【设疑】 能否通过化学性质将常见的金属进行区分呢?老师播放一段视频,大家猜猜可能是哪种金属?说出判断的依据。 视频中的活动叫打铁花,可以说是民间传统的烟火,已经被列为国家级非物质文化遗产。而现代的烟花却更加绚烂夺目,你知道烟花中添加了哪种金属吗?为什么呢? 我们邀请两位同学分别写出镁、铁燃烧的方程式。 【总结】 对比两个方程式得出: 金属能与氧气反应生成金属氧化物。 【设疑】 常见的金属,铜、铝能否与氧气反应? 【活动二:“烧”金属】 限时2分钟 【设疑】 加热铜、铝出现了哪些现象? 根据实验现象能否判断铜、铝在加热时发生了化学变化? 请写出反应的化学方程式。 氧化铝是一种什么样的物质呢?请大家看一段视频。 【播放视频】 视频中用针刺去,才有白色液体流下。结合资料思考:白色液体是什么?为什么加热时它没有滴下来?(资料:铝熔点:660℃;氧化铝熔点:2050℃) 其实,铝常温下表面就生成一层致密的氧化铝,使铝与氧气隔绝,对铝起保护作用。 【设疑】 所有的金属都能与氧气反应吗?黄金放在高温的环境中,取出来仍然是黄金,体现了金具有什么样的化学性质? 通过学习,你能比较出铝、铜、金的活泼性吗?依据是什么? 【总结】 通过活动二得知:大多数金属能与氧气反应,但反应的难易程度不一样。 【设疑】 世界卫生组织曾多次推荐使用中国传统的厨具--铁锅,为什么?使用铁锅炒菜时加入一定量的食醋效果会更好,你知道其中的奥秘吗?所有的金属都能与酸反应吗?不同金属与酸反应的现象是否相同呢?请同学们展开探究。 【活动三:“溶”金属】 限时2分钟 实验中看到了什么现象,请将左边的金属拖动到相应实验现象的正前方? 【问题】 你能根据此实验现象判断出四种金属的活泼性吗? 镁锌铁与酸反应的气体是什么? 我们以镁与硫酸反应为例: Mg+H2SO4 H2+MgSO4 Mg + 2HCI H2+MgCl2 【问题】 港珠澳大桥是又一个奇迹。 它拥有最大规模的钢桥面铺装工程,它的设计使用寿命长达120年。鉴于造桥的材料,你觉得设计之初面临最大的问题是什么? 通过已学知识,铁生锈与哪些物质有关? 如何设计实验证明铁生锈与水和氧气有关呢? 【活动四:我会设计】 限时2分钟 我们请1-3组、4-6组分别派代表说说设计的思路。 【总结】 结合大家的实验设计,确实能够证明铁生锈与水和氧气有关。你知道哪些防锈的方法? 那么对于具有120年设计使用寿命的港珠澳大桥是如何进行防锈的呢? 请大家课后搜一搜港珠澳大桥的防锈措施,了解一下奇迹背后的故事…… 活动任务单: 1、区分出4种金属,并在末端给其贴上相应的标签。 2、在实验报告中作相应的记录。 两位学生PK找出金属物理性质的正确描述。 学生说一说实例 学生竞答: 1、水银常温下是液体; 2、铜是紫红色,金是金黄色; 3、金属具有良好的导电性; 4、金属钠可用小刀切割; 欣赏视频 铁:燃烧产生火星四射的现象。 镁粉 燃烧产生耀眼的白光。 学生板演方程式 学生思考 活动任务单: 用镊子分别夹取 铜、铝在酒精灯外焰加热约15秒。 观察并记录现象 铜:表面变黑 铝:“溶而不滴”, 表面变暗 铜生成黑色物质 铝表面变暗 学生板演方程式 说明:加热时铝熔化,但被产生的氧化铝包裹住而未滴落下来,体现氧化铝是致密的。 “真金不怕火炼” 很稳定,高温也不与氧气反应。 学生利用希沃课堂活动填空: 铝>铜>金 能够预防缺铁性贫血 铁能够与酸反应 活动任务单: 打磨镁、锌、铁、铜 四种金属,并剪下约2cm竖直放入点滴板的4个空格中; 向四种金属中分别 倒入适量稀盐酸(硫酸),注:最后向镁中滴加酸; 立即用燃着的竹签 点燃镁中产生的大气泡。 镁产生气泡极快 锌产生气泡较快 铁产生气泡较慢 铜表面没有气泡 (学生知识配对活动) 镁>锌>铁>铜 燃着的竹签靠近会爆炸,说明是氢气。 学生写出锌铁与酸反应的化学方程式。 锈蚀 水和氧气 活动任务单: 1-3小组:设计实验证明铁生锈与氧气有关; 4-6小组:设计实验证明铁生锈与水有关。 生描述 学生讨论 利用常识和已学知识区分金属。 锻炼学生的语言表达能力。 以希沃中分组竞争的游戏方式展开物理性质的学习,能活跃气氛,调动氛围。 利用希沃中的课堂活动总结金属的物理性质 利用视频激发学生的兴趣。 夯实基础,为下面总结金属与氧气的反应作铺垫。 利用问题激起学生探究的欲望。 培养学生操作能力。 视频再现,剖析铝未滴落的原因。 考验学生能否根据反应难易程度判断金属的活泼性 在教学中渗透化学与健康的知识,使学生进一步认识到金属能与酸反应,产生探究金属与酸反应的欲望。 培养学生仔细观察实验的能力。 进一步强调元素守恒的观念 与引入的情境相呼应。 培养学生利用控制变量设计实验的能力。 锻炼学生的语言表达能力。 留给学生想象和思考的空间,激发学生继续探究、学习的欲望。
板 书 设 计 基础实验4 常见金属的性质 物理性质 与氧气反应 化学性质 与酸反应 判断金属活泼性 再探:铁的锈蚀
基础实验4 常见金属的性质
一、【教学目标】
1、认识生活中常见金属的物理性质,能利用简单的方法区分常见的金属;
2、实验探究金属的化学性质,初步理解金属活动性强弱;
3、探究钢铁锈蚀的条件,了解在生产和生活中怎样防止钢铁生锈。
二、【教学重点】
1、认识金属的主要物理性质;
2、能通过比较金属与氧气、酸反应的难易程度和反应剧烈程度判断金属的活动性;
3、会探究钢铁锈蚀的条件。
三、【教学难点】
1、通过控制变量法研究不同金属化学性质的差异;
2、会设计对比实验探究影响钢铁生锈的因素。
四、【教学方法】
情境导入法,实验探究法,对比实验法等。
五、【教学流程】
六、【实验准备】
镁、铝、锌、铁、铜金属片,磁铁,砂纸,酒精灯,火柴,小竹签,镊子,石棉网,塑料点滴板,稀盐酸,稀硫酸等。
七、教学过程
教 学 环 节 教师活动 学生活动 设计意图
一、导入 【视频导入】 这就是举世瞩目的港珠澳大桥,被誉为“新世界七大奇迹之一”下面我们通过一段视频来走近奇迹。 【设疑】 港珠澳大桥的建成离不开哪一类材料? 【讲解】 不仅仅在桥梁上,金属材料在生产生活中的应用也十分广泛,那么金属都有什么样的性质呢?本节课我们一起学习常见金属的性质。 欣赏视频 钢材料(金属材料) 利用关于港珠澳大桥的新闻引入本节课,从而带领学生走近港珠澳大桥
二、 物理性质 活动一: “辨” 金 属 三、 化学性质 活动二: “烧” 金 属 活动三: “溶” 金 属 四、 再探 铁的锈蚀 活动四: “研” 金 属 【活动一:“辨”金属】 限时:2min 首先,老师考考大家,能否借助合适的器材,利用最简单的方法区分出常见的金属(镁、锌、铁、铜)。请在小组内进行实验。 注:小组讨论后,完成任务卡讨论结束后,请一个小组派代表阐述区分过程。 【设疑】 金属一般具有哪些物理性质呢?我们邀请两位同学通过游戏来PK一下。 【设疑】 左边都是金属的物理性质的正确描述,你能说说这些性质在生活中的具体应用吗? 你能说一说右边错在哪里吗?能否举例说明? 正确答案错误答案具有金属光泽常温下都为固体有良好的导电性都是银白色有良好的延展性不具有导电性硬度都很大
【设疑】 能否通过化学性质将常见的金属进行区分呢?老师播放一段视频,大家猜猜可能是哪种金属?说出判断的依据。 视频中的活动叫打铁花,可以说是民间传统的烟火,已经被列为国家级非物质文化遗产。而现代的烟花却更加绚烂夺目,你知道烟花中添加了哪种金属吗?为什么呢? 我们邀请两位同学分别写出镁、铁燃烧的方程式。 【总结】 对比两个方程式得出: 金属能与氧气反应生成金属氧化物。 【设疑】 常见的金属,铜、铝能否与氧气反应? 【活动二:“烧”金属】 限时2分钟 【设疑】 加热铜、铝出现了哪些现象? 根据实验现象能否判断铜、铝在加热时发生了化学变化? 请写出反应的化学方程式。 氧化铝是一种什么样的物质呢?请大家看一段视频。 【播放视频】 视频中用针刺去,才有白色液体流下。结合资料思考:白色液体是什么?为什么加热时它没有滴下来?(资料:铝熔点:660℃;氧化铝熔点:2050℃) 其实,铝常温下表面就生成一层致密的氧化铝,使铝与氧气隔绝,对铝起保护作用。 【设疑】 所有的金属都能与氧气反应吗?黄金放在高温的环境中,取出来仍然是黄金,体现了金具有什么样的化学性质? 通过学习,你能比较出铝、铜、金的活泼性吗?依据是什么? 【总结】 通过活动二得知:大多数金属能与氧气反应,但反应的难易程度不一样。 【设疑】 世界卫生组织曾多次推荐使用中国传统的厨具--铁锅,为什么?使用铁锅炒菜时加入一定量的食醋效果会更好,你知道其中的奥秘吗?所有的金属都能与酸反应吗?不同金属与酸反应的现象是否相同呢?请同学们展开探究。 【活动三:“溶”金属】 限时2分钟 实验中看到了什么现象,请将左边的金属拖动到相应实验现象的正前方? 【问题】 你能根据此实验现象判断出四种金属的活泼性吗? 镁锌铁与酸反应的气体是什么? 我们以镁与硫酸反应为例: Mg+H2SO4 H2+MgSO4 Mg + 2HCI H2+MgCl2 【问题】 港珠澳大桥是又一个奇迹。 它拥有最大规模的钢桥面铺装工程,它的设计使用寿命长达120年。鉴于造桥的材料,你觉得设计之初面临最大的问题是什么? 通过已学知识,铁生锈与哪些物质有关? 如何设计实验证明铁生锈与水和氧气有关呢? 【活动四:我会设计】 限时2分钟 我们请1-3组、4-6组分别派代表说说设计的思路。 【总结】 结合大家的实验设计,确实能够证明铁生锈与水和氧气有关。你知道哪些防锈的方法? 那么对于具有120年设计使用寿命的港珠澳大桥是如何进行防锈的呢? 请大家课后搜一搜港珠澳大桥的防锈措施,了解一下奇迹背后的故事…… 活动任务单: 1、区分出4种金属,并在末端给其贴上相应的标签。 2、在实验报告中作相应的记录。 两位学生PK找出金属物理性质的正确描述。 学生说一说实例 学生竞答: 1、水银常温下是液体; 2、铜是紫红色,金是金黄色; 3、金属具有良好的导电性; 4、金属钠可用小刀切割; 欣赏视频 铁:燃烧产生火星四射的现象。 镁粉 燃烧产生耀眼的白光。 学生板演方程式 学生思考 活动任务单: 用镊子分别夹取 铜、铝在酒精灯外焰加热约15秒。 观察并记录现象 铜:表面变黑 铝:“溶而不滴”, 表面变暗 铜生成黑色物质 铝表面变暗 学生板演方程式 说明:加热时铝熔化,但被产生的氧化铝包裹住而未滴落下来,体现氧化铝是致密的。 “真金不怕火炼” 很稳定,高温也不与氧气反应。 学生利用希沃课堂活动填空: 铝>铜>金 能够预防缺铁性贫血 铁能够与酸反应 活动任务单: 打磨镁、锌、铁、铜 四种金属,并剪下约2cm竖直放入点滴板的4个空格中; 向四种金属中分别 倒入适量稀盐酸(硫酸),注:最后向镁中滴加酸; 立即用燃着的竹签 点燃镁中产生的大气泡。 镁产生气泡极快 锌产生气泡较快 铁产生气泡较慢 铜表面没有气泡 (学生知识配对活动) 镁>锌>铁>铜 燃着的竹签靠近会爆炸,说明是氢气。 学生写出锌铁与酸反应的化学方程式。 锈蚀 水和氧气 活动任务单: 1-3小组:设计实验证明铁生锈与氧气有关; 4-6小组:设计实验证明铁生锈与水有关。 生描述 学生讨论 利用常识和已学知识区分金属。 锻炼学生的语言表达能力。 以希沃中分组竞争的游戏方式展开物理性质的学习,能活跃气氛,调动氛围。 利用希沃中的课堂活动总结金属的物理性质 利用视频激发学生的兴趣。 夯实基础,为下面总结金属与氧气的反应作铺垫。 利用问题激起学生探究的欲望。 培养学生操作能力。 视频再现,剖析铝未滴落的原因。 考验学生能否根据反应难易程度判断金属的活泼性 在教学中渗透化学与健康的知识,使学生进一步认识到金属能与酸反应,产生探究金属与酸反应的欲望。 培养学生仔细观察实验的能力。 进一步强调元素守恒的观念 与引入的情境相呼应。 培养学生利用控制变量设计实验的能力。 锻炼学生的语言表达能力。 留给学生想象和思考的空间,激发学生继续探究、学习的欲望。
板 书 设 计 基础实验4 常见金属的性质 物理性质 与氧气反应 化学性质 与酸反应 判断金属活泼性 再探:铁的锈蚀
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
