第八单元海水中的化学测试题(含答案)---2022-2023学年九年级化学鲁教版下册
文档属性
| 名称 | 第八单元海水中的化学测试题(含答案)---2022-2023学年九年级化学鲁教版下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 107.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-28 00:00:00 | ||
图片预览



文档简介
第八单元《海水中的化学》测试题
一、单选题
1.下列除杂(括号内为杂质)和鉴别所用的药品或方法,均正确的是
选项 实验目的 达到实验目的所用的药品或方法
A 除杂:KNO3溶液[Ba(NO3)2] 滴加适量的Na2SO4溶液,过滤
鉴别:氧化铜、铁粉、木炭粉三种黑色固体 取样,分别滴加适量的稀硫酸
B 除杂:铜粉(铁粉) 加入过量的稀盐酸,过滤
鉴别:BaSO4、Na2SO4、CuSO4三种固体 取样,分别加一定量的水
C 除杂:NaCl(Na2CO3) 滴加适量的稀硫酸至不再产生气泡
鉴别:BaCl2溶液、HCl溶液、NaOH溶液 取样,分别滴加Na2CO3溶液
D 除杂:H2(水蒸气和HCl气体) 依次通过浓硫酸和NaOH溶液
鉴别:硬水和软水 取样,分别加肥皂水,搅拌
A.A B.B C.C D.D
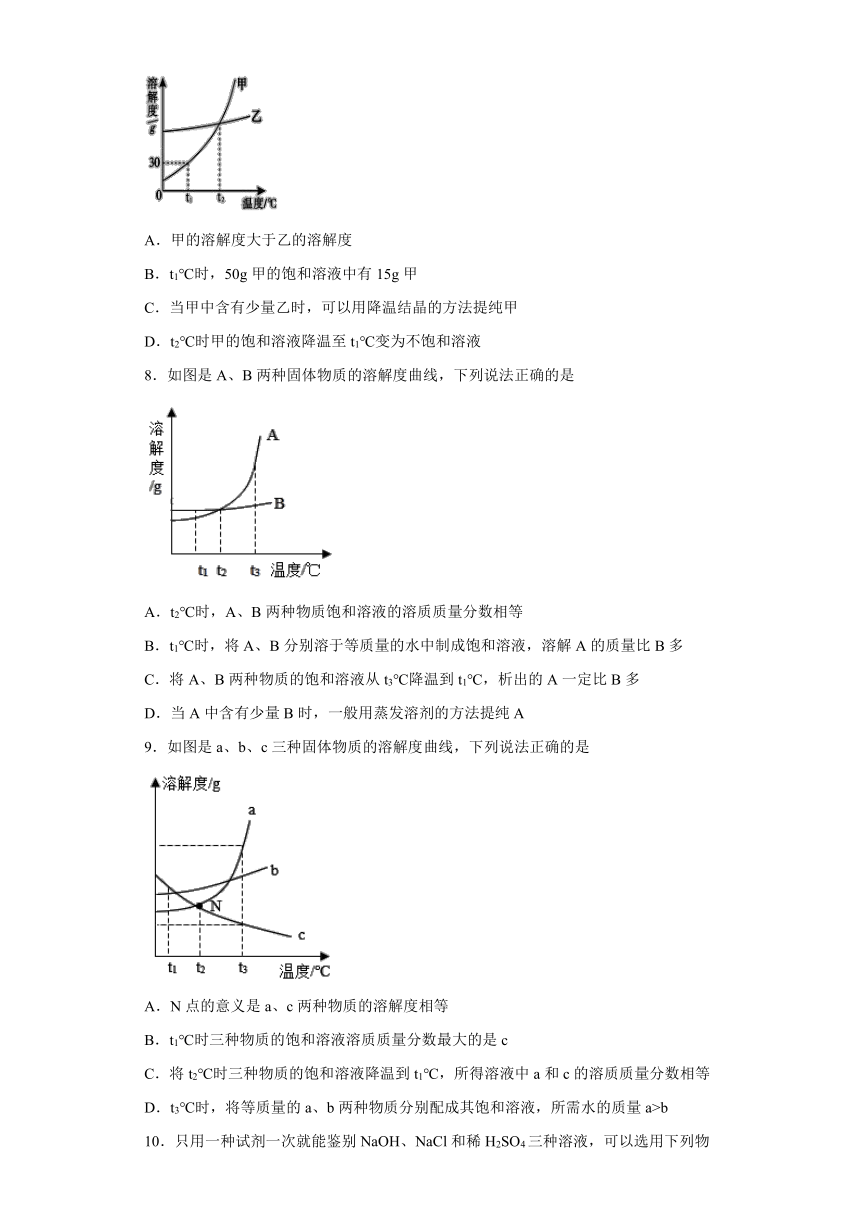
2.下列图像分别与选项中的操作相对应,其中合理的是
A.加热一定质量的高锰酸钾固体 B.向一定质量的饱和石灰水中加入少量CaO
C.向一定质量的氢氧化钠溶液中加入水 D.向一定质量的盐酸中加入AgNO3溶液
3.以下是KNO3的部分溶解度数据,下列说法中正确的是
温度/℃ 20 30 40 60
KNO3溶解度/g 31.6 45.8 63.9 110
A.KNO3的饱和溶液中不能再溶解其他物质
B.将30℃时质量分数为30%的KNO3溶液降温至20℃有KNO3晶体析出
C.40℃时KNO3的溶解度为63.9
D.60℃时,KNO3溶液中的溶质一定比40℃时溶液中的溶质多
4.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,结合图示判断,下列说法错误的是
A.t2℃时,甲的溶解度大于乙的溶解度
B.乙中混有少量甲,用恒温蒸发溶剂的方法提纯乙
C.t1℃时,甲、乙饱和溶液中溶质的质量分数相等
D.t2℃时,甲、乙溶液中所含溶质的质量一定相等
5.某实验小组取一定量的氯酸钾和二氧化锰混合后制氧气,充分反应后将实验剩余固体25.4g加入烧杯中,向烧杯中加入足量的水并充分搅拌,再向烧杯中滴加足量硝酸银溶液,反应后过滤、洗涤、干燥得到固体39.2g,则原混合物中氯酸钾的含量为
A.50% B.70% C.80% D.98%
6.下列叙述不正确的是
A.木炭可作冰箱除味剂
B.用食醋浸泡鸡蛋的方法,可制得无壳鸡蛋
C.将冷碟子放在蜡烛火焰的上方,可得到炭黑
D.油罐着火时用水喷淋的目的是降低油的着火点
7.下图是甲、乙两种物质(不含结晶水)的溶解度曲线。下列说法中正确的是
A.甲的溶解度大于乙的溶解度
B.t1℃时,50g甲的饱和溶液中有15g甲
C.当甲中含有少量乙时,可以用降温结晶的方法提纯甲
D.t2℃时甲的饱和溶液降温至t1℃变为不饱和溶液
8.如图是A、B两种固体物质的溶解度曲线,下列说法正确的是
A.t2℃时,A、B两种物质饱和溶液的溶质质量分数相等
B.t1℃时,将A、B分别溶于等质量的水中制成饱和溶液,溶解A的质量比B多
C.将A、B两种物质的饱和溶液从t3℃降温到t1℃,析出的A一定比B多
D.当A中含有少量B时,一般用蒸发溶剂的方法提纯A
9.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是
A.N点的意义是a、c两种物质的溶解度相等
B.t1℃时三种物质的饱和溶液溶质质量分数最大的是c
C.将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中a和c的溶质质量分数相等
D.t3℃时,将等质量的a、b两种物质分别配成其饱和溶液,所需水的质量a>b
10.只用一种试剂一次就能鉴别NaOH、NaCl和稀H2SO4三种溶液,可以选用下列物质中
A.紫色石蕊试液
B.无色酚酞试液
C.碳酸钠溶液
D.二氧化碳
11.物质的性质决定用途。下列物质的用途与性质对应关系不正确的是( )
物质 用途 性质
A 小苏打 治疗胃酸过多 小苏打能与盐酸发生反应
B 熟石灰 改良酸性土壤 熟石灰能与酸发生中和反应
C 干冰 制造舞台烟雾效果 二氧化碳不燃烧,也不支持燃烧
D 稀有气体 制造多种用途的电光源 通电时可以发出不同颜色的光
A.A B.B C.C D.D
12.下列做法可以达到预期目的的是
A.被蚂蚁(含蚁酸)叮咬后可涂上食醋,减轻痛痒
B.加入净水剂(如明矾),使硬水转化成纯净水
C.NaOH溶液中混有少量的Na2CO3,加入适量盐酸提纯NaOH溶液
D.做测定空气中氧气含量的实验时,使用过量的红磷
二、填空题
13.下表是KCl在不同温度时的溶解度.
温度/℃ 0 10 20 30 40 50 60
溶解度/g 27.6 31.0 34.0 37.0 x 42.6 45.5
小明为测定x的值,取4份40℃的水各50g,分别进行实验,并记录数据如下表.
实验编号 实验1 实验2 实验3 实验4
KCl质量/g 5 15 25 35
溶液质量/g 55 65 70 70
请回答下列问题.
(1)实验中需要用到的仪器有_______(只写一种).
(2)要使实验2的溶液达到饱和,可采取的方法是____________.
(3)由实验可知,40℃时KCl的溶解度x为_______ g.
(4)小明现要配制质量分数为30%的KCl溶液100g,为达实验目的其主要操作是_____________.
14.硫酸、盐酸是重要的化工原料。氯化氢(HCl)是极易溶于水的无色气体,1体积水能够溶解500体积的氯化氢,其水溶液叫盐酸。
(1)在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象:再滴入水,现象是_____________。
(2)向盛有碳酸钠粉末的试管中通入HCl气体,无明显现象:停止通气,再加入少量水,现象是_____________;发生反应的化学方程式是_____________。
(3)浓硫酸在实验室常用作干燥剂,因为浓硫酸有_____________性。
(4)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:_____________。
②与氯化钡溶液反应:_____________。
(5)盐酸的下列用途中,不能用硫酸代替盐酸的是_____________。(填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
15.溶液与人类生产、生活密切相关。如图是甲、乙、丙三种固体物质的溶解度曲线。按要求回答问题:
(1)t2℃时,将20g甲加入100g水中充分溶解,所甲得溶液的质量为_______g。
(2)t3℃时,将丙物质的不饱和溶液变成该温度下的饱和溶液,可采用的方法是_______。
(3)将t2℃时三种物质的饱和溶液降温到t1℃,此时三种溶液的溶质的质量分数由大到小的顺序是_______。
三、实验题
16.实验室中有一包白色固体是由氯化钠、氯化钡、硫酸铜、碳酸钠中的两种或两种以上的物质组成。某课外活动小组对这包白色固体进行了如下的探究实验:(假设下面各步都刚好完全反应)
根据上述实验回答下列问题:
(1)玻璃棒在操作Ⅰ、Ⅱ中的作用是___________________________________________。
(2)白色固体中可能含有_________________,写出步骤①中发生反应的化学方程式_______
(3)白色沉淀C为______________________________。
四、计算题
17.将Na2CO3和NaCl固体混合物22.3g放入烧杯中,加入182.1g稀盐酸恰好完全反应.待没有气泡溢出后,称量烧杯中剩余物质总质量为200g.请计算:
(1)生成二氧化碳的质量是_________ ;
(2)求所得溶液中溶质的质量分数是多少?
18.某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如下图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如下表:
(1)计算石灰石样品中CaCO3的质量分数。
(2)若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能(填“偏大”、“偏小”或“准确”),原因是什么。
试卷第6页,共6页
参考答案:
1.B
2.D
3.B
4.D
5.B
6.D
7.C
8.A
9.B
10.A
11.C
12.D
13. 烧杯 增加溶质、降低温度、蒸发溶剂 40 水的温度升高至50℃以上,称取30gKCl固体溶于70g水中
14.(1)纸条变红
(2) 固体粉末溶解,有气泡冒出
(3)吸水
(4)
(5)②③
15.(1)115
(2)加入丙物质或蒸发溶剂
(3)乙>甲>丙
16. 引流 氯化钠(NaCl) BaCl2+Na2CO3=BaCO3↓+2NaCl 氯化银(AgCl)
17. 4.4g 解:设碳酸钠的质量为x,生成氯化钠的质量为y
x=10.6g,y=11.7g
所得溶液中溶质的质量分数==11.7%
答:所得溶液中溶质的质量分数为11.7%。
18.(1)76.9%;(2)偏小;有二氧化碳溶解在水中或在容器中没有完全散逸出来
一、单选题
1.下列除杂(括号内为杂质)和鉴别所用的药品或方法,均正确的是
选项 实验目的 达到实验目的所用的药品或方法
A 除杂:KNO3溶液[Ba(NO3)2] 滴加适量的Na2SO4溶液,过滤
鉴别:氧化铜、铁粉、木炭粉三种黑色固体 取样,分别滴加适量的稀硫酸
B 除杂:铜粉(铁粉) 加入过量的稀盐酸,过滤
鉴别:BaSO4、Na2SO4、CuSO4三种固体 取样,分别加一定量的水
C 除杂:NaCl(Na2CO3) 滴加适量的稀硫酸至不再产生气泡
鉴别:BaCl2溶液、HCl溶液、NaOH溶液 取样,分别滴加Na2CO3溶液
D 除杂:H2(水蒸气和HCl气体) 依次通过浓硫酸和NaOH溶液
鉴别:硬水和软水 取样,分别加肥皂水,搅拌
A.A B.B C.C D.D
2.下列图像分别与选项中的操作相对应,其中合理的是
A.加热一定质量的高锰酸钾固体 B.向一定质量的饱和石灰水中加入少量CaO
C.向一定质量的氢氧化钠溶液中加入水 D.向一定质量的盐酸中加入AgNO3溶液
3.以下是KNO3的部分溶解度数据,下列说法中正确的是
温度/℃ 20 30 40 60
KNO3溶解度/g 31.6 45.8 63.9 110
A.KNO3的饱和溶液中不能再溶解其他物质
B.将30℃时质量分数为30%的KNO3溶液降温至20℃有KNO3晶体析出
C.40℃时KNO3的溶解度为63.9
D.60℃时,KNO3溶液中的溶质一定比40℃时溶液中的溶质多
4.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,结合图示判断,下列说法错误的是
A.t2℃时,甲的溶解度大于乙的溶解度
B.乙中混有少量甲,用恒温蒸发溶剂的方法提纯乙
C.t1℃时,甲、乙饱和溶液中溶质的质量分数相等
D.t2℃时,甲、乙溶液中所含溶质的质量一定相等
5.某实验小组取一定量的氯酸钾和二氧化锰混合后制氧气,充分反应后将实验剩余固体25.4g加入烧杯中,向烧杯中加入足量的水并充分搅拌,再向烧杯中滴加足量硝酸银溶液,反应后过滤、洗涤、干燥得到固体39.2g,则原混合物中氯酸钾的含量为
A.50% B.70% C.80% D.98%
6.下列叙述不正确的是
A.木炭可作冰箱除味剂
B.用食醋浸泡鸡蛋的方法,可制得无壳鸡蛋
C.将冷碟子放在蜡烛火焰的上方,可得到炭黑
D.油罐着火时用水喷淋的目的是降低油的着火点
7.下图是甲、乙两种物质(不含结晶水)的溶解度曲线。下列说法中正确的是
A.甲的溶解度大于乙的溶解度
B.t1℃时,50g甲的饱和溶液中有15g甲
C.当甲中含有少量乙时,可以用降温结晶的方法提纯甲
D.t2℃时甲的饱和溶液降温至t1℃变为不饱和溶液
8.如图是A、B两种固体物质的溶解度曲线,下列说法正确的是
A.t2℃时,A、B两种物质饱和溶液的溶质质量分数相等
B.t1℃时,将A、B分别溶于等质量的水中制成饱和溶液,溶解A的质量比B多
C.将A、B两种物质的饱和溶液从t3℃降温到t1℃,析出的A一定比B多
D.当A中含有少量B时,一般用蒸发溶剂的方法提纯A
9.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是
A.N点的意义是a、c两种物质的溶解度相等
B.t1℃时三种物质的饱和溶液溶质质量分数最大的是c
C.将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中a和c的溶质质量分数相等
D.t3℃时,将等质量的a、b两种物质分别配成其饱和溶液,所需水的质量a>b
10.只用一种试剂一次就能鉴别NaOH、NaCl和稀H2SO4三种溶液,可以选用下列物质中
A.紫色石蕊试液
B.无色酚酞试液
C.碳酸钠溶液
D.二氧化碳
11.物质的性质决定用途。下列物质的用途与性质对应关系不正确的是( )
物质 用途 性质
A 小苏打 治疗胃酸过多 小苏打能与盐酸发生反应
B 熟石灰 改良酸性土壤 熟石灰能与酸发生中和反应
C 干冰 制造舞台烟雾效果 二氧化碳不燃烧,也不支持燃烧
D 稀有气体 制造多种用途的电光源 通电时可以发出不同颜色的光
A.A B.B C.C D.D
12.下列做法可以达到预期目的的是
A.被蚂蚁(含蚁酸)叮咬后可涂上食醋,减轻痛痒
B.加入净水剂(如明矾),使硬水转化成纯净水
C.NaOH溶液中混有少量的Na2CO3,加入适量盐酸提纯NaOH溶液
D.做测定空气中氧气含量的实验时,使用过量的红磷
二、填空题
13.下表是KCl在不同温度时的溶解度.
温度/℃ 0 10 20 30 40 50 60
溶解度/g 27.6 31.0 34.0 37.0 x 42.6 45.5
小明为测定x的值,取4份40℃的水各50g,分别进行实验,并记录数据如下表.
实验编号 实验1 实验2 实验3 实验4
KCl质量/g 5 15 25 35
溶液质量/g 55 65 70 70
请回答下列问题.
(1)实验中需要用到的仪器有_______(只写一种).
(2)要使实验2的溶液达到饱和,可采取的方法是____________.
(3)由实验可知,40℃时KCl的溶解度x为_______ g.
(4)小明现要配制质量分数为30%的KCl溶液100g,为达实验目的其主要操作是_____________.
14.硫酸、盐酸是重要的化工原料。氯化氢(HCl)是极易溶于水的无色气体,1体积水能够溶解500体积的氯化氢,其水溶液叫盐酸。
(1)在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象:再滴入水,现象是_____________。
(2)向盛有碳酸钠粉末的试管中通入HCl气体,无明显现象:停止通气,再加入少量水,现象是_____________;发生反应的化学方程式是_____________。
(3)浓硫酸在实验室常用作干燥剂,因为浓硫酸有_____________性。
(4)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:_____________。
②与氯化钡溶液反应:_____________。
(5)盐酸的下列用途中,不能用硫酸代替盐酸的是_____________。(填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
15.溶液与人类生产、生活密切相关。如图是甲、乙、丙三种固体物质的溶解度曲线。按要求回答问题:
(1)t2℃时,将20g甲加入100g水中充分溶解,所甲得溶液的质量为_______g。
(2)t3℃时,将丙物质的不饱和溶液变成该温度下的饱和溶液,可采用的方法是_______。
(3)将t2℃时三种物质的饱和溶液降温到t1℃,此时三种溶液的溶质的质量分数由大到小的顺序是_______。
三、实验题
16.实验室中有一包白色固体是由氯化钠、氯化钡、硫酸铜、碳酸钠中的两种或两种以上的物质组成。某课外活动小组对这包白色固体进行了如下的探究实验:(假设下面各步都刚好完全反应)
根据上述实验回答下列问题:
(1)玻璃棒在操作Ⅰ、Ⅱ中的作用是___________________________________________。
(2)白色固体中可能含有_________________,写出步骤①中发生反应的化学方程式_______
(3)白色沉淀C为______________________________。
四、计算题
17.将Na2CO3和NaCl固体混合物22.3g放入烧杯中,加入182.1g稀盐酸恰好完全反应.待没有气泡溢出后,称量烧杯中剩余物质总质量为200g.请计算:
(1)生成二氧化碳的质量是_________ ;
(2)求所得溶液中溶质的质量分数是多少?
18.某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如下图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如下表:
(1)计算石灰石样品中CaCO3的质量分数。
(2)若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能(填“偏大”、“偏小”或“准确”),原因是什么。
试卷第6页,共6页
参考答案:
1.B
2.D
3.B
4.D
5.B
6.D
7.C
8.A
9.B
10.A
11.C
12.D
13. 烧杯 增加溶质、降低温度、蒸发溶剂 40 水的温度升高至50℃以上,称取30gKCl固体溶于70g水中
14.(1)纸条变红
(2) 固体粉末溶解,有气泡冒出
(3)吸水
(4)
(5)②③
15.(1)115
(2)加入丙物质或蒸发溶剂
(3)乙>甲>丙
16. 引流 氯化钠(NaCl) BaCl2+Na2CO3=BaCO3↓+2NaCl 氯化银(AgCl)
17. 4.4g 解:设碳酸钠的质量为x,生成氯化钠的质量为y
x=10.6g,y=11.7g
所得溶液中溶质的质量分数==11.7%
答:所得溶液中溶质的质量分数为11.7%。
18.(1)76.9%;(2)偏小;有二氧化碳溶解在水中或在容器中没有完全散逸出来
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
