甘肃省张掖市高台县2022-2023学年高二下学期5月月考化学试题(含答案)
文档属性
| 名称 | 甘肃省张掖市高台县2022-2023学年高二下学期5月月考化学试题(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 701.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-30 00:00:00 | ||
图片预览




文档简介
高台县2022-2023学年高二下学期5月月考
化学
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。共8页,总分100分,考试时间75分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Ga 70 Au 197
第I卷(选择题 共42分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.中华古诗词精深唯美。下列有关说法错误的是( )
A.“百宝都从海舶来,玻璃大镜比门排”制玻璃的原料之一可用于制作光导纤维
B.“纷纷灿烂如星陨,赫赫喧豗似火攻”烟花利用的“焰色试验”属于化学变化
C.“美人首饰侯王印,尽是沙中浪底来”说明金的性质稳定,在自然界中以游离形态存在
D.“粉身碎骨全不怕,要留清白在人间”有化学能和热能的相互转化
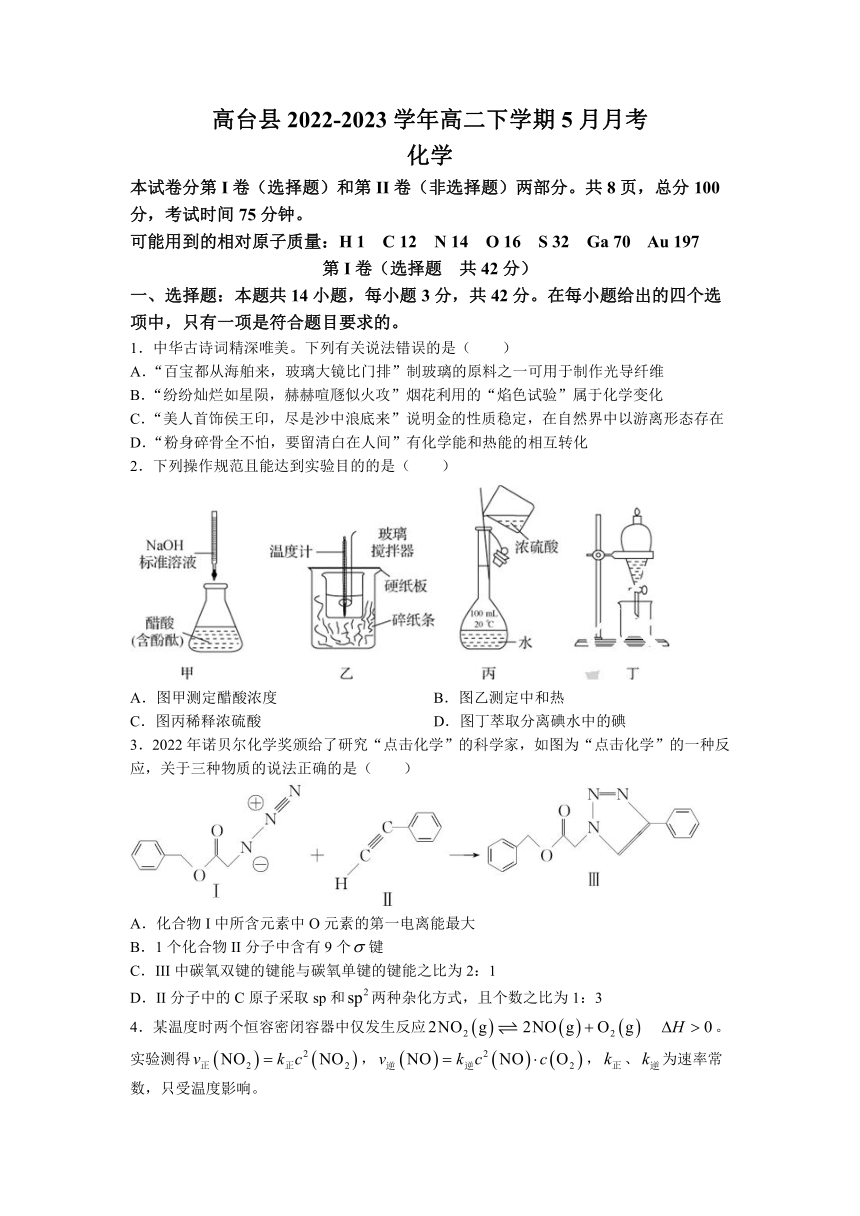
2.下列操作规范且能达到实验目的的是( )
A.图甲测定醋酸浓度 B.图乙测定中和热
C.图丙稀释浓硫酸 D.图丁萃取分离碘水中的碘
3.2022年诺贝尔化学奖颁给了研究“点击化学”的科学家,如图为“点击化学”的一种反应,关于三种物质的说法正确的是( )
A.化合物I中所含元素中O元素的第一电离能最大
B.1个化合物II分子中含有9个键
C.III中碳氧双键的键能与碳氧单键的键能之比为2:1
D.II分子中的C原子采取sp和两种杂化方式,且个数之比为1:3
4.某温度时两个恒容密闭容器中仅发生反应 。实验测得,,、为速率常数,只受温度影响。
容器编号 起始浓度/ 平衡浓度/
I 0.6 0 0 0.2
II 0.6 0.1 0
下列说法错误的是( )
A.升高温度,该反应的化学平衡常数增大
B.I中的平衡转化率约为66.7%
C.II中达到平衡状态时,
D.升高温度,该反应的增大,减小
5.生物还原法是指微生物在缺氧或厌氧条件下,在电子供体的作用下将还原为更易被去除的,根据电子供体的不同可分为自养还原和异养还原。为去除水中锑酸盐,某大学建立升流式硫自养固定床生物反应器,其反应机理如图。下列说法正确的是( )
A.在自养还原过程中,S做氧化剂
B.歧化反应的离子方程式是
C.反应的副产物是,全部来源于歧化反应
D.在生物反应器中可以实现S单质的循环利用
6.已知呈粉红色,呈蓝色,为无色。现将溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在 ,用该溶液做实验,溶液的颜色变化如图,以下结论和解释正确的是( )
A.等物质的量的和中键数之比为3:2
B.由实验①可推知
C.实验②是由于增大,导致平衡逆向移动
D.由实验③可知配离子的稳定性:
7.用含铁废铜制备胆矾的流程如图所示,下列说法错误的是( )
A.“溶解”中加入的只发生一个反应,离子方程式为
B.流程中可用CuO代替
C.加热者沸的目的是促使氢氧化铁沉淀颗粒长大,防止生成胶状沉淀
D.“系列操作”前加入的目的是抑制的水解
8.绿矾结构如图所示,下列说法错误的是( )
A.中心离子价层电子排布式为
B.为配体,中心离子的配位数为7
C.绿矾中存在的作用力有配位键、氢键、离子键
D.绿矾受热分解产生红棕色固体的同时可能生成
9.下列解释事实的化学方程式或离子方程式错误的是( )
A.用制备:
B.含氟牙膏防治龋齿的原理:
C.泡沬灭火器的原理:
D.用FeS除去废水中的:
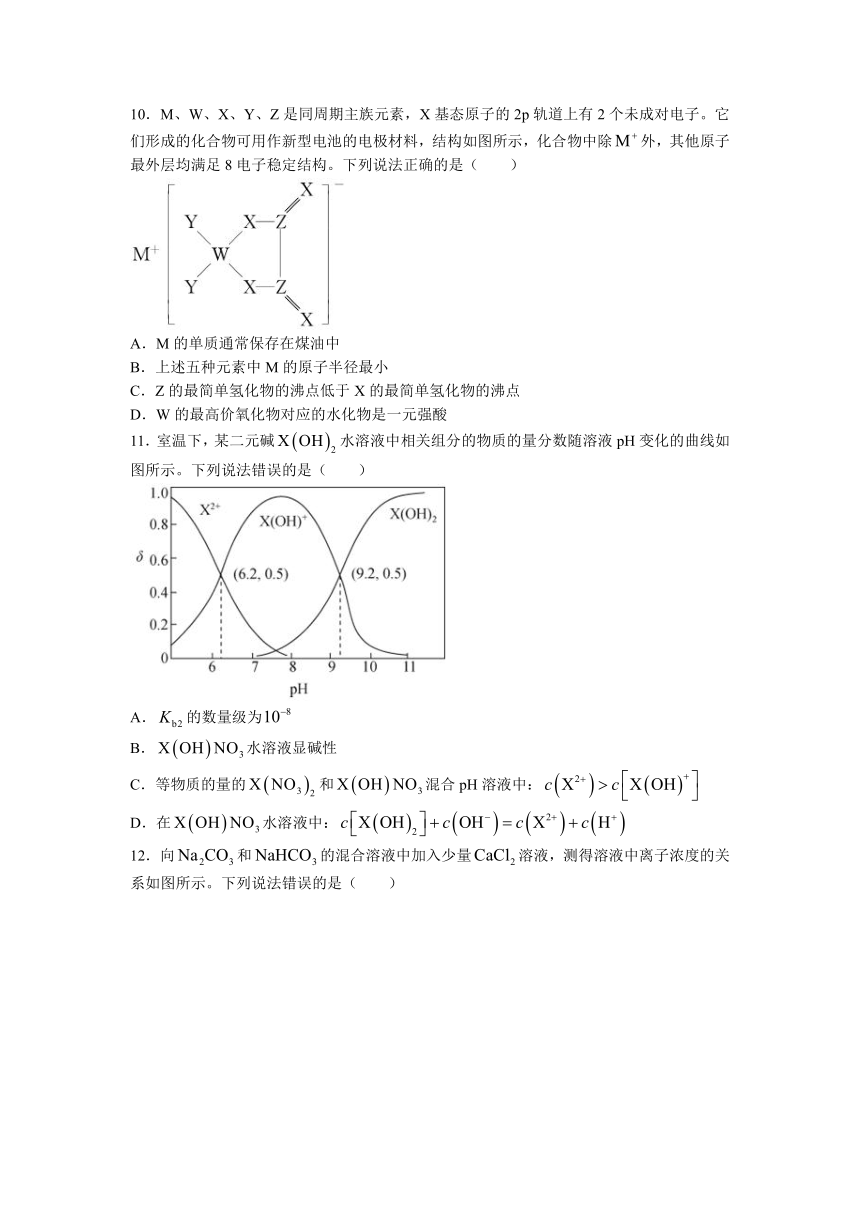
10.M、W、X、Y、Z是同周期主族元素,X基态原子的2p轨道上有2个未成对电子。它们形成的化合物可用作新型电池的电极材料,结构如图所示,化合物中除外,其他原子最外层均满足8电子稳定结构。下列说法正确的是( )
A.M的单质通常保存在煤油中
B.上述五种元素中M的原子半径最小
C.Z的最简单氢化物的沸点低于X的最简单氢化物的沸点
D.W的最高价氧化物对应的水化物是一元强酸
11.室温下,某二元碱水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示。下列说法错误的是( )
A.的数量级为
B.水溶液显碱性
C.等物质的量的和混合pH溶液中:
D.在水溶液中:
12.向和的混合溶液中加入少量溶液,测得溶液中离子浓度的关系如图所示。下列说法错误的是( )
A.该溶液中存在:
B.a,b两点对应的溶液中pH较大的为a点
C.向b点溶液中通入可使b点溶液向c点溶液转化
D.b点对应的溶液中存在:
13.下列关于物质的结构或性质及解释均正确的是( )
选项 物质的结构或性质 解释
A 键角: 水分子中O上孤电子对数比氨分子中N上的多
B 稳定性: HF分子间氢键强于HCl分子间作用力
C 熔点:碳化硅>金刚石 的键能大于的键能
D 酸性: 的极性大于的极性,导致的羧基中的羟基极性更大,氢更易电离
14.中国科学家研究在Pd/SVG催化剂上还原NO生成和的路径,各基元反应及活化能如图所示。下列说法错误的是( )
A.生成的各基元反应中,N元素均被还原
B.生成的总反应方程式为
C.决定NO生成速率的基元反应为
D.在Pd/SVG催化剂上,NO更容易被还原为
第II卷(非选择题 共58分)
三、非选择题:本题共4小题,共58分。
15.(13分)已知298K时,几种物质的电离平衡常数(K)如下表:
化学式 HClO
电离常数
(1)25℃时,和混合溶液的,则溶液中的________。
(2)溶液和溶液反应的离子方程式为________。
(3)25℃时,浓度均为的NaClO溶液和溶液,二者离子总浓度________(填字母)。
A.前者大 B.后者大 C.相等
(4)若将的HCl和两溶液分别加水稀释,pH变化如图所示,图中a、b、c三点对应溶液的导电能力由强到弱的顺序是________。
(5)25℃时,将的氨水与的盐酸等体积混合,反应平衡时溶液中,用含a的代数式表示的电离常数________。
16.(15分)废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为。某探究小组回收处理流程如图:
回答下列问题:
(1)①基态Se原子的简化电子排布式为________;②镓(Ga)和铟(In)位于元素周期表第IIIA族,属于________区;③基态Cu原子的价电子排布图为________。
(2)“高温焙烧”得到的经凝华变为白色晶体,易溶于水和极性有机溶剂,则其属于________晶体。
(3)滤液I中含有一种深蓝色的配合物离子,写出该离子的结构式:________。
(4)“回流过滤”中加入的是一种液态化合物,极易与水反应生成两种酸,写出与水反应的化学方程式:________。
(5)氮化镓是研制微电子器件、光电子器件的新型半导体材料。
①一种GaN的晶体属于六方晶系,上下底面为菱形,晶胞如图甲,三个晶胞围成一个六棱柱,如图乙。下列说法错误的是________(填字母)。
a.每个N周围距离最近的N数目为8
b.N原子位于Ga原子构成的四面体空隙中,Ga原子也位于N原子构成的四面体空隙中
c.晶胞的俯视图为
d.晶体密度为
②如图表示氮化镓与铜组装成的人工光合系统的电池工作原理。当电路中转移1.6mol电子时,电池中液体质量________(填“增重”或“减轻”)________g。
17.(15分)硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业上的硫氰化铵转化法制备硫氰化钾的实验装置如图所示:
已知:①是不溶于水,密度比水大的油状液体;②不溶于;③三颈烧瓶内盛放有、水和催化剂;④硫氰化钾熔点为172℃。
回答下列问题:
I.制备:
反应原理:
(1)①实验前,检查装置气密性良好后,装入药品。装置B中的试剂是________(填名称)。
②三颈烧瓶的下层液体需浸没导气管口,目的是________。
(2)实验开始时,打开,加热装置A、D。将A中产生的气体缓缓通入D中,发生反应,该反应比较缓慢,当看到三颈烧瓶中________现象时说明该反应接近完全。
II.制备KSCN:
(3)熄灭A处的酒精灯,关闭,移开水浴,将装置D继续加热至105℃,当完全分解后,打开,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为________。
(4)①装置E可用于处理尾气,多孔球泡的作用是________。
②已知酸性重铬酸钾溶液能将氧化生成浅黄色沉淀,铬元素被还原为,写出其氧化的离子方程式:________。
III.制备KSCN晶体:
(5)先滤去三颈烧瓶中的固体催化剂,再对滤液进行减压蒸发、________、过滤、洗涤、干燥,得到硫氰化钾晶体。
18.(15分)捕集技术能有效解决温室效应及能源短缺问题。
(1)催化加氢制的反应体系中,发生的反应如下:
反应I:
反应II:
反应III:
将与按照一定流速通过催化剂反应,测得的转化率与产物的选择性选择性]随温度变化如图所示:
①________(用含、的式子表示)。
②反应III的平衡常数表达式为________。
③340℃时,原料气按相同流速通过催化剂反应,出口处测得气体中________。
(2)电催化还原生成含碳产物(如CO、等)原理如图所示:
若阴极产物为,则该电极反应式为________。
(3)对于反应 在一定条件下存在:或,相应的速率与温度关系如图所示。
该反应的平衡常数________(用含、的代数式表示),图中A、B、C、D四个点中,能表示反应已达到平衡状态的是________。
参考答案
一、选择题
1.B 2.A 3.D 4.D 5.B
6.D 7.A 8.B 9.C 10.C
11.C 12.A 13.D 14.D
二、非选择题
15.(1)5:9(2分)
(2)(3分)
(3)B(2分)
(4)(3分)
(5)(3分)
16.(1)①(1分) ②p(1分)
③(2分)
(2)分子(1分)
(3)(2分)
(4)(2分)
(5)①a(2分) ②减轻(2分) 7.2(2分)
17.(1)①碱石灰(或氢氧化钠或氧化钙)(2分) ②使反应物氨和二硫化碳充分接触,防止发生倒吸(2分,充分接触和防倒吸各1分)
(2)二硫化碳油层消失(2分)
(3)(写成一水合氨也给分)(2分)
(4)①增大气体与溶液的接触面积,有利于尾气硫化氢和氨的充分吸收(2分) ②(3分)
(5)冷却结晶(2分)
18.(1)①(2分) ②(2分) ③45:1:4(3分)
(2)(3分)
(3)(3分) C(2分)
化学
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。共8页,总分100分,考试时间75分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Ga 70 Au 197
第I卷(选择题 共42分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.中华古诗词精深唯美。下列有关说法错误的是( )
A.“百宝都从海舶来,玻璃大镜比门排”制玻璃的原料之一可用于制作光导纤维
B.“纷纷灿烂如星陨,赫赫喧豗似火攻”烟花利用的“焰色试验”属于化学变化
C.“美人首饰侯王印,尽是沙中浪底来”说明金的性质稳定,在自然界中以游离形态存在
D.“粉身碎骨全不怕,要留清白在人间”有化学能和热能的相互转化
2.下列操作规范且能达到实验目的的是( )
A.图甲测定醋酸浓度 B.图乙测定中和热
C.图丙稀释浓硫酸 D.图丁萃取分离碘水中的碘
3.2022年诺贝尔化学奖颁给了研究“点击化学”的科学家,如图为“点击化学”的一种反应,关于三种物质的说法正确的是( )
A.化合物I中所含元素中O元素的第一电离能最大
B.1个化合物II分子中含有9个键
C.III中碳氧双键的键能与碳氧单键的键能之比为2:1
D.II分子中的C原子采取sp和两种杂化方式,且个数之比为1:3
4.某温度时两个恒容密闭容器中仅发生反应 。实验测得,,、为速率常数,只受温度影响。
容器编号 起始浓度/ 平衡浓度/
I 0.6 0 0 0.2
II 0.6 0.1 0
下列说法错误的是( )
A.升高温度,该反应的化学平衡常数增大
B.I中的平衡转化率约为66.7%
C.II中达到平衡状态时,
D.升高温度,该反应的增大,减小
5.生物还原法是指微生物在缺氧或厌氧条件下,在电子供体的作用下将还原为更易被去除的,根据电子供体的不同可分为自养还原和异养还原。为去除水中锑酸盐,某大学建立升流式硫自养固定床生物反应器,其反应机理如图。下列说法正确的是( )
A.在自养还原过程中,S做氧化剂
B.歧化反应的离子方程式是
C.反应的副产物是,全部来源于歧化反应
D.在生物反应器中可以实现S单质的循环利用
6.已知呈粉红色,呈蓝色,为无色。现将溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在 ,用该溶液做实验,溶液的颜色变化如图,以下结论和解释正确的是( )
A.等物质的量的和中键数之比为3:2
B.由实验①可推知
C.实验②是由于增大,导致平衡逆向移动
D.由实验③可知配离子的稳定性:
7.用含铁废铜制备胆矾的流程如图所示,下列说法错误的是( )
A.“溶解”中加入的只发生一个反应,离子方程式为
B.流程中可用CuO代替
C.加热者沸的目的是促使氢氧化铁沉淀颗粒长大,防止生成胶状沉淀
D.“系列操作”前加入的目的是抑制的水解
8.绿矾结构如图所示,下列说法错误的是( )
A.中心离子价层电子排布式为
B.为配体,中心离子的配位数为7
C.绿矾中存在的作用力有配位键、氢键、离子键
D.绿矾受热分解产生红棕色固体的同时可能生成
9.下列解释事实的化学方程式或离子方程式错误的是( )
A.用制备:
B.含氟牙膏防治龋齿的原理:
C.泡沬灭火器的原理:
D.用FeS除去废水中的:
10.M、W、X、Y、Z是同周期主族元素,X基态原子的2p轨道上有2个未成对电子。它们形成的化合物可用作新型电池的电极材料,结构如图所示,化合物中除外,其他原子最外层均满足8电子稳定结构。下列说法正确的是( )
A.M的单质通常保存在煤油中
B.上述五种元素中M的原子半径最小
C.Z的最简单氢化物的沸点低于X的最简单氢化物的沸点
D.W的最高价氧化物对应的水化物是一元强酸
11.室温下,某二元碱水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示。下列说法错误的是( )
A.的数量级为
B.水溶液显碱性
C.等物质的量的和混合pH溶液中:
D.在水溶液中:
12.向和的混合溶液中加入少量溶液,测得溶液中离子浓度的关系如图所示。下列说法错误的是( )
A.该溶液中存在:
B.a,b两点对应的溶液中pH较大的为a点
C.向b点溶液中通入可使b点溶液向c点溶液转化
D.b点对应的溶液中存在:
13.下列关于物质的结构或性质及解释均正确的是( )
选项 物质的结构或性质 解释
A 键角: 水分子中O上孤电子对数比氨分子中N上的多
B 稳定性: HF分子间氢键强于HCl分子间作用力
C 熔点:碳化硅>金刚石 的键能大于的键能
D 酸性: 的极性大于的极性,导致的羧基中的羟基极性更大,氢更易电离
14.中国科学家研究在Pd/SVG催化剂上还原NO生成和的路径,各基元反应及活化能如图所示。下列说法错误的是( )
A.生成的各基元反应中,N元素均被还原
B.生成的总反应方程式为
C.决定NO生成速率的基元反应为
D.在Pd/SVG催化剂上,NO更容易被还原为
第II卷(非选择题 共58分)
三、非选择题:本题共4小题,共58分。
15.(13分)已知298K时,几种物质的电离平衡常数(K)如下表:
化学式 HClO
电离常数
(1)25℃时,和混合溶液的,则溶液中的________。
(2)溶液和溶液反应的离子方程式为________。
(3)25℃时,浓度均为的NaClO溶液和溶液,二者离子总浓度________(填字母)。
A.前者大 B.后者大 C.相等
(4)若将的HCl和两溶液分别加水稀释,pH变化如图所示,图中a、b、c三点对应溶液的导电能力由强到弱的顺序是________。
(5)25℃时,将的氨水与的盐酸等体积混合,反应平衡时溶液中,用含a的代数式表示的电离常数________。
16.(15分)废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为。某探究小组回收处理流程如图:
回答下列问题:
(1)①基态Se原子的简化电子排布式为________;②镓(Ga)和铟(In)位于元素周期表第IIIA族,属于________区;③基态Cu原子的价电子排布图为________。
(2)“高温焙烧”得到的经凝华变为白色晶体,易溶于水和极性有机溶剂,则其属于________晶体。
(3)滤液I中含有一种深蓝色的配合物离子,写出该离子的结构式:________。
(4)“回流过滤”中加入的是一种液态化合物,极易与水反应生成两种酸,写出与水反应的化学方程式:________。
(5)氮化镓是研制微电子器件、光电子器件的新型半导体材料。
①一种GaN的晶体属于六方晶系,上下底面为菱形,晶胞如图甲,三个晶胞围成一个六棱柱,如图乙。下列说法错误的是________(填字母)。
a.每个N周围距离最近的N数目为8
b.N原子位于Ga原子构成的四面体空隙中,Ga原子也位于N原子构成的四面体空隙中
c.晶胞的俯视图为
d.晶体密度为
②如图表示氮化镓与铜组装成的人工光合系统的电池工作原理。当电路中转移1.6mol电子时,电池中液体质量________(填“增重”或“减轻”)________g。
17.(15分)硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业上的硫氰化铵转化法制备硫氰化钾的实验装置如图所示:
已知:①是不溶于水,密度比水大的油状液体;②不溶于;③三颈烧瓶内盛放有、水和催化剂;④硫氰化钾熔点为172℃。
回答下列问题:
I.制备:
反应原理:
(1)①实验前,检查装置气密性良好后,装入药品。装置B中的试剂是________(填名称)。
②三颈烧瓶的下层液体需浸没导气管口,目的是________。
(2)实验开始时,打开,加热装置A、D。将A中产生的气体缓缓通入D中,发生反应,该反应比较缓慢,当看到三颈烧瓶中________现象时说明该反应接近完全。
II.制备KSCN:
(3)熄灭A处的酒精灯,关闭,移开水浴,将装置D继续加热至105℃,当完全分解后,打开,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为________。
(4)①装置E可用于处理尾气,多孔球泡的作用是________。
②已知酸性重铬酸钾溶液能将氧化生成浅黄色沉淀,铬元素被还原为,写出其氧化的离子方程式:________。
III.制备KSCN晶体:
(5)先滤去三颈烧瓶中的固体催化剂,再对滤液进行减压蒸发、________、过滤、洗涤、干燥,得到硫氰化钾晶体。
18.(15分)捕集技术能有效解决温室效应及能源短缺问题。
(1)催化加氢制的反应体系中,发生的反应如下:
反应I:
反应II:
反应III:
将与按照一定流速通过催化剂反应,测得的转化率与产物的选择性选择性]随温度变化如图所示:
①________(用含、的式子表示)。
②反应III的平衡常数表达式为________。
③340℃时,原料气按相同流速通过催化剂反应,出口处测得气体中________。
(2)电催化还原生成含碳产物(如CO、等)原理如图所示:
若阴极产物为,则该电极反应式为________。
(3)对于反应 在一定条件下存在:或,相应的速率与温度关系如图所示。
该反应的平衡常数________(用含、的代数式表示),图中A、B、C、D四个点中,能表示反应已达到平衡状态的是________。
参考答案
一、选择题
1.B 2.A 3.D 4.D 5.B
6.D 7.A 8.B 9.C 10.C
11.C 12.A 13.D 14.D
二、非选择题
15.(1)5:9(2分)
(2)(3分)
(3)B(2分)
(4)(3分)
(5)(3分)
16.(1)①(1分) ②p(1分)
③(2分)
(2)分子(1分)
(3)(2分)
(4)(2分)
(5)①a(2分) ②减轻(2分) 7.2(2分)
17.(1)①碱石灰(或氢氧化钠或氧化钙)(2分) ②使反应物氨和二硫化碳充分接触,防止发生倒吸(2分,充分接触和防倒吸各1分)
(2)二硫化碳油层消失(2分)
(3)(写成一水合氨也给分)(2分)
(4)①增大气体与溶液的接触面积,有利于尾气硫化氢和氨的充分吸收(2分) ②(3分)
(5)冷却结晶(2分)
18.(1)①(2分) ②(2分) ③45:1:4(3分)
(2)(3分)
(3)(3分) C(2分)
同课章节目录
