6.1.3奇思妙“用”的化学电池 课件.pptx
文档属性
| 名称 | 6.1.3奇思妙“用”的化学电池 课件.pptx |

|
|
| 格式 | zip | ||
| 文件大小 | 40.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-01 00:00:00 | ||
图片预览



文档简介
(共31张PPT)
吴 彦
奇思妙“用”的化学电池
第六章 化学反应与能量
第1节 化学反应与能量变化
一、历史回顾,引入新课
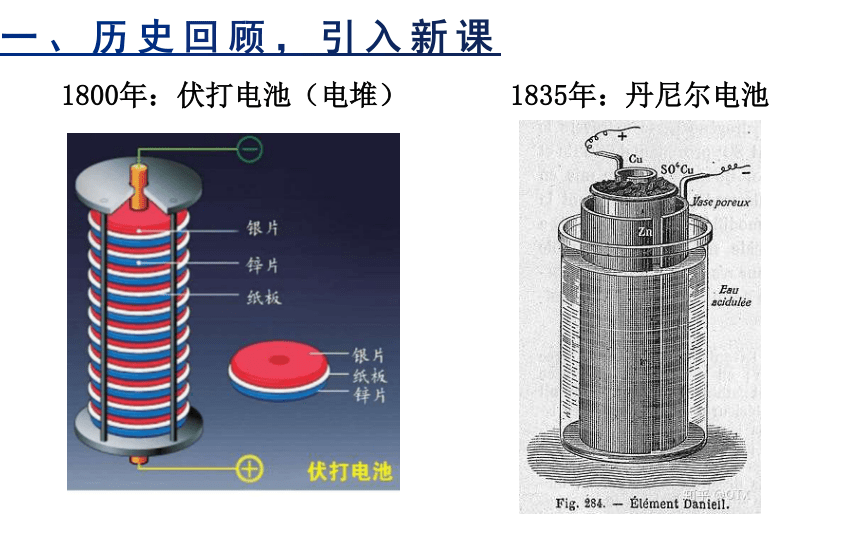
1800年:伏打电池(电堆)
1835年:丹尼尔电池
一、历史回顾,引入新课
1859年:铅酸蓄电池
1887 年:锌锰电池
一、历史回顾,引入新课
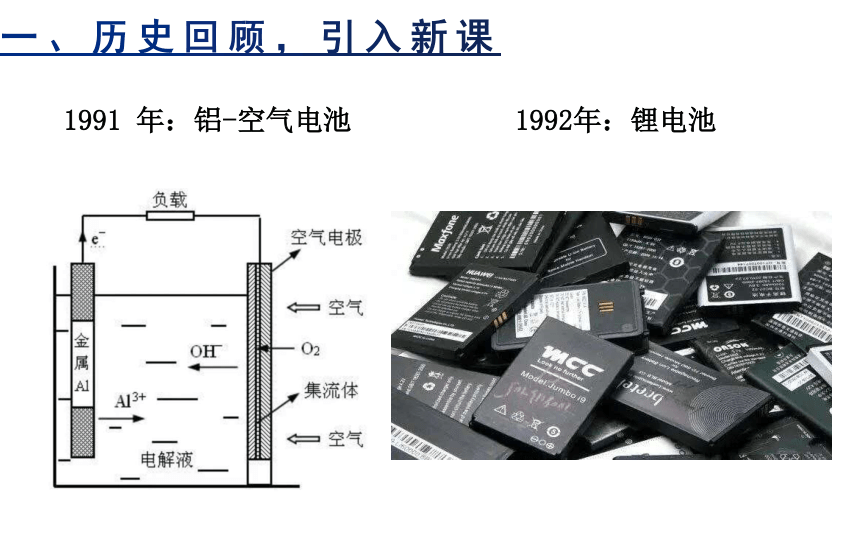
1991 年:铝-空气电池
1992年:锂电池
一、历史回顾,引入新课
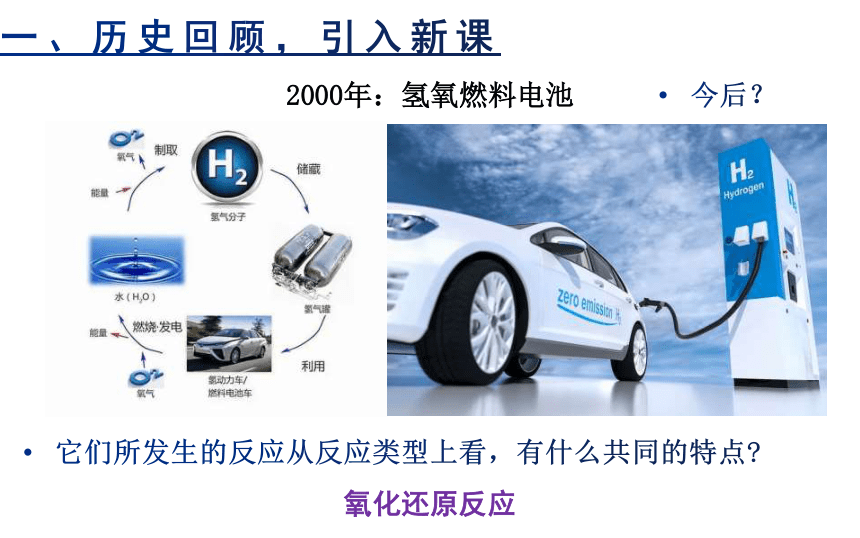
2000年:氢氧燃料电池
今后?
它们所发生的反应从反应类型上看,有什么共同的特点
氧化还原反应
二、了解“前世”,明确方向
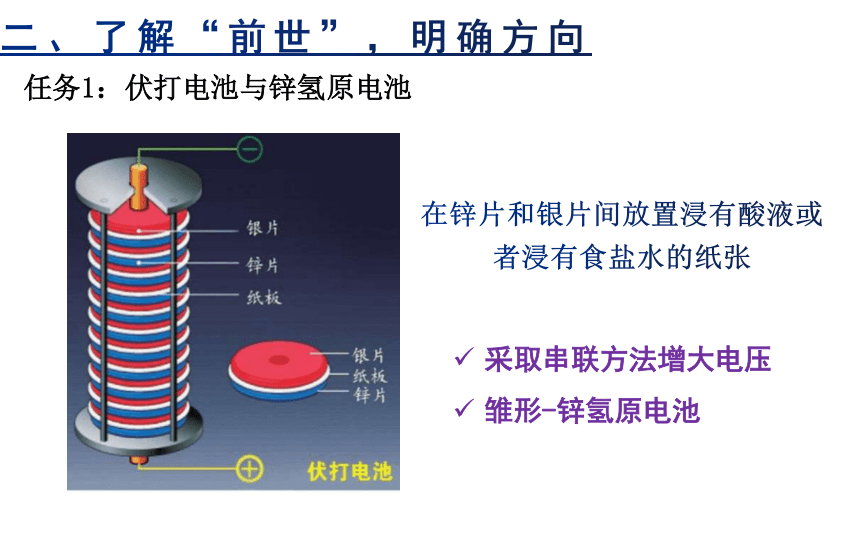
任务1:伏打电池与锌氢原电池
在锌片和银片间放置浸有酸液或者浸有食盐水的纸张
采取串联方法增大电压
雏形-锌氢原电池
二、了解“前世”,明确方向
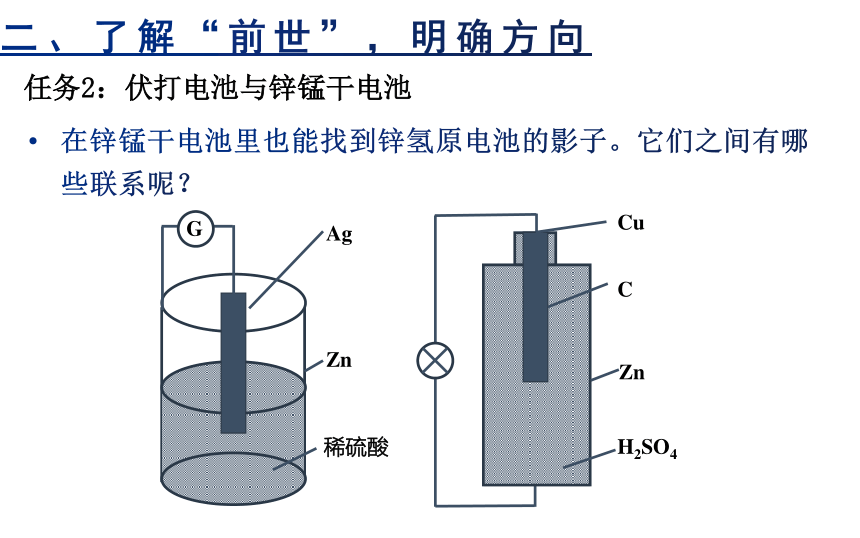
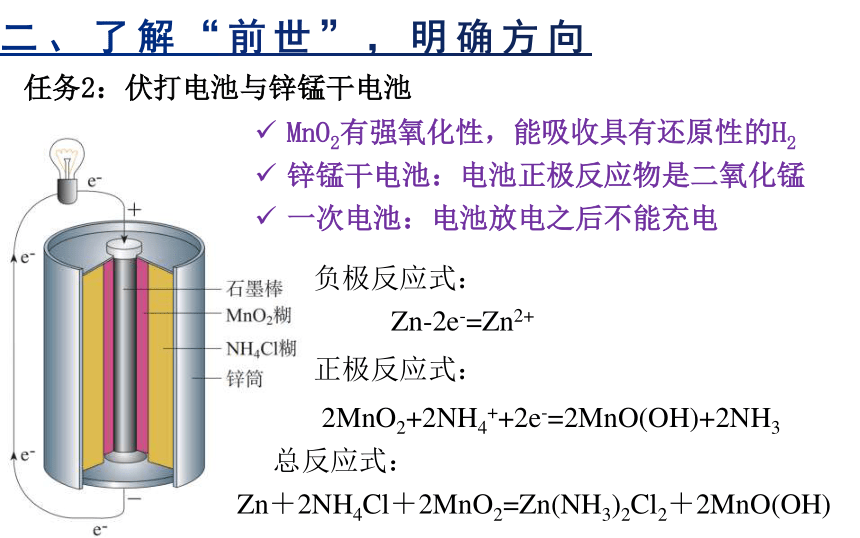
任务2:伏打电池与锌锰干电池
在锌锰干电池里也能找到锌氢原电池的影子。它们之间有哪些联系呢?
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
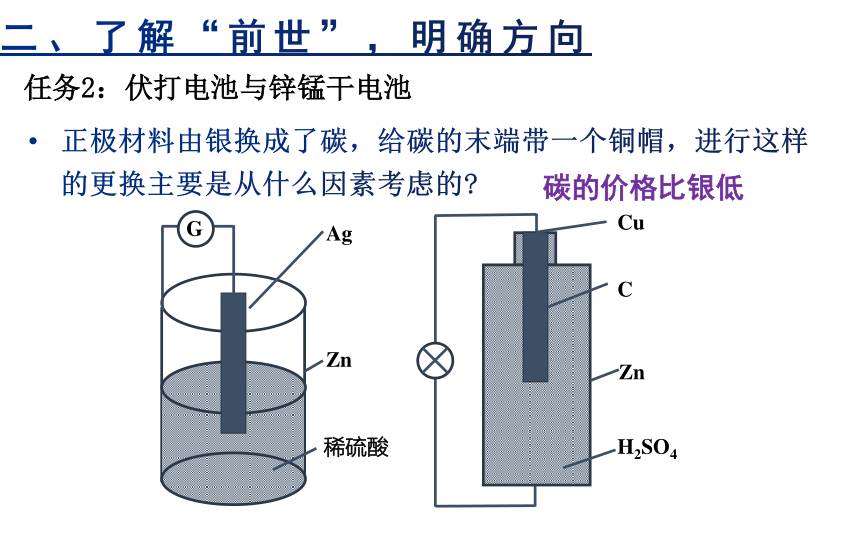
任务2:伏打电池与锌锰干电池
正极材料由银换成了碳,给碳的末端带一个铜帽,进行这样的更换主要是从什么因素考虑的
碳的价格比银低
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
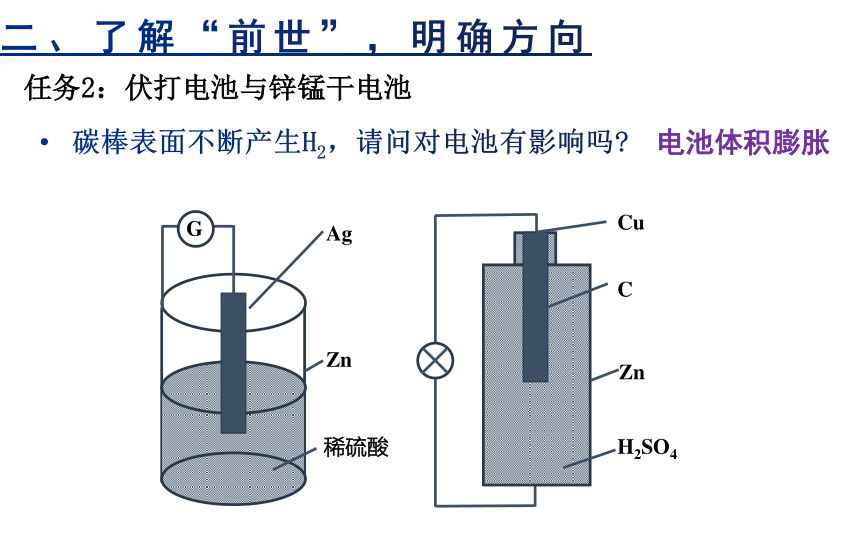
任务2:伏打电池与锌锰干电池
碳棒表面不断产生H2,请问对电池有影响吗
电池体积膨胀
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
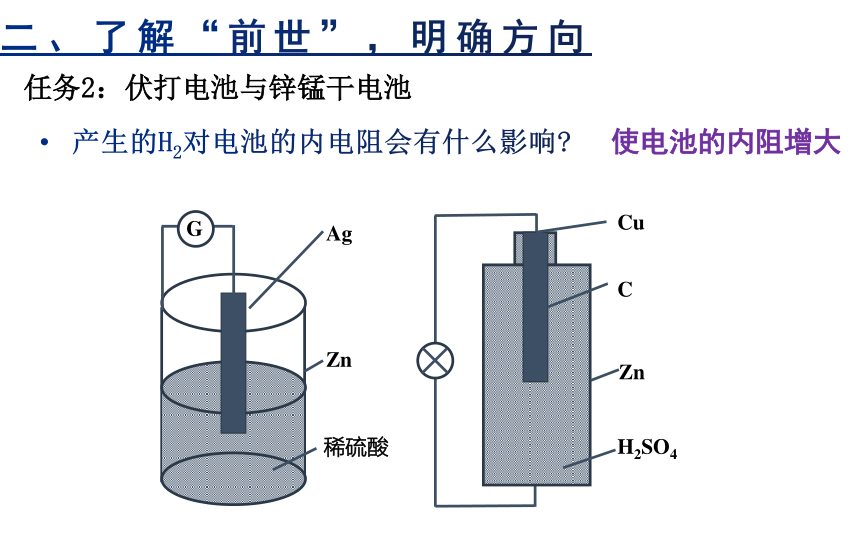
任务2:伏打电池与锌锰干电池
产生的H2对电池的内电阻会有什么影响
使电池的内阻增大
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
任务2:伏打电池与锌锰干电池
MnO2有强氧化性,能吸收具有还原性的H2
锌锰干电池:电池正极反应物是二氧化锰
一次电池:电池放电之后不能充电
Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnO(OH)
总反应式:
负极反应式:
正极反应式:
Zn-2e-=Zn2+
2MnO2+2NH4++2e-=2MnO(OH)+2NH3
二、了解“前世”,明确方向
任务3:伏打电池的另一种形式——食盐水NaCl溶液作电解质
用NaCl溶液作电解质溶液的电池真的能产生电流吗
二、了解“前世”,明确方向
任务3:伏打电池的另一种形式——食盐水NaCl溶液作电解质
【实验】锌片、石墨片、NaCl溶液
用NaCl溶液作电解质溶液的电池真的能产生电流吗
负极反应式:
2Zn-4e-+4OH-=2Zn(OH)2
正极反应式:
O2+2H2O+4e-=4OH-
总反应式:
O2+2Zn+2H2O=2Zn(OH)2
伏打电池用食盐水作电解质比用H2SO4作电解质有什么优点?
二、了解“前世”,明确方向
任务4:伏打电池与铝-空气电池
三、解读“今生”,优化升级
任务1:汽车电池的探究
你知道汽车电池经历了哪几个研发阶段?
每一个阶段电池的名称叫什么?
电池分别有什么优缺点?
每个阶段创新优化的指导思想又是什么?
铅酸蓄电池
碱性电池(锂电池)
氢氧燃料电池
三、解读“今生”,优化升级
任务1:汽车电池的探究
铅酸蓄电池
负极:Pb-2e +SO42-=PbSO4
正极:PbO2+2e +4H++SO42-=PbSO4+2H2O
电池总反应式:Pb+PbO2+2H2SO4=2PbSO4+2H2O
优点:
电压稳定、使用方便、安全可靠、 价格低廉,二次电池
缺点:
能量低、笨重、污染环境
三、解读“今生”,优化升级
任务1:汽车电池的探究
负极:4Li-4e-=4Li+
正极:FeS2+4e-=Fe+2S2-
电池总反应式:4Li+FeS2=Fe+2Li2S
优点:工作电压高、 负载自放电率低、循环寿命长、环保性高
缺点:低温输出功率小、有安全隐患
Li
FeS2
碱性电池(锂电池)
三、解读“今生”,优化升级
任务1:汽车电池的探究
负极:2H2-4e-=4H+
正极:O2+4H++4e-=2H2O
电池总反应式:2H2+O2=2H2O
优点:
零排放、运行平稳、无噪声
缺点:
成本高昂
氢氧燃料电池
三、解读“今生”,优化升级
任务2:了解锂电池的应用领域
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
为什么是锂离子电池得到广泛应用而不是其他离子电池呢?
锂离子半径小,容易在正极和负极材料之间脱出和嵌入
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
四、畅想“未来”,永无止境
手机、电脑等电子产品如何在质量和体积一定的条件下,提高电池的电容量呢
等质量的短周期金属单质分别与足量稀硫酸反应,请按产生H2质量由多到少排列。
国家能源局发布的 2021年全国电力工业统计数据显示,2021年全国发电装机容量约 23.8亿千瓦,同比增长7.9%。其中,风电装机容量约3.3亿千瓦,同比增长16.6%;阳能发电装机容量约3.1亿千瓦,同比增长 20.9%。国家倡导清洁能源,未来火电发电量将持续下降,风电、光伏发电量将保持上升趋势。
Be(
Li(
Al(
Mg(
Na(
四、畅想“未来”,永无止境
有没有比上述金属材料更轻的负极反应物
2000年
1992年
1890年
1899年
1836年
1856年
H2
Zn
Li
Al
Mg
Ca
Na
Fe
Ni
Pb
......
Be
比容量大,效率高
轻型移动电源的最佳选择
放电,速率快
技术先进,资源丰富,市场价额巨大
性价比高,无记忆效应
电池的性能
金属-空气电池
化学电源的起点
车载移动电源
H2
Zn
Li
Al
Mg
Ca
Na
Fe
Ni
Pb
...
Be
燃料电池
电池的材料
电池的发展
课堂小结
还原产物
氧化剂
得电子
氧化产物
还原剂
失电子
原理维度
电极产物
过程
电极反应物
失电子场所
电子导体
得电子场所
装置维度
阳离子移向
阴离子移向
电子移动方向
离子导体
现象
今日作业
1.梳理课堂笔记。
2.【练透】《化学反应与能量变化》第三课时1-13。
吴 彦
奇思妙“用”的化学电池
第六章 化学反应与能量
第1节 化学反应与能量变化
一、历史回顾,引入新课
1800年:伏打电池(电堆)
1835年:丹尼尔电池
一、历史回顾,引入新课
1859年:铅酸蓄电池
1887 年:锌锰电池
一、历史回顾,引入新课
1991 年:铝-空气电池
1992年:锂电池
一、历史回顾,引入新课
2000年:氢氧燃料电池
今后?
它们所发生的反应从反应类型上看,有什么共同的特点
氧化还原反应
二、了解“前世”,明确方向
任务1:伏打电池与锌氢原电池
在锌片和银片间放置浸有酸液或者浸有食盐水的纸张
采取串联方法增大电压
雏形-锌氢原电池
二、了解“前世”,明确方向
任务2:伏打电池与锌锰干电池
在锌锰干电池里也能找到锌氢原电池的影子。它们之间有哪些联系呢?
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
任务2:伏打电池与锌锰干电池
正极材料由银换成了碳,给碳的末端带一个铜帽,进行这样的更换主要是从什么因素考虑的
碳的价格比银低
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
任务2:伏打电池与锌锰干电池
碳棒表面不断产生H2,请问对电池有影响吗
电池体积膨胀
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
任务2:伏打电池与锌锰干电池
产生的H2对电池的内电阻会有什么影响
使电池的内阻增大
G
Ag
Zn
稀硫酸
C
Zn
Cu
H2SO4
二、了解“前世”,明确方向
任务2:伏打电池与锌锰干电池
MnO2有强氧化性,能吸收具有还原性的H2
锌锰干电池:电池正极反应物是二氧化锰
一次电池:电池放电之后不能充电
Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnO(OH)
总反应式:
负极反应式:
正极反应式:
Zn-2e-=Zn2+
2MnO2+2NH4++2e-=2MnO(OH)+2NH3
二、了解“前世”,明确方向
任务3:伏打电池的另一种形式——食盐水NaCl溶液作电解质
用NaCl溶液作电解质溶液的电池真的能产生电流吗
二、了解“前世”,明确方向
任务3:伏打电池的另一种形式——食盐水NaCl溶液作电解质
【实验】锌片、石墨片、NaCl溶液
用NaCl溶液作电解质溶液的电池真的能产生电流吗
负极反应式:
2Zn-4e-+4OH-=2Zn(OH)2
正极反应式:
O2+2H2O+4e-=4OH-
总反应式:
O2+2Zn+2H2O=2Zn(OH)2
伏打电池用食盐水作电解质比用H2SO4作电解质有什么优点?
二、了解“前世”,明确方向
任务4:伏打电池与铝-空气电池
三、解读“今生”,优化升级
任务1:汽车电池的探究
你知道汽车电池经历了哪几个研发阶段?
每一个阶段电池的名称叫什么?
电池分别有什么优缺点?
每个阶段创新优化的指导思想又是什么?
铅酸蓄电池
碱性电池(锂电池)
氢氧燃料电池
三、解读“今生”,优化升级
任务1:汽车电池的探究
铅酸蓄电池
负极:Pb-2e +SO42-=PbSO4
正极:PbO2+2e +4H++SO42-=PbSO4+2H2O
电池总反应式:Pb+PbO2+2H2SO4=2PbSO4+2H2O
优点:
电压稳定、使用方便、安全可靠、 价格低廉,二次电池
缺点:
能量低、笨重、污染环境
三、解读“今生”,优化升级
任务1:汽车电池的探究
负极:4Li-4e-=4Li+
正极:FeS2+4e-=Fe+2S2-
电池总反应式:4Li+FeS2=Fe+2Li2S
优点:工作电压高、 负载自放电率低、循环寿命长、环保性高
缺点:低温输出功率小、有安全隐患
Li
FeS2
碱性电池(锂电池)
三、解读“今生”,优化升级
任务1:汽车电池的探究
负极:2H2-4e-=4H+
正极:O2+4H++4e-=2H2O
电池总反应式:2H2+O2=2H2O
优点:
零排放、运行平稳、无噪声
缺点:
成本高昂
氢氧燃料电池
三、解读“今生”,优化升级
任务2:了解锂电池的应用领域
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
为什么是锂离子电池得到广泛应用而不是其他离子电池呢?
锂离子半径小,容易在正极和负极材料之间脱出和嵌入
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
三、解读“今生”,优化升级
任务3:锂离子、钠离子和铝离子电池
四、畅想“未来”,永无止境
手机、电脑等电子产品如何在质量和体积一定的条件下,提高电池的电容量呢
等质量的短周期金属单质分别与足量稀硫酸反应,请按产生H2质量由多到少排列。
国家能源局发布的 2021年全国电力工业统计数据显示,2021年全国发电装机容量约 23.8亿千瓦,同比增长7.9%。其中,风电装机容量约3.3亿千瓦,同比增长16.6%;阳能发电装机容量约3.1亿千瓦,同比增长 20.9%。国家倡导清洁能源,未来火电发电量将持续下降,风电、光伏发电量将保持上升趋势。
Be(
Li(
Al(
Mg(
Na(
四、畅想“未来”,永无止境
有没有比上述金属材料更轻的负极反应物
2000年
1992年
1890年
1899年
1836年
1856年
H2
Zn
Li
Al
Mg
Ca
Na
Fe
Ni
Pb
......
Be
比容量大,效率高
轻型移动电源的最佳选择
放电,速率快
技术先进,资源丰富,市场价额巨大
性价比高,无记忆效应
电池的性能
金属-空气电池
化学电源的起点
车载移动电源
H2
Zn
Li
Al
Mg
Ca
Na
Fe
Ni
Pb
...
Be
燃料电池
电池的材料
电池的发展
课堂小结
还原产物
氧化剂
得电子
氧化产物
还原剂
失电子
原理维度
电极产物
过程
电极反应物
失电子场所
电子导体
得电子场所
装置维度
阳离子移向
阴离子移向
电子移动方向
离子导体
现象
今日作业
1.梳理课堂笔记。
2.【练透】《化学反应与能量变化》第三课时1-13。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
