7.2 乙烯与有机高分子材料 课件.pptx
文档属性
| 名称 | 7.2 乙烯与有机高分子材料 课件.pptx |

|
|
| 格式 | pptx | ||
| 文件大小 | 36.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-01 00:00:00 | ||
图片预览



文档简介
(共23张PPT)
吴 彦
乙烯
第七章 有机化合物
第2节 乙烯与有机高分子材料
一、播放视频,认识用途
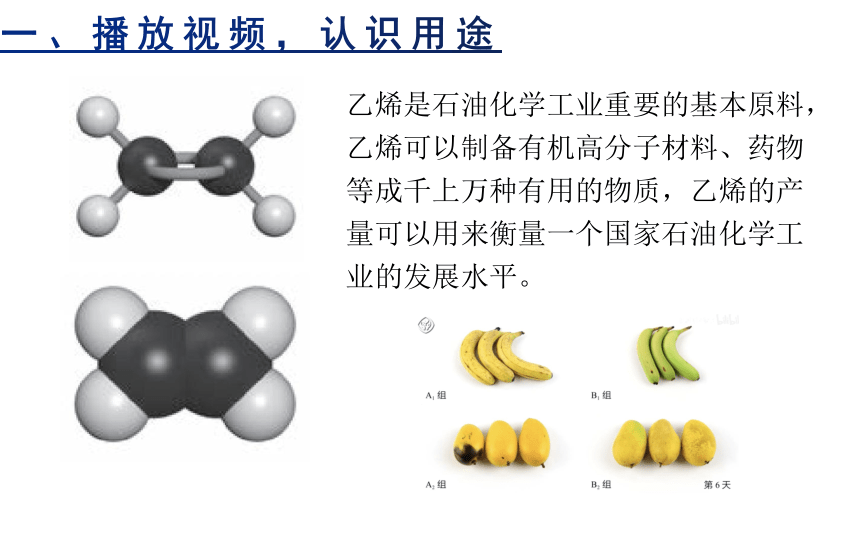
乙烯是石油化学工业重要的基本原料,乙烯可以制备有机高分子材料、药物等成千上万种有用的物质,乙烯的产量可以用来衡量一个国家石油化学工业的发展水平。
一、播放视频,认识用途
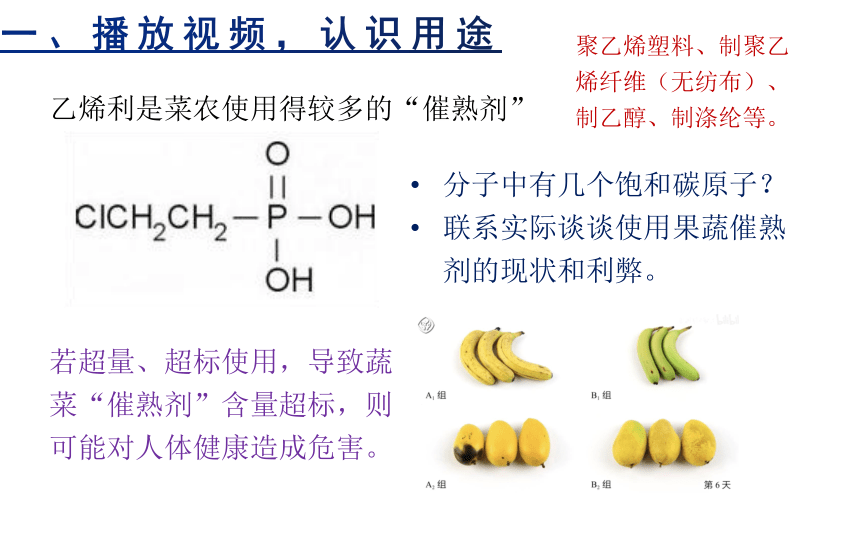
乙烯利是菜农使用得较多的“催熟剂”
分子中有几个饱和碳原子?
联系实际谈谈使用果蔬催熟剂的现状和利弊。
若超量、超标使用,导致蔬菜“催熟剂”含量超标,则可能对人体健康造成危害。
聚乙烯塑料、制聚乙烯纤维(无纺布)、制乙醇、制涤纶等。
二、探究性质,推测结构
【实验】1.乙烯与溴反应
步骤:将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
现象:乙烯使溴的四氯化碳溶液褪色。
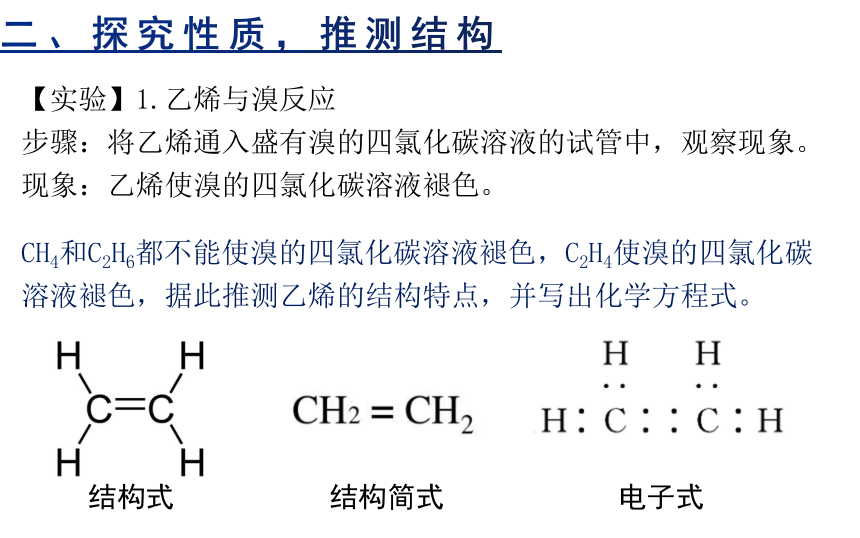
CH4和C2H6都不能使溴的四氯化碳溶液褪色,C2H4使溴的四氯化碳溶液褪色,据此推测乙烯的结构特点,并写出化学方程式。
结构式
结构简式
电子式
二、探究性质,推测结构
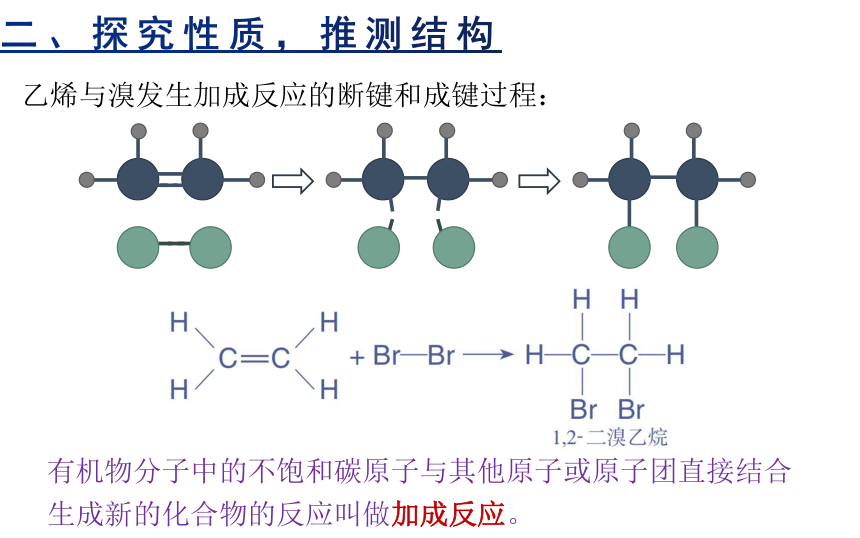
乙烯与溴发生加成反应的断键和成键过程:
有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。
二、探究性质,推测结构
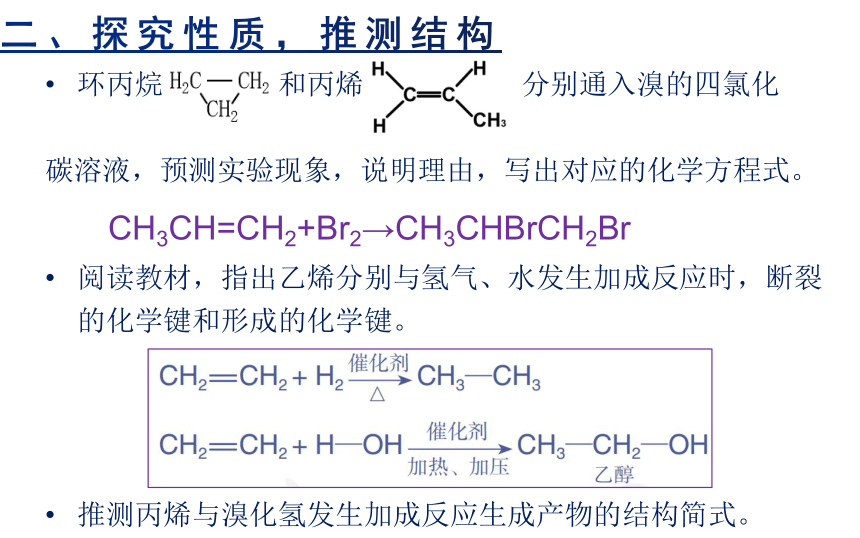
环丙烷 和丙烯 分别通入溴的四氯化
碳溶液,预测实验现象,说明理由,写出对应的化学方程式。
CH3CH=CH2+Br2→CH3CHBrCH2Br
阅读教材,指出乙烯分别与氢气、水发生加成反应时,断裂的化学键和形成的化学键。
推测丙烯与溴化氢发生加成反应生成产物的结构简式。
二、探究性质,推测结构
【实验】2.乙烯与高锰酸钾溶液反应
步骤:将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
现象:酸性高锰酸钾溶液褪色。
能否用酸性高锰酸钾溶液鉴别乙烷与乙烯(或甲烷与乙烯)?
能否用酸性高锰酸钾溶液除去甲烷中的乙烯?
除去甲烷中混有的乙烯可以选择什么试剂?
√
×,会在甲烷中引入新的杂质气体 CO2
溴的四氯化碳溶液
二、探究性质,推测结构
【实验】3.乙烯在空气中燃烧
步骤:点燃纯净的乙烯,观察燃烧时的现象。
现象:乙烯能在空气中燃烧,火焰明亮且伴有黑烟,生成二氧化碳和水,同时放出大量的热。
乙烯在空气中燃烧时产生黑烟的原因是供氧不足造成的吗
体积的乙烯、乙烷分别完全燃烧,乙烷耗氧量比乙烯耗氧量大
乙烯含碳量较大,导致燃烧不充分形成黑烟。
C2H4 + 3O2→2CO2 + 2H2O
点燃
2C2H6 + 7O2→4CO2 + 6H2O
点燃
二、探究性质,推测结构
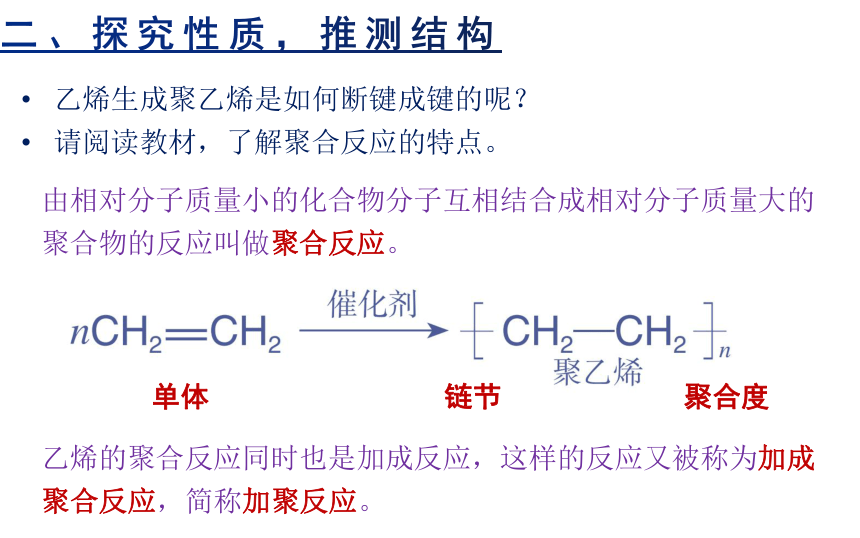
乙烯生成聚乙烯是如何断键成键的呢?
请阅读教材,了解聚合反应的特点。
由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。
乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
单体
链节
聚合度
二、探究性质,推测结构
n CH3CH=CH2
CH CH2
CH3
n ClCH=CH2
CH2 CH
Cl
n CF2=CF2
C C
F
F
F
F
丙烯
聚丙烯
氯乙烯
聚氯乙烯
四氟乙烯
聚四氟乙烯
(1)CH3CH3、H2C CH2、CH(CH3)3
(2)CH2=CH2、CH2=C(CH3)2、
(3)CH CH、CH CCH3、CH3C CCH3
(4) 、 、
CH2
三、求同存异,探究分类
下列各组有机物的共同特点是什么?
这12种有机物的共同特点是什么
(1)分子中的碳原子均为饱和碳原子——饱和烃
(2)分子中都含有碳碳双键——不饱和烃(烯烃)
(3)分子中都含有碳碳三键——不饱和烃(炔烃)
(4)分子中都含有苯环——芳香烃
12种有机物都为仅含有碳和氢两种元素的烃,也称为碳氢化合物
CH3
CH=CH2
CH2
CH2
CH2
CH2
CH
CH
烃与有机高分子材料
Ω(C6H6) 异常性质 结构特点 结构简式
4 不能使溴水和酸性KMnO4溶液褪色 苯分子为平面正六边形结构,不存在单键和双键交替,6个碳原子之间的键完全相同,是介于碳碳单键和碳碳双键之间的独特的键。
四、搭建模型,探究结构
甲烷 结构式 球棍模型
结构特点 (1)正四面体空间结构,碳原子位于中心,4个氢原子位于正四面体的4个顶点 (2)4个C—H键是极性键,键长相等。 (3)4个C—H键之间的夹角(键角)相等,是109°28',甲烷分子中任意4个原子不共面。 (4)4个氢原子的空间位置是等同的,用1个氯原子取代任意1个氢原子都得到相同的一氯甲烷,即CH3Cl没有同分异构体;用2个氯原子取代任意2个氢原子也得到相同的二氯甲烷,即CH2Cl,没有同分异构体;同理,CHCl3和CCl4都没有同分异构体。
四、搭建模型,探究结构
乙烷 乙烯 乙炔 分子式 结构式 分子式 结构式 分子式 结构式
C2H6 C2H4 C2H2
结构特点 (1)立体结构 (2)键角:109°28 (3)一个分子内有一个碳碳非极性单键和六个碳氢极性键 (4)六个氢原子的空间位置等同 (5)碳原子有四个单键,只有单键的碳是饱和碳原子 (1)平面结构 (2)键角:120° (3)一个分子内有一个碳碳非极性双键和四个碳氢极性键 (4)四个氢原子的空间位置等同 (5)碳原子有四个共价键,双键中的碳是不饱和碳原子 (1)直线形 (2)键角:180° (3)一个分子内有一个碳碳非极性三键和二个碳氢极性键 (4)两个氢原子的空间位置等同 (5)碳原子有四个共价键,三键中的碳是不饱和碳原子
搭建苯乙烯的球棍模型。思考苯乙烯(C8H8)分子中共平面的原子最多有几个,共直线的原子最多有几个。
16
4
CH CH
塑料
多数塑料绝缘性好、耐化学腐蚀,耐热性差。
塑料
五、联系实际,探究用途
橡胶树被称为会“流泪”的树。
天然橡胶就是由橡胶树割胶时流出的胶乳经凝固、干燥后而制得。
从结构上看,天然橡胶易老化的主要原因是什么?
橡胶
天然橡胶分子结构中的碳碳双键易发生化学反应。
五、联系实际,探究用途
橡胶硫化结构的变化及性能有哪些改善?
橡胶硫化使线型的高分子链之间通过硫原子形成化学键,产生交联,形成网状结构。硫化橡胶具有更好的强度、韧性、弹性和化学稳定性。
生胶
硫化胶
橡胶
五、联系实际,探究用途
阅读教材,了解纤维的分类,归纳总结合成纤维有哪些优良性能和用途。
(1)纤维分类:纤维分为天然纤维、再生纤维、合成纤维;再生纤维与合成纤维统称为化学纤维。
(2)合成纤维的性能:具有强度高、弹性好、耐磨、耐化学腐蚀、不易虫蛀等优良性能。
(3)用途:除了供人类穿着外,还可以制成绳索、渔网、工业用滤布,以及飞机、船舶的结构材料等。
纤维
一、乙烯
1.乙烯的用途
2.化学性质与结构
(1)加成——与H2、H2O、HCl反应
(2)氧化反应——与酸性KMnO4溶液、O2反应
(3)加聚反应——生成聚乙烯
二、烃的分类
1.烯烃、炔烃和芳香烃的定义
2.烃的分类标准
课堂小结
乙 烯
课堂小结
一、烃的分子结构
1.苯的结构:平面正六边形
2.乙烷、乙烯、乙炔的球棍模型
(1)乙烷:立体结构
(2)乙烯:平面结构
(3)乙炔:直线结构
二、有机高分子材料
塑料、橡胶、纤维
烃与有机高分子材料
今日作业
1.梳理课堂笔记。
2.【练透】
吴 彦
乙烯
第七章 有机化合物
第2节 乙烯与有机高分子材料
一、播放视频,认识用途
乙烯是石油化学工业重要的基本原料,乙烯可以制备有机高分子材料、药物等成千上万种有用的物质,乙烯的产量可以用来衡量一个国家石油化学工业的发展水平。
一、播放视频,认识用途
乙烯利是菜农使用得较多的“催熟剂”
分子中有几个饱和碳原子?
联系实际谈谈使用果蔬催熟剂的现状和利弊。
若超量、超标使用,导致蔬菜“催熟剂”含量超标,则可能对人体健康造成危害。
聚乙烯塑料、制聚乙烯纤维(无纺布)、制乙醇、制涤纶等。
二、探究性质,推测结构
【实验】1.乙烯与溴反应
步骤:将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
现象:乙烯使溴的四氯化碳溶液褪色。
CH4和C2H6都不能使溴的四氯化碳溶液褪色,C2H4使溴的四氯化碳溶液褪色,据此推测乙烯的结构特点,并写出化学方程式。
结构式
结构简式
电子式
二、探究性质,推测结构
乙烯与溴发生加成反应的断键和成键过程:
有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。
二、探究性质,推测结构
环丙烷 和丙烯 分别通入溴的四氯化
碳溶液,预测实验现象,说明理由,写出对应的化学方程式。
CH3CH=CH2+Br2→CH3CHBrCH2Br
阅读教材,指出乙烯分别与氢气、水发生加成反应时,断裂的化学键和形成的化学键。
推测丙烯与溴化氢发生加成反应生成产物的结构简式。
二、探究性质,推测结构
【实验】2.乙烯与高锰酸钾溶液反应
步骤:将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
现象:酸性高锰酸钾溶液褪色。
能否用酸性高锰酸钾溶液鉴别乙烷与乙烯(或甲烷与乙烯)?
能否用酸性高锰酸钾溶液除去甲烷中的乙烯?
除去甲烷中混有的乙烯可以选择什么试剂?
√
×,会在甲烷中引入新的杂质气体 CO2
溴的四氯化碳溶液
二、探究性质,推测结构
【实验】3.乙烯在空气中燃烧
步骤:点燃纯净的乙烯,观察燃烧时的现象。
现象:乙烯能在空气中燃烧,火焰明亮且伴有黑烟,生成二氧化碳和水,同时放出大量的热。
乙烯在空气中燃烧时产生黑烟的原因是供氧不足造成的吗
体积的乙烯、乙烷分别完全燃烧,乙烷耗氧量比乙烯耗氧量大
乙烯含碳量较大,导致燃烧不充分形成黑烟。
C2H4 + 3O2→2CO2 + 2H2O
点燃
2C2H6 + 7O2→4CO2 + 6H2O
点燃
二、探究性质,推测结构
乙烯生成聚乙烯是如何断键成键的呢?
请阅读教材,了解聚合反应的特点。
由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。
乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
单体
链节
聚合度
二、探究性质,推测结构
n CH3CH=CH2
CH CH2
CH3
n ClCH=CH2
CH2 CH
Cl
n CF2=CF2
C C
F
F
F
F
丙烯
聚丙烯
氯乙烯
聚氯乙烯
四氟乙烯
聚四氟乙烯
(1)CH3CH3、H2C CH2、CH(CH3)3
(2)CH2=CH2、CH2=C(CH3)2、
(3)CH CH、CH CCH3、CH3C CCH3
(4) 、 、
CH2
三、求同存异,探究分类
下列各组有机物的共同特点是什么?
这12种有机物的共同特点是什么
(1)分子中的碳原子均为饱和碳原子——饱和烃
(2)分子中都含有碳碳双键——不饱和烃(烯烃)
(3)分子中都含有碳碳三键——不饱和烃(炔烃)
(4)分子中都含有苯环——芳香烃
12种有机物都为仅含有碳和氢两种元素的烃,也称为碳氢化合物
CH3
CH=CH2
CH2
CH2
CH2
CH2
CH
CH
烃与有机高分子材料
Ω(C6H6) 异常性质 结构特点 结构简式
4 不能使溴水和酸性KMnO4溶液褪色 苯分子为平面正六边形结构,不存在单键和双键交替,6个碳原子之间的键完全相同,是介于碳碳单键和碳碳双键之间的独特的键。
四、搭建模型,探究结构
甲烷 结构式 球棍模型
结构特点 (1)正四面体空间结构,碳原子位于中心,4个氢原子位于正四面体的4个顶点 (2)4个C—H键是极性键,键长相等。 (3)4个C—H键之间的夹角(键角)相等,是109°28',甲烷分子中任意4个原子不共面。 (4)4个氢原子的空间位置是等同的,用1个氯原子取代任意1个氢原子都得到相同的一氯甲烷,即CH3Cl没有同分异构体;用2个氯原子取代任意2个氢原子也得到相同的二氯甲烷,即CH2Cl,没有同分异构体;同理,CHCl3和CCl4都没有同分异构体。
四、搭建模型,探究结构
乙烷 乙烯 乙炔 分子式 结构式 分子式 结构式 分子式 结构式
C2H6 C2H4 C2H2
结构特点 (1)立体结构 (2)键角:109°28 (3)一个分子内有一个碳碳非极性单键和六个碳氢极性键 (4)六个氢原子的空间位置等同 (5)碳原子有四个单键,只有单键的碳是饱和碳原子 (1)平面结构 (2)键角:120° (3)一个分子内有一个碳碳非极性双键和四个碳氢极性键 (4)四个氢原子的空间位置等同 (5)碳原子有四个共价键,双键中的碳是不饱和碳原子 (1)直线形 (2)键角:180° (3)一个分子内有一个碳碳非极性三键和二个碳氢极性键 (4)两个氢原子的空间位置等同 (5)碳原子有四个共价键,三键中的碳是不饱和碳原子
搭建苯乙烯的球棍模型。思考苯乙烯(C8H8)分子中共平面的原子最多有几个,共直线的原子最多有几个。
16
4
CH CH
塑料
多数塑料绝缘性好、耐化学腐蚀,耐热性差。
塑料
五、联系实际,探究用途
橡胶树被称为会“流泪”的树。
天然橡胶就是由橡胶树割胶时流出的胶乳经凝固、干燥后而制得。
从结构上看,天然橡胶易老化的主要原因是什么?
橡胶
天然橡胶分子结构中的碳碳双键易发生化学反应。
五、联系实际,探究用途
橡胶硫化结构的变化及性能有哪些改善?
橡胶硫化使线型的高分子链之间通过硫原子形成化学键,产生交联,形成网状结构。硫化橡胶具有更好的强度、韧性、弹性和化学稳定性。
生胶
硫化胶
橡胶
五、联系实际,探究用途
阅读教材,了解纤维的分类,归纳总结合成纤维有哪些优良性能和用途。
(1)纤维分类:纤维分为天然纤维、再生纤维、合成纤维;再生纤维与合成纤维统称为化学纤维。
(2)合成纤维的性能:具有强度高、弹性好、耐磨、耐化学腐蚀、不易虫蛀等优良性能。
(3)用途:除了供人类穿着外,还可以制成绳索、渔网、工业用滤布,以及飞机、船舶的结构材料等。
纤维
一、乙烯
1.乙烯的用途
2.化学性质与结构
(1)加成——与H2、H2O、HCl反应
(2)氧化反应——与酸性KMnO4溶液、O2反应
(3)加聚反应——生成聚乙烯
二、烃的分类
1.烯烃、炔烃和芳香烃的定义
2.烃的分类标准
课堂小结
乙 烯
课堂小结
一、烃的分子结构
1.苯的结构:平面正六边形
2.乙烷、乙烯、乙炔的球棍模型
(1)乙烷:立体结构
(2)乙烯:平面结构
(3)乙炔:直线结构
二、有机高分子材料
塑料、橡胶、纤维
烃与有机高分子材料
今日作业
1.梳理课堂笔记。
2.【练透】
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
