2023年浙江中考科学三轮冲刺——易错5金属活动性顺序(含解析)
文档属性
| 名称 | 2023年浙江中考科学三轮冲刺——易错5金属活动性顺序(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 140.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-06-02 13:27:01 | ||
图片预览



文档简介
2023年浙江中考科学三轮冲刺——易错5金属活动性顺序
一.选择题(共15小题)
1.(2023 婺城区三模)小明将甲、乙、丙三种金属与两种溶液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为( )
A.甲>乙>丙 B.乙>丙>甲 C.丙>甲>乙 D.甲>丙>乙
2.(2023 柯桥区一模)如图曲线能正确反映下列化学变化中y与x(加入的物质质量)变化关系的是
( )
A.铜粉中滴入稀硫酸;y代表氢气的质量
B.CaCl2溶液中通入CO2气体:y代表沉淀的质量
C.NaOH溶液中滴入稀盐酸:y代表混合溶液的pH
D.CuCl2和HCl的混合溶液中加入NaOH溶液,y代表沉淀的质量
3.(2023 文成县模拟)小文同学通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A.Fe>Cu>R>Ag B.Fe>R>Cu>Ag C.R>Fe>Cu>Ag D.Fe>Ag>Cu>R
4.(2023 文成县二模)已知一铜、锌合金粉末,加入到AgNO3溶液中,如果过滤后得到的固体中物质的种类为a,滤液中溶质的种类为b,则下列说法正确的是( )
A.若向固体中滴加稀盐酸,有气泡产生,则a+b=4
B.若a+b=4,则滤纸上一定有Ag和Cu,滤液中一定含有Zn(NO3)2和Cu(NO3)2
C.若溶液呈蓝色,则a=1
D.若a+b=3,则滤液中可能不含AgNO3
5.(2023 瑞安市模拟)有A,B两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
6.(2023 临安区一模)钯、镍、铜在电子工业中有广泛应用。小明想比较这三种金属的活动性强弱,做了如图所示实验,只有实验④有明显的现象。则这三种金属的活动性顺序排序正确的是( )
A.铜>镍>钯 B.铜>钯>镍 C.镍>钯>铜 D.镍>铜>钯
7.(2023 鹿城区模拟)已知X、Y、Z三种金属,它们之间存在下列反应,请你选择它们的活动性顺序表示正确的是( )
①X+H2SO4═XSO4+H2↑
②Z+YSO4═ZSO4+Y
③Y、Z与H2SO4不发生反应
A.X>Y>Z B.Y>X>Z C.Z>X>Y D.X>Z>Y
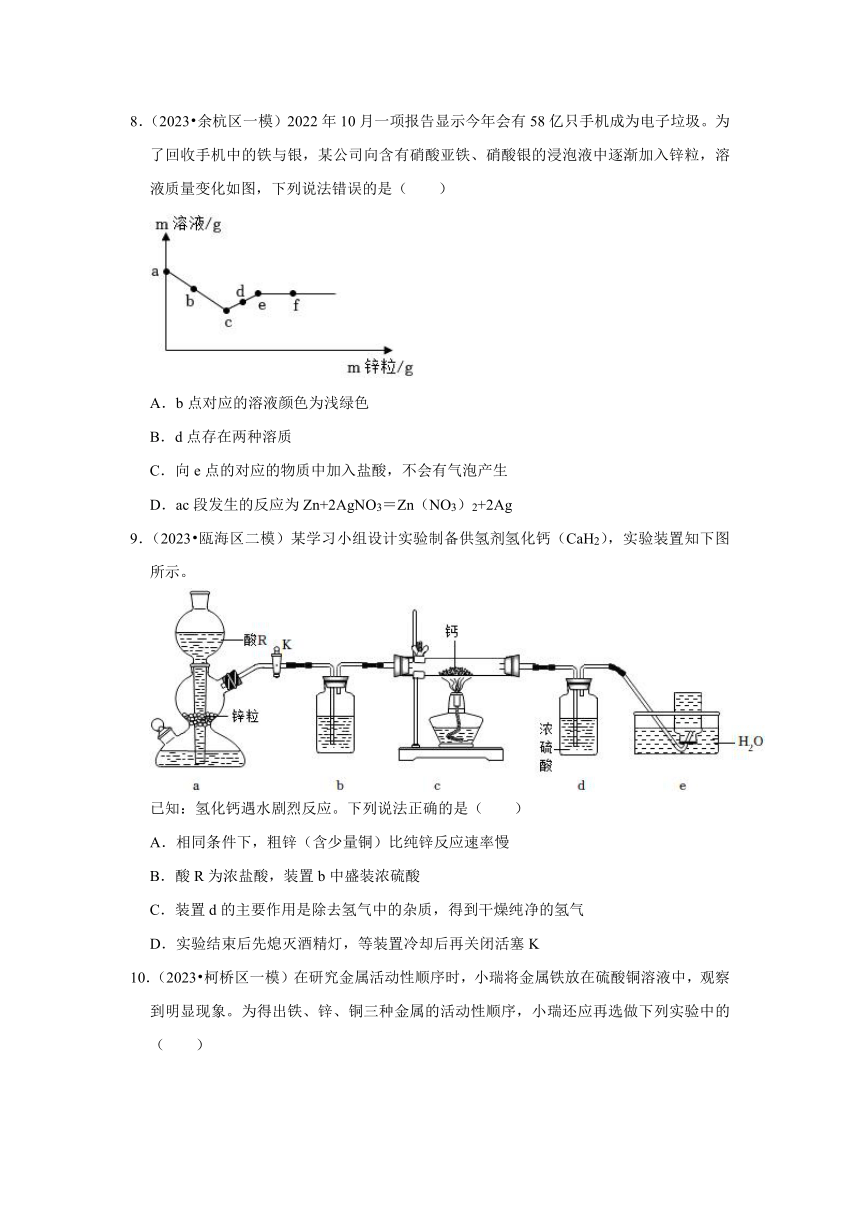
8.(2023 余杭区一模)2022年10月一项报告显示今年会有58亿只手机成为电子垃圾。为了回收手机中的铁与银,某公司向含有硝酸亚铁、硝酸银的浸泡液中逐渐加入锌粒,溶液质量变化如图,下列说法错误的是( )
A.b点对应的溶液颜色为浅绿色
B.d点存在两种溶质
C.向e点的对应的物质中加入盐酸,不会有气泡产生
D.ac段发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag
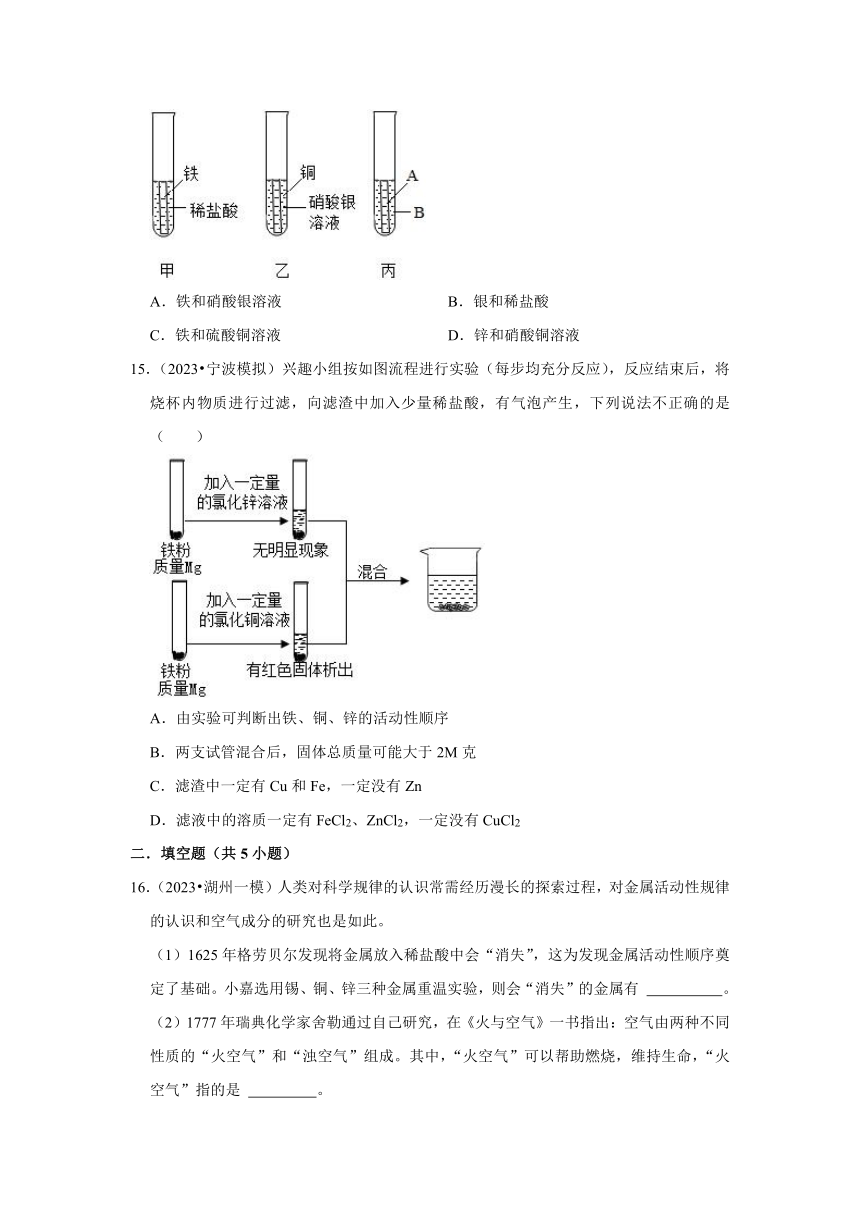
9.(2023 瓯海区二模)某学习小组设计实验制备供氢剂氢化钙(CaH2),实验装置知下图所示。
已知:氢化钙遇水剧烈反应。下列说法正确的是( )
A.相同条件下,粗锌(含少量铜)比纯锌反应速率慢
B.酸R为浓盐酸,装置b中盛装浓硫酸
C.装置d的主要作用是除去氢气中的杂质,得到干燥纯净的氢气
D.实验结束后先熄灭酒精灯,等装置冷却后再关闭活塞K
10.(2023 柯桥区一模)在研究金属活动性顺序时,小瑞将金属铁放在硫酸铜溶液中,观察到明显现象。为得出铁、锌、铜三种金属的活动性顺序,小瑞还应再选做下列实验中的( )
A. B. C. D.
11.(2023 宁波模拟)向AgNO3溶液中加入过量铜粉,充分反应后过滤,得滤渣和滤液,则( )
A.滤渣含有Ag、Cu
B.滤液呈无色
C.滤液中一定含有AgNO3
D.向滤渣中滴加稀硫酸有气泡产生
12.(2023 温州模拟)某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是( )
A.Cu的活动性比Ag强,只用盐酸无法探究两者活动性强弱
B.当溶质种类为1种时,金属单质种类可能为2种
C.c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+
D.从m1变化到m2时,溶液中硝酸铜的质量分数不变
13.(2023 湖州模拟)向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤。下列情况中,可能存在的是( )
A.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Cu2+
D.滤纸上有Ag、Cu、Fe,滤液中有Ag+、Cu2+
14.(2023 平阳县模拟)如图某兴趣小组通过实验得出Fe、Cu、Ag 三种金属的活动性顺序,则丙试管中的金属A和溶液B可能的组合是( )
A.铁和硝酸银溶液 B.银和稀盐酸
C.铁和硫酸铜溶液 D.锌和硝酸铜溶液
15.(2023 宁波模拟)兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,有气泡产生,下列说法不正确的是( )
A.由实验可判断出铁、铜、锌的活动性顺序
B.两支试管混合后,固体总质量可能大于2M克
C.滤渣中一定有Cu和Fe,一定没有Zn
D.滤液中的溶质一定有FeCl2、ZnCl2,一定没有CuCl2
二.填空题(共5小题)
16.(2023 湖州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识和空气成分的研究也是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,这为发现金属活动性顺序奠定了基础。小嘉选用锡、铜、锌三种金属重温实验,则会“消失”的金属有 。
(2)1777年瑞典化学家舍勒通过自己研究,在《火与空气》一书指出:空气由两种不同性质的“火空气”和“浊空气”组成。其中,“火空气”可以帮助燃烧,维持生命,“火空气”指的是 。
17.(2023 路桥区一模)氢是实现碳中和的能源载体。
(1)1781年,普里斯特利用金属M与稀盐酸反应制得一定量的氢气。M可能是锌、铜、银三种金属中的 ,该反应的微观示意图如右图,其中表示反应后溶液中金属离子的微粒是 (选填“A”“B”或“C”)。
(2)煤制氢的原理可表示为C+H2OX+H2。则X中肯定含有的元素是 。
18.(2023 温州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识正是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,为发现金属活动性顺序奠定了基础。小明选用镁、铜、锌三种金属进行验证实验,则“消失”的金属有 。
(2)1766年卡文迪许用金属与酸反应制取了一种可燃性气体,称之为“可燃空气”,为探索金属活动性打开了新思路。“可燃空气”是 。
(3)1865年贝开托夫设想找到一种化合物,使之与金属发生反应,根据反应的难易程度来判断金属活动性的强弱。小明运用该规律开展实验,在硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示,则a点时溶液中金属阳离子有 。
19.(2023 南浔区一模)镍(Ni)是一中常见金属,在生产生活中发挥着重要的作用。
(1)用于制造合金。具有“记忆”本领的钛镍合金属于 (选填“纯净物”或“混合物”);
(2)用于电镀工业。铁表面镀镍不易锈蚀,原因是隔绝了铁与 接触;
(3)已知镍的金属活动性位于镁和铜之间,下列四种方案,能验证镁、镍、铜三种金属的活动性顺序方案有 (填写字母)。
20.(2022 永嘉县模拟)有一包固体粉末X可能含有锌、铁、氧化铜中的一种或几种。现将m g该固体粉末加入到一定质量的稀盐酸中,充分反应后剩余ng固体。
(1)若固体粉末X中含有铁、氧化铜,则m n(填“>”“=”或“<”)。
(2)若充分反应后溶液中含有四种阳离子,剩余固体为 (填“纯净物”或“混合物”)。
2023年浙江中考科学三轮冲刺——易错5金属活动性顺序
参考答案与试题解析
一.选择题(共15小题)
1.(2023 婺城区三模)小明将甲、乙、丙三种金属与两种溶液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为( )
A.甲>乙>丙 B.乙>丙>甲 C.丙>甲>乙 D.甲>丙>乙
【解答】解:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,甲能与盐酸反应,乙、丙不能与盐酸反应,说明甲的位置排在氢的前面,乙、丙的位置排在氢的后面,即甲>H>乙、丙。
如果把乙、丙分别放入硝酸银溶液中,乙能与硝酸银溶液反应,丙不能,说明乙的金属活动性比银强,丙的金属活动性比银弱,即乙>银>丙。
则三种金属的活动性顺序为:甲>乙>丙。
故选:A。
2.(2023 柯桥区一模)如图曲线能正确反映下列化学变化中y与x(加入的物质质量)变化关系的是
( )
A.铜粉中滴入稀硫酸;y代表氢气的质量
B.CaCl2溶液中通入CO2气体:y代表沉淀的质量
C.NaOH溶液中滴入稀盐酸:y代表混合溶液的pH
D.CuCl2和HCl的混合溶液中加入NaOH溶液,y代表沉淀的质量
【解答】解:A、铜的金属活动性位于氢后,将铜粉加入稀硫酸中时,没有氢气生成,与图像不符,故A错误;
B、氯化钙和二氧化碳不能反应,与图像不符,故B错误;
C、氢氧化钠与稀盐酸立即开始反应,则溶液的pH会立即减小,与图像不符,故C错误;
D、氢氧化钠溶液先和稀盐酸反应,生成氯化钠和水,此时不会生成沉淀。当稀盐酸完全反应后,氢氧化钠再和氯化铜反应,生成氢氧化铜沉淀,故D正确。
故选:D。
3.(2023 文成县模拟)小文同学通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A.Fe>Cu>R>Ag B.Fe>R>Cu>Ag C.R>Fe>Cu>Ag D.Fe>Ag>Cu>R
【解答】解:由表中的信息可知,1a可与盐酸反应,说明金属活动性Fe位于H前,2指代的金属与盐酸不反应,说明2a和2b对应金属的活动性位于H后,3指代的金属能与硝酸银反应,说明3指代的金属的活动性在银之前,R能与硝酸铜反应,说明R的金属的活动性>铜,说明金属活动性为Fe>R>Cu>Ag。
故选:B。
4.(2023 文成县二模)已知一铜、锌合金粉末,加入到AgNO3溶液中,如果过滤后得到的固体中物质的种类为a,滤液中溶质的种类为b,则下列说法正确的是( )
A.若向固体中滴加稀盐酸,有气泡产生,则a+b=4
B.若a+b=4,则滤纸上一定有Ag和Cu,滤液中一定含有Zn(NO3)2和Cu(NO3)2
C.若溶液呈蓝色,则a=1
D.若a+b=3,则滤液中可能不含AgNO3
【解答】解:由金属活动性顺序表可知,金属的活动性Zn>Cu>Ag,向AgNO3溶液中加入一定质量的Zn和Cu的混合粉末,Zn首先与硝酸银溶液反应,Zn反应完成时,Cu再与硝酸银反应,化学方程式为:①Zn+2AgNO3=2Ag+Zn(NO3)2,②Cu+2AgNO3=2Ag+Cu(NO3)2,所以
A、若滴加稀盐酸产生气泡,说明锌有剩余,则滤渣是锌、铜、银,即a=3,滤液含有硝酸锌,即b=1,因此a+b=4,故A正确;
B、结合D的分析,若硝酸银过量时,溶液中的溶质为硝酸铜、硝酸锌和硝酸银,此时b=3,则a+b=4,故B错误;
C、若溶液呈蓝色,说明铜和硝酸银发生反应产生硝酸铜溶液,所以滤渣一定含有银,一定没有锌,可能含有铜,因此a可能=1或2,故C错误;
D、当a=1时,则得到的金属为银,Cu和Zn全部反应,硝酸银溶液足量。恰好反应时,溶液中的溶质为硝酸铜和硝酸锌,此时b=2,即a+b=3,则一定没有硝酸银,故D错误。
故选:A。
5.(2023 瑞安市模拟)有A,B两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
【解答】解:A、反应生成H2的质量与反应时间的关系图所示,相同时间内B放出氢气的质量大于A,可判断金属活动性顺序是B>A,故A错误;
B、根据反应生成H2的质量与反应时间的关系图所示,在两种金属完全反应后,放出H2的质量是A>B,故B正确;
C、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:A>B,故C错误;
D、金属的相对原子质量和化合价不确定,所以不能确定参加反应的金属的质量,故D错误。
故选:B。
6.(2023 临安区一模)钯、镍、铜在电子工业中有广泛应用。小明想比较这三种金属的活动性强弱,做了如图所示实验,只有实验④有明显的现象。则这三种金属的活动性顺序排序正确的是( )
A.铜>镍>钯 B.铜>钯>镍 C.镍>钯>铜 D.镍>铜>钯
【解答】解:①中无现象,说明了金属的活动性是铜<氢;
②中无现象,说明了金属的活动性是钯<氢;
③中无现象,说明了金属的活动性是铜>钯;
④有明显的现象,说明了金属的活动性是镍>氢;
由以上可知,金属的活动性顺序是:镍>铜>钯。
故选:D。
7.(2023 鹿城区模拟)已知X、Y、Z三种金属,它们之间存在下列反应,请你选择它们的活动性顺序表示正确的是( )
①X+H2SO4═XSO4+H2↑
②Z+YSO4═ZSO4+Y
③Y、Z与H2SO4不发生反应
A.X>Y>Z B.Y>X>Z C.Z>X>Y D.X>Z>Y
【解答】解:①X+H2SO4═XSO4+H2↑,说明X的位置排在氢的前面,即X>H。
③Y、Z与H2SO4不发生反应,说明Y、Z的位置排在氢的后面,即H>Y、Z。
②Z+YSO4═ZSO4+Y,说明Z的金属活动性比Y强,即Z>Y。
则X、Y和Z的金属活动性顺序为:X>Z>Y。
故选:D。
8.(2023 余杭区一模)2022年10月一项报告显示今年会有58亿只手机成为电子垃圾。为了回收手机中的铁与银,某公司向含有硝酸亚铁、硝酸银的浸泡液中逐渐加入锌粒,溶液质量变化如图,下列说法错误的是( )
A.b点对应的溶液颜色为浅绿色
B.d点存在两种溶质
C.向e点的对应的物质中加入盐酸,不会有气泡产生
D.ac段发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag
【解答】解:A、ac段的反应是锌和硝酸银反应生成硝酸锌和银,硝酸亚铁还没参与反应,则b点对应的溶液颜色为浅绿色,故选项说法正确。
B、d点时硝酸银已经完全反应,硝酸亚铁还没反应完,则d点存在生成的硝酸锌和没反应完的硝酸亚铁两种溶质,故选项说法正确。
C、e点时锌和硝酸银、硝酸亚铁恰好完全反应,对应物质中有生成的铁,铁和盐酸反应会生成氢气,则向e点的对应的物质中加入盐酸,会有气泡产生,故选项说法错误。
D、ac段是锌和硝酸银反应,发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag,故选项说法正确。
故选:C。
9.(2023 瓯海区二模)某学习小组设计实验制备供氢剂氢化钙(CaH2),实验装置知下图所示。
已知:氢化钙遇水剧烈反应。下列说法正确的是( )
A.相同条件下,粗锌(含少量铜)比纯锌反应速率慢
B.酸R为浓盐酸,装置b中盛装浓硫酸
C.装置d的主要作用是除去氢气中的杂质,得到干燥纯净的氢气
D.实验结束后先熄灭酒精灯,等装置冷却后再关闭活塞K
【解答】解:A、锌和铜与酸混合,能够形成原电池,能够加快反应速率,相同条件下,粗锌(含少量铜)比纯锌反应速率快,该选项不正确。
B、酸R为稀硫酸,不能用浓盐酸,是因为浓盐酸易挥发,该选项不正确。
C、装置d的主要作用是防止水蒸气进入玻璃管中,该选项不正确。
D、实验结束后先熄灭酒精灯,等装置冷却后再关闭活塞K,以防止浓硫酸倒吸入玻璃管中,该选项正确。
故选:D。
10.(2023 柯桥区一模)在研究金属活动性顺序时,小瑞将金属铁放在硫酸铜溶液中,观察到明显现象。为得出铁、锌、铜三种金属的活动性顺序,小瑞还应再选做下列实验中的( )
A. B. C. D.
【解答】解:在研究金属活动性顺序时,小瑞将金属铁放在硫酸铜溶液中,观察到明显现象,说明了金属活动性铁>铜。为得出铁、锌、铜三种金属的活动性顺序,还需再证明锌
>铁,故小瑞还应再做B实验,铁和硫酸锌溶液不反应,说明铁的金属活动性比锌弱,即锌>铁。
故选:B。
11.(2023 宁波模拟)向AgNO3溶液中加入过量铜粉,充分反应后过滤,得滤渣和滤液,则( )
A.滤渣含有Ag、Cu
B.滤液呈无色
C.滤液中一定含有AgNO3
D.向滤渣中滴加稀硫酸有气泡产生
【解答】解:A、向AgNO3溶液中加入过量铜粉,铜与硝酸银溶液反应生成硝酸铜溶液和银,铜粉是过量的,硝酸银完全反应,充分反应后过滤,滤渣中含有Ag、Cu,故选项说法正确。
B、滤液为硝酸铜溶液,为蓝色溶液,故选项说法错误。
C、铜粉是过量的,硝酸银完全反应,滤液中一定不含AgNO3,故选项说法错误。
D、滤渣中含有Ag、Cu,向滤渣中滴加稀硫酸,均不反应,没有气泡产生,故选项说法错误。
故选:A。
12.(2023 温州模拟)某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是( )
A.Cu的活动性比Ag强,只用盐酸无法探究两者活动性强弱
B.当溶质种类为1种时,金属单质种类可能为2种
C.c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+
D.从m1变化到m2时,溶液中硝酸铜的质量分数不变
【解答】解:A、Cu的活动性比Ag强,铜、银均不能与稀盐酸反应,只用盐酸无法探究两者活动性强弱,故选项说法正确。
B、当溶质种类为1种时,可能是锌与硝酸铜恰好完全反应,金属单质种类可能为银、铜2种,故选项说法正确。
C、c~d间(不含两点),发生的是锌与硝酸铜的反应,溶液中金属离子为Zn2+、Cu2+,故选项说法正确。
D、从m1变化到m2时,发生的是Zn+2AgNO3═Zn(NO3)2+2Ag,由反应时的质量比可知,每65份质量的锌可置换出216份质量的银,溶液的质量会减少,则溶液中硝酸铜的质量分数增大,故选项说法错误。
故选:D。
13.(2023 湖州模拟)向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤。下列情况中,可能存在的是( )
A.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Cu2+
D.滤纸上有Ag、Cu、Fe,滤液中有Ag+、Cu2+
【解答】解:向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,铁先和硝酸银反应生成硝酸亚铁和银,后和硝酸铜反应生成硝酸亚铁和铜。
A、滤纸上有Cu,滤液中一定没有Ag+,该选项不正确。
B、滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+,例如硝酸银过量时,该选项正确。
C、滤纸上有Ag、Cu、Fe,滤液中一定没有Cu2+,该选项不正确。
D、滤纸上有Ag、Cu、Fe,滤液中一定没有Ag+、Cu2+,该选项不正确。
故选:B。
14.(2023 平阳县模拟)如图某兴趣小组通过实验得出Fe、Cu、Ag 三种金属的活动性顺序,则丙试管中的金属A和溶液B可能的组合是( )
A.铁和硝酸银溶液 B.银和稀盐酸
C.铁和硫酸铜溶液 D.锌和硝酸铜溶液
【解答】解:甲中铁能与盐酸反应,可知,Fe>H;由乙中铜能置换硝酸银中的铜,可知Cu>Ag;
A、硝酸银溶液和铁能反应,说明Ag<Fe,不能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项不符合题意;
B、稀盐酸和银不能反应,说明H>Ag,不能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项不符合题意;
C、铁能和硫酸铜溶液反应,说明Fe>Cu,能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项符合题意;
D、锌能和硝酸铜溶液反应,说明Zn>Cu,不能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项不符合题意。
故选:C。
15.(2023 宁波模拟)兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,有气泡产生,下列说法不正确的是( )
A.由实验可判断出铁、铜、锌的活动性顺序
B.两支试管混合后,固体总质量可能大于2M克
C.滤渣中一定有Cu和Fe,一定没有Zn
D.滤液中的溶质一定有FeCl2、ZnCl2,一定没有CuCl2
【解答】解:由于金属的活动性强弱是:锌>铁>铜,在进行实验时,铁不能与氯化锌反应,能与氯化铜反应生成了氯化亚铁和铜,反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,有气泡产生,说明了铁有剩余;所以:
A、根据铁不能与氯化锌反应,能与氯化铜反应,可以判断出铁、铜、锌的活动性顺序,故A说法正确;
B、由于每56份质量的铁能置换出64份质量的铜,铁不能置换氯化锌中的锌,所以两支试管混合后,第一支试管没反应的铁可以继续与第二支试管中的氯化铜反应,所以固体总质量一定大于2M,故B说法错误;
C、由上述分析可知,滤渣中一定有Cu和Fe,一定没有Zn,故C说法正确;
D、由上述分析可知,滤液中的溶质一定有FeCl2、ZnCl2,一定没有CuCl2,故D说法正确;
故选:B。
二.填空题(共5小题)
16.(2023 湖州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识和空气成分的研究也是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,这为发现金属活动性顺序奠定了基础。小嘉选用锡、铜、锌三种金属重温实验,则会“消失”的金属有 锡、锌 。
(2)1777年瑞典化学家舍勒通过自己研究,在《火与空气》一书指出:空气由两种不同性质的“火空气”和“浊空气”组成。其中,“火空气”可以帮助燃烧,维持生命,“火空气”指的是 氧气 。
【解答】解:(1)在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,锡、铜、锌三种金属重温实验,在金属活动性顺序中,锡、锌的位置排在氢的前面,则会“消失”的金属有锡、锌。
(2)由题意,空气由两种不同性质的“火空气”和“浊空气”组成。其中,“火空气”可以帮助燃烧,维持生命,“火空气”指的是能支持燃烧的氧气。
故答案为:
(1)锡、锌;
(2)氧气。
17.(2023 路桥区一模)氢是实现碳中和的能源载体。
(1)1781年,普里斯特利用金属M与稀盐酸反应制得一定量的氢气。M可能是锌、铜、银三种金属中的 锌 ,该反应的微观示意图如右图,其中表示反应后溶液中金属离子的微粒是 C (选填“A”“B”或“C”)。
(2)煤制氢的原理可表示为C+H2OX+H2。则X中肯定含有的元素是 CO 。
【解答】解:(1)在金属活动性顺序中,锌排在氢的前面,能与盐酸反应生成氢气,而铜和银排在氢的后面,与盐酸不反应,因此M可能是锌;由微观反应示意图可知,A表示氢离子,B表示氯离子,C表示锌离子;故答案为:锌;C;
(2)由C+H2OX+H2可知,反应前有1个碳原子、1个氧原子和2个氢原子,反应后有2个氢原子,则每个X分子中含有1个碳原子与1个氧原子,则X的化学式为CO;故答案为:CO。
18.(2023 温州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识正是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,为发现金属活动性顺序奠定了基础。小明选用镁、铜、锌三种金属进行验证实验,则“消失”的金属有 镁、锌 。
(2)1766年卡文迪许用金属与酸反应制取了一种可燃性气体,称之为“可燃空气”,为探索金属活动性打开了新思路。“可燃空气”是 氢气 。
(3)1865年贝开托夫设想找到一种化合物,使之与金属发生反应,根据反应的难易程度来判断金属活动性的强弱。小明运用该规律开展实验,在硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示,则a点时溶液中金属阳离子有 Zn2+、Fe2+ 。
【解答】解:(1)小明选用镁、铜、锌三种金属进行验证实验,在金属活动性顺序中,镁、锌位于氢前,能和稀盐酸反应,铜位于氢后,不能和稀盐酸反应,则“消失”的金属有镁、锌。
(2)活泼金属与酸反应生成可燃性的氢气,卡文迪许称之为“可燃空气”,则“可燃空气”是氢气。
(3)在硝酸银和硝酸亚铁的混合溶液中加入锌粉,锌先和硝酸银反应生成硝酸锌和银,由化学方程式的质量关系可知,反应后溶液质量减小,硝酸银反应完后,锌再和硝酸亚铁反应生成硝酸锌和铁,由化学方程式的质量关系可知,反应后溶液质量增大,则a点时硝酸银恰好完全反应,溶液中所含的金属阳离子有Zn2+、Fe2+。
故答案为:
(1)镁、锌;
(2)氢气;
(3)Zn2+、Fe2+。
19.(2023 南浔区一模)镍(Ni)是一中常见金属,在生产生活中发挥着重要的作用。
(1)用于制造合金。具有“记忆”本领的钛镍合金属于 混合物 (选填“纯净物”或“混合物”);
(2)用于电镀工业。铁表面镀镍不易锈蚀,原因是隔绝了铁与 氧气、水 接触;
(3)已知镍的金属活动性位于镁和铜之间,下列四种方案,能验证镁、镍、铜三种金属的活动性顺序方案有 BC (填写字母)。
【解答】解:(1)钛镍合金是由多种物质组成的,属于混合物;故答案为:混合物;
(2)铁与氧气和水接触会发生锈蚀,铁表面镀镍不易锈蚀,原因是隔绝了铁与氧气、水的接触;故答案为:氧气、水;
(3)已知镍的金属活动性位于镁和铜之间,即三种金属活动性由强到弱依次为镁、镍、铜。
A、镁、镍均能会置换出硫酸铜溶液中的铜,说明铜最不活泼,但无法证明镁和镍的活动性强弱,不合题意;
B、镍与硫酸镁不反应,镍能置换出硫酸铜溶液中的铜,说明活动性镁>镍>铜,符合题意;
C、镁能置换出硫酸镍中的镍,说明镁的活动性大于镍;镍能置换出硫酸铜溶液中的铜,说明活动性镁>镍>铜,符合题意;
D、镍和铜均不能与硫酸镁溶液反应,说明镁最活泼,但无法证明镍和铜的活动性强弱,不合题意;
故答案为:BC。
20.(2022 永嘉县模拟)有一包固体粉末X可能含有锌、铁、氧化铜中的一种或几种。现将m g该固体粉末加入到一定质量的稀盐酸中,充分反应后剩余ng固体。
(1)若固体粉末X中含有铁、氧化铜,则m > n(填“>”“=”或“<”)。
(2)若充分反应后溶液中含有四种阳离子,剩余固体为 纯净物 (填“纯净物”或“混合物”)。
【解答】解:(1)固体粉末中铁都会与盐酸反应生成盐而形成溶液,即使氧化铜和盐酸反应生成氯化铜,铁可以将氯化铜中的铜置换出来,得到的也只是氧化铜中铜元素的质量,所以m>n;
(2)若充分反应后溶液中含有四种阳离子,溶液中只能含有锌离子、亚铁离子、铜离子、氢离子,所以剩余固体只能是锌置换出部分氯化铜中的铜,一定为纯净物。
故答案为:(1)>;
(2)纯净物。
一.选择题(共15小题)
1.(2023 婺城区三模)小明将甲、乙、丙三种金属与两种溶液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为( )
A.甲>乙>丙 B.乙>丙>甲 C.丙>甲>乙 D.甲>丙>乙
2.(2023 柯桥区一模)如图曲线能正确反映下列化学变化中y与x(加入的物质质量)变化关系的是
( )
A.铜粉中滴入稀硫酸;y代表氢气的质量
B.CaCl2溶液中通入CO2气体:y代表沉淀的质量
C.NaOH溶液中滴入稀盐酸:y代表混合溶液的pH
D.CuCl2和HCl的混合溶液中加入NaOH溶液,y代表沉淀的质量
3.(2023 文成县模拟)小文同学通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A.Fe>Cu>R>Ag B.Fe>R>Cu>Ag C.R>Fe>Cu>Ag D.Fe>Ag>Cu>R
4.(2023 文成县二模)已知一铜、锌合金粉末,加入到AgNO3溶液中,如果过滤后得到的固体中物质的种类为a,滤液中溶质的种类为b,则下列说法正确的是( )
A.若向固体中滴加稀盐酸,有气泡产生,则a+b=4
B.若a+b=4,则滤纸上一定有Ag和Cu,滤液中一定含有Zn(NO3)2和Cu(NO3)2
C.若溶液呈蓝色,则a=1
D.若a+b=3,则滤液中可能不含AgNO3
5.(2023 瑞安市模拟)有A,B两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
6.(2023 临安区一模)钯、镍、铜在电子工业中有广泛应用。小明想比较这三种金属的活动性强弱,做了如图所示实验,只有实验④有明显的现象。则这三种金属的活动性顺序排序正确的是( )
A.铜>镍>钯 B.铜>钯>镍 C.镍>钯>铜 D.镍>铜>钯
7.(2023 鹿城区模拟)已知X、Y、Z三种金属,它们之间存在下列反应,请你选择它们的活动性顺序表示正确的是( )
①X+H2SO4═XSO4+H2↑
②Z+YSO4═ZSO4+Y
③Y、Z与H2SO4不发生反应
A.X>Y>Z B.Y>X>Z C.Z>X>Y D.X>Z>Y
8.(2023 余杭区一模)2022年10月一项报告显示今年会有58亿只手机成为电子垃圾。为了回收手机中的铁与银,某公司向含有硝酸亚铁、硝酸银的浸泡液中逐渐加入锌粒,溶液质量变化如图,下列说法错误的是( )
A.b点对应的溶液颜色为浅绿色
B.d点存在两种溶质
C.向e点的对应的物质中加入盐酸,不会有气泡产生
D.ac段发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag
9.(2023 瓯海区二模)某学习小组设计实验制备供氢剂氢化钙(CaH2),实验装置知下图所示。
已知:氢化钙遇水剧烈反应。下列说法正确的是( )
A.相同条件下,粗锌(含少量铜)比纯锌反应速率慢
B.酸R为浓盐酸,装置b中盛装浓硫酸
C.装置d的主要作用是除去氢气中的杂质,得到干燥纯净的氢气
D.实验结束后先熄灭酒精灯,等装置冷却后再关闭活塞K
10.(2023 柯桥区一模)在研究金属活动性顺序时,小瑞将金属铁放在硫酸铜溶液中,观察到明显现象。为得出铁、锌、铜三种金属的活动性顺序,小瑞还应再选做下列实验中的( )
A. B. C. D.
11.(2023 宁波模拟)向AgNO3溶液中加入过量铜粉,充分反应后过滤,得滤渣和滤液,则( )
A.滤渣含有Ag、Cu
B.滤液呈无色
C.滤液中一定含有AgNO3
D.向滤渣中滴加稀硫酸有气泡产生
12.(2023 温州模拟)某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是( )
A.Cu的活动性比Ag强,只用盐酸无法探究两者活动性强弱
B.当溶质种类为1种时,金属单质种类可能为2种
C.c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+
D.从m1变化到m2时,溶液中硝酸铜的质量分数不变
13.(2023 湖州模拟)向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤。下列情况中,可能存在的是( )
A.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Cu2+
D.滤纸上有Ag、Cu、Fe,滤液中有Ag+、Cu2+
14.(2023 平阳县模拟)如图某兴趣小组通过实验得出Fe、Cu、Ag 三种金属的活动性顺序,则丙试管中的金属A和溶液B可能的组合是( )
A.铁和硝酸银溶液 B.银和稀盐酸
C.铁和硫酸铜溶液 D.锌和硝酸铜溶液
15.(2023 宁波模拟)兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,有气泡产生,下列说法不正确的是( )
A.由实验可判断出铁、铜、锌的活动性顺序
B.两支试管混合后,固体总质量可能大于2M克
C.滤渣中一定有Cu和Fe,一定没有Zn
D.滤液中的溶质一定有FeCl2、ZnCl2,一定没有CuCl2
二.填空题(共5小题)
16.(2023 湖州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识和空气成分的研究也是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,这为发现金属活动性顺序奠定了基础。小嘉选用锡、铜、锌三种金属重温实验,则会“消失”的金属有 。
(2)1777年瑞典化学家舍勒通过自己研究,在《火与空气》一书指出:空气由两种不同性质的“火空气”和“浊空气”组成。其中,“火空气”可以帮助燃烧,维持生命,“火空气”指的是 。
17.(2023 路桥区一模)氢是实现碳中和的能源载体。
(1)1781年,普里斯特利用金属M与稀盐酸反应制得一定量的氢气。M可能是锌、铜、银三种金属中的 ,该反应的微观示意图如右图,其中表示反应后溶液中金属离子的微粒是 (选填“A”“B”或“C”)。
(2)煤制氢的原理可表示为C+H2OX+H2。则X中肯定含有的元素是 。
18.(2023 温州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识正是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,为发现金属活动性顺序奠定了基础。小明选用镁、铜、锌三种金属进行验证实验,则“消失”的金属有 。
(2)1766年卡文迪许用金属与酸反应制取了一种可燃性气体,称之为“可燃空气”,为探索金属活动性打开了新思路。“可燃空气”是 。
(3)1865年贝开托夫设想找到一种化合物,使之与金属发生反应,根据反应的难易程度来判断金属活动性的强弱。小明运用该规律开展实验,在硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示,则a点时溶液中金属阳离子有 。
19.(2023 南浔区一模)镍(Ni)是一中常见金属,在生产生活中发挥着重要的作用。
(1)用于制造合金。具有“记忆”本领的钛镍合金属于 (选填“纯净物”或“混合物”);
(2)用于电镀工业。铁表面镀镍不易锈蚀,原因是隔绝了铁与 接触;
(3)已知镍的金属活动性位于镁和铜之间,下列四种方案,能验证镁、镍、铜三种金属的活动性顺序方案有 (填写字母)。
20.(2022 永嘉县模拟)有一包固体粉末X可能含有锌、铁、氧化铜中的一种或几种。现将m g该固体粉末加入到一定质量的稀盐酸中,充分反应后剩余ng固体。
(1)若固体粉末X中含有铁、氧化铜,则m n(填“>”“=”或“<”)。
(2)若充分反应后溶液中含有四种阳离子,剩余固体为 (填“纯净物”或“混合物”)。
2023年浙江中考科学三轮冲刺——易错5金属活动性顺序
参考答案与试题解析
一.选择题(共15小题)
1.(2023 婺城区三模)小明将甲、乙、丙三种金属与两种溶液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为( )
A.甲>乙>丙 B.乙>丙>甲 C.丙>甲>乙 D.甲>丙>乙
【解答】解:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,甲能与盐酸反应,乙、丙不能与盐酸反应,说明甲的位置排在氢的前面,乙、丙的位置排在氢的后面,即甲>H>乙、丙。
如果把乙、丙分别放入硝酸银溶液中,乙能与硝酸银溶液反应,丙不能,说明乙的金属活动性比银强,丙的金属活动性比银弱,即乙>银>丙。
则三种金属的活动性顺序为:甲>乙>丙。
故选:A。
2.(2023 柯桥区一模)如图曲线能正确反映下列化学变化中y与x(加入的物质质量)变化关系的是
( )
A.铜粉中滴入稀硫酸;y代表氢气的质量
B.CaCl2溶液中通入CO2气体:y代表沉淀的质量
C.NaOH溶液中滴入稀盐酸:y代表混合溶液的pH
D.CuCl2和HCl的混合溶液中加入NaOH溶液,y代表沉淀的质量
【解答】解:A、铜的金属活动性位于氢后,将铜粉加入稀硫酸中时,没有氢气生成,与图像不符,故A错误;
B、氯化钙和二氧化碳不能反应,与图像不符,故B错误;
C、氢氧化钠与稀盐酸立即开始反应,则溶液的pH会立即减小,与图像不符,故C错误;
D、氢氧化钠溶液先和稀盐酸反应,生成氯化钠和水,此时不会生成沉淀。当稀盐酸完全反应后,氢氧化钠再和氯化铜反应,生成氢氧化铜沉淀,故D正确。
故选:D。
3.(2023 文成县模拟)小文同学通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A.Fe>Cu>R>Ag B.Fe>R>Cu>Ag C.R>Fe>Cu>Ag D.Fe>Ag>Cu>R
【解答】解:由表中的信息可知,1a可与盐酸反应,说明金属活动性Fe位于H前,2指代的金属与盐酸不反应,说明2a和2b对应金属的活动性位于H后,3指代的金属能与硝酸银反应,说明3指代的金属的活动性在银之前,R能与硝酸铜反应,说明R的金属的活动性>铜,说明金属活动性为Fe>R>Cu>Ag。
故选:B。
4.(2023 文成县二模)已知一铜、锌合金粉末,加入到AgNO3溶液中,如果过滤后得到的固体中物质的种类为a,滤液中溶质的种类为b,则下列说法正确的是( )
A.若向固体中滴加稀盐酸,有气泡产生,则a+b=4
B.若a+b=4,则滤纸上一定有Ag和Cu,滤液中一定含有Zn(NO3)2和Cu(NO3)2
C.若溶液呈蓝色,则a=1
D.若a+b=3,则滤液中可能不含AgNO3
【解答】解:由金属活动性顺序表可知,金属的活动性Zn>Cu>Ag,向AgNO3溶液中加入一定质量的Zn和Cu的混合粉末,Zn首先与硝酸银溶液反应,Zn反应完成时,Cu再与硝酸银反应,化学方程式为:①Zn+2AgNO3=2Ag+Zn(NO3)2,②Cu+2AgNO3=2Ag+Cu(NO3)2,所以
A、若滴加稀盐酸产生气泡,说明锌有剩余,则滤渣是锌、铜、银,即a=3,滤液含有硝酸锌,即b=1,因此a+b=4,故A正确;
B、结合D的分析,若硝酸银过量时,溶液中的溶质为硝酸铜、硝酸锌和硝酸银,此时b=3,则a+b=4,故B错误;
C、若溶液呈蓝色,说明铜和硝酸银发生反应产生硝酸铜溶液,所以滤渣一定含有银,一定没有锌,可能含有铜,因此a可能=1或2,故C错误;
D、当a=1时,则得到的金属为银,Cu和Zn全部反应,硝酸银溶液足量。恰好反应时,溶液中的溶质为硝酸铜和硝酸锌,此时b=2,即a+b=3,则一定没有硝酸银,故D错误。
故选:A。
5.(2023 瑞安市模拟)有A,B两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
【解答】解:A、反应生成H2的质量与反应时间的关系图所示,相同时间内B放出氢气的质量大于A,可判断金属活动性顺序是B>A,故A错误;
B、根据反应生成H2的质量与反应时间的关系图所示,在两种金属完全反应后,放出H2的质量是A>B,故B正确;
C、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:A>B,故C错误;
D、金属的相对原子质量和化合价不确定,所以不能确定参加反应的金属的质量,故D错误。
故选:B。
6.(2023 临安区一模)钯、镍、铜在电子工业中有广泛应用。小明想比较这三种金属的活动性强弱,做了如图所示实验,只有实验④有明显的现象。则这三种金属的活动性顺序排序正确的是( )
A.铜>镍>钯 B.铜>钯>镍 C.镍>钯>铜 D.镍>铜>钯
【解答】解:①中无现象,说明了金属的活动性是铜<氢;
②中无现象,说明了金属的活动性是钯<氢;
③中无现象,说明了金属的活动性是铜>钯;
④有明显的现象,说明了金属的活动性是镍>氢;
由以上可知,金属的活动性顺序是:镍>铜>钯。
故选:D。
7.(2023 鹿城区模拟)已知X、Y、Z三种金属,它们之间存在下列反应,请你选择它们的活动性顺序表示正确的是( )
①X+H2SO4═XSO4+H2↑
②Z+YSO4═ZSO4+Y
③Y、Z与H2SO4不发生反应
A.X>Y>Z B.Y>X>Z C.Z>X>Y D.X>Z>Y
【解答】解:①X+H2SO4═XSO4+H2↑,说明X的位置排在氢的前面,即X>H。
③Y、Z与H2SO4不发生反应,说明Y、Z的位置排在氢的后面,即H>Y、Z。
②Z+YSO4═ZSO4+Y,说明Z的金属活动性比Y强,即Z>Y。
则X、Y和Z的金属活动性顺序为:X>Z>Y。
故选:D。
8.(2023 余杭区一模)2022年10月一项报告显示今年会有58亿只手机成为电子垃圾。为了回收手机中的铁与银,某公司向含有硝酸亚铁、硝酸银的浸泡液中逐渐加入锌粒,溶液质量变化如图,下列说法错误的是( )
A.b点对应的溶液颜色为浅绿色
B.d点存在两种溶质
C.向e点的对应的物质中加入盐酸,不会有气泡产生
D.ac段发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag
【解答】解:A、ac段的反应是锌和硝酸银反应生成硝酸锌和银,硝酸亚铁还没参与反应,则b点对应的溶液颜色为浅绿色,故选项说法正确。
B、d点时硝酸银已经完全反应,硝酸亚铁还没反应完,则d点存在生成的硝酸锌和没反应完的硝酸亚铁两种溶质,故选项说法正确。
C、e点时锌和硝酸银、硝酸亚铁恰好完全反应,对应物质中有生成的铁,铁和盐酸反应会生成氢气,则向e点的对应的物质中加入盐酸,会有气泡产生,故选项说法错误。
D、ac段是锌和硝酸银反应,发生的反应为Zn+2AgNO3=Zn(NO3)2+2Ag,故选项说法正确。
故选:C。
9.(2023 瓯海区二模)某学习小组设计实验制备供氢剂氢化钙(CaH2),实验装置知下图所示。
已知:氢化钙遇水剧烈反应。下列说法正确的是( )
A.相同条件下,粗锌(含少量铜)比纯锌反应速率慢
B.酸R为浓盐酸,装置b中盛装浓硫酸
C.装置d的主要作用是除去氢气中的杂质,得到干燥纯净的氢气
D.实验结束后先熄灭酒精灯,等装置冷却后再关闭活塞K
【解答】解:A、锌和铜与酸混合,能够形成原电池,能够加快反应速率,相同条件下,粗锌(含少量铜)比纯锌反应速率快,该选项不正确。
B、酸R为稀硫酸,不能用浓盐酸,是因为浓盐酸易挥发,该选项不正确。
C、装置d的主要作用是防止水蒸气进入玻璃管中,该选项不正确。
D、实验结束后先熄灭酒精灯,等装置冷却后再关闭活塞K,以防止浓硫酸倒吸入玻璃管中,该选项正确。
故选:D。
10.(2023 柯桥区一模)在研究金属活动性顺序时,小瑞将金属铁放在硫酸铜溶液中,观察到明显现象。为得出铁、锌、铜三种金属的活动性顺序,小瑞还应再选做下列实验中的( )
A. B. C. D.
【解答】解:在研究金属活动性顺序时,小瑞将金属铁放在硫酸铜溶液中,观察到明显现象,说明了金属活动性铁>铜。为得出铁、锌、铜三种金属的活动性顺序,还需再证明锌
>铁,故小瑞还应再做B实验,铁和硫酸锌溶液不反应,说明铁的金属活动性比锌弱,即锌>铁。
故选:B。
11.(2023 宁波模拟)向AgNO3溶液中加入过量铜粉,充分反应后过滤,得滤渣和滤液,则( )
A.滤渣含有Ag、Cu
B.滤液呈无色
C.滤液中一定含有AgNO3
D.向滤渣中滴加稀硫酸有气泡产生
【解答】解:A、向AgNO3溶液中加入过量铜粉,铜与硝酸银溶液反应生成硝酸铜溶液和银,铜粉是过量的,硝酸银完全反应,充分反应后过滤,滤渣中含有Ag、Cu,故选项说法正确。
B、滤液为硝酸铜溶液,为蓝色溶液,故选项说法错误。
C、铜粉是过量的,硝酸银完全反应,滤液中一定不含AgNO3,故选项说法错误。
D、滤渣中含有Ag、Cu,向滤渣中滴加稀硫酸,均不反应,没有气泡产生,故选项说法错误。
故选:A。
12.(2023 温州模拟)某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是( )
A.Cu的活动性比Ag强,只用盐酸无法探究两者活动性强弱
B.当溶质种类为1种时,金属单质种类可能为2种
C.c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+
D.从m1变化到m2时,溶液中硝酸铜的质量分数不变
【解答】解:A、Cu的活动性比Ag强,铜、银均不能与稀盐酸反应,只用盐酸无法探究两者活动性强弱,故选项说法正确。
B、当溶质种类为1种时,可能是锌与硝酸铜恰好完全反应,金属单质种类可能为银、铜2种,故选项说法正确。
C、c~d间(不含两点),发生的是锌与硝酸铜的反应,溶液中金属离子为Zn2+、Cu2+,故选项说法正确。
D、从m1变化到m2时,发生的是Zn+2AgNO3═Zn(NO3)2+2Ag,由反应时的质量比可知,每65份质量的锌可置换出216份质量的银,溶液的质量会减少,则溶液中硝酸铜的质量分数增大,故选项说法错误。
故选:D。
13.(2023 湖州模拟)向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤。下列情况中,可能存在的是( )
A.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+
B.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Cu2+
D.滤纸上有Ag、Cu、Fe,滤液中有Ag+、Cu2+
【解答】解:向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,铁先和硝酸银反应生成硝酸亚铁和银,后和硝酸铜反应生成硝酸亚铁和铜。
A、滤纸上有Cu,滤液中一定没有Ag+,该选项不正确。
B、滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+,例如硝酸银过量时,该选项正确。
C、滤纸上有Ag、Cu、Fe,滤液中一定没有Cu2+,该选项不正确。
D、滤纸上有Ag、Cu、Fe,滤液中一定没有Ag+、Cu2+,该选项不正确。
故选:B。
14.(2023 平阳县模拟)如图某兴趣小组通过实验得出Fe、Cu、Ag 三种金属的活动性顺序,则丙试管中的金属A和溶液B可能的组合是( )
A.铁和硝酸银溶液 B.银和稀盐酸
C.铁和硫酸铜溶液 D.锌和硝酸铜溶液
【解答】解:甲中铁能与盐酸反应,可知,Fe>H;由乙中铜能置换硝酸银中的铜,可知Cu>Ag;
A、硝酸银溶液和铁能反应,说明Ag<Fe,不能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项不符合题意;
B、稀盐酸和银不能反应,说明H>Ag,不能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项不符合题意;
C、铁能和硫酸铜溶液反应,说明Fe>Cu,能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项符合题意;
D、锌能和硝酸铜溶液反应,说明Zn>Cu,不能得出Fe、Cu、Ag 三种金属的活动性顺序,故本选项不符合题意。
故选:C。
15.(2023 宁波模拟)兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,有气泡产生,下列说法不正确的是( )
A.由实验可判断出铁、铜、锌的活动性顺序
B.两支试管混合后,固体总质量可能大于2M克
C.滤渣中一定有Cu和Fe,一定没有Zn
D.滤液中的溶质一定有FeCl2、ZnCl2,一定没有CuCl2
【解答】解:由于金属的活动性强弱是:锌>铁>铜,在进行实验时,铁不能与氯化锌反应,能与氯化铜反应生成了氯化亚铁和铜,反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,有气泡产生,说明了铁有剩余;所以:
A、根据铁不能与氯化锌反应,能与氯化铜反应,可以判断出铁、铜、锌的活动性顺序,故A说法正确;
B、由于每56份质量的铁能置换出64份质量的铜,铁不能置换氯化锌中的锌,所以两支试管混合后,第一支试管没反应的铁可以继续与第二支试管中的氯化铜反应,所以固体总质量一定大于2M,故B说法错误;
C、由上述分析可知,滤渣中一定有Cu和Fe,一定没有Zn,故C说法正确;
D、由上述分析可知,滤液中的溶质一定有FeCl2、ZnCl2,一定没有CuCl2,故D说法正确;
故选:B。
二.填空题(共5小题)
16.(2023 湖州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识和空气成分的研究也是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,这为发现金属活动性顺序奠定了基础。小嘉选用锡、铜、锌三种金属重温实验,则会“消失”的金属有 锡、锌 。
(2)1777年瑞典化学家舍勒通过自己研究,在《火与空气》一书指出:空气由两种不同性质的“火空气”和“浊空气”组成。其中,“火空气”可以帮助燃烧,维持生命,“火空气”指的是 氧气 。
【解答】解:(1)在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,锡、铜、锌三种金属重温实验,在金属活动性顺序中,锡、锌的位置排在氢的前面,则会“消失”的金属有锡、锌。
(2)由题意,空气由两种不同性质的“火空气”和“浊空气”组成。其中,“火空气”可以帮助燃烧,维持生命,“火空气”指的是能支持燃烧的氧气。
故答案为:
(1)锡、锌;
(2)氧气。
17.(2023 路桥区一模)氢是实现碳中和的能源载体。
(1)1781年,普里斯特利用金属M与稀盐酸反应制得一定量的氢气。M可能是锌、铜、银三种金属中的 锌 ,该反应的微观示意图如右图,其中表示反应后溶液中金属离子的微粒是 C (选填“A”“B”或“C”)。
(2)煤制氢的原理可表示为C+H2OX+H2。则X中肯定含有的元素是 CO 。
【解答】解:(1)在金属活动性顺序中,锌排在氢的前面,能与盐酸反应生成氢气,而铜和银排在氢的后面,与盐酸不反应,因此M可能是锌;由微观反应示意图可知,A表示氢离子,B表示氯离子,C表示锌离子;故答案为:锌;C;
(2)由C+H2OX+H2可知,反应前有1个碳原子、1个氧原子和2个氢原子,反应后有2个氢原子,则每个X分子中含有1个碳原子与1个氧原子,则X的化学式为CO;故答案为:CO。
18.(2023 温州一模)人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识正是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,为发现金属活动性顺序奠定了基础。小明选用镁、铜、锌三种金属进行验证实验,则“消失”的金属有 镁、锌 。
(2)1766年卡文迪许用金属与酸反应制取了一种可燃性气体,称之为“可燃空气”,为探索金属活动性打开了新思路。“可燃空气”是 氢气 。
(3)1865年贝开托夫设想找到一种化合物,使之与金属发生反应,根据反应的难易程度来判断金属活动性的强弱。小明运用该规律开展实验,在硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示,则a点时溶液中金属阳离子有 Zn2+、Fe2+ 。
【解答】解:(1)小明选用镁、铜、锌三种金属进行验证实验,在金属活动性顺序中,镁、锌位于氢前,能和稀盐酸反应,铜位于氢后,不能和稀盐酸反应,则“消失”的金属有镁、锌。
(2)活泼金属与酸反应生成可燃性的氢气,卡文迪许称之为“可燃空气”,则“可燃空气”是氢气。
(3)在硝酸银和硝酸亚铁的混合溶液中加入锌粉,锌先和硝酸银反应生成硝酸锌和银,由化学方程式的质量关系可知,反应后溶液质量减小,硝酸银反应完后,锌再和硝酸亚铁反应生成硝酸锌和铁,由化学方程式的质量关系可知,反应后溶液质量增大,则a点时硝酸银恰好完全反应,溶液中所含的金属阳离子有Zn2+、Fe2+。
故答案为:
(1)镁、锌;
(2)氢气;
(3)Zn2+、Fe2+。
19.(2023 南浔区一模)镍(Ni)是一中常见金属,在生产生活中发挥着重要的作用。
(1)用于制造合金。具有“记忆”本领的钛镍合金属于 混合物 (选填“纯净物”或“混合物”);
(2)用于电镀工业。铁表面镀镍不易锈蚀,原因是隔绝了铁与 氧气、水 接触;
(3)已知镍的金属活动性位于镁和铜之间,下列四种方案,能验证镁、镍、铜三种金属的活动性顺序方案有 BC (填写字母)。
【解答】解:(1)钛镍合金是由多种物质组成的,属于混合物;故答案为:混合物;
(2)铁与氧气和水接触会发生锈蚀,铁表面镀镍不易锈蚀,原因是隔绝了铁与氧气、水的接触;故答案为:氧气、水;
(3)已知镍的金属活动性位于镁和铜之间,即三种金属活动性由强到弱依次为镁、镍、铜。
A、镁、镍均能会置换出硫酸铜溶液中的铜,说明铜最不活泼,但无法证明镁和镍的活动性强弱,不合题意;
B、镍与硫酸镁不反应,镍能置换出硫酸铜溶液中的铜,说明活动性镁>镍>铜,符合题意;
C、镁能置换出硫酸镍中的镍,说明镁的活动性大于镍;镍能置换出硫酸铜溶液中的铜,说明活动性镁>镍>铜,符合题意;
D、镍和铜均不能与硫酸镁溶液反应,说明镁最活泼,但无法证明镍和铜的活动性强弱,不合题意;
故答案为:BC。
20.(2022 永嘉县模拟)有一包固体粉末X可能含有锌、铁、氧化铜中的一种或几种。现将m g该固体粉末加入到一定质量的稀盐酸中,充分反应后剩余ng固体。
(1)若固体粉末X中含有铁、氧化铜,则m > n(填“>”“=”或“<”)。
(2)若充分反应后溶液中含有四种阳离子,剩余固体为 纯净物 (填“纯净物”或“混合物”)。
【解答】解:(1)固体粉末中铁都会与盐酸反应生成盐而形成溶液,即使氧化铜和盐酸反应生成氯化铜,铁可以将氯化铜中的铜置换出来,得到的也只是氧化铜中铜元素的质量,所以m>n;
(2)若充分反应后溶液中含有四种阳离子,溶液中只能含有锌离子、亚铁离子、铜离子、氢离子,所以剩余固体只能是锌置换出部分氯化铜中的铜,一定为纯净物。
故答案为:(1)>;
(2)纯净物。
同课章节目录
